
05.09.2022
Описание препарата Актемра® (концентрат для приготовления раствора для инфузий, 20 мг/мл) основано на официальной инструкции, утверждено компанией-производителем в 2022 году
Дата согласования: 05.09.2022
Содержание
- Действующее вещество
- ATX
- Фармакологическая группа
- Нозологическая классификация (МКБ-10)
- Состав
- Описание лекарственной формы
- Фармакологическое действие
- Фармакодинамика
- Фармакокинетика
- Показания
- Противопоказания
- Применение при беременности и кормлении грудью
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Передозировка
- Особые указания
- Форма выпуска
- Производитель
- Условия отпуска из аптек
- Условия хранения
- Срок годности
- Заказ в аптеках Москвы
Действующее вещество
ATX
Фармакологическая группа
Состав
| Концентрат для приготовления раствора для инфузий | 1 мл |
| действующее вещество: | |
| тоцилизумаб | 20 мг |
| вспомогательные вещества: полисорбат 80 — 0,5 мг; сахароза — 50,0 мг; натрия гидрофосфата додекагидрат — q.s.; натрия дигидрофосфата дигидрат — q.s.; вода для инъекций — q.s. |
Описание лекарственной формы
Прозрачная или опалесцирующая бесцветная или светло-желтого цвета жидкость.
Фармакологическое действие
Фармакологическое действие
—
иммунодепрессивное.
Фармакодинамика
Механизм действия
Тоцилизумаб — рекомбинантное гуманизированное моноклональное антитело к человеческому рецептору ИЛ-6 из подкласса иммуноглобулинов IgG1. Тоцилизумаб связывается и подавляет как растворимые, так и мембранные рецепторы ИЛ-6 (sIL-6R и mIL-6R). ИЛ-6 является многофункциональным цитокином, вырабатываемым различными типами клеток, и участвует в паракринной регуляции, системных физиологических и патологических процессах, таких как стимуляция секреции Ig, активация Т-клеток, стимуляция выработки белков острой фазы в печени и стимуляция гемопоэза. ИЛ-6 вовлечен в патогенез различных заболеваний, в том числе воспалительных заболеваний, остеопороза и новообразований.
Нельзя исключить вероятность отрицательного воздействия тоцилизумаба на противоопухолевую и противоинфекционную защиту организма. Роль ингибирования рецептора ИЛ-6 в развитии опухолей неизвестна.
У пациентов с коронавирусной инфекцией (COVID-19, COronaVIrus Disease 2019), получавших тоцилизумаб в дозе 8 мг/кг однократно, снижение показателя С-реактивного белка (СРБ) до нормальных значений наблюдалось уже на 7-й день.
Клиническая эффективность при ревматоидном артрите (РА)
Эффективность препарата у пациентов, получавших тоцилизумаб как в монотерапии, так и в комбинации с метотрексатом (МТ) или базисными противовоспалительными препаратами (БПВП), не зависела от наличия или отсутствия ревматоидного фактора, возраста, пола, расовой принадлежности, числа предшествующих курсов лечения или стадии заболевания. Ответ на терапию возникал быстро (уже на 2-й неделе), в дальнейшем усиливался и сохранялся более 3 лет.
У пациентов, получавших тоцилизумаб в дозе 8 мг/кг, существенно снижается индекс активности заболевания по шкале (Desease Activity Score, 28 суставов (DAS28) по сравнению с пациентами, получавшими плацебо + БПВП. Число пациентов, достигших клинической ремиссии (DAS28 <2,6) на 24-й неделе, было значительно больше в группе терапии тоцилизумабом (27,5–33,6%) по сравнению с контрольной группой (0,8–12,1%). К 52-й неделе терапии число пациентов, достигших DAS28 <2,6, увеличивается до 47% по сравнению с 33% на 24-й неделе терапии.
Хороший или удовлетворительный ответ по критериям EULAR отмечался чаще у пациентов, получавших тоцилизумаб, чем получавших плацебо + БПВП.
Через 2 года терапии тоцилизумабом/МТ у 14% пациентов наблюдался значительный клинический ответ (АКР 70 (критерии Американской Коллегии Ревматологов, АКР) сохранялся на протяжении 24 недель и более).
Рентгенологическая оценка. У 83% пациентов, получавших терапию тоцилизумабом/МТ в течение года, не зарегистрировано прогрессирования деструкции суставов (изменение суммарного индекса Шарпа равно нулю или менее) по сравнению с 67% пациентов, получавших плацебо/МТ. Данный результат сохранялся на протяжении 2 лет терапии. У 93% пациентов отсутствовало прогрессирование деструкции суставов.
Показатели качества жизни. У пациентов, получавших тоцилизумаб в дозе 8 мг/кг (монотерапия или в сочетании с БПВП), по сравнению с теми, кто получал MT/БПВП, наблюдалось клинически значимое улучшение функциональной активности (по индексу HAQ-DI), снижение утомляемости (по шкале функциональной оценки терапии хронических заболеваний по показателю утомляемости FACIT-Fatigue), а также улучшение как показателей физического, так и показателей психического здоровья по опроснику SF-36.
Лабораторные показатели. После введения тоцилизумаба происходит быстрое снижение средних значений острофазовых показателей, CРБ, СОЭ, сывороточного амилоида А и фибриногена, снижение числа тромбоцитов в пределах нормальных значений, а также увеличение гемоглобина, которое в наибольшей степени наблюдалось у пациентов с хронической анемией, связанной с РА.
Клиническая эффективность у пациентов с ранним ревматоидным артритом (рРА), ранее не получавших терапию МТ
При применении тоцилизумаба в монотерапии в дозе 8 мг/кг и тоцилизумаба в дозе 4 или 8 мг/кг каждые 4 недели в комбинации с МТ индекс активности заболевания по шкале DAS28 существенно снижается в группах, получавших тоцилизумаб в дозе 8 мг/кг, по сравнению с пациентами, получавшими монотерапию МТ. Число пациентов, достигших клинической ремиссии (DAS28 <2.6) на 24-й неделе, значительно больше в группах, получавших тоцилизумаб (38,7–44,8%), по сравнению с группой монотерапии МТ (15%). К 52-й неделе число пациентов, достигших DAS28 <2,6 в группах терапии тоцилизумабом, увеличивается до 39,4–49% по сравнению с 19,5% в группе монотерапии МТ. Число пациентов, достигших ответа АКР 20, 50, 70, также существенно выше в группах терапии тоцилизумабом (70,2–74,5; 47,6–56,9; 30,1–38,6% на 24-й неделе и 63–67,2; 49,3–55,9; 36–43,1% на 52-й неделе соответственно) по сравнению с группой монотерапии МТ (65,2; 43,2; 25,4% на 24-й неделе и 57,1; 40,8; 28,9% на 52-й неделе соответственно).
Рентгенологическая оценка. Отсутствие прогрессирования деструкции суставов (изменение суммарного индекса Шарпа равно нулю или менее) наблюдается у 82–83% пациентов, получавших тоцилизумаб в дозе 8 мг/кг в качестве монотерапии или в комбинации с МТ, по сравнению с 73% пациентов в группе монотерапии МТ.
Показатели качества жизни. Клинически значимое улучшение функциональной активности по индексу HAQ-DI наблюдается у пациентов, получавших тоцилизумаб в дозе 8 мг/кг в качестве монотерапии или в комбинации с МТ, по сравнению с теми, кто получал монотерапию МТ.
При монотерапии тоцилизумабом (в дозе 8 мг/кг в/в каждые 4 недели у пациентов с РА, c непереносимостью МТ или при нецелесообразности продолжения терапии МТ (в т.ч. при неадекватном ответе на терапию МТ) наблюдалось более выраженное статистически значимое снижение активности заболевания по шкале DAS28 по сравнению с монотерапией адалимумабом (в дозе 40 мг п/к каждые 2 недели). Количество пациентов, ответивших на терапию с показателями DAS28 <2,6 и DAS28 ≤3,2, было больше при терапии тоцилизумабом, чем при терапии адалимумабом (39,9 против 10,5% и 51,5 против 19,8% соответственно). Ответы АКР 20, 50, 70 наблюдались у 65, 47,2, 32,5% пациентов, получавших тоцилизумаб, по сравнению с 49,4, 27,8, 17,9% пациентов, получавших адалимумаб.
Клиническая эффективность при полиартикулярном ювенильном идиопатическом артрите (пЮИА)
Ответы АКР 30, 50, 70, 90 были получены у 89,4, 83,0, 62,2 и 26,1% пациентов соответственно. Доля пациентов с ответом АКР 30, 50, 70 на 40-й неделе терапии относительно показателей на начало терапии составила 74,4, 73,2 и 64,6% соответственно.
Клиническая эффективность при системном ювенильном идиопатическом артрите (сЮИА)
Эффективность тоцилизумаба для лечения активного сЮИА изучалась в 12-недельном рандомизированном двойном слепом плацебо- контролируемом периоде исследования с 2 параллельными группами. На 12-й неделе доля пациентов, достигших ответа АКР 30, 50, 70, 90 при ЮИА, также была больше в группе терапии тоцилизумабом, чем в группе плацебо: 90,7 против 24,3%, 85,3 против 10,8%, 70,7 против 8,1%, 37,3 против 5,4%, соответственно (р<0,0001). Ответ на терапию сохранялся и в открытом расширенном периоде исследования.
Системные эффекты. У 85% пациентов, имевших исходно лихорадку, через 12 недель терапии тоцилизумабом лихорадка отсутствовала по сравнению с 21% пациентов, получавших плацебо (р<0,0001). Кроме того, у 64% пациентов, имевших сыпь исходно, через 12 недель терапии тоцилизумабом сыпь отсутствовала по сравнению с 11% пациентов, получавших плацебо (р=0,0008).
Наблюдалось значимое снижение интенсивности болевого синдрома в группе терапии тоцилизумабом по сравнению с плацебо на 12-й неделе. Скорректированное среднее изменение оценки боли по визуальной аналоговой шкале (ВАШ) после 12 недель терапии тоцилизумабом соответствовало 41 пункту (от 0 до 100 пунктов) по сравнению с 1 пунктом у пациентов, получавших плацебо (р<0,0001). Системные эффекты сохранялись и в продолжающемся открытом расширенном периоде исследования.
Снижение дозы ГКС. У 8 из 31 пациента в группе плацебо и у 48 из 70 пациентов в группе тоцилизумаба, получавших ГКС исходно, наблюдался ответ АКР 70 при ЮИА на 6-й или 8-й неделе, что позволило снизить дозу ГКС. При этом 24% пациентов в группе тоцилизумаба и 3% пациентов в группе плацебо смогли снизить дозу ГКС как минимум на 20% без последующего снижения частоты ответа по критериям АКР 30 при ЮИА или без возникновения системных проявлений к 12-й неделе (р=0,028). Снижение дозы ГКС продолжилось, при этом 44 пациента не получали ГКС на 44-й неделе и ответы АКР не изменялись.
Показатели качества жизни. На 12-й неделе доля пациентов в группе тоцилизумаба, демонстрирующих минимальное клинически значимое улучшение показателя по опроснику CHAQ-DI (определенного как снижение индивидуального общего балла на ≥0,13), была значительно выше, чем доля пациентов в группе плацебо — 77% против 19% соответственно (р<0,0001). Ответы сохранялись и в продолжающемся открытом расширенном периоде исследования.
Лабораторные показатели. Исходно у 67% пациентов из группы тоцилизумаба содержание Hb было ниже нормального диапазона. У 80% из этих пациентов на 12-й неделе наблюдалось увеличение Hb в пределах нормального диапазона по сравнению с 7% пациентов в группе плацебо (р<0,0001). У 88% пациентов из группы тоцилизумаба, имевших исходно сниженное содержание Hb, его уровень увеличился на ≥10 г/л к 6-й неделе, в группе плацебо частота повышения составила 3% (р<0,0001).
Доля пациентов, имевших исходно тромбоцитоз и у которых на 12-й неделе наблюдалось нормальное число тромбоцитов, была выше в группе тоцилизумаба по сравнению с группой плацебо — 90 против 4% (р<0,0001).
После введения тоцилизумаба происходило быстрое снижение средних значений острофазовых показателей: CРБ, СОЭ и сывороточного амилоида А.
Клиническая эффективность при COVID-19
Исследование совместной исследовательской группы RECOVERY (рандомизированная оценка терапии по поводу COVID-19) у госпитализированных взрослых пациентов с диагнозом COVID-19. Исследование RECOVERY представляло собой крупномасштабное рандомизированное контролируемое открытое многоцентровое платформенное исследование, проведенное в Великобритании для оценки эффективности и безопасности потенциальных вариантов терапии у госпитализированных взрослых пациентов с тяжелой формой COVID-19. Все пациенты, подходящие для включения в исследование, получали стандартную терапию и прошли начальную (основную) рандомизацию. Пациенты, подходящие для включения в исследование, имели подозреваемую на основании клинических признаков или лабораторно подтвержденную инфекцию SARS-CoV-2 и не имели медицинских противопоказаний к применению любого из рассматриваемых в исследовании видов терапии. Пациенты с клиническими подтверждениями прогрессирующей инфекции COVID-19 (определяемыми как уровень сатурации крови кислородом (SpO2) <92% при дыхании атмосферным воздухом или получение терапии кислородом, а также уровень CРБ ≥75 мг/л) могли пройти вторую рандомизацию в группы, получавшие либо тоцилизумаб в/в, либо только стандартную терапию.
Анализы эффективности были проведены в популяции в соответствии с назначенным лечением (intent-to-treat, ITT), которая включала в себя 4116 рандомизированных пациентов: 2022 пациента были рандомизированы в группу, получавшую тоцилизумаб + стандартную терапию, 2094 пациента — в группу, получавшую только стандартную терапию. Исходные демографические характеристики и характеристики заболевания популяции ITT были надлежащим образом сбалансированы между группами терапии. Средний возраст участников составлял 63,6 года (стандартное отклонение (СО): 13,6 года). Большинство пациентов были мужского пола (67%) и относились к европеоидной расе (76%). Медиана (диапазон) значений уровня СРБ составляла 143 мг/л (75–982). На исходном уровне 0,2% (n=9) пациентов не получали дополнительный кислород, 45% пациентов требовалась низкопоточная кислородная терапия, 41% пациентов — высокопоточная кислородная терапия и 14% пациентов — инвазивная искусственная вентиляция легких (ИВЛ); 82% пациентов получали системные ГКС. Наиболее частыми сопутствующими заболеваниями были сахарный диабет (28,4%), заболевание сердца (22,6%) и хроническая болезнь легких (23,3%).
Первичным показателем исхода было время до момента смерти в период до дня 28-го. Отношение рисков, демонстрирующее сравнение группы, получавшей тоцилизумаб + стандартную терапию, с группой, получавшей только стандартную терапию, составило 0,85 (95% ДИ: от 0,76 до 0,94), статистически значимый результат (p=0,0028). Расчетные показатели вероятности смерти ко дню 28-му составили 30,7 и 34,9% в группах, получавших тоцилизумаб и только стандартную терапию, соответственно. Расчетная разность рисков составила -4,1% (95% ДИ: от -7,0 до -1,3%), что согласуется с результатами первичного анализа. Отношение рисков в заранее определенной подгруппе пациентов, получавших системные ГКС на исходном уровне, составляло 0,79 (95% ДИ: от 0,70 до 0,89), а в заранее определенной подгруппе пациентов, не получавших системные ГКС на исходном уровне, отношение рисков составило 1,16 (95% ДИ: от 0,91 до 1,48).
Медиана времени до выписки из стационара составляла 19 дней в группе, получавшей тоцилизумаб + стандартную терапию, и >28 дней в группе, получавшей стандартную терапию (отношение рисков (95% ДИ) = 1,22 (от 1,12 до 1,33).
Среди пациентов, которым не требовалась инвазивная ИВЛ на исходном уровне, доля пациентов, у которых появилась потребность в ИВЛ или наступила смерть ко дню 28-му, составляла 35% (619/1754) в группе, получавшей тоцилизумаб + стандартную терапию, и 42% (754/1800) в группе, получавшей только стандартную терапию (отношение рисков (95% ДИ) = 0,84 (от 0,77 до 0,92) p<0,0001).
Исследование ML42528 (EMPACTA). Исследование ML42528 представляло собой глобальное рандомизированное двойное слепое плацебо-контролируемое многоцентровое исследование III фазы по оценке эффективности и безопасности применения тоцилизумаба для в/в введения в комбинации со стандартной терапией у госпитализированных взрослых пациентов с пневмонией, ассоциированной с COVID-19, не находящихся на ИВЛ. Для включения в исследование подходили пациенты в возрасте по меньшей мере 18 лет, имевшие инфекцию SARS-CoV-2, подтвержденную положительным результатом теста методом полимеразной цепной реакции с обратной транскриптазой (ОТ-ПЦР), имевшие пневмонию, подтвержденную результатами рентгенологического исследования, и уровень SpO2 <94% при дыхании атмосферным воздухом. Стандартная терапия могла включать в себя противовирусную терапию, применение системных ГКС в низких дозах и поддерживающую терапию. Пациенты были рандомизированы в соотношении 2:1 в группы, получавшие одну инфузию тоцилизумаба в дозе 8 мг/кг, при максимальной дозе 800 мг либо плацебо. Если клинические признаки или симптомы ухудшались или не улучшались, могла быть введена одна дополнительная инфузия тоцилизумаба или плацебо по слепой схеме через 8–24 часа после проведения первой инфузии.
Из 389 пациентов, которые были рандомизированы, анализы эффективности были проведены в модифицированной популяции в соответствии с назначенным лечением (modified intent-to-treat, mITT), которая включала в себя пациентов, получивших любое количество исследуемого лекарственного препарата (249 пациентов в группе тоцилизумаба; 128 пациентов в группе плацебо). Исходные демографические характеристики и характеристики заболевания были в целом сбалансированы между группами терапии. В популяции mITT (n=377) на момент рандомизации медиана возраста составляла 57 лет (диапазон: от 20 до 95); 59,2% пациентов были мужского пола, 56% пациентов имели испанское или латиноамериканское этническое происхождение, 52,8% пациентов принадлежали к европеоидной расе, 20,4% пациентов были американскими индейцами/представителями коренного населения Аляски, 15,1% пациентов были представителями негроидной расы/афроамериканцами и 1,6% пациентов были представителями монголоидной расы. На исходном уровне 35 (9,3%) пациентов не получали дополнительный кислород, 242 (64,2%) пациентам требовалась низкопоточная кислородная терапия и 100 (26,5%) пациентам — высокопоточная кислородная терапия. Медиана времени с момента возникновения симптомов составляла 8 дней. На исходном уровне в обеих группах терапии в совокупности 72,7% пациентов получали системные ГКС и 47,7% пациентов — ремдесивир. Значения медианы (диапазон) уровня СРБ и ферритина составляли соответственно 136,10 мг/л (2,5–3776,0) и 1,4 пмоль/мл (0,03–122,3). Наиболее частыми сопутствующими заболеваниями были артериальная гипертензия (48,3%), сахарный диабет (40,6%), гиперлипидемия (27,6%) и ожирение (24,4%).
Первичной конечной точкой оценки эффективности была совокупная доля пациентов, у которых появилась потребность в ИВЛ или наступила смерть ко дню 28-му. У пациентов, которые получали тоцилизумаб, наблюдалось статистически значимое улучшение в отношении времени до прогрессирования до ИВЛ или смерти в сравнении с пациентами, которые получали плацебо (значение p для логрангового критерия = 0,0360; ОР = 0,56 (95% ДИ: от 0,33 до 0,97). Совокупная доля пациентов, у которых появилась потребность в ИВЛ или наступила смерть ко дню 28-му (оценка с использованием метода Каплана-Мейера), составила 12,0% (95% ДИ: от 8,52 до 16,86%) в группе, получавшей тоцилизумаб, и 19,3% (95% ДИ: от 13,34 до 27,36%) в группе, получавшей плацебо.
Медиана времени до выписки из стационара либо «готовности к выписке» за период до дня 28-го составляла 6,0 дня в группе, получавшей тоцилизумаб, и 7,5 дня в группе, получавшей плацебо (ОР = 1,16 (95% ДИ: от 0,91 до 1,48).
Показатель смертности на день 28-й составлял 10,4% в группе, получавшей тоцилизумаб, в сравнении с 8,6% в группе, получавшей плацебо (взвешенная разница (группа тоцилизумаба — группа плацебо): 2,0% (95% ДИ: от -5,2 до 7,8%). Показатель смертности на день 60-й (ретроспективный анализ) составлял 11,2% в группе, получавшей тоцилизумаб, в сравнении с 10,9% в группе, получавшей плацебо (взвешенная разница (группа тоцилизумаба — группа плацебо): 0,5% (95% ДИ: от -6,9 до 6,8%).
Исследование WA42380 (COVACTA). Исследование WA42380 представляло собой глобальное рандомизированное двойное слепое плацебо-контролируемое многоцентровое исследование III фазы по оценке эффективности и безопасности применения тоцилизумаба для в/в введения в комбинации со стандартной терапией у взрослых пациентов, госпитализированных с тяжелой пневмонией, ассоциированной с COVID-19. Для включения в исследование подходили пациенты в возрасте, по меньшей мере, 18 лет, имевшие инфекцию SARS-CoV-2, подтвержденную положительным результатом теста методом ОТ-ПЦР, имевшие пневмонию, подтвержденную результатами рентгенологического исследования, и показатель SpO2 ≤93% при дыхании атмосферным воздухом либо отношение парциального давления кислорода в артериальной крови к фракции кислорода во вдыхаемом воздухе 300 мм рт.ст. или менее. Стандартная терапия могла включать в себя противовирусную терапию, применение ГКС в низких дозах, применение реконвалесцентной плазмы и другую поддерживающую терапию. Пациенты были рандомизированы в соотношении 2:1 в группы, получавшие одну инфузию тоцилизумаба в дозе 8 мг/кг при максимальной дозе 800 мг либо плацебо. Если клинические признаки или симптомы ухудшались или не улучшались, могла быть введена одна дополнительная инфузия тоцилизумаба или плацебо по слепой схеме, через 8–24 часа после проведения первой инфузии.
Из 452 пациентов, которые были рандомизированы, анализы эффективности были проведены в популяции mITT, которая включала в себя пациентов, получивших любое количество исследуемого лекарственного препарата (294 пациента в группе тоцилизумаба; 144 пациента в группе плацебо). Исходные демографические характеристики и характеристики заболевания были в целом сбалансированы между группами терапии. Для популяции mITT в целом (n=438) на момент рандомизации медиана возраста составляла 62 года (диапазон: 22–96, при этом 44,3% пациентов были в возрасте от 65 лет или старше); 69,9% пациентов были мужского пола, 32,2% пациентов были испанского или латиноамериканского этнического происхождения, 57,5% пациентов принадлежали к европеоидной расе, 15,1% пациентов были представителями негроидной расы/афроамериканцами и 8,7% пациентов были представителями монголоидной расы. На исходном уровне 3,4% пациентов не получали дополнительный кислород, 27,9% пациентов получали низкопоточную кислородную терапию, 30,4% пациентов находились на неинвазивной ИВЛ или получали высокопоточную кислородную терапию и 38,4% пациентов находились на инвазивной ИВЛ. Медиана времени с момента возникновения симптомов составляла 11,0 дней. На исходном уровне в обеих группах терапии в совокупности 22,4% пациентов получали системные ГКС и 5,7% пациентов — ремдесивир. Значения медианы (диапазон) уровня ИЛ-6, СРБ и ферритина составляли соответственно 85,8 нг/л (3,1–4020), 155,15 мг/л (1,1–99,6) и 2,20 пмоль/мл (0,0–75,3). Наиболее частыми сопутствующими заболеваниями были артериальная гипертензия (62,1%), сахарный диабет (38,1%), нарушения со стороны сердечно-сосудистой системы (28,1%) и ожирение (20,5%).
Первичной конечной точкой для оценки эффективности был клинический статус в день 28-й, оцениваемый с использованием порядковой шкалы со следующими 7 категориями:
1. Выписан из стационара (либо «готов к выписке», что определяется как достижение нормальной температуры тела и частоты дыхания, а также стабильного SpO2 при дыхании атмосферным воздухом или при использовании ≤2 л дополнительного кислорода).
2. В общей палате (или «готов к переводу в общую палату»), без потребности в дополнительном кислороде.
3. В общей палате (или «готов к переводу в общую палату»), требуется дополнительный кислород.
4. В отделении интенсивной терапии или в общей палате, требуется неинвазивная вентиляция легких или высокопоточная кислородная терапия.
5. В отделении интенсивной терапии, требуется интубация или ИВЛ.
6. В отделении интенсивной терапии, требуется экстракорпоральная мембранная оксигенация (ЭКМО) или ИВЛ и дополнительная поддержка органов (например, применение вазопрессорных препаратов, заместительная почечная терапия).
7. Смерть.
При сравнении группы, получавшей тоцилизумаб, с группой, получавшей плацебо, не было выявлено статистически значимого различия в распределении оценок клинического статуса по порядковой шкале с 7 категориями в день 28-й. Медианой категории клинического статуса в день 28-й была категория 1,0 в группе, получавшей тоцилизумаб, и 2,0 в группе, получавшей плацебо (отношение шансов (ОШ) 1,19 (95% ДИ: 0,81, 1,76).
Медиана времени до выписки из стационара либо «готовности к выписке» за период до дня 28-го составляла 20 дней в группе, получавшей тоцилизумаб, и 28 дней в группе, получавшей плацебо (ОР = 1,35 (95% ДИ: от 1,02 до 1,79).
Показатель смертности на день 28-й составлял 19,7% в группе, получавшей тоцилизумаб, в сравнении с 19,4% в группе, получавшей плацебо (взвешенная разница (группа тоцилизумаба — группа плацебо): 0,3% (95% ДИ: от -7,6 до 8,2). Показатель смертности на день 60-й составлял 24,5% в группе, получавшей тоцилизумаб, в сравнении с 25,0% в группе, получавшей плацебо (взвешенная разница (группа тоцилизумаба — группа плацебо): -0,5% (95% ДИ: от -9,1 до 8,0).
Исследование WA42511 (REMDACTA). Исследование WA42511 представляло собой глобальное рандомизированное двойное слепое плацебо-контролируемое многоцентровое исследование III фазы, проведенное с целью оценки эффективности и безопасности применения тоцилизумаба для в/в введения в комбинации с ремдесивиром в сравнении с соответствующим плацебо в комбинации с ремдесивиром у госпитализированных взрослых пациентов с тяжелой пневмонией, ассоциированной с COVID-19. Для включения в исследование подходили пациенты в возрасте по меньшей мере 12 лет с подтвержденной инфекцией SARS-CoV-2, включая положительный результат теста методом полимеразной цепной реакции (ПЦР), и пневмонией, подтвержденной результатами рентгенологического исследования, которым требовался дополнительный кислород в количестве >6 л/мин для поддержания уровня SpO2 >93%. Пациенты были рандомизированы в соотношении 2:1 в группы, получавшие по слепой схеме либо тоцилизумаб + ремдесивир, либо соответствующее плацебо + ремдесивир. Исследуемую терапию применяли в комбинации со стандартной терапией в соответствии с локальными руководствами (например, ГКС, поддерживающая терапия). Пациенты, распределенные в группу лечения комбинацией тоцилизумаб + ремдесивир, получили одну инфузию тоцилизумаба в дозе 8 мг/кг, при максимальной дозе 800 мг, а пациенты, распределенные в группу лечения комбинацией плацебо + ремдесивир, получили одну инфузию плацебо. В обеих группах в случаях, если клинические признаки или симптомы ухудшались или не улучшались, могла быть введена одна дополнительная инфузия тоцилизумаба или плацебо по слепой схеме, через 8–24 часа после проведения первой инфузии.
Из 649 пациентов, которые были рандомизированы, анализы эффективности были проведены в популяции mITT, которая включала в себя пациентов, получивших любое количество тоцилизумаба/плацебо (430 пациентов в группе лечения комбинацией тоцилизумаб + ремдесивир; 210 пациентов в группе лечения комбинацией плацебо + ремдесивир). Исходные демографические характеристики и характеристики заболевания были в целом сбалансированными между группами терапии. Для популяции mITT в целом (n=640) на момент рандомизации медиана возраста составляла 60 лет (диапазон: от 20 до 93 лет, при этом 38,3% пациентов были в возрасте от 65 лет или старше); 63,3% пациентов были мужского пола, 51,6% пациентов были испанского или латиноамериканского этнического происхождения, 67% пациентов принадлежали к европеоидной расе, 10,9% пациентов были представителями негроидной расы/афроамериканцами и 3,4% пациентов были представителями монголоидной расы. На исходном уровне 6,6% пациентов получали низкопоточную кислородную терапию, 79,8% пациентов находились на неинвазивной ИВЛ или получали высокопоточную кислородную терапию и 13,6% пациентов находились на инвазивной ИВЛ. Медиана времени с момента возникновения симптомов составляла 8 дней. На исходном уровне большинство пациентов получали ГКС (84,2% во всех группах терапии в совокупности). Значения медианы (диапазон) уровня СРБ и ферритина составляли 98,20 мг/л (1,3–418,3) и 2,13 пмоль/мл (0,1–30,8) соответственно. Наиболее частыми сопутствующими заболеваниями были артериальная гипертензия (61,7%), сахарный диабет (39,5%) и ожирение (27%).
Первичной конечной точкой для оценки эффективности было время с момента рандомизации до выписки из стационара либо «готовности к выписке» за период до дня 28-го. Не было выявлено статистически значимой разницы между группами терапии в отношении времени до выписки из стационара либо «готовности к выписке» за период до дня 28-го (ОР: 0,965 (95% ДИ: от 0,78 до 1,19) или времени до начала использования ИВЛ или смерти за период до дня 28-го (ОР: 0,980 (95% ДИ: от 0,72 до 1,34).
Показатель смертности на день 28-й составлял 18,1% в группе, получавшей тоцилизумаб, в сравнении с 19,5% в группе, получавшей плацебо (взвешенная разница (группа тоцилизумаба — группа плацебо): -1,3% (95% ДИ: от -7,8 до 5,2%). Показатель смертности на день 60-й составлял 22,6% в группе, получавшей тоцилизумаб, в сравнении с 25,7% в группе, получавшей плацебо (взвешенная разница (группа тоцилизумаба — группа плацебо): -3,0% (95% ДИ: от -10,1 до 4%).
Метаанализ по результатам исследований RECOVERY, EMPACTA (исследование ML42528), COVACTA (исследование WA42380) и REMDACTA (исследование WA42511) для пациентов, получавших терапию системными ГКС на исходном уровне. Метаанализ на уровне исследований был проведен по результатам 3 исследований компании Рош и исследования RECOVERY. Для каждого исследования была введена оценка ОР для времени до момента смерти за период до дня 28-го в подгруппе пациентов, получавших системные кортикостероиды на исходном уровне (тоцилизумаб — 597 пациентов и плацебо — 313 пациентов из исследований компании Рош; тоцилизумаб — 1664 пациента и стандартная терапия — 1721 пациент из исследования RECOVERY).
Комбинированный показатель ОР указывал на то, что терапия тоцилизумабом (n=2261) приводила к относительному уменьшению на 19% риска смерти за период до дня 28-го (ОР = 0,81; 95% ДИ: 0,72, 0,90; p=0,0002) в сравнении со стандартной терапией (n=2034).
Отношение рисков Кокса для исследований компании Рош. Логранговый показатель O-E для исследования RECOVERY, в котором значение ОР было вычислено путем принятия In(ОР) равным (O-E)/V при нормальной дисперсии 1/V.
Модель с фиксированными эффектами, в которую In(ОР) был включен в качестве ответа и V – в качестве весов для оценки объединенного эффекта.
CT = стандартная терапия, ТЦЗ = тоцилизумаб
Источник данных компании Рош: root/clinical_studies/R04877533/share/pool_COVID19/prod/outdata_vad.
Рисунок 1. Метаанализ времени до момента смерти за период до дня 28-го в субпопуляции пациентов, получавших кортикостероиды на исходном уровне.
Доклинические данные безопасности
Канцерогенность. Исследования по изучению канцерогенности тоцилизумаба не проводились. Имеющиеся доклинические данные демонстрируют вклад плейотропного ИЛ-6 в прогрессирование злокачественных новообразований и устойчивость к апоптозу при различных формах рака. Эти данные не предполагают, что лечение тоцилизумабом приводит к существенному риску развития и прогрессирования рака.
Мутагенность. Стандартные генотоксические тесты как в прокариотических, так и в эукариотических клетках были отрицательными.
Влияние на фертильность. Имеющиеся доклинические данные не предполагают влияния аналогов тоцилизумаба на фертильность. В исследованиях по изучению хронической токсичности у яванских макак и у самок или самцов мышей с недостаточностью ИЛ-6 отрицательного влияния тоцилизумаба на эндокринные или репродуктивные органы не обнаружено.
Тератогенность. Не обнаружено прямого или опосредованного неблагоприятного влияния на беременность или внутриутробное развитие при в/в введении тоцилизумаба яванским макакам на ранних сроках гестационного периода.
Прочее. Отмечалось незначительное увеличение случаев спонтанного выкидыша/ внутриутробной гибели плода при высоком уровне системного кумулятивного воздействия (более чем в 100 раз превышающего таковое у человека) при введении дозы 50 мг/кг/сутки в сравнении с плацебо или меньшим уровнем вводимых доз. Частота выкидыша была в пределах исторического контроля для яванских макак, содержащихся в неволе; отдельные случаи выкидыша/внутриутробной гибели не демонстрировали какой-либо взаимосвязи между данными явлениями и дозой или продолжительностью введения тоцилизумаба.
Несмотря на то что ИЛ-6, по-видимому, не играет решающей роли в развитии плода или иммунологической регуляции системы «мать—плод», взаимосвязь этих явлений с введением тоцилизумаба не может быть исключена.
Наблюдалась экскреция мышиного аналога тоцилизумаба в молоко лактирующих мышей.
Применение мышиного аналога тоцилизумаба не оказывало токсичного действия на ювенильных мышей. В частности, не наблюдалось нарушения роста скелета, иммунной функции и полового развития.
Фармакокинетика
Фармакокинетика (ФК) тоцилизумаба характеризуется нелинейным выведением, представляющим комбинацию линейного клиренса и выведения по Михаэлис-Ментен. Нелинейная часть выведения тоцилизумаба приводит к более чем дозозависимому увеличению экспозиции. Фармакокинетические параметры тоцилизумаба не меняются с течением времени. Так как общий клиренс зависит от концентрации тоцилизумаба в сыворотке, T1/2 тоцилизумаба также является зависимым от его концентрации и может быть рассчитан только при наличии значения сывороточной концентрации. Популяционный ФК-анализ, проведенный во всех популяциях пациентов, не выявил связи между кажущимся клиренсом и наличием антител к тоцилизумабу.
Ревматоидный артрит (РА)
ФК тоцилизумаба сопоставима у здоровых добровольцев и пациентов с РА.
Таблица 1
Прогнозируемые средние ФК-параметры (± стандартное отклонение, СО) тоцилизумаба при равновесном состоянии у пациентов с РА
| Параметр тоцилизумаба | 4 мг/кг 1 раз в четыре недели | 8 мг/кг 1 раз в четыре недели |
| Максимальная концентрация (Cmax), мкг/мл | 83,8 ± 23,1 | 182 ± 50,4 |
| Минимальная концентрация (Ctrough), мкг/мл | 0,5 ± 1,5 | 15,9 ± 13,1 |
| Средняя концентрация (Cmean), мкг/мл | 17,8 ± 6,1 | 56,6 ± 19,3 |
| Кумулятивная Cmax | 1,01 | 1,09 |
| Кумулятивная Ctrough | 2,62 | 2,47 |
| Кумулятивная Cmeanили площадь под кривой «концентрация-время» (AUCτ)* | 1,09 | 1,32 |
*На протяжении 4 недель.
При высоких значениях концентрации тоцилизумаба в сыворотке линейный клиренс преобладает над общим клиренсом тоцилизумаба и конечный T1/2 составляет приблизительно 21,5 дней (на основе приблизительных параметров популяции пациентов). В то время как после в/в введения Cmax дозозависимо увеличивается между дозами 4 и 8 мг/кг каждые 4 недели, более чем дозозависимое увеличение наблюдалось для Cmean и Ctrough. В равновесном состоянии значения Cmean и Ctrough были в 3,2 и 32 раза выше при применении тоцилизумаба в дозе 8 мг/кг по сравнению с дозой 4 мг/кг соответственно.
Коэффициенты накопления AUC и Cmax после многократного применения тоцилизумаба в дозах 4 и 8 мг/кг каждые 4 недели были ниже, чем коэффициенты накопления Ctrough (2,62 и 2,47), благодаря участию нелинейного клиренса при более низких концентрациях тоцилизумаба.
Более 90% равновесного состояния при Cmax достигается после первой в/в инфузии; 90% равновесное состояние при AUCτ и Cmean достигается после первой и третьей в/в инфузии тоцилизумаба в дозе 4 и 8 мг/кг, соответственно; приблизительно 90% равновесное состояние при Ctrough достигается после четвертой в/в инфузии тоцилизумаба.
Масса тела является значимым фактором, влияющим на ФК тоцилизумаба. При в/в инфузии, рассчитанной в мг/кг, у пациента с массой тела ≥100 кг ожидается более высокая средняя экспозиция в равновесном состоянии по сравнению со средним значением в популяции пациентов. Таким образом, не рекомендуется увеличение дозы препарата выше 800 мг на одну инфузию у пациентов с массой тела ≥100 кг (см. «Способ применения и дозы»).
Полиартикулярный ювенильный идиопатический артрит (пЮИА)
После в/в применения приблизительно 90% равновесное состояние достигается к 12-й неделе при введении в дозе 10 мг/кг (масса тела <30 кг) и к 16-й неделе при введении в дозе 8 мг/кг (масса тела ≥30 кг).
Таблица 2
Прогнозируемые средние ФК-параметры (± стандартное отклонение, СО) тоцилизумаба при равновесном состоянии у пациентов с пЮИА
| Параметр тоцилизумаба | 8 мг/кг 1 раз в четыре недели (масса тела ≥30 кг) | 10 мг/кг 1 раз в четыре недели (масса тела <30 кг) |
| Максимальная концентрация (Cmax), мкг/мл | 183 ± 42,3 | 168 ± 24,8 |
| Минимальная концентрация (Ctrough), мкг/мл | 6,55 ± 7,93 | 1,47 ± 2,44 |
| Средняя концентрация (Cmean), мкг/мл | 42,2 ± 13,4 | 31,6 ± 7,84 |
| Кумулятивная Cmax | 1,04 | 1,01 |
| Кумулятивная Ctrough | 2,22 | 1,43 |
| Кумулятивная Cmeanили площадь под кривой «концентрация-время» (AUCτ)* | 1,16 | 1,05 |
*На протяжении 4 недель.
Системный ювенильный идиопатический артрит (сЮИА)
После в/в применения приблизительно 90% равновесное состояние достигается к 8-й неделе при введении в дозе 12 и 8 мг/кг 1 раз в 2 недели.
Таблица 3
Прогнозируемые средние ФК-параметры (± СО) тоцилизумаба при равновесном состоянии у пациентов с сЮИА
| Параметр тоцилизумаба | 8 мг/кг 1 раз в 2 недели (масса тела ≥30 кг) | 10 мг/кг 1 раз в 2 недели (масса тела <30 кг) |
| Cmax, мкг/мл | 256 ± 60,8 | 274 ± 63,8 |
| Ctrough, мкг/мл | 69,7 ± 29,1 | 68,4 ± 30,0 |
| Cmean, мкг/мл | 119 ± 36,0 | 123 ± 36,0 |
| Кумулятивная Cmax | 1,42 | 1,37 |
| Кумулятивная Ctrough | 3,20 | 3,41 |
| Кумулятивная Cmean или площадь под кривой «концентрация-время» (AUCτ)* | 2,01 | 1,95 |
*На протяжении 2 недель
ФК-параметры тоцилизумаба у пациентов в возрасте до 2 лет были сопоставимы с ФК-параметрами у пациентов старше 2 лет с массой тела <30 кг при в/в применении тоцилизумаба (в дозе 12 мг/кг каждые 2 недели).
COVID-19
Фармакокинетику тоцилизумаба у взрослых пациентов с COVID-19 оценивали в исследованиях WA42380 (COVACTA) и CA42481 (MARIPOSA) посредством популяционного ФК-анализа, в который было включено 380 взрослых пациентов. Пациенты получали 1 или 2 в/в инфузии тоцилизумаба в дозе 8 мг/кг, которые вводили с интервалом как минимум 8 часов.
Таблица 4
Расчетные средние (±СО) ФК-параметры после в/в введения тоцилизумаба в дозе 8 мг/кг
| Параметр фармакокинетики тоцилизумаба | 8 мг/кг | |
| Одна доза | Две дозы | |
| Cmax, мкг/мл | 154 (34,9) | 296 (64,7) |
| Cдень 28-й, мкг/мл | 0,934 (1,93) | 8,94 (8,5) |
В ходе популяционного ФК-анализа масса тела и тяжесть заболевания были определены как значимые ковариаты, которые оказывают влияние на ФК тоцилизумаба. При режиме дозирования тоцилизумаба 8 мг/кг и максимальной дозой 800 мг в рамках отдельной категории порядковой шкалы (ПШ) у пациентов с массой тела менее 60 кг экспозиция была на 20% ниже, по сравнению с пациентами со средней массой тела 80 кг. Экспозиция у пациентов с массой тела более 100 кг находилась в том же диапазоне экспозиций, что и у пациентов со средней массой тела 80 кг. Для пациента с массой тела 80 кг экспозиция снижалась с увеличением тяжести заболевания, для каждой последующей категории ПШ экспозиция соответственно снижалась на 13%.
Распределение
После в/в введения тоцилизумаб претерпевает двухфазное выведение из системного кровотока. У пациентов с РА объем распределения в центральной камере составляет 3,5 л, в периферической камере — 2,9 л, а объем распределения в равновесном состоянии составляет 6,4 л.
У детей с пЮИА объем распределения в центральной камере составляет 1,98 л, в периферической камере — 2,1 л, а объем распределения в равновесном состоянии — 4,08 л.
У детей с сЮИА объем распределения в центральной камере составляет 1,87 л, в периферической камере — 2,14 л, а объем распределения в равновесном состоянии — 4,01 л.
У взрослых пациентов с COVID-19 объем распределения в центральной камере составляет 4,52 л, в периферической камере — 4,23, таким образом, объем распределения — 8,75 л.
Выведение
Общий клиренс тоцилизумаба зависит от концентрации и представляет собой сумму линейного и нелинейного клиренса. Линейный клиренс составляет 12,5 мл/ч у пациентов с РА, 5,8 мл/ч у детей с пЮИА и 5,7 мл/ч у детей с сЮИА. Нелинейный клиренс, зависящий от концентрации, имеет наибольшее значение при низких концентрациях тоцилизумаба. При более высоких концентрациях тоцилизумаба преобладает линейный клиренс в связи с насыщением пути нелинейного клиренса. Так как общий клиренс зависит от сывороточной концентрации тоцилизумаба, T1/2 тоцилизумаба также является зависимым от его концентрации и может быть рассчитан только при наличии значения сывороточной концентрации.
При РА зависимый от концентрации кажущийся T1/2 для тоцилизумаба в равновесном состоянии в дозе 4 мг/кг один раз в 4 недели составляет до 11 дней, а для тоцилизумаба в дозе 8 мг/кг один раз в 4 недели — до 13 дней. При высоких значениях концентрации тоцилизумаба в сыворотке линейный клиренс преобладает над общим клиренсом тоцилизумаба и конечный T1/2 составляет приблизительно 21,5 дней (на основе приблизительных параметров популяции пациентов).
У детей с пЮИА эффективный T1/2 тоцилизумаба в равновесном состоянии (между введениями в дозе 8 мг/кг для детей с массой тела ≥30 кг или в дозе 10 мг/кг для детей с массой тела <30 кг) составляет до 17 дней.
У детей с сЮИА эффективный T1/2 тоцилизумаба в равновесном состоянии (между введениями в дозе 8 и 12 мг/кг) составляет до 16 дней.
У взрослых пациентов с COVID-19 сывороточные концентрации были ниже предела количественного определения по прошествии 35 дней (в среднем) после введения одной инфузии тоцилизумаба в дозе 8 мг/кг. Средний линейный клиренс в популяционном ФК-анализе составил 17,6 мл/ч у пациентов с категорией 3 ПШ (пациенты, которым требуется поддерживающая терапия кислородом) на исходном уровне, 22,5 мл/ч у пациентов с категорией 4 ПШ (пациенты, которым требуется высокопоточная кислородная терапия или неинвазивная вентиляция легких) на исходном уровне, 29 мл/ч у пациентов с категорией 5 ПШ (пациенты, которым требуется ИВЛ) на исходном уровне, 35 мл/ч у пациентов с категорией 6 ПШ (пациенты, которым требуется ЭКМО или ИВЛ и дополнительная поддержка органов) на исходном уровне.
ФК у особых групп пациентов
Пациенты с печеночной недостаточностью. ФК тоцилизумаба у пациентов с печеночной недостаточностью не изучалась.
Пациенты с почечной недостаточностью. Специальных исследований у пациентов с почечной недостаточностью не проводилось. У большинства пациентов с РА, учтенных в популяционном ФК-анализе, была нормальная функция почек или нарушение функции почек легкой степени тяжести (расчетный клиренс креатинина по формуле Кокрофта-Голта), которое не влияло на фармакокинетику тоцилизумаба. Коррекции дозы тоцилизумаба пациентам с нарушением функции почек легкой степени тяжести не требуется.
Пол, раса, пожилой возраст. Популяционный ФК-анализ у взрослых пациентов с РА показал, что возраст, пол и раса не влияют на ФК тоцилизумаба. Коррекции дозы тоцилизумаба не требуется.
Показания
- ревматоидный артрит со средней или высокой степенью активности у взрослых как в виде монотерапии, так и в комбинации с MT и/или с другими базисными противовоспалительными препаратами (БПВП), в т.ч. для торможения рентгенологически доказанной деструкции суставов;
- активный полиартикулярный ювенильный идиопатический артрит у пациентов в возрасте 2 лет и старше как в виде монотерапии, так и в комбинации с МТ;
- активный системный ювенильный идиопатический артрит у пациентов в возрасте 2 лет и старше как в виде монотерапии, так и в комбинации с МТ;
- лечение новой коронавирусной инфекции (COVID-19) у госпитализированных взрослых пациентов, получающих системные ГКС, которым требуется поддерживающая терапия кислородом или ИВЛ.
Противопоказания
- гиперчувствительность к тоцилизумабу, любому компоненту препарата в анамнезе;
- активные инфекционные заболевания (в т.ч. туберкулез), за исключением COVID-19;
- комбинация с ингибиторами ФНО-альфа или применение в течение 1 месяца после лечения анти-ФНО-антителами;
- повышение активности печеночных ферментов в ≥10 раз от ВГН; абсолютное число нейтрофилов (АЧН) <1·109/л; число тромбоцитов <50·103/мкл (COVID-19).
- детский возраст до 2 лет для пациентов с полиартикулярным ювенильным идиопатическим артритом и системным ювенильным идиопатическим артритом.
- детский возраст до 18 лет для пациентов с ревматоидным артритом;
- детский возраст до 18 лет для пациентов с новой коронавирусной инфекцией (COVID-19) (данные отсутствуют).
С осторожностью: рецидивирующие или хронические инфекции в анамнезе, а также сопутствующие заболевания (например, дивертикулит, сахарный диабет и интерстициальное заболевание легких), предрасполагающие к развитию инфекций; язвенное поражение органов ЖКТ или дивертикулит в анамнезе; активное заболевание печени или печеночная недостаточность; показатели АЛТ или АСТ, превышающие ВГН более чем в 1,5 раза; уровень тромбоцитов ниже 100·103/мкл.
Применение при беременности и кормлении грудью
Беременность. Безопасность и эффективность применения препарата Актемра® при беременности изучены недостаточно. Исследования у обезьян не обнаружили дисморфогенетического потенциала препарата Актемра®. Однако при введении препарата в высоких дозах обнаружен повышенный риск спонтанного выкидыша/внутриутробной гибели. Значение данной информации для людей не известно (см. «Фармакодинамика»). Не следует применять тоцилизумаб во время беременности, за исключением тех случаев, когда имеется очевидная клиническая необходимость.
Период грудного вскармливания. Неизвестно, выводится ли препарат Актемра® с грудным молоком у человека. Несмотря на выделение эндогенных IgG в грудное молоко, системная абсорбция препарата при грудном вскармливании маловероятна в связи с быстрой протеолитической деградацией таких белков в системе пищеварения. При принятии решения о продолжении/прерывании кормления грудью или продолжении/отмене терапии тоцилизумабом следует принимать во внимание пользу от грудного вскармливания для ребенка и пользу от продолжения терапии для матери.
Способ применения и дозы
Реклама: ООО «РЛС-Патент», ИНН 5044031277, erid=4CQwVszH9pUkpHxmQQo
Реклама: ООО «РЛС-Патент», ИНН 5044031277, erid=4CQwVszH9pUkpHxmQQo
Лечение должны назначать медицинские специалисты, имеющие опыт в постановке диагноза и терапии РА, COVID-19, сЮИА и пЮИА.
Препарат предназначен для введения как в амбулаторно-поликлинических, так и в стационарных условиях.
Стандартный режим дозирования
Ревматоидный артрит
Рекомендуемая доза составляет 8 мг/кг 1 раз в четыре недели.
Не рекомендуется увеличение дозы свыше 800 мг на одну инфузию пациентам с массой тела выше 100 кг (см. «Фармакокинетика»).
Рекомендации по коррекции дозы при изменении лабораторных показателей (см. «Особые указания»)
— Повышение активности печеночных ферментов
| Значение показателя | Коррекция лечения |
| Превышение ВГН в >1–3 раза | При необходимости провести коррекцию дозы одновременно назначаемого МТ/БПВП. При устойчивом повышении активности трансаминаз в этом диапазоне снизить дозу препарата Актемра® до 4 мг/кг или прервать лечение препаратом до нормализации показателей АЛТ или АСТ. Возобновить лечение препаратом в дозе 4 или 8 мг/кг в соответствии с клинической необходимостью |
| Превышение ВГН в >3–5 раз (подтвержденное при повторном исследовании, см. «Особые указания») | Прервать лечение препаратом Актемра® до снижения показателя до уровня, менее чем в 3 раза превышающего ВГН; далее следовать рекомендациям для превышения ВГН в >1–3 раза. Прекратить лечение препаратом Актемра® при устойчивом повышении показателя, превышающем ВГН более чем в 3 раза |
| Превышение ВГН более чем в 5 раз | Прекратить лечение препаратом Актемра® |
— Низкое АЧН
Пациентам, ранее не получавшим лечение препаратом Актемра®, не рекомендуется начинать применение препарата при показателе АЧН ниже 2·109/л.
| Значение показателя (число клеток ·109/л) | Коррекция лечения |
| АЧН >1 | Дозу не изменять |
| АЧН 0,5–1 | Прервать лечение препаратом Актемра®. При увеличении показателя до >1·109/л возобновить лечение препаратом в дозе 4 мг/кг и увеличить дозу до 8 мг/кг в соответствии с клинической необходимостью |
| АЧН <0,5 | Прекратить лечение препаратом Актемра® |
— Низкое число тромбоцитов
| Значение показателя (число клеток ·103/мкл) | Коррекция лечения |
| 50–100 | Прервать лечение препаратом Актемра®. При увеличении показателя >100·103/мкл возобновить лечение препаратом в дозе 4 мг/кг и увеличить дозу до 8 мг/кг в соответствии с клинической необходимостью |
| <50 | Прекратить лечение препаратом Актемра® |
COVID-19
Рекомендуемая доза для лечения COVID-19 составляет 8 мг/кг в виде однократной в/в инфузии в течение 60 минут у пациентов, получающих системные ГКС и которым требуется поддерживающая терапия кислородом или ИВЛ (см. «Фармакодинамика»).
Если клинические признаки или симптомы ухудшаются или не улучшаются после введения одной инфузии, можно ввести дополнительную инфузию препарата Актемра® в дозе 8 мг/кг через, как минимум, 8 часов после первой инфузии.
Не рекомендуется увеличение дозы свыше 800 мг на одну инфузию пациентам с массой тела более 100 кг (см. «Фармакокинетика»).
Применение препарата Актемра® не рекомендуется пациентам с COVID-19, у которых наблюдается любое из следующих отклонений в лабораторных показателях.
| Тип лабораторного исследования | Значение лабораторного показателя | Действие |
| Печеночные ферменты | ≥10·ВГН | Применение препарата Актемра®не рекомендуется |
| АЧН | <1·109/л | |
| Число тромбоцитов | <50·103/мкл |
Особые группы пациентов
Дети
сЮИА. Рекомендуемая доза у пациентов старше 2 лет составляет 8 мг/кг один раз в 2 недели у пациентов с массой тела ≥30 кг или 12 мг/кг один раз в 2 недели у пациентов с массой тела <30 кг. Дозу следует рассчитывать исходя из массы тела пациента при каждом введении препарата. Изменение дозы должно быть основано только на соответствующем изменении массы тела пациента с течением времени.
Безопасность и эффективность внутривенного введения препарата Актемра® у детей в возрасте до 2 лет не установлены.
У пациентов с сЮИА рекомендуется прерывание терапии тоцилизумабом при изменениях в лабораторных показателях, приведенных в таблицах ниже. При необходимости следует изменить дозу одновременно назначаемого МТ и/или других сопутствующих препаратов или прекратить их прием, а также прервать введение тоцилизумаба до оценки клинической ситуации. Решение о прекращении терапии тоцилизумабом при возникновении изменений в лабораторных показателях должно основываться на медицинской оценке состояния конкретного пациента, поскольку существует множество сопутствующих заболеваний, которые могут оказывать влияние на лабораторные показатели при сЮИА.
— Повышение активности печеночных ферментов
| Значение показателя | Коррекция лечения |
| Превышение ВГН в >1–3 раза | При необходимости провести коррекцию дозы одновременно назначаемого МТ. При устойчивом повышении активности трансаминаз в этом диапазоне прервать лечение препаратом до нормализации показателей АЛТ/АСТ |
| Превышение ВГН в >3–5 раз | При необходимости провести коррекцию дозы одновременно назначаемого МТ. Прервать лечение препаратом Актемра® до снижения показателя до уровня, менее чем в 3 раза превышающего ВГН; далее следовать рекомендациям для превышения ВГН в >1–3 раза |
| Превышение ВГН более чем в 5 раз | Прекратить лечение препаратом Актемра®. Решение о прекращении терапии препаратом Актемра® при сЮИА при возникновении изменений в лабораторных показателях должно основываться на медицинской оценке состояния конкретного пациента |
— Низкое АЧН
| Значение показателя (число клеток·109/л) | Коррекция лечения |
| АЧН >1 | Дозу не изменять |
| АЧН 0,5–1 | Прервать лечение препаратом Актемра®. При увеличении показателя до >1·109/л возобновить лечение препаратом Актемра® |
| АЧН <0,5 | Прекратить лечение препаратом Актемра®. Решение о прекращении терапии препаратом Актемра® при сЮИА в случае возникновения изменений в лабораторных показателях должно основываться на медицинской оценке состояния конкретного пациента |
— Низкое число тромбоцитов
| Значение показателя (число клеток ·103/мкл) | Коррекция лечения |
| 50–100 | При необходимости провести коррекцию дозы одновременно назначаемого МТ. Прервать лечение препаратом Актемра®. При увеличении показателя >100·103/мкл возобновить лечение препаратом Актемра® |
| <50 | Прекратить лечение препаратом Актемра®. Решение о прекращении терапии препаратом Актемра® при сЮИА в случае возникновения изменений в лабораторных показателях должно основываться на медицинской оценке состояния конкретного пациента |
Клинических данных недостаточно, чтобы оценить влияние снижения дозы тоцилизумаба у пациентов с сЮИА, у которых наблюдались изменения в лабораторных показателях.
Имеющиеся данные свидетельствуют о том, что клиническое улучшение наблюдается в течение 6 недель после начала лечения препаратом Актемра®. В случае, если у пациента не наблюдается улучшения в течение данного периода времени, целесообразность продолжения терапии должна быть тщательно пересмотрена.
пЮИА. Рекомендуемая доза у пациентов старше 2 лет составляет 8 мг/кг один раз в 4 недели у пациентов с массой тела ≥30 кг или 10 мг/кг один раз в 4 недели у пациентов с массой тела <30 кг. Дозу следует рассчитывать исходя из массы тела пациента при каждом введении препарата. Изменение дозы должно быть основано только на соответствующем изменении массы тела пациента с течением времени.
Безопасность и эффективность внутривенного введения препарата Актемра® у детей в возрасте до 2 лет не установлены.
У пациентов с пЮИА рекомендуется прерывание терапии тоцилизумабом при изменениях в лабораторных показателях, приведенных в таблицах ниже. При необходимости следует изменить дозу одновременно назначаемого МТ и/или других сопутствующих препаратов или прекратить их прием, а также прервать введение тоцилизумаба до оценки клинической ситуации. Поскольку существует множество сопутствующих заболеваний, которые могут оказывать влияние на лабораторные показатели при пЮИА, решение о прекращении терапии тоцилизумабом в случае возникновения изменений в лабораторных показателях должно основываться на медицинской оценке состояния конкретного пациента.
— Повышение активности печеночных ферментов
| Значение показателя | Коррекция лечения |
| Превышение ВГН в >1–3 раза | При необходимости провести коррекцию дозы одновременно назначаемого МТ. При устойчивом повышении активности трансаминаз в этом диапазоне прервать лечение препаратом до нормализации показателей АЛТ/АСТ |
| Превышение ВГН в >3–5 раз | При необходимости провести коррекцию дозы одновременно назначаемого МТ. Прервать лечение препаратом Актемра® до снижения показателя до уровня, менее чем в 3 раза превышающего ВГН; далее следовать рекомендациям для превышения ВГН в >1–3 раза |
| Превышение ВГН более чем в 5 раз | Прекратить лечение препаратом Актемра®. Решение о прекращении терапии препаратом Актемра® при пЮИА в случае возникновения изменений в лабораторных показателях должно основываться на медицинской оценке состояния конкретного пациента |
— Низкое АЧН
| Значение показателя (число клеток·109/л) | Коррекция лечения |
| АЧН >1 | Дозу не изменять |
| АЧН 0,5–1 | Прервать лечение препаратом Актемра®. При увеличении показателя до >1·109/л возобновить лечение препаратом Актемра® |
| АЧН <0,5 | Прекратить лечение препаратом Актемра®. Решение о прекращении терапии препаратом Актемра® при пЮИА в случае возникновения изменений в лабораторных показателях должно основываться на медицинской оценке состояния конкретного пациента |
— Низкое число тромбоцитов
| Значение показателя (число клеток·103/мкл) | Коррекция лечения |
| 50–100 | При необходимости провести коррекцию дозы одновременно назначаемого МТ. Прервать лечение препаратом Актемра®. При увеличении показателя >100·103/мкл возобновить лечение препаратом Актемра® |
| <50 | Прекратить лечение препаратом Актемра®. Решение о прекращении терапии препаратом Актемра® при пЮИА в случае возникновения изменений в лабораторных показателях должно основываться на медицинской оценке состояния конкретного пациента |
Возможность снижения дозы тоцилизумаба в связи с возникновением изменений в лабораторных показателях у пациентов с пЮИА не изучалась.
Имеющиеся данные свидетельствуют о том, что клиническое улучшение наблюдается в течение 12 недель после начала лечения препаратом Актемра®. Целесообразность продолжения терапии должна быть тщательно пересмотрена, если у пациента не наблюдается улучшения в течение данного периода времени.
Пациенты пожилого возраста. Коррекции дозы у пациентов пожилого возраста (≥65 лет) не требуется.
Пациенты с нарушением функции почек. Коррекции дозы у пациентов с нарушением функции почек легкой степени тяжести не требуется (см. ФК у особых групп пациентов). Применение тоцилизумаба у пациентов с умеренным и тяжелым нарушением функции почек не изучалось (см. ФК у особых групп пациентов).
Пациенты с нарушением функции печени. Безопасность и эффективность тоцилизумаба у пациентов с нарушением функции печени не изучались.
Способ применения
После разведения препарат Актемра® пациентам с РА, сЮИА, пЮИА и COVID-19 следует вводить в виде в/в инфузии в течение 1 часа.
Пациенты с РА, сЮИА, пЮИА и COVID-19 с массой тела ≥30 кг
Препарат Актемра®следует развести до объема 100 мл стерильным апирогенным раствором натрия хлорида 9 мг/мл (0,9%) с соблюдением правил асептики.
Инструкции по разведению лекарственного препарата перед введением представлены ниже.
Пациенты с сЮИА и пЮИА с массой тела <30 кг
Препарат Актемра®следует развести до объема 50 мл стерильным апирогенным раствором натрия хлорида 9 мг/мл (0,9%) с соблюдением правил асептики.
Инструкции по разведению лекарственного препарата перед введением представлены ниже.
При появлении у пациента признаков и симптомов инфузионной реакции следует уменьшить скорость инфузии или прекратить введение препарата и немедленно назначить соответствующие препараты/поддерживающую терапию (см. «Особые указания»).
Приготовление раствора лекарственного препарата
Препарат Актемра® должен вводиться медицинским персоналом. Препарат предназначен для введения как в амбулаторно-поликлинических, так и в стационарных условиях.
Препарат Актемра® в лекарственной форме для внутривенного введения не предназначен для подкожного введения!
Подготовка препарата к введению должна проводиться в асептических условиях.
Перед введением необходимо осмотреть приготовленный раствор на предмет отсутствия посторонних частиц или изменения окраски.
Следует вводить только прозрачный или опалесцирующий бесцветный или светло-желтый раствор без видимых посторонних частиц.
Следует использовать стерильную иглу и шприц для приготовления раствора для инфузий препарата Актемра®.
Пациенты с РА и COVID-19
1. Рассчитать количество препарата, необходимое для введения пациенту (из расчета 0,4 мл/кг).
2. В асептических условиях из инфузионного флакона (пакета), содержащего 100 мл 0,9% раствора натрия хлорида (раствор должен быть стерильным и апирогенным), отобрать одноразовым стерильным шприцем количество 0,9% раствора натрия хлорида, равное рассчитанному для введения количеству препарата Актемра®.
3. Другим одноразовым стерильным шприцем в асептических условиях из флакона с препаратом Актемра® отобрать рассчитанное количество препарата и ввести его в инфузионный флакон (пакет) с 0,9% раствором натрия хлорида; в результате объем приготовленного раствора должен быть равным 100 мл.
4. Для перемешивания аккуратно перевернуть флакон (пакет) во избежание пенообразования.
Пациенты с пЮИА и сЮИА с массой тела ≥30 кг
1. Рассчитать количество препарата, необходимое для введения пациенту (из расчета 0,4 мл/кг).
2. В асептических условиях из инфузионного флакона (пакета), содержащего 100 мл 0,9% раствора натрия хлорида (раствор должен быть стерильным и апирогенным), отобрать одноразовым стерильным шприцем количество 0,9% раствора натрия хлорида, равное рассчитанному для введения количеству препарата Актемра®.
3. Другим одноразовым стерильным шприцем в асептических условиях из флакона с препаратом Актемра® отобрать рассчитанное количество препарата и ввести его в инфузионный флакон (пакет) с 0,9% раствором натрия хлорида; в результате объем приготовленного раствора должен быть равным 100 мл.
4. Для перемешивания аккуратно перевернуть флакон (пакет) во избежание пенообразования.
Пациенты с пЮИА с массой тела <30 кг
1. Рассчитать количество препарата, необходимое для введения пациенту (из расчета 0,5 мл/кг).
2. В асептических условиях из инфузионного флакона (пакета), содержащего 50 мл 0,9% раствора натрия хлорида (раствор должен быть стерильным и апирогенным), отобрать одноразовым стерильным шприцем количество 0,9% раствора натрия хлорида, равное количеству, рассчитанному для введения препарата Актемра®.
3. Другим одноразовым стерильным шприцем в асептических условиях из флакона с препаратом Актемра® отобрать рассчитанное количество препарата и ввести его в инфузионный флакон (пакет) с 0,9% раствором натрия хлорида; в результате объем приготовленного раствора должен быть равным 50 мл.
4. Для перемешивания аккуратно перевернуть флакон (пакет) во избежание пенообразования.
Пациенты с сЮИА с массой тела <30 кг
1. Рассчитать количество препарата, необходимое для введения пациенту (из расчета 0,6 мл/кг).
2. В асептических условиях из инфузионного флакона (пакета), содержащего 50 мл 0,9% раствора натрия хлорида (раствор должен быть стерильным и апирогенным), отобрать одноразовым стерильным шприцем количество 0,9% раствора натрия хлорида, равное рассчитанному для введения количеству препарата Актемра®.
3. Другим одноразовым стерильным шприцем в асептических условиях из флакона с препаратом Актемра® отобрать рассчитанное количество препарата и ввести его в инфузионный флакон (пакет) с 0,9% раствором натрия хлорида; в результате объем приготовленного раствора должен быть равным 50 мл.
4. Для перемешивания аккуратно перевернуть флакон (пакет) во избежание пенообразования.
Препарат Актемра® предназначен только для однократного применения.
Правила хранения приготовленного раствора
Приготовленный инфузионный раствор препарата Актемра® физически и химически стабилен в 0,9% растворе натрия хлорида в течение 24 ч при температуре 30 °С.
С микробиологической точки зрения приготовленный раствор должен быть использован немедленно.
Если препарат не используется сразу, то время и условия хранения приготовленного раствора являются ответственностью пользователя и не должны превышать 24 ч при температуре от 2 до 8 °С (хранить в холодильнике) и только в том случае, если приготовление раствора проводилось в контролируемых и валидируемых асептических условиях.
Инструкция по уничтожению неиспользованного препарата, а также по истечении срока годности
Попадание лекарственных препаратов в окружающую среду должно быть сведено к минимуму. Не следует утилизировать препарат с помощью сточных вод или вместе с бытовыми отходами. По возможности необходимо использовать специальные системы для утилизации лекарственных препаратов.
Побочные действия
Резюме профиля безопасности
Наиболее часто отмечавшимися нежелательными реакциями (наблюдались у ≥5% пациентов, получавших тоцилизумаб в виде монотерапии или в комбинации с БПВП для лечения РА, сЮИА и пЮИА) были инфекции верхних дыхательных путей, назофарингит, головная боль, артериальная гипертензия и повышение активности АЛТ.
Наиболее серьезными нежелательными реакциями были серьезные инфекции, осложнения дивертикулита и реакции гиперчувствительности.
Наиболее часто отмечавшимися нежелательными реакциями (наблюдались у ≥5% пациентов, получавших тоцилизумаб для лечения COVID-19) были повышение активности печеночных трансаминаз, запор и инфекция мочевыводящих путей.
Нежелательные реакции, выявленные в ходе клинических исследований и/или при пострегистрационном применении препарата Актемра® на основании спонтанных сообщений, случаев, описанных в литературных источниках, и случаев, наблюдаемых в рамках программ неинтервенционных исследований, представлены в таблицах 5 и 6 в соответствии с системно-органной классификацией медицинского словаря для нормативно-правовой деятельности MedDRA. Для описания частоты развития нежелательных реакций используются следующие категории: очень часто (≥1/10); часто (≥1/100, но <1/10), нечасто (≥1/1000, но <1/100); редко (≥1/10000, но <1/1000); очень редко (<1/10000). В каждой группе (по частоте возникновения) нежелательные реакции представлены в порядке убывания степени их серьезности.
РА
Профиль безопасности тоцилизумаба был изучен в 4 плацебо-контролируемых исследованиях (исследования II, III, IV и V), 1 контролируемом исследовании с применением МТ (исследование I) и в ходе расширенных периодов к данным исследованиям (см. «Фармакодинамика»).
Двойной слепой контролируемый период исследования составил 6 месяцев в четырех исследованиях (исследования I, III, IV и V) и до 2 лет в одном исследовании (исследование II). В двойных слепых контролируемых исследованиях 774 пациента получали тоцилизумаб в дозе 4 мг/кг в комбинации с МТ, 1870 пациентов получали тоцилизумаб в дозе 8 мг/кг в комбинации с МТ или другими БПВП и 288 пациентов получали тоцилизумаб в дозе 8 мг/кг в качестве монотерапии.
Популяция пациентов с длительной экспозицией препарата включает всех пациентов, которые получили по меньшей мере одну дозу тоцилизумаба во время двойного слепого контролируемого периода или во время открытого расширенного периода. Из 4009 пациентов в данной популяции 3577 пациентов получали терапию в течение по меньшей мере 6 месяцев, 3296 пациентов — в течение по меньшей мере одного года, 2806 пациентов — в течение по меньшей мере 2 лет и 1222 пациента — в течение 3 лет.
Таблица 5
Перечень нежелательных реакций, наблюдавшихся у пациентов с РА, получавших тоцилизумаб в качестве монотерапии или в комбинации с МТ или другими БПВП в период проведения двойного слепого контролируемого исследования или при пострегистрационном применении
| Системно-органная классификация | Категории частоты развития нежелательных реакций, представленных с использованием терминов предпочтительного употребления | |||
| Очень часто | Часто | Нечасто | Редко/Очень редко | |
| Инфекции и инвазии | Инфекции верхних дыхательных путей | Воспаление подкожной клетчатки, пневмония, простой герпес полости рта, опоясывающий лишай (Herpes zoster) | Дивертикулит | |
| Нарушения со стороны крови и лимфатической системы | Лейкопения, нейтропения, гипофибриногенемия | |||
| Нарушения со стороны иммунной системы | Анафилаксия (с летальным исходом)2,3,4 | |||
| Эндокринные нарушения | Гипотиреоз | |||
| Нарушения метаболизма и питания | Гиперхолестеринемия1 | Гипертриглицеридемия | ||
| Нарушения со стороны нервной системы | Головная боль, головокружение | |||
| Нарушения со стороны органа зрения | Конъюнктивит | |||
| Нарушения со стороны сосудов | Повышение артериального давления | |||
| Нарушения со стороны дыхательной системы, органов грудной клетки и средостения | Кашель, одышка | |||
| Желудочно-кишечные нарушения | Боль в животе, язвенный стоматит, гастрит | Стоматит, язва желудка | ||
| Нарушения со стороны печени и желчевыводящих путей | Лекарственное поражение печени, гепатит, желтуха; очень редко — печеночная недостаточность | |||
| Нарушения со стороны кожи и подкожных тканей | Сыпь, зуд, крапивница | Синдром Стивенса-Джонсона4 | ||
| Нарушения со стороны почек и мочевыводящих путей | Нефролитиаз | |||
| Общие нарушения и реакции в месте введения | Периферический отек, реакции гиперчувствительности | |||
| Лабораторные и инструментальные данные | Повышение активности печеночных трансаминаз, увеличение массы тела, повышение общего билирубина1 |
1Включены повышения уровней, собранные в рамках рутинного мониторинга лабораторных показателей (см. текст ниже).
2См. «Противопоказания».
3См. «Особые указания».
4Данная нежелательная реакция была выявлена при пострегистрационном применении, но не наблюдалась в контролируемых клинических исследованиях. Категория частоты была рассчитана исходя из верхней границы 95% доверительного интервала, вычисленного на основании общего количества пациентов, получавших тоцилизумаб в клинических исследованиях.
Описания отдельных нежелательных реакций
Инфекции
В 6-месячных контролируемых исследованиях частота возникновения всех инфекций среди пациентов, получавших тоцилизумаб в дозе 8 мг/кг + БПВП, составила 127 явлений на 100 пациенто-лет по сравнению с 112 явлениями на 100 пациенто-лет в группе пациентов, получавших плацебо + БПВП. В популяции пациентов с длительной экспозицией препарата общая частота возникновения инфекций на фоне терапии препаратом Актемра® составила 108 явлений на 100 пациенто-лет экспозиции.
В 6-месячных контролируемых клинических исследованиях частота возникновения серьезных инфекций среди пациентов, получавших тоцилизумаб в дозе 8 мг/кг + БПВП, составила 5,3 явления на 100 пациенто-лет экспозиции по сравнению с 3,9 явления на 100 пациенто-лет экспозиции в группе пациентов, получавших плацебо + БПВП. В исследовании монотерапии частота возникновения серьезных инфекций составила 3,6 явления на 100 пациенто-лет экспозиции в группе пациентов, получавших тоцилизумаб, и 1,5 явления на 100 пациенто-лет экспозиции в группе пациентов, получавших МТ.
В популяции пациентов с длительной экспозицией препарата общая частота возникновения серьезных инфекций (бактериальных, вирусных и грибковых) составила 4,7 явления на 100 пациенто-лет экспозиции. Серьезные инфекции, некоторые из которых были с летальным исходом, включали активный туберкулез в легочной или внелегочной форме, инвазивные легочные инфекции, включая кандидоз, аспергиллез, кокцидиоидомикоз и пневмоцистную пневмонию, пневмонию, воспаление подкожной клетчатки, опоясывающий лишай (Herpes zoster), гастроэнтерит, дивертикулит, сепсис и бактериальный артрит. Сообщалось о случаях возникновения оппортунистических инфекций.
Интерстициальное заболевание легких
Нарушение функции легких может повысить риск развития инфекций. При пострегистрационном применении препарата были получены сообщения о развитии интерстициального заболевания легких (включая пневмонит и фиброз легких); некоторые из этих случаев привели к летальному исходу.
Перфорация ЖКТ
На протяжении 6-месячных контролируемых клинических исследований общая частота возникновения явлений, связанных с перфорацией ЖКТ, составила 0,26 явления на 100 пациенто-лет у пациентов, получавших терапию тоцилизумабом. В популяции пациентов с длительной экспозицией препарата общая частота возникновения явлений, связанных с перфорацией ЖКТ, составила 0,28 явления на 100 пациенто-лет. Случаи перфорации ЖКТ у пациентов, получавших тоцилизумаб, в основном, как отмечалось, были представлены в виде осложнений дивертикулита, включая генерализованный гнойный перитонит, перфорацию нижних отделов ЖКТ, свищ и абсцесс.
Инфузионные реакции
В 6-месячных контролируемых исследованиях нежелательные явления, связанные с инфузиями (отдельные явления, возникшие во время инфузии или в течение 24 часов после инфузии), отмечались у 6,9% пациентов в группе, получавшей тоцилизумаб в дозе 8 мг/кг + БПВП, и у 5,1% пациентов в группе, получавшей плацебо + БПВП. Явления, возникшие во время инфузии, преимущественно представляли собой эпизоды повышения артериального давления; явления, возникшие в течение 24 часов после завершения инфузии, представляли собой головную боль и реакции со стороны кожи (сыпь, крапивница). Эти реакции не приводили к ограничению терапии.
Частота возникновения анафилактических реакций (которые наблюдались в общей сложности у 8 из 4009 пациентов, 0,2%) была в несколько раз выше в группе, получавшей препарат в дозе 4 мг/кг, в сравнении с группой, получавшей препарат в дозе 8 мг/кг.
Клинически значимые реакции гиперчувствительности, связанные с введением тоцилизумаба и потребовавшие прекращения терапии, отмечались в общей сложности у 56 из 4009 пациентов (1,4%), получавших тоцилизумаб в ходе контролируемых и открытых клинических исследований. Данные реакции наблюдались, как правило, в период между второй и пятой инфузией тоцилизумаба (см. «Особые указания»). При пострегистрационном применении тоцилизумаба отмечались случаи анафилаксии с летальным исходом (см. «Особые указания»).
Иммуногенность
В общей сложности у 2876 пациентов были проведены анализы на антитела к тоцилизумабу в рамках 6-месячных контролируемых клинических исследований. Из 46 пациентов (1,6%) с антителами к тоцилизумабу в 6 случаях отмечалась значимая лекарственная реакция гиперчувствительности, приведшая в 5 случаях к прекращению лечения. У 30 пациентов (1,1%) выработались нейтрализующие антитела.
Отклонения показателей общего анализа крови
Нейтрофилы. В 6-месячных контролируемых исследованиях явления снижения числа нейтрофилов до уровня ниже 1·109/л отмечались у 3,4% пациентов, получавших тоцилизумаб в дозе 8 мг/кг + БПВП, в сравнении с <0,1% пациентов, получавших плацебо + БПВП. Примерно у половины пациентов снижение АЧН ниже 1·109/л возникло в пределах 8 недель после начала терапии. О снижении числа нейтрофилов ниже 0,5·109/л сообщалось у 0,3% пациентов, получавших тоцилизумаб в дозе 8 мг/кг + БПВП. Сообщалось о случаях инфекций, сопровождавшихся нейтропенией.
Во время двойного слепого контролируемого периода и при длительной экспозиции характер и частота возникновения явлений, связанных с уменьшением показателя нейтрофилов, оставались такими же, как и в 6-месячных контролируемых клинических исследованиях.
Тромбоциты. В 6-месячных контролируемых исследованиях явления снижения числа тромбоцитов до уровня ниже 100·103/мкл отмечались у 1,7% пациентов, получавших тоцилизумаб в дозе 8 мг/кг + БПВП, в сравнении с <1% пациентов, получавших плацебо + БПВП. Эти явления снижения уровня тромбоцитов не сопровождались развитием эпизодов кровотечений.
Во время двойного слепого контролируемого периода и при длительной экспозиции характер и частота возникновения явлений, связанных с уменьшением числа тромбоцитов, оставались такими же, как и в 6-месячных контролируемых клинических исследованиях.
При пострегистрационном применении в очень редких случаях сообщалось об эпизодах панцитопении.
Повышение активности печеночных трансаминаз. В ходе 6-месячных контролируемых исследований наблюдалось транзиторное повышение показателей АЛТ/АСТ выше 3× ВГН у 2,1% пациентов, получавших тоцилизумаб в дозе 8 мг/кг, в сравнении с 4,9% пациентов, получавших МТ, и у 6,5% пациентов, получавших тоцилизумаб в дозе 8 мг/кг + БПВП, в сравнении с 1,5% пациентов, получавших плацебо + БПВП. Присоединение к монотерапии тоцилизумабом препаратов, обладающих потенциальным гепатотоксическим действием (например, МТ), приводило к увеличению частоты случаев повышения активности трансаминаз. Повышение показателей АЛТ/АСТ более чем в 5 раз относительно ВГН наблюдалось у 0,7% пациентов, получавших монотерапию тоцилизумабом, и у 1,4% пациентов, получавших тоцилизумаб + БПВП; в большинстве из этих случаев терапия тоцилизумабом была отменена.
В течение двойного слепого контролируемого периода исследования частота случаев повышения уровня непрямого билирубина выше ВГН, оцениваемых в рамках рутинного мониторинга лабораторных показателей, составила 6,2% у пациентов, получавших тоцилизумаб в дозе 8 мг/кг + БПВП. У 5,8% пациентов наблюдалось повышение уровня непрямого билирубина в диапазоне от >1 до 2×ВГН, а у 0,4% — >2×ВГН.
Во время двойного слепого контролируемого периода и при длительной экспозиции характер и частота возникновения явлений, связанных с повышением активности АЛТ/АСТ, оставались такими же, как и в 6-месячных контролируемых клинических исследованиях.
Показатели липидного обмена. В ходе 6-месячных контролируемых исследований часто сообщалось о повышении показателей липидного обмена, таких как общий холестерин, триглицериды, ЛПНП и/или ЛПВП. При рутинном мониторинге лабораторных показателей примерно у 24% пациентов, получавших препарат Актемра® в рамках проведения клинических исследований, наблюдалось стойкое повышение уровня общего холестерина ≥6,2 ммоль/л, а у 15% — стойкое повышение уровня ЛПНП до ≥4,1 ммоль/л. Повышение, наблюдавшееся в показателях липидного обмена, реагировало на лечение гиполипидемическими препаратами.
Во время двойного слепого контролируемого периода и при длительной экспозиции характер и частота возникновения явлений, связанных с повышением показателей, характеризующих липидный обмен, оставались такими же, как и в 6-месячных контролируемых клинических исследованиях.
Злокачественные новообразования
Клинических данных недостаточно для оценки потенциальной частоты возникновения злокачественных новообразований после применения тоцилизумаба. Оценка долгосрочной безопасности терапии продолжается.
Кожные реакции
При пострегистрационном применении в редких случаях сообщалось об эпизодах синдрома Стивенса-Джонсона.
COVID-19
Оценка безопасности применения препарата Актемра® у пациентов с COVID-19 была основана на результатах, полученных в 3 рандомизированных двойных слепых плацебо-контролируемых исследованиях (исследования ML42528, WA42380 и WA42511).
В общей сложности 974 пациента получили терапию препаратом Актемра® в рамках проведения данных исследований. Сбор данных по безопасности в рамках проведения исследования RECOVERY был ограничен и здесь не представлен.
Следующие нежелательные реакции, перечисленные в соответствии с системно-органной классификацией медицинского словаря для нормативно-правовой деятельности MedDRA в таблице 6, были отнесены к событиям, которые наблюдались не менее чем у 3% пациентов, получавших терапию препаратом Актемра®, и чаще, чем у пациентов, получавших плацебо, в объединенной популяции пациентов для оценки безопасности применения препарата в рамках проведения клинических исследований ML42528, WA42380 и WA42511.
Таблица 6
Перечень нежелательных реакций1, выявленных в объединенной популяции для оценки безопасности в рамках проведения клинических исследований препарата Актемра® у пациентов COVID-192
| Системно-органный класс | Часто |
| Инфекции и инвазии | Инфекция мочевыводящих путей |
| Нарушения метаболизма и питания | Гипокалиемия |
| Психические нарушения | Тревожность, бессонница |
| Нарушения со стороны сосудов | Повышение артериального давления |
| Желудочно-кишечные нарушения | Запор, диарея, тошнота |
| Нарушения со стороны печени и желчевыводящих путей | Повышение активности печеночных трансаминаз |
1Пациенты учитываются один раз в каждой категории независимо от количества реакций.
2Включены реакции, о которых сообщалось в исследованиях WA42511, WA42380 и ML42528.
Описание отдельных нежелательных реакций
Инфекции
В объединенной популяции пациентов для оценки безопасности в ходе проведения исследований ML42528, WA42380 и WA42511 частота событий, связанных с инфекциями/серьезными инфекциями, была сбалансирована между пациентами с COVID-19, получавшими тоцилизумаб (30,3/18,6%, n=974) и плацебо (32,1/22,8%, n=483).
Профиль безопасности, наблюдаемый на исходном уровне в группе, получавшей лечение системными ГКС, соответствовал профилю безопасности применения тоцилизумаба в общей популяции, представленному в таблице 6. В данной подгруппе инфекции и серьезные инфекции наблюдались у 27,8 и 18,1% пациентов, получавших тоцилизумаб в/в, и у 30,5 и 22,9% пациентов, получавших плацебо, соответственно.
Изменения лабораторных показателей
Частота изменений, наблюдаемых в лабораторных показателях, была в целом сходной между пациентами с COVID-19, получившими в/в одну или две дозы препарата Актемра®, по сравнению с теми, кто получал плацебо в рандомизированных двойных слепых плацебо-контролируемых исследованиях, за редким исключением. Снижение числа тромбоцитов и нейтрофилов, а также повышение активности АЛТ и АСТ чаще наблюдалось у пациентов, получавших препарат Актемра®, по сравнению с плацебо (см. «Способ применения и дозы» и «Особые указания»).
сЮИА и пЮИА
Профиль безопасности применения тоцилизумаба в популяции детей обобщен ниже в разделах, касающихся пЮИА и сЮИА. В целом, нежелательные реакции у пациентов с пЮИА и сЮИА были схожи по типу с теми, которые наблюдались у пациентов с РА; см. «Побочные действия» выше.
Нежелательные реакции у пациентов с пЮИА и сЮИА, получавших тоцилизумаб, перечислены в таблице 7 и представлены в соответствии с системно-органной классификацией медицинского словаря для нормативно-правовой деятельности MedDRA. Для описания частоты развития нежелательных реакций используются следующие категории: очень часто (≥1/10); часто (≥1/100, но <1/10) и нечасто (≥1/1000, но <1/100).
Таблица 7
Перечень нежелательных реакций, наблюдавшихся у пациентов с сЮИА или пЮИА, получавших тоцилизумаб в качестве монотерапии или в комбинации с МТ
| Системно-органный класс | Термин предпочтительного употребления | Частота возникновения | ||
| Очень часто | Часто | Нечасто | ||
| Инфекции и инвазии | ||||
| Инфекции верхних дыхательных путей | пЮИА, сЮИА | |||
| Назофарингит | пЮИА, сЮИА | |||
| Нарушения со стороны нервной системы | ||||
| Головная боль | пЮИА | сЮИА | ||
| Желудочно-кишечные нарушения | ||||
| Тошнота | пЮИА | |||
| Диарея | пЮИА, сЮИА | |||
| Общие нарушения и реакции в месте введения | ||||
| Инфузионные реакции | пЮИА1, сЮИА2 | |||
| Лабораторные и инструментальные данные | ||||
| Повышение активности печеночных трансаминаз | пЮИА | |||
| Снижение числа нейтрофилов | сЮИА | пЮИА | ||
| Снижение числа тромбоцитов | сЮИА | пЮИА | ||
| Повышение уровня холестерина | сЮИА | пЮИА |
1Инфузионные реакции у пациентов с пЮИА включали головную боль, тошноту и повышение артериального давления, но не ограничивались ими.
2Инфузионные реакции у пациентов с сЮИА включали сыпь, крапивницу, диарею, дискомфорт в эпигастрии, артралгию и головную боль, но не ограничивались ими.
пЮИА
Профиль безопасности препарата Актемра® в/в при пЮИА был изучен у 188 пациентов от 2 до 17 лет. Общая продолжительность воздействия препарата на пациентов составила 184,4 пациенто-лет. Частота развития нежелательных реакций у пациентов с пЮИА представлена в таблице 7. Типы нежелательных реакций, наблюдавшихся у пациентов с пЮИА, были аналогичны тем, которые наблюдались у пациентов с РА и сЮИА (см. «Побочные действия» выше). По сравнению с популяцией взрослых пациентов с РА в популяции пациентов с пЮИА чаще регистрировались такие явления, как назофарингит, головная боль, тошнота и снижение числа нейтрофилов. Случаи повышения уровня холестерина в популяции пациентов с пЮИА отмечались реже, чем в популяции взрослых пациентов с РА.
Инфекции
Частота возникновения инфекций в популяции всех пациентов, получавших тоцилизумаб, составила 163,7 явления на 100 пациенто-лет. Наиболее часто регистрируемыми явлениями были назофарингит и инфекции верхних дыхательных путей. Частота возникновения серьезных инфекций была численно выше у пациентов с массой тела <30 кг, получавших тоцилизумаб в дозе 10 мг/кг (12,2 явления на 100 пациенто-лет), в сравнении с пациентами с массой тела ≥30 кг, получавшими тоцилизумаб в дозе 8 мг/кг (4,0 явления на 100 пациенто-лет). Частота возникновения инфекций, которые привели к прерыванию терапии, также была численно выше среди пациентов с массой тела <30 кг, получавших тоцилизумаб в дозе 10 мг/кг (21,%), в сравнении с пациентами с массой тела ≥30 кг, получавшими тоцилизумаб в дозе 8 мг/кг (7,6%).
Инфузионные реакции
У пациентов с пЮИА инфузионные реакции определяют как все явления, развившиеся во время инфузии или в течение 24 часов после инфузии. В популяции всех пациентов, получавших тоцилизумаб, у 11 пациентов (5,9%) развились инфузионные реакции во время инфузии, а у 38 пациентов (20,2%) данное явление развилось в течение 24 часов после инфузии. Наиболее частыми явлениями, развившимися во время инфузии, были головная боль, тошнота и гипотензия, а наиболее частыми явлениями, развившимися в течение 24 часов после инфузии, были головокружение и гипотензия. В целом нежелательные реакции, наблюдавшиеся во время инфузии или в течение 24 часов после нее, были сходными по характеру с нежелательными реакциями, наблюдавшимися у пациентов с РА и сЮИА (см. «Побочные действия» выше).
О клинически значимых реакциях гиперчувствительности, связанных с тоцилизумабом и требующих прекращения лечения, не сообщалось.
Иммуногенность
У одного пациента из группы, получавшей тоцилизумаб в дозе 10 мг/кг, с массой тела <30 кг, был получен положительный результат анализа на антитела к тоцилизумабу, без развития реакции гиперчувствительности; впоследствии этот пациент был исключен из исследования.
Нейтрофилы
В ходе рутинного мониторинга лабораторных показателей в популяции всех пациентов, получавших тоцилизумаб, снижение числа нейтрофилов до уровня ниже 1·109/л наблюдалось у 3,7% пациентов.
Тромбоциты
В ходе рутинного мониторинга лабораторных показателей в популяции всех пациентов, получавших тоцилизумаб, у 1% пациентов наблюдалось снижение числа тромбоцитов до уровня ≤50·103/мкл, которое не сопровождалось развитием эпизодов кровотечений.
Повышение активности печеночных трансаминаз
В ходе рутинного мониторинга лабораторных показателей в популяции всех пациентов, получавших тоцилизумаб, явления, связанные с повышением активности АЛТ или АСТ до уровня ≥3×ВГН, наблюдались у 3,7 и <1% пациентов соответственно.
Показатели липидного обмена
В ходе рутинного мониторинга лабораторных показателей, выполняемого в рамках проведения исследования препарата Актемра® в/в (исследование WA19977), у 3,4 и 10,4% пациентов наблюдалось повышение ЛПНП до уровня ≥130 мг/дл и общего холестерина до уровня ≥200 мг/дл в любой временной точке в ходе терапии, выполняемой в рамках исследования, соответственно, по сравнению с исходным уровнем.
сЮИА
Профиль безопасности препарата Актемра® в/в при сЮИА был изучен у 112 пациентов от 2 до 17 лет. В 12-недельной двойной слепой контролируемой части исследования 75 пациентов получали терапию тоцилизумабом (8 или 12 мг/кг в зависимости от массы тела). По прошествии 12 недель или в момент перехода на терапию препаратом Актемра® из-за ухудшения течения заболевания пациенты получили лечение в рамках открытого расширенного периода исследования.
В целом нежелательные реакции у пациентов с сЮИА были схожи по типу с теми, которые наблюдались у пациентов с РА (см. «Побочные действия» выше). Частота развития нежелательных реакций у пациентов с сЮИА представлена в таблице 7. По сравнению с популяцией взрослых пациентов с РА, у пациентов с сЮИА чаще наблюдались назофарингит, снижение числа нейтрофилов, повышение активности печеночных трансаминаз и диарея. Случаи повышения уровня холестерина в популяции пациентов с сЮИА отмечались реже, чем в популяции взрослых пациентов с РА.
Инфекции
В 12-недельной контролируемой фазе исследования частота возникновения всех инфекций в группе пациентов, получавших препарат Актемра® в/в, составила 344,7 случая на 100 пациенто-лет и 287,0 случая на 100 пациенто-лет в группе пациентов, получавших плацебо. В ходе открытого расширенного периода исследования (часть II) общая частота возникновения инфекций осталась сходной и составила 306,6 случая на 100 пациенто-лет.
В 12-недельной контролируемой фазе исследования частота возникновения серьезных инфекций в группе пациентов, получавших в/в препарат Актемра®, составила 11,5 случая на 100 пациенто-лет. Через один год в ходе открытого расширенного периода исследования общая частота возникновения серьезных инфекций осталась стабильной и составила 11,3 случая на 100 пациенто-лет. Серьезные инфекции были сходными с серьезными инфекциями, наблюдавшимися у пациентов с РА, дополнительно отмечались случаи ветряной оспы и отита среднего уха.
Инфузионные реакции
Инфузионные реакции определяют как все явления, развившиеся во время инфузии или в течение 24 часов после нее. В 12-недельной контролируемой фазе исследования у 4% пациентов из группы, получавшей тоцилизумаб, отмечались явления, произошедшие во время инфузии. Одно явление (ангионевротический отек) было оценено как серьезное и жизнеугрожающее, и пациент был исключен из исследования.
В 12-недельной контролируемой фазе исследования у 16% пациентов из группы, получавшей тоцилизумаб, и у 5,4% пациентов из группы, получавшей плацебо, инфузионная реакция развилась в течение 24 часов после инфузии. В группе, получавшей тоцилизумаб, явления включали сыпь, крапивницу, диарею, дискомфорт в эпигастрии, артралгию и головную боль (но не ограничиваясь ими). Одно из этих явлений (крапивница) было оценено как серьезное.
Клинически значимые реакции гиперчувствительности, связанные с введением тоцилизумаба и потребовавшие прекращения терапии, отмечались у 1 из 112 пациентов (<1%), получавших тоцилизумаб в ходе контролируемого исследования, включая открытое клиническое исследование.
Иммуногенность
У всех 112 пациентов на исходном уровне был проведен анализ на антитела к тоцилизумабу. У двух пациентов были обнаружены антитела к тоцилизумабу, при этом у одного из этих пациентов развилась реакция гиперчувствительности, которая привела к прекращению терапии. Частота образования антител к тоцилизумабу может быть недооценена из-за влияния тоцилизумаба на результаты анализа и более высокой концентрации препарата, наблюдаемой у детей по сравнению со взрослыми.
Нейтрофилы
В ходе рутинного мониторинга лабораторных показателей, выполняемого в рамках 12-недельной контролируемой фазы исследования, снижение числа нейтрофилов до уровня ниже 1·109/л наблюдалось у 7% пациентов из группы, получавшей тоцилизумаб; в группе, получавшей плацебо, такого снижения не наблюдалось.
В ходе открытого расширенного периода исследования уменьшение числа нейтрофилов до уровня ниже 1·109/л наблюдалось у 15% пациентов из группы, получавшей тоцилизумаб.
Тромбоциты
В ходе рутинного мониторинга лабораторных показателей, выполняемого в рамках 12-недельной контролируемой фазы исследования, у 3% пациентов из группы, получавшей плацебо, и у 1% пациентов из группы, получавшей тоцилизумаб, наблюдалось снижение числа тромбоцитов до уровня ≤100·103/мкл.
В ходе открытого расширенного периода исследования у 3% пациентов из группы, получавшей тоцилизумаб, наблюдалось снижение числа тромбоцитов до уровня ниже 100·103/мкл, которое не сопровождалось развитием эпизодов кровотечений.
Повышение активности печеночных трансаминаз
В ходе рутинного мониторинга лабораторных показателей, выполняемого в рамках 12-недельной контролируемой фазы исследования, явления, связанные с повышением активности АЛТ или АСТ до уровня ≥3×ВГН, наблюдались у 5 и 3% пациентов соответственно в группе, получавшей тоцилизумаб, и у 0% пациентов в группе, получавшей плацебо.
В ходе открытого расширенного периода исследования явления, связанные с повышением активности АЛТ или АСТ до уровня ≥3×ВГН, наблюдались у 12 и 4% пациентов соответственно в группе, получавшей тоцилизумаб.
Иммуноглобулин G
Уровень IgG снижается во время терапии. Снижение до нижней границы нормы было отмечено у 15 пациентов в определенный момент исследования.
Показатели липидного обмена
В ходе рутинного мониторинга лабораторных показателей, выполняемого в рамках 12-недельной контролируемой фазы исследования (исследование WA18221), у 13,4 и 33,3% пациентов наблюдалось повышение ЛПНП до уровня ≥130 мг/дл и общего холестерина до уровня ≥200 мг/дл в любой временной точке в ходе терапии, выполняемой в рамках исследования, соответственно, по сравнению с исходным уровнем.
В ходе открытого расширенного периода исследования (исследование WA18221) у 13,2 и 27,7% пациентов наблюдалось повышение ЛПНП до уровня ≥130 мг/дл и общего холестерина до уровня ≥200 мг/дл в любой временной точке в ходе терапии, выполняемой в рамках исследования, соответственно.
Взаимодействие
Реклама: ООО «ВЕДАНТА», ИНН 7714886235, erid 4CQwVszH9pUkKJ7jUDd
Реклама: ООО «РЛС-Библиомед» ИНН 7714758963
Реклама: ООО «ВЕДАНТА», ИНН 7714886235, erid 4CQwVszH9pUkKJ7jUDd
Реклама: ООО «РЛС-Библиомед» ИНН 7714758963
Исследования взаимодействий были проведены только у взрослых пациентов.
Одновременное однократное введение тоцилизумаба в дозе 10 мг/кг и МТ в дозе 10–25 мг один раз в неделю не оказывало клинически значимого влияния на экспозицию МТ.
Популяционные ФК-анализы не выявили какого-либо воздействия МТ, НПВП или ГКС на клиренс тоцилизумаба.
Экспрессия печеночных изоферментов системы CYP450 подавляется под действием цитокинов, таких как ИЛ-6, которые стимулируют хроническое воспаление. Таким образом, при проведении терапии средствами, ингибирующими действие цитокинов (например, тоцилизумаб), экспрессия изоферментов CYP450 может быть нарушена.
В исследованиях in vitro, проведенных на культуре гепатоцитов человека, было показано, что ИЛ-6 вызывает снижение экспрессии ферментов CYP1A2, CYP2C9, CYP2C19 и CYP3A4. Применение тоцилизумаба нормализует экспрессию этих изоферментов.
В исследовании у пациентов с РА концентрация симвастатина (CYP3A4) через 1 неделю после однократного введения тоцилизумаба снижалась на 57%, т.е. была немного повышенной или аналогичной таковой у здоровых добровольцев.
В начале или при завершении курса терапии тоцилизумабом следует наблюдать за пациентами, получающими лекарственные средства в индивидуально подобранных дозах и которые метаболизируются посредством изоферментов CYP450 3A4, 1A2 или 2C9 (например, метилпреднизолон, дексаметазон (с возможностью развития синдрома отмены ГКС, предназначенных для приема внутрь), аторвастатин, блокаторы кальциевых каналов, теофиллин, варфарин, фенпрокумон, фенитоин, циклоспорин или бензодиазепины), поскольку для поддержания терапевтического эффекта может потребоваться коррекция их дозы.
Учитывая длительный T1/2 тоцилизумаба, его действие на активность изоферментов CYP450 может сохраняться в течение нескольких недель после прекращения терапии.
Передозировка
Доступные данные о передозировке препарата Актемра® ограничены. В одном случае непреднамеренной передозировки препарата в дозе 40 мг/кг у пациента с множественной миеломой нежелательных реакций не отмечено. Не отмечалось также серьезных нежелательных реакций у здоровых добровольцев, которые получали однократно препарат Актемра® в дозе до 28 мг/кг, хотя наблюдалась нейтропения, требующая снижения дозы.
Особые указания
В медицинской документации пациента следует указывать торговое наименование препарата (Актемра®) и номер серии.
РА, пЮИА и сЮИА
Инфекции. У пациентов, получающих иммуносупрессанты (в т.ч. препарат Актемра®), отмечались серьезные случаи возникновения инфекций, некоторые из них сопровождались летальным исходом (см. «Побочные действия»). Не следует начинать лечение препаратом Актемра® пациентам с активными инфекциями (см. «Противопоказания»). Введение препарата Актемра® должно быть приостановлено в случае развития у пациента серьезной инфекции, до момента взятия инфекции под контроль (см. «Побочные действия»). Медицинским работникам следует соблюдать осторожность при рассмотрении вопроса о применении препарата Актемра® у пациентов с рецидивирующими или хроническими инфекциями в анамнезе, а также с сопутствующими заболеваниями (например, дивертикулитом, сахарным диабетом и интерстициальным заболеванием легких), предрасполагающими к развитию инфекций.
Следует проявлять особую осторожность с целью своевременного выявления серьезных инфекций у пациентов, получающих терапию биологическими препаратами, поскольку признаки и симптомы острого воспаления могут быть стерты в связи с подавлением реакции острой фазы. Следует учитывать влияние тоцилизумаба на уровень СРБ, число нейтрофилов и на признаки и симптомы развития инфекций при обследовании пациента на предмет возможного развития инфекции.
Необходимо проинструктировать пациентов (включая детей раннего возраста с сЮИА или пЮИА, которые не всегда способны описать симптомы) и родителей/опекунов пациентов с сЮИА или пЮИА о немедленном обращении к врачу при любых симптомах, свидетельствующих о появлении инфекции, с целью обеспечения быстрой диагностики и назначения необходимого лечения.
Туберкулез. Как и при назначении других биологических препаратов, перед началом терапии препаратом Актемра® пациенты с РА, сЮИА и пЮИА должны пройти обследование на латентный туберкулез. Пациенты, у которых был выявлен латентный туберкулез, должны пройти стандартный курс антимикобактериальной терапии перед началом лечения препаратом Актемра®. Лечащему врачу следует помнить о риске получения ложноотрицательных результатов туберкулиновой кожной пробы и квантиферонового теста, особенно у пациентов с тяжелыми заболеваниями или ослабленным иммунитетом.
Пациенты должны быть проинструктированы о необходимости обратиться к врачу, если признаки/симптомы (например, стойкий кашель, истощение/снижение массы тела, субфебрильная температура), указывающие на туберкулезную инфекцию, возникают во время или после терапии препаратом Актемра®.
Реактивация вирусных инфекций. Были описаны случаи реактивации вирусной инфекции (например, вирусного гепатита B) при применении биологических препаратов для лечения РА. Пациенты, имевшие положительный результат при скрининговом обследовании на гепатит, не включались в клинические исследования тоцилизумаба.
Осложнения дивертикулита. О случаях перфорации дивертикула, как осложнения дивертикулита при применении препарата Актемра® у пациентов с РА, сообщалось нечасто (см. «Побочные действия»). Следует соблюдать осторожность при применении препарата Актемра® у пациентов с язвенным поражением органов ЖКТ или дивертикулитом в анамнезе. Пациенты с симптомами, возможно указывающими на осложнения дивертикулита, такими как боль в животе, кровотечение и/или необъяснимые изменения в частоте и характере стула, сопровождающиеся повышением температуры тела, должны быть немедленно обследованы с целью раннего выявления дивертикулита, который может быть связан с перфорацией ЖКТ.
Реакции гиперчувствительности. При инфузии препарата Актемра® наблюдались серьезные реакции гиперчувствительности (см. «Побочные действия»). Такие реакции могут быть более тяжелыми и потенциально летальными у пациентов, у которых наблюдались реакции гиперчувствительности во время предшествующих инфузий, даже если они получали премедикацию стероидами и антигистаминными препаратами. Должно быть предусмотрено наличие необходимого оборудования и персонала для оказания экстренной помощи в случае развития анафилактической реакции во время терапии препаратом Актемра®. При возникновении анафилактической реакции или другой серьезной реакции гиперчувствительности/серьезной инфузионной реакции введение препарата Актемра® следует немедленно прекратить, при этом терапия препаратом Актемра® должна быть отменена.
Активные заболевания печени и печеночная недостаточность. Терапия препаратом Актемра®, особенно одновременно с МТ, может быть ассоциирована с повышением активности печеночных трансаминаз, поэтому следует проявлять осторожность при назначении терапии пациентам с активным заболеванием печени или печеночной недостаточностью (см. «Способ применения и дозы» и «Побочные действия»).
Гепатотоксичность. При лечении препаратом Актемра® часто наблюдалось преходящее или периодическое легкое и умеренное повышение активности печеночных трансаминаз (см. «Побочные действия»). Частота возникновения такого повышения возрастала при применении препарата Актемра® совместно с препаратами, обладающими потенциально гепатотоксическим действием (например, МТ). При наличии клинических показаний следует рассмотреть возможность выполнения других функциональных печеночных проб, включая оценку уровня билирубина.
При применении препарата Актемра® наблюдалось серьезное лекарственное поражение печени, включая острую печеночную недостаточность, гепатит и желтуху (см. «Побочные действия»). Серьезные поражения печени отмечались в интервале от 2 недель до >5 лет после начала терапии препаратом Актемра®. Сообщалось о случаях развития печеночной недостаточности, которые привели к трансплантации печени. Пациентам следует рекомендовать немедленно обратиться за медицинской помощью при появлении признаков и симптомов поражения печени.
Следует соблюдать осторожность при решении вопроса о начале терапии препаратом Актемра® у пациентов с показателями АЛТ или АСТ, превышающими ВГН более чем в 1,5 раза. Терапия препаратом Актемра® не рекомендуется при показателях АЛТ или
АСТ, превышающих ВГН более чем в 5 раз у пациентов с РА, пЮИА и сЮИА.
У пациентов с РА, пЮИА и сЮИА следует контролировать АЛТ/АСТ каждые 4–8 недель на протяжении первых 6 месяцев после начала терапии, а в дальнейшем — каждые 12 недель. Рекомендации по дозированию, а также отмене препарата Актемра® в зависимости от активности трансаминаз, представлены в разделе «Способ применения и дозы». Следует прекратить лечение препаратом Актемра® при повышении показателей АЛТ или АСТ в 3–5 раз выше ВГН, подтвержденном повторным анализом.
Отклонения показателей общего анализа крови. После лечения тоцилизумабом в дозе 8 мг/кг в комбинации с МТ наблюдалось снижение числа нейтрофилов и тромбоцитов (см. «Побочные действия»). Может быть повышен риск развития нейтропении у пациентов, которые ранее получали лечение антагонистом ФНО.
Пациентам, ранее не получавшим лечение препаратом Актемра®, не рекомендуется начинать лечение с АЧН менее 2·109/л. Следует проявлять осторожность при рассмотрении вопроса о начале лечения препаратом Актемра® у пациентов с низким уровнем тромбоцитов (т.е. с уровнем тромбоцитов ниже 100·103/мкл). У пациентов с РА, сЮИА и пЮИА с АЧН <0,5·109/л или числом тромбоцитов <50·103/мкл продолжать лечение не рекомендуется.
Тяжелая нейтропения может быть связана с повышенным риском развития серьезных инфекций, хотя до настоящего времени в клинических исследованиях препарата Актемра® не было выявлено четкой связи между снижением числа нейтрофилов и возникновением серьезных инфекций.
У пациентов с РА следует контролировать показатели нейтрофилов и тромбоцитов в период с 4-й по 8-ю неделю после начала терапии и в дальнейшем в соответствии со стандартами клинической практики. Рекомендации по коррекции дозы в зависимости от АЧН и уровня тромбоцитов представлены в разделе «Способ применения и дозы».
У пациентов с сЮИА и пЮИА показатели нейтрофилов и тромбоцитов следует контролировать в день проведения 2-й инфузии, а в дальнейшем в соответствии со стандартами клинической практики (см. «Способ применения и дозы»).
Показатели липидного обмена. У пациентов, получавших тоцилизумаб, наблюдалось повышение показателей липидного обмена, включая общий холестерин, ЛПНП, ЛПВП и триглицериды (см. «Побочные действия»). У большинства пациентов индекс атерогенности не повышался, а повышение концентрации общего холестерина эффективно корригировалось гиполипидемическими препаратами.
При РА, пЮИА и сЮИА следует оценивать показатели липидного обмена у пациентов в период с 4 по 8 неделю после начала терапии препаратом Актемра®. При ведении пациентов следует руководствоваться локальными рекомендациями по лечению гиперлипидемии.
Нарушения со стороны нервной системы. Врачи должны проявлять особую осторожность с целью раннего выявления симптомов, возможно указывающих на дебют демиелинизирующих заболеваний ЦНС. В настоящее время влияние препарата Актемра® на развитие демиелинизирующих заболеваний ЦНС не известно.
Злокачественные новообразования. У пациентов с РА повышен риск развития злокачественных новообразований. Иммуномодулирующие лекарственные препараты могут повышать риск развития злокачественных новообразований.
Иммунизация. Не следует проводить иммунизацию живыми и живыми ослабленными вакцинами одновременно с терапией препаратом Актемра®, поскольку клиническая безопасность подобного сочетания не установлена. В рандомизированном открытом исследовании у взрослых пациентов с РА, получавших терапию препаратом Актемра® и МТ, ответ на 23-валентную пневмококковую полисахаридную вакцину и столбнячный анатоксин был сопоставим с таковым у пациентов, получающих монотерапию МТ. Всем пациентам, особенно пациентам с сЮИА и пЮИА, рекомендуется пройти вакцинацию в соответствии с национальным календарем прививок до начала лечения препаратом Актемра®. Следует соблюдать интервал (в соответствии с действующим национальным календарем прививок) у пациентов, получающих терапию иммуносупрессивными препаратами, между иммунизацией живыми вакцинами и началом терапии препаратом Актемра®.
Риск развития сердечно-сосудистых заболеваний. У пациентов с РА имеется повышенный риск развития сердечно-сосудистых заболеваний, поэтому факторы риска (например, повышение артериального давления, гиперлипидемия) должны контролироваться в рамках стандартного лечения.
Комбинация с антагонистами ФНО. Опыт применения препарата Актемра® с антагонистами ФНО или другими биологическими препаратами для лечения пациентов с РА, сЮИА или пЮИА отсутствует. Не рекомендуется применять препарат Актемра® с другими биологическими препаратами.
Содержание натрия. Данный препарат содержит 1,17 ммоль (или 26,55 мг) натрия в пересчете на максимальную дозу 1200 мг. Необходимо учитывать пациентам, находящимся на диете с ограничением поступления натрия. Данный лекарственный препарат в дозах менее 1025 мг содержит менее 1 ммоль натрия (23 мг), т. е. практически не содержит натрий.
COVID-19
При новой коронавирусной инфекции COVID-19 препарат Актемра® следует применять в условиях стационара.
Эффективность применения препарата Актемра® не была установлена при лечении пациентов с COVID-19, у которых не был повышен уровень СРБ (см. «Фармакодинамика»).
Препарат Актемра® не должен назначаться пациентам с COVID-19, не получающим системные ГКС, поскольку в этой подгруппе нельзя исключить увеличение уровня смертности (см. «Фармакодинамика»).
Инфекции. Пациентам с COVID-19 не следует назначать препарат Актемра®, если у них имеется какая-либо другая сопутствующая тяжелая активная инфекция. Медицинским работникам следует соблюдать осторожность при применении препарата Актемра® у пациентов с рецидивирующими или хроническими инфекциями в анамнезе, а также при сопутствующих заболеваниях (например, при дивертикулите, сахарном диабете и интерстициальном заболевании легких), предрасполагающих к развитию инфекций.
Гепатотоксичность. У госпитализированных пациентов с COVID-19 может быть повышена активность АЛТ или АСТ. Полиорганная недостаточность с поражением печени признана осложнением тяжелой формы COVID-19. При принятии решения о применении тоцилизумаба следует сбалансировать потенциальную пользу, получаемую от лечения COVID-19, с потенциальным риском неотложной терапии тоцилизумабом. У пациентов с COVID-19 с повышением активности АЛТ или АСТ, превышающей ВГН более чем в 10 раз, применение препарата Актемра® не рекомендуется. У пациентов с COVID-19 следует мониторировать активность АЛТ/АСТ в соответствии с текущей стандартной клинической практикой.
Отклонения показателей общего анализа крови. У пациентов с COVID-19 с АЧН <1·109/л или числом тромбоцитов <50·103/мкл лечение не рекомендуется. Показатели нейтрофилов и тромбоцитов следует мониторировать в соответствии с текущей стандартной клинической практикой (см. «Способ применения и дозы»).
Дети
Синдром активации макрофагов у пациентов с сЮИА. Синдром активации макрофагов является серьезным жизнеугрожающим состоянием, которое может развиться у пациентов с сЮИА. В клинических исследованиях применение тоцилизумаба у пациентов в период возникновения синдрома активации макрофагов не изучалось.
Влияние на способность управлять транспортными средствами, механизмами. Исследования по изучению влияния препарата на способность управлять транспортными средствами и механизмами не проводились. Однако учитывая тот факт, что при терапии препаратом Актемра® часто наблюдалось головокружение, пациентам, испытывающим данную нежелательную реакцию, следует рекомендовать не управлять транспортными средствами и механизмами до тех пор, пока головокружение не прекратится.
Форма выпуска
Концентрат для приготовления раствора для инфузий, 20 мг/мл. По 4 мл (80 мг/4 мл), 10 мл (200 мг/10 мл) или 20 мл (400 мг/20 мл) препарата во флаконах, изготовленных из бесцветного стекла (гидролитический класс 1 ЕФ), укупоренных крышкой из бутилкаучука, обжатых алюминиевыми колпачками и закрытых пластмассовыми крышками; цвет колпачка и крышки соответствует цвету, которым выделена дозировка препарата на этикетке флакона и на пачке. 1 флакон вместе с инструкцией по применению помещают в картонную пачку с картонными вкладышами (перегородками) внутри.
С целью контроля первого вскрытия на пачку наносится защитная голографическая наклейка.
Упаковка на ОАО «Фармстандарт-УфаВИТА». 1 флакон помещают в пластиковый поддон или в картонный вкладыш, который вместе с инструкцией по медицинскому применению помещают в пачку из картона импортного.
С целью контроля первого вскрытия на пачку наклеивают самоклеящиеся круглые стикеры с надписью «Контроль вскрытия».
Производитель
Производитель. Чугай Фарма Мануфектуринг Ко. Лтд., Япония/Chugai Pharma Manufacturing Co. Ltd, 16-3, Kiyohara Kogyodanchi, Utsunomiya city, Tochigi, Japan.
Владелец регистрационного удостоверения. Ф. Хоффманн-Ля Рош Лтд., Швейцария/F. Hoffmann-La Roche Ltd, Grenzacherstrasse 124, 4070 Basel, Switzerland.
Организация, принимающая претензии потребителя. Претензии потребителей направлять в компанию АО «Рош-Москва» по адресу 107031, Россия, Москва, Трубная площадь, 2, пом. 1, этаж 1-й, комн. 42.
Тел.: (495) 229-29-99; факс: (495) 229-79-99
или через форму обратной связи на сайте:
www.roche.ru
В случае упаковки на ОАО «Фармстандарт-УфаВИТА» претензии потребителей направлять по адресу 450077, Россия, Республика Башкортостан, г. Уфа, ул. Худайбердина, 28.
Тел./факс: (347) 272-92-85.
www.pharmstd.ru
Условия отпуска из аптек
По рецепту.
Условия хранения
В защищенном от света месте, при температуре 2–8 °C (не замораживать).
Хранить в недоступном для детей месте.
Срок годности
2 года 6 мес.
Не применять по истечении срока годности, указанного на упаковке.
Представленная информация о ценах на препараты не является предложением о продаже или покупке товара.
Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в
соответствии со статьей 55 Федерального закона «Об обращении лекарственных средств» от 12.04.2010 № 61-ФЗ.
Состав
В 1 мл концентрата, рассчитанного для приготовления инфузионных растворов, содержится 20 мг действующего вещества тоцилизумаба и вспомогательные соединения: сахароза, полисорбат 80, додекагидрат и дигидрат натрия гидрофосфата, вода инъекционная.
Форма выпуска
Препарат Актемра реализуется во флаконах объемом 4/10/20 мл. В одной картонной пачке обычно находится 4 или 1 флакон. Сам концентрат представляет собой опалесцирующую бесцветную жидкость.
Фармакологическое действие
Актемра обладает иммунодепрессивным влиянием.
Фармакодинамика и фармакокинетика
Тоцилизумаб является рекомбинантным гуманизированным моноклональным антителом к рецепторам интерлейкина 6 (сокр. ИЛ-6) в человеческом организме и относится к подклассу иммуноглобулинов изотипу IgG1. В основе механизма действия лежит селективное связывание и подавление как растворимых, так и мембранных рецепторов на ИЛ-6.
Интерлейкин 6 – это показатель иммунного ответа, его — многофункциональный цитокин вырабатывают различные типы клеток, принимающие участие в паракринной регуляции, в патологических процессах и системных физиологических реакциях, например, активация Т-лимфоцитов, стимуляция выработки Ig, гемопоэза, белков острой фазы воспаления (стресс-белков) в печени. Так как Интерлейкин 6 вовлечен в патогенез заболеваний, воспалительных процессов, новообразований, то не следует исключать отрицательное воздействие тоцилизумаба, к примеру, на противоинфекционную или противоопухолевую защиту организма.
При ревматоидном артрите (РА) терапевтический эффект наблюдается спустя 0,5 года при использовании дозы 8 мг/кг и возникает в отношении всех критериев АКР (Американская коллегия ревматологов), включая количество отекших суставов, оценка болевого синдрома, общее улучшение, данные опросника HAQ, анализ С-реактивного белка. Ответ на лечение возникает быстро – со ІІ недели и усиливается в течение всей терапии, сохраняясь более 1,5 года.
Исследования показали, что доза тоцилизумаба 8 мг/кг при проведении монотерапии и в комбинации с БПВП + Метотрексат, дает статистически значимое (р<0,0001) увеличение показателя гемоглобина на 24 неделе (наиболее выражено у пациентов, страдающих хронической анемией, сопровождающей РА).
После введения препарата происходит быстрое снижение острофазовых показателей, включая C-реактивный белок, СОЭ, сывороточный амилоид А, в пределах нормы снижается число тромбоцитов.
Фармакокинетические показатели
- Максимальная концентрация тоцилизумаба и величина дозы имеют прямо пропорциональную зависимость. Стандартная дозировка в 8 мг/кг в 4 недели дает Cmax 183 мкг/мл при низком коэффициенте кумуляции до 1,22. При низких концентрациях клиренс является нелинейным.
- Распределение: поступая в организм в/в тоцилизумаб подвергается двухфазному выведению из системного кровяного русла, при ревматоидном артрите объем распределения до 3,5 л, на периферии — до 2,91 л, при достижении равновесного состояния — 6,41 л.
- Элиминация: общий клиренс разделен на линейный — 12,5 мл/ч и нелинейный клиренс, который зависит от дозы и наиболее значим при низких концентрациях. Кажущийся период полувыведения, который зависит от концентрации тоцилизумаба для дозы 4 мг/кг в 4 недели составляет 11 суток, а для дозы 8 мг/кг в 4 недели — 13 суток.
Показания к применению
Лекарство Актемра назначают при ревматоидном артрите средней или высокой степени активности как монотерапию, либо в сочетании с Метотрексатом, а также с прочими ключевыми противовоспалительными препаратами.
Противопоказания
- инфекционные заболевания в активной фазе, включая туберкулез (необходимо провести исследования для выявления латентного туберкулеза);
- гиперчувствительность к любому компоненту Актемры;
- иммунизация живыми или живыми, но ослабленными вакцинами;
- беременные/кормящие грудью пациентки.
Возможное применение с осторожностью:
- при рецидивирующей инфекции, имеющейся в анамнезе;
- наличие сопутствующих заболеваний, которые могут привести к развитию инфекции, например: сахарный диабет, дивертикулит и пр.;
- заболевания печени, недостаточность печеночной функции;
- нейтропения.
Побочные действия
- Очень часто (у 1 пациента из 10) наблюдалось развитие инфекций верхних дыхательных путей, а также флегмоны, инфекций, вызванных Herpes simplex, Herpes zoster, дивертикулита.
- Встречались случаи возникновения язвы в ротовой полости, гастрита, стоматита.
- Системные нежелательные реакции со стороны эпидермиса проявлялись в виде сыпи, зуда, нечасто — крапивницы.
- Возможны головные боли, головокружение, повышение АД.
- Реакции гиперчувствительности.
Актемра, инструкция по применению (Способ и дозировка)
Стандартная дозировка
Водить следует в/в капельно дозу 8 мг/кг в течение 60 мин, не чаще чем раз в четыре недели.
Препарат Актемра рекомендовано разводить до 100 мл при помощи стерильного 0,9% раствора натрия хлорида с учетом соблюдения асептических условий.
Алгоритм приготовления раствора
- Отмерьте количество препарата, исходя из расчета 0,4 мл на 1 кг веса пациента.
- Отберите, используя одноразовый стерильный шприц, из инфузионного пакета (100 мл) 0,9% раствор натрия хлорида (стерильный и апирогенный) в соответствии с рассчитанным для введения количеством Актемры .
- Возьмите другой одноразовый стерильный шприц и, соблюдая асептические условия, отберите из флакона препарат Актемра, затем — введите его в инфузионный пакет с натрия хлоридом, получив в результате приготовленный раствор объемом равным 100 мл.
- Переворачивайте пакет, чтобы аккуратно перемешать раствор, избегайте пенообразования, проверьте содержимое на предмет отсутствия посторонних частиц либо изменений окраски. Внимание! Введению подлежат лишь бесцветные опалесцирующие либо светло-желтые, только что приготовленные растворы.
Перечень правил хранения приготовленного раствора
Не смотря на то, что приготовленный раствор является физически и химически стабильным первые 24 часа (температура не должна превышать + 2–8 °C), но с микробиологической точки зрения его необходимо вводить немедленно. В противном случае – последствия становятся ответственностью пользователя.
Передозировка
Был зафиксирован случай непреднамеренной передозировки препаратом. Пациент с множественной миеломой использовал дозу 40 мг/кг и нежелательных реакций не возникло. Здоровые добровольцы, согласившиеся однократно получить 28 мг/кг Актемры, столкнулись с развитием нейтропении, влияющей на снижение дозы.
Взаимодействие
- Актемра имеет клинически значимое влияние на изоферменты CYP (исключение: СYP2C19, CYP2D6), что необходимо учитывать при коррекции доз препаратов, являющихся субстратами для CYP450 и имеющих узкий терапевтический индекс.
- Концентрация Симвастатина (является субстратом СYP3A4) спустя 1 неделю после однократной дозы тоцилизумаба снижается на 57%.
- Терапия Актемрой требует тщательного наблюдения за пациентами, принимавшими ЛС, метаболизирующимися посредством таких изоферментов как CYP450 3A4, 1A2 и 2C9. К ним относятся: Аторвастатин, Теофиллин, БКК, Циклоспорин, Варфарин, фенитоин и бензодиазепины. Чтобы обеспечить терапевтический эффект вышеперечисленных препаратов, может понадобиться увеличение их дозировки. Кроме того, следует учитывать длительный период полувыведения Актемры, ведь влияние на активность изоферментов группы CYP450 может продолжаться несколько недель после отмены препарата.
Условия продажи
Актемра должна отпускаться по рецепту.
Условия хранения
Темнота, 2-8 °С (замораживать запрещено).
Дети не должны иметь доступ к флаконам с концентратом Актемра.
Срок годности
В оригинальной упаковке возможно хранение 2,5 года.
Детям
Не было получено данных о безопасности и эффективности использования тоцилизумаба у детей.
При беременности и лактации
Принято считать, что интерлейкин 6 не играет решающей роли во внутриутробном развитии или иммунной регуляции системы матери и плода, однако, взаимосвязь с использованием тоцилизумаба исключать нельзя.
Аналоги
Совпадения по коду АТХ 4-го уровня:
- Зенапакс (конц. для инф. р-ра, активное в-во даклизумаб);
- Иларис (порошок для инф. р-ра, активное в-во канакинумаб).
Отзывы об Актемре
Найти отзывы достаточно сложно. Многих интересует данный препарат и они пытаются его достать. Об Актемре было упомянуто на центральном телевидении как о новейшем прогрессивном средстве при ревматоидном артрите. Это достаточно дорогое ЛС нового поколения, на которое многие возлагают серьезные надежды.
Цена Актемры, где купить
Купить Актемру 4 мл возможно по цене — около 45000 рублей.
- Интернет-аптеки РоссииРоссия
ЛюксФарма* специальное предложение
-
Актемра (Тоцилизумаб) 200мг раствор для ин. 20мг/мл 10мл №1
-
Актемра (Тоцилизумаб) 80мг раствор для ин. 20мг/мл 4мл №1
-
Актемра раствор для инъекций 162мг/0,9мл №4
-
Актемра (Тоцилизумаб) 20мг/мл 20мл (400мг) №1
показать еще
Актемра (400мг/20мл)
МНН: Тоцилизумаб
Производитель: Чугай Фарма Мануфактуринг Ко., Лтд.
Анатомо-терапевтическо-химическая классификация: Tocilizumab
Номер регистрации в РК:
№ РК-ЛС-5№014976
Информация о регистрации в РК:
29.05.2015 — 29.05.2020
Информация о реестрах и регистрах
Информация по ценам и ограничения
Предельная цена закупа в РК:
327 454.47 KZT
- Скачать инструкцию медикамента
Торговое название
Актемра
Международное непатентованное название
Тоцилизумаб
Лекарственная форма
Концентрат для приготовления инфузионного раствора 80 мг/4 мл, 200 мг/10мл, 400 мг/20 мл
Состав
Один флакон содержит
активное вещество – тоцилизумаб 80 мг, 200 мг, 400 мг
вспомогательные вещества: сахароза, полисорбат 80, динатрия фосфата додекагидрат, натрия дигидрофосфата дигидрат, вода для инъекций
Описание
Прозрачная или опалесцирующая жидкость от бесцветного до светло-желтого цвета
Фармакотерапевтическая группа
Иммунодепрессанты. Ингибиторы интерлейкина. Тоцилизумаб.
Код АТХ L04AC07
Фармакологические свойства
Фармакокинетика
Фармакокинетические параметры тоцилизумаба оценивались с использованием популяционного фармакокинетического анализа данных 1793 больных ревматоидным артритом, получавших инфузию тоцилизумаба (в дозе 4 мг/кг или 8 мг/кг) в течение 1 часа каждые 4 недели на протяжении 24 недель.
Для тоцилизумаба при применении в дозе 8 мг/кг каждые 4 недели характерны следующие средние расчетные показатели (± стандартное отклонение): AUC (площадь под кривой) в равновесном состоянии – 35 000±15 500 мкг × ч/мл, Cmin (минимальная концентрация) и Cmax (максимальная концентрация) – 9,74±10,5 мкг/мл и 183±85,6 мкг/мл, соответственно. Коэффициенты кумуляции для AUC и Cmaх низки: 1,22 и 1,06, соответственно. Коэффициент кумуляции был выше для Cmin (2,35), что ожидалось из-за нелинейного клиренса при низких концентрациях. Равновесное состояние было достигнуто после первого введения и через 8 и 20 недель для Cmax, AUC и Cmin, соответственно. Показатели AUC, Cmin и Cmax возрастают при увеличении массы тела. При массе тела ≥100 кг расчетная средняя (± стандартное отклонение) AUC в равновесном состоянии составила 55 500 ± 14 100 мкг×ч/мл, Cmin и Cmax 19,0 ± 12,0 мкг/мл и 269 ± 57 мкг/мл, что выше средних значений экспозиции в популяции пациентов (AUC =35 000±15 500 мкг × ч/мл, Cmin = 9,74±10,5 мкг/мл и Cmax =183±85,6 мкг/мл). Кривая зависимости ответа от дозы становится более плоской при повышении воздействия, т.е. при каждом инкрементальном увеличении концентрации тоцилизумаба, увеличение ответа возрастает в меньшей степени, поэтому у пациентов, получавших более 800 мг тоцилизумаба, не наблюдалось клинически значимого роста эффективности. Поэтому не рекомендуется увеличивать дозу препарата выше 800 мг на одну инфузию.
Распределение
У пациентов с ревматоидным артритом Vd (объем распределения) в центральной камере составляет 3,5 л, в периферической камере – 2,9 л, а Vd в равновесном состоянии составляет 6,4 л.
Выведение Общий клиренс тоцилизумаба зависит от концентрации и представляет собой сумму значений линейного и нелинейного клиренса. Линейный клиренс по расчетам популяционного фармакокинетического анализа составил 12,5 мл/час. Нелинейный клиренс зависит от концентрации и играет важную роль при низких концентрациях тоцилизумаба. При высоких концентрациях тоцилизумаба, когда механизмы нелинейного клиренса насыщаются, линейный клиренс имеет большее значение.
Период полувыведения тоцилизумаба (Т1/2) у пациентов с ревматоидным артритом зависит от концентрации: 11 дней для дозы 4 мг/кг и 13 дней для дозы 8 мг/кг при в/в введении 1 раз в 4 недели.
Фармакокинетические параметры тоцилизумаба не меняются с течением времени. Более, чем дозозависимое увеличение AUC (площадь по кривой) и Cmin (минимальная концентрация препарата), отмечается для доз 4 и 8 мг/кг каждые четыре недели. Cmax (максимальная концентрация препарата) увеличивается прямо пропорционально увеличению дозы. В равновесном состоянии расчетные AUC и Cmin были в 2,7 и 6,5 раз выше при дозе 8 мг/кг по сравнению с дозой 4 мг/кг соответственно.
Фармакокинетика у особых групп пациентов
Печеночная недостаточность
Специальных исследований не проводилось.
Почечная недостаточность
Специальных исследований не проводилось. Большинство пациентов в популяционном фармакокинетическом анализе имели нормальную функцию почек или нарушения легкой степени (клиренс креатинина 50 – 80 мл/мин). Почечная недостаточность легкой степени не оказывала влияния на фармакокинетику тоцилизумаба.
Другие группы больных
Не требуется коррекции дозы у больных различного возраста, пола или расы.
Системный ювенильный идиопатический артрит (сЮИА)
Фармакокинетика тоцилизумаба определялась с помощью популяционного фармакокинетического анализа базы данных, включающей в себя 75 пациентов с сЮИА, получавших тоцилизумаб в дозе 8 мг/кг (пациенты с массой тела ≥ 30 кг) или 12 мг/кг (пациенты с массой тела < 30 кг) один раз в 2 недели. Расчетные средние значения (± стандартное отклонение) AUC2нед, Cmax и Cmin тоцилизумаба составили 32200 ± 9960 мкг×ч/мл, 245 ± 57,2 мкг/мл и 57,5 ± 23,3 мкг/мл, соответственно. Коэффициент кумуляции для Cmin (12 нед/2 нед) – 3,2±1,3. Cmin тоцилизумаба стабилизировалась после 12 недели. Расчетные средние показатели экспозиции тоцилизумаба не отличались в группе пациентов с массой тела ≥30 кг и в группе пациентов с массой тела <30 кг.
У пациентов с сЮИА, объем распределения в центральной камере составлял 35 мл/кг, в периферической камере – 60 мл/кг, объем распределения в равновесном состоянии — 95 мл/кг. Линейный клиренс, рассчитываемый в качестве параметра в популяционном фармакокинетическом анализе, составил 0,142 мл/ч/кг.
Период полувыведения тоцилизумаба на 12-й неделе терапии у пациентов с сЮИА составляет до 23 суток в обеих весовых категориях (доза 8 мг/кг для массы тела ≥ 30 кг и 12 мг/кг для массы тела < 30 кг).
Ювенильный идиопатический полиартрит
Фармакокинетические параметры тоцилизумаба оценивались с использованием популяционного фармакокинетического анализа данных 188 больных ювенильным идиопатическим полиартритом.
Для тоцилизумаба при применении в дозе 8 мг/кг каждые 4 недели характерны следующие показатели (пациенты с массой тела ≥ 30 кг): расчетные средние (± стандартное отклонение) AUC4нед. в равновесном состоянии, Cmin и Cmax тоцилизумаба составили 29500 ± 8660 мкг×ч/мл, 182 37 мкг/мл и 7,49 8,2 мкг/мл, соответственно.
Для тоцилизумаба при применении в дозе 10 мг/кг, каждые 4 недели, характерны следующие показатели (пациенты с массой тела < 30 кг): расчетные средние (± стандартное отклонение) AUC4нед. в равновесном состоянии, Cmin и Cmax тоцилизумаба составили 23200 ± 6100 мкг×ч/мл, 175 32 мкг/мл и 2,35 3,59 мкг/мл, соответственно.
Коэффициенты кумуляции для AUC4нед. составили 1,05 и 1,16, а для Cmin – 1,43 и 2,22 для доз 10 мг/кг (масса тела < 30 кг) и 8 мг/кг (масса тела ≥ 30 кг), соответственно. Кумуляция для Cmax не наблюдалась.
У пациентов с ювенильным идиопатическим полиартритом объем распределения в центральной камере составлял 50 мл/кг, в периферической камере – 53 мл/кг, объем распределения в равновесном состоянии – 103 мл/кг. Линейный клиренс, рассчитываемый в качестве параметра в популяционном фармакокинетическом анализе, составил 0,146 мл/ч/кг.
Период полувыведения тоцилизумаба во время перерыва в дозировании в равновесном состоянии у пациентов с ювенильным идиопатическим полиартритом составляет до 16 суток в обеих весовых категориях (доза 8 мг/кг для массы тела ≥ 30 кг и 10 мг/кг для массы тела < 30 кг).
Фармакодинамика
Тоцилизумаб представляет собой гуманизированное рекомбинантное моноклональное антитело к рецептору интерлейкина-6 (IL-6), принадлежащее к подклассу иммуноглобулинов IgG1. Тоцилизумаб производится по технологии рекомбинантных ДНК из клеток яичника китайского хомячка. Тоцилизумаб связывается специфически с растворимыми и мембранными рецепторами IL-6 (sIL-6R и mIL-6R) и подавляет сигналы, опосредуемые этими рецепторами. Интерлейкин-6 представляет собой многофункциональный цитокин, вырабатываемый различными типами клеток, вовлеченных в локальные паракринные функции, а также в регуляцию системных физиологических и патологических процессов, таких как индукцию секреции иммуноглобулинов, активацию Т-клеток, выработку ферментов острого воспаления печени и стмуляцию гемопоэза. IL-6 также вовлечен в патогенез воспалительных заболеваний, остеопороза и развития злокачественных опухолей.
Нельзя исключить вероятность отрицательного воздействия тоцилизумаба на противоопухолевую и противоинфекционную защиту организма. Роль ингибирования рецептора ИЛ-6 в развитии опухолей неизвестна.
Клиническая эффективность при ревматоидном артрите
Эффективность препарата у пациентов, получавших тоцилизумаб как в монотерапии, так и в комбинации с метотрексатом или болезнь-модифицирующими антиревматическими препаратами (БМАРП), не зависела от наличия или отсутствия ревматоидного фактора, возраста, пола, расовой принадлежности, числа предшествующих курсов лечения или стадии заболевания. Ответ на терапию возникал быстро (уже на второй неделе), в дальнейшем усиливался и сохранялся более 3 лет в продолжающихся открытых расширенных исследованиях.
У пациентов, получавших тоцилизумаб в дозе 8 мг/кг, существенно снижается индекс активности заболевания по шкале DAS28 по сравнению с пациентами, получавшими плацебо + БМАРП. Число пациентов, достигших клинической ремиссии (DAS28<2,6) на 24 неделе, было значительно больше в группе терапии тоцилизумабом (28-34%) по сравнению с контрольной группой (1-12%). К 52 неделе терапии число пациентов, достигших DAS28<2,6, увеличивается до 47% по сравнению с 33% на 24 неделе терапии.
Хороший или удовлетворительный ответ по критериям EULAR отмечался чаще у пациентов, получавших тоцилизумаб, чем у получавших плацебо + БМАРП. Через 2 года терапии тоцилизумабом/метотрексатом (МТ) у 14% пациентов наблюдался значительный клинический ответ (ACR70 сохранялся на протяжении 24 недель и более).
Рентгенологическая оценка
У 83% пациентов, получавших терапию тоцилизумабом/МТ в течение года, не зарегистрировано прогрессирования деструкции суставов (изменение суммарного индекса Шарпа равно нулю или менее) по сравнению с 67% пациентов, получавших плацебо/МТ. Данный результат сохранялся на протяжении 2 лет терапии. У 93% пациентов отсутствовало прогрессирование деструкции суставов между 52 и 104 неделями терапии.
Показатели качества жизни
У пациентов, получавших тоцилизумаб в дозе 8 мг/кг (монотерапия или в сочетании с БМАРП), по сравнению с теми, кто получал МТ/БМАРП, наблюдалось клинически значимое улучшение функциональной активности (по индексу HAQ-DI), снижение утомляемости (по шкале функциональной оценки терапии хронических заболеваний по показателю утомляемости FACIT-Fatigue), а также улучшение показателей как физического, так и психического здоровья по опроснику SF-36.
Лабораторные показатели
После введения тоцилизумаба происходит быстрое снижение средних значений острофазовых показателей, С-реактивного белка, СОЭ и сывороточного амилоида А, снижение числа тромбоцитов в пределах нормальных значений, а также увеличение гемоглобина, которое в большей степени наблюдалось у пациентов с хронической анемией, связанной с ревматоидным артритом.
Клиническая эффективность у пациентов с ранним ревматоидным артритом, ранее не получавших терапию МТ
При применении тоцилизумаба в монотерапии в дозе 8 мг/кг тоцилизумаба в дозе 4 или 8 мг/кг каждые 4 недели в комбинации с МТ индекс активности заболевания по шкале DAS28 существенно снижается в группах, получавших тоцилизумаб в дозе 8 мг/кг, по сравнению с пациентами, получавшими монотерапию МТ. Число пациентов, достигших клинической ремиссии (DAS28<2,6) на 24 неделе, было значительно больше в группе терапии тоцилизумабом (38,7-44,8%) по сравнению с группой монотерапии МТ (15%). К 52 неделе терапии число пациентов, достигших DAS28<2,6 в группах терапии тоцилизумабом, увеличивается до 39,4-49% по сравнению с 19,5% в группе монотерапии МТ. Число пациентов, достигших ответа ACR 20, 50, 70, также существенно выше в группах терапии тоцилизумабом (70,2-74,5%, 47,6-56,9%, 30,1-38,6% на 24 неделе и 63-67,2%, 49,3-55,9%, 36-43,1% на 52 неделе соответственно) по сравнению с группой монотерапии МТ (65,2%, 43,2%, 25,4% на 24 неделе и 57,1%, 40,8%, 28,9% на 52 неделе соответственно). Рентгенологическая оценка
Отсутствие прогрессирования деструкции суставов (изменение суммарного индекса Шарпа равно нулю или менее) наблюдается у 82-83% пациентов, получавших тоцилизумаб в дозе 8 мг/кг в качестве монотерапии или в комбинации с МТ, по сравнению с 73% пациентов в группе монотерапии МТ.
Показатели качества жизни
Клинически значимое улучшение функциональной активности (по индексу HAQ-DI) наблюдается у пациентов, получавших тоцилизумаб в дозе 8 мг/кг в качестве монотерапии или в комбинации с МТ, по сравнению с теми, кто получал монотерапию МТ.
При монотерапии тоцилизумабом (в дозе 8 мг/кг внутривенно каждые 4 недели у пациентов с РА, с непереносимостью МТ или при нецелесообразности продолжения терапии МТ, в том числе при неадекватном ответе на терапию МТ) наблюдалось более выраженное статистически значимое снижение активности заболевания по шкале DAS28 по сравнению с монотерапией адалимумабом (в дозе 40 мг подкожно каждые 2 недели). Количество пациентов, ответивших на терапию с показателями DAS28<2,6 и DAS28≤3,2, было больше при терапии тоцилизумабом, чем при терапии адалимумабом (39,9% против 10,5% и 51,5% против 19,8% соответственно). Ответы ACR 20,50,70 наблюдались у 65%, 47,2%, 32,5% пациентов, получавших тоцилизумаб, по сравнению с 49,4%, 27,8%, 17,9% пациентов, получавших адалимумаб.
Клиническая эффективность при полиартикулярном ювенильном идиопатическом артрите
Ответы ACR 20, 50, 70, 90 были получены у 89,4%, 83,0%, 62,2% и 26,1% пациентов, соответственно. Доля пациентов с ответом ACR 20, 50, 70 на 40 неделе терапии относительно показателей на начало терапии составила 74,4, 73,2% и 64,6% соответственно.
Клиническая эффективность при системном ювенильном идиопатическом артрите
Эффективность тоцилизумаба для лечения активного сЮИА изучалась в 12-недельном рандомизированном двойном слепом плацебо контролируемом периоде исследования с 2 параллельными группами. На 12 неделе доля пациентов, достигших ответа ACR20, 50, 70, 90 при ЮИА была больше в группе терапии тоцилизумабом, чем в группе плацебо: 90,7% против 24,3%, 85,3% против 10,8%, 70,7% против 8,1% соответственно (р<0,0001). Ответ на терапию сохранялся и в открытом расширенном периоде исследования.
Системные эффекты
У 85% пациентов, имевших исходно лихорадку, через 12 недель терапии тоцилизумабом лихорадка отсутствовала по сравнению с 21% пациентов, получавших плацебо (р<0,0001). Кроме того, у 64% пациентов, имевших исходно сыпь, через 12 недель терапии тоцилизумабом сыпь отсутствовала по сравнению с 21% пациентов, получавших плацебо (р=0,0008). Наблюдалось значительное снижение интенсивности болевого синдрома в группе терапии тоцилизумабом по сравнению с плацебо на 12 неделе. Скорректированное среднее изменение оценки боли по визуальной аналоговой шкале (ВАШ) после 12 недель терапии тоцилизумабом соответствовало 41 пункту (от 0 до 100) по сравнению с 1 пунктом у пациентов, получавших плацебо (р<0,0001). Регрессия системных эффектов сохранялась и в открытом расширенном периоде исследования.
Снижение дозы глюкокортикостероидов
У 8 из 31 пациента в группе плацебо и у 48 из 70 пациентов в группе тоцилизумаба, получавших глюкокортикостероиды исходно, наблюдался ответ ACR 70 при ЮИА на 6 или 8 неделе, что позволило снизить дозу глюкокортикостероидов. При этом 24% пациентов в группе тоцилизумаба и 3% пациентов в группе плацебо смогли снизить дозу глюкокортикостероидов как минимум на 20% без последующего снижения частоты ответа по критериям ACR 30 при ЮИА или возникновения системных проявлений к 12 неделе (р=0.028). Снижение дозы глюкокортикостероидов продолжилось, при этом 44 пациента не получали глюкокортикостероиды на 44 неделе и ответы ACR не изменились.
Показатели качества жизни
На 12 неделе доля пациентов в группе тоцилизумаба, демонстрирующих минимальное клинически значимое улучшение по опроснику CHAQ-DI, (определенного как снижение индивидуального общего балла на ≥ 0,13) была значительно выше, чем доля пациентов в группе плацебо – 77% против 19% соответственно (р<0,0001). Данный ответ сохранялся и в открытом расширенном периоде исследования.
Лабораторные показатели
Исходно у 67% пациентов из группы тоцилизумаба содержание гемоглобина было ниже нормального уровня. У 80% этих пациентов на 12 неделе наблюдалось увеличение уровня гемоглобина до нормальных пределов по сравнению с 7% пациентов в группе плацебо (р<0,0001). У 88% пациентов, получавших тоцилизумаб, имевших исходно сниженное содержание гемоглобина, его уровень увеличился более, чем на 10 г/л к 6 неделе, в группе плацебо частота повышения составила 3% (р<0,0001). Доля пациентов, имевших исходно тромбоцитоз и у которых на 12 неделе наблюдалось нормальное нормальное число тромбоцитов, была выше в группе пациентов, получавших тоцилизумаб по сравнению с группой плацебо – 90% против 4% (р<0,0001). После введения тоцилизумаба происходило быстрое снижение средних значений острофазовых показателей: С-реактивного белка, СОЭ и сывороточного амилоида А.
Показания к применению
-
в комбинации с метотрексатом или в монотерапии (при непереносимости метотрексата или в случаях, когда назначение метотрексата не показано) для лечения ревматоидного артрита высокой степени активности у взрослых пациентов, ранее не получавших метотрексат
-
в комбинации с метотрексатом или в монотерапии (при непереносимости метотрексата или в случаях, когда назначение метотрексата не показано) для лечения ревматоидного артрита средней или высокой степени активности (в том числе ранний ревматоидный артрит при длительности заболевания менее 6 мес у пациентов,) у взрослых пациентов, не ответивших на терапию БМАРП или антагонистами фактора некроза опухолей, в том числе для предотвращения прогрессирования рентгенологически доказанной деструкции суставов
-
системный ювенильный идиопатический артрит в монотерапии (при непереносимости метотрексата или в случаях, когда назначение метотрексата не показано) или в комбинации с метотрекстатом у детей старше 2 лет, не ответивших на терапию нестероидными противовоспалительными средствами и системными кортикостероидами
-
ювенильный идиопатический полиартрит (при положительном или отрицательном результате анализа на ревматоидный фактор, а также при олигоартрите) в монотерапии (при непереносимости метотрексата или в случаях, когда назначение метотрексата не показано) или в комбинации с метотрекстатом у детей старше 2 лет, не ответивших на ранее проводимое лечение, включавшее метотрексат.
Способ применения и дозы
Разведение препарата должно проводиться медработником с соблюдением правил асептики. Препарат разводят стерильным 0,9% раствором натрия хлорида. Раствор вводят внутривенно капельно в течение как минимум 1 часа.
Ревматоидный артрит
Рекомендуемая доза для взрослых – 8 мг/кг массы тела один раз в 4 недели в виде внутривенной инфузии в течение 1 часа. Актемра применяется в виде монотерапии или в комбинации с метотрексатом и/или другими препаратами базовой терапии.
В асептических условиях отбирают требуемое количество раствора (0,4 мл/кг массы тела) и разбавляют до требуемой концентрации в 100 мл 0,9% стерильного апирогенного раствора натрия хлорида. Предварительно необходимо удалить из этого пакета (флакона) раствор в количестве, равном объему Актемры, требуемого для введения данному пациенту. Для перемешивания раствора пакет (флакон) бережно переворачивают во избежание пенообразования.
Ювенильный идиопатический полиартрит
Внутривенно капельно 1 раз в 4 недели в дозе:
|
Пациентам с массой тела менее 30 кг |
10 мг/кг |
|
Пациентам с массой тела 30 кг и более |
8 мг/кг |
Изменение дозы возможно исключительно в случае стойкого изменения массы тела пациента. Актемра применяется в виде монотерапии или в комбинации с метотрексатом.
В асептических условиях отбирают требуемое количество раствора (из расчета 0,4 мл/кг массы тела для пациентов с массой тела 30 кг и более; или из расчета 0,5 мл/кг массы тела для пациентов с массой тела менее 30 кг) и разбавляют до требуемой концентрации в 100 мл 0,9% стерильного апирогенного раствора натрия хлорида. Предварительно необходимо удалить из этого пакета (флакона) раствор в количестве, равном объему Актемры, требуемой для введения данному пациенту. Для перемешивания раствора пакет (флакон) бережно переворачивают во избежание пенообразования.
Системный ювенильный идиопатический артрит (сЮИА)
Внутривенно капельно 1 раз в 2 недели в дозе:
|
Пациентам с массой тела менее 30 кг |
12 мг/кг каждые 2 недели |
|
Пациентам с массой 30 кг и более |
8 мг/кг каждые 2 недели |
В асептических условиях отбирают требуемое количество раствора (из расчета 0,4 мл/кг массы тела для пациентов с массой тела 30 кг и более; или из расчета 0,6 мл/кг массы тела для пациентов с массой тела менее 30 кг) и разбавляют до требуемой концентрации в 100 мл 0,9% стерильного апирогенного раствора натрия хлорида. Предварительно необходимо удалить из этого пакета (флакона) раствор в количестве, равном объему Актемры, требуемой для введения данному пациенту. Для перемешивания раствора пакет (флакон) бережно переворачивают во избежание пенообразования.
Пакет (флакон) с Актемрой перед введением следует осмотреть на предмет выявления видимых частиц или изменения цвета. Вводить можно только прозрачный, или слегка опалесцирующий, бесцветный или светло-желтого цвета раствор, не содержащий видимых частиц.
Готовый инфузионный раствор в 0,9% растворе натрия хлорида химически и физически стабилен при температуре не выше 30 °С в течение 24 часов.
С микробиологической точки зрения, готовый для инфузий раствор должен быть использован немедленно. Если раствор не использован немедленно, раствор не должен храниться более 24 часов при температуре от 2 °С до 8 °С, если только разведение не произведено в контролируемых и валидированных асептических условиях.
Дозирование Актемры в соответствии с отклонениями лабораторных показателей (в том числе и у детей)
Повышение уровня ферментов печени (АЛТ/АСТ)
|
Значения лабораторных показателей |
Действия |
|
От более одного до 3 раз выше верхней границы нормы (до 3 ВГН) |
При необходимости снизить дозу метотрексата, назначаемого одновременно При стойком повышении показателей АЛТ/АСТ снизить дозу тоцилизумаба до 4 мг/кг массы тела или приостановить введение препарата Актемра до нормализации уровней АЛТ/АСТ. Возобновить лечение тоцилизумабом в дозе 4 мг/кг или 8 мг/кг массы тела, в соответствии с клиническим ответом |
|
В 3-5 раз выше верхней границы нормы (3 – 5 ВГН) (подтверждено при повторном тестировании) |
Приостановить лечение препаратом Актемра, пока показатели не снизятся менее 3 ВГН и следовать рекомендациям для диапазона 1 – 3 ВГН. При стойком превышении более 3 ВГН прекратить лечение препаратом Актемра |
|
Более чем в 5 раз выше верхней границы нормы (> 5 ВГН) |
Прекратить введение препарата Актемра |
Низкое абсолютное число нейтрофилов (ANC)
Пациентам, ранее не получавшим препарат Актемра, не рекомендуется начинать терапию при абсолютном числе нейтрофилов менее 2х109/л.
|
Значение лабораторных показателей (клеток x 109/л) |
Действия |
|
ANC > 1 |
Поддерживать дозу |
|
ANC 0,5 до 1 |
Приостановить введение препарата Актемра. Когда ANC превысит 1 x 109/л, возобновить введение препарата Актемра в дозе 4 мг/кг и повышать до 8 мг/кг массы тела в соответствии с клиническим ответом |
|
ANC < 0.5 |
Прекратить лечение препаратом Актемра |
Низкое количество тромбоцитов
|
Значение лабораторных показателей (клеток x 109/л) |
Действия |
|
50 – 100 |
Приостановить введение препарата Актемра. При достижении содержания тромбоцитов > 100 x 109/л, возобновить введение препарата Актемра в дозе 4 мг/кг и повышать дозу до 8 мг/кг массы тела, в соответствии с клиническим ответом |
|
< 50 |
Прекратить лечение препаратом Актемра |
Исследования по изучению эффективности снижения дозы тоцилизумаба у пациентов с ювенильным идиопатическим полиартритом и сЮИА не проводились. При обнаружении изменений в лабораторных показателях используются те же рекомендации (прерывание лечения), что и для пациентов с РА. При необходимости следует изменить дозу или прекратить прием метотрексата и/или других одновременно назначаемых препаратов и прервать лечение тоцилизумабом до проведения оценки общей клинической картины. В случае с ювенильным идиопатическим полиартритом и сЮИА решение о прекращении приема тоцилизумаба вследствие отклонений в лабораторных показателях должно быть принято в зависимости от индивидуальной клинической ситуации.
Дозирование в особых случаях
Пациенты детского возраста
Безопасность и эффективность препарата Актемра изучались только при сЮИА и ювенильным идиопатическим полиартритом. Применение препарата у детей младше 2 лет не изучалось.
Пациенты пожилого возраста
Коррекции дозы у пациентов пожилого возраста (старше 65 лет) не требуется.
Пациенты с почечной недостаточностью
Коррекции дозы у пациентов с легкой степенью почечной недостаточности не требуется. Применение тоцилизумаба у пациентов с умеренной и тяжелой степенью почечной недостаточности не изучалось.
Пациенты с печеночной недостаточностью
Безопасность и эффективность препарата Актемра у пациентов с печеночной недостаточностью не изучались.
Побочные действия
Ревматоидный артрит
Профиль безопасности тоцилизумаба изучался в 5 двойных слепых плацебо-контролируемых клинических исследованиях III фазы и в их наблюдательных периодах.
Вся контролируемая популяция включала всех пациентов, принимавших участие в двойном слепом периоде каждого базового исследования, с момента рандомизации до первого изменения режима лечения или при достижении 2 лет. Период лечения и наблюдения в 4 исследованиях составил 6 месяцев, в 1 исследовании – до 2 лет. При этом 774 пациента получали тоцилизумаб в дозе 4 мг/кг в комбинации с метотрексатом, 1870 пациентов – в дозе 8 мг в комбинации с метотрексатом/другими БМАРП и 288 пациентов – монотерапию тоцилизумабом в дозе 8 мг/кг.
Вся исследуемая популяция включала всех пациентов, получивших как минимум одну дозу препарата, как в двойном слепом плацебо-контролируемом периоде исследований, так и в открытом наблюдательном периоде этих исследований. Из 4009 пациентов 3577 пациентов получали терапию не менее 6 месяцев, 3296 пациентов – не менее 1 года, 2806 пациентов – не менее 2 лет и 1222 пациентов – в течение 3 лет.
Для описания частоты нежелательных реакций используются следующие категории: очень часто (≥ 1/10), часто (≥ 1/100 до <1/10), нечасто (≥ 1/1000 до <1/100), редко (≥ 1/10000 к <1/1000), очень редко (<1/10000). Приведенные ниже нежелательные реакции перечислены в порядке клинической значимости для пациента.
Таблица 1. Обобщенные данные о нежелательных реакциях, зарегистрированных у больных с ревматоидным артритом, получавших тоцилизумаб в качестве монотерапии или в комбинации с метотрексатом или другими БМАРП.
|
Системно-органный класс |
Очень часто |
Часто |
Нечасто |
|
Инфекционные и паразитарные заболевания |
Инфекции верхних дыхательных путей |
Флегмона, инфекции ротовой полости, вызванные Herpes simplex, Herpes zoster |
Дивертикулит |
|
Со стороны системы пищеварения |
Боль в животе, язвы ротовой полости, гастрит |
Стоматит, язва желудка |
|
|
Со стороны кожи и подкожной клетчатки |
Сыпь, зуд, крапивница |
||
|
Со стороны нервной системы |
Головная боль, головокружение |
||
|
Изменения лабораторных показателей |
Повышение активности печеночных трансаминаз,увеличение массы тела |
Повышение общего билирубина |
|
|
Со стороны сердечно-сосудистой системы |
Повышение артериального давления |
||
|
Со стороны крови и лимфатической системы |
Лейкопения, нейтропения |
||
|
Со стороны обмена веществ и питания |
Гиперхолестеринемия |
Гипертриглицеридемия |
|
|
Со стороны организма в целом и реакции в месте введения |
Периферические отеки, реакции гиперчувствительности, реакция в месте введения инъекции |
||
|
Со стороны дыхательной системы |
Кашель, одышка |
||
|
Со стороны органа зрения |
Конъюнктивит |
||
|
Со стороны мочевыделительной системы |
Нефролитиаз |
||
|
Со стороны эндокринной системы |
Гипотиреоз |
Инфекции
По данным 6-месячных контролируемых исследований частота всех инфекций при введении тоцилизумаба в дозе 8 мг/кг в комбинации с БМАРП составила 127 случаев на 100 пациенто-лет в сравнении с 112 случаями на 100 пациенто-лет в группе пациентов, получавших плацебо в комбинации с БМАРП. Во всей исследуемой популяции общая частота инфекций составила 108 случаев на 100 пациенто-лет.
По данным 6-месячных контролируемых клинических исследований частота серьезных инфекций (бактериальных, вирусных и грибковых) в группе пациентов, получавших тоцилизумаб в дозе 8 мг/кг в комбинации с БМАРП, составила 5,3 случая на 100 пациенто-лет в сравнении с 3,9 случаями на 100 пациенто-лет в группе пациентов, получавших плацебо в комбинации с БМАРП. При монотерапии тоцилизумабом частота серьезных инфекций составила 3,6 случая на 100 пациенто-лет по сравнению с монотерапией метотрексатом (1,5 случаев на 100 пациенто-лет).
Во всей исследуемой популяции общая частота серьезных инфекций составила 4,7 случаев на 100 пациенто-лет. Регистрировались следующие серьезные инфекционные заболевания: пневмония, флегмона, инфекции, вызванные Herpes zoster, гастроэнтерит, дивертикулит, сепсис, бактериальный артрит, некоторые из них сопровождались фатальным исходом. Также сообщалось о случаях возникновения оппортунистических инфекций.
Интерстициальная болезнь легких
Исходно нарушенная функция легких может приводить к повышению риска развития инфекционных осложнений. Были зарегистрированы случаи развития интерстициальной болезни легких ((включая пневмонит и интерстициальный фиброз), включая случаи с летальным исходом.
Перфорации желудочно-кишечного тракта
Во время проведения 6-месячных контролируемых исследований в группе пациентов, получавших тоцилизумаб, общая частота перфораций ЖКТ составила 0,26 случаев на 100 пациенто-лет, а во всей исследуемой популяции – 0,28 случаев на 100 пациенто-лет. Главным образом, случаи перфорации ЖКТ сообщались как осложнения дивертикулита и включали разлитой гнойный перитонит, перфорацию нижних отделов ЖКТ, свищи и абсцессы.
Инфузионные реакции
Во время проведения 6-месячных контролируемых исследований нежелательные реакции, связанные с введением препарата (нежелательные реакции, возникающие во время введения препарата или в течение 24 часов после введения), были выявлены у 6,9% пациентов, получавших 8 мг/кг тоцилизумаба в комбинации с БМАРП, и у 5,1% пациентов, получавших плацебо в комбинации с БМАРП. Нежелательными реакциями, которые отмечались во время введения препарата, в основном, были эпизоды повышения артериального давления. Нежелательными реакциями, которые отмечались в течение 24 часов после окончания введения препарата, являлись головная боль и реакции со стороны кожных покровов (сыпь, крапивница). Эти реакции не приводили к ограничению терапии.
Частота анафилаксии (у 6 из 3778 пациентов) была в несколько раз выше у пациентов, получавших препарат в дозе 4 мг/кг, чем у пациентов, получавших препарат в дозе 8 мг/кг. В контролируемых и открытых клинических исследованиях клинически значимые реакции гиперчувствительности, обусловленные введением тоцилизумаба и потребовавшие прекращения лечения, отмечались у 0,3% (3/3778) пациентов. В основном данные реакции наблюдались в период между 2-й и 5-й инфузией тоцилизумаба.
Иммуногенность
В 6-месячных контролируемых исследованиях в общей сложности 2876 пациентов прошли тесты на наличие антител к тоцилизумабу. У 46 (1,6%) пациентов были обнаружены антитела, и у 5 из них были отмечены клинически значимые реакции гиперчувствительности, что привело к полной отмене лечения. У 1,1% (30/2876) пациентов выявлены нейтрализующие антитела.
Гематологическая токсичность
Снижение количества нейтрофилов
В 6-месячных контролируемых исследованиях снижение абсолютного числа нейтрофилов (АЧН) до 1х109/л и менее наблюдалось у 3,4% пациентов, получавших комбинированную терапию тоцилизумаб 8 мг/кг + БМАРП по сравнению с менее чем 0,1% пациентов, получавших плацебо + БМАРП. Примерно у половины пациентов, у которых наблюдалось снижение АЧН ниже 0,5х109/л, данные побочные действия развивались в течение первых 8 недель терапии. Снижение АЧН ниже 0,5х109/л наблюдалось у 0,3% пациентов получавших тоцилизумаб 8 мг/кг + БМАРП. Также были зарегистрированы случаи развития инфекционных осложнений на фоне нейтропении.
Снижение количества тромбоцитов
В 6-месячных контролируемых исследованиях снижение числа тромбоцитов ниже 100 × 103/мкл было отмечено у 1,7% пациентов, получавших тоцилизумаб в дозе 8 мг/кг в комбинации с БПРП, по сравнению менее чем с 1% пациентов, получавших плацебо в комбинации с БПРП. Данные изменения не сопровождались развитием эпизодов кровотечения.
Были зарегистрированы очень редкие случаи развития панцитопении.
Повышение активности «печеночных» трансаминаз
В ходе проведения 6-месячных клинических исследований транзиторное повышение активности АЛТ/АСТ (более чем в 3 раза превышающее верхнюю границу нормы, ВГН) наблюдалось у 2,1% пациентов, получавших тоцилизумаб в дозе 8 мг/кг, и у 4,9% пациентов, получавших метотрексат. Данные изменения возникали у 6,5% пациентов, получавших тоцилизумаб в дозе 8 мг/кг в комбинации с БМАРП, и у 1,5% пациентов, получавших плацебо в комбинации с БМАРП. Присоединение к монотерапии тоцилизумабом препаратов, обладающих потенциальным гепатотоксическим действием (например, метотрексат), приводило к увеличению частоты случаев повышения активности трансаминаз. Повышение активности АЛТ/АСТ более чем в 5 раз превышающее ВГН наблюдалось у 0,7% пациентов, получавших монотерапию тоцилизумабом, и у 1,4% пациентов, получавших тоцилизумаб в комбинации с БМАРП. При этом большинство пациентов прекратили терапию препаратом. Повышение активности печеночных трансаминаз не сопровождалось клинически значимым увеличением уровня прямого билирубина, а также клиническими проявлениями гепатита или печеночной недостаточности. При рутинном мониторинге лабораторных показателей, у пациентов, получавших тоцилизумаб в дозе 8 мг/кг в комбинации с БПРП, частота превышения верхней границы нормы непрямого билирубина составила 6,2%.
Изменение показателей липидного обмена
Во время проведения контролируемых исследований продолжительностью 6 месяцев при терапии тоцилизумабом наблюдалось повышение показателей липидного обмена (общего холестерина, триглицеридов, ЛПВП, ЛПНП). Стойкое повышение показателя общего холестерина > 6,2 ммоль/л (240 мг/дл) наблюдалось приблизительно у 24% пациентов, а стойкое повышение показателя ЛПНП ≥ 4,1 ммоль/л (160 мг/дл) – у 15% пациентов.
У большинства пациентов индекс атерогенности не повышался, а повышение уровня общего холестерина эффективно корректировалось гиполипидемическими препаратами.
Ранний ревматоидный артрит
В исследовании WA19926 проводилась оценка 1162 пациентов с ранним РА умеренной и тяжелой степени, не получавших ранее терапию метотрексатом и другими биологическими препаратами. Общий профиль безопасности, наблюдавшийся в группе пациентов, получавших тоцилизумаб, совпадал с ранее известным профилем безопасности препарата.
Монотерапия рематоидного артрита: тоцилизумаб и адалимумаб
Во время проведения 24-недельного двойного слепого параллельного исследования (монотерапия тоцилизумабом в дозе 8 мг/кг один раз в четыре недели внутривенно (N=162) и монотерапия адалимумабом в дозе 40 мг один раз в две недели подкожно (N=162)), общий клинический профиль нежелательных реакций в обеих группах совпадал. Процентное соотношение пациентов с серьезными нежелательными явлениями в обеих терапевтических группах было аналогичным (тоцилизумаб — 11,7% и адалимумаб — 9,9%); самым распространенным нежелательным явлением являлись инфекции (3,1% в каждой группе). Оба препарата вызывали схожий характер изменения лабораторных показателей (снижение уровней нейтрофилов и тромбоцитов, увеличение уровней АСТ, АЛТ и липидов), однако выраженность и частота этих изменений были выше в группе тоцилизумаба. У четверых (2,5%) пациентов в группе тоцилизумаба и двоих (1,2%) пациентов в группе адалимумаба наблюдалось снижение числа нейтрофилов 3 или 4 степени. У 11 (6,8%) пациентов в группе тоцилизумаба и у 5 (3,1%) пациентов в группе адалимумаба наблюдалось увеличение уровня АЛТ степени 2 и выше. Среднее увеличение ЛПНП по сравнению с исходным значением составило 0,64 ммоль/л (25 мг/дл) у пациентов, получавших тоцилизумаб, и 0,19 ммоль/л (7 мг/дл) у пациентов, получавших адалимумаб. Профиль безопасности, наблюдавшийся в группе тоцилизумаба, совпадал с известным профилем безопасности препарата; новых или неожиданных нежелательных реакций на препарат выявлено не было.
Ювенильный идиопатический полиартрит
Безопасность тоцилизумаба изучалась у 188 пациентов детского возраста (2-17 лет) с ювенильным идиопатическим полиартритом. Общий показатель воздействия препарата во всей популяции составил 184,4 пациенто-лет. В целом, типы нежелательных реакций у пациентов с ювенильным идиопатическим полиартритом совпадали с типами реакций, наблюдаемых у пациентов с РА и сЮИА.
Инфекции
Частота возникновения инфекций во всей популяции пациентов, получавшей тоцилизумаб, составил 163,7 случаев на 100 пациенто-лет. К наиболее распространенным нежелательным явлениям относились назофарингит и инфекции верхних дыхательных путей. Частота возникновения серьезных инфекций была количественно выше у пациентов с массой тела менее 30 кг, получавших тоцилизумаб в дозе 10 мг/кг (12,2 случаев на 100 пациенто-лет), по сравнению с пациентами с массой тела от 30 кг и более, получавших препарат в дозе 8 мг/кг (4,0 случая на 100 пациенто-лет). Распространенность инфекций, приводящих к необходимости прерывания терапии, также была количественно выше у пациентов с массой тела менее 30 кг, получавших тоцилизумаб в дозе 10 мг/кг (21,4%) по сравнению с пациентами с массой тела от 30 кг и более, получавших препарат в дозе 8 мг/кг (7,6%).
Инфузионные реакции
У пациентов с ювенильным идиопатическим полиартритом инфузионные реакции определяются как все явления, имеющие место во время инфузии или в течение 24 часов после нее. Во всей популяции пациентов, получавших тоцилизумаб, у 11 (5.9%) пациентов реакции возникли во время инфузии, а у 38 (20,3%) пациентов – в течение 24 часов после внутривенной инфузии. К наиболее распространенным реакциям, имевшим место во время инфузии, относились головная боль, тошнота и пониженное артериальное давление; самыми распространенными реакциями, возникшими в течение 24 часов после инфузии, были головокружение и пониженное артериальное давление. В целом, реакции, наблюдавшиеся во время инфузии и в течение 24 часов после нее, совпадали с реакциями, имевшими место у пациентов с РА и сЮИА. Не сообщалось о случаях клинически значимых реакций гиперчувствительности, связанных с использованием тоцилизумаба и потребовавших прекращения терапии.
Иммуногенность
У одного пациента с массой тела менее 30 кг, получавшего препарат в дозе 10 мг/кг, были обнаружены антитела к тоцилизумабу без сопутствующих реакций гиперчувствительности. Впоследствии, это пациент прекратил участие в исследовании.
Снижение количества нейтрофилов
При мониторинге лабораторных показателей снижение АЧН менее 1х109/л наблюдалось у 3,7%.
Снижение количества тромбоцитов
При мониторинге лабораторных показателей снижение количества тромбоцитов менее 50х109/л наблюдалось у 1% пациентов. Данные изменения не сопровождались развитием эпизодов кровотечения.
Повышение активности «печеночных» трансаминаз
При мониторинге лабораторных показателей повышение активности АЛТ или АСТ (более чем в 3 раза превышающее ВГН) имело место у 3,7% и менее, чем у 1% пациентов соответственно.
Изменения показателей липидного обмена
При мониторинге лабораторных показателей повышение уровня общего холестерина в 1,5 – 2 раза выше ВГН наблюдалось у одного пациента (0,5%) и повышение показателей ЛПНП в 1,5-2 раза выше ВГН – у 1 пациента (0,5%).
Системный ювенильный идиопатический артрит
Безопасность тоцилизумаба исследовалась у 112 пациентов детского возраста (от 2 до 17 лет) с сЮИА. Во время 12-недельного двойного слепого плацебо- контролируемого клинического исследования 75 пациентов получали терапию тоцилизумабом (8 или 12 мг/кг в зависимости от массы тела). Через 12 недель или после прекращения участия в двойной слепой фазе исследования по причине ухудшения течения заболевания, пациенты получали терапию в ходе наблюдательной фазы исследования.
В целом, нежелательные реакции у пациентов с сЮИА совпадали с реакциями, наблюдавшимися у пациентов с РА. По сравнению с взрослыми у детей чаще встречались назофарингит, снижение количества нейтрофилов, повышение активности «печеночных» трансаминаз и диарея; повышение уровня холестерина встречалось реже.
Инфекции
В 12-недельном контролируемом периоде исследования частота всех инфекций в группе пациентов, получавших терапию тоцилизумабом, составила 344.7 случаев на 100 пациенто-лет в сравнении с 287 случаями на 100 пациенто-лет в группе пациентов, получавших плацебо. В наблюдательном периоде исследования (часть II) общая частота инфекций оставалась на уровне 306.6 случаев на 100 пациенто-лет.
В 12-недельном контролируемом периоде исследования частота серьезных инфекций в группе пациентов, получавших тоцилизумаб, составила 11,5 случаев на 100 пациенто-лет. В наблюдательном периоде исследования частота серьезных инфекций в группе пациентов, получавших тоцилизумаб, оставалась стабильной на уровне 11.3 случаев на 100 пациенто-лет. Зарегистрированные серьезные инфекции не отличались от таковых у пациентов с ревматоидным артритом, за исключением ветряной оспы и среднего отита.
Инфузионные реакции
Реакции, связанные с инфузией, у пациентов с сЮИА определялись как любое явление, возникающее во время или в течение 24 часов после инфузии. В 12-недельном контролируемом периоде исследования 4% пациентов, получавших терапию тоцилизумабом, испытали нежелательные явления, возникавшие во время инфузии; у одного пациента терапия тоцилизумабом была отменена в связи с развитием серьезного и опасного для жизни ангионевротического отека.
В 12-недельном контролируемом периоде клинического исследования у 16% пациентов, получавших тоцилизумаб, и у 5,4% пациентов, получавших плацебо, возникли нежелательные явления в течение 24 часов после проведения инфузии. У пациентов, получавших тоцилизумаб, к нежелательным явлениям относились в т.ч. сыпь, крапивница, диарея, дискомфорт в эпигастрии, артралгия, головная боль и другие.
Менее чем у 1% (1/112) пациентов, получавших тоцилизумаб в контролируемый и открытый периоды клинического исследования, зарегистрирована клинически значимая реакция гиперчувствительности, связанная с терапией и потребовавшая ее отмены.
Иммуногенность
В начале исследования все 112 пациентов прошли обследование на наличие антител к тоцилизумабу. Антитела к тоцилизумабу были выявлены у 2 из 112 обследованных пациентов. У одного из них развилась реакция гиперчувствительности, что привело к отмене лечения.
Снижение количества нейтрофилов
При рутинном мониторинге лабораторных показателей в ходе 12-недельного контролируемого исследования, снижение числа нейтрофилов ниже 1×109/л имело место у 7% пациентов, получавших тоцилизумаб, и отсутствовало у пациентов, получавших плацебо. В наблюдательном периоде исследования снижение числа нейтрофилов ниже 1×109/л зарегистрировано у 15% пациентов, получающих тоцилизумаб. Четкой связи между снижением числа нейтрофилов ниже 1×109/л и развитием серьезных инфекционных заболеваний не отмечалось.
Снижение количества тромбоцитов
При рутинном мониторинге лабораторных показателей в 12-недельном контролируемом периоде клинического исследования снижение числа тромбоцитов до уровня 100×109/л и менее возникло у 1% пациентов, получавших тоцилизумаб, и у 3% пациентов, получавших плацебо.
В наблюдательном периоде исследования снижение числа тромбоцитов ниже 100×103/мкл зарегистрировано у 3% пациентов, получающих тоцилизумаб. Данные изменения не сопровождались развитием эпизодов кровотечения.
Повышение активности “печеночных” трансаминаз
При рутинном мониторинге лабораторных показателей в 12-недельном контролируемом периоде клинического исследования, повышение активности АЛТ или АСТ (более чем в 3 раза превышающее ВГН) имело место у 5% и 3% пациентов, соответственно, в группе тоцилизумаба, и у 0% пациентов в группе плацебо.
В наблюдательном периоде исследования повышение активности АЛТ или АСТ (более чем в 3 раза превышающее ВГН) имело место у 12% и 4% пациентов, соответственно, в группе тоцилизумаба.
Изменение показателей липидного обмена
При рутинном мониторинге лабораторных показателей в 12-недельном контролируемом периоде клинического исследования повышение показателя общего холестерина в 1,5-2 раза выше ВГН возникало у 1.5% пациентов, получавших тоцилизумаб, и у 0% пациентов, получавших плацебо. Повышение показателя ЛПНП в 1,5-2 раза выше ВГН возникало у 1.9% пациентов, получавших тоцилизумаб, и у 0% пациентов, получавших плацебо.
В продолжающемся открытом расширенном наблюдательном периоде исследования характер и частота повышения показателей липидного обмена соответствовали результатам, зарегистрированным в 12-недельном контролируемом периоде клинического исследования.
Пострегистрационное применение
Профиль безопасности препарата при пострегистрационном применении согласуется с данными клинических исследований, за исключением случаев развития фатальной анафилаксии и случаев развития синдрома Стивенса-Джонсона во время терапии тоцилизумабом.
Противопоказания
-
гиперчувствительность к тоцилизумабу или другим компонентам препарата
-
острые инфекционные заболевания и хронические инфекции в стадии обострения
-
нейтропения (абсолютное число нейтрофилов менее 0,5×109/л)
-
тромбоцитопения (число тромбоцитов менее 50×109/л)
-
увеличение показателей АЛТ/АСТ более чем в 5 раз по сравнению с верхними границами нормы (более 5N)
-
беременность и период лактации
-
детский возраст до 2 лет
Лекарственные взаимодействия
Данные популяционного фармакокинетического анализа не выявили какого-либо влияния метотрексата, нестероидных противовоспалительных или кортикостероидных препаратов на клиренс тоцилизумаба. Одновременное введение Актемры в дозе 10 мг/кг массы тела с метотрексатом в дозе 10-25 мг один раз в неделю не имело достоверного клинического эффекта на экспозицию метотрексата.
Не существует данных о применении Актемры в комбинации с другими биопрепаратами.
Цитокины, стимулирующие хроническое воспаление, например, интерлейкин-6, подавляют экспрессию монооксидаз печени системы цитохрома CYP450. При лечении Актемрой, мощным ингибитором цитокинов, возможен обратный эффект. В исследованиях на гепатоцитах продемонстрировано, что интерлейкин-6 вызывает снижение выработки энзимов CYP1A2, CYP2C9, CYP2C19 и CYP3A4, а Актемра нормализует выработку этих энзимов. Влияние тоцилизумаба на изоферменты CYP (кроме СYP2C19 и CYP2D6 имеет клиническое значение для препаратов, являющихся субстратами CYP450, с узким терапевтическим индексом, и/или для которых дозы подбираются индивидуально.
В клиническом исследовании с участием больных ревматоидным артритом отмечено снижение концентрации симвастатина (CYP2A4) до нормального, или несколько повышенного уровня через неделю после однократного введения Актемры.
При начале или остановке лечения Актемрой следует наблюдать за пациентами, принимающими препараты, которые метаболизируются посредством энзимов системы цитохрома CYP450 – 3А4, 1А2 или 2С9 (например, аторвастатин, блокаторы кальциевых каналов, теофиллин, варфарин, фенитоин, циклоспорин или бензодиазепины), так как дозы этих препаратов нуждаются в корректировке для поддержания их терапевтического эффекта. Учитывая длительный период полувыведения тоцилизумаба, влияние Актемры на активность энзимов системы цитохрома CYP 450 может сохраняться в течение нескольких недель после прекращения терапии.
Особые указания
В медицинской документации следует указывать торговое наименование препарата.
Инфекции
У пациентов, получающих иммуносупрессанты (в т.ч. тоцилизумаб) наблюдались серьезные случаи возникновения инфекционных заболеваний (иногда с летальным исходом). Лечение Актемрой не начинают у больных с инфекционным заболеванием в активной фазе. Введение Актемры прекращают, если у пациента появились признаки серьезного инфекционного заболевания до его излечения.
С осторожностью назначают Актемру пациентам с рецидивирующим инфекционным заболеванием в анамнезе и с сопутствующими заболеваниями (дивертикулит, диабет), которые могут предрасполагать пациента к инфекционным заболеваниям.
Рекомендуется с особой тщательностью наблюдать пациентов, получающих биологические препараты по поводу ревматоидного артрита, сЮИА или ювенильного идиопатического полиартрита, для своевременного выявления признаков серьезных инфекций, так как симптомы острого воспаления могут быть ослаблены вследствие подавления острой фазы воспаления этими препаратами. Пациентов и родителей/опекунов детей с сЮИА/ ювенильным идиопатическим полиартритом надо проинформировать, что при появлении первых признаков инфекционного заболевания следует обратиться к лечащему врачу или медработнику для своевременной оценки состояния и назначения соответствующего лечения.
Осложнения со стороны дивертикулитов
Существуют сообщения об осложнениях со стороны дивертикулитов в виде перфорации стенки. Актемру применяют с осторожностью у больных с указаниями на язвенное поражение или дивертикулиты тонкого кишечника в анамнезе. Больные с симптомами возможной перфорации дивертикулита, такими как боль в животе, должны быть обследованы на предмет желудочно-кишечной перфорации.
Туберкулез
Перед началом лечения Актемрой пациенты (как и при лечении ревматоидного артрита, сЮИА или ювенильного идиопатического полиартрита другими биопрепаратами) должны пройти обследование на выявление латентно протекающего туберкулеза. При обнаружении латентного туберкулеза пациенты должны пройти стандартное противотуберкулезное лечение, прежде чем начать лечение Актемрой. Пациентам необходимо рекомендовать обратиться за специализированной помощью в случае появления во время или после терапии тоцилизумабом признаков/симптомов, аналогичных с симптомами туберкулеза (постоянный кашель, потеря веса, слабовыраженная лихорадка).
Вакцинация
Не рекомендуется вакцинация живыми и живыми ослабленными вакцинами пациентов, которые находятся на лечении Актемрой, так как клиническая безопасность этого не установлена.
В рандомизированном открытом исследовании иммунный ответ на 23-валентную полисахаридную вакцину и столбнячный анатоксин у взрослых пациентов с РА, получавших тоцилизумаб в комбинации с метотрексатом, был сравним с ответом, наблюдавшимся у пациентов, получавших только метотрексат.
Пациентам с системным ювенильным идиопатическим артритом и полиартикулярным ювенильным идиопатическим артритом рекомендуется пройти вакцинацию в соответствии с национальным календарем вакцинации до начала терапии Актемрой. Следует соблюдать интервал (в соответствии с действующими рекомендациями по иммунизации) у пациентов, получающих терапию иммуносупрессивными препаратами, между иммунизацией живыми вакцинами и началом терапии препаратом.
Реакции гиперчувствительности
В связи с применением тоцилизумаба сообщалось о случаях реакций гиперчувствительности, включая анафилаксию. При пострегистрационном применении серьезные явления гиперчувствительности и анафилаксии (в т.ч. с летальным исходом) возникали у пациентов, получавших различные дозы тоцилизумаба независимо от наличия сопутствующей терапии для лечения ревматоидного артрита, премедикации и/или реакций гиперчувствительности в анамнезе. Данные явления возникали уже во время первой инфузии препарата. При введении тоцилизумаба должен быть предусмотрен комплекс необходимых мероприятий для лечения возможной анафилактической реакции во время инфузии. При возникновении анафилактической реакции или другой серьезной реакции гиперчувствительности введение тоцилизумаба следует немедленно остановить и не возобновлять терапию препаратом в дальнейшем.
Активные заболевания печени и печеночная недостаточность
При лечении Актемрой, особенно в комбинации с метотрексатом, могут повышаться уровни печеночных трансаминаз. Поэтому больным с активным заболеванием печени и печеночной недостаточностью Актемру назначают с осторожностью, так как безопасность и эффективность у данной группы больных изучена не достаточно.
Реактивация вирусных инфекций
У пациентов с ревматоидным артритом, получавших терапию биологическими препаратами, наблюдались случаи реактивации вирусной инфекции (например, вирусного гепатита В). Пациенты, имевшие положительный результат при скрининговом обследовании на гепатит, не включались в клинические исследования тоцилизумаба.
Демиелинизирующие заболевания
Врачам следует проявлять особую осторожность с целью раннего выявления симптомов, возможно указывающих на развитие демиелинизирующих заболеваний ЦНС. В настоящее время способность тоцилизумаба вызывать демиелинизирующие заболевания ЦНС не известна.
Изменения лабораторных показателей
Снижение количества нейтрофилов
При лечении Актемрой высока частота нейтропении. Возникшая на фоне лечения нейтропения в клинических исследованиях не была связана с серьезными инфекциями. С осторожностью назначают Актемру пациентам с низким абсолютным числом нейтрофилов, то есть ANC < 2х109/л. Лечение не рекомендуется начинать при ANC ниже 0,5×109/л. Содержание нейтрофилов следует отслеживать в течение 4-8 недель после начала лечения, а также периодически на протяжении всего периода лечения. При ювенильном идиопатическом полиартрите и сЮИА число нейтрофилов следует контролировать в день проведения 2-й инфузии, а в дальнейшем в соответствии с клинической практикой. В зависимости от содержания нейтрофилов дозу Актемры корректируют в соответствии с рекомендациями в разделе «Способ применения и дозы».
Снижение количества тромбоцитов
Лечение Актемрой связано со снижением содержания тромбоцитов. Возникшая на фоне лечения тромбоцитопения в клинических исследованиях не была связана с серьезными кровотечениями. С осторожностью назначают Актемру при содержании тромбоцитов ниже 100×109/л. Лечение не рекомендуется начинать при содержании тромбоцитов ниже 50×109/л. Содержание тромбоцитов следует отслеживать в течение 4-8 недель после начала лечения, а также периодически на протяжении всего периода лечения. При ювенильном идиопатическом полиартрите и сЮИА число тромбоцитов следует контролировать в день проведения 2-й инфузии, а в дальнейшем в соответствии с клинической практикой. В зависимости от содержания тромбоцитов дозу Актемры модифицируют в соответствии с рекомендациями в разделе «Способ применения и дозы».
Повышение уровня «печеночных» трансаминаз
Небольшое или умеренное повышение уровней печеночных трансаминаз (АСТ и АЛТ) при лечении Актемрой, которое наблюдалось в клинических исследованиях, не сопровождалось признаками прогрессирования заболеваний печени. Повышение уровня ферментов печени наблюдалось чаще в группах больных, получавших в комбинации с Актемрой потенциально гепатотоксические препараты (например, метотрексат). С осторожностью следует начинать лечение Актемрой при повышении уровня трансаминаз более чем в 1,5 раза превышающем верхний предел нормы. Лечение Актемрой не рекомендуется, если уровень трансаминаз превышает верхний предел нормы в 5 раз. Уровни трансаминаз следует отслеживать в первые 4-8 недель после начала лечения, а также периодически на протяжении всего периода лечения. При ювенильном идиопатическом полиартрите и сЮИА уровни АЛТ и АСТ следует контролировать в день проведения 2-й инфузии, а в дальнейшем в соответствии с клинической практикой. В зависимости от степени повышения уровня ферментов печени дозу подбирают в соответствии с рекомендациями в разделе «Способ применения и дозы».
Неврологические расстройства
Медицинским работникам следует проявлять особую осторожность с целью раннего выявления симптомов, которые могут указывать на развитие демиелинизирующего заболевания ЦНС. В настоящее время способность тоцилизумаба вызывать демиелинизирующие заболевания ЦНС неизвестна.
Злокачественные новообразования
У пациентов с ревматоидным артритом повышен риск развития злокачественных опухолей. Иммуномодулирующие лекарственные средства могут увеличивать этот риск.
Риск развития сердечно-сосудистых заболеваний
У пациентов с ревматоидным артритом повышен риск развития сердечно-сосудистых заболеваний. Лечение патологий, являющихся факторами риска (артериальная гипертензия, гиперлипидемия) проводится в рамках стандартной терапевтической практики.
Комбинированная терапия вместе с антагонистами ФНО
Данные по совместному применению препарата Актемра и антагонистов ФНО или других биологических препаратов для лечения ревматоидного артрита, сЮИА или ювенильного идиопатического полиартрита отсутствуют. Не рекомендуется использовать Актемру с другими биологическими препаратами.
Содержание натрия
Препарат Актемра содержит натрий (1,17 ммоль или 26,55 мг в максимальной дозе 1200 мг). Данный факт должен учитываться пациентами, соблюдающими гипонатриевую диету. Дозировка Актемры ниже 1025 г содержит менее 1 ммоль (23 мг) натрия, т.е., практически не содержит натрий.
Системный ювенильный идиопатический артрит
Синдром активации макрофагов является серьезным и опасным для жизни состоянием, которое может развиться у пациентов с сЮИА. В клинических исследованиях эффективность и безопасность тоцилизумаба не изучались в период возникновения синдрома активации макрофагов.
Беременность и период лактации
Не следует применять препарат Актемра в период беременности и лактации.
Особенности влияния лекарственного средства на способность управлять транспортным средством и потенциально опасными механизмами
Исследования влияния тоцилизумаба на способность к вождению автомобиля и управлению механизмами не проводились. В настоящее время не существует информации, указывающей на то, что препарат каким-либо образом влияет на способность к управлению автотранспортом и работе с различными механизмами.
Передозировка
Доступные данные о передозировке тоцилизумабом ограничены. В одном случае непреднамеренной передозировки препарата в дозе 40 мг/кг у пациента с множественной миеломой нежелательных реакций не отмечено. Не отмечалось также серьезных нежелательных реакций у здоровых добровольцев, которые получали однократно тоцилизумаб в дозе до 28 мг/кг, хотя наблюдалась нейтропения, потребовавшая снижения дозы.
Лечение: симптоматическое.
Форма выпуска и упаковка
По 80мг/4мл, 200мг/10мл, 400мг/20мл помещают во флаконы бесцветного нейтрального стекла типа 1 вместимостью 10 мл (для дозировки 80мг/4мл) или 20 мл (для дозировок 200мг/10мл и 400мг/20мл), укупоренные пробками из бутилкаучука с покрытием из фтористого полимера и алюминиевыми колпачками с пластиковыми крышками «flip-off».
По 1 флакону вместе с инструкцией по медицинскому применению на государственном и русском языках помещают в пачку из картона.
Условия хранения
В оригинальной упаковке при температуре от 2 °С до 8 °С. Не замораживать. Хранить в недоступном для детей месте!
Срок хранения
2.5 года
Не применять по истечении срока годности, указанного на упаковке
Условия отпуска из аптек
По рецепту
Производитель
Чугай Фарма Мануфактуринг Ко. Лтд., Уцуномия-Сити, Япония
Владелец регистрационного удостоверения
Ф. Хоффманн-Ля Рош Лтд., Базель, Швейцария
Упаковщик
Ф. Хоффманн-Ля Рош Лтд., Кайзераугст, Швейцария
Адрес организации, принимающей на территории Республики Казахстан претензии от потребителей по качеству товара и ответственной за фармаконадзор
ТОО «Рош Казахстан»
050000, г.Алматы, ул. Кунаева, 77,
Бизнес-центр «Park View Office Tower», 15 этаж
Тел.: +7 (727) 321 24 24, факс: + 7 (727) 321 24 25
e-mail: kz.safety@roche.com, kz.quality@roche.com
CDS 11.0, EU SmPC EMEA/H/C/000955/II/0032-II39, approved by EMA 01.09.2014
| 319744121477976496_ru.doc | 231 кб |
| 379792441477977664_kz.doc | 220.5 кб |
Отправить прикрепленные файлы на почту
Национальный центр экспертизы лекарственных средств, изделий медицинского назначения и медицинской техники
Актемра® (Actemra®) инструкция по применению
📜 Инструкция по применению Актемра®
💊 Состав препарата Актемра®
✅ Применение препарата Актемра®
📅 Условия хранения Актемра®
⏳ Срок годности Актемра®
Описание лекарственного препарата
Актемра®
(Actemra®)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для печатного издания справочника Видаль 2023 года.
Дата обновления: 2022.11.16
Код ATX:
L04AC07
(Тоцилизумаб)
Лекарственные формы
| Актемра® |
Концентрат д/пригот. р-ра д/инфузий 80 мг/4 мл: фл. 1 шт. рег. №: ЛСР-003012/09 |
|
|
Концентрат д/пригот. р-ра д/инфузий 200 мг/10 мл: фл. 1 шт. рег. №: ЛСР-003012/09 |
||
|
Концентрат д/пригот. р-ра д/инфузий 400 мг/20 мл: фл. 1 шт. рег. №: ЛСР-003012/09 |
Форма выпуска, упаковка и состав
препарата Актемра®
Концентрат для приготовления раствора для инфузий в виде прозрачной или опалесцирующей, бесцветной или светло-желтого цвета жидкости.
Вспомогательные вещества: полисорбат 80 — 0.5 мг, сахароза — 50 мг, натрия гидрофосфата додекагидрат — q.s., натрия дигидрофосфата дигидрат — q.s., вода д/и — q.s.
4 мл — флаконы бесцветного стекла (1) — пачки картонные с вкладышами картонными (перегородками)×.
4 мл — флаконы бесцветного стекла (1) — поддоны пластиковые* (1) — пачки из картона импортного××.
Концентрат для приготовления раствора для инфузий в виде прозрачной или опалесцирующей, бесцветной или светло-желтого цвета жидкости.
Вспомогательные вещества: полисорбат 80 — 0.5 мг, сахароза — 50 мг, натрия гидрофосфата додекагидрат — q.s., натрия дигидрофосфата дигидрат — q.s., вода д/и — q.s.
10 мл — флаконы бесцветного стекла (1) — пачки картонные с вкладышами картонными (перегородками)×.
10 мл — флаконы бесцветного стекла (1) — поддоны пластиковые* (1) — пачки из картона импортного××.
Концентрат для приготовления раствора для инфузий в виде прозрачной или опалесцирующей, бесцветной или светло-желтого цвета жидкости.
Вспомогательные вещества: полисорбат 80 — 0.5 мг, сахароза — 50 мг, натрия гидрофосфата додекагидрат — q.s., натрия дигидрофосфата дигидрат — q.s., вода д/и — q.s.
20 мл — флаконы бесцветного стекла (1) — пачки картонные с вкладышами картонными (перегородками)×.
20 мл — флаконы бесцветного стекла (1) — поддоны пластиковые* (1) — пачки из картона импортного××.
× с целью контроля первого вскрытия на пачку наносится защитная голографическая наклейка.
×× с целью контроля первого вскрытия на пачку наклеивают самоклеящиеся круглые стикеры с надписью «контроль вскрытия» (в случае упаковки на ОАО «Фармстандарт-УфаВИТА»).
* поддоны пластиковые или вкладыши картонные.
Фармакологическое действие
Механизм действия
Тоцилизумаб — рекомбинантное гуманизированное моноклональное антитело к человеческому рецептору интерлейкина-6 (ИЛ-6) из подкласса иммуноглобулинов IgG1. Тоцилизумаб связывается и подавляет как растворимые, так и мембранные рецепторы ИЛ-6 (sIL-6R и mIL-6R). ИЛ-6 является многофункциональным цитокином, вырабатываемым различными типами клеток, и участвует в паракринной регуляции, системных физиологических и патологических процессах, таких как стимуляция секреции Ig, активация Т-клеток, стимуляция выработки белков острой фазы в печени и стимуляция гемопоэза. ИЛ-6 вовлечен в патогенез различных заболеваний, в т.ч. воспалительных заболеваний, остеопороза и новообразований.
Нельзя исключить вероятность отрицательного воздействия тоцилизумаба на противоопухолевую и противоинфекционную защиту организма. Роль ингибирования рецептора ИЛ-6 в развитии опухолей неизвестна.
У пациентов с коронавирусной инфекцией (COVID-19, COronaVIrus Disease 2019), получавших тоцилизумаб в дозе 8 мг/кг однократно, снижение показателя C-реактивного белка (CРБ) до нормальных значений наблюдалось уже на 7 день.
Клиническая эффективность при ревматоидном артрите (РА)
Эффективность препарата у пациентов, получавших тоцилизумаб как в монотерапии, так и в комбинации с метотрексатом (МТ) или базисными противовоспалительными препаратами (БПВП), не зависела от наличия и отсутствия ревматоидного фактора, возраста, пола, расовой принадлежности, числа предшествующих курсов лечения или стадии заболевания. Ответ на терапию возникал быстро (уже на второй неделе), в дальнейшем усиливался и сохранялся более 3 лет в продолжающихся открытых расширенных исследованиях.
У пациентов, получавших тоцилизумаб в дозе 8 мг/кг, существенно снижался индекс активности заболевания по шкале DAS28 по сравнению с пациентами, получавшими плацебо + БПВП. Число пациентов, достигших клинической ремиссии (DAS28 <2.6) на 24 неделе, было значительно больше в группе терапии тоцилизумабом (27.5-33.6%) по сравнению с контрольной группой (0.8-12.1%). К 52 неделе терапии число пациентов, достигших DAS28 <2.6, увеличивается до 47% по сравнению с 33% на 24 неделе терапии. Хороший или удовлетворительный ответ по критериям EULAR отмечался чаще у пациентов, получавших тоцилизумаб, чем получавших плацебо + БПВП.
Через 2 года терапии тоцилизумабом/МТ у 14% пациентов наблюдался значительный клинический ответ (АКР 70 (критерии Американской Коллегии Ревматологов, АКР) сохранялся на протяжении 24 недель и более).
Рентгенологическая оценка
У 83% пациентов, получавших терапию тоцилизумабом/МТ в течение года, не зарегистрировано прогрессирования деструкции суставов (изменение суммарного индекса Шарпа равно нулю или менее) по сравнению с 67% пациентов, получавших плацебо/МТ. Данный результат сохранялся на протяжении 2 лет терапии. У 93% пациентов отсутствовало прогрессирование деструкции суставов между 52 и 104 неделями терапии.
Показатели качества жизни
У пациентов, получавших тоцилизумаб в дозе 8 мг/кг (монотерапия или в сочетании с БПВП), по сравнению с теми, кто получал МТ/БПВП, наблюдалось клинически значимое улучшение функциональной активности (по индексу HAQ-DI), снижение утомляемости (по шкале функциональной оценки терапии хронических заболеваний по показателю утомляемости FACIT-Fatigue), а также улучшение как показателей физического, так и показателей психического здоровья по опроснику SF-36.
Лабораторные показатели
После введения тоцилизумаба происходит быстрое снижение средних значений острофазовых показателей, С-реактивного белка, СОЭ, сывороточного амилоида А и фибриногена, снижение числа тромбоцитов в пределах нормальных значений, а также увеличение гемоглобина, которое в наибольшей степени наблюдалось у пациентов с хронической анемией, связанной с РА.
Клиническая эффективность у пациентов с ранним ревматоидным артритом (рРА), ранее не получавших терапию МТ
При применении тоцилизумаба в монотерапии в дозе 8 мг/кг и тоцилизумаба в дозе 4 или 8 мг/кг каждые 4 недели в комбинации с МТ индекс активности заболевания по шкале DAS28 существенно снижается в группах, получавших тоцилизумаб в дозе 8 мг/кг, по сравнению с пациентами, получавшими монотерапию МТ. Число пациентов, достигших клинической ремиссии (DAS28 <2.6) на 24 неделе, значительно больше в группах, получавших тоцилизумаб (38.7-44.8%), по сравнению с группой монотерапии МТ (15%). К 52 неделе число пациентов, достигших DAS28 <2.6 в группах терапии тоцилизумабом, увеличивается до 39.4-49% по сравнению с 19.5% в группе монотерапии МТ. Число пациентов, достигших ответа АКР 20, 50, 70, также существенно выше в группах терапии тоцилизумабом (70.2-74.5%; 47.6-56.9%; 30.1-38.6% на 24 неделе и 63-67.2%; 49.3-55.9%; 36-43.1% на 52 неделе, соответственно) по сравнению с группой монотерапии МТ (65.2%; 43.2%; 25.4% на 24 неделе и 57.1%; 40.8%; 28.9% на 52 неделе, соответственно).
Рентгенологическая оценка
Отсутствие прогрессирования деструкции суставов (изменение суммарного индекса Шарпа равно нулю или менее) наблюдается у 82-83% пациентов, получавших тоцилизумаб в дозе 8 мг/кг в качестве монотерапии или в комбинации с МТ, по сравнению с 73% пациентов в группе монотерапии МТ.
Показатели качества жизни
Клинически значимое улучшение функциональной активности по индексу HAQ-DI наблюдается у пациентов, получавших тоцилизумаб в дозе 8 мг/кг в качестве монотерапии или комбинации с МТ, по сравнению с теми, кто получал монотерапию МТ.
При монотерапии тоцилизумабом (в дозе 8 мг/кг в/в каждые 4 недели у пациентов с РА, с непереносимостью МТ или при нецелесообразности продолжения терапии МТ (в т.ч. при неадекватном ответе на терапию МТ)) наблюдалось более выраженное статистически значимое снижение активности заболевания по шкале DAS28 по сравнению с монотерапией адалимумабом (в дозе 40 мг п/к каждые 2 недели). Количество пациентов, ответивших на терапию с показателями DAS28 <2.6 и DAS28 ≤3.2, было больше при терапии тоцилизумабом, чем при терапии адалимумабом (39.9% против 10.5% и 51.5% против 19.8%, соответственно). Ответы АКР 20, 50, 70 наблюдались у 65%, 47.2%, 32.5% пациентов, получавших тоцилизумаб, по сравнению с 49.4%, 27.8%, 17.9% пациентов, получавших адалимумаб.
Клиническая эффективность при полиартикулярном ювенильном идиопатическом артрите (пЮИА)
Ответы АКР 30, 50, 70, 90 были получены у 89.4%, 83.0%, 62.2% и 26.1% пациентов, соответственно. Доля пациентов с ответом АКР 30, 50, 70 на 40 неделе терапии относительно показателей на начало терапии составила 74.4%, 73.2% и 64.6% соответственно.
Клиническая эффективность при системном ювенильном идиопатическом артрите (сЮИА)
Эффективность тоцилизумаба для лечения активного сЮИА изучалась в 12-недельном рандомизированном двойном слепом плацебо контролируемом периоде исследования с 2 параллельными группами. На 12 неделе доля пациентов, достигших ответа АКР 30, 50, 70, 90 при ЮИА, также была больше в группе терапии тоцилизумабом, чем в группе плацебо: 90.7% против 24.3%, 85.3% против 10.8%, 70.7% против 8.1%, 37.3% против 5.4%, соответственно (р<0.0001). Ответ на терапию сохранялся и в открытом расширенном периоде исследования.
Системные эффекты
У 85% пациентов, имевших исходно лихорадку, через 12 недель терапии тоцилизумабом лихорадка отсутствовала по сравнению с 21% пациентов, получавших плацебо (р<0.0001). Кроме того, у 64% пациентов, имевших сыпь исходно, через 12 недель терапии тоцилизумабом сыпь отсутствовала по сравнению с 11% пациентов, получавших плацебо (р=0.0008).
Наблюдалось значимое снижение интенсивности болевого синдрома в группе терапии тоцилизумабом по сравнению с плацебо на 12 неделе. Скорректированное среднее изменение оценки боли по визуальной аналоговой шкале (ВАШ) после 12 недель терапии тоцилизумабом соответствовало 41 пункту (от 0 до 100 пунктов) по сравнению с 1 пунктом у пациентов, получавших плацебо (р<0.0001). Системные эффекты сохранялись и в продолжающемся открытом расширенном периоде исследования.
Снижение дозы ГКС
У 8 из 31 пациента в группе плацебо и у 48 из 70 пациентов в группе тоцилизумаба, получавших ГКС исходно, наблюдался ответ АКР 70 при ЮИА на 6 или 8 неделе, что позволило снизить дозу ГКС. При этом 24% пациентов в группе тоцилизумаба и 3% пациентов в группе плацебо смогли снизить дозу ГКС как минимум на 20% без последующего снижения частоты ответа по критериям АКР 30 при ЮИА или возникновения системных проявлений к 12 неделе (р=0.028). Снижение дозы ГКС продолжилось, при этом 44 пациента не получали ГКС на 44 неделе, и ответы АКР не изменялись.
Показатели качества жизни
На 12 неделе доля пациентов в группе тоцилизумаба, демонстрирующих минимальное клинически значимое улучшение показателя по опроснику CHAQ-DI (определенного как снижение индивидуального общего балла на ≥0.13), была значительно выше, чем доля пациентов в группе плацебо — 77% против 19%, соответственно (р<0.0001). Ответы сохранялись и в продолжающемся открытом расширенном периоде исследования.
Лабораторные показатели
Исходно у 67% пациентов из группы тоцилизумаба содержание гемоглобина было ниже нормального диапазона. У 80% из этих пациентов на 12 неделе наблюдалось увеличение Hb в пределах нормального диапазона по сравнению с 7% пациентов в группе плацебо (р<0.0001). У 88% пациентов из группы тоцилизумаба, имевших исходно сниженное содержание гемоглобина, его уровень увеличился на ≥10 г/л к 6 неделе, в группе плацебо частота повышения составила 3% (р<0.0001).
Доля пациентов, имевших исходно тромбоцитоз и у которых на 12 неделе наблюдалось нормальное число тромбоцитов, была выше в группе тоцилизумаба по сравнению с группой плацебо — 90% против 4% (р<0.0001).
После введения тоцилизумаба происходило быстрое снижение средних значений острофазовых показателей: С-реактивного белка, СОЭ и сывороточного амилоида А.
Клиническая эффективность при COVID-19
Исследование совместной исследовательской группы RECOVERY (рандомизированная оценка терапии по поводу COVID-19) у госпитализированных взрослых пациентов с диагнозом COVID-19
Исследование RECOVERY представляло собой крупномасштабное, рандомизированное, контролируемое, открытое, многоцентровое платформенное исследование, проведенное в Великобритании для оценки эффективности и безопасности потенциальных вариантов терапии у госпитализированных взрослых пациентов с тяжелой формой COVID-19. Все пациенты, подходящие для включения в исследование, получали стандартную терапию и прошли начальную (основную) рандомизацию. Пациенты, подходящие для включения в исследование, имели подозреваемую на основании клинических признаков или лабораторно подтвержденную инфекцию SARS-CoV-2 и не имели медицинских противопоказаний к применению любого из рассматриваемых в исследовании видов терапии. Пациенты с клиническими подтверждениями прогрессирующей инфекции COVID-19 (определяемыми как уровень сатурации крови кислородом (SpO2) <92% при дыхании атмосферным воздухом или получение терапии кислородом, а также уровень CРБ≥75мг/л) могли пройти вторую рандомизацию в группы, получавшие либо тоцилизумаб в/в, либо только стандартную терапию.
Анализы эффективности были проведены в популяции в соответствии с назначенным лечением (intent-to-treat, ITT), которая включала в себя 4116 рандомизированных пациентов: 2022 пациента были рандомизированы в группу, получавшую тоцилизумаб + стандартную терапию, 2094 пациента — в группу, получавшую только стандартную терапию. Исходные демографические характеристики и характеристики заболевания популяции ITT были надлежащим образом сбалансированы между группами терапии. Средний возраст участников составлял 63.6 года (стандартное отклонение [СО]: 13.6 года). Большинство пациентов были мужского пола (67%) и относились к европеоидной расе (76%). Медиана (диапазон) значений уровня CРБ составляла 143 мг/л (75-982). На исходном уровне 0.2% (N=9) пациентов не получали дополнительный кислород, 45% пациентов требовалась низкопоточная кислородная терапия, 41% пациентов требовалась высокопоточная кислородная терапия и 14% пациентов требовалась инвазивная искусственная вентиляция легких (ИВЛ); 82% пациентов получали системные ГКС. Наиболее частыми сопутствующими заболеваниями были сахарный диабет (28.4%), заболевание сердца (22.6%) и хроническая болезнь легких (23.3%).
Первичным показателем исхода было время до момента смерти в период до дня 28. Отношение рисков, демонстрирующее сравнение группы, получавшей тоцилизумаб + стандартную терапию, с группой, получавшей только стандартную терапию, составило 0.85 (95% ДИ: от 0.76 до 0.94), статистически значимый результат (р=0.0028). Расчетные показатели вероятности смерти ко дню 28 составили 30.7% и 34.9% в группах, получавших тоцилизумаб и только стандартную терапию соответственно. Расчетная разность рисков составила -4.1% (95% ДИ: от -7.0 до -1.3%), что согласуется с результатами первичного анализа. Отношение рисков в заранее определенной подгруппе пациентов, получавших системные ГКС на исходном уровне, составляло 0.79 (95% ДИ: от 0.70 до 0.89), а в заранее определенной подгруппе пациентов, не получавших системные ГКС на исходном уровне, отношение рисков составило 1.16 (95% ДИ: от 0. 91 до 1.48).
Медиана времени до выписки из стационара составляла 19 дней в группе, получавшей тоцилизумаб + стандартную терапию, и >28 дней в группе, получавшей стандартную терапию (отношение рисков [95% ДИ] = 1.22 [от 1.12 до 1.33]).
Среди пациентов, которым не требовалась инвазивная ИВЛ на исходном уровне, доля пациентов, у которых появилась потребность в ИВЛ или наступила смерть ко дню 28, составляла 35% (619/1754) в группе, получавшей тоцилизумаб + стандартную терапию, и 42% (754/1800) в группе, получавшей только стандартную терапию (отношение рисков [95% ДИ] = 0.84 [от 0.77 до 0.92] р<0.0001).
Исследование ML42528 (EMPACTA)
Исследование ML42528 представляло собой глобальное рандомизированное, двойное слепое, плацебо-контролируемое, многоцентровое исследование III фазы по оценке эффективности и безопасности применения тоцилизумаба для в/в введения в комбинации со стандартной терапией у госпитализированных взрослых пациентов с пневмонией, ассоциированной с COVID-19, не находящихся на ИВЛ. Для включения в исследование подходили пациенты в возрасте, по меньшей мере, 18 лет, имевшие инфекцию SARS-CoV-2, подтвержденную положительным результатом теста методом полимеразной цепной реакции с обратной транскриптазой (ОТ-ПЦР), имевшие пневмонию, подтвержденную результатами рентгенологического исследования, и уровень SpO2 <94% при дыхании атмосферным воздухом. Стандартная терапия могла включать в себя противовирусную терапию, применение системных ГКС в низких дозах и поддерживающую терапию. Пациенты были рандомизированы в соотношении 2:1 в группы, получавшие одну инфузию тоцилизумаба в дозе 8 мг/кг, при максимальной дозе 800 мг, либо плацебо. Если клинические признаки или симптомы ухудшались или не улучшались, могла быть введена одна дополнительная инфузия тоцилизумаба или плацебо по слепой схеме через 8-24 ч после проведения первой инфузии.
Из 389 пациентов, которые были рандомизированы, анализы эффективности были проведены в модифицированной популяции в соответствии с назначенным лечением (modified intent-to-treat, mITT), которая включала в себя пациентов, получивших любое количество исследуемого лекарственного препарата (249 пациентов в группе тоцилизумаба; 128 пациентов в группе плацебо). Исходные демографические характеристики и характеристики заболевания были в целом сбалансированы между группами терапии. В популяции mITT (n=377) на момент рандомизации медиана возраста составляла 57 лет (диапазон: от 20 до 95); 59.2% пациентов были мужского пола, 56% пациентов имели испанское или латиноамериканское этническое происхождение, 52.8% пациентов принадлежали к европеоидной расе, 20.4% пациентов были американскими индейцами/представителями коренного населения Аляски, 15.1% пациентов были представителями негроидной расы/афроамериканцами и 1.6% пациентов были представителями монголоидной расы. На исходном уровне 35 (9.3%) пациентов не получали дополнительный кислород, 242 (64.2%) пациентам требовалась низкопоточная кислородная терапия и 100 (26.5%) пациентам требовалась высокопоточная кислородная терапия. Медиана времени с момента возникновения симптомов составляла 8.0 дня. На исходном уровне в обеих группах терапии в совокупности 72.7% пациентов получали системные глюкокортикостероиды и 47.7% пациентов получали ремдесивир. Значения медианы (диапазон) уровня СРВ и ферритина составляли, соответственно, 136.10 мг/л (2.5- 3776.0) и 1.4 пмоль/мл (0.03-122.3). Наиболее частыми сопутствующими заболеваниями были артериальная гипертензия (48.3%), сахарный диабет (40.6%), гиперлипидемия (27.6%) и ожирение (24.4%).
Первичной конечной точкой оценки эффективности была совокупная доля пациентов, у которых появилась потребность в ИВЛ или наступила смерть ко дню 28. Для пациентов, которые получали тоцилизумаб, наблюдалось статистически значимое улучшение в отношении времени до прогрессирования до ИВЛ или смерти в сравнении с пациентами, которые получали плацебо (значение р для логрангового критерия = 0.0360; ОР [95% ДИ] = 0.56 [от 0.33 до 0.97]). Совокупная доля пациентов, у которых появилась потребность в ИВЛ или наступила смерть ко дню 28 (оценка с использованием метода Каплана-Мейера), составила 12.0% (95% ДИ: от 8.52 до 16.86%) в группе, получавшей тоцилизумаб, и 19.3% (95% ДИ: от 13.34 до 27.36%) в группе, получавшей плацебо
Медиана времени до выписки из стационара либо «готовности к выписке» за период до дня 28 составляла 6.0 дня в группе, получавшей тоцилизумаб, и 7.5 дня в группе, получавшей плацебо (отношение рисков =1.16 [95% ДИ: от 0.91 до 1.48]).
Показатель смертности на день 28 составлял 10.4% в группе, получавшей тоцилизумаб, в сравнении с 8.6% в группе, получавшей плацебо (взвешенная разница (группа тоцилизумаба — группа плацебо): 2.0% [95% ДИ: от -5.2 до 7.8%]). Показатель смертности на день 60 (ретроспективный анализ) составлял 11.2% в группе, получавшей тоцилизумаб, в сравнении с 10.9% в группе, получавшей плацебо (взвешенная разница (группа тоцилизумаба — группа плацебо): 0.5% [95% ДИ: от -6.9 до 6.8%]).
Исследование WA42380 (COVACTA)
Исследование WA42380 представляло собой глобальное рандомизированное, двойное слепое, плацебо-контролируемое, многоцентровое исследование III фазы по оценке эффективности и безопасности применения тоцилизумаба для внутривенного введения в комбинации со стандартной терапией у взрослых пациентов, госпитализированных с тяжелой пневмонией, ассоциированной с COVID-19. Для включения в исследование подходили пациенты в возрасте, по меньшей мере, 18 лет, имевшие инфекцию SARS-CoV-2, подтвержденную положительным результатом теста методом ОТ-ПЦР, имевшие пневмонию, подтвержденную результатами рентгенологического исследования, и показатель SpO2≤93% при дыхании атмосферным воздухом, либо отношение парциального давления кислорода в артериальной крови к фракции кислорода во вдыхаемом воздухе 300 мм рт. ст. или менее. Стандартная терапия могла включать в себя противовирусную терапию, применение ГКС в низких дозах, применение реконвалесцентной плазмы и другую поддерживающую терапию. Пациенты были рандомизированы в соотношении 2:1 в группы, получавшие одну инфузию тоцилизумаба в дозе 8 мг/кг, при максимальной дозе 800 мг, либо плацебо. Если клинические признаки или симптомы ухудшались или не улучшались, могла быть введена одна дополнительная инфузия тоцилизумаба или плацебо по слепой схеме, через 8-24 часа после проведения первой инфузии.
Из 452 пациентов, которые были рандомизированы, анализы эффективности были проведены в популяции mITT, которая включала в себя пациентов, получивших любое количество исследуемого лекарственного препарата (294 пациента в группе тоцилизумаба; 144 пациента в группе плацебо). Исходные демографические характеристики и характеристики заболевания были в целом сбалансированы между группами терапии. Для популяции mITT в целом (п=438) на момент рандомизации медиана возраста составляла 62 года (диапазон: 22-96, при этом 44.3% пациентов были в возрасте 65 лет или старше); 69.9% пациентов были мужского пола, 32.2% пациентов были испанского или латиноамериканского этнического происхождения, 57.5% пациентов принадлежали к европеоидной расе, 15.1% пациентов были представителями негроидной расы/афроамериканцами и 8.7% пациентов были представителями монголоидной расы. На исходном уровне 3.4% пациентов не получали дополнительный кислород, 27.9% пациентов получали низкопоточную кислородную терапию, 30.4% пациентов находились на неинвазивной ИВЛ или получали высокопоточную кислородную терапию и 38.4% пациентов находились на инвазивной ИВЛ. Медиана времени с момента возникновения симптомов составляла 11.0 дней. На исходном уровне в обеих группах терапии в совокупности 22.4% пациентов получали системные глюкокортикостероиды и 5.7% пациентов получали ремдесивир. Значения медианы (диапазон) уровня ИЛ-6, CРБ и ферритина составляли, соответственно, 85.8 нг/л (3.1-4020), 155.15 мг/л (1.1-499.6) и 2.20 пмоль/мл (0.0-75.3). Наиболее частыми сопутствующими заболеваниями были артериальная гипертензия (62.1%), сахарный диабет (38.1%), нарушения со стороны сердечно-сосудистой системы (28.1%) и ожирение (20.5%).
Первичной конечной точкой для оценки эффективности был клинический статус в день 28, оцениваемый с использованием порядковой шкалы со следующими 7 категориями:
- выписан из стационара (либо «готов к выписке», что определяется как достижение нормальной температуры тела и частоты дыхания, а также стабильного уровня сатурации крови кислородом при дыхании атмосферным воздухом или при использовании ≤2 л дополнительного кислорода);
- в общей палате (или «готов к переводу в общую палату»), без потребности в дополнительном кислороде;
- в общей палате (или «готов к переводу в общую палату»), требуется дополнительный кислород;
- в ОИТ или в общей палате, требуется неинвазивная вентиляция легких или высокопоточная кислородная терапия;
- в отделении интенсивной терапии, требуется интубация или ИВЛ;
- в ОИТ, требуется экстракорпоральная мембранная оксигенация или ИВЛ и дополнительная поддержка органов (например, применение вазопрессорных препаратов, заместительная почечная терапия);
- смерть.
При сравнении группы, получавшей тоцилизумаб, с группой, получавшей плацебо, не было выявлено статистически значимого различия в распределении оценок клинического статуса по порядковой шкале с 7 категориями в день 28. Медиана категории клинического статуса в день 28 была категория 1.0 в группе, получавшей тоцилизумаб, и 2.0 в группе, получавшей плацебо (отношение шансов (ОШ) 1.19 [95% ДИ: 0.81, 1.76]).
Медиана времени до выписки из стационара либо «готовности к выписке» за период до дня 28 составляла 20 дней в группе, получавшей тоцилизумаб, и 28 дней в группе, получавшей плацебо (отношение рисков = 1.35 [95% ДИ: от 1.02 до 1.79]).
Показатель смертности на день 28 составлял 19.7% в группе, получавшей тоцилизумаб, в сравнении с 19.4% в группе, получавшей плацебо (взвешенная разница (группа тоцилизумаба — группа плацебо): 0.3% [95% ДИ: от -7.6 до 8.2]. Показатель смертности на день 60 составлял 24.5% в группе, получавшей тоцилизумаб, в сравнении с 25.0% в группе, получавшей плацебо (взвешенная разница (группа тоцилизумаба — группа плацебо): -0.5% [95% ДИ: от -9.1 до 8.0]).
Исследование WA42511 (REMDACTA)
Исследование WA42511 представляло собой глобальное рандомизированное, двойное слепое, плацебо-контролируемое, многоцентровое исследование III фазы, проведенное с целью оценки эффективности и безопасности применения тоцилизумаба для внутривенного введения в комбинации с ремдесивиром в сравнении с соответствующим плацебо в комбинации с ремдесивиром, у госпитализированных взрослых пациентов с тяжелой пневмонией, ассоциированной с COVID-19. Для включения в исследование подходили пациенты в возрасте, по меньшей мере, 12 лет с подтвержденной инфекцией SARS-CoV-2, включая положительный результат теста методом полимеразной цепной реакции (ПЦР), и пневмонией, подтвержденной результатами рентгенологического исследования, которым требовался дополнительный кислород в количестве >6 л/мин для поддержания уровня SpO2>93%. Пациенты были рандомизированы в соотношении 2:1 в группы, получавшие по слепой схеме либо тоцилизумаб + ремдесивир, либо соответствующее плацебо + ремдесивир. Исследуемую терапию применяли в комбинации со стандартной терапией в соответствии с локальными руководствами (например, ГКС, поддерживающая терапия). Пациенты, распределенные в группу лечения комбинацией тоцилизумаб + ремдесивир, получили одну инфузию тоцилизумаба в дозе 8 мг/кг, при максимальной дозе 800 мг, а пациенты, распределенные в группу лечения комбинацией плацебо + ремдесивир, получили одну инфузию плацебо. В обеих группах в случаях, если клинические признаки или симптомы ухудшались или не улучшались, могла быть введена одна дополнительная инфузия тоцилизумаба или плацебо по слепой схеме, через 8-24 часа после проведения первой инфузии.
Из 649 пациентов, которые были рандомизированы, анализы эффективности были проведены в популяции mITT, которая включала в себя пациентов, получивших любое количество тоцилизумаба/плацебо (430 пациентов в группе лечения комбинацией тоцилизумаб + ремдесивир; 210 пациентов в группе лечения комбинацией плацебо + ремдесивир). Исходные демографические характеристики и характеристики заболевания были в целом сбалансированными между группами терапии. Для популяции mITT в целом (п=640) на момент рандомизации медиана возраста составляла 60 лет (диапазон: от 20 до 93 лет, при этом 38.3% пациентов были в возрасте 65 лет или старше); 63.3% пациентов были мужского пола, 51.6% пациентов были испанского или латиноамериканского этнического происхождения, 67% пациентов принадлежали к европеоидной расе, 10.9% пациентов были представителями негроидной расы/афроамериканцами и 3.4% пациентов были представителями монголоидной расы. На исходном уровне 6.6% пациентов получали низкопоточную кислородную терапию, 79.8% пациентов находились на неинвазивной ИВЛ или получали высокопоточную кислородную терапию и 13.6% пациентов находились на инвазивной ИВЛ. Медиана времени с момента возникновения симптомов составляла 8 дней. На исходном уровне большинство пациентов получали ГКС (84.2% во всех группах терапии в совокупности). Значения медианы (диапазон) уровня CРБ и ферритина составляли 98.20 мг/л (1.3-418.3) и 2.13 пмоль/мл (0.1-30.8) соответственно. Наиболее частыми сопутствующими заболеваниями были артериальная гипертензия (61.7%), сахарный диабет (39.5%) и ожирение (27%).
Первичной конечной точкой для оценки эффективности было время с момента рандомизации до выписки из стационара либо «готовности к выписке» за период до дня 28. Не было выявлено статистически значимой разницы между группами терапии в отношении времени до выписки из стационара либо «готовности к выписке» за период до дня 28 (отношение рисков: 0.965 [95% ДИ: от 0.78 до 1.19]) или времени до начала использования ИВЛ или смерти за период до дня 28 (отношение рисков: 0.980 [95% ДИ: от 0.72 до 1.34]). Показатель смертности на день 28 составлял 18.1% в группе, получавшей тоцилизумаб, в сравнении с 19.5% в группе, получавшей плацебо (взвешенная разница (группа тоцилизумаба — группа плацебо): -1.3% [95% ДИ: от -7.8 до 5.2%]). Показатель смертности на день 60 составлял 22.6% в группе, получавшей тоцилизумаб, в сравнении с 25.7% в группе, получавшей плацебо (взвешенная разница (группа тоцилизумаба — группа плацебо): -3.0% [95% ДИ: от -10.1 до 4%]).
Метаанализ по результатам исследований RECOVERY, EMPACTA (исследование ML42528), COVACTA (исследование WA42380) и REMDACTA (исследование WA42511) для пациентов, получавших терапию системными ГКС на исходном уровне
Метаанализ на уровне исследований был проведен по результатам 3 исследований компании Рош и исследования RECOVERY. Для каждого исследования была введена оценка отношения рисков для времени до момента смерти за период до дня 28 в подгруппе пациентов, получавших системные кортикостероиды на исходном уровне (тоцилизумаб 597 пациентов, и плацебо: 313 пациентов из исследований компании Рош; тоцилизумаб: 1664 пациента, и стандартная терапия: 1721 пациент из исследования RECOVERY).
Комбинированный показатель отношения рисков указывал на то, что терапия тоцилизумабом (п=2261) приводила к относительному уменьшению на 19% риска смерти за период до дня 28 (отношение рисков = 0.81; 95% ДИ: 0.72, 0.90; р=0.0002) в сравнении со стандартной терапией (п=2034).
Рисунок 1. Метаанализ времени до момента смерти за период до дня 28 в субпопуляции пациентов, получавших кортикостероиды на исходном уровне.
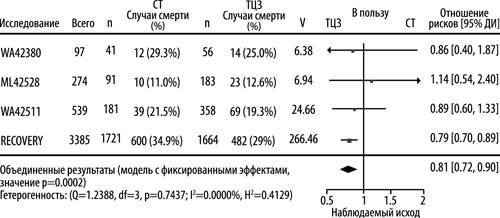
Отношение рисков Кокса для исследований компании Рош. Логранговый показатель O-E для исследования RECOVERY, в котором значение ОР было вычислено путем принятия In(ОР) равным (O-E)/V при нормальной дисперсии I/V.
Модель с фиксированными эффектами, в которую In(ОР) был включен в качестве ответа и V — в качестве весов для оценки объединенного эффекта.
СТ — стандартная терапия, ТЦЗ — тоцилизумаб
Источник данных компании Рош:
root/clinical_studies/R04877533/share/pool_COVID19/prod/outdata_vad
Доклинические данные безопасности
Канцерогенность: исследования по изучению канцерогенности тоцилизумаба не проводились. Имеющиеся доклинические данные демонстрируют вклад плейотропного ИЛ-6 в прогрессирование злокачественных новообразований и устойчивость к апоптозу при различных формах рака. Эти данные не предполагают, что лечение тоцилизумабом приводит к существенному риску развития и прогрессирования рака.
Мутагенность: стандартные генотоксические тесты как в прокариотических, так и в эукариотических клетках были отрицательными.
Влияние на фертильность: имеющиеся доклинические данные не предполагают влияния аналогов тоцилизумаба на фертильность. В исследованиях по изучению хронической токсичности у яванских макак и у самок или самцов мышей с недостаточностью ИЛ-6 отрицательного влияния тоцилизумаба на эндокринные или репродуктивные органы не обнаружено.
Тератогенность: не обнаружено прямого или опосредованного неблагоприятного влияния на беременность или внутриутробное развитие при в/в введении тоцилизумаба яванским макакам на ранних сроках гестационного периода.
Прочее: отмечалось незначительное увеличение случаев спонтанного выкидыша/внутриутробной гибели плода при высоком уровне системного кумулятивного воздействия (более чем в 100 раз превышающего таковое у человека) при введении дозы 50 мг/кг/сут в сравнении с плацебо или меньшим уровнем вводимых доз. Частота выкидыша была в пределах исторического контроля для яванских макак, содержащихся в неволе; отдельные случаи выкидыша/внутриутробной гибели не демонстрировали какой-либо взаимосвязи между данными явлениями и дозой или продолжительностью введения тоцилизумаба. Несмотря на то, что ИЛ-6, по-видимому, не играет решающей роли в развитии плода или иммунологической регуляции системы мать-плод, взаимосвязь этих явлений с введением тоцилизумаба не может быть исключена.
Наблюдалась экскреция мышиного аналога тоцилизумаба в молоко лактирующих мышей. Применение мышиного аналога тоцилизумаба не оказывало токсичного действия на ювенильных мышей. В частности, не наблюдалось нарушения роста скелета, иммунной функции и полового развития.
Фармакокинетика
Фармакокинетика тоцилизумаба характеризуется нелинейным выведением, представляющим комбинацию линейного клиренса и выведения по Михаэлис-Ментен. Нелинейная часть выведения тоцилизумаба приводит к более чем дозозависимому увеличению экспозиции. Фармакокинетические параметры тоцилизумаба не меняются с течением времени. Т.к. общий клиренс зависит от концентрации тоцилизумаба в сыворотке, Т1/2 тоцилизумаба также является зависимым от его концентрации и может быть рассчитан только при наличии значения сывороточной концентрации. Популяционный фармакокинетический анализ, проведенный во всех популяциях пациентов, не выявил связи между кажущимся клиренсом и наличием антител к тоцилизумабу.
Ревматоидный артрит
Фармакокинетика тоцилизумаба сопоставима у здоровых добровольцев и пациентов с РА.
Таблица 1. Прогнозируемые средние фармакокинетические параметры (± стандартное отклонение, СО) тоцилизумаба при равновесном состоянии у пациентов с РА
* t на протяжении 4 недель.
При высоких значениях концентрации тоцилизумаба в сыворотке линейный клиренс преобладает над общим клиренсом тоцилизумаба, и конечный Т1/2 составляет приблизительно 21.5 дней (на основе приблизительных параметров популяции пациентов). В то время как после в/в введения Cmax дозозависимо увеличивается между дозами 4 мг/кг и 8 мг/кг каждые 4 недели, более чем дозозависимое увеличение наблюдалось для Cmean и Ctrough. В равновесном состоянии значения Cmean и Ctrough были в 3.2 и 32 раза выше при применении тоцилизумаба в дозе 8 мг/кг по сравнению с дозой 4 мг/кг, соответственно.
Коэффициенты накопления AUC и Cmax после многократного применения тоцилизумаба в дозах 4 мг/кг и 8 мг/кг каждые 4 недели были ниже, чем коэффициенты накопления Ctrough (2.62 и 2.47), благодаря участию нелинейного клиренса при более низких концентрациях тоцилизумаба.
Более 90% равновесного состояния при Cmax достигается после первой в/в инфузии; 90% равновесное состояние при AUCt и Cmean достигается после первой и третьей в/в инфузии тоцилизумаба в дозе 4 мг/кг и 8 мг/кг, соответственно; приблизительно 90% равновесное состояние при Ctrough достигается после четвертой в/в инфузии тоцилизумаба.
Масса тела является значимым фактором, влияющим на фармакокинетику тоцилизумаба. При в/в инфузии, рассчитанной в мг на кг массы тела, у пациента с массой тела ≥100 кг ожидается более высокая средняя экспозиция в равновесном состоянии по сравнению со средним значением в популяции пациентов. Таким образом, не рекомендуется увеличение дозы препарата выше 800 мг на одну инфузию у пациентов с массой тела ≥100 кг (см. раздел «Режим дозирования»).
Полиартикулярный ювенильный идиопатический артрит (пЮИА)
После в/в применения приблизительно 90% равновесное состояние достигается к 12 неделе при введении в дозе 10 мг/кг (масса тела <30 кг) и к 16 неделе при введении в дозе 8 мг/кг (масса тела ≥30 кг).
Таблица 2. Прогнозируемые средние фармакокинетические параметры (± стандартное отклонение, СО) тоцилизумаба при равновесном состоянии у пациентов с пЮИА
* t на протяжении 4 недель.
Системный ювенильный идиопатический артрит
После в/в применения приблизительно 90% равновесное состояние достигается к восьмой неделе при введении в дозе 12 мг/кг и 8 мг/кг 1 раз в 2 недели.
Таблица 3. Прогнозируемые средние фармакокинетические параметры (± стандартное отклонение, СО) тоцилизумаба при равновесном состоянии у пациентов с сЮИА
* t на протяжении 2 недель.
Фармакокинетические параметры тоцилизумаба у пациентов в возрасте до 2 лет были сопоставимы с фармакокинетическими параметрами у пациентов старше 2 лет с массой тела <30 кг при в/в применении тоцилизумаба (в дозе 12 мг/кг каждые 2 недели).
COVID-19
Фармакокинетику тоцилизумаба у взрослых пациентов с COVID-19 оценивали в исследованиях WA42380 (COVATA) и CA42481 (MARIPOSA) посредством популяционного фармакокинетического анализа, в который было включено 380 взрослых пациентов. Пациенты получали одну или две в/в инфузии тоцилизумаба в дозе 8 мг/кг, которые вводили с интервалом, как минимум, 8 ч.
Таблица 4. Расчетные средние (±СО) фармакокинетические параметры после в/в введения тоцилизумаба в дозе 8 мг/кг
В ходе популяционного фармакокинетического анализа масса тела и тяжесть заболевания были определены как значимые ковариаты, которые оказывают влияние на фармакокинетику тоцилизумаба. При режиме дозирования тоцилизумаба 8 мг/кг и максимальной дозой 800 мг в рамках отдельной категории порядковой шкалы (ПШ) по сравнению с пациентами со средней массой тела 80 кг у пациентов с массой тела менее 60 кг экспозиция была на 20% ниже. Экспозиция у пациентов с массой тела более 100 кг находилась в том же диапазоне экспозиций, что и у пациентов со средней массой тела 80 кг. Для пациента с массой тела 80 кг экспозиция снижалась с увеличением тяжести заболевания, для каждой последующей категории ПШ, экспозиция соответственно снижалась на 13%.
Распределение
После в/в введения тоцилизумаб претерпевает двухфазное выведение из системного кровотока. У пациентов с РА Vd в центральной камере составляет 3.5 л, в периферической камере – 2.9 л, а Vd в равновесном состоянии составляет 6.4 л.
У детей с пЮИА Vd в центральной камере составляет 1.98 л, в периферической камере – 2.1 л, а Vd в равновесном состоянии составляет 4.08 л.
У детей с сЮИА Vd в центральной камере составляет 1.87 л, в периферической камере – 2.14 л, а Vd в равновесном состоянии составляет 4.01 л.
У взрослых пациентов с COVID-19 Vd в центральной камере составляет 4.52 л, в периферической камере — 4.23, таким образом, Vd составляет 8.75 л
Выведение
Общий клиренс тоцилизумаба зависит от концентрации и представляет собой сумму линейного и нелинейного клиренса. Линейный клиренс составляет 12.5 мл/ч у пациентов с РА, 5.8 мл/ч у детей с пЮИА и 5.7 мл/ч у детей с сЮИА. Нелинейный клиренс, зависящий от концентрации, имеет наибольшее значение при низких концентрациях тоцилизумаба. При более высоких концентрациях тоцилизумаба преобладает линейный клиренс в связи с насыщением пути нелинейного клиренса. Т.к. общий клиренс зависит от сывороточной концентрации тоцилизумаба, Т1/2 тоцилизумаба также является зависимым от его концентрации и может быть рассчитан только при наличии значения сывороточной концентрации.
При РА зависимый от концентрации кажущийся Т1/2 для тоцилизумаба в равновесном состоянии в дозе 4 мг/кг 1 раз в 4 недели составляет до 11 дней, а для тоцилизумаба в дозе 8 мг/кг 1 раз в 4 недели – до 13 дней. При высоких значениях концентрации тоцилизумаба в сыворотке линейный клиренс преобладает над общим клиренсом тоцилизумаба, и конечный Т1/2 составляет приблизительно 21.5 дней (на основе приблизительных параметров популяции пациентов).
У детей с пЮИА эффективный Т1/2 тоцилизумаба в равновесном состоянии (между введениями в дозе 8 мг/кг для детей с массой тела ≥30 кг или в дозе 10 мг/кг для детей с массой тела <30 кг в равновесном состоянии) составляет до 17 дней.
У детей с сЮИА эффективный Т1/2 тоцилизумаба в равновесном состоянии (между введениями в дозе 8 мг/кг и 12 мг/кг) составляет до 16 дней.
У взрослых пациентов с COVID-19 сывороточные концентрации были ниже предела количественного определения по прошествии 35 дней (в среднем) после введения одной инфузии тоцилизумаба в дозе 8 мг/кг. Средний линейный клиренс в популяционном фармакокинетическом анализе составил 17.6 мл/ч у пациентов с категорией 3 ПШ (ПШ 3 — пациенты, которым требуется поддерживающая терапия кислородом) на исходном уровне, 22.5 мл/ч у пациентов с категорией 4 ПШ (пациенты, которым требуется высокопоточная кислородная терапия или неинвазивная вентиляция легких) на исходном уровне, 29 мл/ч у пациентов с категорией 5 ПШ (пациенты, которым требуется ИВЛ) на исходном уровне, 35 мл/ч у пациентов с категорией 6ПШ (пациенты, которым требуется экстракорпоральная мембранная оксигенация (ЭКМО) или ИВЛ и дополнительная поддержка органов) на исходном уровне.
Фармакокинетика у особых групп пациентов
Пациенты с печеночной недостаточностью. Фармакокинетика тоцилизумаба у пациентов с печеночной недостаточностью не изучалась.
Пациенты с почечной недостаточностью. Специальных исследований у пациентов с почечной недостаточностью не проводилось. У большинства пациентов с РА, учтенных в популяционном фармакокинетическом анализе, была нормальная функция почек или нарушение функции почек легкой степени тяжести (расчетный КК по формуле Кокрофта-Голта), которое не влияло на фармакокинетику тоцилизумаба. Коррекции дозы тоцилизумаба пациентам с нарушением функции почек легкой степени тяжести не требуется.
Пол, раса, пожилой возраст. Популяционный фармакокинетический анализ у взрослых пациентов с РА показал, что возраст, пол и раса не влияют на фармакокинетику тоцилизумаба. Коррекции дозы тоцилизумаба не требуется.
Показания препарата
Актемра®
- ревматоидный артрит со средней или высокой степенью активности у взрослых как в виде монотерапии, так и в комбинации с метотрексатом и/или с другими базисными противовоспалительными препаратами, в т.ч. для торможения рентгенологически доказанной деструкции суставов;
- активный полиартикулярный ювенильный идиопатический артрит у пациентов в возрасте 2 лет и старше как в виде монотерапии, так и в комбинации с метотрексатом;
- активный системный ювенильный идиопатический артрит у пациентов в возрасте 2 лет и старше как в виде монотерапии, так и в комбинации с метотрексатом;
- лечение новой коронавирусной инфекции (COVID-19) у госпитализированных взрослых пациентов, получающих системные глюкокортикоиды, которым требуется поддерживающая терапия кислородом или ИВЛ.
Режим дозирования
Лечение должны назначать медицинские специалисты, имеющие опыт в постановке диагноза и терапии РА, COVID-19, сЮИА и пЮИА.
Препарат предназначен для введения как в амбулаторно-поликлинических, так и в стационарных условиях.
Стандартный режим дозирования
Ревматоидный артрит
Рекомендуемая доза составляет 8 мг/кг массы тела 1 раз в 4 недели.
Не рекомендуется увеличение дозы свыше 800 мг на одну инфузию пациентам с массой тела выше 100 кг (см. раздел «Фармакокинетика»).
Рекомендации по коррекции дозы при изменении лабораторных показателей (см. раздел «Особые указания»)
Повышение активности печеночных ферментов
Низкое АЧН
У пациентов, ранее не получавших лечение препаратом Актемра®, не рекомендуется начинать применение препарата при показателе АЧН ниже 2×109/л.
Низкое число тромбоцитов
COVID-19
Рекомендуемая доза для лечения COVID-19 составляет 8 мг/кг в виде однократной в/в инфузии в течение 60 мин у пациентов, получающих системные ГКС и которым требуется поддерживающая терапия кислородом или ИВЛ (см. раздел «Фармакологическое действие»).
Если клинические признаки или симптомы ухудшаются или не улучшаются после введения одной инфузии, можно ввести дополнительную инфузию препарата Актемра® в дозе 8 мг/кг через, как минимум, 8 ч после первой инфузии.
Не рекомендуется увеличение дозы свыше 800 мг на одну инфузию пациентам с массой тела более 100 кг (см. раздел «Фармакокинетика»).
Применение препарата Актемра® не рекомендуется пациентам с COVID-19, у которых наблюдается любое из следующих отклонений в лабораторных показателях.
Особые группы пациентов
Дети
сЮИА
Рекомендуемая доза у пациентов старше 2 лет составляет 8 мг/кг 1 раз в 2 недели у пациентов с массой тела ≥30 кг или 12 мг/кг 1 раз в 2 недели у пациентов с массой тела <30 кг. Дозу следует рассчитывать исходя из массы тела пациента при каждом введении препарата. Изменение дозы должно быть основано только на соответствующем изменении массы тела пациента с течением времени.
Безопасность и эффективность в/в введения препарата Актемра® у детей в возрасте до 2 лет не установлены.
У пациентов с сЮИА рекомендуется прерывание терапии тоцилизумабом при изменениях в лабораторных показателях, приведенных в таблицах ниже. При необходимости следует изменить дозу одновременно назначаемого МТ и/или других сопутствующих препаратов или прекратить их прием, а также прервать введение тоцилизумаба до оценки клинической ситуации. Решение о прекращении терапии тоцилизумабом при возникновении изменений лабораторных показателей должно основываться на медицинской оценке состояния конкретного пациента, поскольку существует множество сопутствующих заболеваний, которые могут оказывать влияние на лабораторные показатели при сЮИА.
Повышение активности печеночных ферментов
Низкое АЧН
Низкое число тромбоцитов
Клинических данных недостаточно, чтобы оценить влияние снижения дозы тоцилизумаба у пациентов с сЮИА, у которых наблюдались изменения в лабораторных показателях. Имеющиеся данные свидетельствуют о том, что клиническое улучшение наблюдается в течение 6 недель после начала лечения препаратом Актемра®. В случае, если у пациента не наблюдается улучшения в течение данного периода времени, целесообразность продолжения терапии должна быть тщательно пересмотрена.
пЮИА
Рекомендуемая доза у пациентов старше 2 лет составляет 8 мг/кг 1 раз в 4 недели у пациентов с массой тела ≥30 кг или 10 мг/кг 1 раз в 4 недели у пациентов с массой тела <30 кг. Дозу следует рассчитывать исходя из массы тела пациента при каждом введении препарата. Изменение дозы должно быть основано только на соответствующем изменении массы тела пациента с течением времени.
Безопасность и эффективность в/в введения препарата Актемра® у детей в возрасте до 2 лет не установлены.
У пациентов с пЮИА рекомендуется прерывание терапии тоцилизумабом при изменениях лабораторных показателей, приведенных в таблицах ниже. При необходимости следует изменить дозу одновременно назначаемого МТ и/или других сопутствующих препаратов или прекратить их прием, а также прервать введение тоцилизумаба до оценки клинической ситуации. Поскольку существует множество сопутствующих заболеваний, которые могут оказывать влияние на лабораторные показатели при пЮИА, решение о прекращении терапии тоцилизумабом в случае возникновения изменений лабораторных показателей должно основываться на медицинской оценке состояния конкретного пациента.
Повышение активности печеночных ферментов
Низкое АЧН
Низкое число тромбоцитов
Возможность снижения дозы тоцилизумаба в связи с возникновением изменений в лабораторных показателях у пациентов с пЮИА не изучалась.
Имеющиеся данные свидетельствуют о том, что клиническое улучшение наблюдается в течение 12 недель после начала лечения препаратом Актемра®. Целесообразность продолжения терапии должна быть тщательно пересмотрена, если у пациента не наблюдается улучшения в течение данного периода времени.
Пациенты пожилого возраста
Коррекции дозы у пациентов пожилого возраста (≥ 65 лет) не требуется.
Пациенты с нарушением функции почек
Коррекции дозы у пациентов с нарушением функции почек легкой степени тяжести не требуется (см. раздел «Фармакокинетика»). Применение тоцилизумаба у пациентов с умеренным и тяжелым нарушением функции почек не изучалось (см. раздел «Фармакокинетика»).
Пациенты с нарушением функции печени
Безопасность и эффективность тоцилизумаба у пациентов с нарушением функции печени не изучались.
Способ применения
После разведения препарат Актемра® пациентам с РА, сЮИА, пЮИА и COVID-19 следует вводить в виде в/в инфузии в течение 1 ч.
Пациенты с РА, сЮИА, пЮИА и COVID-19 с массой тела ≥30 кг
Препарат Актемра® следует развести до объема 100 мл стерильным апирогенным раствором натрия хлорида 9 мг/мл (0.9%) с соблюдением правил асептики.
Инструкции по разведению лекарственного препарата перед введением представлены ниже.
Пациенты с сЮИА и пЮИА с массой тела <30 кг
Препарат Актемра® следует развести до объема 50 мл стерильным апирогенным раствором натрия хлорида 9 мг/мл (0.9%) с соблюдением правил асептики.
Инструкции по разведению лекарственного препарата перед введением представлены ниже.
При появлении у пациента признаков и симптомов инфузионной реакции следует уменьшить скорость инфузии или прекратить введение препарата и немедленно назначить соответствующие препараты/поддерживающую терапию (см. раздел «Особые указания»).
Приготовление раствора лекарственного препарата
Препарат Актемра® должен вводиться медицинским персоналом. Препарат предназначен для введения как в амбулаторно-поликлинических, так и в стационарных условиях.
Препарат Актемра® в лекарственной форме для внутривенного введения не предназначен для подкожного введения!
Подготовка препарата к введению должна проводиться в асептических условиях.
Перед введением необходимо осмотреть приготовленный раствор на предмет отсутствия посторонних частиц или изменения окраски.
Следует вводить только прозрачный или опалесцирующий бесцветный или светло-желтый раствор без видимых посторонних частиц
Следует использовать стерильную иглу и шприц для приготовления раствора для инфузий препарата Актемра®.
Пациенты с РА и COVID-19
- Рассчитать количество препарата, необходимое для введения пациенту (из расчета 0.4 мл на 1 кг массы тела (0.4 мл/кг)).
- В асептических условиях из инфузионного флакона (пакета), содержащего 100 мл 0.9% раствора натрия хлорида (раствор должен быть стерильным и апирогенным), отобрать одноразовым стерильным шприцем количество 0.9% раствора натрия хлорида, равное рассчитанному для введения количеству препарата Актемра®.
- Другим одноразовым стерильным шприцем в асептических условиях из флакона с препаратом Актемра® отобрать рассчитанное количество препарата и ввести его в инфузионный флакон (пакет) с 0.9% раствором натрия хлорида; в результате объем приготовленного раствора должен быть равным 100 мл.
- Для перемешивания аккуратно перевернуть флакон (пакет) во избежание пенообразования.
Пациенты с пЮИА и сЮИА с массой тела ≥30 кг
- Рассчитать количество препарата, необходимое для введения пациенту (из расчета 0.4 мл на 1 кг массы тела (0.4 мл/кг)).
- В асептических условиях из инфузионного флакона (пакета), содержащего 100 мл 0.9% раствора натрия хлорида (раствор должен быть стерильным и апирогенным), отобрать одноразовым стерильным шприцем количество 0.9% раствора натрия хлорида, равное рассчитанному для введения количеству препарата Актемра®.
- Другим одноразовым стерильным шприцем в асептических условиях из флакона с препаратом Актемра® отобрать рассчитанное количество препарата и ввести его в инфузионный флакон (пакет) с 0.9% раствором натрия хлорида; в результате объем приготовленного раствора должен быть равным 100 мл.
- Для перемешивания аккуратно перевернуть флакон (пакет) во избежание пенообразования.
Пациенты с пЮИА с массой тела <30 кг
- Рассчитать количество препарата, необходимое для введения пациенту (из расчета 0.5 мл на 1 кг массы тела (0.5 мл/кг)).
- В асептических условиях из инфузионного флакона (пакета), содержащего 50 мл 0.9% раствора натрия хлорида (раствор должен быть стерильным и апирогенным), отобрать одноразовым стерильным шприцем количество 0.9% раствора натрия хлорида, равное количеству, рассчитанному для введения препарата Актемра®.
- Другим одноразовым стерильным шприцем в асептических условиях из флакона с препаратом Актемра® отобрать рассчитанное количество препарата и ввести его в инфузионный флакон (пакет) с 0.9% раствором натрия хлорида; в результате объем приготовленного раствора должен быть равным 50 мл.
- Для перемешивания аккуратно перевернуть флакон (пакет) во избежание пенообразования.
Пациенты с сЮИА с массой тела <30 кг
- Рассчитать количество препарата, необходимое для введения пациенту (из расчета 0.6 мл на 1 кг массы тела (0.6 мл/кг)).
- В асептических условиях из инфузионного флакона (пакета), содержащего 50 мл 0.9% раствора натрия хлорида (раствор должен быть стерильным и апирогенным), отобрать одноразовым стерильным шприцем количество 0.9% раствора натрия хлорида, равное количеству, рассчитанному для введения препарата Актемра®.
- Другим одноразовым стерильным шприцем в асептических условиях из флакона с препаратом Актемра® отобрать рассчитанное количество препарата и ввести его в инфузионный флакон (пакет) с 0.9% раствором натрия хлорида; в результате объем приготовленного раствора должен быть равным 50 мл.
- Для перемешивания аккуратно перевернуть флакон (пакет) во избежание пенообразования.
Препарат Актемра® предназначен только для однократного применения.
Правила хранения приготовленного раствора
Приготовленный инфузионный раствор препарата Актемра® физически и химически стабилен в 0.9% растворе натрия хлорида в течение 24 ч при температуре 30°С.
С микробиологической точки зрения приготовленный раствор должен быть использован немедленно.
Если препарат не используется сразу, то время и условия хранения приготовленного раствора являются ответственностью пользователя и не должны превышать 24 ч при температуре от 2°С до 8°С (хранить в холодильнике) и только в том случае, если приготовление раствора проводилось в контролируемых и валидируемых асептических условиях.
Инструкция по уничтожению неиспользованного препарата, а также по истечении срока годности
Попадание лекарственных препаратов в окружающую среду должно быть сведено к минимуму. Не следует утилизировать препарат с помощью сточных вод или вместе с бытовыми отходами. По возможности необходимо использовать специальные системы для утилизации лекарственных препаратов.
Побочное действие
Наиболее часто отмечавшимися нежелательными реакциями (наблюдались у ≥5% пациентов, получавших тоцилизумаб в виде монотерапии или в комбинации с БПВП для лечения РА, сЮИА и пЮИА) были инфекции верхних дыхательных путей, назофарингит, головная боль, артериальная гипертензия и повышение активности АЛТ.
Наиболее серьезными нежелательными реакциями были серьезные инфекции, осложнения дивертикулита и реакции гиперчувствительности.
Наиболее часто отмечавшимися нежелательными реакциями (наблюдались у ≥5% пациентов, получавших тоцилизумаб для лечения COVID-19) были повышение активности печеночных трансаминаз, запор и инфекция мочевыводящих путей.
Нежелательные реакции, выявленные в ходе клинических исследований и/или при пострегистрационном применении препарата Актемра® на основании спонтанных сообщений, случаев, описанных в литературных источниках, и случаев, наблюдаемых в рамках программ неинтервенционных исследований, представлены в таблицах 5 и 6 в соответствии с системно-органной классификацией медицинского словаря для нормативно-правовой деятельности MedDRA. Для описания частоты развития нежелательных реакций используются следующие категории: очень часто (≥1/10); часто (≥1/100, но <1/10), нечасто (≥1/1000, но <1/100), редко (≥1/10000, но <1/1 000), очень редко (<1/10000). В каждой группе (по частоте возникновения) нежелательные реакции представлены в порядке убывания степени их серьезности.
РА
Профиль безопасности тоцилизумаба был изучен в 4 плацебо-контролируемых исследованиях (исследования II, III, IV и V), 1 контролируемом исследовании с применением МТ (исследование I) и в ходе расширенных периодов к данным исследованиям (см. раздел «Фармакологическое действие»).
Двойной слепой контролируемый период исследования составил 6 месяцев в четырех исследованиях (исследования I, III, IV и V) и до 2 лет в одном исследовании (исследование II). В двойных слепых контролируемых исследованиях 774 пациента получали тоцилизумаб в дозе 4 мг/кг в комбинации с МТ, 1870 пациентов получали тоцилизумаб в дозе 8 мг/кг в комбинации с МТ или другими БПВП и 288 пациентов получали тоцилизумаб в дозе 8 мг/кг в качестве монотерапии.
Популяция пациентов с длительной экспозицией препарата включает всех пациентов, которые получили по меньшей мере одну дозу тоцилизумаба во время двойного слепого контролируемого периода или во время открытого расширенного периода. Из 4009 пациентов в данной популяции 3577 пациентов получали терапию в течение по меньшей мере 6 месяцев, 3296 пациентов — в течение по меньшей мере одного года, 2806 пациентов получали терапию в течение по меньшей мере 2 лет и 1222 пациента — в течение 3 лет.
Таблица 5. Перечень нежелательных реакций, наблюдавшихся у пациентов с РА, получавших тоцилизумаб в качестве монотерапии или в комбинации с МТ или другими БПВП в период проведения двойного слепого контролируемого исследования или при пострегистрационном применении
*Включены повышения уровней, собранные в рамках рутинного мониторинга лабораторных показателей (см. текст ниже).
1 См. раздел «Противопоказания».
2 См. раздел «Особые указания».
3 Данная нежелательная реакция была выявлена при пострегистрационном применении, но не наблюдалась в контролируемых клинических исследованиях. Категория частоты была рассчитана исходя из верхней границы 95% доверительного интервала, вычисленного на основании общего количества пациентов, получавших тоцилизумаб в клинических исследованиях.
Инфекции
В 6-месячных контролируемых исследованиях частота возникновения всех инфекций среди пациентов, получавших тоцилизумаб в дозе 8 мг/кг + БПВП, составила 127 явлений на 100 пациенто-лет по сравнению с 112 явлениями на 100 пациенто-лет в группе пациентов, получавших плацебо + БПВП. В популяции пациентов с длительной экспозицией препарата общая частота возникновения инфекций на фоне терапии препаратом Актемра® составила 108 явлений на 100 пациенто-лет экспозиции.
В 6-месячных контролируемых клинических исследованиях частота возникновения серьезных инфекций среди пациентов, получавших тоцилизумаб в дозе 8 мг/кг + БПВП, составила 5.3 явления на 100 пациенто-лет экспозиции по сравнению с 3.9 явления на 100 пациенто-лет экспозиции в группе пациентов, получавших плацебо + БПВП. В исследовании монотерапии частота возникновения серьезных инфекций составила 3.6 явления на 100 пациенто-лет экспозиции в группе пациентов, получавших тоцилизумаб, и 1.5 явления на 100 пациенто-лет экспозиции в группе пациентов, получавших МТ.
В популяции пациентов с длительной экспозицией препарата общая частота возникновения серьезных инфекций (бактериальных, вирусных и грибковых) составила 4.7 явления на 100 пациенто-лет экспозиции. Серьезные инфекции, некоторые из которых были с летальным исходом, включали активный туберкулез в легочной или внелегочной форме, инвазивные легочные инфекции, включая кандидоз, аспергиллез, кокцидиоидомикоз и пневмоцистную пневмонию, пневмонию, воспаление подкожной клетчатки, опоясывающий лишай (Herpes zoster), гастроэнтерит, дивертикулит, сепсис и бактериальный артрит. Сообщалось о случаях возникновения оппортунистических инфекций.
Интерстициальное заболевание легких
Нарушение функции легких может повысить риск развития инфекций. При пострегистрационном применении препарата были получены сообщения о развитии интерстициального заболевания легких (включая пневмонит и фиброз легких); некоторые из этих случаев привели к летальному исходу.
Перфорация ЖКТ
На протяжении 6-месячных контролируемых клинических исследований общая частота возникновения явлений, связанных с перфорацией ЖКТ, составила 0.26 явления на 100 пациенто-лет у пациентов, получавших терапию тоцилизумабом. В популяции пациентов с длительной экспозицией препарата общая частота возникновения явлений, связанных с перфорацией ЖКТ, составила 0.28 явления на 100 пациенто-лет. Случаи перфорации ЖКТ у пациентов, получавших тоцилизумаб, в основном, как отмечалось, были представлены в виде осложнений дивертикулита, включая генерализованный гнойный перитонит, перфорацию нижних отделов ЖКТ, свищ и абсцесс.
Инфузионные реакции
В 6-месячных контролируемых исследованиях нежелательные явления, связанные с инфузиями (отдельные явления, возникшие во время инфузии или в течение 24 ч после инфузии), отмечались у 6.9% пациентов в группе, получавшей тоцилизумаб в дозе 8 мг/кг + БПВП, и у 5.1% пациентов в группе, получавшей плацебо + БПВП. Явления, возникшие во время инфузии, преимущественно представляли собой эпизоды повышения АД; явления, возникшие в течение 24 ч после завершения инфузии, представляли собой головную боль и реакции со стороны кожи (сыпь, крапивница). Эти реакции не приводили к ограничению терапии.
Частота возникновения анафилактических реакций (которые наблюдались в общей сложности у 8 из 4009 пациентов, 0.2%) была в несколько раз выше в группе, получавшей препарат в дозе 4 мг/кг, в сравнении с группой, получавшей препарат в дозе 8 мг/кг. Клинически значимые реакции гиперчувствительности, связанные с введением тоцилизумаба и потребовавшие прекращения терапии, отмечались в общей сложности у 56 из 4009 пациентов (1.4%), получавших тоцилизумаб в ходе контролируемых и открытых клинических исследований. Данные реакции наблюдались, как правило, в период между второй и пятой инфузией тоцилизумаба (см. раздел «Особые указания»). При пострегистрационном применении тоцилизумаба отмечались случаи анафилаксии с летальным исходом (см. раздел «Особые указания»).
Иммуногенность
В общей сложности у 2876 пациентов были проведены анализы на антитела к тоцилизумабу в рамках 6-месячных контролируемых клинических исследований. Из 46 пациентов (1.6%) с антителами к тоцилизумабу в 6 случаях отмечалась значимая лекарственная реакция гиперчувствительности, приведшая в 5 случаях к прекращению лечения. У 30 пациентов (1.1%) выработались нейтрализующие антитела.
Отклонения показателей общего анализа крови
Нейтрофилы. В 6-месячных контролируемых исследованиях явления снижения числа нейтрофилов до уровня ниже 1×109/л отмечались у 3.4% пациентов, получавших тоцилизумаб в дозе 8 мг/кг + БПВП, в сравнении с <0.1% пациентов, получавших плацебо + БПВП. Примерно у половины пациентов снижение АЧН ниже 1×109/л возникло в пределах 8 недель после начала терапии. О снижении числа нейтрофилов ниже 0.5×109/л сообщалось у 0.3% пациентов, получавших тоцилизумаб в дозе 8 мг/кг + БПВП. Сообщалось о случаях инфекций, сопровождавшихся нейтропенией.
Во время двойного слепого контролируемого периода и при длительной экспозиции характер и частота возникновения явлений, связанных с уменьшением показателя нейтрофилов, оставались такими же, как и в 6-месячных контролируемых клинических исследованиях.
Тромбоциты. В 6-месячных контролируемых исследованиях явления снижения числа тромбоцитов до уровня ниже 100 ×103/мкл отмечались у 1.7% пациентов, получавших тоцилизумаб в дозе 8 мг/кг + БПВП, в сравнении с <1% пациентов, получавших плацебо + БПВП. Эти явления снижения уровня тромбоцитов не сопровождались развитием эпизодов кровотечений.
Во время двойного слепого контролируемого периода и при длительной экспозиции характер и частота возникновения явлений, связанных с уменьшением числа тромбоцитов, оставались такими же, как и в 6-месячных контролируемых клинических исследованиях. При пострегистрационном применении в очень редких случаях сообщалось об эпизодах панцитопении.
Повышение активности печеночных трансаминаз
В ходе 6-месячных контролируемых исследований наблюдалось транзиторное повышение показателей АЛТ/АСТ выше 3×ВГН у 2.1% пациентов, получавших тоцилизумаб в дозе 8 мг/кг, в сравнении с 4.9% пациентов, получавших МТ, и у 6.5% пациентов, получавших тоцилизумаб в дозе 8 мг/кг + БПВП, в сравнении с 1.5% пациентов, получавших плацебо + БПВП. Присоединение к монотерапии тоцилизумабом препаратов, обладающих потенциальным гепатотоксическим действием (например, МТ), приводило к увеличению частоты случаев повышения активности трансаминаз. Повышение показателей АЛТ/АСТ более чем в 5 раз относительно ВГН наблюдалось у 0.7% пациентов, получавших монотерапию тоцилизумабом, и у 1.4% пациентов, получавших тоцилизумаб + БПВП; в большинстве из этих случаев терапия тоцилизумабом была отменена.
В течение двойного слепого контролируемого периода исследования частота случаев повышения уровня непрямого билирубина выше ВГН, оцениваемых в рамках рутинного мониторинга лабораторных показателей, составила 6.2% у пациентов, получавших тоцилизумаб в дозе 8 мг/кг + БПВП. У 5.8% пациентов наблюдалось повышение уровня непрямого билирубина в диапазоне от >1 до 2 ×ВГН, а у 0.4% — >2×ВГН.
Во время двойного слепого контролируемого периода и при длительной экспозиции характер и частота возникновения явлений, связанных с повышением активности АЛТ/АСТ, оставались такими же, как и в 6-месячных контролируемых клинических исследованиях.
Показатели липидного обмена
В ходе 6-месячных контролируемых исследований часто сообщалось о повышении показателей липидного обмена, таких как общий холестерин, триглицериды, ЛПНП и/или ЛПВП. При рутинном мониторинге лабораторных показателей примерно у 24% пациентов, получавших препарат Актемра® в рамках проведения клинических исследований, наблюдалось стойкое повышение уровня общего холестерина ≥6.2 ммоль/л, а у 15% — стойкое повышение уровня ЛПНП до ≥4.1 ммоль/л. Повышение, наблюдавшееся в показателях липидного обмена, реагировало на лечение гиполипидемическими препаратами.
Во время двойного слепого контролируемого периода и при длительной экспозиции характер и частота возникновения явлений, связанных с повышением показателей, характеризующих липидный обмен, оставались такими же, как и в 6-месячных контролируемых клинических исследованиях.
Злокачественные новообразования
Клинических данных недостаточно для оценки потенциальной частоты возникновения злокачественных новообразований после применения тоцилизумаба. Оценка долгосрочной безопасности терапии продолжается.
Кожные реакции
При пострегистрационном применении в редких случаях сообщалось об эпизодах синдрома Стивенса-Джонсона.
COVID-19
Оценка безопасности применения препарата Актемра® у пациентов с COVID-19 была основана на результатах, полученных в 3 рандомизированных двойных слепых плацебо-контролируемых исследованиях (исследования ML42528, WA42380 и WA42511).
В общей сложности 974 пациента получили терапию препаратом Актемра® в рамках проведения данных исследований. Сбор данных по безопасности в рамках проведения исследования RECOVERY был ограничен и здесь не представлен.
Следующие нежелательные реакции, перечисленные в соответствии с системно-органной классификацией медицинского словаря для нормативно-правовой деятельности MedDRA в таблице 6, были отнесены к событиям, которые наблюдались не менее чем у 3% пациентов, получавших терапию препаратом Актемра®, и чаще, чем у пациентов, получавших плацебо, в объединенной популяции пациентов для оценки безопасности применения препарата в рамках проведения клинических исследований ML42528, WA42380 и WA42511.
Таблица 6. Перечень нежелательных реакций1, выявленных в объединенной популяции для оценки безопасности в рамках проведения клинических исследований препарата Актемра® у пациентов COVID-192
1 Пациенты учитываются один раз в каждой категории независимо от количества реакций.
2 Включены реакции, о которых сообщалось в исследованиях WA42511, WA42380 и ML42528.
Описание отдельных нежелательных реакций
Инфекции
В объединенной популяции пациентов для оценки безопасности в ходе проведения исследований ML42528, WA42380 и WA42511 частота событий, связанных с инфекциями/серьезными инфекциями, была сбалансирована между пациентами с COVID-19, получавшими тоцилизумаб (30.3%/18.6%, n = 974) и плацебо (32.1%/22.8%, n = 483). Профиль безопасности, наблюдаемый на исходном уровне в группе, получавшей лечение системными ГКС, соответствовал профилю безопасности применения тоцилизумаба в общей популяции, представленному в таблице 6. В данной подгруппе инфекции и серьезные инфекции наблюдались у 27.8% и 18.1% пациентов, получавших тоцилизумаб в/в, и у 30.5% и 22.9% пациентов, получавших плацебо, соответственно.
Изменения лабораторных показателей
Частота изменений, наблюдаемых в лабораторных показателях, была в целом сходной между пациентами с COVID-19, получившими в/в одну или две дозы препарата Актемра®, по сравнению с теми, кто получал плацебо в рандомизированных двойных слепых плацебо-контролируемых исследованиях, за редким исключением. Снижение числа тромбоцитов и нейтрофилов, а также повышение активности АЛТ и АСТ чаще наблюдалось у пациентов, получавших препарат Актемра®, по сравнению с плацебо (см. разделы «Режим дозирования» и «Особые указания»).
сЮИА и пЮИА
Профиль безопасности применения тоцилизумаба в популяции детей обобщен ниже в разделах, касающихся пЮИА и сЮИА. В целом, нежелательные реакции у пациентов с пЮИА и сЮИА были схожи по типу с теми, которые наблюдались у пациентов с РА (см. раздел «Побочное действие» выше).
Нежелательные реакции у пациентов с пЮИА и сЮИА, получавших тоцилизумаб, перечислены в таблице 7 и представлены в соответствии с системно-органной классификацией медицинского словаря для нормативно-правовой деятельности MedDRA. Для описания частоты развития нежелательных реакций используются следующие категории: очень часто (≥1/10); часто (≥1/100, но <1/10) и нечасто (≥1/1000, но <1/100).
Таблица 7. Перечень нежелательных реакций, наблюдавшихся у пациентов с сЮИА или пЮИА, получавших тоцилизумаб в качестве монотерапии или в комбинации с МТ
1 Инфузионные реакции у пациентов с пЮИА включали головную боль, тошноту и повышение АД, но не ограничивались ими.
2 Инфузионные реакции у пациентов с сЮИА включали сыпь, крапивницу, диарею, дискомфорт в эпигастрии, артралгию и головную боль, но не ограничивались ими.
пЮИА
Профиль безопасности препарата Актемра® в/в при пЮИА был изучен у 188 пациентов в возрасте от 2 до 17 лет. Общая продолжительность воздействия препарата на пациентов составила 184.4 пациенто-лет. Частота развития нежелательных реакций у пациентов с пЮИА представлена в таблице 7. Типы нежелательных реакций, наблюдавшихся у пациентов с пЮИА, были аналогичны тем, которые наблюдались у пациентов с РА и сЮИА (см. раздел «Побочное действие» выше). По сравнению с популяцией взрослых пациентов с РА в популяции пациентов с пЮИА чаще регистрировались такие явления, как назофарингит, головная боль, тошнота и снижение числа нейтрофилов. Случаи повышения уровня холестерина в популяции пациентов с пЮИА отмечались реже, чем в популяции взрослых пациентов с РА.
Инфекции
Частота возникновения инфекций в популяции всех пациентов, получавших тоцилизумаб, составила 163.7 явления на 100 пациенто-лет. Наиболее часто регистрируемыми явлениями были назофарингит и инфекции верхних дыхательных путей. Частота возникновения серьезных инфекций была численно выше у пациентов с массой тела <30 кг, получавших тоцилизумаб в дозе 10 мг/кг (12.2 явления на 100 пациенто-лет), в сравнении с пациентами с массой тела ≥30 кг, получавшими тоцилизумаб в дозе 8 мг/кг (4.0 явления на 100 пациенто-лет). Частота возникновения инфекций, которые привели к прерыванию терапии, также была численно выше среди пациентов с массой тела <30 кг, получавших тоцилизумаб в дозе 10 мг/кг (21.4%), в сравнении с пациентами с массой тела >30 кг, получавшими тоцилизумаб в дозе 8 мг/кг (7.6%).
Инфузионные реакции
У пациентов с пЮИА инфузионные реакции определяют, как все явления, развившиеся во время инфузии или в течение 24 часов после инфузии. В популяции всех пациентов, получавших тоцилизумаб, у 11 пациентов (5.9%) развились инфузионные реакции во время инфузии, а у 38 пациентов (20.2%) данное явление развилось в течение 24 ч после инфузии. Наиболее частыми явлениями, развившимися во время инфузии, были головная боль, тошнота и артериальная гипотензия, а наиболее частыми явлениями, развившимися в течение 24 ч после инфузии, были головокружение и артериальная гипотензия. В целом, нежелательные реакции, наблюдавшиеся во время инфузии или в течение 24 ч после нее, были сходными по характеру с нежелательными реакциями, наблюдавшимися у пациентов с РА и сЮИА (см. раздел «Побочное действие» выше).
О клинически значимых реакциях гиперчувствительности, связанных с тоцилизумабом и требующих прекращения лечения, не сообщалось.
Иммуногенность
У одного пациента из группы, получавшей тоцилизумаб в дозе 10 мг/кг, с массой тела <30 кг, был получен положительный результат анализа на антитела к тоцилизумабу, без развития реакции гиперчувствительности; впоследствии этот пациент был исключен из исследования.
Нейтрофилы
В ходе рутинного мониторинга лабораторных показателей в популяции всех пациентов, получавших тоцилизумаб, снижение числа нейтрофилов до уровня ниже 1×109/л наблюдалось у 3.7% пациентов.
Тромбоциты
В ходе рутинного мониторинга лабораторных показателей в популяции всех пациентов, получавших тоцилизумаб, у 1% пациентов наблюдалось снижение числа тромбоцитов до уровня ≤ 50×103/мкл, которое не сопровождалось развитием эпизодов кровотечений.
Повышение активности печеночных трансаминаз
В ходе рутинного мониторинга лабораторных показателей в популяции всех пациентов, получавших тоцилизумаб, явления, связанные с повышением активности АЛТ или АСТ до уровня ≥3×ВГН, наблюдались у 3.7% и <1% пациентов соответственно.
Показатели липидного обмена
В ходе рутинного мониторинга лабораторных показателей, выполняемого в рамках проведения исследования препарата Актемра® в/в (исследование WA19977), у 3.4% и 10.4% пациентов наблюдалось повышение ЛПНП до уровня ≥130 мг/дл и общего холестерина до уровня ≥200 мг/дл в любой временной точке в ходе терапии, выполняемой в рамках исследования, соответственно, по сравнению с исходным уровнем.
сЮИА
Профиль безопасности препарата Актемра® в/в при сЮИА был изучен у 112 пациентов в возрасте от 2 до 17 лет. В 12-недельной двойной слепой контролируемой части исследования 75 пациентов получали терапию тоцилизумабом (8 мг/кг или 12 мг/кг в зависимости от массы тела). По прошествии 12 недель или в момент перехода на терапию препаратом Актемра® из-за ухудшения течения заболевания пациенты получили лечение в рамках открытого расширенного периода исследования.
В целом, нежелательные реакции у пациентов с сЮИА были схожи по типу с теми, которые наблюдались у пациентов с РА (см. раздел «Побочное действие» выше). Частота развития нежелательных реакций у пациентов с сЮИА представлена в таблице 7. По сравнению с популяцией взрослых пациентов с РА, у пациентов с сЮИА чаще наблюдались назофарингит, снижение числа нейтрофилов, повышение активности печеночных трансаминаз и диарея. Случаи повышения уровня холестерина в популяции пациентов с сЮИА отмечались реже, чем в популяции взрослых пациентов с РА.
Инфекции
В 12-недельной контролируемой фазе исследования частота возникновения всех инфекций в группе пациентов, получавших препарат Актемра® в/в, составила 344.7 случая на 100 пациенто-лет и 287.0 случая на 100 пациенто-лет в группе пациентов, получавших плацебо. В ходе открытого расширенного периода исследования (часть II) общая частота возникновения инфекций осталась сходной и составила 306.6 случая на 100 пациенто-лет.
В 12-недельной контролируемой фазе исследования частота возникновения серьезных инфекций в группе пациентов, получавших в/в препарат Актемра®, составила 11.5 случая на 100 пациенто-лет. Через один год в ходе открытого расширенного периода исследования общая частота возникновения серьезных инфекций осталась стабильной и составила 11.3 случая на 100 пациенто-лет. Серьезные инфекции были сходными с серьезными инфекциями, наблюдавшимися у пациентов с РА, дополнительно отмечались случаи ветряной оспы и отита среднего уха.
Инфузионные реакции
Инфузионные реакции определяют, как все явления, развившиеся во время инфузии или в течение 24 ч после нее. В 12-недельной контролируемой фазе исследования у 4% пациентов из группы, получавшей тоцилизумаб, отмечались явления, произошедшие во время инфузии. Одно явление (ангионевротический отек) было оценено как серьезное и жизнеугрожающее, и пациент был исключен из исследования.
В 12-недельной контролируемой фазе исследования у 16% пациентов из группы, получавшей тоцилизумаб, и у 5.4% пациентов из группы, получавшей плацебо, инфузионная реакция развилась в течение 24 ч после инфузии. В группе, получавшей тоцилизумаб, явления включали сыпь, крапивницу, диарею, дискомфорт в эпигастрии, артралгию и головную боль (но не ограничиваясь ими). Одно из этих явлений (крапивница) было оценено как серьезное.
Клинически значимые реакции гиперчувствительности, связанные с введением тоцилизумаба и потребовавшие прекращения терапии, отмечались у 1 из 112 пациентов (<1%), получавших тоцилизумаб в ходе контролируемого исследования, включая открытое клиническое исследование.
Иммуногенность
У всех 112 пациентов на исходном уровне был проведен анализ на антитела к тоцилизумабу. У двух пациентов были обнаружены антитела к тоцилизумабу, при этом у одного из этих пациентов развилась реакция гиперчувствительности, которая привела к прекращению терапии. Частота образования антител к тоцилизумабу может быть недооценена из-за влияния тоцилизумаба на результаты анализа и более высокой концентрации препарата, наблюдаемой у детей по сравнению со взрослыми.
Нейтрофилы
В ходе рутинного мониторинга лабораторных показателей, выполняемого в рамках 12-недельной контролируемой фазы исследования, снижение числа нейтрофилов до уровня ниже 1×109/л наблюдалось у 7% пациентов из группы, получавшей тоцилизумаб; в группе, получавшей плацебо, такого снижения не наблюдалось.
В ходе открытого расширенного периода исследования уменьшение числа нейтрофилов до уровня ниже 1×109/л наблюдалось у 15% пациентов из группы, получавшей тоцилизумаб.
Тромбоциты
В ходе рутинного мониторинга лабораторных показателей, выполняемого в рамках 12-недельной контролируемой фазы исследования, у 3% пациентов из группы, получавшей плацебо, и у 1% пациентов из группы, получавшей тоцилизумаб, наблюдалось снижение числа тромбоцитов до уровня ≤100×103/мкл.
В ходе открытого расширенного периода исследования у 3% пациентов из группы, получавшей тоцилизумаб, наблюдалось снижение числа тромбоцитов до уровня ниже 100×103/мкл, которое не сопровождалось развитием эпизодов кровотечений.
Повышение активности печеночных трансаминаз
В ходе рутинного мониторинга лабораторных показателей, выполняемого в рамках 12-недельной контролируемой фазы исследования, явления, связанные с повышением активности АЛТ или АСТ до уровня ≥3×ВГН, наблюдались у 5% и 3% пациентов соответственно в группе, получавшей тоцилизумаб, и у 0% пациентов в группе, получавшей плацебо.
В ходе открытого расширенного периода исследования явления, связанные с повышением активности АЛТ или АСТ до уровня ≥3×ВГН, наблюдались у 12% и 4% пациентов соответственно в группе, получавшей тоцилизумаб.
Иммуноглобулин G
Уровень IgG снижается во время терапии. Снижение до нижней границы нормы было отмечено у 15 пациентов в определенный момент исследования.
Показатели липидного обмена
В ходе рутинного мониторинга лабораторных показателей, выполняемого в рамках 12-недельной контролируемой фазы исследования (исследование WA18221), у 13.4% и 33.3% пациентов наблюдалось повышение ЛПНП до уровня ≥130 мг/дл и общего холестерина до уровня ≥200 мг/дл в любой временной точке в ходе терапии, выполняемой в рамках исследования, соответственно, по сравнению с исходным уровнем.
В ходе открытого расширенного периода исследования (исследование WA18221) у 13.2% и 27.7% пациентов наблюдалось повышение ЛПНП до уровня ≥130 мг/дл и общего холестерина до уровня ≥200 мг/дл в любой временной точке в ходе терапии, выполняемой в рамках исследования, соответственно.
Противопоказания к применению
- повышенная чувствительность к тоцилизумабу, любому компоненту препарата в анамнезе;
- активные инфекционные заболевания (в т.ч. туберкулез), за исключением COVID-19;
- детский возраст до 2 лет для пациентов с полиартикулярным ювенильным идиопатическим артритом и системным ювенильным идиопатическим артритом;
- возраст до 18 лет для пациентов с ревматоидным артритом;
- комбинация с ингибиторами ФНОα или применение в течение 1 месяца после лечения анти-ФНО антителами;
- детский возраст до 18 лет для пациентов с новой коронавирусной инфекцией (COVID-19) (данные отсутствуют);
- повышение активности печеночных ферментов в ≥10 раз от ВГН; абсолютное число нейтрофилов (АЧН) <1×109/л; число тромбоцитов <50×103/мкл (COVID-19).
С осторожностью
Рецидивирующие или хронические инфекции в анамнезе, а также сопутствующие заболевания (например, дивертикулит, сахарный диабет и интерстициальное заболевание легких), предрасполагающие к развитию инфекций.
Язвенное поражение органов ЖКТ или дивертикулит в анамнезе.
Активное заболевание печени или печеночная недостаточность.
Показатели АЛТ или АСТ, превышающие ВГН более чем в 1.5 раза.
Уровень тромбоцитов ниже 100×103/мкл.
Применение при беременности и кормлении грудью
Беременность
Безопасность и эффективность применения препарата Актемра® при беременности изучены недостаточно. Исследования у обезьян не обнаружили дисморфогенетического потенциала препарата Актемра®. Однако при введении препарата в высоких дозах обнаружен повышенный риск спонтанного выкидыша/внутриутробной гибели. Значение данной информации для людей неизвестно (см. раздел «Фармакологическое действие»).
Не следует применять тоцилизумаб во время беременности, за исключением тех случаев, когда имеется очевидная клиническая необходимость.
Период грудного вскармливания
Неизвестно, выводится ли препарат Актемра® с грудным молоком у человека. Несмотря на выделение эндогенных IgG в грудное молоко, системная абсорбция препарата при грудном вскармливании маловероятна в связи с быстрой протеолитической деградацией таких белков в системе пищеварения.
При принятии решения о продолжении/прерывании кормления грудью или продолжении/отмене терапии тоцилизумабом следует принимать во внимание пользу от грудного вскармливания для ребенка и пользу от продолжения терапии для матери.
Применение при нарушениях функции печени
Противопоказание: повышение активности печеночных ферментов в ≥10 раз от ВГН; абсолютное число нейтрофилов (АЧН) <1×109/л; число тромбоцитов <50×103/мкл (COVID-19).
С осторожностью: активное заболевание печени или печеночная недостаточность
Применение при нарушениях функции почек
Применение тоцилизумаба у пациентов с почечной недостаточностью умеренной и тяжелой степени не изучалось.
Специальных исследований у пациентов с почечной недостаточностью не проводилось. У большинства пациентов с РА, учтенных в популяционном фармакокинетическом анализе, была нормальная функция почек или нарушение функции почек легкой степени тяжести (расчетный КК по формуле Кокрофта-Голта), которое не влияло на фармакокинетику тоцилизумаба. Коррекции дозы тоцилизумаба пациентам с нарушением функции почек легкой степени тяжести не требуется.
Применение у детей
Противопоказания: детский возраст до 2 лет для пациентов с полиартикулярным ювенильным идиопатическим артритом и системным ювенильным идиопатическим артритом; возраст до 18 лет для пациентов с ревматоидным артритом; детский возраст до 18 лет для пациентов с COVID-19.
Применение у пожилых пациентов
Коррекции дозы у пациентов пожилого возраста (65 лет и старше) не требуется.
Особые указания
В медицинской документации пациента следует указывать торговое наименование препарата (Актемра®) и номер серии.
РА, пЮИА и сЮИА
Инфекции
У пациентов, получающих иммуносупрессанты (в т.ч. препарат Актемра®) отмечались серьезные случаи возникновения инфекций, некоторые из них с летальным исходом (см. раздел «Побочное действие»). Не следует начинать лечение препаратом Актемра® пациентам с активными инфекциями (см. раздел «Противопоказания»). Введение препарата Актемра® должно быть приостановлено в случае развития у пациента серьезной инфекции, до момента взятия инфекции под контроль (см. раздел «Побочное действие»). Медицинским работникам следует соблюдать осторожность при рассмотрении вопроса о применении препарата Актемра® у пациентов с рецидивирующими или хроническими инфекциями в анамнезе, а также с сопутствующими заболеваниями (например, дивертикулитом, сахарным диабетом и интерстициальным заболеванием легких), предрасполагающих к развитию инфекций.
Следует проявлять особую осторожность с целью своевременного выявления серьезных инфекций у пациентов, получающих терапию биологическими препаратами, поскольку признаки или симптомы острого воспаления могут быть стерты в связи с подавлением реакции острой фазы. Следует учитывать влияние тоцилизумаба на уровень CРБ, число нейтрофилов и на признаки и симптомы развития инфекций при обследовании пациента на предмет возможного развития инфекции.
Необходимо проинструктировать пациентов (включая детей раннего возраста с сЮИА или пЮИА, которые не всегда способны описать симптомы) и родителей/опекунов пациентов с пЮИА или сЮИА о немедленном обращении к врачу при любых симптомах, свидетельствующих о появлении инфекции, с целью обеспечения быстрой диагностики и назначения необходимого лечения.
Туберкулез
Как и при назначении других биологических препаратов, перед началом терапии препаратом Актемра® пациенты с РА, сЮИА и пЮИА должны пройти на латентный туберкулез. Пациенты, у которых был выявлен латентный туберкулез, должны пройти стандартный курс антимикобактериальной терапии перед началом лечения препаратом Актемра®. Лечащему врачу следует помнить о риске получения ложноотрицательных результатов туберкулиновой кожной пробы и квантиферонового теста, особенно у пациентов с тяжелыми заболеваниями или ослабленным иммунитетом. Пациенты должны быть проинструктированы о необходимости обратиться к врачу, если признаки/симптомы (например, стойкий кашель, истощение/снижение массы тела, субфебрильная температура), указывающие на туберкулезную инфекцию, возникают во время или после терапии препаратом Актемра®.
Реактивация вирусных инфекций
Были описаны случаи реактивации вирусной инфекции (например, вирусного гепатита В) при применении биологических препаратов для лечения РА. Пациенты, имевшие положительный результат при скрининговом обследовании на гепатит, не включались в клинические исследования тоцилизумаба.
Осложнения дивертикулита
О случаях перфорации дивертикула, как осложнения дивертикулита при применении препарата Актемра® у пациентов с РА, сообщалось нечасто (см. раздел «Побочное действие»). Следует соблюдать осторожность при применении препарата Актемра® у пациентов с язвенным поражением органов ЖКТ или дивертикулитом в анамнезе. Пациенты с симптомами, возможно указывающими на осложнения дивертикулита, такими как боль в животе, кровотечение и/или необъяснимые изменения в частоте и характере стула, сопровождающиеся повышением температуры тела, должны быть немедленно обследованы с целью раннего выявления дивертикулита, который может быть связан с перфорацией ЖКТ.
Реакции гиперчувствительности
При инфузии препарата Актемра® наблюдались серьезные реакции гиперчувствительности (см. раздел «Побочное действие»). Такие реакции могут быть более тяжелыми и потенциально летальными у пациентов, у которых наблюдались реакции гиперчувствительности во время предшествующих инфузий, даже если они получали премедикацию стероидами и антигистаминными препаратами. Должно быть предусмотрено наличие необходимого оборудования и персонала для оказания экстренной помощи в случае развития анафилактической реакции во время терапии препаратом Актемра®. При возникновении анафилактической реакции или другой серьезной реакции гиперчувствительности/серьезной инфузионной реакции, введение препарата Актемра® следует немедленно прекратить, при этом терапия препаратом Актемра® должна быть отменена.
Активные заболевания печени и печеночная недостаточность
Терапия препаратом Актемра®, особенно одновременно с МТ, может быть ассоциирована с повышением активности печеночных трансаминаз, поэтому следует проявлять осторожность у пациентов с активным заболеванием печени или печеночной недостаточностью (см. разделы «Режим дозирования», «Побочное действие»).
Гепатотоксичность
При лечении препаратом Актемра® часто наблюдалось преходящее или периодическое легкое и умеренное повышение активности печеночных трансаминаз (см. раздел «Побочное действие»). Частота возникновения такого повышения возрастала при применении препарата Актемра® совместно с препаратами, обладающими потенциально гепатотоксическим действием (например, МТ). При наличии клинических показаний следует рассмотреть возможность выполнения других функциональных печеночных проб, включая оценку уровня билирубина.
При применении препарата Актемра® наблюдалось серьезное лекарственное поражение печени, включая острую печеночную недостаточность, гепатит и желтуху (см. раздел «Побочное действие»). Серьезные поражения печени отмечались в интервале от 2 недель до >5 лет после начала терапии препаратом Актемра®. Сообщалось о случаях развития печеночной недостаточности, которые привели к трансплантации печени. Пациентам следует рекомендовать немедленно обратиться за медицинской помощью при появлении признаков и симптомов поражения печени.
Следует соблюдать осторожность при решении вопроса о начале терапии препаратом Актемра® у пациентов с показателями АЛТ или АСТ, превышающими ВГН более чем в 1.5 раза. Терапия препаратом Актемра® не рекомендуется при показателях АЛТ или АСТ, превышающих ВГН более чем в 5 раз у пациентов с РА, пЮИА и сЮИА.
У пациентов с РА, пЮИА и сЮИА следует контролировать АЛТ/АСТ каждые 4-8 недель на протяжении первых 6 месяцев после начала терапии, а в дальнейшем — каждые 12 недель. Рекомендации по дозированию, включая отмену препарата Актемра® в зависимости от активности трансаминаз, представлены в разделе «Режим дозирования». Следует прекратить лечение препаратом Актемра® при повышении показателей АЛТ или АСТ в 3-5 раз выше ВГН, подтвержденном повторным анализом.
Отклонения показателей общего анализа крови
После лечения тоцилизумабом в дозе 8 мг/кг в комбинации с МТ наблюдалось снижение числа нейтрофилов и тромбоцитов (см. раздел «Побочное действие»). Может быть повышен риск развития нейтропении у пациентов, которые ранее получали лечение антагонистом ФНО.
Пациентам, ранее не получавшим лечение препаратом Актемра®, не рекомендуется начинать лечение с АЧН менее 2×109/л. Следует проявлять осторожность при рассмотрении вопроса о начале лечения препаратом Актемра® у пациентов с низким уровнем тромбоцитов (т. е. с уровнем тромбоцитов ниже 100×103/мкл). У пациентов с РА, сЮИА и пЮИА, с АЧН <0.5×109/л или числом тромбоцитов <50×103/мкл продолжать лечение не рекомендуется.
Тяжелая нейтропения может быть связана с повышенным риском развития серьезных инфекций, хотя до настоящего времени в клинических исследованиях препарата Актемра® не было выявлено четкой связи между снижением числа нейтрофилов и возникновением серьезных инфекций.
У пациентов с РА следует контролировать показатели нейтрофилов и тромбоцитов в период с 4 по 8 неделю после начала терапии и в дальнейшем в соответствии со стандартами клинической практики. Рекомендации по коррекции дозы в зависимости от АЧН и уровня тромбоцитов представлены в разделе «Режим дозирования».
У пациентов с сЮИА и пЮИА показатели нейтрофилов и тромбоцитов следует контролировать в день проведения 2 инфузии, а в дальнейшем в соответствии со стандартами клинической практики (см. раздел «Режим дозирования»).
Показатели липидного обмена
У пациентов, получавших тоцилизумаб, наблюдалось повышение показателей липидного обмена, включая общий холестерин, ЛПНП, ЛПВП и триглицериды (см. раздел «Побочное действие»). У большинства пациентов индекс атерогенности не повышался, а повышение концентрации общего холестерина эффективно корригировалось гиполипидемическими препаратами.
При РА, пЮИА и сЮИА следует оценивать показатели липидного обмена у пациентов в период с 4 по 8 неделю после начала терапии препаратом Актемра®. При ведении пациентов следует руководствоваться локальными рекомендациями по лечению гиперлипидемии.
Нарушения со стороны нервной системы
Врачи должны проявлять особую осторожность с целью раннего выявления симптомов, возможно указывающих на дебют демиелинизирующих заболеваний ЦНС. В настоящее время влияние препарата Актемра® на развитие демиелинизирующих заболеваний ЦНС не известно.
Злокачественные новообразования
У пациентов с РА повышен риск развития злокачественных новообразований. Иммуномодулирующие лекарственные препараты могут повышать риск развития злокачественных новообразований.
Иммунизация
Не следует проводить иммунизацию живыми и живыми ослабленными вакцинами одновременно с терапией препаратом Актемра®, поскольку клиническая безопасность подобного сочетания не установлена. В рандомизированном открытом исследовании у взрослых пациентов с РА, получавших терапию препаратом Актемра® и МТ, ответ на 23-валентную пневмококковую полисахаридную вакцину и столбнячный анатоксин был сопоставим с таковым у пациентов, получающих монотерапию МТ. Всем пациентам, особенно пациентам с сЮИА и пЮИА, рекомендуется пройти вакцинацию в соответствии с национальным календарем прививок до начала лечения препаратом Актемра®. Следует соблюдать интервал (в соответствии с действующими национальным календарем прививок) у пациентов, получающих терапию иммуносупрессивными препаратами, между иммунизацией живыми вакцинами и началом терапии препаратом Актемра®.
Риск развития сердечно-сосудистых заболеваний
У пациентов с РА имеется повышенный риск развития сердечно-сосудистых заболеваний, поэтому факторы риска (например, повышение АД, гиперлипидемия) должны контролироваться в рамках стандартного лечения.
Комбинация с антагонистами ФНО
Опыт применения препарата Актемра® с антагонистами ФНО или другими биологическими препаратами для лечения пациентов с РА, сЮИА или пЮИА отсутствует. Не рекомендуется применять препарат Актемра® с другими биологическими препаратами.
Содержание натрия
Данный препарат содержит 1.17 ммоль (или 26.55 мг) натрия в пересчете на максимальную дозу 1200 мг. Необходимо учитывать пациентам, находящимся на диете с ограничением поступления натрия. Данный лекарственный препарат в дозах менее 1025 мг содержит менее 1 ммоль натрия (23 мг), т. е. практически «не содержит натрий».
COVID-19
При новой коронавирусной инфекции COVID-19 препарат Актемра® следует применять в условиях стационара.
Эффективность применения препарата Актемра® не была установлена при лечении пациентов с COVID-19, у которых не был повышен уровень CРБ (см. раздел «Фармакологическое действие»).
Препарат Актемра® не должен назначаться пациентам с COVID-19, не получающим системные ГКС, поскольку в этой подгруппе нельзя исключить увеличение уровня смертности (см. раздел «Фармакологическое действие»).
Инфекции
Пациентам с COVID-19 не следует назначать препарат Актемра®, если у них имеется какая- либо другая сопутствующая тяжелая активная инфекция. Медицинским работникам следует соблюдать осторожность при применении препарата Актемра® у пациентов с рецидивирующими или хроническими инфекциями в анамнезе, а также при сопутствующих заболеваниях (например, при дивертикулите, сахарном диабете и интерстициальном заболевании легких), предрасполагающих к развитию инфекций.
Гепатотоксичность
У госпитализированных пациентов с COVID-19 может быть повышена активность АЛТ или АСТ. Полиорганная недостаточность с поражением печени признана осложнением тяжелой формы COVID-19. При принятии решения о применении тоцилизумаба следует сбалансировать потенциальную пользу, получаемую от лечения COVID-19, с потенциальным риском неотложной терапии тоцилизумабом. У пациентов с COVID-19 с повышением активности АЛТ или АСТ, превышающей ВГН более чем в 10 раз, применение препарата Актемра® не рекомендуется. У пациентов с COVID-19 следует мониторировать активность АЛТ/АСТ в соответствии с текущей стандартной клинической практикой.
Отклонения показателей общего анализа крови
У пациентов с COVID-19 с АЧН <1×109/л или числом тромбоцитов <50 ×103/мкл лечение не рекомендуется. Показатели нейтрофилов и тромбоцитов следует мониторировать в соответствии с текущей стандартной клинической практикой (см. раздел «Режим дозирования»).
Дети
Синдром активации макрофагов у пациентов с сЮИА
Синдром активации макрофагов является серьезным жизнеугрожающим состоянием, которое может развиться у пациентов с сЮИА. В клинических исследованиях применение тоцилизумаба у пациентов в период возникновения синдрома активации макрофагов не изучалось.
Влияние на способность к управлению транспортными средствами и механизмами
Исследования по изучению влияния препарата на способность управлять транспортными средствами и механизмами не проводились. Однако, учитывая тот факт, что при терапии препаратом Актемра® часто наблюдалось головокружение, пациентам, испытывающим данную нежелательную реакцию, следует рекомендовать не управлять транспортными средствами и механизмами до тех пор, пока головокружение не прекратится.
Передозировка
Доступные данные о передозировке препарата Актемра® ограничены. В одном случае непреднамеренной передозировки препарата в дозе 40 мг/кг у пациента с множественной миеломой нежелательных реакций не отмечено. Не отмечалось также серьезных нежелательных реакций у здоровых добровольцев, которые получали однократно препарат Актемра® в дозе до 28 мг/кг, хотя наблюдалась нейтропения, требующая снижения дозы.
Лекарственное взаимодействие
Исследования взаимодействия были проведены только у взрослых пациентов.
Одновременное однократное введение тоцилизумаба в дозе 10 мг/кг и метотрексата в дозе 10-25 мг 1 раз в неделю не оказывало клинически значимого влияния на экспозицию метотрексата.
Популяционные фармакокинетические анализы клинических не выявил какого-либо воздействия метотрексата, НПВП или ГКС на клиренс тоцилизумаба.
Экспрессия печеночных изоферментов системы CYP450 подавляется под действием цитокинов, таких как ИЛ-6, которые стимулируют хроническое воспаление. Таким образом, при проведении терапии средствами, ингибирующими действие цитокинов (например, тоцилизумаб), экспрессия изоферментов CYP450 может быть нарушена.
В исследованиях in vitro, проведенных на культуре гепатоцитов человека, было показано, что ИЛ-6 вызывает снижение экспрессии изоферментов CYP1A2, CYP2C9, CYP2C19 и CYP3A4. Применение тоцилизумаба нормализует экспрессию этих изоферментов.
В исследовании у пациентов с РА концентрация симвастатина (субстрат CYP3A4) через 1 неделю после однократного введения тоцилизумаба снижалась на 57%, т.е. была немного повышенной или аналогичной таковой у здоровых добровольцев.
В начале или при завершении курса терапии тоцилизумабом следует наблюдать за пациентами, получающими лекарственные средства в индивидуально подобранных дозах, и которые метаболизируются посредством изоферментов CYP450 3A4, 1A2 или 2C9, например, метилпреднизолон, дексаметазон (с возможностью развития синдрома отмены ГКС, предназначенных для приема внутрь), аторвастатин, блокаторы кальциевых каналов, теофиллин, варфарин, фенпрокумон, фенитоин, циклоспорин или бензодиазепины, поскольку для поддержания терапевтического эффекта может потребоваться увеличение их дозы.
Учитывая длительный T1/2 тоцилизумаба, его действие на активность изоферментов CYP450 может сохраняться в течение нескольких недель после прекращения терапии.
Условия хранения препарата Актемра®
Препарат следует хранить в недоступном для детей, защищенном от света месте при температуре от 2° до 8°С; не замораживать.
Срок годности препарата Актемра®
Срок годности — 2 года 6 месяцев. Не применять по истечении срока годности.
Условия реализации
Препарат отпускают по рецепту.
Контакты для обращений
Ф.ХОФФМАНН-ЛЯ РОШ ЛТД.
(Швейцария)

|
|
Претензии потребителей следует направлять |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Актемру относят к иммунодепрессантам, которые используются в терапии ревматических заболеваний суставов. Медикамент позволяет остановить патогенез болезни, не дать ей дальше развиваться.
Врачи рекомендуют это лекарство для терапии:
- ревматоидного артрита (можно применять с 2-летнего возраста);
- периартикулярного ЮИА (средство наряду с метотрексатом является элементом комплекса лечебных мероприятий);
- болей в суставах, коленях.
Решение о дозировке, схеме использования препарата «Актемра» принимает доктор, принимая во внимание тяжесть, специфику заболевания, возрастные и индивидуальные особенности пациента.
При каких симптомах и болезнях применяют препарат Актемра?
Ревматоидный артрит, боли в суставах, боли в коленях, лечение ревматоидного артрита, лечение суставов, лечение болей в коленях
«Актемра» – новое слово в борьбе с распространенным хроническим заболеванием соединительных тканей, приводящим к разрушению суставов.
Состав
Действующим компонентом является тоцилизумаб, 20 мг которого находится в 1 мл. Его дополняют составляющие вспомогательного действия, включая сахарозу, полисорбат80, воду для инъекций, другие.
Показания к применению «Актемра»
Прописывают при нарушениях в соединительных тканях с хроническим течением, провоцирующим разрушение симметричных суставов (РА умеренная либо высокая степень). Взрослым применяется лечебный курс одним средством и комбинированный с метотрексатом, иными базовыми препаратами противовоспалительного действия.
Противопоказания к применению «Актемра»
Медикамент способен навредить:
- людям, гиперчувствительным к какой-либо составляющей;
- при заболеваниях инфекционного типа (включая те, что вызываются палочками Коха);
- в период вынашивания ребенка;
- при лактации.
Осторожно назначается людям при наличии:
- рецидивирующих форм инфекции;
- воспаления дивертикулита, диабета и прочих вторичных недугов, способствующих развитию инфицирования;
- серьезных проблем с печенью, включая печеночную недостаточность;
- низкого уровня нейтрофилов (нейтропении).
Рекомендации по применению
Стандартная дозировка предполагает:
- внутривенное вливание с помощью капельницы 8 мг на килограмм веса на протяжении минимум часа, раз в 28 дней.
В условиях асептики актемру разбавляют до 100 мл стерильным 0,9 % раствором натрия хлорида.
Смесь готовят следующим образом:
- Определяется нужное количество актемры (рассчитывая, что 0,4 мл идет на 1 кг).
- Из 100 мл емкости (может быть бутылкой, пакетом) с раствором натрия хлорида 0,9 %, соблюдая асептику, с помощью шприца (стерильного) отбирается количество, идентичное рассчитанному для ввода актемры.
- Другой шприц (при соблюдении аналогичных требований) служит для забора из бутылочки с актемрой рассчитанного объема медикамента с последующим его вливанием в используемую для инфузии емкость с раствором натрия хлорида. В итоге получается 100 мл.
- Нельзя допускать образования пены. Перемешивают, аккуратно перевернув емкость.
- Прежде чем вводить пациенту, раствор осматривается и проверяется на наличие посторонних включений, изменения цвета.
Для введения пользуются исключительно прозрачной либо опалесцирующей жидкостью без цвета, либо со светло-желтой окраской. Не допускается посторонних примесей.
Раствор нуждается в правильном хранении, что предполагает следующее:
- готовый раствор актемры для вливания остается стабилен (по физическим и химическим параметрам) в 0,9 % растворе натрия хлорида сутки при 30 градусах;
- с позиции микробиологии им необходимо воспользоваться по назначению сразу после того, как он был сделан;
- правильность хранения неиспользованного раствора является зоной ответственности пользователя. Нельзя допускать превышения допустимого времени – 24 часа, температурных границ – 2-8 °C. И это касается ситуаций, когда компоненты смешивали при строгом соблюдении асептики.
Существуют разные варианты дозирования и использования средства:
- детям – риски с результативностью не определены;
- людям старше 65 лет – обычная дозировка;
- людям с почечной недостаточностью (в легкой форме) – обычное дозирование, при более сложных формах случаи не были изучены;
- людям с печеночной недостаточностью – не проводили изучений по вопросам опасности и результативности.
Применение при беременности и кормлении грудью
Вопросы, связанные с опасностью и действенностью актемры при вынашивании ребенка, мало изучались. При опытах на обезьянах не был обнаружен дисморфогенетический потенциал лекарства. Но когда вводили животным лекарство в высоких дозировках, выявили значимую опасность для плода. Это могло провоцировать самопроизвольный выкидыш, смерть эмбриона.
Нет данных по поводу поступления ребенку лекарства с материнским молоком. Эндогенные антитела в молоко выделяются, но вероятность системного впитывания медпрепарата при таком кормлении минимальная. Это объясняется тем, что расщепляющая регрессия этих белков в пищеварительной системе происходит быстро.
Фармакологическое действие
«Актемра» относится к медпрепаратам с иммунодепрессивным действием.
Фармакодинамика лечебного средства:
Активное вещество актемры – представитель рекомбинантных известных антител моноклонального типа к цитокину, выполняющему много функций – рецептору человека «интерлейкин-6», относящемуся к иммуноглобулинам IgG1. Рецепторы растворимого и мембранного плана подавляются тоцилизумабом, связывающимся селективно. ИЛ-6 вырабатывают разные по типу клетки, которые являются участниками:
- паракринного процесса регуляции;
- процессов физиологии и патологии на системной основе (стимулирование секреции иммуноглобулинов, активирования Т-клеток, стимулирование производства белков печени при острой фазе, кроветворения).
Рецептор вовлекается в патогенез воспалений, новых образований, болезни с потерей кальция в костях и т. д.
Есть предположение о негативном воздействии тоцилизумаба на иммунитет в отношении опухолей и инфекций. Отсутствуют сведения о роли подавления ИЛ-6 в процессе опухолевого развития.
Клиническая эффективность при лечении (РА) актемрой при дозировке 8 мг/кг действующего компонента:
- результат в пределах 20-70 % (по нормам Американской коллегии ревматологов) спустя полгода отмечали чаще, чем при применении взятых для сравнения медпрепаратов независимо от того, был ли ревматоидный аспект, и вместе с тем влияния возраста, половой принадлежности, расы, количества пройденных лечебных курсов, тяжести заболевания. Организм быстро отвечал на терапию (уже после 7 дней), наблюдалось усиление эффекта на протяжении всего терапевтического курса, сохранялся больше 1,5 года;
- значительнее были улучшения, чем у получавших лечение «плацебо» с метотрексатом и/либо базисными противовоспалительными препаратами (БПВП), относительно таких критериев АКР, как:
- количество суставов с присутствующей болезненностью и отеками;
- общая оценка результативности терапии с точки зрения врача и больного;
- уровень нарушения функций;
- оценка выраженности боли и т. п.
- существеннее, чем при лечебном комплексе плацебо с БПВП, уменьшался индекс действенности болезни по градации шкалы DAS-28.
Кроме того, по критериям Европейской лиги против ревматизма намного чаще был отмечен хороший либо умеренный результат у тех, кто лечился препаратом «Актемра» в сравнении с комплексом «плацебо+БПВП».
Рентгенологическое оценивание:
- Замедление поражения суставной структуры – сравнивая представителей с несоответствующим ожиданию откликом на метотрексат (МТ), изменением при этом модифицированного индекса Sharp, костной эрозии и уменьшения щели в суставах, с группой больных, получавших актемру, ощутимо меньшая симптоматика прогрессирующего разрушительного процесса были у последних.
- Показатели уровня нарушений в плане функциональности, усталости при хроническом течении болезни, здоровья в физическом смысле и психики улучшились – клинически значимее при терапии только одной актемрой (8 мг/кг тоцилизумаба) либо в комбинации с БПВП, нежели MT и/или БПВП.
- Понижение у больных индивидуального суммарного балла больше 0,25 (улучшения по критерию HAQ-DI) – к 24-й неделе доля пациентов, использовавших актемру (8 мг/кг), существенно превышала долю получавших в качестве лечения «плацебо» с МТ/БПВП.
- Рост гемоглобина во время применения терапии только актемрой (8 мг/кг) и в сочетании с БПВП/MT значителен с позиций статистики и виден к началу 24-й недели. Максимальное повышение выявили у представителей с анемией в хронической форме, имеющей связь с артритом. Среднее значение возросло к началу 2-й недели, было в норме все 24.
- Средние показатели в острой фазе (реактивный белок, СОЭ, сывороточный амилоид А) – после вывода активного компонента актемры быстро шли на понижение при уменьшении тромбоцитов, хотя они оставались в пределах нормативов.
Параметры фармакокинетики актермы (тоцилизумаба) неизменны.
В зависимости от дозировки для тоцилизумаба 4 мг/кг либо 8 мг/кг максимально увеличивались Area Under the Curve (AUC) и Cmin каждые 28 дней. У показателя Cmax и дозой зависимость прямо пропорциональна. Если сравнить в условиях положения равновесия дозировки 8 мг/кг и 4 мг/кг, то расчетные показатели AUC и Cmin выше соответственно в 2,7 и 6,5 раза.
Активный компонент актемры (8 мг/кг) каждые 28 дней характеризуется:
- расчетным средним показателем AUC в состоянии равновесия — 35000±15500 мкг × ч/мл;
- Cmin – 9,74±10,5 мкг/мл;
- Cmax – 183±85,6 мкг/мл;
- коэффициентами накопления AUC и Cmax – 1,22 и 1,06;
- коэффициентом накопления биологически активного вещества Cmin, который выше по причине нелинейного клиренса при низких концентрациях – 2,35.
Равновесного состояния достигли после 1-го ввода и спустя 8 и 20 недель соответственно для Cmax, AUC и Cmin.
Характеристика активного компонента (4 мг/кг) каждые 28 дней:
- расчетное среднее AUC (с учетом норм отклонений) в состоянии равновесия — 13000±5800 мкг × ч/мл;
- Cmin – 1,49±2,13 мкг/мл;
- Cmax – 88,3±41,4 мкг/мл;
- коэффициенты накопления для AUC и Cmax – соответственно 1,11 и 1,02, для Cmin — 1,96.
Равновесного состояния для Cmax и AUC достигли после первого применения, для Cmin спустя 16 недель.
Тоцилизумаб распределяется следующим образом:
- выводится из кровообращения в 2 фазы после внутривенного ввода;
- при наличии РА объем в центре 3,5 л, на периферии – 2,91 л, в положении равновесия – 6,41 л.
Выведение актемры:
на клиренс (общий) активного компонента, который состоит из линейного и нелинейного компонента, влияет плотность. Линейный – 12,5 мл/ч, нелинейный зависит от плотности, максимален при низкой сосредоточенности активной составляющей. Более высокой насыщенности тоцилизумаба характерен линейный клиренс, что связано с насыщением пути нелинейного.
Концентрация влияет на период полувыведения. Он для дозировки 4 мг/кг тоцилизумаба при однократном на 28 дней вводе равен 11 дням, при удвоенной дозировке — 13 дням.
Фармакокинетические особенности актемры для отдельных групп:
- с печеночной недостаточностью – аспект не был изучен;
- с почечной недостаточностью – специальные исследования по данной категории больных не проводились;
- с работой почек в пределах норм, легкими нарушениями данной функции – в большей части случаев клиренс креатинина, который определялся по формуле Кокрофта-Голта, был в пределах 80 и 50 мл/мин. и не оказывал влияния на фармакокинетикие параметры активного компонента;
- с легкими нарушениями почечных функций – корректировка дозировки актемры не нужна.
Популяционный анализ, который проводили на взрослых пациентах, страдающих РА, не выявил зависимости фармакокинетических параметров активного компонента лекарства от возрастных, половых, расовых факторов. Поэтому коррекция доз в таких случаях не нужна.
Результаты доклинических исследований лекарства:
- В отношении влияния канцерогенов медикамент не испытывали. Доклинические сведения позволяют утверждать, что злокачественные новообразования и стойкость к апоптозу разных раковых форм прогрессируют под влиянием плейотропного ИЛ-6. И это не предусматривает того, что терапия актемрой влечет появление значительных рисков для развития, прогрессирования раковых заболеваний. Полугодичные исследования, во время которых на яванских макаках, грызунах с недостаточным количеством ИЛ-6 изучали токсичность хронического характера, не показали нарушений пролиферации.
- Отрицательными были результаты стандартных генотоксических тестов на мутогенность в клетках прокариотического и эукариотического типа.
- Влияние терапии на фертильность животных неизвестно, поскольку таких исследований не проводили. Но согласно имеющимся доклиническим данным тоцилизумаб не оказывает такого влияния. Изучая хроническую токсичность на обезьянах и грызунах, не обнаружили отрицательных изменений эндокринных или репродуктивных органов.
- Не выявили негативных последствий (прямых либо опосредованных) такой терапии животных в период ожидания детенышей, эмбриофетального развития. Опыты на тератогенность проводили в гестационном периоде, причем на ранних сроках.
- Иные результаты свидетельствуют о небольшом росте эпизодов непреднамеренных выкидышей, смерти плода в утробе, когда воздействовали на высоком уровне системно и кумулятивно при суточной дозировке 50 мг на килограмм, сравнивая с действием плацебо либо меньшими дозировками. По частоте самопроизвольных абортов нормы исторического контроля для живущих в невольных условиях обезьян нарушены не были. Не было обнаружено взаимосвязи доз, используемых при вводе активного компонента лекарства, и выкидышей/гибели эмбриона. Но нельзя исключать взаимосвязи использования тоцилизумаба и развития плода либо иммунологической регуляции в системе «мама-плод», невзирая на то, что у ИЛ-6, вероятнее всего, в этих процессах не первостепенная роль.
Побочные действия «Актемра»
Нежелательные реакции бывают с разной частотой, для которой используют описание следующими категориями:
больше или равно 1:
- на 10 – очень частые реакции;
- на 100 и меньше 1 на 10 – частые случаи;
- на 1000 и меньше 1 на 100 – нечастые проявления.
Терапия актемрой сопровождается прогрессом инфекций:
- верхних отделов дыхательных путей – очень частые реакции;
- кожи, подкожных тканей в острой бактериальной форме – частые эпизоды;
- дивертикулов – нечастые проявления.
Органы пищеварения могут реагировать на актемру:
- язвенными поражениями полости рта, гастритами – частые случаи;
- стоматитом – нечастые проявления.
Кожные покровы с придатками:
- частые случаи высыпаний, зуда;
- нечастые – появления крапивницы.
Нервные пути на фоне лечения реагируют:
- головной болью, дурнотой – частые проявления.
Сердце и сосуды:
- скачки давления – частые эпизоды.
Ухудшение общего самочувствия в ходе терапевтического курса может быть при повышенной чувствительности.
Результаты лабораторных анализов показывают:
- лейкопению, нейтропению, гиперхолестеринемию, рост активности трансаминаз печени – частые явления;
- гипертриглицеридемию, рост уровня билирубина – нечасто.
Дальше ознакомимся с отдельными нежелательными эффектами при лечебных мероприятиях с актемрой.
Появление и развитие инфекций:
- Исследования, подконтрольно проводимые на фоне ввода тоцилизумаба (8 мг/кг) вместе с БПВП и при использовании «плацебо+БПВП», свидетельствуют о частоте возникновения инфекций, соответственно равной 127 и 112 эпизодам на сотню человек-лет. Долговременные исследования открытого типа показывают частоту воспалений при лечении актемрой совместно с БПВП на сотню человек-лет 116 эпизодов.
- Исследования, проводимые подконтрольно в клинических условиях, демонстрируют частотность тяжелых инфекций среди представителей группы, получавшей актемру (8 мг/кг) параллельно с БПВП, на уровне 5,3 раз на сотню человек-лет, в то время как 3,9 случая было при использовании схемы «плацебо+БПВП». На лечение только актемрой реакция серьезными инфекциями была 3,6 раза на сотню человек-лет, на монотерапию метотрексатом 1,5 в аналогичных условиях.
Длительные исследования, проводимые открыто, показали побочные реакции на ввод актемры совместно с БПВП в виде серьезного воспаления с частотой 3,9 на 1 сотню человек-лет.
Из серьезных инфекций зафиксировали:
- воспаление легких;
- флегмону;
- опоясывающий лишай;
- катар желудка и кишок;
- воспаление дивертикулов;
- заражение крови;
- артрит бактериального характера.
Подобное инфицирование в ходе использования лекарства изредка завершались фатально. Есть сведения о проявлении оппортунистических заболеваниях инфекционного характера.
- Перфорация стенок органов ЖКТ:
На полугодичных контролируемых исследованиях, проводимых под контролем, среди представителей, лечившихся актемрой, у 0,1 % (нечастые явления) отмечали возникновение сквозных дефектов стенок органов пищеварения. В подавляющем большинстве это были негативные последствия после дивертикулита с гнойным воспалением брюшины, перфорацией стенок органов нижних зон ЖКТ, нарывами.
- Типы реакций внутривенного введения:
Побочные явления, имеющие связь с актемрой (проявления непосредственно во время ввода либо на протяжении 24 часов с момента ввода), были зафиксированы у 6,9 % больных, которые принимали дозировку 8 мг/кг вместе с БПВП, у 5,1 % – при лечебной схеме «плацебо+БПВП». При непосредственном вводе лекарства, в основном, встречались эпизодичные повышения давления. А в течение суток после завершения процедуры поступали жалобы на головную боль, появление кожных высыпаний, а также были реакции в виде крапивницы. Однако все это не требовало ограничивать лечебные мероприятия.
Анафилаксию наблюдали у 6 из 3778 человек. Такая частота при дозировке 4 мг на килограмм в несколько раз превышала аналогичный показатель при удвоенной дозировке. У 0,3 % пациентов в ходе открытых испытаний (под контролем в клинических условиях) отмечали значительную повышенную чувствительность на фоне лечения актемрой. Эти случаи требовали отмены средства. Большая часть сопутствующих проявлений наблюдалась в промежутке 2-5 введений.
- Иммуногенность:
При проведении обследований 2876 человек на наличие антител к активному компоненту лекарственного средства у 1,6 % они были определены. Пятерым из этой группы нужна была полная отмена лечебного курса по причине повышенной чувствительности. 30 больных, которые были обследованы, имели антитела (нейтрализаторы).
Динамика показателей в лабораторных анализах была следующая:
Сбои в плане гематологии:
Определили падение уровня нейтрофилов ниже 1·109/л у 3,4 % больных, которым совместно с БПВП вводилась «Актемра» (8 мг/кг). Около половины эпизодов фиксировались на 8-ой неделе, в то время как в группе, получавшей «плацебо+БПВП», показатель был меньше 0,1 %. Уменьшения нейтрофилов до уровня ниже 0,5·109/л были замечены у 0,3 % больных с лечебным курсом БПВП с актемрой (8 мг/кг). Отчетливой взаимосвязи данных снижений с тяжелыми инфекционными болезнями не фиксировали.
- Тромбоциты снижались до отметки меньше 100·103/мкл у 1,7 % человек с терапией актемрой (8 мг/кг) и БПВП. Для представителей группы, принимавшей «плацебо+БПВП», менее чем 1 %. Кровотечений при этом не было зафиксировано.
- Возрастала активность трансаминаз печени при лечении только актемрой (8 мг/кг) у 2,1 % человек и 4,9 % – МТ, в комплексе с БПВП соответственно у 6,5 % и 1,5 %.
- Чаще фиксировали эпизодичный рост активности трансаминаз, когда присоединяли к монокурсу тоцилизумабом лекарства потенциального гепатотоксического действия, к примеру, МТ. Повышение такой активности наблюдалось у 0,7 % человек с монолечением актемрой, а в комплексе с БПВП – в 2 раза больше. Для большей части больных актемру отменили. При этих повышениях не было заметного роста уровня прямого билирубина, таких клинических проявлений, как гепатит, печеночная недостаточность.
- Возрастали при лечении такие параметры липидного обмена, как общий холестерин (больше 6,2 ммоль/л у 24 % человек), триглицериды, ЛПВП и ЛПНП (больше равно 4,1 ммоль/л – у 15 %). Это было подмечено в ходе полугодичных испытаний открытого типа. У преобладающего количества больных не наблюдалось роста индекса атерогенности, а холестерин поддавался коррекции с помощью гиполипидемических средств.
Особые указания
При наличии инфекций в активной фазе не рекомендовано начинать терапевтические мероприятия с актемрой. Развитие серьезных воспалительных процессов – весомый повод для прерывания курса до полного избавления от проблемы. Необходимо соблюдение осторожности при применении лекарственного средства:
- больными, в анамнезах которых отмечены рецидивирующие инфекции;
- при наличии параллельных заболеваний, способствующих прогрессированию инфекции (дивертикулита, диабета и т. п.).
Пациенты с РА, принимающие лекарства биологического типа, требуют обследования, чтобы на ранних этапах выявить у них опасные инфекции. Биологическими препаратами, которые способны устранять острые фазы, может быть стерта симптоматика с признаками острых воспалений. Больным нужно дать инструкции, как себя вести при любой симптоматике, которая говорит о возникновении инфекций. Им срочно нужно обратиться к доктору для прохождения диагностики и получения необходимой терапии.
В практике были эпизоды с перфорацией дивертикулов. Это были осложнения после дивертикулита. Рекомендовано с осторожностью назначать актемру людям с язвами органов пищеварительного тракта, а также с наличием признаков воспаления дивертикулов. Симптомом такого осложненного состояния являются болевые ощущения в области живота. Этим пациентам нужно немедленное обследование, чтобы выявить перфорацию ЖКТ на ранних этапах.
При туберкулезе до принятия решений лечиться данным медикаментом, подобно случаям применения иных биологических препаратов для оказания помощи при РА, нужна предварительная диагностика с целью выявления латентной формы заболевания. В случаях подтверждения сначала назначается курс стандартного антимикробного и бактериального лечения.
Что касается иммунизации, то не стоит использовать живые, ослабленные живые вакцины наряду с актемрой из-за неустановленного факта безопасности подобной комбинации. Кроме того, нет сведений о вторичном инфицировании вакцинированными людьми (живыми вакцинами) тех, кто лечиться тоцилизумабом.
Для людей с реакциями гиперчувствительности при использовании лекарства на основе тоцилизумаба (доля таких пациентов 0,3 %) обязаны быть в доступе медикаменты, требуемые для оказания помощи при анафилактических реакциях. Их применяют безотлагательно.
Серьезные проблемы с печенью, включая активные стадии заболеваний, печеночную недостаточность, при применении актемры, в особенности совместно с МТ, могут связываться с ростом активности трансаминаз печени. Поскольку не было проведено достаточного количества исследований по вопросу безопасности использования лекарства в таких случаях, при назначении медикамента требуется осторожность.
Использование лекарства ассоциируется с развитием нейтропении. В практике проведения клинических опытов данное заболевание на фоне лечения актемрой не ассоциировали с прогрессом серьезных воспалительных процессов. Осторожно назначают средство в случаях наличия АЧН меньше 2,0·109 /л. А показатель АЧН менее 0,5·109/л служит весомым аргументом для отказа от использования медикамента. Кроме того, нужен мониторинг количества нейтрофилов на протяжении 4-8-й недели с момента старта лечения. Дальнейший контроль состояния ведется соответственно клинической практике. Есть рекомендованная дозировка, которая устанавливается в зависимости от уровня АЧН.
Тромбоцитопению ассоциировали с применением актемры. При проведении клинических исследований уровень тромбоцитов снижался, но это не связывали с таким проявлением, как кровотечение серьезного характера. Взвешенность решения по поводу назначения курса требуется в случаях снижения количества тромбоцитов, которое превышает уровень 100 ·103/мкл. Не следует использовать данное средство при понижении уровня в 2 раза и больше. Кроме того, показан мониторинг тромбоцитов на этапе 4-8-я недели, дальше — соответственно клинической практике. При этом используют рекомендованные дозировки.
Печеночные трансаминазы активнее действовали, но этот рост активности был легким или умеренным. Признаки печеночной недостаточности не присутствовали. Применение медикамента в комплексе с препаратами потенциального гепатотоксического действия (к примеру, МТ) способствовала увеличению частоты подобных проявлений. Нужно взвешенно назначать актемру при АЛТ/АСТ выше ВГН больше полтора раза. Рекомендован отказ от такой терапии при больше пятикратном превышении АЛТ/АСТ над ВГН. Контроль изменений показателей нужно обеспечить особенно на 4-8-й неделе, начиная со старта. В разделе инструкции о дозах и способах применения есть рекомендованные дозировки.
Что касается динамики показателей липидного обмена, то фиксировалось их повышение. Их контроль и оценку ситуации нужно обеспечить через 28-56 дней после старта лечебного курса. Ведущий пациента доктор, как правило, руководствуется рекомендациями по терапии гиперлипидемии.
В отношении влияния на возможность управления транспортом, выполнения точных работ и управления механизмами исследований не проводилось. Если брать во внимание механизм действия с профилем безопасности, данное лекарственное средство не оказывает подобного влияния.
Передозировка
Случаи с передозировкой были, но доступ к этим данным ограничен. Непреднамеренное превышение дозы (40 мг/кг) один раз зафиксирован у больного со множественной миеломой, но все обошлось без нежелательных последствий. Серьезные нежелательные проявления также не отметил у себя доброволец (здоровый человек) после однократного получения дозы до 28 мг/кг. Однако у него наблюдали влияющую на понижение дозировки нейтропению.
Лекарственное взаимодействие
В ходе популяционного анализа фармакокинетических параметров при проведении клинических исследований не было выявлено какого-либо из воздействий МТ, НПВС либо кортикостероидов на коэффициент очищения вещества тоцилизумаб.
Параллельный одноразовый ввод 10 мг/кг тоцилизумаба с 10–25 мг МТ раз в 7 дней не влиял (клинически значимо) на поведение МТ.
Вопросы использования комбинирования вещества тоцилизумаб и других биологических БПВП не были изучены.
Цитокины способствуют подавлению образования изоферментов CYP450 печени. К примеру, ИЛ-6 – один из тех цитокинов, которые способны на стимуляцию хронических воспалений. Тоцилизумаб относится к группе средств, ингибирующих активность цитокинов. А значит, лечение медикаментами с подобными активными компонентами может нарушать экспрессию печеночных изоферментов.
Результаты опытов вне живого организма на культуре человеческих гепатоцитов показали уменьшение экспрессии ряда изоферментов (CYP1A2, CYP2C9, CYP2C19 и CYP3A4) под воздействием ИЛ-6. Тоцилизумаб данный процесс приводит в норму.
Изоферменты CYP (за исключением СYP2C19, CYP2D6) попадают под влияние препарата «Актемра». Это много значит в клинической практике медикаментов, которые представляют собой субстраты CYP450. Такие лекарственные средства имеют узкий терапевтический индекс, подбор доз проходит в индивидуальном порядке.
Однократный ввод тоцилизумаба понижал концентрацию симвастатина (субстрата СYP3A4) на 57 %. Такое изменение до аналогичного либо незначительно повышенного уровня у добровольцев (здоровых людей) достигалось через 7 дней.
На старте либо финише терапевтического курса пациенты могут нуждаться в тщательном наблюдении. Это касается тех, кто лечился средствами, способными на метаболизм под влиянием CYP450 3A4, 1A2 либо 2C9. В этой группе определено место:
- аторвастатину;
- БКК;
- теофиллину;
- варфарину;
- фенитоину;
- циклоспорину;
- бензодиазепину и т. п.
В подобных ситуациях может потребоваться повышение доз. С учетом периода полувыведения актемры есть вероятность сохранения ее воздействия на изоферменты CYP450. Это может длиться несколько недель после того, как завершают лечение.
Условия хранения
Хранить без доступа детям, защищая от попадания света, соблюдая температурный режим 2-8 °C. Заморозка запрещается.
Средство годно 2,5 года.
Условия отпуска
Рецептурный препарат.

