Лекарственная форма
|
|
ЦЕФТОНИТ® |
Суспензия для инъекций рег. 44-3-3.17-3703№ПВР-3-29.11/02820 |
Форма выпуска, состав и упаковка
Суспензия для инъекций от белого до темно-кремового цвета.
Вспомогательные вещества: бутилгидрокситолуол (ионол), кремния диоксид коллоидный безводный (аэросил 300), триглицериды насыщенных жирных кислот (миритол 318).
Расфасована по 100 мл в стеклянные флаконы, герметично укупоренные резиновыми пробками, укрепленными алюминиевыми колпачками с клипсами контроля первого вскрытия. Флаконы с препаратом допускается упаковывать в индивидуальные пачки из картона. Каждая потребительская упаковка снабжена инструкцией по применению препарата.
Фармакологические (биологические) свойства и эффекты
Антибиотик группы цефалоспоринов.
Цефтиофура гидрохлорид, входящий в состав препарата, цефалоспориновый антибиотик III поколения, широкого спектра действия, оказывающий бактерицидное действие. Активен в отношении грамотрицательных и грамположительных бактерий, включая штаммы, продуцирующие β-лактамазы, и некоторые анаэробные бактерии: Actinobacillus spp., Actinobacillus pleuropneumoniae, Actinomyces spp., Actinomyces pyogenes, Bacillus spp., Citrobacter spp., Enterobacter spp., Escherichia spp., Escherichia coli, Fusobacterium spp, Fusobacterium necrophorum, Histophilus somni (Haemophilus somnus), Haemophilus spp., Haemophilus parasuis, Klebsiella spp., Pasteurella spp., в т.ч. Pasteurella (Mannheimia) haemolytica, Pasteurella multocida, Porphyromonas spp., Porphyromonas assacharolytica (Bacteroides melaninogenicus), Porphyromonas levii, Proteus spp., Salmonella spp., Salmonella choleraesuis, Salmonella typhimurium, Staphylococcus aureus, Staphylococcus spp.,Streptococcus suis, Streptococcus zooepidemicus, Streptococcus equi, Streptococcus agalactiae, Streptococcus dysgalactiae, Streptococcus uberis и Streptococcus bovis.
Механизм бактерицидного действия цефтиофура заключается в ингибировании функциональной активности бактериальных ферментов транспептидаз, участвующих в связывании основного компонента клеточной стенки микроорганизмов — пептидогликана, что приводит к нарушению осмотического баланса и разрушению бактериальной клетки.
После парентерального введения препарата цефтиофур поступает в системный кровоток, быстро метаболизируется с образованием десфуроилцефтиофура, который обладает эквивалентной цефтиофуру антибактериальной активностью, обратимо связывается с белками плазмы и концентрируется в местах воспаления. Cmax цефтиофура и его метаболитов в крови достигается через 0.5-2 ч и сохраняется на терапевтическом уровне не менее 20 ч. Выводится из организма, главным образом, с мочой (свыше 55%) и частично с фекалиями.
Цефтонит® по степени воздействия на организм относится к малоопасным веществам (4 класс опасности по ГОСТ 12.1.007-76).
Показания к применению препарата ЦЕФТОНИТ®
Крупному рогатому скоту для лечения заболеваний бактериальной этиологии, возбудители которых чувствительны к цефтиофуру, в т.ч.
- инфекции органов дыхания, вызываемые Pasteurella haemolytica, Pasteurella multocida, Haemophilus somnus;
- некробактериоз, вызываемый Fusobacterium necrophorum и Porphyromonas assacharolytica (Bacteroides melaninogenicus);
- острый эндометрит.
Свиньям для лечения заболеваний, возбудители которых чувствительны к цефтиофуру, в т.ч.:
- инфекции органов дыхания, вызываемые Pasteurella haemolytica, Pasteurella multocida, Actinobacillus pleuropneumoniae и Streptococcus suis.
Порядок применения
Цефтонит® вводят крупному рогатому скоту 1 раз/сут п/к в дозе 1 мл на 50 кг массы животного (1 мг цефтиофура на 1 кг). Курс лечения при заболеваниях дыхательных путей составляет 3-5 дней, при некробактериозе — 3 дня, при эндометрите — 5 дней.
Свиньям при заболеваниях органов дыхания препарат вводяи в/м 1 раз/сут в дозе 1 мл на 16 кг массы животного (3 мг цефтиофура на 1 кг) в течение 3 дней.
Перед каждым использованием флакон с препаратом следует тщательно встряхнуть.
Особенностей действия при первом применении и отмене лекарственного препарата не выявлено.
Следует избегать пропусков при введении очередной дозы препарата, т.к. это может привести к снижению терапевтической эффективности. При пропуске одной или нескольких доз препарата курс применения необходимо возобновить в предусмотренном режиме дозирования. Не следует превышать рекомендуемую дозу для компенсации пропущенной.
Побочные эффекты
При использовании препарата Цефтонит® согласно инструкции по применению побочных явлений и осложнений, как правило, не наблюдается. В редких случаях в месте инъекции возможно развитие отека, который рассасывается самопроизвольно в течение нескольких суток. При повышенной индивидуальной чувствительности животного к антибиотикам группы цефалоспоринов и возникновении аллергических реакций использование препарата прекращают, животному назначают антигистаминные препараты и симптоматическую терапию.
При передозировке препарата у животного может наблюдаться снижение аппетита, воспалительная реакция в месте инъекции.
Противопоказания к применению препарата ЦЕФТОНИТ®
- индивидуальная повышенная чувствительность животных к цефтиофуру и другим бета-лактамным антибиотикам.
Особые указания и меры личной профилактики
Цефтонит® не следует применять одновременно с антибиотиками группы тетрациклина и левомицетином в связи с возможным снижением его бактерицидной активности, с антибиотиками группы аминогликозидов, фуросемидом и этакриновой кислотой из-за возможного усиления нефротоксического эффекта.
Особенности применения препарата самкам во время беременности и лактации не установлены.
Убой на мясо крупного рогатого скота разрешается не ранее чем через 8 суток, свиней — не ранее чем через 5 суток после последнего введения лекарственного препарата. Мясо животных, вынужденно убитых до истечения указанного срока, может быть использовано для кормления пушных зверей. Молоко дойных коров в период применения препарата разрешается использовать в пищевых целях без ограничений.
Меры личной профилактики
При применении препарата Цефтонит® следует соблюдать общие правила личной гигиены и техники безопасности, предусмотренные при работе с лекарственными препаратами. Во время работы с препаратом запрещается пить, курить и принимать пищу. По окончании работы с препаратом руки следует вымыть теплой водой с мылом.
Людям с гиперчувствительностью к компонентам препарата следует избегать прямого контакта с препаратом Цефтонит®. При случайном контакте лекарственного препарата с кожей или слизистыми оболочками глаз их необходимо промыть большим количеством воды. В случае появления аллергических реакций или при случайном попадании препарата в организм человека следует немедленно обратиться в медицинское учреждение (при себе иметь инструкцию по применению препарата или этикетку).
Пустую тару из-под лекарственного препарата запрещается использовать для бытовых целей; она подлежит утилизации с бытовыми отходами.
Условия хранения ЦЕФТОНИТ®
Препарат следует хранить в закрытой упаковке производителя, отдельно от продуктов питания и кормов, в защищенном от прямых солнечных лучей, недоступном для детей месте при температуре от 5° до 25°С.
Неиспользованный лекарственный препарат утилизируют в соответствии с требованиями действующего законодательства.
Срок годности ЦЕФТОНИТ®
Срок годности при соблюдении условий хранения в закрытой упаковке производителя — 3 года со дня производства; после первого вскрытия первичной упаковки — не более 28 суток. Запрещается применять Цефтонит® по истечении срока годности.
Условия отпуска
Препарат отпускают без рецепта.
Контакты для обращений
|
|
410010 Саратов, |
ЦЕФТОНИТ® отзывы
Помогите другим с выбором, оставьте отзыв об ЦЕФТОНИТ®
Оставить отзыв
Цефалоспориновые антибиотики применяются в клинической практике с начала 60-х годов и за эти годы синтезировано более 50 препаратов этой группы. (Periti P.J Chemother 1996) В настоящее время цефалоспорины занимают ведущее место при лечении различных инфекций в ветеринарной практике; в большинстве случаев им отдается предпочтение в схемах начальной эмпирической терапии инфекций различной локализации. В то же время ограничивающим фактором применения цефалоспоринов является развитие резистентности микроорганизмов в результате продукции ими бета-лактамаз.
Особенно эта проблема стала актуальна в последние годы из-за широкого применения цефалоспоринов, иногда неоправданного и часто бесконтрольного. Использование одних и тех же антибиотиков для лечения животных и людей должно быть ограничено.
Понижение эффективности антибиотиков, связано с нарушением правил использования антибиотиков, занижение дозы (однократное применение вместо двух или трехкратного в сутки). Использование цефтриаксона 1 раз в сутки при том, что концентрация этого препарата поддерживается в течение 16 часов. Однократное введение в блокаде не отменяет двух или трехкратное использование препарата в сутки. Если антибиотик применялся местно для блокады однократно, то с интервалом 8-12 часов он должен быть введен внутримышечно или внутривенно.
Также большее предпочтение в выборе препарата должно отдаваться препаратам с низкой токсичностью для макроорганизма.
Спектр действия препарата никак не связан с его токсичностью. Современные антибиотики: цефалоспорины 3 и 4 поколения, карбапенемы, защищенные пенициллины, обладают высокой терапевтической активностью, широким спектром действия и при этом минимальным токсическим действием на организм животного, в отличие от левомецитина, который при узком спектре действия и бактериостатическом эффекте весьма опасен для макроорганизма, поэтому данный препарат не используется и запрещен в большинстве развитых стран мира. Также ушло в прошлое использование в ветеринарной практике стрептомицина, канамицина, бицилина, наих заменили гораздо более безопасные, эффективные, с широким спектром действия препараты.
Процент устойчивых штаммов у стафилококков составляет: к бензилпенициллину – 80-95%, к тетрациклину – 70-85%, к левомицетину – 30-55%.
Следует уделить внимание способу введения антибиотика
Внутривенное или внутриартериальное введение может в ряде случаев быть эффективнее, чем внутримышечное введение того же антибиотика. А при инфекции в ЦНС интратекальное введение антибиотика эффективнее настолько, что другое использование их является неоправданным и формирование контрольной группы в медицине представляется на сегодняшний день не этичным.
Принципы рациональной антибиотикотерапии должны стать руководством для ветеринарных врачей всех специальностей. Эти принципы применимы для антибиотиков любой группы, в том числе цефалоспоринов.
Антибиотик должен избирательно подавлять жизнедеятельность патогенного микроорганизма, не оказывая существенного воздействия на гомеостаз организма пациента.
Для воздействия на инфекционно-воспалительный процесс антибиотик должен поступать в ткани очага в достаточной (минимальной подавляющей) концентрацией.
Назначение терапии должно осуществляться с учетом чувствительности возбудителя.
Начальная (эмпирическая) противомикробная терапия проводится с учетом органолептических свойств возбудителя, основывается на знаниях о наиболее вероятном микробном «пейзаже» гнойной раны.
Исходя из полиэтиологической теории, целесообразно проведение полиантибактериальной терапии препаратами с перекрывающими полями противомикробного спектра.
Дозы, путь введения, кратность введения противомикробного препарата должны основываться на необходимости создания в очаге воспаления минимальной подавляющей концентрации.
Назначение антибактериального препарата должно сопровождаться комплексной «терапией сопровождения» направленной на регуляцию тех звеньев гомеостаза, которые наиболее подвергаются агрессии данным препаратом (группой).
При проведении противомикробной терапии необходимо учитывать химиорезистентность микроорганизмов и включать в комплекс мероприятия, направленные на ее преодоление.
Антимикробная терапия должна состоять не только из собственного антибактериального средства, но и из мероприятий, направленных на создание условий неблагоприятных для жизнедеятельности микроорганизмов, и на уменьшение количества патогенов в ране.
Существуют органолептические ориентиры для выбора антибиотика до получения результатов лабораторных исследований. При получении из очага гнойного воспаления густого, сливкообразного гноя, предположительным возбудителем является стафилококковая флора. Наличие жидкого, зловонного гноя, некротизированных тканей в ране дает основание предполагать, что одним из участников микробной ассоциации является грамоотрицательная бациллярная флора. Если гной из раны не получен, при сдавлении краев раны выделяется в скудном количестве мутно-красноватая жидкость-это, вероятно, анаэробная микрофлора.
Так как цефалоспорины наиболее часто используются в ветеринарии, необходимо подробнее рассмотреть эту группу препаратов. В зависимости от спектра антимикробной активности цефалоспорины принято разделять на четыре поколения. Сравнительная характеристика различных поколений цефалоспоринов представлена в табл.1.
Таблица.1.
| Сравнительная активность in vitro цефалоспориновых антибиотиков | ||||
| Поколения цефалоспоринов | Активность в отношении | Стабильность к бета-лактамазам | ||
| грамположительных бактерий | грамотрицательных бактерий | стафилококков | грамотрицательных бактерий | |
| Первое | +++ | +/- | ++ | — |
| Второе | ++ | + | ++ | +/- |
| Третье | + | +++ | + | + |
| Четвертое | ++ | +++ | ++ | ++ |
Цефалоспорины I
поколения характеризуются высокой активностью преимущественно в отношении грамположительных бактерий (стафилококков, стрептококков, пневмококков). Их активность в отношении грамотрицательных бактерий ограниченна (в основном E.coli, Salmonella spp., Shigella spp., P.mirabilis) в связи с тем, что препараты легко подвергались гидролизу бета-лактамазами.
Цефалоспорины II
поколения характеризуются повышенной (по сравнению с цефалоспоринами I поколения) активностью в отношении грамотрицательных бактерий, прежде всего Haemophilus infuenzae и большей стабильностью к бета-лактамазам; в то же время эти препараты сохраняют высокую активность в отношении грамположительных микроорганизмов. Ограничением применения препаратов II поколения является низкая активность в отношении некоторых грамотрицательных микроорганизмов (Enterobacter spp., Citrobacter spp., Serratia spp., P.rettgeri, Klebsiella spp., P.vulgaris) и природная устойчивость Pseudomonas spp. и Acinetobacter spp.
Цефалоспорины III
поколения (цефотаксим, цефтриаксон, цефтазидим, цефоперазон) обладают высокой активностью в отношении большинства грамотрицательных бактерий. Однако в последнее десятилетие наблюдается существенное повышение резистентности грамотрицательных микроорганизмов к цефалоспоринам III поколения, в основном за счет продукции ими бета-лактамаз различных типов и классов. Важный механизм резистентности обусловлен гиперпродукцией хромосомных бета-лактамаз за счет мутаций в регуляторных областях генома, приводящих к дерепрессии синтеза фермента. Другим важным механизмом резистентности микроорганизмов к цефалоспоринам является продукция плазмидных бета-лактамаз расширенного спектра (наиболее часто отмечается у штаммов Klebsiella spp. — примерно в 30%), гидролизующих все цефалоспорины III поколения, что определяет их клиническую неэффективность в этих случаях. Рутинные лабораторные методы оценки антибиотикочувствительности часто не выявляют этот механизм резистентности, и лаборатория может выдать врачу неправильный результат, что создает дополнительные сложности лечения этих инфекций.
Сложности в подборе эффективного антибиотика стимулируют поиск новых антибактериальных препаратов, которые, с одной стороны, позволили бы преодолеть проблему мультирезистентности грамотрицательных возбудителей инфекций, особенно продуцентов бета-лактмаз расширенного спектра, и, с другой стороны, обладали бы более высокой активностью в отношении грамположительных микроорганизмов. Этот поиск привел к созданию в середине 90-х годов новых цефалоспориновых антибиотиков, которые были отнесены к препаратам IV поколения — цефепим и цефпиром, цефкином (Кобактан для внутривенного использования).
Особенностью химической структуры молекулы цефалоспоринов IV поколения является наличие одновременно отрицательного и положительного зарядов. Цефемовое ядро антибиотиков несет отрицательный заряд. Четвертичный азот циклопентапиридиновой группы несет положительный заряд и придает молекуле биполярную структуру, которая обеспечивает быстрое проникновение антибиотиков через наружную мембрану грамотрицательных бактерий и соединение с пенициллинсвязывающими белками, что снижает вероятность их гидролиза бета-лактамазами, локализующимися в периплазматическом пространстве. Кроме того, положительный заряд служит проводником молекулы для нахождения благоприятной позиции в пориновом канале бактериальной клетки.
Аминотиазолин-метокси-иминогруппа, прикрепленная в 7 положении цефемового ядра, оказывает более выраженное действие на грамотрицательные микробы и придает устойчивость к бета-лактамазам.
Эти свойства цефалоспоринов IV поколения (быстрое проникновение через наружную мембрану бактерий, низкое сродство к бета-лактамазам и эффективное связывание с пенициллинсвязывающими белками) обеспечивают их активность в отношении грамотрицательных бактерий, в том числе штаммов, резистентных к цефалоспоринам III поколения.
У цефалоспоринов IV поколения широкий, хорошо сбалансированный антимикробный спектр. Они сочетают активность цефалоспоринов I-II поколения в отношении грамположительных микроорганизмов (метициллин-чувствительные стафилококки, стрептококки, пневмококки) и некоторых анаэробов с высокой активностью цефалоспоринов III поколения в отношении грамотрицательных бактерий (семейство Enterobacteriaceae, Neisseriaceae, Haemophilus influenzae, Moraxella catarrhalis, Pseudomonas spp., Acinetobacter spp.).
Активность цефалоспоринов IV поколения в отношении грамотрицательных бактерий не уступает или превышает таковую наиболее активных цефалоспоринов III поколения — цефотаксима и цефтриаксона и сравнима с активностью фторхинолонов и карбапенемов. Цефалоспорины IV поколения, так же как цефтазидим и цефоперазон, проявляет активность в отношении P.aeruginosa. (С.В. Яковлев1999 г).
Цефалоспорины IV поколения в большей степени, чем цефалоспорины III поколения, устойчивы к гидролизу бета-лактамазами, продуцируемыми грамотрицательными бактериями, в том числе расширенного спектра, в связи с чем они часто сохраняют активность даже в отношении штаммов, резистентных к цефалоспоринам III поколения.
Цефалоспорины IV поколения преодолевают механизм резистентности к цефалоспоринам III поколения, связанный с гиперпродукцией хромосомных бета-лактамаз.
Активность цефалоспоринов IV поколения в отношении стафилококков сравнима с активностью цефалоспоринов I и II поколений и превосходит активность цефалоспоринов III поколения.
Цефепим и цефпиром высокоактивны в отношении пневмококков, в том числе штаммов со сниженной чувствительностью к бензилпенициллину.
Однако цефалоспорины IV поколения, как и цефалоспорины других поколений, не активны в отношении метициллинрезистентных стафилококков. В данном случае следует расширить спектр действия антибиотиков ванкомицином.
Цефепим и цефпиром, цефкином(Кобактан для внутривенного использования) обладают определенной активностью в отношении некоторых анаэробов, однако они не действуют на наиболее частых возбудителей анаэробных инфекций брюшной полости и ран, поэтому в этих случаях, как правило, требуется сочетанное назначение с метронидазолом или клиндамицином, ванкомицином.
В многочисленных клинических исследованиях показана высокая эффективность цефалоспоринов IV поколения при лечении различных инфекций, в том числе наиболее тяжелых — пневмонии, перитонита, сепсиса, менингита, инфекций у пациентов с нейтропенией. После использования химиотерапевтических препаратов. (Beaucaire G. 1999).
Какими же в настоящее время представляются перспективы использования цефалоспоринов IV поколения в клинике?
Прежде всего, цефалоспорины IV поколения показаны для эмпирической терапии серьезных инфекций, учитывая их широкий антимикробный спектр и невысокий уровень резистентности микроорганизмов к этим препаратам. К таким инфекциям относятся пневмония тяжелого течения, сепсис, интраабдоминальные (в сочетании с метронидазолом), инфекции у пациентов после политравмы, нуждающихся в интенсивной терапии, инфекции у онкологических больных, инфекции мягких тканей после травмы, при гнойных отитах у собак (в сочетании с амикацином).
Другая важная область применения цефалоспоринов IV поколения — установленный высокий уровень резистентности к цефалоспоринам III поколения грамотрицательных бактерий, выделяемых в конкретном случае, прежде всего у Enterobacter spp., Serratia marcescens, а также других Enterobaсteriaceae (Е.Б. Гельфанд, Б.З. Белоцерковский, Е.А. Алексеева, Е.Ц. Цеденжапов, В.И. Карабак, Б.Р. Гельфанд, 1999-N11).
Стоимость суточной дозы цефалоспоринов IV поколения в нашей стране сопоставима со стоимостью большинства препаратов III поколения. Весьма существенным с этой точки зрения является кобактан для внутривенного использования. Недельная доза этого препарата менее затратна, чем использование цефтазидима или цефоперазона, и гораздо экономнее, чем использование медицинского препарата цефепима(максипима). Более того, цефепим и цефкином (кобактан) могут применяться для лечения смешанных аэробно-анаэробных инфекций (в сочетании с метронидазолом). На основании результатов контролируемых исследований, даже при тяжелых инфекциях, цефалоспорины IV поколения могут назначаться в режиме монотерапии.
В хирургии следует придерживаться следующих правил:
- введение антибиотиков должно начинаться не позднее, чем за 3 часа до разреза;
- применение препаратов менее чем за час не снижает риск развития осложнений;
- должна обеспечиваться достаточная концентрация (выше минимальной подавляющей концентрации) препарата в тканях операционной раны;
- период полувыведения антибиотика должен совпадать или превышать длительность операции;
- препарат должен обладать минимальными побочными эффектами.
Для этой цели хорошо подходит цефкином (Кобактан для внутривенного применения).
В неврологии при проникновении микроорганизмов в ткани мозга; при энцефалитах и открытой/закрытой черепно-мозговой травме проводится антибиотикотерапия препаратами, проникающими через гематоэнцефалический барьер. Выбор антибиотиков зависит от возбудителя заболевания и способности препарата проходить через гематоэнцефалический барьер (таб. 2).
Предпочтение должно отдаваться антибиотикам широкого спектра действия, обладающим бактерицидными свойствами и по возможности низкой токсичностью:
- цефалоспоринам III и IV поколения (цефтазидиму, цефепиму);
- карбопинемам (меронему, тиенаму);
- фторхинолонам (пефлоксацину).
Дозы цефалоспоринов должны составлять 40-50 мг/кг (2 раза в день, внутривенно).
Для лечения бактериального энцефалита, вызванного L.monocytogenes используются аминогликозиды(амикацин).
Как мы видим, цефалоспорины хорошо проникают через гематоэнцефалический барьер, исключением тут является цефоперазон.
Интратекально используют антибиотики: амикацин, карбапенемы, тазоцин(пиперациллин/тазобактам), таривид(офлоксацин), максипим, фортум, ванкомицин, диоксидин.
Таблица. 2. Способности антибиотиков проходить через гематоэнцефалический барьер
| Хорошо | Хорошо проникают при воспалении | Плохо проникают даже при воспалении | Не проникают |
| Изониазид | Азтреонам | Гентамицин | Клиндамицин |
| Пефлоксацин | Амикацин | Карбенициллин | Линкомицин |
| Рифампицин | Амоксициллин | Макролиды | |
| Ко-тримоксазол | Ампициллин | Норфлоксацин | |
| Хлорамфеникол | Ванкомицин | Ломефлоксацин | |
| Меронем | Стрептомицин | ||
| Офлоксацин | |||
| Цефалоспорины 3- 4 поколения | |||
| Ципрофлоксацин |
С появлением цефкинома (Кобактана для внутривенных инъекций) область применения цефалоспоринов IV поколения значительно расширилось ввиду его гораздо большей доступности, чем цефепима. Цефалоспорины IV поколения в практике ветеринарных врачей нашей клиники используются после операций на позвоночнике, для премедикации у пациентов, которым требуется вмешательство на спинном, головном мозге. Широкий спектр и хорошая биодоступность Кобактана для внутривенных инъекций позволяют использовать его перед большинством проводимых в ветеринарии операций.
В нашей практике цефалоспорины IV поколения используются для лечения пациентов с тяжелой политравмой, с множественными переломами, разрывами внутренних органов (мочевого пузыря, отрывами уретры и у кобелей — предстательной железы).
У собак с открытой черепно-мозговой травмой использование цефалоспоринов IV имеет прямое показание, так как эти антибиотики хорошо проникают через поврежденный гематоэнцефалический барьер.
Клинический пример лечения гнойного отита, осложненного энцефалитом, у собаки породы шарпей
В клинику поступил кобель 3 лет с симптомами атаксии. Неврологическое обследование выявило атаксию центрального происхождения. Проведена магнитно-резонансная томография, поставлен диагноз «энцефалит».
Назначено лечение: манит внутривенно и цефтазидим внутривенно.
Лечение проводилось 14 суток. После этого проведена операция по удалению слухового прохода.
После операции продолжена терапия с использованием цефтазидима, однако гнойное выделяемое продолжало наблюдаться (рис 7). С целью расширения спектра действия данному пациенту был назначен Кобактан для внутривенных инъекций в дозе 25 мг/кг 2 раза в день внутривенно в течение 7 дней. Уменьшение и прекращение гнойного отделяемого наблюдалось в течение 1-2 дней (рис 8).
При внутривенном введении кобактана не отмечено аллергических реакций и других побочных эффектов.
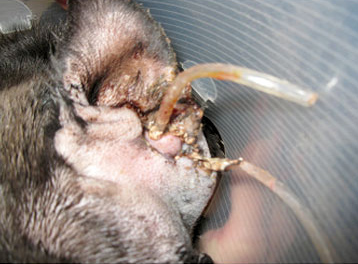
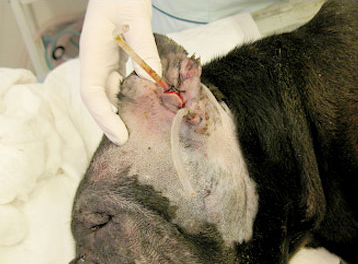 Рис. 7. Кобель породы шарпей. После удаления слухового прохода наблюдается гнойное отделяемое, несмотря на использование цефтазидима.
Рис. 7. Кобель породы шарпей. После удаления слухового прохода наблюдается гнойное отделяемое, несмотря на использование цефтазидима.
Рис. 8. Та же собака после замены цефтазидима на кобактан для внутривенных инъекций, наблюдается отсутствие гнойного отделяемого.
Таким образом, цефалоспорины IV поколения являются высокоэффективными и перспективными препаратами для лечения собак и кошек. Представляется рациональным более широкое внедрение и использование этих средств в клинической практике.
Цефалоспорины
Цефалоспорины — это природные и полусннтетические антибиотики, полученные на основе 7-аминоцефалоспориновой кислоты. Они обладают широким спектром, антибактериального действия, устойчивостью к действию стафилококковой пенициллиназы, неполной перекрестной аллергией с пенициллинами. Устойчивость бактерий к цефалоспоринам в процессе лечения развивается медленно. На микробную клетку цефалоспорины действуют бактерицидно, по механизму действия, как и пенициллины, относятся к ингибиторам синтеза клеточной стенки бактерий.
Из культуральной жидкости гриба Cephalosporium acremonium был выделен первый антибиотик этой группы — цефалоспорин С. В дальнейшем были получены полусинтетические антибиотики (цефалотин, цефалоридин, цефалексин, цефалоглицин, цефрадин, цефазолин, цефанон и др.), более эффективные по сравнению с природными цефалоспоринами.
Для парентерального введения широко используют цефалотин и цефалоридин, а для пероральиого — цефалексин. Цефалотин и цефалексин, выпускаемые отечественной промышленностью, активны в отношении кокков и большинства штаммов кишечной палочки, протея, сальмонелл и других грамотрицательных бактерий:
Цефалоспорины применяют главным образом при сепсисе, респираторных и желудочно-кишечных заболеваниях животных.
Цефалоридин — Cefaloridinum. Синонимы: цепорин, Kefladin, Ceporan.
Кристаллический порошок белого цвета, хорошо растворим в воде. Водные растворы препарата темнеют на свету.
Препарат оказывает бактерицидное действие на грамположительные и грамотрицательные (в том числе пенициллиназообразующие) кокковые микроорганизмы, клостридии, возбудителен сибирской язвы, эшерихий, сальмонелл, шигелл; менее активен в отношении энтерококков; не эффективен против синегнойной палочки, микобактерий, риккетсий, вирусов, простейших, а также большинства штаммов протея и b-лактамазообразующих штаммов грамотрицательных бактерий.
При пероральном применении цефалоридин плохо всасывается, поэтому его применяют только парентерально. При внутримышечном и внутривенном введении хорошо проникает в органы и ткани и удерживается в терапевтических концентрациях до 8 ч. Из организма выводится в основном почками.
Препарат можно использовать при наличии аллергии к пенициллинам. При введении цефалоридина в ряде случаев отмечают нефротоксическое действие.
Цефалоридин вводят внутривенно (микроструйно или капельно) или внутримышечно 3 раза в сутки в дозах на 1 кг массы животного: лошадям и крупному рогатому скоту 10—20 мг, собакам 5—15 мг. При тяжелом течении болезни показано внутривенное введение препарата в дозе 25 мг на 1 кг массы животного 4 раза в сутки.
Цефалотин — Cefalotinum. Синонимы: Cepovenin, Keflin.
Белый кристаллический порошок, хорошо растворим в воде. Спектр антимикробного действия сходен со спектром цефалоридина. Цефалотин не разрушается стафилококковой пенициллиназой, но разлагается под действием пенициллиназы, вырабатываемой грамотрицательными бактериями.
Как и цефалоридин, препарат применяют только парентерально вследствие плохой всасываемости в желудочно-кишечном тракте. Быстрее, чем цефалоридин, выводится из организма, находясь в терапевтической концентрации в крови в течение 3— 4 ч.
Цефалотин в связи с болезненностью при внутримышечном введении вводят главным образом внутривенно 4—6 раз в сутки в следующих дозах: лошадям и крупному рогатому скоту 10—15 мг, собакам 5—10 мг на 1 кг массы животного.
Цефалексин — Cefalexinum. Синонимы: Ceporex, Keflex.
Белый кристаллический, слегка гигроскопичный порошок, растворим в воде.
По спектру антимикробного действия цефалексин не отличается от цефалотина и цефалоридина, однако он устойчив в кислой среде и действует при пероральном применении. Препарат быстро и почти полностью всасывается из желудочно-кишечного тракта, выделяется в значительных количествах с мочой в измененном виде; небольшая часть антибиотика выводится с желчью.
Цефалексин применяют перорально 4 раза в сутки в дозах на 1 кг массы животного: лошадям и крупному рогатому скоту 10—15 мг, собакам 5—12 мг.
Выпускают препараты цефалоспоринов для парентерального введения в герметически закрытых флаконах: цефалоридин — по 0,25, 0,5 и 1 г; цефалотин — по 0,5, 1 и 2 г; цефалексин выпускают в капсулах по 0,25 и 0,5 г.
При применении цефалоспоринов в высших дозах необходим контроль за функцией почек в связи с возможным нефротоксическим действием.
Хранят цефалоспорины по списку Б в сухом, защищенном от света месте при температуре не выше 10°С. Срок годности 2 года.
The cephalosporins, and the closely related cephamycins, are similar to penicillins in several respects, sharing pharmacological group features.
Cephalosporins include cephamycins, which differ from other cephalosporins in that they contain a 7-alpha-methoxy group, which imparts resistance to extended-spectrum beta-lactamases. The early cephalosporins differed mainly with respect to pharmacokinetic characteristics. Whereas penicillins were classified based on source (natural vs semisynthetic) and spectra, cephalosporins are classified by generation (1–4). Later generations are more resistant to beta-lactam destruction and are often characterized by extended but variable spectra.
First-generation cephalosporins include cephaloridine, cephapirin, cefazolin, cephalexin, cephradine, and cefadroxil. Cephalosporins in this group are usually quite active against many gram-positive bacteria but are only moderately active against gram-negative organisms. They are ineffective against Enterococcus spp, Pseudomonas aeruginosa, and methicillin-resistant Staphylococcus. Susceptible gram-negative bacteria include Escherichia coli and Proteus, Klebsiella, Salmonella, Shigella, and Enterobacter spp. Cefazolin is more effective against E coli than cephalexin, to which it is minimally susceptible. Although generally less susceptible to beta-lactamase destruction than penicillins, cephalosporins are susceptible to cephalosporinases and are not as effective against anaerobes as are the penicillins.
Second-generation cephalosporins include cefamandole, cefoxitin (a cephamycin), cefotiam, cefachlor, cefuroxime, and ceforanide. These agents are generally active against both gram-positive and gram-negative bacteria. Moreover, they are relatively resistant to beta-lactamases compared with first-generation drugs. They are not effective against Enterococcus spp, Salmonella spp, methicillin-resistant Staphylococcus spp, P aeruginosa (with the frequent exception of cefoxitin), Actinobacter spp, and many obligate anaerobes (again, cefoxitin is an exception).
The third-generation cephalosporins include ceftiofur, ceftriaxone, cefsulodin, cefotaxime, cefoperazone, moxalactam (not a true cephalosporin), and several others, including cefpodoxime and cefovecin, approved for use in dogs and for use in dogs and cats, respectively. Cefepime is a fourth-generation cephalosporin. The spectrum of third- and fourth-generation cephalosporins varies and should be confirmed based on bacteriologic culture and antimicrobial susceptibility testing before use. The spectrum of veterinary third-generation cephalosporins should not be considered extended in that efficacy often does not include Pseudomonas or other problematic coliforms.
Ceftiofur is a third-generation cephalosporin with a gram-negative spectrum that is more similar to that of first-generation cephalosporins. Ceftiofur has been specifically approved for use in cattle with bronchopneumonia, especially if due to Mannheimia haemolytica or Pasteurella multocida. Although it is approved for use in dogs to treat urinary tract infections (injectable), other more convenient drugs are generally used. Cefpodoxime and cefovecin are particularly effective against Staphylococcus pseudintermedius, yet retain fair efficacy toward gram-negative organisms such as E coli, Klebsiella, and Proteus.
Some drugs approved for use in people have only moderate activity against gram-positive bacteria (again, enterococci are resistant) but have extensive activity against a wide variety of gram-negative bacteria, including Pseudomonas spp, Proteus vulgaris, Enterobacter spp, and Citrobacter spp (eg, cefotaxime and ceftazidime). Third- and fourth-generation cephalosporins were designed to be increasingly resistant to beta-lactamases. However, differences in chemical structure have been overcome by the formation of extended-spectrum beta-lactamases that target third- and fourth-generation drugs (but not, as a general rule, cephamycins).
The physical and chemical properties of the cephalosporins are similar to those of the penicillins, although the cephalosporins are somewhat more stable to pH and temperature changes. Cephalosporins are weak acids derived from 7-aminocephalosporanic acid. They are used either as the free base form for PO administration (if acid stable) or as sodium salts in aqueous solution for parenteral delivery (sodium salt of cephalothin contains 2.4 mEq of sodium/g). Cephalosporins also contain a beta-lactam nucleus susceptible to beta-lactamase (cephalosporinase) hydrolysis. These beta-lactamases may or may not also target penicillins. Modifications of the 7-aminocephalosporanic acid nucleus and substitutions on the side chains via semisynthetic means have produced differences among cephalosporins in antibacterial spectra, beta-lactamase sensitivities, and pharmacokinetics.
Extended-spectrum beta-lactamases (ESBLs) have been increasingly identified in a number of bacteria, mainly Enterobacteriaceae(including E coli) and Klebsiella spp; however, ESBL production has also been increasing in Salmonella spp. The ESBLs are plasma-mediated enzymes that hydrolyze the oxyimino side chain on extended-spectrum cephalosporins, including third- and fourth-generation drugs such as cefotaxime, ceftriazone, and ceftazidime. Plasmids encoding ESBL genes also often encode for other resistance genes that may affect other classes of antimicrobials. The presence of ESBLs can be determined on susceptibility testing based on resistance to these drugs but susceptibility to clavulanic acid, tazobactam, or sulbactam.
Limited information regarding the pharmacokinetics of cephalosporins in animals is available.
Only a few cephalosporins are acid stable and thus effective when administered PO (eg, cephalexin, cephradine, cefadroxil, cefpodoxime, and cefachlor). They are usually well absorbed, and bioavailability is 75%–90% in small animals. Although cefpodoxime has acceptable bioavailability in neonatal foals, older foals and adult horses have poor bioavailability of any of the oral cephalosporins. There is no information regarding bioavailability of human generic products when used in an extralabel fashion in veterinary patients. The others are administered either IV or IM, with plasma concentrations peaking ~30 minutes after injection.
Ceftiofur crystalline-free acid and cefovecin are the two sustained-release formulations approved for veterinary use. Cefovecin is sustained release in small animals due to its intrinsic long elimination half-life, whereas ceftiofur crystalline-free acid is sustained release due to its vehicle.
Cephalosporins are distributed into most body fluids and tissues, including kidneys, lungs, joints, bone, soft tissues, pericardial fluid, and the biliary tract; however, in general, the volume of distribution is < 0.3 L/kg. This low volume of distribution suggests that distribution primarily remains in the extracellular fluid. However, poor penetration into the CSF, even in inflammation, is a notable feature of the standard cephalosporins. Cephalosporins are substrates for P-glycoprotein efflux from the CNS. The third-generation cephalosporins (eg, moxalactam) may achieve good penetration into the CSF.
The degree of plasma-protein binding is variable (eg, 20% for cefadroxil and 80% for cefazolin). The high degree of protein binding of cefovecin (90% in dogs; 99% in cats) contributes to its long elimination half-life (5.5 days in dogs, 6.9 days in cats). However, drug concentrations in transudate remain above the MIC90 of both Staphylococcus intermedius and E coli for up to 14 days. Third- or fourth-generation cephalosporins are often able to penetrate the blood-brain barrier and are frequently indicated in bacterial meningitis due to susceptible pathogens. In general, cephalosporins poorly penetrate the ocular humor.
Several cephalosporins (eg, cephalothin, cephapirin, ceftiofur, cephacetrile, and cefotaxime) are actively deacetylated, primarily in the liver but also in other tissues. The deacetylated derivatives are much less active, with the exception of ceftiofur. Ceftiofur is metabolized to several active metabolites, including an acetylated metabolite (desfuroylceftiofur), that can contribute substantially to efficacy. However, esfuroylceftiofur is less active than ceftiofur against S aureus and Proteus spp. Few of the other cephalosporins are metabolized to any appreciable extent.
Most cephalosporins, including cefpodoxime and cefovecin, are rapidly renally excreted. Tubular secretion predominates, although glomerular filtration is important in some cases (cephalexin and cefazolin). In the case of renal failure, dosages might be decreased, although the need for doing so is not clear because there is a low risk of adverse effects at high concentrations. Biliary elimination of the newer cephalosporins (eg, cefoperazone) may be appreciable. Therefore, hepatic insufficiency may lead to drug accumulation. Generally, these beta-lactam antimicrobials maintain effective blood concentrations for only 6–8 hours. Exceptions include ceftiofur, cefpodoxime, and cefovecin.
![]()
 Рис. 7. Кобель породы шарпей. После удаления слухового прохода наблюдается гнойное отделяемое, несмотря на использование цефтазидима.
Рис. 7. Кобель породы шарпей. После удаления слухового прохода наблюдается гнойное отделяемое, несмотря на использование цефтазидима.
Рис. 8. Та же собака после замены цефтазидима на кобактан для внутривенных инъекций, наблюдается отсутствие гнойного отделяемого.
Таким образом, цефалоспорины IV поколения являются высокоэффективными и перспективными препаратами для лечения собак и кошек. Представляется рациональным более широкое внедрение и использование этих средств в клинической практике.
Цефалоспорины
Цефалоспорины — это природные и полусннтетические антибиотики, полученные на основе 7-аминоцефалоспориновой кислоты. Они обладают широким спектром, антибактериального действия, устойчивостью к действию стафилококковой пенициллиназы, неполной перекрестной аллергией с пенициллинами. Устойчивость бактерий к цефалоспоринам в процессе лечения развивается медленно. На микробную клетку цефалоспорины действуют бактерицидно, по механизму действия, как и пенициллины, относятся к ингибиторам синтеза клеточной стенки бактерий.
Из культуральной жидкости гриба Cephalosporium acremonium был выделен первый антибиотик этой группы — цефалоспорин С. В дальнейшем были получены полусинтетические антибиотики (цефалотин, цефалоридин, цефалексин, цефалоглицин, цефрадин, цефазолин, цефанон и др.), более эффективные по сравнению с природными цефалоспоринами.
Для парентерального введения широко используют цефалотин и цефалоридин, а для пероральиого — цефалексин. Цефалотин и цефалексин, выпускаемые отечественной промышленностью, активны в отношении кокков и большинства штаммов кишечной палочки, протея, сальмонелл и других грамотрицательных бактерий:
Цефалоспорины применяют главным образом при сепсисе, респираторных и желудочно-кишечных заболеваниях животных.
Цефалоридин — Cefaloridinum. Синонимы: цепорин, Kefladin, Ceporan.
Кристаллический порошок белого цвета, хорошо растворим в воде. Водные растворы препарата темнеют на свету.
Препарат оказывает бактерицидное действие на грамположительные и грамотрицательные (в том числе пенициллиназообразующие) кокковые микроорганизмы, клостридии, возбудителен сибирской язвы, эшерихий, сальмонелл, шигелл; менее активен в отношении энтерококков; не эффективен против синегнойной палочки, микобактерий, риккетсий, вирусов, простейших, а также большинства штаммов протея и b-лактамазообразующих штаммов грамотрицательных бактерий.
При пероральном применении цефалоридин плохо всасывается, поэтому его применяют только парентерально. При внутримышечном и внутривенном введении хорошо проникает в органы и ткани и удерживается в терапевтических концентрациях до 8 ч. Из организма выводится в основном почками.
Препарат можно использовать при наличии аллергии к пенициллинам. При введении цефалоридина в ряде случаев отмечают нефротоксическое действие.
Цефалоридин вводят внутривенно (микроструйно или капельно) или внутримышечно 3 раза в сутки в дозах на 1 кг массы животного: лошадям и крупному рогатому скоту 10—20 мг, собакам 5—15 мг. При тяжелом течении болезни показано внутривенное введение препарата в дозе 25 мг на 1 кг массы животного 4 раза в сутки.
Цефалотин — Cefalotinum. Синонимы: Cepovenin, Keflin.
Белый кристаллический порошок, хорошо растворим в воде. Спектр антимикробного действия сходен со спектром цефалоридина. Цефалотин не разрушается стафилококковой пенициллиназой, но разлагается под действием пенициллиназы, вырабатываемой грамотрицательными бактериями.
Как и цефалоридин, препарат применяют только парентерально вследствие плохой всасываемости в желудочно-кишечном тракте. Быстрее, чем цефалоридин, выводится из организма, находясь в терапевтической концентрации в крови в течение 3— 4 ч.
Цефалотин в связи с болезненностью при внутримышечном введении вводят главным образом внутривенно 4—6 раз в сутки в следующих дозах: лошадям и крупному рогатому скоту 10—15 мг, собакам 5—10 мг на 1 кг массы животного.
Цефалексин — Cefalexinum. Синонимы: Ceporex, Keflex.
Белый кристаллический, слегка гигроскопичный порошок, растворим в воде.
По спектру антимикробного действия цефалексин не отличается от цефалотина и цефалоридина, однако он устойчив в кислой среде и действует при пероральном применении. Препарат быстро и почти полностью всасывается из желудочно-кишечного тракта, выделяется в значительных количествах с мочой в измененном виде; небольшая часть антибиотика выводится с желчью.
Цефалексин применяют перорально 4 раза в сутки в дозах на 1 кг массы животного: лошадям и крупному рогатому скоту 10—15 мг, собакам 5—12 мг.
Выпускают препараты цефалоспоринов для парентерального введения в герметически закрытых флаконах: цефалоридин — по 0,25, 0,5 и 1 г; цефалотин — по 0,5, 1 и 2 г; цефалексин выпускают в капсулах по 0,25 и 0,5 г.
При применении цефалоспоринов в высших дозах необходим контроль за функцией почек в связи с возможным нефротоксическим действием.
Хранят цефалоспорины по списку Б в сухом, защищенном от света месте при температуре не выше 10°С. Срок годности 2 года.
The cephalosporins, and the closely related cephamycins, are similar to penicillins in several respects, sharing pharmacological group features.
Cephalosporins include cephamycins, which differ from other cephalosporins in that they contain a 7-alpha-methoxy group, which imparts resistance to extended-spectrum beta-lactamases. The early cephalosporins differed mainly with respect to pharmacokinetic characteristics. Whereas penicillins were classified based on source (natural vs semisynthetic) and spectra, cephalosporins are classified by generation (1–4). Later generations are more resistant to beta-lactam destruction and are often characterized by extended but variable spectra.
First-generation cephalosporins include cephaloridine, cephapirin, cefazolin, cephalexin, cephradine, and cefadroxil. Cephalosporins in this group are usually quite active against many gram-positive bacteria but are only moderately active against gram-negative organisms. They are ineffective against Enterococcus spp, Pseudomonas aeruginosa, and methicillin-resistant Staphylococcus. Susceptible gram-negative bacteria include Escherichia coli and Proteus, Klebsiella, Salmonella, Shigella, and Enterobacter spp. Cefazolin is more effective against E coli than cephalexin, to which it is minimally susceptible. Although generally less susceptible to beta-lactamase destruction than penicillins, cephalosporins are susceptible to cephalosporinases and are not as effective against anaerobes as are the penicillins.
Second-generation cephalosporins include cefamandole, cefoxitin (a cephamycin), cefotiam, cefachlor, cefuroxime, and ceforanide. These agents are generally active against both gram-positive and gram-negative bacteria. Moreover, they are relatively resistant to beta-lactamases compared with first-generation drugs. They are not effective against Enterococcus spp, Salmonella spp, methicillin-resistant Staphylococcus spp, P aeruginosa (with the frequent exception of cefoxitin), Actinobacter spp, and many obligate anaerobes (again, cefoxitin is an exception).
The third-generation cephalosporins include ceftiofur, ceftriaxone, cefsulodin, cefotaxime, cefoperazone, moxalactam (not a true cephalosporin), and several others, including cefpodoxime and cefovecin, approved for use in dogs and for use in dogs and cats, respectively. Cefepime is a fourth-generation cephalosporin. The spectrum of third- and fourth-generation cephalosporins varies and should be confirmed based on bacteriologic culture and antimicrobial susceptibility testing before use. The spectrum of veterinary third-generation cephalosporins should not be considered extended in that efficacy often does not include Pseudomonas or other problematic coliforms.
Ceftiofur is a third-generation cephalosporin with a gram-negative spectrum that is more similar to that of first-generation cephalosporins. Ceftiofur has been specifically approved for use in cattle with bronchopneumonia, especially if due to Mannheimia haemolytica or Pasteurella multocida. Although it is approved for use in dogs to treat urinary tract infections (injectable), other more convenient drugs are generally used. Cefpodoxime and cefovecin are particularly effective against Staphylococcus pseudintermedius, yet retain fair efficacy toward gram-negative organisms such as E coli, Klebsiella, and Proteus.
Some drugs approved for use in people have only moderate activity against gram-positive bacteria (again, enterococci are resistant) but have extensive activity against a wide variety of gram-negative bacteria, including Pseudomonas spp, Proteus vulgaris, Enterobacter spp, and Citrobacter spp (eg, cefotaxime and ceftazidime). Third- and fourth-generation cephalosporins were designed to be increasingly resistant to beta-lactamases. However, differences in chemical structure have been overcome by the formation of extended-spectrum beta-lactamases that target third- and fourth-generation drugs (but not, as a general rule, cephamycins).
The physical and chemical properties of the cephalosporins are similar to those of the penicillins, although the cephalosporins are somewhat more stable to pH and temperature changes. Cephalosporins are weak acids derived from 7-aminocephalosporanic acid. They are used either as the free base form for PO administration (if acid stable) or as sodium salts in aqueous solution for parenteral delivery (sodium salt of cephalothin contains 2.4 mEq of sodium/g). Cephalosporins also contain a beta-lactam nucleus susceptible to beta-lactamase (cephalosporinase) hydrolysis. These beta-lactamases may or may not also target penicillins. Modifications of the 7-aminocephalosporanic acid nucleus and substitutions on the side chains via semisynthetic means have produced differences among cephalosporins in antibacterial spectra, beta-lactamase sensitivities, and pharmacokinetics.
Extended-spectrum beta-lactamases (ESBLs) have been increasingly identified in a number of bacteria, mainly Enterobacteriaceae(including E coli) and Klebsiella spp; however, ESBL production has also been increasing in Salmonella spp. The ESBLs are plasma-mediated enzymes that hydrolyze the oxyimino side chain on extended-spectrum cephalosporins, including third- and fourth-generation drugs such as cefotaxime, ceftriazone, and ceftazidime. Plasmids encoding ESBL genes also often encode for other resistance genes that may affect other classes of antimicrobials. The presence of ESBLs can be determined on susceptibility testing based on resistance to these drugs but susceptibility to clavulanic acid, tazobactam, or sulbactam.
Limited information regarding the pharmacokinetics of cephalosporins in animals is available.
Only a few cephalosporins are acid stable and thus effective when administered PO (eg, cephalexin, cephradine, cefadroxil, cefpodoxime, and cefachlor). They are usually well absorbed, and bioavailability is 75%–90% in small animals. Although cefpodoxime has acceptable bioavailability in neonatal foals, older foals and adult horses have poor bioavailability of any of the oral cephalosporins. There is no information regarding bioavailability of human generic products when used in an extralabel fashion in veterinary patients. The others are administered either IV or IM, with plasma concentrations peaking ~30 minutes after injection.
Ceftiofur crystalline-free acid and cefovecin are the two sustained-release formulations approved for veterinary use. Cefovecin is sustained release in small animals due to its intrinsic long elimination half-life, whereas ceftiofur crystalline-free acid is sustained release due to its vehicle.
Cephalosporins are distributed into most body fluids and tissues, including kidneys, lungs, joints, bone, soft tissues, pericardial fluid, and the biliary tract; however, in general, the volume of distribution is < 0.3 L/kg. This low volume of distribution suggests that distribution primarily remains in the extracellular fluid. However, poor penetration into the CSF, even in inflammation, is a notable feature of the standard cephalosporins. Cephalosporins are substrates for P-glycoprotein efflux from the CNS. The third-generation cephalosporins (eg, moxalactam) may achieve good penetration into the CSF.
The degree of plasma-protein binding is variable (eg, 20% for cefadroxil and 80% for cefazolin). The high degree of protein binding of cefovecin (90% in dogs; 99% in cats) contributes to its long elimination half-life (5.5 days in dogs, 6.9 days in cats). However, drug concentrations in transudate remain above the MIC90 of both Staphylococcus intermedius and E coli for up to 14 days. Third- or fourth-generation cephalosporins are often able to penetrate the blood-brain barrier and are frequently indicated in bacterial meningitis due to susceptible pathogens. In general, cephalosporins poorly penetrate the ocular humor.
Several cephalosporins (eg, cephalothin, cephapirin, ceftiofur, cephacetrile, and cefotaxime) are actively deacetylated, primarily in the liver but also in other tissues. The deacetylated derivatives are much less active, with the exception of ceftiofur. Ceftiofur is metabolized to several active metabolites, including an acetylated metabolite (desfuroylceftiofur), that can contribute substantially to efficacy. However, esfuroylceftiofur is less active than ceftiofur against S aureus and Proteus spp. Few of the other cephalosporins are metabolized to any appreciable extent.
Most cephalosporins, including cefpodoxime and cefovecin, are rapidly renally excreted. Tubular secretion predominates, although glomerular filtration is important in some cases (cephalexin and cefazolin). In the case of renal failure, dosages might be decreased, although the need for doing so is not clear because there is a low risk of adverse effects at high concentrations. Biliary elimination of the newer cephalosporins (eg, cefoperazone) may be appreciable. Therefore, hepatic insufficiency may lead to drug accumulation. Generally, these beta-lactam antimicrobials maintain effective blood concentrations for only 6–8 hours. Exceptions include ceftiofur, cefpodoxime, and cefovecin.
![]()
Plasma half-lives of cephalosporins are quite variable, being as short as 30–120 minutes but generally longer than those of penicillins. For example, the half-life of the approved cephalexin product in dogs after administration PO is 7.3 hours (9 hours if given with food). Third-generation cephalosporins tend to have longer plasma half-lives in people; however, this is not always the case in other animals—substantial species differences exist. A selection of pharmacokinetic values for cephalosporins is listed in the table Elimination, Distribution, and Clearance of Cephalosporins Elimination, Distribution, and Clearance of Cephalosporins ![]() to serve as a guide. Dosage modifications are often required in hepatic and renal disease.
to serve as a guide. Dosage modifications are often required in hepatic and renal disease.
First-generation cephalosporins have proved useful, particularly for infections involving Staphylococcus spp (eg, oral cephalexin for dermatitis) and for surgical prophylaxis (eg, cefazolin). However, their efficacy appears to be declining because of emerging resistance, including methicillin-resistant organisms. Ceftiofur is approved for use in a variety of production animals. It is approved for bovine respiratory disease principally due to Pasteurella spp and in urinary tract infections in dogs. Use of ceftiofur for treatment of soft-tissue infections in dogs is not recommended because proper dosages and safety have not been documented. Cefpodoxime (PO) has been approved for use in dogs, and cefovecin (SC) has been approved for use in dogs and cats.
Cephalosporins are particularly useful to treat infections of soft tissue and bone due to bacteria that are resistant to other commonly used antimicrobials. Cefazolin (IV) has been administered prophylactically 1 hour before surgery. More than most penicillins, cephalosporins may penetrate tissues and fluids sufficiently (CSF being an exception for most) to be effective in management of osteomyelitis, prostatitis, and arthritis.
Orally administered cephalosporins can be effective in management of urinary tract infections, except those due to P aeruginosa. Cephalexin should be anticipated to be ineffective against E coli. Cephapirin benzathine is used for dry-cow treatment, and cephapirin sodium is used to treat mastitis in lactating cattle. Except for cephapirin, extralabel use of cephalosporins is prohibited in major food-producing animal species (cattle, swine, chickens, and turkeys). Although not expressly prohibited in minor food-producing animal species, cephalosporins should be viewed as restricted-class antimicrobials due to their critical importance in human medicine.
![]()
A selection of general dosages for some cephalosporins is listed in Dosages of Cephalosporins Dosages of Cephalosporins ![]() . The dose rate and frequency should be adjusted as needed for the individual animal.
. The dose rate and frequency should be adjusted as needed for the individual animal.
The approved cephalosporins are relatively nontoxic and have a relatively high therapeutic index. Cephalosporins injections IM can be painful, and repeated IV administration may lead to local phlebitis. Nausea, vomiting, and diarrhea may occasionally occur. Antimicrobial-induced colitis due to perturbations in GI flora has been reported. Hypersensitivity reactions of several forms have occurred, with cross-reactivity to penicillin allergies possible. Superinfection may arise with the use of cephalosporins, and Pseudomonas or Candida spp are likely opportunistic pathogens. Cephalosporins do have nephrotoxic potential via immune complex deposition in the glomerular basement membrane or direct toxicity causing acute tubular necrosis; however, these effects are rarely seen at clinically relevant doses.
In vitro incompatibilities are quite common for cephalosporin and cephamycin preparations; an exception exists when mixing with weak bases such as aminoglycosides. Potential pharmacokinetic interactions are similar to those of the penicillin group. Cephalosporins can be synergistic against a number of pathogens.
Several laboratory determinations may be altered by the cephalosporins. Activities of ALP, AST, ALT, and lactate dehydrogenase as well as BUN concentration may be increased. False-positive Coombs test results and urine glucose test results are also possible. Hypernatremia may be caused by the sodium salts of various cephalosporins.
Although prolonged tissue residues for most cephalosporins are not anticipated, withdrawal times are not available for most of the cephalosporins because they are not approved for use in food-producing animals in most countries. In the US, cephalosporins (excluding cephapirin) are prohibited from extralabel drug use (ELDU) except for indication in major species (cattle, swine, chickens and turkeys). This includes deviations from the approved dose, treatment duration, frequency, or administration route on the product label; the use of a product in an unapproved major species or animal production class; and the use of the product for the purpose of disease prevention. In the US, ELDU is permissible in minor species (including small ruminants, camelids, and game birds). Withdrawal times can vary between products, so it is imperative to follow the label meat and milk withdrawal times for the particular product used.
For instances of permissible ELDU, it is recommended to contact a country-specific advisory program to obtain evidence-based withdrawal recommendations extrapolated from known species pharmacokinetics. In the US, veterinarians may contact the Food Animal Residue Avoidance Databank (FARAD, www.farad.org) for withdrawal recommendations.
Цефалоспорины
Цефалоспорины
— это группа антибиотиков имеющих в
основе своей структуры 7-аминоцефалоспориновую
кислоту. Первый биосинтетический
антибиотик цефалоспорин С был выделен
из грибка Cephalosporium acremonium. Позже были
получены полусинтетические цефалоспорины:
цефалотин, цефалоридин, цефазолин,
цефуроксим, цефатоксим, цефкином и др.
Цефалоспорины обладают широким спектром
антимикробной активности, они не
разрушаются пенициллиназой, поэтому
высокоэффективны в отношении
пенициллиноустойчивых микроорганизмов.
Они проявляют бактерицидное действие
в отношении кокков, эшерихий, сальмонелл
и других гармотрицательных микроорганизмов.
Механизм действия цефалоспоринов
аналогичесн пенициллинам. Они нарушают
биосинтез клеточной мембраны (угнетают
активность фермента транспептидазы).
Применяют цефалоспорины при различной
респираторной, желудочно-кишечной
патологии заразного и незаразного
происхождения. При применении
цефалоспоринов могут развиваться
аллергические реакции: нефро- и
нейротокисческое действие. Противопоказаны
беременным животным.
Цефалотина
натриевая соль — Cephalotinum natrium (кефлин,
цефалотин, цепорацин и др.).
Белый кристаллический
порошок, хорошо растворимый в воде.
Форма
выпуска. В
герметически закрытых флаконах по 0,5;
1 и 2 г.
Хранение.
Список “Б”. В сухом затемненном месте
при комнатной температуре.
Действие.
К цефалотину чувствительны большинство
грамположительных и грамотрицательных
микроорганизмов. Устойчив к пенициллиназе.
Хорошо всасывается при внутримышечном
введении, в организме задерживается
4-6 часов.
Применение.
При гнойно-воспалительной патологии,
сепсисе, перитоните, инфекциях дыхательной,
мочевыводящей систем и др. Назначают
внутримышечно, иногда внутривенно в
дозах (мг/кг) лошади и КРС — 10-15; собакам
— 5-10, четыре раза в сутки.
Цефалексин
-Сephalexinum (цепорекс, цефаксин,цефлон,
кефлекс и др.).
Белый
с желтоватым оттенком порошок со
специфическим запахом, плохо растворим
в воде, нерастворим в спирте.
Форма
выпуска.
Капсулы по 0,25 г ; по 35 г в банках из
оранжевого стекла емкостью 150 мл. В
каждой банке содержится 1,5 г активного
вещества.
Хранение.
Список “Б”. В сухом темном месте при
комнатной температуре. Приготовленную
водную суспензию при комнатной температуре
— 6 дней, в холодильнике — 14 дней.
Действие.
Широкий спектр действия. Оказывает
бактерицидное действие на грамположительные
и грамотрицательные микроорганизмы:
стрептококки, пневмококки, менингококки,
гонококки, эшерихии, сальмонеллы, шигеллы
и др. Кислотоустойчив, хорошо всасывается
при энтеральном введении (через 1,5-2
часа), в организме задерживается 6-8
часов, выводится с мочой.
Применение.
При острой и хронической респираторной
патологии, болезнях мочевыводящей
системы (циститы, нефриты, пиелиты и
т.д.), инфекциях кожи и мягких тканей
(пиодермии, фурункулезы, абсцессы,
флегмоны и др.) и другой патологии.
Назначают энтерально в форме капсул
или водной суспензии четыре раза в сутки
в дозах (мг/кг): лошадям и крупному
рогатому скоту — 10-15, овцам, козам, свиньям
— 8-12; собакам — 5-12 мг/кг.
Цефалоридин —
Cephaloridinum (цепорин, цефлорин и др.).
Белый
кристаллический порошок, хорошо
растворимый в воде. Растворы
светочувствительны.
Форма
выпуска.
Порошок во флаконах по 0,25; 0,5 и 1 г.
Хранение.
Список “Б”. В темном месте при температуре
не выше +100С.
Действие.
Бактерицидно на кокковые формы
микрорганизмов (стафилококки, пневмококки,
стрептококки, менингококки, гонококки),
сибироязвенную палочку, спирохеты,
лептоспиры и др. При энтеральном введении
не всасывается. После парентерального
введения быстро всасывается, в организме
удерживается 8 часов, выводится с мочой.
Применение.
При острой и хронической патологии
дыхательной и мочевыводящей систем,
сепсисе, инфекциях кожи, мышц и др.
Назначают внутримышечно, иногда
внутривенно 3 раза в сутки в дозах (мг/кг
массы): лошадям и крупному рогатому
скоту 10-20, овцам, козам, свиньям — 10-20,
собакам 5-15 мг/кг.
Кобактан 2,5% —
Cobactan 2,5%.
Маслянистая
суспензия. В 1 мл содержит 25 мг цефкинома
(действующее начало).
Форма
выпуска.
Флаконы по 50 мл.
Хранение.
Список “Б”. В сухом темном месте при
температуре от +2 до +250С.
Срок хранения 3 года.
Действие.
Кобактан проявляет широкий спектр
действия как на грамположительные, так
и на грамотрицательные бактерии, в том
числе пастереллы, эшерихии, сальмонеллы,
стрептококки, клостридии и др.
Применение.
При желудочно-кишечной и респираторной
патологии заразного и незаразного
происхождения. Назначают внутримышечно
1 раз в сутки в дозе 2 мл препарата на 50
кг массы животного.
Цефотaксим —
Сefоtaxim (кофоран, цефотакс, хемцеф).
Белый, с желтоватым
оттенком порошок, хорошо растворяется
в воде.
Форма
выпуска.
Порошок во флаконах по 0,5; 1 и 2 г.
Хранение.
Список “Б”. В сухом темном месте.
Действие.
Бактерицидное на грамположительные и
гармотрицательные микроорганизмы.
Хорошо всасывается при внутримышечном
введении, проникает в плевральную,
перитониальную и др. полости. Терапевтическая
концентрация сохраняется 12 часов.
Применение.
При болезнях дыхательной, мочевыводящей
систем, гинекологических заболеваниях,
менингитах, плевритах, перитонитах и
др. Назначают внутримышечно 2 раза в
сутки в дозах (мг/кг): лошадям и КРС —
8-12; овцам, козам, свиньям — 10-15, собакам
и кроликам — 15-20 мг/кг.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #

