Один флакон содержит: действующего вещества – цефепима –1 г (в виде цефепима гидрохлорида и L-аргинина).
Порошок от белого до светло-желтого цвета.
Прочие β-лактамные антибиотики. Цефалоспорины IV поколения.
Код АТХ: J01DЕ01.
Фармакодинамика
Механизм действия
цефепима основан на нарушении синтеза бактериальной клеточной стенки (в фазе роста) путём ингибирования пенициллин-связывающих протонов (ПСП) таких как транспептидазы. Это приводит к бактерицидному эффекту.
Активен в отношении грамположительных аэробов:
Staphylococcus aureus и Staphylococcus epidermidis (только метициллиночувствительные штаммы)
Staphylococcus saprophyticus
Streptococcus pyogenes (группа A)
Streptococcus agalactiae (группа В)
Streptococcus pneumoniae
Streptococcus viridans
Грамотрицательных аэробов
Enterobacter spp. (в т.ч. Enterobacter cloacae, Enterobacter aerogenes, Enterobacter agglomerans и Enterobacter sakazakii)
Proteus mirabilis
Proteus vulgaris
Acinetobacter calcoaceticus подгруппа Iwoffii
Acinetobacter pittii
Citrobacter diversus
Citrobacter freundii
Haemophilus ducreyi
Haemophilus influenzae (включая штаммы, продуцирующие β-лактамазу)
Hafnia alvei
Morganella morganii
Moraxella catarrhalis (включая штаммы, продуцирующие β-лактамазы)
Providencia rettgeri
Providencia stuartii
Serratia marcescens
Serralia liquifaciens.
Виды микроорганизмов, которые могут приобретать устойчивость
Аэробные грамположительные микроорганизмы
Staphylococcus aureus*
Staphylococcus epidermidis+
Staphylococcus haemolyticus+
Staphylococcus hominis+
Аэробные грамотрицательные микроорганизмы
Acinetobacter baumannii
Enterobacter cloacae
Escherichia coli%
Klebsiella oxytoca%
Klebsiella pneumonia%
Pseudomonas aeruginosa
Устойчивые виды
Аэробные грамположительные микроорганизмы
Enterococcus spp.
Listeria monocytogenes
Staphylococcus aureus (метициллин-резистентный)
Аэробные грамотрицательные микроорганизмы
Legionella spp.
Stenotrophomonas maltophilia
Анаэробные микроорганизмы
Bacteroides fragilis
Clostridium difficile
Другие микроорганизмы
Chlamydia spp.
Chlamydophila spp.
Mycoplasma spp.
Примечания:
*— в амбулаторной практике уровень резистентности составляет <10%;
+ — по меньшей мере, в одной области, уровень резистентности составляет более 50%;
% — все штаммы, продуцирующие бета-лактамазы расширенного спектра, устойчивы.
Большинство изолятов энтерококков, например, Enterococcus faecalis и устойчивых к метициллину стафилококков, устойчивы к цефепиму. Цефепим неактивен против многих изолятов Stenotrophomonas maltophilia.
Фармакокинетика
Фармакокинетика цефепима линейная в диапазоне от 250 мг до 2 г. Кумуляции препарата у здоровых взрослых добровольцев мужского пола при применении средних терапевтических доз в течение 9 дней не наблюдалось.
Абсорбция
Средние концентрации цефепима в плазме у здоровых взрослых добровольцев мужского пола после однократной 30-минутной инфузии (в/в) цефепима 500 мг, 1 г и 2 г наблюдались в разное время (см. Таблицу 1).
После внутримышечного применения цефепим полностью абсорбируется. Средние концентрации цефепима в плазме в разное время после однократной внутримышечной инъекции приведены в Таблице 2. Фармакокинетика линейна в диапазоне от 500 мг до 2 г внутримышечно и остается неизменной вне зависимости от продолжительности лечения.
Таблица 1
|
Средние концентрации цефепима в плазме в мкг/мл и фармакокинетические параметры (± стандартное отклонение) после внутривенного введения |
|||
|
Параметры |
Цефепим (в мкг/мл) после внутривенного введения |
||
|
500 мг |
1000 мг |
2000 мг |
|
|
0,5 ч |
38,2 |
78,7 |
163,1 |
|
1,0 ч |
21,6 |
44,5 |
85,8 |
|
2,0 ч |
11,6 |
24,3 |
44,8 |
|
4,2 ч |
5,0 |
10,5 |
19,2 |
|
8,0 ч |
1,4 |
2,4 |
3,9 |
|
12,0 ч |
0,2 |
0,6 |
1,1 |
|
Сmax, мкг/мл |
39,1 (3,5) |
81,7 (5,1) |
163,9 (25,2) |
|
AUC, ч·мкг/мл |
70,8 (6,7) |
148,5 (15,1) |
284,8 (30,3) |
Таблица 2
|
Средние концентрации цефепима в плазме в мкг/мл и фармакокинетические параметры (± стандартное отклонение) после внутримышечного введения |
|||
|
Параметры |
Цефепим (в мкг/мл) после внутримышечного введения |
||
|
500 мг |
1000 мг |
2000 мг |
|
|
0,5 ч |
8,2 |
14,8 |
36,1 |
|
1,0 ч |
12,5 |
25,9 |
49,9 |
|
2,0 ч |
12,0 |
26,3 |
51,3 |
|
4,2 ч |
6,9 |
16 |
31,5 |
|
8,0 ч |
1,9 |
4,5 |
8,7 |
|
12,0 ч |
0,7 |
1,4 |
2,3 |
|
Сmax, мкг/мл |
13,9 (3,4) |
29,6 (4,4) |
57,5 (9,5) |
|
Тmax, мкг/мл |
1,4 (0,9) |
1,6 (0,4) |
1,5 (0,4) |
|
AUC, ч·мкг/мл |
60,0 (8,0) |
137,0 (11,0) |
262,0 (23,3) |
Распределение
Объем распределения цефепима в равновесном состоянии составляет 18 (±2) л. Связывание с белками сыворотки крови составляет около 20% и не зависит от концентрации цефепима в сыворотке крови. Цефепим выделяется с грудным молоком. Новорожденный на грудном вскармливании, потребляющий примерно 1000 мл грудного молока в день, может получить примерно 0,5 мг цефепима в день.
Цефепим проникает через воспаленный гематоэнцефалический барьер. В настоящее время клиническая значимость этих данных является неопределённой.
Метаболизм и выведение
Цефепим метаболизируется до N-метилпирролидина (NMP), который быстро преобразовывается в N-оксид (NMP-N-оксид). Примерно 85 % дозы выводится с мочой в неизменном виде. Менее 1% дозы – в виде
N-метилпирролидина, 6,8 % — NMP-N-оксида и 2,5 % в виде эпимера цефепима. Выведение цефепима осуществляется путем почечной экскреции со средним (± SD) периодом полувыведения 2 (± 0,3) часа и общим клиренсом
120 (±  мл/мин у здоровых добровольцев. Поскольку почечная экскреция является основным способом выведения, у пациентов с нарушением функции почек и пациентов, находящихся на гемодиализе, требуется коррекция дозы.
мл/мин у здоровых добровольцев. Поскольку почечная экскреция является основным способом выведения, у пациентов с нарушением функции почек и пациентов, находящихся на гемодиализе, требуется коррекция дозы.
Почечная недостаточность: средний период полувыведения у пациентов, нуждающихся в гемодиализе, составил 13,5 (± 2,7) часов и у пациентов, нуждающихся в непрерывном перитонеальном диализе, 19 (± 2) часов. Общий клиренс цефепима снижался пропорционально клиренсу креатинина у пациентов с нарушенной функцией почек, что служит основанием для коррекции дозы в этой группе пациентов.
Печеночная недостаточность: фармакокинетика цефепима не изменяется у пациентов с печеночной недостаточностью при применении разовой дозы в 1 г.
Пациенты пожилого возраста: фармакокинетика цефепима у пациентов пожилого возраста (65 лет и старше) мужского и женского пола, у которых средний (SD) клиренс креатинина был 74 (± 15) мл/мин характеризуется снижением общего клиренса цефепима в зависимости от клиренса креатинина. Таким образом, доза цефепима у пациентов пожилого возраста должна быть скорректирована по мере необходимости, если клиренс креатинина составляет 50 мл/мин или менее.
Дети: фармакокинетика цефепима у детей в возрасте от 1 месяца до 11 лет: после применения разовой и многократной дозы каждые 8 часов и каждые 12 часов общий клиренс и объем распределения в равновесном состоянии составляли в среднем 3,3 (± 1) мл/мин/кг и 0,3 (± 0,1) л/кг, соответственно. Выведение с мочой в неизмененном виде составило 60,4 (± 30,4) % от дозы, а средний почечный клиренс 2 (± 1,1) мл/мин/кг. Ни возраст, ни пол на общий клиренс и объем распределения с поправкой на массу тела не влияли. Кумуляции препарата не наблюдалось при применении 50 мг/кг каждые 12 часов, в то время как Cmax, AUC и Тmах увеличились примерно на 15 % в равновесном состоянии после применения 50 мг на кг каждые 8 часов. Доза в 50 мг/кг внутривенно у детей сравнима с дозой в 2 г внутривенно у взрослых. Абсолютная биодоступность цефепима после применения дозы в 50 мг/кг внутримышечно составила 82,3 (± 15) % у восьми пациентов.
Взрослые
Лечение инфекций, вызванных чувствительными штаммами соответствующих микроорганизмов:
— пневмония (от умеренной до тяжелой), вызванная Streptococcus pneumoniae, включая случаи с одновременной бактериемией, Pseudomonas aeruginosa, Klebsiella pneumonia или Enterobacter species;
— эмпирическая терапия пациентов с нейтропенической лихорадкой. Цефепим в качестве монотерапии показан для эмпирического лечения пациентов с фебрильной нейтропенией. У пациентов с высоким риском тяжелой инфекции (в том числе у пациентов с недавно перенесённой трансплантацией костного мозга в анамнезе (данных в поддержку эффективности монотерапии цефепимом у этих пациентов недостаточно; если необходимо, рекомендуется комбинированная терапия с антибиотиками из группы аминогликозидов или гликопептидов с учётом индивидуального профиля риска пациента), гипотонией, гематологической злокачественной опухолью, тяжелой или длительной нейтропенией) — в составе комбинированной терапии;
— неосложненные и осложненные инфекции мочевыводящих путей (в том числе пиелонефрит), вызванные Escherichia coli или Klebsiella pneumoniae, любой степени тяжести, а также легкие и умеренно тяжелые инфекции, вызванные Proteus mirabilis, включая случаи, связанные с одновременной бактериемией этими микроорганизмами;
— неосложнённые инфекции кожи и ее структур, вызванные Staphylococcus aureus (только метициллин-чувствительные штаммы) или Streptococcus pyogenes;
— осложнённые интраабдоминальные инфекции (в сочетании с метронидазолом), вызванные Echerichia coli, стрептококками группы viridens, Pseudomonas aeruginosa, Klebsiella pneumoniae, Enterobacter species или Bacteroides fragilis.
Дети
Инфекции, вызванные микроорганизмами, чувствительными к цефепиму:
— бактериемия, связанная с одной из упомянутых инфекций, или предположительно связанная;
— тяжёлая пневмония;
— тяжёлые инфекции мочевыводящих путей;
— бактериальный менингит;
— эмпирическое лечение фебрильных эпизодов у пациентов с умеренной (нейтрофилы < 1000/мм3) или тяжёлой (нейтрофилы ≤ 500/мм3) нейтропенией. У пациентов с высоким риском серьёзной инфекции (например, у пациентов с недавней трансплантацией костного мозга, низким начальным артериальным давлением, онкогематологическими заболеваниями или тяжёлой, или длительной нейтропенией) антимикробная монотерапия не применима. Имеющиеся данные по эффективности монотерапии цефепимом у таких пациентов недостаточны. Если необходимо, рекомендуется комбинированная терапия с антибиотиком из группы аминогликозидов или гликопептидов с учётом индивидуального профиля риска пациента.
Чтобы уменьшить развитие лекарственноустойчивых бактерий и поддерживать эффективность Цефепима и других антибактериальных препаратов, лекарственное средство следует использовать только для лечения инфекций, которые вызваны чувствительными бактериями. Когда информация о культуре и восприимчивости доступна, препарат следует использовать только для лечения инфекций, которые вызваны чувствительными бактериями. При отсутствии таких данных выбору эмпирической терапии могут способствовать эпидемиологические данные.
Повышенная чувствительность к цефепиму или L-аргинину, а также к цефалоспориновым антибиотикам, пенициллинам или другим β-лактамным антибиотикам. Детский возраст до 1 месяца.
Дозы и способ введения препарата зависят от чувствительности возбудителя, тяжести инфекции, функции почек и общего состояния пациента.
Рекомендации относительно дозирования лекарственного средства приведены в таблице 1.
Таблица 1. Дозирование у пациентов с нормальной функцией почек (клиренс креатинина (КК) более 50 мл/мин)
|
Локализация и тип инфекции |
Доза |
Частота |
Продолжитель-ность2 (дни) |
|
Взрослые и дети старше 12 лет (с массой тела более 40 кг) |
|||
|
Пневмония умеренной или тяжелой степени, вызванная S. pneumoniae*, P. aeruginosa1, К. pneumoniae или Enterobacter spp. |
1-2 г в/в |
Каждые 12 ч |
10 |
|
Эмпирическая терапия пациентов с фебрильной нейтропенией |
2 г в/в |
Каждые 8 ч |
7** |
|
Неосложненные или осложненные инфекции мочевых путей, включая пиелонефрит |
0,5-1 г в/в или в/м*** |
Каждые 12 ч |
7-10 |
|
Тяжелые неосложнённые или осложненные инфекции мочевых путей, в том числе пиелонефрит |
2 г в/в |
Каждые 12 ч |
10 |
|
Инфекции кожи и ее структур, вызываемые S. aureus или S.pyogens. |
2 г в/в |
Каждые 12 ч |
10 |
|
Осложнённые интраабдоминальные инфекции (в сочетании с метронидазолом) |
2 г в/в |
8-12 ч |
7-10 |
|
Дети в возрасте от 1 месяца до 12 лет (с массой тела ≤ 40 кг): |
|||
|
Возраст
|
пневмония, осложнённые инфекции мочевыводящих путей. |
Очень тяжёлые инфекции: сепсис, бактериальный менингит, эмпирическое лечение эпизодов фебрильной нейтропении. |
|
|
2 месяца – 12 лет (с массой тела ≤ 40 кг) |
50 мг/кг массы тела каждые 12 часов Серьёзные инфекции: 50 мг/кг массы тела каждые 8 часов |
50 мг/кг массы тела каждые 8 часов |
|
|
Продолжительность: 10 дней 7-10 дней |
|||
|
От 1 до 2 месяцев |
30 мг/кг массы тела каждые 12 часов Серьёзные инфекции: 30 мг/кг массы тела каждые 8 часов |
30 мг/кг массы тела каждые 8 часов |
|
|
Продолжительность: 10 дней 7-10 дней |
* В том числе случаи, связанные с одновременной бактериемией.
** Или до окончания нейтропении. У пациентов со снижением температуры, но нейтропенией более 7 дней, должна быть пересмотрена необходимость продолжения антибактериальной терапии.
*** Внутримышечный путь введения показан только для легкой и умеренной неосложненной или осложненной инфекции мочевыводящих путей, вызванной E. coli.
1 При лечении пневмонии, вызванной P. aeruginosa: 2 г вводить в/в каждые 8 часов.
2 Продолжительность лечения, как правило, составляет от 7 до 10 дней. Максимальная продолжительность в целом – не менее 7, но не более 14 дней. Продолжительность эмпирического лечения фебрильной нейтропении: от 7 дней до исчезновения нейтропении.
Опыт применения у детей в возрасте до 1 месяца ограничен и основывается на расчете доз, исходя из опыта применения дозы 50 мг/кг массы тела, полученной на основании фармакокинетических данных у пациентов старше 1 месяца, что соответствует дозе 30 мг/кг массы тела каждые 12 или 8 часов для детей в возрасте от 1 до 2 месяцев. Дети этого возраста должны тщательно контролироваться во время введения препарата.
У детей с массой тела более 40 кг рекомендуется доза, как для взрослых (смотрите таблицу). У детей старше 12 лет с массой тела менее 40 кг рекомендуется доза, как для детей с массой тела ≤ 40 кг. Максимальная доза у детей не должна превышать максимальную дозу для взрослых (2,0 г каждые 8 часов).
Продолжительность лечения, как правило, составляет от 7 до 10 дней. В целом цефепим рекомендуется применять не менее 7, но не более 14 дней.
При эмпирическом лечении фебрильной нейтропении продолжительность лечения обычно составляет до 7 дней или до окончания нейтропении.
Пациенты с нарушенной функцией почек. Цефепим выводится почками путем клубочковой фильтрации, поэтому больным с нарушениями функции почек (клиренс креатинина (КК) менее 50 мл/мин) дозу Цефепима необходимо откорректировать. У этих пациентов рекомендуемая начальная доза цефепима должна быть такой же, как у пациентов с КК более 50 мл/мин, за исключением пациентов, подвергающихся гемодиализу (таблица 2).
Таблица 2. Рекомендуемые дозы Цефепима для взрослых.
|
КК (мл/мин) |
Интервал приема доз (часы) |
||
|
24 часа |
12 часов |
8 часов |
|
|
> 50 |
500-2000 мг |
2000 мг |
|
|
Коррекция дозы не требуется |
|||
|
30-50 |
500-2000 мг |
500 мг |
|
|
11-29 |
500-1000 мг |
||
|
≤ 10 |
250-500 мг |
||
|
Гемодиализ * |
1000 мг 1 доза, затем по 500 мг |
500 мг |
* В день проведения диализа инъекцию лекарственного средства необходимо выполнять после окончания процедуры диализа.
Если известна только концентрация креатинина в сыворотке крови, тогда КК можно определять по нижеуказанным формулам.
Мужчины: КК (мл/мин) = масса тела (кг)×(140 – возраст) : 72×креатинин плазмы крови (мг/дл).
Женщины: КК (мл/мин) = показатель у мужчин×0,85.
При гемодиализе за 3 ч удаляется приблизительно 68 % дозы препарата. При непрерывном амбулаторном перитонеальном диализе препарат можно применять в исходных рекомендованных дозах – 500 мг, 1 г или 2 г в зависимости от тяжести инфекции с интервалом 48 ч.
У детей при нарушении функции почек рекомендуются изменения режима дозирования, пропорциональные тем, которые принимаются у взрослых, в соответствии с приведённой ниже таблицей.
|
Дети в возрасте от 1 месяца до 12 лет (с массой тела ≤ 40 кг): |
||
|
Клиренс креатинина (мл/мин) |
Тяжёлые инфекции: пневмония, осложнённые инфекции мочевыводящих путей. |
Очень тяжёлые инфекции: сепсис, бактериальный менингит, эмпирическое лечение эпизодов фебрильной нейтропении. |
|
˃ 50 |
50 мг/кг массы тела каждые 12 часов |
50 мг/кг массы тела каждые 8 часов |
|
Регулировка дозы не требуется |
||
|
30 — 50 |
50 мг/кг массы тела каждые 24 часа |
50 мг/кг массы тела каждые 12 часов |
|
11 — 29 |
25 мг/кг массы тела каждые 24 часа |
50 мг/кг массы тела каждые 24 часа |
|
≤ 10 |
12,5 мг/кг массы тела каждые 24 часа |
25 мг/кг массы тела каждые 24 часа |
Расчет показателей КК у детей
КК (мл/мин/1,73 м2) = 0,55×рост (см): креатинин плазмы крови (мг/дл) или
КК (мл/мин/1,73 м2) = 0,52×рост (см): креатинин плазмы крови (мг/дл) −3,6.
Цефепим после восстановления вводят внутримышечно, внутривенно струйно медленно в течение 3-5 мин либо капельно путём инфузии в течение не менее 30 мин.
Приготовление раствора для внутривенного введения
Цефепим восстанавливают одним из следующих растворителей: стерильная вода для инъекций; 0,9 % раствор хлорида натрия для инъекций; 5 % раствор декстрозы для инъекций; стерильная бактериостатическая вода для инъекций с парабенами или бензиловым спиртом в количествах, указанных в таблице 3.
Восстановленный раствор разбавляют одним из следующих совместимых инфузионных растворов для внутривенного введения: 0,9 % раствор хлорида натрия; 5 % и 10 % раствор декстрозы; 5% раствор декстрозы с 0,9 % раствором хлорида натрия; 1/6 М раствор натрия лактата; раствор Рингера лактата; раствор Рингера лактата с 5 % раствором глюкозы.
Приготовление раствора для внутримышечного введения
Цефепим восстанавливают одним из следующих растворителей: стерильная вода для инъекций; 0,9 % раствор хлорида натрия для инъекций; 5 % раствор декстрозы для инъекций; стерильная бактериостатическая вода для инъекций с парабенами или бензиловым спиртом в количествах, указанных в таблице 3.
|
Путь введения |
Объем раствора для разведения (мл) |
Приблизительный объем полученного раствора (мл) |
Приблизительная концентрация Цефепима (мг/мл) |
|
В/в введение: |
|||
|
1 г/флакон |
10 |
11,4 |
90 |
|
В/м введение: |
|||
|
1 г/флакон |
3 |
4,4 |
230 |
Восстановленный раствор лекарственного средства может быть от светло-жёлтого до янтарно-жёлтого цвета.
Перед введением приготовленного раствора лекарственного средства необходимо убедиться, что раствор является прозрачным и не содержит нерастворённых частиц.
Имеются литературные данные о физико-химической несовместимости цефепима с метронидазолом, ванкомицином, гентамицином, тобрамицином, нетилмицином и аминофиллином. В связи с отсутствием собственных иссследований совместимости, данное лекарственное средство не следует смешивать с другими лекарственными средствами.
Описанная ниже частота возникновения побочных реакций соответствует шкале: очень часто ≥ 1/10; часто: ≥1/100 и <1/10; нечасто: ≥ 1/1000 и <1/100; редко: ≥ 1/10000 и <1/1000; очень редко: <1/10000, частота неизвестна – невозможно оценить на основе имеющихся данных.
Инфекции и инвазии. Нечасто: оральный кандидоз. Редко: неспецифический кандидоз.
Нарушения со стороны крови и лимфатической системы. Очень часто: положительная реакция Кумбса. Часто: анемия. Редко: эозинофилия, нейтропения, тромбоцитопения, лейкопения, снижение гематокрита, панцитопения, пролонгация протромбинового времени и активированного частичного тромбопластинового времени, кровотечения. Частота неизвестна: апластическая анемия, гемолитическая анемия, агранулоцитоз.
Нарушения со стороны иммунной системы. Редко: аллергические реакции, зуд, крапивница и лихорадка. Частота неизвестна: анафилактический шок, ангионевротический отёк.
Нарушения метаболизма и питания. Частота неизвестна: ложноположительная реакция на глюкозу в моче.
Нарушения со стороны нервной системы. Нечасто: головная боль. Редко: судороги, парастезия, изменение вкуса, головокружение. Частота неизвестна: кома, ступор, энцефалопатия, нарушение сознания, миоклонус.
Нарушения со стороны органа слуха и лабиринта. Редко: тиннитус (звон в ушах).
Нарушения со стороны сердца. Очень редко: артериальная гипотензия.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения. Очень редко: одышка.
Нарушения со стороны сосудов. Очень редко: вазодилатация.
Желудочно-кишечные нарушения. Часто: диарея. Нечасто: тошнота, рвота, стоматит. Очень редко: боль в животе, колит, псевдомембранозный колит, запор, диспепсия, язвы в полости рта.
Нарушения со стороны печени и желчевыводящих путей. Редко: умеренное и преходящее повышение уровня трансаминаз (АсТ, АлТ), увеличение билирубина в сыворотке крови, нарушения функций печени, включая холестаз.
Нарушения со стороны кожи и подкожной клетчатки. Часто: сыпь. Нечасто: эритема, крапивница, кожный зуд. Редко: отек, аллергические реакции, эритема. Частота неизвестна: токсический эпидермальный некролиз, синдром Стивенса-Джонсона, эритема многоформная.
Нарушения со стороны костно-мышечной системы и соединительной ткани. Очень редко: боль в суставах.
Нарушения со стороны почек и мочевыводящей системы. Редко: увеличение мочевины, креатинина в сыворотке крови, токсическая нефропатия, почечная недостаточность.
Нарушения со стороны репродуктивной системы и молочной железы. Очень редко: вагинит.
Общие нарушения и реакции в месте введения. Нечасто: раздражение в месте введения, флебит и тромбофлебит, боль и воспаление в месте инъекции. Редко: озноб.
Лабораторные и инструментальные данные. Редко: ложноположительная реакция на глюкозу в моче. Очень редко: увеличение щелочной фосфатазы в сыворотке крови, фосфатов, кальция, калия, уменьшение концентрации кальция в сыворотке крови.
Сообщение о нежелательных реакциях. Важно сообщать о подозреваемых нежелательных реакциях после регистрации лекарственного средства с целью обеспечения непрерывного мониторинга соотношения «польза–риск» лекарственного средства. Медицинским работникам рекомендуется сообщать о любых подозреваемых нежелательных реакциях лекарственного средства через национальные системы сообщения.
Возможны случаи повышения активности пероральных антикоагулянтов у пациентов, получающих цефалоспорины.
Применяя высокие дозы аминогликозидов одновременно с Цефепимом, необходимо следить за функцией почек из-за потенциальной нефротоксичности и ототоксичности аминогликозидных антибиотиков. Нефротоксичность отмечалась после одновременного применения других цефалоспоринов с сильнодействующими диуретиками (такими как фуросемид).
Перед началом лечения Цефепимом следует тщательно собрать анамнез с целью определения наличия у пациента реакции гиперчувствительности к Цефепиму или любому другому препарату группы цефалоспоринов, пенициллинов или β-лактамных антибиотиков. При наличии сомнений необходимо присутствие врача при первом введении для принятия неотложных мер в случае возникновения анафилактической реакции. При возникновении аллергических реакций необходимо прекратить введение препарата. Рекомендуется соблюдать особую осторожность при необходимости введения цефепима пациентам с бронхиальной астмой или любыми аллергическими реакциями в анамнезе.
Нарушения функций почек
У пациентов с почечной недостаточностью (клиренс креатинина ≤ 50 мл/мин) или другими факторами, которые влияют на функцию почек, доза цефепима должна быть скорректирована, чтобы компенсировать более медленный клиренс лекарственного средства почками. Поскольку у пациентов с нарушениями функций почек или другими факторами, которые влияют на функции почек, при обычных дозах уровень цефепима в сыворотке может быть высоким и сохраняться длительно, у них поддерживающая доза должна быть уменьшена. Во время постмаркетинговых наблюдений были зарегистрированы серьёзные побочные эффекты в виде обратимой энцефалопатии (расстройства сознания со спутанностью сознания, галлюцинациями, ступором и комой), афазия, миоклонус, судороги и бессудорожный эпилептический статус и/или почечная недостаточность. В большинстве случаев энцефалопатия наблюдалась у пациентов с почечной недостаточностью, которые получали дозы цефепима выше рекомендуемых. Обычно нейротоксичсеике симптомы проходили после прекращения лечения цефепимом или после гемодиализа, но были случаи со смертельным исходом.
Если происходит нейротоксичность, связанная с терапией цефепимом, прекратите применение цефепима и примите соответствующие меры. При развитии суперинфекций во время лечения необходимо принять соответствующие меры.
Многие цефалоспорины, включая цефепим, были связаны с уменьшением активности протромбина. К группам риска относятся пациенты с почечной или печёночной недостаточностью или плохим состоянием питания, а также пациенты, получающие длительный курс антимикробной терапии. У пациентов с факторами риска следует контролировать протромбиновое время и применять экзогенный витамин К по мере надобности.
Влияние на результаты лабораторных исследований
При проведении анализа мочи на глюкозурию возможен ложноположительный результат. Цефалоспорины склонны абсорбироваться на поверхности эритроцитов и вступать в реакцию с антителами, направленными против препаратов, результатом чего является положительный тест Кумбса.
Пациентам, у которых развивается гемолитическая анемия, следует прекратить введение препарата и провести соответствующую терапию. Положительный тест Кумбса может наблюдаться у новорожденных, чьи матери получали антибиотики группы цефалоспоринов до родов.
Длительное применение Цефепима может приводить к колонизации нечувствительной микрофлорой. При развитии суперинфекций во время лечения необходимо принять соответствующие меры.
В случае появления диареи на фоне лечения, следует учитывать возможность развития антибиотик-ассоциированной диареи, в том числе псевдомембранозного колита, диагностика которого основывается на данных колоноскопии. Легкие формы колита не требуют назначения симптоматической терапии; умеренные или тяжелые случаи могут потребовать специального лечения. Антибиотик-ассоциированная диарея может наблюдаться в течение двух и более месяцев после применения антибактериальных препаратов. Если такой диагноз подозревается, следует прекратить терапию цефепимом и начать соответствующее лечение.
Целесообразно следить за функцией почек при одновременном применении Цефепима с потенциально нефротоксичными антибиотиками (особенно аминогликозидами) и сильными диуретиками.
Антибактериальная активность цефепима
Из-за относительно ограниченного спектра антибактериальной активности, цефепим не подходит для лечения некоторых видов инфекций, особенно когда возбудитель ещё не установлен и не определена чувствительность выявленных микроорганизмов к цефепиму. По крайней мере, должна быть очень высокая вероятность того, что цефепим подходит для лечения данной инфекции.
Исследования на животных не установили наличие прямого или косвенного вредного влияния на течение беременности, развитие эмбриона, плода и постнатальное развитие потомства. Потенциальный риск для людей не известен. Цефепим проникает через плацентарный барьер. Клинических данных о применении Цефепима женщинами в период беременности недостаточно. Цефепим беременным можно назначать только тогда, когда ожидаемая польза для матери превышает потенциальный риск для плода. В малых концентрациях Цефепим проникает в грудное молоко. Поэтому при назначении Цефепима кормление грудью необходимо прекратить.
Исследований о влиянии на способность управлять транспортными средствами и другими механизмами не проводилось. Следует иметь в виду потенциальные побочные эффекты, такие как нарушение сознания, головокружение, спутанность сознания или галлюцинации, которые могут повлиять на способность управлять транспортными средствами и другими механизмами. Пациентам рекомендуется соблюдать осторожность и не управлять транспортом или другими сложными механизмами.
Безопасность и эффективность цефепима при лечении неосложненных и осложненных инфекций мочевыводящих путей (включая пиелонефрит), неосложненных инфекций кожи и мягких тканей, пневмонии, а также при эмпирическом лечении пациентов с нейтропенической лихорадкой была подтверждена в отношении детей в возрасте от 1 месяца до 16 лет. Применение Цефепима в этих возрастных группах обосновано результатами адекватных и хорошо контролируемых исследований применения цефепима у взрослых и дополнительными данными касательно фармакокинетики и безопасности, полученными в ходе исследований с участием детей.
Безопасность и эффективность применения у детей в возрасте до 1 месяца не изучена. Существует недостаточное количество клинических данных, подтверждающих целесообразность применения Цефепима у детей в возрасте до 1 месяца или для лечения тяжелых инфекций у детей в случаях, где подозреваемым или установленным возбудителем является Haemophilus influenzae типа b.
У пациентов с менингитом, у которых инфекция распространяется из удаленного очага, или у пациентов с подозреваемым или диагностированным менингитом, должен применяться альтернативный препарат с доказанной клинической эффективностью.
В ходе клинических исследований Цефепим применяли у более 6400 взрослых пациентов (35 % старше 65 лет, и 16 % 75 лет и старше). При применении обычной рекомендуемой дозы для взрослых клиническая эффективность и безопасность препарата были сопоставимы с таковыми у взрослых пациентов, не относящихся к пожилому и старческому возрасту.
Серьезные нежелательные явления наблюдались у пациентов пожилого возраста с почечной недостаточностью, у которых коррекция доз цефепима не осуществлялась, в том числе сообщалось об опасных для жизни или смертельных случаях, включая: энцефалопатию, миоклонус и судороги.
Препарат, как известно, выводится, главным образом, почками, и риск возникновения токсических реакций может быть выше у пациентов с нарушенной функцией почек. В силу того, что у пациентов пожилого возраста ухудшение почечной функции более вероятно, чем у пациентов других групп, следует обратить особое внимание на выбор дозы. Также должен осуществляться постоянный контроль функции почек.
Симптомы. Проявляются в случаях существенного превышения рекомендуемых доз, особенно у больных с нарушенной функцией почек. Симптомы передозировки включают энцефалопатию (нарушения сознания, включая спутанность сознания, галлюцинации, ступор и кому), миоклонус, судороги, нервно-мышечную возбудимость и неконвульсивный эпилептический статус.
Лечение. Необходимо прекратить введение препарата, провести симптоматическую терапию. Применение гемодиализа ускоряет удаление Цефепима из организма; перитонеальный диализ малоэффективен. Тяжелые аллергические реакции немедленного типа требуют применения адреналина и других форм интенсивной терапии.
1,0 г во флаконах из стекла. 1 флакон вместе с листком-вкладышем помещают в пачку из картона (№1).
10 флаконов вместе с листком-вкладышем помещают в пачку из картона с картонным вкладышем (№10).
Для стационаров: 50 флаконов вместе с 2 инструкциями по применению помещают в коробку из картона (№50).
В защищенном от света месте, при температуре не выше 25°С. Хранить в недоступном для детей месте.
2 года. Не использовать по истечении срока годности.
По рецепту.
Информация о производителе
Открытое акционерное общество «Борисовский завод медицинских препаратов», Республика Беларусь, Минская обл., г. Борисов, ул. Чапаева, 64, тел/факс +375(177) 735612, 731156.
Цефепим (Cefepime)
💊 Состав препарата Цефепим
✅ Применение препарата Цефепим
Описание активных компонентов препарата
Цефепим
(Cefepime)
Приведенная научная информация является обобщающей и не может быть использована для принятия
решения о возможности применения конкретного лекарственного препарата.
Дата обновления: 2020.11.24
Владелец регистрационного удостоверения:
Лекарственная форма
| Цефепим |
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 или 50 шт. рег. №: ЛП-001406 |
Форма выпуска, упаковка и состав
препарата Цефепим
1 г — флаконы (1) — пачки картонные.
1 г — флаконы (50) — пачки картонные.
Фармакологическое действие
Цефалоспориновый антибиотик IV поколения для парентерального применения. Оказывает бактерицидное действие, нарушая синтез клеточной стенки микроорганизмов.
Активен в отношении большинства грамотрицательных бактерий, в т.ч. продуцирующих β-лактамазы, включая Pseudomonas aeruginosa. Более активен, чем цефалоспорины III поколения, в отношении грамположительных кокков.
Не активен в отношении Enterococcus spp., Listeria spp., Legionella spp., некоторых анаэробных бактерий (Bacteroides fragilis, Clostridium difficile).
Цефепим характеризуется высокой стабильностью в отношении различных плазмидных и хромосомных β-лактамаз.
Фармакокинетика
Связывание с белками плазмы составляет менее 19% и не зависит от концентрации цефепима в сыворотке крови.
Терапевтические концентрации цефепима обнаруживаются в моче, желчи, перитонеальной жидкости, экссудате волдыря, слизистом секрете бронхов, мокроте, тканях предстательной железы, аппендиксе и желчном пузыре, спинномозговой жидкости при менингите.
У здоровых людей при в/в введении цефепима в дозе 2 г с интервалом 8 ч в течение 9 дней не наблюдалось кумуляции в организме.
Средний T1/2 из организма в среднем составляет около 2 ч, средний общий клиренс — 120 мл/мин. Цефепим выводится почками, главным образом путем клубочковой фильтрации (средний почечный клиренс — составляет 110 мл/мин). В моче обнаруживается приблизительно 85% введенного цефепима в неизмененном виде.
У больных в возрасте 65 лет или старше с нормальной функцией почек величина почечного клиренса меньше, чем у молодых больных.
У больных с нарушениями функции почек увеличивается T1/2. У больных с тяжелыми нарушениями функции почек, при которых требуется проведение гемодиализа, T1/2 в среднем составляет 13 ч, проведение перитонеального диализа — 19 ч.
Фармакокинетика цефепима у больных с нарушением функции печени, муковисцидозом не изменена.
Возраст и пол пациентов не оказывали существенного влияния на общий клиренс из организма и Vd с учетом поправки на массу тела каждого. При введении цефепима в дозе 50 мг/кг каждые 12 ч кумуляции не отмечалось, а при введении в этой же дозе каждые 8 ч в равновесном состоянии Cmax, AUC и T1/2 увеличивались примерно на 15%.
Показания активных веществ препарата
Цефепим
Лечение инфекционно-воспалительных заболеваний, вызванных чувствительными к цефепиму микроорганизмами: инфекции нижних отделов дыхательных путей (включая пневмонию и бронхит), инфекции мочевыводящих путей (как осложненные, так и неосложненные), инфекции кожи и мягких тканей, интраабдоминальные инфекции (включая перитонит и инфекции желчных путей), гинекологические инфекции, септицемия, нейтропеническая лихорадка (в качестве эмпирической терапии), бактериальный менингит у детей.
Профилактика инфекций при проведении полостных хирургических операций.
Открыть список кодов МКБ-10
| Код МКБ-10 | Показание |
| A40 | Стрептококковый сепсис |
| A41 | Другой сепсис |
| D70 | Агранулоцитоз |
| G00 | Бактериальный менингит, не классифицированный в других рубриках |
| J15 | Бактериальная пневмония, не классифицированная в других рубриках |
| J20 | Острый бронхит |
| J42 | Хронический бронхит неуточненный |
| K65.0 | Острый перитонит (в т.ч. абсцесс) |
| K81.0 | Острый холецистит |
| K81.1 | Хронический холецистит |
| K83.0 | Холангит |
| L01 | Импетиго |
| L02 | Абсцесс кожи, фурункул и карбункул |
| L03 | Флегмона |
| L08.0 | Пиодермия |
| L08.8 | Другие уточненные местные инфекции кожи и подкожной клетчатки |
| N10 | Острый тубулоинстерстициальный нефрит (острый пиелонефрит) |
| N11 | Хронический тубулоинтерстициальный нефрит (хронический пиелонефрит) |
| N30 | Цистит |
| N34 | Уретрит и уретральный синдром |
| N41 | Воспалительные болезни предстательной железы |
| N70 | Сальпингит и оофорит |
| N71 | Воспалительная болезнь матки, кроме шейки матки (в т.ч. эндометрит, миометрит, метрит, пиометра, абсцесс матки) |
| N72 | Воспалительная болезнь шейки матки (в т.ч. цервицит, эндоцервицит, экзоцервицит) |
| N73.5 | Тазовый перитонит у женщин неуточненный |
| T79.3 | Посттравматическая раневая инфекция, не классифицированная в других рубриках |
| Z29.2 | Другой вид профилактической химиотерапии (введение антибиотиков с профилактической целью) |
Режим дозирования
Способ применения и режим дозирования конкретного препарата зависят от его формы выпуска и других факторов. Оптимальный режим дозирования определяет врач. Следует строго соблюдать соответствие используемой лекарственной формы конкретного препарата показаниям к применению и режиму дозирования.
Индивидуальный, в зависимости от чувствительности возбудителя, тяжести инфекции, возраста пациента, от состояния функции почек.
Вводят в/м или в/в. В/в путь введения предпочтителен для больных с тяжелыми или угрожающими жизни инфекциями, особенно при угрозе шока.
Побочное действие
Со стороны пищеварительной системы: возможны диарея, тошнота, рвота, колиты (включая псевдомембранозный колит); редко — боли в животе, запор, изменение вкуса.
Аллергические реакции: возможны — сыпь, зуд, крапивница; редко — анафилактические реакции.
Со стороны ЦНС и периферической нервной системы: возможны — головные боли; редко — головокружение, парестезии; в отдельных случаях — судороги.
Дерматологические реакции: редко — покраснение кожи. Наиболее часто у детей — сыпь.
Со стороны системы кроветворения: возможна анемия.
Со стороны показателей лабораторных исследований: возможны повышение активности АЛТ, АСТ, ЩФ, повышение общего билирубина, эозинофилия, увеличение протромбинового времени; редко — временное повышение азота мочевины крови и/или креатинина сыворотки, транзиторная тромбоцитопения, транзиторная лейкопения и нейтропения; часто — положительный результат теста Кумбса без гемолиза.
Прочие: возможны повышение температуры тела, вагинит, эритема; редко — генитальный зуд, неспецифический кандидоз.
Местные реакции: при в/в вливании возможны флебиты, редко — воспаление); при в/м введении возможно воспаление или боль.
Противопоказания к применению
Повышенная чувствительность к цефепиму или L-аргинину, а также к цефалоспориновым антибиотикам, пенициллинам или другим бета-лактамным антибиотикам.
Применение при беременности и кормлении грудью
Адекватных и строго контролируемых исследований безопасности применения цефепима при беременности не проведено; применение возможно только под наблюдением врача.
Цефепим выделяется с грудным молоком в очень низких концентрациях. В период лактации применять с осторожностью.
В экспериментальных исследованиях не выявлено влияния на репродуктивную функцию и фетотоксического действия цефепима.
Применение при нарушениях функции почек
При нарушениях функции почек (КК менее 30 мл/мин) необходима коррекция режима дозирования. Исходная доза цефепима должна быть такой же, как и для больных с нормальной функцией почек. Поддерживающие дозы определяют в зависимости от значений КК или концентрации креатинина сыворотки
Применение у детей
Безопасность и эффективность применения цефепима у детей в возрасте до 2 мес не установлены. Для детей старше 2 мес применение возможно согласно режиму дозирования. Детям с нарушениями функции почек рекомендуются такие же изменения режима дозирования, как и взрослым, поскольку фармакокинетика цефепима у взрослых и детей имеет сходный характер.
Особые указания
При применении у пациентов, находящихся в группе повышенного риска возникновения инфекции за счет смешанной аэробно/анаэробной микрофлоры (в т.ч. в случаях, когда одним из возбудителей является Bacteroides fragilis), до идентификации возбудителя рекомендуется одновременно с цефепимом назначить препарат, активный в отношении анаэробов.
С осторожностью применяют у пациентов с риском развития аллергических реакций, особенно на лекарственные препараты.
При развитии аллергических реакций цефепим следует отменить.
При серьезных реакциях гиперчувствительности немедленного типа может потребоваться применение эпинефрина (адреналина) и других форм поддерживающего лечения.
При появлении диареи на фоне лечения следует учитывать возможность развития псевдомембранозного колита. В таких случаях цефепим следует немедленно отменить и при необходимости назначить соответствующее лечение.
При развитии суперинфекции цефепим следует немедленно отменить и назначить соответствующее лечение.
Безопасность и эффективность применения цефепима у детей в возрасте до 2 мес не установлены.
С особой осторожностью применяют цефепим совместно с аминогликозидами и «петлевыми» диуретиками.
Лекарственное взаимодействие
При одновременном введении раствора цефепима с растворами метронидазола, ванкомицина, гентамицина, тобрамицина сульфата и нетилмицина сульфата возможно фармацевтическое взаимодействие.
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Аналоги препарата
Децефим
(ФАРМАСИНТЕЗ, Россия)
Кефсепим
(ДЖОДАС ЭКСПОИМ, Россия)
Максицеф®
(ПФК ПРЕБЕНД, Россия)
Мовизар
(YOUCARE PHARMACEUTICAL GROUP, Китай)
Цепим®
(БИОКОМ ТЕХНОЛОГИЯ, Республика Беларусь)
Цефепим
(SK MEDITECH, Индия)
Цефепим
(ПРОТЕК-СВМ, Россия)
Цефепим
(ФАРМГИД, Россия)
Цефепим
(КРАСФАРМА, Россия)
Цефепим
(БИОСИНТЕЗ, Россия)
Все аналоги

Внешний вид упаковки может отличаться от фотографии
Средняя цена в аптеках
119 ₽
Среди
3899
аптек,
подключенных к Ютеке в вашем регионе
Оплата и способы получения
в Москве
Оплата и способы получения
в Москве
Самовывоз
Сегодня бесплатно из 958 аптек
Завтра или позже бесплатно из 3899 аптек
Оплата картой или наличными в аптеке
Доставка
Конкретный срок и стоимость доставки зависят от вашего адреса
Информация о товаре
Форма выпуска:
порошок для приготовления раствора для внутривенного и внутримышечного введения
Количество в упаковке:
1 шт.
Производитель:
Борисовский ЗМП
Страна:
Беларусь
Страна производства может отличаться, проверяйте при получении заказа
Аналоги Цефепим
• В наличии в 4 аптеках
• Самовывоз сегодня
• Доставка недоступна
• В наличии в 3537 аптеках
• Самовывоз сегодня
• Доставка недоступна
• В наличии в 23 аптеках
• Самовывоз сегодня
• Доставка недоступна
Инструкция на Цефепим 1 г, порошок для приготовления раствора для внутривенного и внутримышечного введения, 1 шт.
Состав
1 флакон содержит: цефепима гидрохлорид 1 г.
Описание
раствор для инъекций и инфузий
Фармакологическое действие
Цефепим — антибактериальное средство из группы цефалоспоринов IV поколения. Действует бактерицидно, нарушая синтез клеточной стенки микроорганизмов. Обладает широким спектром действия в отношении грамположительных и грамотрицательных бактерий, штаммов, резистентных к аминогликозидам и/или цефалоспориновым антибиотикам III поколения. Высокоустойчив к гидролизу большинства бета-лактамаз и быстро проникает в грамотрицательные бактериальные клетки. Внутри бактериальной клетки молекулярной мишенью является пенициллин-связывающие белки. Активен in vivo и in vitro в отношении грамположительных аэробов: Staphylococcus aureus (только метициллиночувствительные штаммы), Streptococcus pneumoniae, Streptococcus pyogenes (группа A), Streptococcus группы viridans; грамотрицательных аэробов: Enterobacter spp., Escherichia coli, Klebsiella pneumoniae, Proteus mirabilis, Pseudomonas aeruginosa. In vitro активен (но клиническая значимость неизвестна) в отношении грамположительных аэробов: Staphylococcus epidermidis (только метициллиночувствительные штаммы), Staphylococcus saprophyticus, Streptococcus agalactiae (группа В); грамотрицательных аэробов: Acinetobacter lwoffii, Citrobacter diversus, Citrobacter freundii, Enterobacter agglomerans, Haemophilus influenzae (включая штаммы, продуцирующие бета-лактамазу), Hafnia alvei, Klebsiella oxytoca, Moraxella catarrhalis (включая штаммы, продуцирующие бета-лактамазы), Morganella morganii, Proteus vulgaris, Providencia rettgeri, Providencia stuartii, Serratia marcescens. Большинство штаммов Enterococcus, в т.ч. Enterococcus faecalis, метициллинорезистентные стафилококки, Stenotrophomonas (ранее известная как Xanthomonas maltophilia и Pseudomonas maltophilia), Clostridium difficile не чувствительны к цефепиму.
Цефепим: Показания
Пневмония (среднетяжелая и тяжелая), вызванная Streptococcus pneumoniae (в т.ч. случаи ассоциации с сопутствующей бактериемией), Pseudomonas aeruginosa, Klebsiella pneumoniae или Enterobacter spp.. Фебрильная нейтропения (эмпирическая терапия). Осложненные и неосложненные инфекции мочевыводящих путей (включая пиелонефрит), вызванные Escherichia coli, Klebsiella pneumoniae, Proteus mirabilis. Неосложненные инфекции кожи и мягких тканей, вызванные Staphylococcus aureus (только метициллиночувствительные штаммы), Streptococcus pyogenes. Осложненные интраабдоминальные инфекции (в комбинации с метронидазолом), вызванные Escherichia coli, Klebsiella pneumoniae, Pseudomonas aeruginosa, Enterobacter spp., Bacteroides fragilis.
Способ применения и дозы
В/в инфузионно (в течение не менее 30 мин) или в/м (только при осложненных или неосложненных инфекциях мочевыводящих путей легкой и средней тяжести, вызванных E. coli). Пневмония (среднетяжелая и тяжелая), вызванная Streptococcus pneumoniae (в т.ч. случаи ассоциации с сопутствующей бактериемией), Pseudomonas aeruginosa, Klebsiella pneumoniae или Enterobacter spp.: в/в 1-2 г каждые 12 ч в течение 10 дней. Фебрильная нейтропения (эмпирическая терапия): в/в 2 г каждые 8 ч в течение 7 дней или до разрешения нейтропении. Осложненные или неосложненные инфекции мочевыводящих путей легкой и средней тяжести, вызванных E. coli, Klebsiella pneumoniae, Proteus mirabilis: в/в или в/м (только для инфекций, вызванных E. coli) по 0.5-1 г каждые 12 ч в течение 7-10 дней. Тяжелые осложненные или неосложненные инфекции мочевыводящих путей (включая пиелонефрит), вызванные E. coli или Klebsiella pneumoniae: в/в 2 г каждые 12 ч в течение 10 дней. Среднетяжелые и тяжелые инфекции кожи и мягких тканей, вызванные Staphylococcus aureus (только метициллиночувствительные штаммы), Streptococcus pyogenes: в/в 2 г каждые 12 ч в течение 10 дней. Осложненные интраабдоминальные инфекции (в комбинации с метронидазолом), вызванные Escherichia coli, Klebsiella pneumoniae, Pseudomonas aeruginosa, Enterobacter spp., Bacteroides fragilis: в/в 2 г каждые 12 ч в течение 7-10 дней. У детей от 2 мес до 16 лет и с массой тела до 40 кг рекомендуемый режим дозирования по всем показаниям (исключая фебрильную нейтропению) — 50 мг/кг каждые 12 ч в/в; при фебрильной нейтропении — 50 мг/кг каждые 8 ч. Продолжительность лечения как у взрослых. При ХПН дозу назначают в зависимости от тяжести инфекции и КК: более 60 мл/мин — 0.5-1-2 г каждые 12 ч или 2 г каждые 8 ч, КК 30-60 мл/мин — 0.5-1-2 г каждые 24 ч или 2 г каждые 12 ч, при КК 11-29 мл/мин — 0.5-1-2 г каждые 24 ч, менее 11 мл/мин — 0.25-0.5-1 г каждые 24 ч; постоянный амбулаторный перитонеальный диализ — 0.5-1-2 г каждые 48 ч. Пациентам, находящимся на гемодиализе в 1-й день вводят 1 г, затем по 0.5 г каждые 24 ч для всех инфекций и по 1 г каждые 24 ч для лечения фебрильной нейтропении. В день проведения гемодиализа, препарат вводят после окончания сеанса гемодиализа; желательно вводить цефепим каждый день в одно и то же время. Данные по применению препарата у детей с сопутствующей ХПН недоступны, однако, учитывая сходство фармакокинетики у детей и у взрослых, режим дозирования (уменьшение дозы или увеличение интервала между введениями) у детей с ХПН сходен с режимом дозирования у взрослых. Для в/в введения растворяют в стерильной воде для инъекций, 5% растворе декстрозы или 0.9% растворе NaCl; для в/м введения — в стерильной воде для инъекций с парабеном или бензиловым спиртом, в 0.5 и 1% растворе лидокаина.
Цефепим: Противопоказания
Гиперчувствительность (в т.ч. к др. цефалоспоринам, пенициллинам, др. бета-лактамным антибиотикам), детский возраст (до 2 мес).
Цефепим: Побочные действия
Аллергические реакции: кожная сыпь (в т.ч. эритематозные высыпания), зуд, лихорадка, анафилактоидные реакции, положительная реакция Кумбса, эозинофилия, мультиформная экссудативная эритема (в т.ч. синдром Стивенса-Джонсона), редко — токсический эпидермальный некролиз (синдром Лайелла).
Местные реакции: при в/в введении — флебиты, при в/м — гиперемия и болезненность в месте введения.
Со стороны нервной системы: головная боль, головокружение, бессонница, парестезии, чувство беспокойства, спутанность сознания, судороги.
Со стороны мочеполовой системы: вагинит.
Со стороны мочевыделительной системы: нарушение функции почек.
Со стороны пищеварительной системы: диарея, тошнота, рвота, запоры, боль в животе, диспепсия, псевдомембранозный колит.
Со стороны органов кроветворения: анемия, тромбоцитопения, лейкопения, нейтропения, панцитопения, гемолитическая анемия, кровотечения.
Со стороны дыхательной системы: кашель.
Со стороны ССС: тахикардия, одышка, периферические отеки.
Лабораторные показатели: снижение гематокрита, увеличение протромбинового времени, повышение концентрации мочевины, гиперкреатининемия, гиперкальциемия, повышение активности «печеночных» трансаминаз и ЩФ, гипербилирубинемия.
Прочие: боль в горле, боль в груди, повышенное потоотделение, боли в спине, астения, развитие суперинфекции, орофарингеальный кандидоз.
Взаимодействие
Фармацевтически несовместим с др. противомикробными ЛС и гепарином. Несовмести с раствором метронидазола (перед введением раствора метронидазола для профилактики инфекций при проведении хирургических вмешательств следует промыть инфузионную систему от раствора цефепима). Повышает нефро- и ототоксичность аминогликозидов.
Особые указания
При возникновении псевдомембранозного колита с длительной диареей прекращают прием и назначают ванкомицин (внутрь) или метронидазол. Возможна перекрестная гиперчувствительность у пациентов с аллергическими реакциями на пенициллины. При сочетанной тяжелой почечной и печеночной недостаточности следует регулярно определять концентрацию препарата в плазме (проводят коррекцию дозы в зависимости от КК). При длительном лечении необходим регулярный контроль периферической крови, показателей функционального состояния печени и почек. При смешанной аэробно-анаэробной инфекции до идентификации возбудителей целесообразна комбинация с ЛС активным в отношении анаэробов. Больным, у которых из удаленного очага инфекции происходит менингеальная диссеминация, имеются подозрения на менингит или диагноз менингита подтвержден, следует назначить альтернативный антибиотик с подтвержденной для данной ситуации клинической эффективностью. Возможно обнаружение положительного теста Кумбса, ложноположительного теста на глюкозу в моче. Приготовленный раствор хранить не более 24 ч при комнатной температуре или в течение 7 дней — в холодильнике. Изменение цвета не влияет на активность препарата.
Условия отпуска
Производитель
Борисовский завод, Беларусь
Основные сведения
Торговое название
Цефепим
Действующее вещество (МНН)
Цефепим
Форма выпуска
порошок для приготовления раствора для внутривенного и внутримышечного введения
Первичная упаковка
флакон
Производитель
Борисовский ЗМП
Условия хранения
В защищенном от света месте, при температуре не выше 25 °C
Представлено описание активных веществ лекарственного препарата. Описание препарата основано на официально утвержденной инструкции по применению от компании-производителя. Приведенное описание носит исключительно информационный характер и не может быть использовано для принятия решения о возможности применения конкретного лекарственного препарата.
Сертификаты Цефепим 1 г, порошок для приготовления раствора для внутривенного и внутримышечного введения, 1 шт.


Дозировки и формы выпуска Цефепим
• В наличии в 22 аптеках
• Самовывоз завтра или позже
• Доставка недоступна
• В наличии в 230 аптеках
• Самовывоз сегодня
• Доставка недоступна
• В наличии в 79 аптеках
• Самовывоз сегодня
• Доставка недоступна
• В наличии в 2 аптеках
• Самовывоз сегодня
• Доставка недоступна
Цены в аптеках на Цефепим 1 г, порошок для приготовления раствора для внутривенного и внутримышечного введения, 1 шт.
История стоимости Цефепим 1 г, порошок для приготовления раствора для внутривенного и внутримышечного введения, 1 шт.
Указана средняя стоимость товара в аптеках региона Москва и МО за период и разница по сравнению с предыдущим периодом
Цены Цефепим и наличие в аптеках в Москве
1 г, порошок для приготовления раствора для внутривенного и внутримышечного введения, 1 шт.
| Список аптек | Адрес | Часы работы | Цена |
|---|---|---|---|
| Ваша № 1
Aptstore |
Луганская ул, 5, Москва |
09:00-22:00 Пн-Пт, 09:00-21:00 Сб-Вс |
41 ₽ |
| Ваша №1
Aptstore |
Кропоткинский пер, 4с1, Москва |
08:00-22:00 Пн-Пт, 09:00-22:00 Сб, 10:00-22:00 Вс |
41 ₽ |
| Аптечество |
Ключевая ул, 16с29, Москва |
08:00-21:00 Пн-Пт, 09:00-21:00 Сб-Вс |
47 ₽ |
| Апрель |
Ленина ул, 4, Хотьково, Сергиев Посад го, МО |
09:00-20:00 Пн-Вс |
59 ₽ |
| Монастырев |
Ленина ул, 1, Павловская Слобода с, Истра ГО, МО |
09:00-22:00 Пн-Вс |
77 ₽ |
| 305 Аптека
ЗдравСити |
Сергиев Посад-6, 1А, Сергиево-Посадский р-н, МО (на въезде в Военный городок, на территории рынка) |
09:30-19:00 Пн-Пт, 09:30-17:00 Сб-Вс |
106 ₽ |
| 33 Аптека
ЗдравСити |
г.Сергиев Посад, площадь Красногорская, д. 1 |
10:00-19:00 Пн-Вс |
106 ₽ |
| 36,6
ЗдравСити |
Никольская ул, 10, Москва |
08:00-23:00 Пн-Вс |
106 ₽ |
| 468 Аптека
ЗдравСити |
г.Жуковский, Чкалова, д. 41 |
Круглосуточно |
106 ₽ |
| Apteka
ЗдравСити |
Курыжова, 7, Южный мкр, Домодедово, МО |
09:00-22:00 Пн-Вс |
106 ₽ |
| Ipharm
ЗдравСити |
Энтузиастов ш, 3 к 1, Москва |
Круглосуточно |
106 ₽ |
| REDApteka
Оплата только наличными ЗдравСити |
Семеновская пл, 7 к 17А, Москва |
09:00-21:00 Пн-Пт |
106 ₽ |
| А+А
ЗдравСити |
Юшуньская малая. ул, 3, Москва |
09:00-21:00 Пн-Вс |
106 ₽ |
| АBC
ЗдравСити |
Нахимовский пр, 22, Москва |
Круглосуточно |
106 ₽ |
| Абикон Медика
ЗдравСити |
Армавирская ул, 3, Москва |
09:00-21:00 Пн-Сб, 10:00-21:00 Вс |
106 ₽ |
| Аве
Оплата только наличными ЗдравСити |
Пресненский Вал ул, 7c1, Москва |
10:00-22:00 Пн-Вс |
106 ₽ |
| № 17
ЗдравСити |
Рижское ш, 41А, Волоколамск, МО |
09:00-18:00 Пн-Пт, 09:00-15:00 Сб-Вс |
106 ₽ |
| № 458
ЗдравСити |
Ласточкин пр-д, 16, Балашиха, МО |
08:00-21:00 Пн-Вс |
106 ₽ |
| №1
ЗдравСити |
Маршала Жукова пр, 49, Москва |
09:00-21:00 Пн-Вс |
106 ₽ |
| №206 На Рязанском проспекте
ЗдравСити |
Рязанский пр, 71к1, Москва |
08:00-21:00 Пн-Пт, 09:00-19:00 Сб, 10:00-18:00 Вс |
106 ₽ |
Считает, что товар плохой
Цефепим мне назначил врач, когда у меня появилась пневмония, как осложнение после простуды. После первой инъекции, у меня появилось покраснение кожи, сильный жар и я потеряла сознание. Меня спасли врачи «скорой». Больше я никогда не буду принимать этот антибиотик, он мне категорически не подходит, несмотря на низкую цену.
Считает, что товар хороший
Цефепим – современный антибиотик с высокой эффективностью. Относится к цефалоспоринам 4 поколения. Он безопасен для пациентов всех возрастов, назначается при инфекционно-воспалительных заболеваниях. Часто применяется в ЛОР-практике для лечения синуситов, отитов и абсцессов, подходит для лечения ангины, фурункулеза. Препарат имеет низкую стоимость/
Считает, что товар отличный
У моего ребенка была сильная ангина и помог только цефепим, который нам назначили в стационаре. Облегчение наступило уже после второй инъекции, но курс нужно было обязательно закончить. Хороший и безопасный препарат, который эффективно устраняет инфекцию, не вызывает побочных явлений и подходит детям и взрослым. Цена адекватная.
Популярные товары в категории
Популярные товары в Ютеке
Купить Цефепим, 1 г, порошок для приготовления раствора для внутривенного и внутримышечного введения, 1 шт. в Москве с доставкой в аптеку или домой, сделав заказ через Ютеку
Цена Цефепим, 1 г, порошок для приготовления раствора для внутривенного и внутримышечного введения, 1 шт. в Москве от 41 руб. на сайте и в приложении
Подробная инструкция по применению Цефепим, 1 г, порошок для приготовления раствора для внутривенного и внутримышечного введения, 1 шт.
Информация на сайте не является призывом или рекомендацией к самолечению и не заменяет консультацию специалиста (врача), которая обязательна перед назначением и/или применением любого лекарственного препарата.
Дистанционная торговля лекарственными препаратами осуществляется исключительно аптечными организациями, имеющими действующую лицензию на фармацевтическую деятельность, а также разрешение на дистанционную торговлю лекарственными препаратами. Дистанционная торговля рецептурными лекарственными препаратами, наркотическими и психотропными, а также спиртосодержащими лекарственными препаратами запрещена действующим законодательством РФ и не осуществляется.
Цефепим Промомед — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер:
ЛП-005926
Торговое наименование:
Цефепим
Международное непатентованное или группировочное наименование:
цефепим
Лекарственная форма:
порошок для приготовления раствора для внутривенного и внутримышечного введения
Состав
на 1 флакон:
| 0,5 г | 1,0 г | 2,0 г | |
|
Действующее вещество: |
|||
|
Цефепима гидрохлорида моногидрат |
0,5945 г |
1,1891 г |
2,3782 г |
|
(в пересчете на цефепим) |
0,5 г |
1,0 г |
2,0 г |
| Вспомогательное вещество: | |||
| L-аргинин |
0,3625 г |
0,725 г |
1,450 г |
Описание:
белый или белый с желтоватым оттенком кристаллический порошок
Фармакотерапевтическая группа:
антибиотик-цефалоспорин
Код ATX:
J01DE01
Фармакологические свойства
Фармакодинамика
Цефепим является цефалоспориновым антибиотиком широкого спектра действия. Цефепим подавляет синтез белков клеточной стенки бактерий, обладает широким спектром бактерицидного действия в отношении различных грамположительных и грамотрицательных бактерий, в том числе большинства штаммов, резистентных к аминогликозидам или цефалоспориновым антибиотикам третьего поколения, таким как цефтазидим. Цефепим высоко устойчив к гидролизу большинством бета-лактамаз, он имеет низкое сродство к бета-лактамазам и быстро проникает в клетки грамотрицательных бактерий. Доказано, что цефепим обладает очень высоким сродством к пенициллин-связывающему белку (ПСБ) типа 3, высоким сродством -к ПСБ типа 2 и умеренным сродством — к ПСБ типов 1а и 1б. Цефепим оказывает бактерицидное действие в отношении широкого спектра бактерий. Цефепим активен в отношении следующих микроорганизмов:
Грамположителъные аэробы:
Staphylococcus aureus (включая штаммы, продуцирующие бета-лактамазу);
Staphylococcus epidermidis (включая штаммы, продуцирующие бета-лактамазу);
другие штаммы Staphylococcus spp., включая Staphylococcus hominis, Staphylococcus saprophyticus;
Streptococcus pyogenes (стрептококки группы A);
Streptococcus agalactiae (стрептококки группы В);
Streptococcus pneumoniae (включая штаммы со средней устойчивостью к пенициллину — минимальная подавляющая концентрация от 0,1 до 1 мкг/мл);
другие бета-гемолитические Streptococcus spp. (группы С, G, F), Streptococcus bovis (группа D), Streptococcus spp. группы viridans.
Примечание: большинство штаммов энтерококков, например, Enterococcus faecalis, и стафилококки, резистентные к метициллину, устойчивы к действию большинства цефалоспориновых антибиотиков, включая цефепим.
Грамотрицательные аэробы:
Acinetobacter calcoaceticus (подштаммы anitratus, Iwoffii);
Aeromonas hydrophila;
Capnocytophaga spp.;
Citrobacter spp., включая Citrobacter diversus, Citrobacter freundii,
Campylоbасter jejuni;
Enterobacter spp., включая Enterobacter cloacae, Enterobacter aerogenes, Enterobacter sakazakii;
Escherichia coli;
Gardnerella vaginalis;
Haemophilus ducreyi;
Haemophilus influenzae (включая штаммы, продуцирующие бета-лактамазу);
Haemophilus parainfluenzae;
Hafnia alvei;
Klebsiella spp., включая Klebsiella pneumoniae, Klebsiella oxytoca, Klebsiella ozaenae;
Legionella spp.;
Morganella morganii;
Moraxella catarrhalis (Branhamella catarrhalis) (включая штаммы, продуцирующие бета-лактамазы);
Neisseria gonorrhoeae (включая штаммы, продуцирующие бета-лактамазу);
Neisseria meningitidis;
Pantoea agglomerans (ранее известный как Enterobacter agglomerans);
Proteus spp., включая Proteus mirabilis, Proteus vulgaris;
Providencia spp., включая Providencia rettgeri, Providencia stuartii;
Pseudomonas spp., включая Pseudomonas aeruginosa, Pseudomonas putida, Pseudomonas stutzeri, Salmonella spp.;
Serratia, включая Serratia marcescens, Serratia liquefaciens;
Shigella spp.;
Yersinia enterocolitica.
Примечание: цефепим неактивен в отношении многих штаммов Stenotrophomonas maltophilia, ранее известных как Xanthomonas maltophilia и Pseudomonas maltophilia).
Анаэробы:
Bacteroides spp.;
Clostridium perfringens;
Fusobacterium spp.;
Mobiluncus spp.;
Peptostreptococcus spp.;
Prevotella melaninogenica (известный как Bacteroides melaninogenicus);
Veillonella spp.
Примечание: цефепим неактивен в отношении Bacteroides fragilis и Clostridium difficile.
Фармакокинетика
Средние концентрации цефепима в плазме крови взрослых здоровых мужчин в различные сроки после однократного внутривенного введения в течение 30 мин до 12 ч и максимальная концентрация (Сmах) приведены ниже в таблице.
Средние концентрации цефепима в плазме (мкг/мл) после внутривенного введения
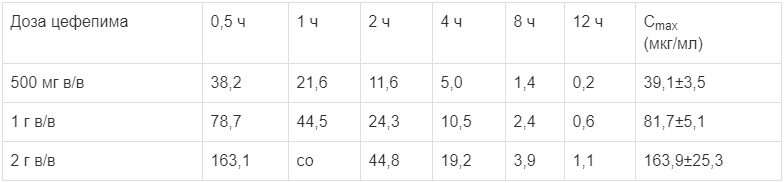 После внутримышечного введения цефепим всасывается полностью.
После внутримышечного введения цефепим всасывается полностью.
Сmах и время достижения максимальной концентрации (Тmах) после однократного внутримышечного введения приведены ниже в таблице.
Средние концентрации цефепима в плазме (мкг/мл) после внутримышечного введения
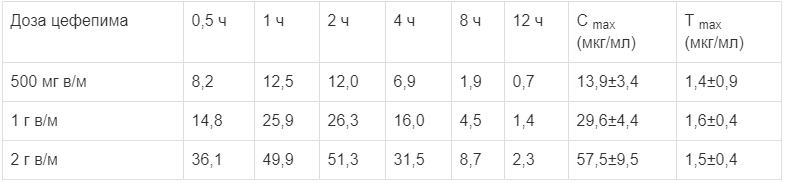 Терапевтические концентрации цефепима обнаруживаются в следующих жидкостях и тканях: моче, желчи, перитонеальной, буллезной жидкости, слизистой оболочке бронхов, мокроте, простате, аппендиксе и желчном пузыре. Связывание цефепима с белками сыворотки крови составляет в среднем 16,4 % и нс зависит от концентрации препарата в сыворотке крови.
Терапевтические концентрации цефепима обнаруживаются в следующих жидкостях и тканях: моче, желчи, перитонеальной, буллезной жидкости, слизистой оболочке бронхов, мокроте, простате, аппендиксе и желчном пузыре. Связывание цефепима с белками сыворотки крови составляет в среднем 16,4 % и нс зависит от концентрации препарата в сыворотке крови.
Цефепим метаболизируется в N-метилпирролидин, который быстро превращается в оксид N-метилпирролидина.
Цефепим выводится преимущественно почками, путем клубочковой фильтрации (почечный клиренс составляет в среднем 110 мл/мин). В моче обнаруживается приблизительно 85 % от введенной дозы неизмененного цефепима, менее 1 % N-метилпирролидина, около 6,8 % оксида N-метилпирролидина и около 2,5 % эпимера цефепима.
После введения доз от 250 мг до 2 г период полувыведения цефепима из организма составляет в среднем около 2 часов. Общий клиренс составляет в среднем 120 мл/мин. При внутривенном ведении препарата здоровым добровольцам в дозе 2 г каждые 8 часов в течение 9 дней кумуляции препарата не наблюдалось.
Пациенты с нарушениями функции почек
Период полувыведения из организма при почечной недостаточности увеличивается, при этом наблюдается линейная зависимость между общим клиренсом и клиренсом креатинина. При тяжёлых нарушениях функции почек, требующих проведения сеансов диализа, период полувыведения составляет в среднем 13 часов при гемодиализе и 19 часов при непрерывном перитонеальном диализе. При нарушенной функции почек требуется корректировка дозы.
Пациенты с нарушениями функции печени
Фармакокинетика цефепима у пациентов с нарушенной функцией печени не изменяется. Корректировки дозы для таких пациентов не требуется.
Пациенты старше 65 лет
После однократного внутривенного введения 1 г препарата здоровым добровольцам старше 65 лет отмечалось увеличение площади под кривой зависимости «концентрация-время» (AUC) и уменьшение почечного клиренса по сравнению с молодыми добровольцами. При нарушенной функции почек пациентам старшего возраста требуется корректировка дозы.
Дети
Фармакокинетика препарата исследовалась у детей в возрасте от 2 месяцев до 11 лет после однократного введения дозы 50 мг/кг массы тела внутривенно или внутримышечно, а также после повторного введения препарата (каждые 8-12 часов, в течение не менее 48 часов). После однократного внутривенного введения общий клиренс и объем распределения составляли 3,3 мл/мин/кг и 0,3 л/кг, соответственно. Период полувыведения из организма составлял в среднем 1,7 ч. Выведение цефепима в неизмененном виде почками составляло 60,4 % от введенной дозы, а почечный клиренс — в среднем 2,0 мл/мин/кг.
После многократного внутривенного введения концентрация цефепима в плазме крови в равновесном состоянии, а также другие фармакокинетические параметры не отличались от таковых после однократного введения. Возраст и пол пациентов не оказывали существенного влияния на общий клиренс и объем распределения с учетом поправки на массу тела. После внутримышечного введения максимальная концентрация цефепима в плазме крови в равновесном состоянии составляла в среднем 68 мкг/мл и достигалась в среднем за 0,75 ч. Через 8 ч после внутримышечного введения концентрации цефепима в плазме крови составляли в среднем 6 мкг/мл. Абсолютная биодоступность цефепима после внутримышечной инъекции составляла в среднем 82 %.
Концентрации препарата в спинномозговой жидкости (СМЖ) и в плазме крови у детей с бактериальным менингитом
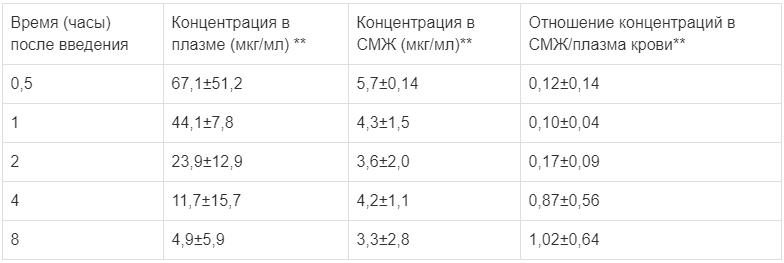 ** возраст пациентов: 3,1 месяца — 12 лет, средний возраст: 3 года. Доза препарата 50 мг/кг массы тела при внутривенном введении в течение от 5 до 20 минут каждые 8 часов. Концентрации в плазме и СМЖ определялись в конце введения на 2 или 3 день лечения препаратом.
** возраст пациентов: 3,1 месяца — 12 лет, средний возраст: 3 года. Доза препарата 50 мг/кг массы тела при внутривенном введении в течение от 5 до 20 минут каждые 8 часов. Концентрации в плазме и СМЖ определялись в конце введения на 2 или 3 день лечения препаратом.
Показания к применению
Инфекционно-воспалительные заболевания, вызванные чувствительными к цефепиму микроорганизмами, у взрослых:
— Инфекции нижних дыхательных путей, включая пневмонию и бронхит;
— Инфекции мочевыводящих путей, как осложнённые, включая пиелонефрит, так и неосложнённые;
— Инфекции кожи и мягких тканей;
— Инфекции брюшной полости, включая перитонит и инфекции желчных путей;
— Гинекологические инфекции;
— Септицемия;
— Фебрильная нейтропения.
Профилактика возможных инфекций при проведении полостных хирургических операций.
Инфекционно-воспалительные заболевания, вызванные чувствительными к цефепиму микроорганизмами, у детей:
— Пневмония;
— Инфекции мочевых путей, как осложнённые, включая пиелонефрит, так и неосложнённые;
— Инфекции кожи и мягких тканей;
— Септицемия;
— Фебрильная нейтропения;
— Бактериальный менингит.
Противопоказания
Гиперчувствительность к цефепиму или L-аргинину, а также к антибиотикам цефалоспориновой группы, пенициллинам или другим бета-лактамным антибиотикам.
Детский возраст до 2-х месяцев.
С осторожностью
Заболевания желудочно-кишечного тракта в анамнезе (особенно колит), почечная недостаточность (клиренс креатинина менее 60 мл/мин).
Применение при беременности и в период грудного вскармливания
Адекватных и контролируемых клинических исследований у беременных женщин не проводилось. При беременности следует применять препарат только в том случае, если предполагаемая польза для матери превышает потенциальный риск для плода.
Цефепим обнаруживается в грудном молоке в очень низких концентрациях.
В период грудного вскармливания следует применять препарат только в том случае, если предполагаемая польза для матери превышает потенциальный риск для ребенка.
Способ применения и дозы
Цефепим может вводиться внутривенно (в/в) или внутримышечно (в/м). Дозы и путь введения зависят от чувствительности возбудителей, тяжести инфекции, состояния функции почек и общего состояния пациента. Внутривенный путь введения рекомендуется для пациентов с тяжёлыми или угрожающими жизни инфекциями, особенно при угрозе возникновения септического шока. Внутримышечно доза до 1 г (объем <3,1 мл) может быть введена как однократная инъекция. Максимальную дозу (2 г/6,2 мл) следует вводить в виде двух инъекций в разные места.
Для детей доза не должна превышать максимальную рекомендуемую дозу для взрослых (2 г в/в каждые 8 часов). Опыт внутримышечного введения цефепима детям ограничен.
Взрослым и детям с массой тела более 40 кг при нормальной функции почек
|
Инфекции мочевых путей, легкой и средней тяжести |
0,5 г-1 г в/в или в/м |
Каждые 12 часов |
|
Другие инфекции, легкой и средней тяжести |
1 г в/в или в/м |
Каждые 12 часов |
|
Тяжелые инфекции |
2 г в/в |
Каждые 12 часов |
|
Очень тяжелые и угрожающие жизни инфекции |
2 г в/в |
Каждые 8 часов |
Обычная продолжительность лечения составляет 7-10 дней; тяжёлые инфекции могут потребовать более продолжительного лечения.
В случае лечения фебрильной нейтропении обычная продолжительность лечения составляет 7 дней или до исчезновения нейтропении.
Профилактика возможных инфекций при проведении хирургических операций
За 60 минут до начала хирургической операции вводится 2 г препарата внутривенно в виде инфузии в течение 30 минут. Сразу после окончания инфузии вводится 500 мг метронидазола внутривенно. Вследствие несовместимости метронидазола и цефепима их не следует вводить одновременно или смешивать. Инфузионную систему перед введением метронидазола следует промыть (см. «Внутривенное введение»). Раствор метронидазола следует приготовить в соответствии с инструкцией по применению метронидазола. Во время длительных (более 12 часов) хирургических операций через 12 часов после первой дозы рекомендуется повторное введение в той же дозе препарата Цефепим с последующим введением метронидазола.
Дети от 2 месяцев с массой тела до 40 кг
Обычная рекомендуемая доза при инфекциях мочевых путей, инфекциях кожи и мягких тканей, пневмонии составляет 50 мг/кг каждые 12 часов в течение 10 дней. В случае тяжелых инфекций — каждые 8 часов. Пациентам с фебрильной нейтропенией, септицемией, бактериальным менингитом следует вводить 50 мг/кг каждые 8 часов в течение 7-10 дней.
Пациенты с нарушением функции почек
Пациентам с нарушенной функцией почек требуется корректировка дозировки цефепима с целью компенсации уменьшенной скорости выведения препарата с мочой. Режим дозирования должен назначаться в зависимости от степени почечной недостаточности, тяжести инфекции и чувствительности микроорганизмов. У пациентов со слабым или умеренным нарушением функции почек исходная доза препарата должна быть такой же, как у пациентов с нормальной функцией почек.
Рекомендуемые поддерживающие дозы цефепима представлены в таблице. Клиренс креатинина для мужчин можно рассчитать исходя из концентрации сывороточного креатинина по следующей формуле:
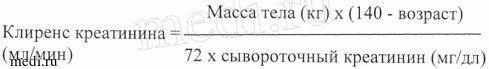
Клиренс креатинина для женщин можно рассчитать, умножив полученное значение на 0,85.
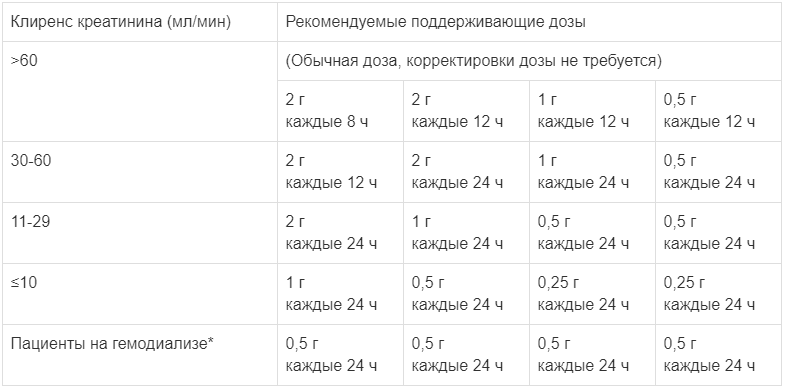 *Для пациентов на гемодиализе рекомендуется уменьшение дозы препарата Цефепим: 1 г первый день лечения и затем 0,5 г в день при всех инфекциях, за исключением фебрильной нейтропении, где доза составляет 1 г в день. В дни диализа Цефепим следует вводить по окончании диализа. По возможности препарат следует вводить в одно и то же время каждый день.
*Для пациентов на гемодиализе рекомендуется уменьшение дозы препарата Цефепим: 1 г первый день лечения и затем 0,5 г в день при всех инфекциях, за исключением фебрильной нейтропении, где доза составляет 1 г в день. В дни диализа Цефепим следует вводить по окончании диализа. По возможности препарат следует вводить в одно и то же время каждый день.
При гемодиализе за 3 часа удаляется из организма приблизительно 68 % введенной дозы препарата.
При непрерывном амбулаторном перитонеальном диализе препарат можно использовать в исходных рекомендованных дозах 0,5 г, 1 г или 2 г в зависимости от тяжести инфекции с интервалом между введением 48 часов.
Дети с нарушением функции почек
Детям при нарушенной функции почек рекомендуется уменьшение дозы или увеличение интервала между введениями, как указано выше в таблице. Клиренс креатинина вычисляется по следующим формулам:

Пациенты с нарушением функции печени
Коррекции дозы для пациентов с нарушением функции печени не требуется.
Внутривенное введение
Рекомендуется для пациентов с тяжёлыми или угрожающими жизни инфекциями, особенно при угрозе возникновения септического шока.
Приготовление раствора для внутривенного введения
Препарат растворяют в 5, 10 или 20 мл стерильной воды для инъекций, 5 % растворе декстрозы и 0,9 % растворе натрия хлорида для инъекций, как указано в приведенной ниже таблице, и вводят в течение 3-5 минут либо непосредственно в вену, либо в систему для внутривенного введения, через которую в организм пациента поступает совместимый раствор для внутривенного введения.
Приготовление раствора для внутривенной инфузии
Приготовленный раствор (см. выше) переносят в инфузионный сосуд с другими совместимыми растворам для внутривенных инфузий (см. ниже) и вводят в течение не менее 30 минут.
 Растворы препарата с концентрацией 1-40 мг/мл совместимы со следующими парентеральными растворами:; раствор 5% декстрозы и 0,9 % раствор натрия хлорида для инъекций;, раствор Рингера лактат.
Растворы препарата с концентрацией 1-40 мг/мл совместимы со следующими парентеральными растворами:; раствор 5% декстрозы и 0,9 % раствор натрия хлорида для инъекций;, раствор Рингера лактат.
Внутримышечное введение: доза до 1 г (объем < 3,1 мл) может быть введена в виде однократной инъекции. Максимальную дозу (2 г/6,2 мл) следует вводить в виде двух инъекций в разные места.
Приготовление раствора для внутримышечного введения
Препарат растворяют в стерильной воде для инъекций, 5 % растворе декстрозы или 0,9 % растворе натрия хлорида для инъекций, бактериостатической воде для инъекций с парабенами или бензиловым спиртом, 0,5 % или 1 % растворе лидокаина, как указано ниже в таблице.
 Хранение растворов для внутривенного и внутримышечного введения
Хранение растворов для внутривенного и внутримышечного введения
Приготовленные растворы препарата для внутримышечного и внутривенного введения стабильны в течение 24 часов при комнатной температуре или 7 дней при хранении в холодильнике (2-8°С).
Как и все растворы для парентерального применения, перед введением приготовленные растворы препарата следует проверить на отсутствие видимых механических включений. В противном случае запрещается использовать приготовленный раствор.
При хранении порошок и приготовленный раствор могут потемнеть, что не влияет на активность и качество препарата.
Побочное действие
Наиболее часто отмечаются побочные эффекты со стороны желудочно-кишечного тракта и аллергические реакции. Ниже перечислены побочные эффекты по органам и системам в соответствии с их частотой: очень часто (≥10 %); часто (≥1 % и <10 %); нечасто (≥0,1 % и <1 %); редко (≥0,01 % и <0,1 %); частота неизвестна (нет данных о частоте развития данного побочного эффекта).
Аллергические реакции
Часто — высыпания на коже;
Нечасто — эритема, крапивница, зуд;
Редко — анафилактические реакции;
Частота неизвестна — анафилактический шок, токсический эпидермальный некролиз, мультиформная эритема, синдром Стивенса-Джонсона, ангионевротический отек.
Инфекции
Нечасто — кандидоз слизистой оболочки полости рта, вагинальные инфекции;
Редко — кандидозы.
Со стороны центральной нервной системы
Нечасто — головная боль;
Редко — судороги, парестезии, дисгезии, головокружение;
Частота неизвестна (пострегистрационный опыт): энцефалопатия (нарушение сознания, включая спутанность сознания, галлюцинации, ступор и кома), миоклонус, судороги и бессудорожный эпилептический статус.
Несмотря на то, что большинство случаев отмечались у пациентов с почечной недостаточностью, которые получали цефепим в дозах, выше рекомендованных, в некоторых случаях нейротоксичность отмечалась у пациентов, которым проводилась коррекция дозы в зависимости от степени почечной недостаточности.
Со стороны мочевыделительной системы
Частота неизвестна — почечная недостаточность, токсическая нефропатия.
Со стороны пищеварительной системы
Часто — диарея;
Нечасто — тошнота, рвота, колит (включая псевдомембранозный колит);
Редко — абдоминальные боли, запор;
Частота неизвестна — нарушения пищеварения.
Со стороны дыхательной системы
Редко — одышка.
Со стороны сердечно-сосудистой системы
Редко — вазодилатация;
Частота неизвестна — кровотечения.
Общие реакции и реакции в месте введения
Часто — флебит в месте введения, боль в месте введения;
Нечасто — повышение температуры и воспаление в месте введения;
Редко — озноб.
Лабораторные показатели
Часто — повышение активности аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (ACT), щелочной фосфатазы (ЩФ), общего билирубина, анемия, эозинофилия, увеличение протромбинового времени или частичного тромбопластинового времени;
Нечасто — повышение азота мочевины крови, креатинина сыворотки, тромбоцитопения, лейкопения и нейтропения;
Частота неизвестна — апластическая анемия, гемолитическая анемия, агранулоцитоз.
Прочие
Редко — генитальный зуд, изменение вкуса, вагинит, эритема, ложноположительная проба Кумбса без гемолиза.
Передозировка
Симптомы: энцефалопатия (спутанность сознания, галлюцинации, ступор, кома), миоклонические судороги, повышенная нервно-мышечная возбудимость.
Лечение: симптоматическая и поддерживающая терапия. В случае значительного превышения рекомендованных доз, особенно у пациентов с нарушением функции почек, показан гемодиализ.
Взаимодействие с другими лекарственными средствами
Раствор препарата фармацевтически несовместим с растворами метронидазола, ванкомицина, гентамицина, тобрамицина сульфата, нетилмицина сульфата, поэтому их нельзя смешивать. Однако при одновременном назначении цефепима и вышеуказанных препаратов каждый из них можно вводить раздельно.
Данные по совместимости растворов цефепима и других лекарственных препаратов, а также их по их стабильности приведены в таблице ниже.
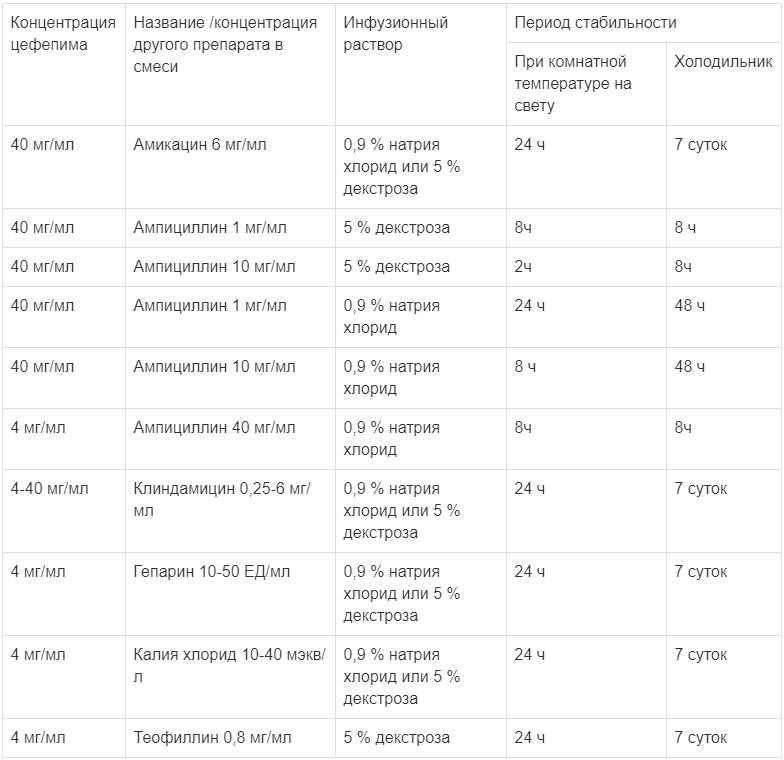 Совместное применение с бактериостатическими антибиотиками может снизить эффективность бета-лактамных антибиотиков.
Совместное применение с бактериостатическими антибиотиками может снизить эффективность бета-лактамных антибиотиков.
Особые указания
При наличии факторов, могущих вызвать нарушение функции почек, требуется корректировка дозы цефепима с целью компенсации уменьшенной скорости выведения препарата с мочой. Режим дозирования зависит от степени почечной недостаточности, тяжести инфекции и чувствительности микроорганизмов. При слабых или умеренных нарушениях функции почек начальная доза препарата такая же, как при нормальной функции почек. Риск развития токсических реакций особенно увеличивается у пожилых пациентов с нарушенной функцией почек.
Во время пострегистрационного наблюдения были зарегистрированы следующие серьезные нежелательные реакции, в том числе угрожающие жизни или приводящие к летальному исходу: энцефалопатия (нарушение сознания, включая спутанность сознания, галлюцинации, ступор и кома), миоклонус, судороги и бессудорожный эпилептический статус.
Большинство случаев отмечалось у пациентов с почечной недостаточностью, которым не проводилась коррекция дозы. Тем не менее, в некоторых случаях нейротоксичность отмечалась у пациентов, которым проводилась коррекция дозы в зависимости от степени почечной недостаточности. В большинстве случаев симптомы нейротоксичности были обратимы и исчезали после отмены препарата и/или после проведения гемодиализа. Если нейротоксичность связана с применением цефепима, следует рассмотреть вопрос о прекращении терапии цефепимом или корректировать дозу у пациентов с почечной недостаточностью. Перед началом лечения следует установить наличие в анамнезе у пациента аллергических реакций на цефепим, другие цефалоспориновые антибиотики, пенициллины и другие бета-лактамные антибиотики, а также других форм аллергии. При применении всех видов бета-лактамных антибиотиков отмечались случаи развития тяжелых реакций гиперчувствительности, иногда с летальным исходом.
Антибиотики группы цефалоспоринов могут быть причиной ложноположительной реакции на глюкозу в моче в тестах, основанных на восстановлении ионов меди (с растворами Бенедикта или Фелинга или с таблетками Клинитест), но не в ферментных тестах (с глюкозоксидазой). В связи с этим для определения глюкозы в моче рекомендуется применять ферментные тесты с глюкозоксидазой.
При развитии аллергической реакции следует прекратить лечение препаратом и предпринять соответствующие меры. При развитии тяжелой аллергической реакции (например, анафилактической реакции) непосредственно во время введения препарата может потребоваться применение эпинефрина и другой поддерживающей терапии.
При назначении эмпирического лечения необходимо принимать во внимание данные о приобретенной устойчивости микроорганизмов-возбудителей.
Устойчивость микроорганизмов может изменяться с течением времени и географического положения. Для идентификации микроорганизма-возбудителя и определения чувствительности к цефепиму следует провести соответствующие тесты. Цефепим может применяться в виде монотерапии даже до идентификации микроорганизма-возбудителя, так как он обладает широким спектром антибактериального действия в отношении грамположительных и грамотрицательных микроорганизмов. При риске смешанной аэробно/анаэробной инфекции (особенно, когда могут присутствовать нечувствительные к цефепиму микроорганизмы) лечение препаратом цефепим в комбинации с препаратом, действующим на анаэробы, можно начинать до идентификации возбудителя.
После идентификации возбудителя и определения чувствительности к антибиотикам лечение следует проводить в соответствии с результатами тестов.
Как и при применении других антибиотиков, лечение препаратом Цефепим может приводить к колонизации нечувствительной микрофлоры. При развитии суперинфекций во время лечения необходимо принятие соответствующих мер.
В исследованиях на крысах не было отмечено влияния на фертильность. Данные о влиянии на фертильность у людей при применении цефепима отсутствуют.
Clostridium difficile — ассоциированная диарея
При применении практически всех антибиотиков широкого спектра действия возможно возникновение диареи, ассоциированной с Clostridium difficile (CDAD — Clostridium difficile-associated diarrhea), которая может протекать как в легкой форме, так и в тяжелой, вплоть до летального исхода.
При возникновении диареи во время лечения препаратом необходимо подтвердить диагноз CDAD. Следует тщательно наблюдать за пациентом на предмет развития CDAD, поскольку регистрировались случаи ее возникновения спустя более двух месяцев после прекращения применения антибиотиков. При подозрении на CDAD или подтверждении данного диагноза необходимо прекратить применение антибиотиков, кроме тех, которые назначены для подавления Clostridium difficile. Нельзя применять лекарственные средства, тормозящие перистальтику кишечника.
Влияние на способность управлять транспортными средствами, механизмами
Изучение влияние препарата на способность к концентрации внимания не проводилось, однако, учитывая возможность развития побочных эффектов со стороны центральной нервной системы, во время лечения препаратом следует воздержаться от управления транспортными средствами и занятий другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций.
Форма выпуска
Порошок для приготовления раствора для внутривенного и внутримышечного введения 0,5 г; 1,0 г; 2,0 г.
0,5 г или 1,0 г или 2,0 г действующего вещества во флаконы из трубки стеклянной для лекарственных средств вместимостью 10 мл, герметично укупоренные резиновыми пробками, обжатые колпачками алюминиевыми или комбинированными.
1; 5; 10 флаконов вместе с инструкцией по медицинскому применению укладывают в индивидуальную пачку из картона.
50 флаконов с приложением равного количества инструкций укладывают в коробку из картона (для стационаров).
Упаковка в комплекте с растворителем — водой для инъекций или 0,9 % раствором натрия хлорида. В комплект входят:
а) 1 флакон с препаратом по 0,5 г и 1 ампула с растворителем на 5 мл или 1 флакон с препаратом по 1,0 г или 2,0 г и 2 ампулы с растворителем на 5 мл;
б) 5 флаконов с препаратом по 0,5 г и 5 ампул с растворителем на 5 мл или 5 флаконов с препаратом по 1,0 г или 2,0 г и 10 ампул с растворителем на 5 мл;
в) 10 флаконов с препаратом по 0,5 г и 10 ампул с растворителем на 5 мл или 10 флаконов с препаратом по 1,0 г или 2,0 г и 20 ампул с растворителем на 5 мл.
Комплект укладывают в индивидуальную пачку из картона вместе с инструкцией по медицинскому применению, скарификатором ампульным.
При использовании ампул с надсечкой, кольцом излома или точкой излома скарификатор ампульный не вкладывают.
Условия хранения
В защищенном от света месте при температуре не выше 30°С.
Хранить в недоступном для детей месте.
Срок годности
3 года.
Не применять по истечении срока годности.
Условия отпуска
Отпускают по рецепту.
Владелец регистрационного удостоверения
ООО «ПРОМОМЕД РУС», Россия.
105005, г. Москва, ул. Почтовая М., дом 2/2, строение 1, пом I ком. 2.
Производитель
АО «Биохимик», Россия.
Юридический адрес: 430030, Республика Мордовия, г. Саранск, ул. Васенко, д. 15 А.
Адрес места производства: 430030, Республика Мордовия, г. Саранск, ул. Васенко, д. 15 А.
Организация, принимающая претензии потребителей
ООО «ПРОМОМЕД РУС», Россия.
129090, г. Москва, пр-т Мира, д.13, стр. 1.
Купить Цефепим Промомед в planetazdorovo.ru
*Цена в Москве. Точная цена в Вашем городе будет указана на сайте аптеки.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Цефепим
Cefepime
Регистрационный номер
Торговое наименование
Цефепим
Международное непатентованное наименование
Лекарственная форма
порошок для приготовления раствора для внутривенного и внутримышечного введения
Состав
Субстанция представляет собой стерильную смесь цефепима гидрохлорида моногидрата и L-аргинина:
| активное вещество: | ||
| цефепим | 0,5 г |
1,0 г |
| (в виде цефепима гидрохлорида моногидрата) | 0,5945 г |
1,1890 г |
| вспомогательное вещество: | ||
| L-аргинин | 0,3972 г |
0,7943 г |
Описание
Порошок от белого до светло-жёлтого цвета.
Фармакотерапевтическая группа
Код АТХ
Фармакологические свойства
Фармакодинамика
Цефепим является цефалоспориновым антибиотиком широкого спектра действия.
Цефепим подавляет синтез белков клеточной стенки бактерий, обладает широким спектром бактерицидного действия в отношении различных грамположительных и грамотрицательных бактерий, в том числе большинства штаммов, резистентных к аминогликозидам или цефалоспориновым антибиотикам третьего поколения, таким как цефтазидим. Цефепим высоко устойчив к гидролизу большинством бета-лактамаз, он имеет низкое сродство к бета-лактамазам и быстро проникает в клетки грамотрицательных бактерий.
Доказано, что цефепим обладает очень высоким сродством к пенициллин-связывающему белку (ПСБ) типа 3, высоким сродством — к ПСБ типа 2 и умеренным сродством — к ПСБ типов 1а и 1б.
Цефепим оказывает бактерицидное действие в отношении широкого спектра бактерий и активен в отношении следующих микроорганизмов:
Грамположительные аэробы:
Staphylococcus aureus (включая штаммы, продуцирующие бета-лактамазу); Staphylococcus epidermidis (включая штаммы, продуцирующие бета-лактамазу); другие штаммы Staphylococcus spp., включая Staphylococcus hominis, Staphylococcus saprophyticus;
Streptococcus pyogenes (стрептококки группы A);
Streptococcus agalactiae (стрептококки группы В);
Streptococcus pneumoniae (включая штаммы со средней устойчивостью к пенициллину — минимальная подавляющая концентрация от 0,1 до 1 мкг/мл); другие бета-гемолитические Streptococcus spp. (группы С, G, F), Streptococcus bovis (группа D), Streptococcus spp. группы Viridans.
Примечание: Большинство штаммов энтерококков, например, Enterococcus faecalis, и стафилококки, резистентные к метиллину, устойчивы к действию большинства цефалоспориновых антибиотиков, включая цефепим.
Грамотрицательные аэробы:
Acinetobacter calcoaceticus (подштаммы anitratus, Iwofii);
Aeromonas hydrophila;
Capnocytophaga spp.;
Citrobacter spp., включая Citrobacter diversus, Citrobacter freundii; Campylobacter jejuni;
Enterobacter spp., включая Enterobacter cloacae, Enterobacter aerogenes, Enterobacter sakazakii;
Escherichia coli;
Gardnerella vaginalis;
Haemophilus ducreyi;
Haemophilus influenza (включая штаммы, продуцирующие бета-лактамазу); Haemophilus parainfluenzae; Hafnia alvei;
Klebsiella spp., включая Klebsiella pneumoniae, Klebsiella oxytoca, Klebsiella ozaenae;
Legionella spp.;
Morganella morganii;
Moraxella catarrhalis (Branhamella catarrhalis) (включая штаммы, продуцирующие бета-лактамазы);
Neisseria gonorrhoeae (включая штаммы, продуцирующие бета-лактамазы); Neisseria meningitidis;
Pantoea agglomerans (ранее известный как Enterobacter agglomerans);
Proteus spp., включая Proteus mirabilis, Proteus vulgaris;
Providencia spp., включая Providencia rettgeri, Providencia stuartii;
Pseudomonas spp., включая Pseudomonas aeruginosa, Pseudomonas putida, Pseudomonas stutzeri;
Salmonella spp.;
Serratia, включая Serratia marcescens, Serratia liquefaciens;
Shigella spp.;
Yersinia enterocolitica.
Примечание: Цефепим неактивен в отношении многих штаммов Stenotrophomonas maltophilia (ранее известный как Xanthomonas maltophilia и Pseudomonas maltophilia).
Анаэробы:
Bacteroides spp.;
Clostridium perfringens;
Fusobacterium spp.;
Mobiluncus spp.;
Peptostreptococcus spp.;
Prevotella melaninogenica (известный как Bacteroides melaninogenicus);
Veillonella spp.
Примечание: Цефепим неактивен в отношении Bacteroides fragilis и Clostridium difficile.
Фармакокинетика
Средние концентрации цефепима в плазме крови взрослых здоровых мужчин в различные сроки после однократного внутривенного введения в течение 30 минут до 12 часов и максимальная концентрация (Cmax) приведены ниже в таблице.
Средние концентрации цефепима в плазме (мкг/мл) после внутривенного введения
| Доза цефепима | 0,5 ч | 1 ч | 2 ч | 4 ч | 8 ч | 12 ч | Сmах (мкг/мл) |
|---|---|---|---|---|---|---|---|
| 500 мг в/в | 38,2 | 21,6 | 11,6 | 5,0 | 1,4 | 0,2 | 39,1 ± 3,5 |
| 1 г в/в | 78,7 | 44,5 | 24,3 | 10,5 | 2,4 | 0,6 | 81,7 ± 5,1 |
| 2 г в/в | 163,1 | 85,8 | 44,8 | 19,2 | 3,9 | 1,1 | 163,9 ± 25,3 |
После внутримышечного введения цефепим всасывается полностью.
Cmax и время достижения максимальной концентрации в плазме крови (Tmax) после однократного внутримышечного введения приведены ниже в таблице.
Средние концентрации цефепима в плазме (мкг/мл) после внутримышечного введения
| Доза цефепима | 0,5 ч | 1 ч | 2 ч | 4 ч | 8 ч | 12 ч | Сmах (мкг/мл) | Тmах (ч) |
|---|---|---|---|---|---|---|---|---|
| 500 мг в/м | 8,2 | 12,5 | 12,0 | 6,9 | 1,9 | 0,7 | 13,9 ± 3,4 | 1,4 ± 0,9 |
| 1 г в/м | 14,8 | 25,9 | 26,3 | 16,0 | 4,5 | 1,4 | 29,6 ± 4,4 | 1,6 ± 0,4 |
| 2 г в/м | 36,1 | 49,9 | 51,3 | 31,5 | 8,7 | 2,3 | 57,5 ± 9,5 | 1,5 ± 0,4 |
Терапевтические концентрации цефепима обнаруживаются в следующих жидкостях и тканях: моче, желчи, перитонеальной и буллезной жидкостях, слизистой оболочке бронхов, мокроте, простате, аппендиксе и желчном пузыре. Связывание цефепима с белками сыворотки крови составляет в среднем 16,4 % и не зависит от концентрации препарата в сыворотке крови. Цефепим метаболизируется в N-метилпирролидин, который быстро превращается в оксид N-метилпирролидина.
Цефепим выводится преимущественно почками, путём клубочковой фильтрации (почечный клиренс составляет в среднем 110 мл/мин). В моче обнаруживается приблизительно 85 % от введённой дозы неизменённого цефепима, менее 1 % N-метилпирролидина, около 6,8 % оксида N-метилпирролидина и около 2,5 % эпимера цефепима.
После введения доз от 250 мг до 2 г период полувыведения цефепима из организма составляет в среднем около 2 часов. Общий клиренс составляет в среднем 120 мл/мин. При внутривенном введении препарата здоровым добровольцам в дозе 2 г каждые 8 часов в течение 9 дней кумуляции препарата не наблюдалось.
Пациенты с нарушениями функции почек
Период полувыведения из организма при почечной недостаточности увеличивается, при этом наблюдается линейная зависимость между общим клиренсом и клиренсом креатинина. При тяжёлых нарушениях функции почек, требующих проведения сеансов диализа, период полувыведения составляет в среднем 13 часов при гемодиализе и 19 часов при непрерывном перитонеальном диализе. При нарушенной функции почек требуется корректировка дозы.
Пациенты с нарушениями функции печени
Фармакокинетика цефепима у пациентов с нарушенной функцией печени не изменяется. Корректировки дозы для таких больных не требуется.
Пациенты старше 65 лет
После однократного внутривенного введения 1 г препарата здоровым добровольцам старше 65 лет отмечалось увеличение площади под кривой зависимости «концентрация — время» (AUC) и уменьшение почечного клиренса по сравнению с молодыми добровольцами. При нарушенной функции почек пациентам старшего возраста требуется корректировка дозы.
Дети
Фармакокинетика препарата исследовалась у детей в возрасте от 2 месяцев до 11 лет после однократного введения дозы 50 мг/кг массы тела внутривенно или внутримышечно, а также после повторного введения препарата (каждые 8–12 часов, в течение не менее 48 часов).
После однократного внутривенного введения общий клиренс и объём распределения составляли 3,3 мл/мин/кг и 0,3 л/кг, соответственно. Период полувыведения из организма составлял в среднем 1,7 часа. Выведение цефепима в неизменном виде почками составляло 60,4 % от введённой дозы, а почечный клиренс — в среднем 2,0 мл/мин/кг.
После многократного внутривенного введения концентрация цефепима в плазме крови в равновесном состоянии, а также другие фармакокинетические параметры не отличались от таковых после однократного введения. Возраст и пол пациентов не оказывали существенного влияния на общий клиренс и объём распределения, с учётом поправки на массу тела.
После внутримышечного введения максимальная концентрация цефепима в плазме крови в равновесном состоянии составляла в среднем 68 мкг/мл и достигалась в среднем за 0,75 часа. Через 8 часов после внутримышечного введения концентрации цефепима в плазме крови составляли в среднем 6 мкг/мл. Абсолютная биодоступность цефепима после внутримышечной инъекции составляла в среднем 82 %.
Концентрация препарата в спинномозговой жидкости (СМЖ) и в плазме крови у детей с бактериальным менингитом
| Время (часы) после введения | Концентрация в плазме (мкг/мл)** | Концентрация в СМЖ (мкг/мл)** | Отношение концентраций в СМЖ/плазма крови** |
|---|---|---|---|
| 0,5 | 67,1 ± 51,2 | 5,7 ± 0,14 | 0,12 ± 0,14 |
| 1 | 44,1 ± 7,8 | 4,3 ± 1,5 | 0,10 ± 0,04 |
| 2 | 23,9 ± 12,9 | 3,6 ± 2,0 | 0,17 ± 0,09 |
| 4 | 11,7 ± 15,7 | 4,2 ± 1,1 | 0,87 ± 0,56 |
| 8 | 4,9 ± 5,9 | 3,3 ± 2,8 | 1,02 ± 0,64 |
**возраст пациентов: 3,1 месяца — 12 лет, средний возраст: 3 года. Доза препарата 50 мг/кг массы тела при внутривенном введении в течение от 5 до 20 минут каждые 8 часов. Концентрация в плазме и СМЖ определялись в конце введения на 2 или 3 день лечения препаратом.
Показания
Инфекционно-воспалительные заболевания, вызванные чувствительными к цефепиму микроорганизмами, у взрослых:
- Инфекции нижних дыхательных путей, включая бронхит и пневмонию;
- Инфекции мочевыводящих путей, как осложнённые, включая пиелонефрит, так и неосложнённые;
- Инфекции кожи и мягких тканей;
- Инфекции брюшной полости, включая перитонит и инфекции желчных путей;
- Гинекологические инфекции;
- Септицемия;
- Фебрильная нейтропения;
- Профилактика инфекций при проведении полостных хирургических операций.
Инфекционно-воспалительные заболевания, вызванные чувствительными к цефепиму микроорганизмами, у детей:
- Пневмония;
- Инфекции мочевыводящих путей, как осложнённые, включая пиелонефрит, так и неосложнённые;
- Инфекции кожи и мягких тканей;
- Септицемия;
- Фебрильная нейтропения;
- Бактериальный менингит.
Противопоказания
- Повышенная чувствительность к цефепиму или L-аргинину, а также к антибиотикам цефалоспориновой группы, пенициллинам или к другим бета-лактамным антибиотикам;
- детский возраст до 2 мес.
С осторожностью
Заболевания желудочно-кишечного тракта (в том числе в анамнезе), особенно колит, почечная недостаточность (клиренс креатинина менее 50 мл/мин).
Применение при беременности и в период грудного вскармливания
В связи с тем, что адекватных и контролируемых клинических исследований у беременных женщин не проводилось, применение при беременности возможно только в тех случаях, когда предполагаемая польза для матери превышает потенциальный риск для плода.
При необходимости применения препарата во время грудного вскармливания следует решить вопрос о прекращении грудного вскармливания, так как цефепим обнаруживается в грудном молоке.
Способ применения и дозы
Внутривенно (в/в) или внутримышечно (в/м). Дозы и путь введения зависят от чувствительности возбудителей, тяжести инфекции, состояния функции почек и общего состояния больного.
Внутривенное введение рекомендуется для больных с тяжёлыми или угрожающими жизни инфекциями, особенно при угрозе возникновения септического шока.
Приготовление раствора для внутривенного введения
Препарат растворяют в 5 или 10 мл стерильной воды для инъекций, 5 % растворе декстрозы и 0,9 % растворе натрия хлорида для инъекций, как указано в приведенной ниже таблице, и вводят в течение 3–5 минут либо непосредственно в вену, либо в систему для внутривенного введения, через которую в организм пациента поступает совместимый раствор для внутривенного введения.
Приготовление раствора для внутривенной инфузии
Приготовленный раствор (см. выше) переносят в инфузионный сосуд с другими совместимыми растворами для внутривенных инфузий (см. ниже) и вводят в течение не менее 30 минут.
| Объём раствора для разведения (мл) | Приблизительный объём полученного раствора (мл) | Приблизительная концентрация цефепима (мг/мл) | |
|---|---|---|---|
| Внутривенное введение: | |||
| 500 мг/флакон | 5 | 5,7 | 90 |
| 1 г/флакон | 10 | 11,4 | 90 |
Растворы препарата с концентрацией 1–40 мг/мл совместимы со следующими парентеральными растворами: 0,9 % раствор натрия хлорида для инъекций; 5 % или 10 % раствор декстрозы для инъекций.
Внутримышечное введение: доза до 1 г (объём <3,1 мл) может быть введена в виде однократной инъекции. Максимальную дозу (2 г/6,2 мл) следует вводить в виде двух инъекций в разные места.
Приготовление раствора для внутримышечного введения
Препарат растворяют в стерильной воде для инъекций, 5 % растворе декстрозы или 0,9 % растворе натрия хлорида для инъекций, 0,5 % или 1 % растворе лидокаина, как указано ниже в таблице.
| Объём раствора для разведения (мл) | Приблизительный объём полученного раствора (мл) | Приблизительная концентрация цефепима (мг/мл) | |
|---|---|---|---|
| Внутримышечное введение: | |||
| 500 мг/флакон | 1,5 | 2,2 | 230 |
| 1 г/флакон | 3,0 | 4,4 | 230 |
Хранение растворов для внутривенного и внутримышечного введения
Применяется только свежеприготовленный раствор.
Как и все растворы для парентерального применения, перед введением приготовленные растворы препарата следует проверить на отсутствие видимых механических включений. В противном случае запрещается использовать приготовленный раствор.
Режимы дозирования цефепима в зависимости от заболевания, массы тела и возраста пациента
Доза для детей не должна превышать максимальную рекомендуемую дозу для взрослых (2 г в/в, каждые 8 часов). Опыт внутримышечного введения препарата детям ограничен.
Взрослые и дети с массой тела более 40 кг при нормальной функции почек
| Инфекции мочевых путей лёгкой и средней тяжести: | 500 мг — 1 г в/в или в/м | каждые 12 часов |
| Другие инфекции лёгкой и средней тяжести: | 1 г в/в или в/м | каждые 12 часов |
| Тяжёлые инфекции: | 2 г в/в | каждые 12 часов |
| Очень тяжёлые и угрожающие жизни инфекции: | 2 г в/в | каждые 8 часов |
Обычная продолжительность лечения составляет 7–10 дней; при тяжёлых инфекциях может потребоваться более продолжительное лечение.
В случае лечения фебрильной нейтропении обычная продолжительность лечения составляет 7 дней или до исчезновения нейтропении.
Профилактика инфекций при проведении хирургических операций
За 60 минут до начала хирургической операции вводят 2 г препарата внутривенно в виде инфузии, в течение 30 минут. Сразу после окончания инфузии пациенту вводят 500 мг метронидазола внутривенно. Раствор метронидазола готовят в соответствии с инструкцией по его применению. Вследствие фармацевтической несовместимости метронидазола и цефепима их не следует смешивать в одном сосуде. Инфузионную систему перед введением метронидазола следует промыть. Во время длительных (более 12 часов) хирургических операций через 12 часов после первой дозы рекомендуется повторное введение цефепима в той же дозе с последующим введением метронидазола.
Дети от 2 месяцев с массой тела до 40 кг
При инфекциях мочевых путей, инфекциях кожи и мягких тканей, пневмонии рекомендуемая доза составляет 50 мг/кг каждые 12 часов в течение 10 дней. В случае тяжёлых инфекций — каждые 8 часов.
Пациентам с фебрильной нейтропенией, септицемией, бактериальным менингитом следует вводить 50 мг/кг каждые 8 часов в течение 7–10 дней.
Пациенты с нарушением функции почек
Больным с нарушением функции почек требуется корректировка дозировки цефепима с целью компенсации уменьшенной скорости выведения препарата с мочой. Режим дозирования зависит от степени нарушения функции почек, тяжести инфекции и чувствительности микроорганизмов. При слабых или умеренных нарушениях функции почек начальная доза препарата такая же, как при нормальной функции почек.
Рекомендуемые поддерживающие дозы цефепима в зависимости от клиренса креатинина представлены в таблице ниже.
Клиренс креатинина для мужчин рассчитывают, исходя из концентрации сывороточного креатинина, по следующей формуле:
Клиренс креатинина (мл /мин) = Масса тела (кг) × (140 — возраст)/ [72 × сывороточный креатинин (мг/дл)]
Клиренс креатинина для женщин рассчитывают по той же формуле, используя фактор 0,85.
| Клиренс креатинина (мл/мин) | Рекомендуемые поддерживающие дозы | |||
|---|---|---|---|---|
| (Обычная доза, корректировки дозы не требуется) | ||||
| >60 |
2 г каждые 8 ч |
2 г каждые 12 ч |
1 г каждые 12 ч |
500 мг каждые 12 ч |
| 30–60 |
2 г каждые 12 ч |
2 г каждые 24 ч |
1 г каждые 24 ч |
500 мг каждые 24 ч |
| 11–29 |
2 г каждые 24 ч |
1 г каждые 24 ч |
500 мг каждые 24 ч |
500 мг каждые 24 ч |
| ≤11 |
1 г каждые 24 ч |
500 мг каждые 24 ч |
250 мг каждые 24 ч |
250 мг каждые 24 ч |
| При непрерывном амбулаторном перитонеальном диализе |
2 г каждые 48 ч |
2 г каждые 48 ч |
1 г каждые 48 ч |
500 мг каждые 48 ч |
| Пациенты на гемодиализе* |
500 мг каждые 24 ч |
500 мг каждые 24 ч |
500 мг каждые 24 ч |
500 мг каждые 24 ч |
* Для пациентов на гемодиализе рекомендуется: 1 г в первый день лечения и затем по 500 мг каждые 24 ч при всех инфекциях, за исключением ферильной нейтропении, где доза составляет 1 г каждые 24 ч. В дни гемодиализа препарат следует вводить по окончании гемодиализа. По возможности препарат следует вводить в одно и то же время каждый день.
При гемодиализе в течение 3 ч из организма удаляется приблизительно 68 % введённой дозы препарата.
Дети с нарушением функции почек
Детям при нарушенной функции почек рекомендуется уменьшение дозы или увеличение интервала между введениями, как указано выше в таблице.
Клиренс креатинина вычисляется по следующим формулам:
Клиренс креатинина (мл / мин /1,732) =0,55 × рост (см)/ сывороточный креатинин (мг/дл)
или
Клиренс креатинина (мл /мин /1,732) = [0,52 × рост (см)/ сывороточный креатинин (мг/ дл)] — 3,6.
Пациенты с нарушением функции печени
Коррекции дозы для пациентов с нарушением функции печени не требуется.
Побочное действие
Наиболее часто отмечаются побочные эффекты со стороны желудочно-кишечного тракта и аллергические реакции.
Ниже перечислены побочные эффекты по органам и системам в соответствии с их частотой: очень частые (≥10 %); частые (≥1 % и <10 %); нечастые (≥ 0,1 % и <1 %); редкие (≥0,01 % и 0,1 %); частота неизвестна (нет данных о частоте развития данного побочного эффекта).
Инфекции: нечасто — кандидоз слизистой оболочки полости рта, вагинальные инфекции; редко — кандидозы.
Аллергические реакции: часто — высыпания на коже; нечасто — эритема, крапивница, зуд; редко — анафилактические реакции; частота неизвестна — анафилактический шок, токсический эпидермальный некролиз, мультиформная эритема, синдром Стивенса-Джонсона.
Со стороны центральной нервной системы: нечасто — головная боль; редко — судороги, парестезии, дисгезии, головокружение; частота неизвестна — спутанность сознания, кратковременная потеря сознания, галлюцинации, кома, ступор, энцефалопатия, миоклонические судороги.
Со стороны сосудов: редко — вазодилатация; частота неизвестна — кровотечения.
Со стороны респираторной системы: редко — одышка.
Со стороны желудочно-кишечного тракта: часто — диарея; нечасто — тошнота, рвота, колит (включая псевдомембранозный колит); редко — абдоминальные боли, запор; частота неизвестна — нарушения пищеварения.
Со стороны мочевыделительной системы: частота неизвестна — почечная недостаточность, токсическая нефропатия.
Общие реакции и реакции в месте введения: часто — флебит в месте введения, боль в месте введения; нечасто — повышение температуры и воспаление в месте введения; редко — озноб.
Прочие: редко — генитальный зуд, изменение вкуса, вагинит, эритема, ложноположительная проба Кумбса без гемолиза.
Изменения со стороны лабораторных показателей: часто — повышение активности аланинаминотрансферазы, аспартатаминотрансферазы, щелочной фосфатазы, общего билирубина, анемия, эозинофилия, увеличение протромбинового времени или частичного тромбопластинового времени; нечасто — повышение азота мочевины крови, креатинина сыворотки, тромбоцитопения, лейкопения и нейтропения; частота неизвестна — апластическая анемия, гемолитическая анемия, агранулоцитоз.
Пострегистрационный опыт: энцефалопатия (нарушение сознания, включая спутанность сознания, галлюцинации, ступор и кома), миоклонус, судороги и бессудорожный эпилептический статус. Несмотря на то, что большинство случаев отмечались у пациентов с почечной недостаточностью, которые получали цефепим в дозах выше рекомендованных, в некоторых случаях нейротоксичность отмечалась у пациентов, которым проводилась коррекция дозы в зависимости от степени почечной недостаточности.
Передозировка
Симптомы (чаще возникают у больных с хронической почечной недостаточностью): судороги, энцефалопатия, сопровождающаяся галлюцинациями, нарушением сознания, ступором, комой, миоклонией, эпилептиформными приступами, нервно-мышечным возбуждением.
Лечение: следует прекратить введение препарата и провести симптоматическую терапию. Применение гемодиализа ускоряет удаление цефепима из организма.
Взаимодействие с другими лекарственными средствами
Данные по совместимости растворов цефепима и других лекарственных препаратов приведены в таблице ниже:
| Концентрация цефепима | Название/концентрация другого препарата в смеси | Инфузионный раствор |
|---|---|---|
| 40 мг/мл | Амикацин 6 мг/мл | 0,9 % натрия хлорид или 5 % декстроза |
| 40 мг/мл | Ампициллин 1 мг/мл | 5 % декстроза |
| 40 мг/мл | Ампициллин 10 мг/мл | 5 % декстроза |
| 40 мг/мл | Ампициллин 1 мг/мл | 0,9 % натрия хлорид |
| 40 мг/мл | Ампициллин 10 мг/мл | 0,9 % натрия хлорид |
| 4 мг/мл | Ампициллин 40 мг/мл | 0,9 % натрия хлорид |
| 4–40 мг/мл | Клиндамицин 0,25–6 мг/мл | 0,9 % натрия хлорид или 5 % декстроза |
| 4 мг/мл | Гепарин 10–50 ЕД/мл | 0,9 % натрия хлорид или 5 % декстроза |
| 4 мг/мл | Калия хлорид 10–40 мэкв/л | 0,9 % натрия хлорид или 5 % декстроза |
| 4 мг/мл | Теофиллин 0,8 мг/мл | 5 % декстроза |
Диуретики, аминогликозиды, полимиксин B снижают канальцевую секрецию цефепима и повышают его концентрацию в сыворотке крови, удлиняют Т½, усиливают нефротоксичность (повышая риск развития нефронекроза). Цефепим повышает ототоксичность аминогликозидов.
Нестероидные противовоспалительные препараты, замедляя выведение цефалоспоринов, повышают риск развития кровотечения. При одновременном применении с бактерицидными антибиотиками (аминогликозиды) проявляется синергизм, с бактериостатическими (макролиды, хлорамфеникол, тетрациклины) — антагонизм.
Несовместим с раствором метронидазола (перед введением раствора метронидазола для профилактики инфекций при проведении хирургических вмешательств следует промыть инфузионную систему от раствора цефепима).
Во избежание возможного лекарственного взаимодействия с другими препаратами, растворы цефепима (как и большинство других бета-лактамных антибиотиков) не должны вводиться одновременно с растворами ванкомицина, гентамицина, тобрамицина, нетилмицина. При назначении цефепима с перечисленными препаратами следует вводить каждый антибиотик отдельно.
Особые указания
При наличии факторов способных вызвать нарушение функции почек, требуется корректировка дозы цефепима с целью компенсации уменьшенной скорости выведения препарата с мочой. Режим дозирования зависит от степени почечной недостаточности, тяжести инфекции и чувствительности микроорганизмов. При слабых или умеренных нарушениях функции почек начальная доза препарата такая же, как при нормальной функции почек. Риск развития токсических реакций особенно увеличивается у пожилых пациентов с нарушенной функцией почек.
Во время пострегистрационного наблюдения были зарегистрированы следующие серьёзные нежелательные реакции, в том числе угрожающие жизни или приводящие к летальному исходу: энцефалопатия (нарушение сознания, включая спутанность сознания, галлюцинации, ступор и кома), миоклонус, судороги и бессудорожный эпилептический статус (см. раздел «Побочное действие»: Пострегистрационный опыт). Большинство случаев отмечались у пациентов с почечной недостаточностью, которым не проводилась коррекция дозы. Тем не менее в некоторых случаях нейротоксичность отмечалась у пациентов, которым проводилась коррекция дозы в зависимости от степени почечной недостаточности. В большинстве случаев симптомы нейротоксичности были обратимы и исчезали после отмены препарата и/или после проведения гемодиализа. Если нейротоксичность связана с применением цефепима, следует рассмотреть вопрос о прекращении терапии цефепимом или корректировать дозу у пациентов с почечной недостаточностью.
Перед началом лечения следует установить наличие в анамнезе у больного аллергических реакций на цефепим, другие цефалоспориновые антибиотики, пенициллины и другие бета-лактамные антибиотики, а также других форм аллергии. При развитии аллергической реакции следует прекратить лечение препаратом и предпринять соответствующие меры. При развитии тяжёлой аллергической реакции (например, анафилактической реакции) непосредственно во время введения препарата может потребоваться применение эпинефрина и другой поддерживающей терапии.
При назначении эмпирического лечения необходимо принимать во внимание данные о приобретённой устойчивости микроорганизмов-возбудителей. Устойчивость микроорганизмов может изменяться с течением времени и географического положения. Для идентификации микроорганизма-возбудителя и определения чувствительности к цефепиму следует провести соответствующие тесты. Цефепим может применяться в виде монотерапии даже до идентификации микроорганизма-возбудителя, так как он обладает широким спектром антибактериального действия в отношении грамположительных и грамотрицательных микроорганизмов. При риске смешанной аэробно/анаэробной инфекции (особенно, когда могут присутствовать нечувствительные к цефепиму микроорганизмы) лечение препаратом цефепим в комбинации с препаратом, действующим на анаэробы, можно начинать до идентификации возбудителя.
После идентификации возбудителя и определения чувствительности к антибиотикам лечение следует проводить в соответствии с результатами тестов. Как и при применении других антибиотиков, лечение препаратом цефепим может приводить к колонизации нечувствительной микрофлоры. При развитии суперинфекций во время лечения необходимо принятие соответствующих мер.
Clostridium difficile — ассоциированная диарея
При применении практически всех антибиотиков широкого спектра действия возможно возникновение диареи, ассоциированной с Clostridium difficile (CDAD — Clostridium difficile — associated diarrhea), которая может протекать как в лёгкой форме, так и в тяжёлой, вплоть до летального исхода.
При возникновении диареи во время лечения препаратом необходимо подтвердить диагноз CDAD. Следует тщательно наблюдать за больным на предмет развития CDAD, поскольку регистрировались случаи её возникновения спустя более двух месяцев после прекращения применения антибиотиков. При подозрении или подтверждении CDAD необходимо прекратить применение антибиотиков, кроме тех, которые назначены для подавления Clostridium difficile.
Влияние на способность управлять транспортными средствами, механизмами
Учитывая возможность развития побочных эффектов со стороны нервной системы, пациентам следует соблюдать осторожность при управлении транспортными средствами и при других потенциально опасных видах деятельности.
Форма выпуска
Порошок для приготовления раствора для внутривенного и внутримышечного введения, 0,5 г и 1,0 г.
По 0,5 г или 1,0 г цефепима во флаконы стеклянные (вместимостью 10 мл) типа ФО, FLP-10, 10R или 10Н, укупоренные резиновыми пробками и обжатые алюминиевыми колпачками.
По 1 или 10 флаконов вместе с инструкцией по медицинскому применению помещают в пачку из картона.
По 10 флаконов вместе с инструкцией по медицинскому применению помещают в пачку из картона с картонным вкладышем для фиксации флаконов.
Для стационаров: по 50 или 270 флаконов вместе с равным количеством инструкций по медицинскому применению помещают в коробку из картона.
Хранение
В защищённом от света месте, при температуре не выше 25 °C.
Хранить в недоступном для детей месте.
Срок годности
2 года.
Не использовать после истечения срока годности, указанного на упаковке.
Условия отпуска из аптек
Отпускают по рецепту
