Фармакологическое действие
Средство растительного происхождения. Циклоартановые тритерпеноиды, в т.ч. шенгманол, ацетилшенгманол, оказывают гипотензивное и седативное действие, повышают сократимость миокарда, не влияя на ЧСС. В сочетании с сапонинами и фитостерином они проявляют гиполипидемическую, антиоксидантную и ангиопротекторную активность.
Оказывает эстрогеноподобное действие за счет связывания с эстрогеновыми рецепторами гипоталамических нейронов (воздействуя на систему гипоталамус-гипофиз-яичники). Это приводит к уменьшению выделения ГнРГ и последующему снижению секреции ЛГ передней долей гипофиза. Снижение выброса гонадотропинов ведет к устранению психоэмоциональных и вегето-сосудистых нарушений, возникающих в преклимактерический и климактерический периоды и обусловленных резким снижением продукции эстрогенов с одновременным увеличением секреции ЛГ и ФСГ.
Повышает диурез, увеличивает секрецию пищеварительных желез, расслабляет гладкие мышцы кишечника и мочевыводящих путей, оказывает жаропонижающее и противовоспалительное действие.
Показания активного вещества
ЦИМИЦИФУГА
Вегето-сосудистые расстройства в период менопаузы, пре- и постменопаузы («приливы», повышенная потливость, нарушение сна, повышенная нервная возбудимость, изменения настроения, апатия и др.) в составе комплексной терапии.
Режим дозирования
Внутрь. Дозу и длительность терапии определяют индивидуально, в зависимости от показаний, ответа на лечение и применяемой лекарственной формы.
Побочное действие
Возможно: аллергические реакции.
Редко: боли в эпигастральной области, увеличение массы тела.
Очень редко: чувство напряжения в молочных железах и менструальноподобные кровотечения.
Противопоказания к применению
Повышенная чувствительность к цимицифуге; эстроген-зависимые опухоли; беременность, период грудного вскармливания; возраст до 18 лет; алкоголизм (для лекарственных форм, в состав которых входит этанол).
С осторожностью: нарушения функции печени, эпилепсия, черепно-мозговая травма, заболевания головного мозга.
Применение при беременности и кормлении грудью
Противопоказано применение при беременности и в период лактации (грудного вскармливания). При необходимости применения в период лактации следует решить вопрос о прекращении грудного вскармливания.
Применение при нарушениях функции печени
С осторожностью применяют у пациентов с нарушениями функции печени.
Применение у детей
Противопоказано применение у детей и подростков в возрасте до 18 лет.
Особые указания
При гастритах с повышенной секрецией применять с осторожностью.
Продолжительность лечения не должна превышать 3 месяцев без консультации врача.
При наступлении беременности необходимо прекратить прием средства и обратиться к врачу.
При изменении характера менструального цикла (нарушение или возобновление менструаций) необходимо проконсультироваться с врачом.
Статьи
Опубликовано в журнале:
«Русский медицинский журнал», 2008, Том 16, №20, с. 3-11
В. Вуттке1, К. Горков2, Д. Сейдлова–Вуттке1
1 Университет в Геттингене, Германия 2 «Бионорика», Ноймаркт, Германия
Из–за повышенного риска рака молочной железы и сердечно–сосудистых заболеваний, таких как инфаркт миокарда или инсульт [7–11], перевешивающих доказанную эффективность гормональной терапии (ГТ) в отношении проявлений климакса, ее положительное влияние на метаболизм в костной ткани и состояние слизистой оболочки влагалища [1–6], пациентки все реже соглашаются на этот вид лечения. Поэтому и врачи, и больные стараются найти альтернативные эстрогенам препараты, прием которых позволил бы купировать симптомы менопаузы и поддерживать прочность костной ткани. Такой альтернативой мог бы быть селективный модулятор рецептора эстрогенов, который подавлял бы проявления климакса и оказывал бы положительное влияние на костную ткань; при этом он был бы лишен неблагоприятных эффектов в отношении ткани молочной железы и матки, характерных для эстрогенов [12,13].
В этом плане весьма перспективны препараты растительного происхождения, поскольку есть убедительные данные в пользу того, что использование некоторых травяных экстрактов облегчает симптоматику климактерического синдрома и улучшает метаболизм в костной ткани у женщин постменопаузального возраста. Одним из таких растительных препаратов является вытяжка из корневищ цимицифуги (Cimicifuga racemosa, клопогон кистевидный). Его эффективность доказана результатами нескольких клинических испытаний; их отрицательна сторона – открытый дизайн или отсутствие плацебо–контроля [14–16]. Лишь однажды проводилось двойное слепое плацебо–контролируемое исследование, в ходе которого удалось продемонстрировать эффективность цимицифуги в отношении проявлений климакса по сравнению с плацебо [17]. При этом, однако, удваивали рекомендуемую суточную дозу (что соответствовало 80 мг растительного препарата вместо стандартных 40 мг). В дальнейшем была предпринята попытка сопоставить эффекты лечения экстрактом цимицифуги BNO 1055 (Климадинон® Бионорика АГ, Германия), с одной стороны, и конъюгированными эстрогенами и плацебо, с другой [18]. Эффективность экстракта цимицифуги BNO 1055 и конъюгированных эстрогенов оказалась сравнимой и значительно превосходила таковую плацебо в отношении проявлений климактерического синдрома. Но в отличие от конъюгированных эстрогенов, плацебо и экстракт цимицифуги BNO 1055 не вызывали утолщения эндометрия.
Исследования на доклиническом этапе, проведенные за последние 10 лет, позволили больше узнать об эффектах экстракта цимицифуги. В опытах in vitro по связыванию экстракта цимицифуги с рекомбинантными рецепторами эстрогенов (ЭРα и ЭРβ) было установлено, что экстракт не связывает ни один из двух эстрогеновых рецепторов. Согласно результатам экспериментов на грызунах экстракт цимицифуги не имеет утеротропного действия [19,20]. На основании этих данных был сделан вывод о том, что экстракты цимицифуги не содержат эстрогеноподобных компонентов, хотя экстракт цимицифуги BNO 1055 замещает радиоактивно меченный 17β–эстрадиол (Е2) в цитозольных препаратах матки свиньи и эндометрия человека [21]. Следовательно, можно предполагать, что пока неизвестные составляющие экстракта цимицифуги BNO 1055 способны взаимодействовать с пока не выявленным эстроген–связывающим белком.
У крыс экстракт цимицифуги BNO 1055 оказывает благоприятное воздействие на гипоталамус, подавляя пульсирующее высвобождение лютеинизирующего гормона (ЛГ), а возможно – и приливы [22]. Экстракты цимицифуги содержат компоненты, связывающие серотониновые рецепторы, и не исключено, что это и есть механизм, благодаря которому приливы ослабевают [23]. Однако Е2 и экстракт цимицифуги BNO 1055 одинаковым образом модулируют экспрессию в костной ткани двух генов, регулируемых эстрогенами. Эффекты экстракта цимицифуги BNO 1055 и Е2 наблюдали в костной ткани у крыс после удаления яичников, недостаточность которых восполняли обоими препаратами на протяжении 12 недель [19]. Оба препарата тормозили экспрессию генов IGF1 и TRAP [19,22]. Все это указывает на то, что на фоне такого лечения активность остеобластов и остеокластов, повышенная вследствие овариэктомии, восстанавливается до нормальных значений, как у интактных животных. У грызунов, которым вводили Е2 и экстракт цимицифуги BNO 1055, Е2 практически полностью предотвращал более чем 50%–ю потерю минеральной плотности костной ткани метафиза большеберцовой кости, в то время как у крыс, получавших экстракт цимицифуги BNO 1055, этот эффект оказался частичным, но все же значимым при сравнении с контрольной группой [19,24]. Также продемонстрировано положительное влияние экстракта цимицифуги на уровень маркеров метаболизма костной ткани и минеральную плотность бедренной кости [25].
Во влагалище Е2 обусловливает пролиферацию эпителия, что способствует выработке бактериями лактата с закислением среды, не допуская тем самым восходящего бактериального инфицирования матки. Тот же самый эффект, хотя и слабовыраженный, можно наблюдать у женщин, принимающих экстракт цимицифуги. В опытах на крысах с удаленными яичниками показано наличие умеренного вагинотропного действия у экстракта цимицифу-ги BNO 1055 [22]. Эстрогены повышают активность системы свертывания крови, что может спровоцировать тромбоэмболию. О наличии таких побочных эффектов у цимицифуги информации нет.
С учетом благоприятного влияния экстракта цимицифуги BNO 1055, а также отсутствия у него эстрогеноподобного действия в отношении матки и эндометрия можно предположить, что этот экстракт обладает органной селективностью [19,22], хотя ее механизмы пока не изучены. Эта активность не опосредована ни одним из двух описанных эстрогеновых рецепторов, но, возможно, связана со стимуляцией их активизирующих и/или подавляющих посредников.
Определенные опасения вызывает предполагаемая гепатотоксичность препаратов цимицифуги, поскольку сообщается о развитии острой печеночной недостаточности, ассоциированной с применением этой растительной добавки [26]. Вопрос о гепатотоксичности интенсивно обсуждался на последнем симпозиуме Националь ного центра нетрадиционной и альтернативной медицины/Национальных институтов здоровья (http://nccam.nih.gov/news/pastmeetings/blackcohosh_mtn gsumm.htm), и было выдвинуто предложение соблюдать необходимые параметры безопасности в ходе проведения клинических исследований. Таким образом, анализируя влияние спиртового экстракта цимицифуги BNO 1055 на проявления климактерического синдрома, также необходимо обращать внимание на параметры анализа крови, которые могли бы указывать на гепатотоксичность. Учитывая скудность информации, касающейся эффектов цимицифуги в отношении остеопороза и состояния слизистой влагалища, а также недостаточность сведений по действию цимицифуги на содержание липидов в крови или факторов гемостаза, ниже будут представлены и эти данные по пациенткам.
Методы
Первичные конечные точки этого двойного слепого плацебо–контролируемого исследования описаны ранее [18]. Вторичной задачей приводимой работы являлось сравнительное изучение влияния экстракта цимицифуги BNO 1055 на уровень маркеров метаболизма костной ткани, менопаузального гормона, связывающего половые гормоны глобулина (ГСПГ) и липидов, а также на цитологию эпителия влагалища и результаты стандартных лабораторных анализов относительно конъюгированных эстрогенов и плацебо.
Дизайн исследования
Описание методов рандомизированного двойного слепого сравнения экстракта цимицифуги BNO 1055 с конъюгированными эстрогенами и плацебо приведено в ранних работах [18]. Ниже представлены сокращенные методы, а основной акцент сделан на специфических показателях, которые упоминались выше.
Исследование проводилось в период с 1998 по 2000 г. в 13 исследовательских центрах Чехии в соот ветствии с положениями Хельсинкской Декларации и Правилами надлежащей клинической практики ICH–GCP. Объем выборки (по 30 женщин в постменопаузе на каждую группу лечения) формировали в зависимости от показателя клинически достоверных различий по первичной конечной точке – ослаблению симптоматики климактерического синдрома, которую определяли по первой версии рейтинговой шкалы постменопаузы [27].
Сбалансированность всех трех групп лечения обеспечивалась перестановочной блоковой рандомизацией [28]. Продолжительность лечения составила 12 недель. Медицинские осмотры и лабораторные анализы крови проводили за 2 недели до начала основных испытаний (в момент старта подготовительной фазы), на 0 неделе (исходно), а затем через 4, 8 и 12 недель.
Перед проведением всех медицинских измерений, связанных с исследованием, всех пациенток информировали в устной или печатной форме о целях исследования, его особенностях, сопряженном риске и преимуществах, длительности лечения и его альтернативах, после чего испытуемые давали добровольное информирование согласие в письменном виде.
Критерии включения и исключения
Критериями включения являлись: наличие менопаузы; возраст от 40 до 60 лет; срок с момента последних менструаций не менее 6 месяцев; индекс массы тела ≤30 кг/м2; концентрация постменопаузального уровня гормонов (Е2) ≤40 пг/мл и уровень фолликулостимулирующего гормона (ФСГ) ≥25 мМЕ/мл в начале подготовительного периода (неделя –2) и на исходном этапе (неделя 0); по меньшей мере, 3 эпизода приливов в сутки в ходе подготовительного периода (согласно записям в дневниках); сумма баллов по первым шести пунктам рейтинговой шкалы менопаузы (MRS) ≥1,7 на неделе –2 и 0, количество баллов по первому пункту шкалы MRS (приливы) ≥0,3 на неделе –2 и 0. Критерии исключения перечислены в таблице 1.
Таблица 1. Критерии исключения
- Овуляторные или ановуляторные циклы в течение подготовительного этапа исследования (признаком которых являются влагалищные кровотечения, уровень Е2>40 пг/мл и ФСГИндекс массы тела >30 кг/м2 (изначально не рассматривался как критерий исключения, но затем такие женщины были исключены из испытаний вследствие повышенного риска гипертрофии эндометрия и меньшей вероятности развития остеопороза по причине выработки эстрогенов в жировой ткани; все это объединяло таких пациенток в отдельную подгруппу, и их распределение между когортами лечения было бы неравномерным)
- Гистерэктомия в анамнезе
- Отсутствие ответа на терапию эстрогенами в прошлом
- Любые противопоказания к лечению эстрогенами или про-гестинами
- Генитальные кровотечения неясного генеза
- Подозрение на эстроген–зависимую карциному молочной железы и/или эндометрия (или верифицированный диагноз)
- Толщина эндометрия >5 мм
- Эндометриоз
- Тромбоэмболии в анамнезе и на момент обследования
- Флебиты
- Острая или хроническая печеночная недостаточность
- Нарушение метаболизма желчных пигментов
- Сахарный диабет
- Серповидно–клеточная анемия
- Клинически значимая гипертриглицеридемия или гиперхолестеринемия
- Перенесенный инфаркт миокарда
- Опухоли половых органов
- Выраженная варикозная болезнь вен
- Доказанная гиперчувствительность к изучаемым препаратам или их компонентам
- Сопутствующее лечение эстрогенами
- Сопутствующее лечение психотропными препаратами, антидепрессантами и успокоительными средствами, прием снотворных
- Неудовлетворительное общее состояние, алкогольная и/или наркотическая зависимость
Изучаемые препараты
Изучаемые препараты представляли собой твердые желатиновые капсулы со стеаратом магния и лактозой в качестве наполнителя. Все капсулы имели одинаковый размер, форму, вес, внешний вид и вкус. Суточная доза равнялась двум капсулам. Женщины из первой группы получали препарат с лиофилизированной водно–спиртовой (58% объема) вытяжкой BNO 1055 из корневищ Cimicifuga racemosa (цимицифуга; Климадинон, Bionorica AG, Ноймаркт, Германия). Каждая капсула (серийный номер 805005) содержала 1,66–2,86 мг нативного экстракта, что соответствовало 20 мг растительного препарата.
Пациентки второй группы принимали суточную дозу из двух капсул, в состав которых входило по 0,3 мг конъюгированных эстрогенов. Эти капсулы (серийный номер 71011210) представляли собой эстрофеминал (Heinrich Mack Nachf., иллертиссен, Германия), включающий эстрон (75–85%), эквилин (6–15%), эквиленин (до 4%), эстрадиол–17α, 17α–дигидроэквилин и 17α–дигидроэквиленин (2–8%). В третьей группе использовали капсулы с плацебо (серийный номер 805001).
После завершения подготовительного этапа длительностью 2 недели испытуемые начинали принимать изучаемый препарат (день 0). Их подвергали рандомизации, а затем выдавали первую упаковку лекарственного средства. Запакованные и помеченные индивидуальные контейнеры с 70 капсулами распределяли на неделе 0 (на недели 1–4), 4 (на недели 5–8) и 8 (на недели 9–12).
Изучаемые препараты изготавливали в соответствии со стандартами качественного производства GMP. Сертификаты анализов, проводимых до и в процессе исследования, а также описания изучаемых препаратов были подшиты к остальной документации.
Исследуемые параметры
Для определения уровня маркеров метаболизма костной ткани – щелочной фосфатазы костной ткани, (ЩФКТ) как критерия остеогенеза, и С–концевых телопептидов коллагена I типа (CrossLaps), как критерия резорбции костной ткани – эстрадиола 17β (иммунореактивного), Л Г, ФСГ и SHBG, а также параметров жирового обмена (общий холестерин, липопротеиды высокой плотности/ЛВП, липопротеиды низкой плотности/ЛНП, триглицериды) исходно и на 4, 8 и 12–й неделях утром натощак у испытуемых брали анализы крови. Поскольку концентрации Е2 и ФСГ являлись основными критерием включения, их дополнительно измеряли за 2 недели до начала основной фазы (неделя –2). Содержание гормонов и CrossLaps анализировали на приборе ELECSYS System (Roche–Diagnostics, Мангейм, Германия), уровень ЩФКТ – с помощью ферментного метода (Hitachi/Roche–Diagnostics, Мангейм, Германия), а показатели жирового обмена – с помощью цветных ферментных тестов. Спецификации исследований представлены в таблице 2.
Таблица 2. Параметры анализов крови
| Параметр анализа/ переменная |
Е2 (пг/мл) |
ФСГ (мМЕ/мл) | ЛГ (мМЕ/мл) | ГСПГ (нмоль/л) | ЩФКТ (Ед/л) | CrossLaps (нг/мл) | Холестерин (мг/дл) | ЛПВП (мг/дл) | ЛПНП (мг/дл) | Триглице-риды (мг/дл) |
| Чувствительность | <5 | <0,1 | 0,3 | 0,35 | 0,01 | 0,01 | 3 | 3 | 3 | 4 |
| Коэффициент вариации | <5% | <5% | <5% | <4% | <1% | <7% | <3% | <2% | <2% | <3% |
Исходно (неделя 0) и через 12 недель устанавливали степень зрелости эпителия влагалища (как меру влияния эстрогенов) с использованием т.н. индекса зрелости [29]. Для этого специальной щеточкой делали соскоб клеток эпителия влагалища, наносили их мазком на предметное стекло микроскопа, сразу же фиксировали и окрашивали по Папаниколау. Для определения индекса зрелости подсчитывали процентное соотношение парабазальных, промежуточных и поверхностных клеток (на 500 клеток).
Исходно и после завершения лечения оценивали стандартные лабораторные показатели безопасности (креатинин, мочевина, мочевая кислота, общий белок, натрий, калий, кальций, железо, общий билирубин, АСТ, АЛТ, γ–ГТ, ЩФ, глюкоза) и проводили развернутый анализ крови (эритроциты, лейкоциты, тромбоциты, формула крови, гемоглобин, гематокрит). В эти же сроки проверяли состояние свертывающей системы крови по активированному тромбопластиновому времени (в секундах) и тромбопластиновому времени (в виде международного нормализованного отношения – INR). В ходе каждого медицинского осмотра определяли уровень АД, частоту сердечных сокращений (в положении сидя/стоя) и массу тела.
Методы статистики
Переменные вычисляли как разницу между исходными и конечными значениями. Множественное сравнение каждой переменной между группами лечения осуществляли путем анализа ковариации (ANCOVA). Исходные показатели и центральная разность были включены в модель ANCOVA в качестве ковариации. Изменение численности пула поверхностных клеток (по результатам цитологии эпителия влагалища) оценивали с помощью обобщенного рангового критерия Вилкоксона. Статистически значимой считалась величина коэффициента р, меньше или равная 0,05. Статистическую обработку результатов выполняли в программе SAS (версия 8.2).
Результаты
Пациенты
Рандомизации подверглись 97 пациенток. Анализ в этой группе проводили в соответствии с принципом назначенного лечения (ITT). Двое испытуемых были преждевременно исключены из исследования вследствие отказа подписывать на исходном этапе бланк добровольного информированного согласия, их дальнейшая судьба не прослеживалась. Всего в результате нарушений протокола исследования из анализа по ITT выбыло 33 женщины: у 5 эпизоды приливов возникали в процессе подготовительного периода реже, чем 3 раза в сутки; в 16 случаях отсутствовали явные проявления постменопаузы (продолжение овуляторных или ановуляторных циклов на протяжении подготовительного периода, признаком которых являлись влагалищные кровотечения, уровень Е2>40 пг/мл и/или ФСГ30 кг/м2). В протокольный анализ включили 62 пациентки (экстракт цимицифуги BNO 1055, n=20; конъюгированные эстрогены, n=22; плацебо, n=20). Исходные характеристики эти испытуемых – возраст, рост, вес, концентрации гормонов, содержание маркеров остеогенеза и резорбции костной ткани – оказались сопоставимы во всех трех группах (табл. 3). Подсчет использованных капсул показал, что степень комплаентности больных (compliance) была высока во всех трех группах.
Таблица 3. Демографические характеристики
| Экстракт цимицифуги BNO 1055 | Конъюгированные эстрогены | Плацебо | ||||
| Возраст, лет | ||||||
| Среднее ± СО | 52,25 | ±3,19 | 52,32 | ±3,03 | 54,05 | ±4,36 |
| Медиана (n) | 52,50 | 20 | 52,00 | 22 | 54,00 | 20 |
| Масса, кг | ||||||
| Среднее ± СО | 67,00 | ±8,05 | 67,86 | ±9,3 | 65,15 | ±7,72 |
| Медиана (n) | 67,50 | 69,00 | 65,00 | |||
| Рост, см | ||||||
| Среднее ± СО | 164,20 | ±6,57 | 167,00 | ±5,27 | 164,05 | ±5,6 |
| Медиана (n) | 165,50 | 167,00 | 164,00 | |||
| Е2, пг/мл | ||||||
| Среднее ± СО | 19,45 | ±10,05 | 17,04 | ±9,23 | 14,57 | ±9,52 |
| Медиана (n) | 20,00 | 19,07 | 12,81 | |||
| ФСГ, мМЕ/мл | ||||||
| Среднее ± СО | 83,92 | ±33,47 | 80,97 | ±25,64 | 30,45 | ±19,6 |
| Медиана (n) | 79,90 | 82,79 | 69,92 | |||
| ЩФКТ, Ед/л | ||||||
| Среднее ± СО | 54,8 | ±14,34 | 52,85 | ±21,48 | 56,06 | ±23,31 |
| Медиана (n) | 56,00 | 20 | 54,50 | 20 | 55,00 | 18 |
| CrossLaps, нг/мл | ||||||
| Среднее ± СО | 0,25 | ±0,20 | 0,24 | ±0,12 | 0,25 | ±1,6 |
| Медиана (n) | 0,22 | 17 | 0,24 | 19 | 0,23 | 17 |
| ЩФ – щелочная фосфатаза |
Гормоны и ГСПГ
В группе получавших конъюгированные эстрогены содержание иммунореактивного Е2 через 4, 8 и 12 не дель заметно превышает аналогичные показатели по сравнению с группой плацебо. В отношении экстракта цимицифуги BNO 1055 такой эффект отсутствовал (рис. 1). Разница в содержании иммунореактивного Е2 между группой плацебо и группой экстракта цимицифуги BNO 1055 была статистически незначимой. Влияние проводимого лечения на концентрацию ФСГ в крови проиллюстрировано на рисунке 2. Во все три момента времени конъюгированные эстрогены ощутимо снижали уровень ФСГ, но не ЛГ (данные не представлены). Экстракт цимицифуги не оказывал заметного воздействия на титры обоих гормонов. Из–за небольшого количества предоставленной сыворотки измерить содержание ГСПГ удалось только у 16 женщин I группы, 20 женщин II группы и 15 женщин III группы, получавших в конце основного периода лечение экстрактом цимицифуги BNO 1055, конъюгированными эстрогенами и плацебо, соответственно. На фоне терапии экстрактом цимицифуги BNO 1055 и плацебо наблюдалось уменьшение этого показателя, в то время как конъюгированные эстрогены значительно повышали концентрацию ГСПГ (рис. 3).
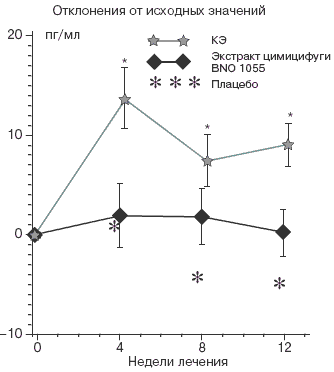
Рис. 1. Анализ гормонального профиля: эстрадиол
*p
На фоне лечения конъюгированными эстрогенами в трех моментах времени наблюдается повышение титров Е2 по сравнению с плацебо и экстракт цимицифуги BNO 1055. Представлены средние значения величин с поправкой на исходные, центральная разность и стандартные ошибки среднего
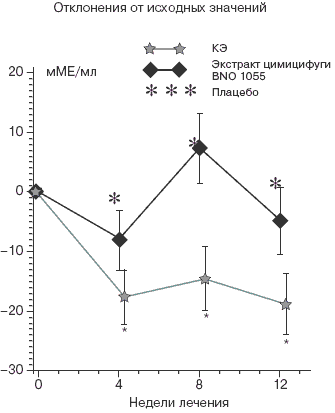
Рис. 2. Анализ гормонального профиля: ФСГ
*p
На фоне лечения конъюгированными эстрогенами в трех моментах времени наблюдается снижение сывороточных титров ФСГ по сравнению с плацебо и экстракт цимицифуги BNO 1055. Представлены средние значения величин с поправкой на исходные, центральная разность и стандартные ошибки среднего
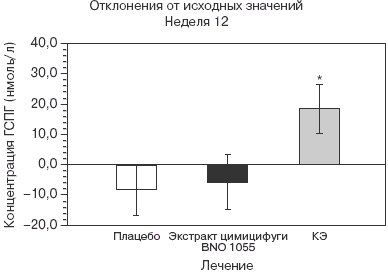
Рис. 3. Анализ содержания глобулина, связывающего половые гормоны (ГСПГ)
*p
По сравнению с плацебо и экстракт цимицифуги BNO 1055 сывороточная концентрация ГСПГ у женщин, получавших конъюгированные эстрогены, достоверно выше. Представлены средние значения величин с поправкой на исходные, центральная разность и стандартные ошибки среднего
Маркеры метаболизма костной ткани
Анализ сывороточных маркеров метаболизма костной ткани у женщин в постменопаузе выявил терапевтическую выгоду экстракта цимицифуги BNO 1055 и конъюгирован-ных эстрогенов. В случае плацебо уровень достоверного маркера резорбции костной ткани – продукта С–концевой деградации коллагена–1α1 костной ткани (т.е. CrossLaps) – нарастает незначительно, но статистически недостоверно. На фоне лечения экстрактом цимицифуги BNO 1055 содержание CrossLaps остается стабильным, а применение конъюгированных эстрогенов приводит к резкому снижению его концентрации через 4 и 12 недель (рис. 4).
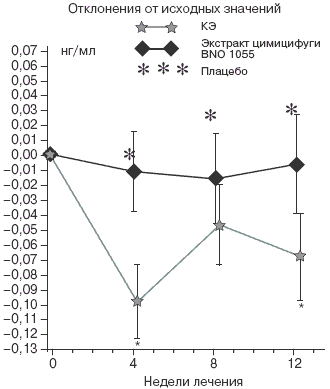
Рис. 4. Метаболизм костной ткани: CrossLaps
*p
На фоне лечения конъюгированными эстрогенами наблюдается достоверное снижение сывороточных титров CrossLaps. Представлены средние значения величин с поправкой на исходные, центральная разность и стандартные ошибки среднего
Через 4 недели титр ЩФКТ, представляющей собой метаболический маркер остеогенеза, заметно увеличивается в группе получавших конъюгированные эстрогены по сравнению с плацебо, но через 8 и 12 недель этот эффект исчезает. Терапия экстрактом цимицифуги BNO 1055 обусловливает достоверный рост уровня ЩФКТ через 12 недель относительно плацебо (рис. 5).
Рис. 5. Метаболизм костной ткани: щелочная фосфатаза костной ткани
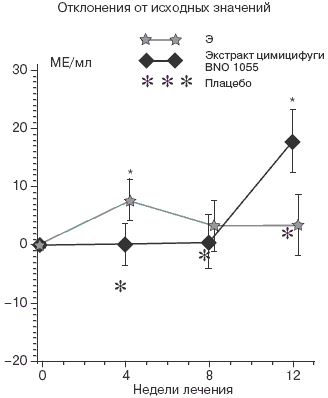
*p
На фоне приема плацебо сывороточные титры ЩФКТ остаются стабильными, в то время как лечение экстрактом цимицифуги BNO 1055 обусловливает достоверное повышение значения этого показателя через 12 недель по сравнению с плацебо и конъюгированными эстрогенами. Представлены средние значения величин с поправкой на исходные, центральная разность и стандартные ошибки среднего
Цитология эпителия влагалища
Если на фоне приема конъюгированных эстрогенов численность пула поверхностных клеток значительно увеличивается по сравнению с плацебо (рРис. 6. Цитология эпителия влагалища
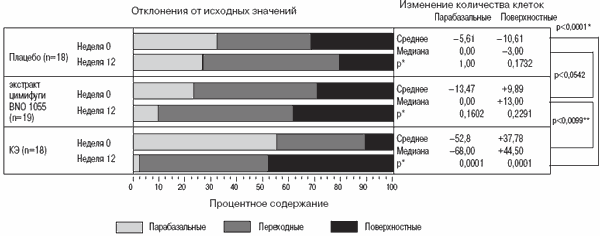
На фоне лечения конъюгированными эстрогенами происходит достоверное увеличение численности пула поверхностных клеток по сравнению с плацебо и экстрактом цимицифуги BNO 1055. Через 12 недель от начала приема экстракта цимицифуги BNO 1055 численность этого пула клеток несколько возрастает до почти достоверной разницы по сравнению с плацебо. В случае плацебо количество поверхностных клеток через 12 недель продолжало сокращаться. Представлены значения Р (обобщенного рангового критерия Вилкоксона) в сравнении с плацебо (*) и экстрактом цимицифуги BNO 1055 (**). КЭ – конъюгированные эстрогены
Метаболизм липидов
Экстракт цимицифуги BNO 1055 и конъюгированные эстрогены не оказывали заметного влияния на концентрацию холестерина в сыворотке крови (общий холестерин, ЛПВП, ЛПНП).
В отличие от плацебо у женщин, получавших конъюгированные эстрогены и экстракт цимицифуги BNO 1055, уровень триглицеридов в сыворотке крови был резко повышен (рис. 7).
Рис. 7. Метаболизм липидов: триглицериды
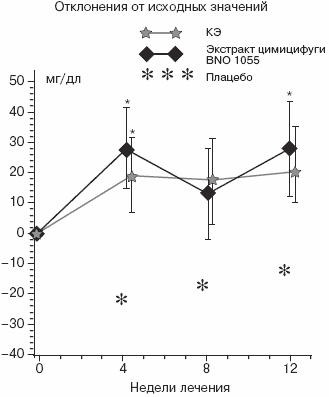
*p
Через 4 недели от начала лечения конъюгированными эстрогенами и экстрактом цимицифуги BNO 1055 наблюдается достоверное повышение сывороточных титров триглицеридов. Представлены средние значения величин с поправкой на исходные, центральная разность и стандартные ошибки среднего
Подробные результаты клинического и биохимического анализов крови приводятся в таблице 4. Согласно полученным данным, проводимое лечение не имело выраженного системного действия. В частности, ни один из трех препаратов не повлиял на состояние свертывающей системы крови (т.е. на значения показателей активированного тромбопластинового времени в секундах и тромбо-пластинового времени в виде INR). Уровень печеночных ферментов (АСТ, АЛТ, γ–ГТ) также оставался стабильным, в случае применения экстракта цимицифуги BNO 1055 имела место тенденция к понижению их концентрации.
Таблица 4. Изменения параметров общего и биохимического анализов крови в ходе исследования (неделя 0 – неделя 12)
| Параметры | Плацебо | Экстракт цимицифуги BNO 1055 | Конъюгированные эстрогены |
| Общий анализ крови | |||
| Тромбоциты, 1010/л | 29,50±118,16 | -3,60±41,32 | 3,27±44,48 |
| Лейкоциты, 1010/л | 0,13±2,10 | 0,16±1,29 | -0,44±1,39 |
| Эритроциты, 107л | -0,11±0,31 | -0,12±0,35 | -0,08±0,31 |
| Гемоглобин, г/л | -5,40±12,21 | -3,92±6,26 | -3,00±6,70 |
| Гематокрит, % | -1,20±3,05 | -1,18±2,71 | -0,85±2,29 |
| Базофилы, % | -0,07±0,37 | 0,04±0,61 | 0,03±0,50 |
| Эозинофилы, % | -0,48±1,84 | -0,36±1,74 | 0,42±1,86 |
| Палочкоядерные нейтрофилы, % | 0,07±0,75 | 0,03±2,04 | -0,58±1,73 |
| Сегментоядерные нейтрофилы, % | 0,47±13,45 | 0,48±10,69 | 3,00±6,54 |
| Лимфоциты, % | 1,27±12,07 | 0,14±11,08 | -1,84±8,37 |
| Моноциты, % | -0,11±3,38 | 0,00±2,28 | -0,21±2,53 |
| Биохимический анализ крови | |||
| Глюкоза, моль/л | 0,32±1,21 | 0,15±0,94 | 0,07±0,70 |
| Мочевина, ммоль/л | -0,14±1,12 | -0,19±1,43 | 0,12±1,07 |
| Креатинин, мкмоль/л | 1,46±11,23 | 0,89±11,88 | 0,88±10,59 |
| Мочевая кислота, мкмоль/л | -41,71±63,94 | 4,00±38,12 | 9,32±67,98 |
| Общий билирубин, мкмоль/дл | -0,11±0,5 | 0,10±0,36 | -0,15±0,39 |
| Общий белок, г/л | 0,71±4,71 | -2,38±4,38 | -0,15±3,88 |
| Железо, мкмоль/л | 0,34±5,75 | 0,37±6,05 | -4,37±9,66 |
| АСТ, nkat/л | -52,00±131,29 | 135,00±259,73 | 0,91±115,118 |
| АЛТ, nkat/л | -83,00±174,06 | -165,50±240,67 | -23,18±301,05 |
| у–ГТ, nkat/л | -58,42±309,47 | -65,50±170,52 | 34,29±290,44 |
| ЩФ, nkat/л | 53,16±444,12 | 19,50±225,12 | 30,00±188,30 |
| Натрий, ммоль/л | 1,34±4,39 | 1,64±3,46 | 0,16±3,17 |
| Калий, моль/л | -0,03±0,33 | 0,25±0,50 | -0,05±0,44 |
| Кальций, нмоль/л | -0,01±0,17 | 0,02±0,17 | -0,03±0,18 |
| Тромбопластиновое время, сек | -0,29±3,24 | -0,58±5,25 | -1,53±7,61 |
| Тромбопластиновое время, INR | -0,01±0,15 | -0,02±0,08 | -0,4±0,20 |
| Данные представлены как среднее ± стандартное отклонение |
Артериальное давление и частота сердечных сокращений
Клинически значимых эффектов проводимой терапии в отношении артериального давления и частоты сердечных сокращений в положении сидя и стоя выявлено не было. В группе плацебо у 1 пациентки возникло головокружение. Головокружение, головные боли и гипертензия, появившиеся у одной из испытуемых группы принимавших экстракт цимицифуги BNO 1055, были отнесены за счет побочного действия лекарственного препарата. И в том, и в другом случае артериальное давление и частота сердечных сокращений оставались постоянными.
По прошествии 12 недель лечения средняя масса тела достоверно не изменялась.
Обсуждение
В ходе проведения этого исследования, дизайн которого был разработан с целью изучить терапевтическую эффективность препарата экстракта цимицифуги BNO 1055 в отношении проявлений климакса, оценивали вторичные параметры. Благоприятные исходы по первичному параметру оказались сопоставимы с эффектами конъюгированных эстрогенов и лучше результатов в группе плацебо [18]. Тем более удивительным стал факт явной эффективности лечения несмотря на то, что проводимое исследование было небольшим и достаточно краткосрочным. По результатам более ранних экспериментов по использованию другого экстракта цимицифуги [30] и опытов на животных с применением препарата экстракта цимицифуги BNO 1055 [22] выявлено статистически достоверное снижение концентрации ЛГ на фоне проводимой терапии. Следовательно, регрессия симптоматики климактерического синдрома может быть опосредована на уровне гипоталамуса, в частности, серотонинергическим действием вытяжек экстракта цимицифуги [23]. В ходе настоящего исследования не удалось пронаблюдать супрессивный эффект экстракта цимицифуги BNO 1055 в отношении ЛГ, однако и конъюгированные эстрогены были лишены способности тормозить высвобождение ЛГ из гипофиза в течение всего периода проведения испытаний. У женщин в постменопаузе эстрогены уменьшают сывороточную концентрацию ФСГ во все три момента времени, а для экстракта цимицифуги BNO 1055 этот эффект не характерен. Известно, что пульсирующий выброс гонадотропин–рилизинг–гормона – один из факторов патогенеза приливов [31], причем активность этого гормона селективно модулируют гипофизарные ЛГ или ФСГ [32]. Не исключено, что именно это лежит в основе механизма, благодаря которому эстрогены способствуют снижению частоты приливов, а серотонинергические [23] и допаминергические [21] эффекты цимицифуги могут опосредовать другие, еще не описанные механизмы.
Повышение титров иммунореактивного Е2 на фоне приема конъюгированных эстрогенов в процессе их метаболизма вполне прогнозируемо, поскольку антисыворотка, используемая для определения Е2, дает перекрестные реакции с эквин–конъюгированными эстрогенами или их метаболитами. В случае экстракта цимицифуги BNO 1055 уровень иммунореактивного Е2 остается постоянным, свидетельствуя тем самым о том, что этот растительный препарат не содержит эстрогеноподобных соединений с иммуносупрессивными свойствами. В опытах in vitro продемонстрировано, что компоненты этой вытяжки цимицифуги не взаимодействуют с рекомбинантными человеческими белками рецепторов эстрогенов α и β [21]. Однако умеренное снижение концентрации ФСГ, зарегистрированное на начальном этапе лечения и сходное с эффектом конъюгированных эстрогенов, позволяет предположить, что экстракт цимицифуги BNO 1055 может действовать аналогично эстрогенам, но через Е2-связывающие белки (а не ЭРа и ЭР(5), обнаруживаемые в эндометрии свиней и человека [21].
Как и ожидалось, содержание ГСПГ значительно повышается на фоне лечения конъюгированными эстрогенами по сравнению с плацебо, а у женщин, принимавших экстракт цимицифуги BNO 1055, этот эффект отсутствует. Кроме того, в группе получавших растительный препарат прослеживается отчетливая тенденция к уменьшению сывороточного уровня печеночных ферментов (АСТ, АЛТ, у–ГТ), а лечение конъюгированными эстрогенами не вызывает таких последствий. В совокупности эти данные указывают на то, что в процессе лечения экстрактом цимицифуги BNO 1055 функции печени и, в частности, обменные процессы, имеющие место в ее паренхиме, не страдают.
Влияние экстракта цимицифуги BNO 1055 в отношении маркеров метаболизма костной ткани характеризуется анаболическим действием. Остеобласты и остеокласты, отвечающие за образование и резорбцию костной ткани, чувствительны к эстрогенам [33-35]. У женщин, находящихся в ре про дуктивной фазе цикла или получающих заместительную гормональную терапию эстрогенами, активность клеток обоих типов сбалансирована: остеокласты разрушают костную ткань, а остеобласты способствуют остеогенезу Механизмы, лежащие в основе метаболизма костной ткани и развития остеопороза из-за недостатка эстрогенов, изучались весьма активно, причем установлено, что у животных после овариэктомии и женщин в постменопаузе активность как остеобластов, так и остеокластов возрастает, однако превалируют функции резорбтивных остеокластов, а это влечет за собой снижение минеральной плотности костей и остеопороз [36]. Таким образом, содержание маркеров активности остеобластов и остеокластов у женщин в постменопаузе и у крыс после удаления яичников увеличивается. Эстрогены способны компенсировать этот дефект и уменьшить тем самым значения суррогатных показателей. Ранее доказана терапевтическая выгода применения экстрактов цимицифуги в отношении маркеров костной ткани в крови и моче, а также минеральной плотности костей у крыс после овариэктомии [19,25], а результаты настоящего исследования подтверждают наличие аналогичного эффекта у женщин в постменопаузе. Препарат цимицифуги BNO 1055 оказывает явное положительное влияние на суррогатные показатели метаболизма костной ткани. Так, критерием остеогенеза (т.е. активности остеобластов) служит ЩФКТ. По сравнению с плацебо и конъюгирован-ными эстрогенами экстракта цимицифуги BNO 1055 резко повышает концентрацию ЩФКТ, отражая тем самым усиление активности остеобластов, которое происходит в первые 4 недели от начала терапии и становится статистически значимым к 12–й неделе. Насколько нам известно, это первое свидетельство в пользу существования у растительных препаратов способности индуцировать остеогенез. Степень резорбции костной ткани, опосредованной остеокластами, оценивают по сывороточной концентрации С–концевых продуктов метаболизма коллагена 1 α 1, специфичного для костной ткани (т.н. CrossLaps). В группе плацебо содержание CrossLaps незначительно нарастает, в то время как прием конъюгированных эстрогенов ассоциируется с заметным уменьшением содержания CrossLaps по сравнению с плацебо, иллюстрируя тем самым хорошо известное антирезорбтивное действие эстрогенов в отношении костной ткани. В группе получавших экстракт цимицифуги BNO 1055 уровень CrossLaps оказался промежуточным (т.е. между значениями показателя в группе плацебо и в группе принимавших эстрогены), что также может указывать на незначительное снижение активности остеокластов с возможным положительным влиянием на минеральную плотность костей. Непродолжительный период лечения (12 недель) недостаточен для того, чтобы анализировать минеральную плотность костей, но из опытов на крысах известно, что эффекты в отношении суррогатных показателей метаболизма костной ткани отражают и состояние минеральной плотности костей [19,25]. Чтобы окончательно подтвердить эти предположения, необходимо провести более длительные исследования в объемной выборке больных с вычислением минеральной плотности костей.
У женщин в постменопаузе, которые не принимают конъюгированных эстрогенов, в эпителии влагалища преобладают парабазальные клетки, а у пациенток, получающих эстрогены – поверхностные клетки [29]. Поскольку в процессе настоящего исследования не были использованы никакие другие эстрогены, скорее всего, сдвиг «индекса зрелости» в пользу промежуточных и поверхностных клеток обусловливает именно изучаемый препарат. Активируя слизистую оболочку влагалища, эстрогены вызывают увеличение численности пула поверхностных клеток. Этот эффект эстрогенов хорошо известен, благодаря ему происходит снижение pH, что препятствует восходящему бактериальному инфицированию. При половом возбуждении эстрогены улучшают смазку. Влияние экстракта цимицифуги BNO 1055 выражено в меньшей степени относительно конъюгированных эстрогенов, тем не менее на фоне его применения численность пула поверхностных клеток также нарастала в масштабах, близких к статистически достоверным по сравнению с плацебо. Описанный эффект ассоциирован с явным уменьшением ощущения сухости во влагалище и сообщался ранее [18]. Аналогичные результаты были получены и в ходе некоторых (но не во всех) более ранних клинических исследованиях других препаратов цимицифуги [14,17]. Их можно наблюдать только у женщин в постменопаузе длительностью, по меньшей мере, 6 месяцев, не принимавших ранее никаких эстрогенов. Это может объяснить, почему в процессе некоторых клинических испытаний экстрактов цимицифуги с привлечением женщин в перименопаузальном периоде (когда уровень эндогенного эстрадиола еще продолжает колебаться) такое благоприятное влияние на цитологию эпителия влагалища отмечено не было [16].
У крыс с удаленными яичниками эстрогены резко снижают титры холестерина, ЛПВП и ЛПНП [37]. То же са мое происходит у женщин, находящихся на гормональной терапии [38]. Однако по результатам настоящего исследования такой эффект не выявлен. Ни конъюгированные эстрогены, ни экстракт цимицифуги BNO 1055 не затрагивали концентрацию холестерина, ЛПВП или ЛПНП. На фоне приема конъюгированных эстрогенов в некоторых случаях повышается содержание триглицеридов, что также было продемонстрировано в настоящем исследовании. Это не было связано, например, с поступлением триглицеридов с пищей, поскольку все анализы крови брались натощак. Нарастание уровня триглицеридов, по всей вероятности, отражает подъем титров липопротеинов очень низкой плотности, ассоциированных с риском атеросклероза. Но эстрогены обладают липолитическим и антилипотропным действием [39], и то же самое может быть справедливо в отношении экстрактов цимицифуги [19].
Терапия конъюгированными эстрогенами и экстрактом цимицифуги BNO 1055 не имела системного эффекта, что проявлялось в стабильном уровне показателей гемограммы, клинического и биохимического анализов крови, факторов свертывающей системы, а также постоянной величиной артериального давления и частоты сердечных сокращений, массой тела. Следует подчеркнуть, что оба вида лечения никак не повлияли на гемостаз. Ранее сообщалось о случае возникновения острой печеночной недостаточности на фоне применения цимицифуги, поэтому при проведении настоящего исследования отдельное внимание уделялось определению концентрации печеночных ферментов. Заре гистрировано незначительное снижение титров АСТ, АЛТ и γ–ГТ, что не доказывает наличия у экстракта цимицифуги BNO 1055 гепатотоксических свойств. Препарат хорошо переносился и не вызывал значимых (по сравнению с плацебо) побочных эффектов.
Некоторые аспекты клинического действия экстракта цимицифуги BNO 1055 аналогичны таковым конъюгированных эстрогенов, в то время как другие отличаются качественно и/или количественно. Ранее было показано, что проводимое лечение купирует многие проявления климакса [18], а по своей эффективности оно сопоставимо с приемом конъюгированных эстрогенов. Оба препарата имели преимущества перед плацебо [18]. Данные, полученные нами в опытах in vitro, свидетельствуют о том, что экстракт цимицифуги BNO 1055 способен взаимодействовать с цитозольными местами (сайтами) связывания эстрогенов человека, крыс и свиней, но не с рекомбинантными белками α– и β–рецепторов эстрогенов (ЭРα и ЭРβ) человека [21]. Механизмы действия препаратов экстракта цимицифуги пока остаются неразгаданными, но, возможно, они опосредованы органоспецифическими эстроген-рецепторными стимулирующими или подавляющими генами. Это может открыть принципиально иные возможности в создании лекарственных препаратов, обладающих органоспецифическим эстрогеноподобным (а следовательно – благоприятным) селективным модулирующим влиянием на Э Р.
Непонятно, одинаковые ли свойства имеют препараты цимицифуги, предлагаемые разными производителями. Есть данные, что водно–спиртовой экстракт отличается от изопропанолового (при тонкослойной хроматографии этих экстрактов получается разное количество полос) [40]. Из–за того, что активные действующие компоненты цимицифуги не определены, остается неизвестным, различаются ли свойства у разных препаратов. В любом случае, назначать следует лишь тот конкретный препарат, эффективность которого доказана клиническими испытаниями.
Заключение
Таким образом, ранее уже сообщалось о благоприятном воздействии экстракта цимицифуги BNO 1055 и конъюгированных эстрогенов на симптоматику климактерического синдрома [18]. Нами же было впервые продемонстрировано, что экстракт цимицифуги BNO 1055 может препятствовать развитию остеопороза, о чем свидетельствуют значения суррогатных сывороточных маркеров метаболизма костной ткани. Кроме того, для этого растительного препарата характерно эстрогеноподобное влияние на слизистую оболочку влагалища. Стабильная концентрация печеночных ферментов и содержание факторов свертывающей системы крови указывают на отсутствие у экстракта цимицифуги BNO 1055 гепатотоксического действия.
Реферат подготовлен Е.Б. Третьяк по материалам статьи W. Wuttke, C. Gorkow, D. Seidlova–Wuttke «Effects of black cohosh (Cimicifuga racemosa) on bone turnover, vaginal mucosa, and various blood parameters in postmenopausal women: a double–blind, placebo–controlled, and conjugated estrogens–controlled study» Menopause: The Journal of The North American Menopause Society 2006, Vol. 13, No 2: 185–196
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Научный центр акушерства, гинекологии и перинатологии им. акад. В.И. Кулакова
Балан В.Е.
Московский областной НИИ акушерства и гинекологии
Юсупова И.У.
Государственный научный центр социальной и судебной психиатрии им. В.П. Сербского, Москва
Филатова Т.С.
Государственный научный центр социальной и судебной психиатрии им. В.П. Сербского, Москва
Ковалева И.А.
Государственный научный центр социальной и судебной психиатрии им. В.П. Сербского, Москва
Агаларзаде Г.Б.
Государственный научный центр социальной и судебной психиатрии им. В.П. Сербского, Москва

Оценка эффективности и безопасности длительного применения экстракта Cimicifuga racemosa в терапии больных с климактерическим синдромом
Авторы:
Рафаэлян И.В., Балан В.Е., Юсупова И.У., Филатова Т.С., Ковалева И.А., Агаларзаде Г.Б.
Как цитировать:
Рафаэлян И.В., Балан В.Е., Юсупова И.У., Филатова Т.С., Ковалева И.А., Агаларзаде Г.Б. Оценка эффективности и безопасности длительного применения экстракта Cimicifuga racemosa в терапии больных с климактерическим синдромом. Российский вестник акушера-гинеколога.
2013;13(6):86‑90.
Rafalian IV, Balan VE, Iusupova IU, Filatova TS, Kovaleva IA, Agalarzade GB. Evaluation of the efficiency and safety of long-term Cimicifuga racemosa extract therapy in patients with climacteric syndrome. Russian Bulletin of Obstetrician-Gynecologist. 2013;13(6):86‑90. (In Russ.)

С увеличением продолжительности жизни особое медико-социальное значение приобретают аспекты, определяющие качество жизни женщин старшей возрастной группы. Менопаузальный возраст, как правило, является возрастом наибольшей социальной активности женщины, накопившей определенный жизненный и творческий опыт, который она с пользой может отдавать обществу. Но именно в этом периоде в женском организме происходят изменения, отрицательно влияющие на качество жизни. Главным фактором является дефицит половых гормонов, что приводит к возникновению различных патологических изменений. Наиболее известным ранним проявлением климактерических расстройств является климактерический синдром — симптомокомплекс, характеризующийся сочетанием нейропсихических, вегетативно-сосудистых, нейроэндокринных нарушений, резко снижающих качество жизни и являющихся предикторами множества более поздних нарушений, в том числе сердечно-сосудистых и обменно-метаболических [1]. Климактерический синдром (КС) наблюдается у 40-80% женщин (E. Velde, van Leu Sden, 1994). Самым частым симптомом КС являются «приливы жара», отмечающиеся, по данным разных авторов, у 50-85% женщин [4, 7, 9] и сохраняющиеся от 3 мес до 15 и более лет.
КС является классическим показанием к проведению традиционной гормональной терапии (ГТ) с использованием натуральных эстрогенов или их аналогов. Однако существуют противопоказания и ограничения к применению ГТ из-за риска развития у части больных патологии эндометрия, молочных желез, неблагоприятного влияния на тромбогенный потенциал крови. Большое значение в этих случаях приобретают альтернативные методы коррекции КС, к которым относят применение фитогормонов (рапонтицин, мальброзия) и Сimicifuga racemosa (CR), обладающей эстрогенноподобными эффектами.
Наиболее изученной и получившей широкую известность при лечении климактерических расстройств в качестве альтернативы заместительной гормональной терапии (ЗГТ). CR занимает 8-е место в Европе среди экстрактов лекарственных растений, назначаемых для лечения климактерического синдрома. Химическими компонентами корней и корневищ CR являются ряд трипертеноидов, производных коричной (циннамовой) кислоты, и эфиры инозидиновой и фукниновой кислот [10]. Механизм действия CR до настоящего времени до конца не изучен. Некоторые исследователи [11] полагают, что наиболее вероятным механизмом действия цимицифуги на ЦНС и симптомы КС является влияние на синтез гонадотропин-рилизинг-гормона, синтез и обмен основных нейротрансмиттеров мозга (допамина, серотонина, адреналина, эндорфинов), снижение выброса ТТГ и ЛГ, являющихся установленными триггерными механизмами возникновения приливов (В.Е. Балан, 1985).
Имеются данные, что механизм действия CR осуществляется через допаминовые (D2) и серотониновые рецепторы в ЦНС, что может способствовать снижению частоты и интенсивности приливов, оказывать антидепрессивное действие и выраженное положительное влияние на сон [6, 8].
Цель исследования — оценка эффективности и безопасности приема климадинона, созданного на основе экстракта цимицифуги рацемозы, в течение 12 мес для лечения климактерического синдрома в сравнении с применением плацебо.
Материал и методы
В исследование включены 70 пациенток, страдавших симптомами КС средней степени тяжести, возраст которых составил 52,0±5,8 года, длительность постменопаузы — 3,0±1,3 года.
Все пациентки методом случайной выборки были разделены на две группы.
1-ю группу составили 35 женщин с КС средней степени тяжести, получавших экстракт СR сухой в дозе 20 мг 2 раза в сутки (климадинон, таблетки, 20 мг) в течение 12 мес.
Во 2-ю группу вошли 35 пациенток с КС средней степени тяжести, получавших плацебо.
Критерии включения в исследование:
— возраст пациенток от 45 до 60 лет в периоде пери- и ранней постменопаузы;
— наличие симптомов климактерического синдрома средней степени тяжести;
— информированное письменное согласие пациенток;
— отсутствие самостоятельной менструации не менее одного года;
— наличие противопоказаний к классической ГТ либо при отказе женщины от приема ГТ.
Критерии исключения из исследования:
— наличие эстрогензависимых опухолей на момент включения в исследование;
— прием препаратов заместительной гормональной терапии в течение менее 3 мес до включения в исследование;
— наличие заболеваний желудочно-кишечного тракта и гепатобилиарного комплекса тяжелой степени;
— наличие заболеваний центральной нервной системы, психических заболеваний, ограничивающих комплаентность приема препаратов;
— непереносимость препарата;
— патология щитовидной железы.
Методы оценки эффективности и безопасности. Оценка степени тяжести симптомов КС производилась с помощью модифицированного менопаузального индекса (ММИ), рассчитанного на основе балльной оценки симптомов КС. При 1-м, 2-м, 4-м визитах проводили забор крови для исследования уровней эстрадиола (Е2), лютеинизирующего гормона (ЛГ), фолликулостимулирующего гормона (ФСГ), пролактина (Prl) хемилюминесцентным методом. Уровни общего холестерина, липопротеидов высокой плотности (ЛПВП), липопротеидов низкой плотности (ЛПНП), триглицеридов, коэффициента атерогенности (КА) оценивали при 1-м и 4-м визитах с помощью спектрофотометрического метода. Исследование уровней креатинина, общего белка, глюкозы, общего билирубина, прямого билирубина, мочевины, щелочной фосфатазы, аспартатаминотрансферазы (АСТ), аланинаминотрансферазы (АЛТ), γ-глутамилтранспептидазы (GGT) проводили при 1-м и 4-м визитах с помощью спектрофотометрического метода. Уровни основных нейротрансмиттеров в плазме и моче (серотонина, норадреналина, дофамина) оценивали с помощью метода высокоэффективной жидкостной хроматографии при 1-м, 2-м и 4-м визитах на базе лаборатории Государственного научного центра социальной и судебной психиатрии им. В.П. Сербского. Биопсию эндометрия выполняли по стандартной методике с применением вакуумного забора (аспирационная биопсия эндометрия с помощью кюретки Pipelle) при первом визите и в конце исследования (4-й визит). Толщину эндометрия оценивали с применением УЗИ во время 1-го, 2-го, 4-го визитов. Толщина эндометрия более 5 мм на фоне лечения рассматривалась как неблагоприятный эффект препарата. Измерение роста, массы тела проводили при 1-м, 2-м, 3-м, 4-м визитах. Всех пациенток обследовали методом маммографии с изучением плотности молочной железы до включения в наблюдение (если подобное исследование проводили в течение 12 мес до момента включения в работу, его не повторяли) и через 12 мес после терапии исследуемым препаратом. Все маммограммы были оценены в соответствии с классификацией J. Wolfe (1976).
Результаты
Установлено достоверное уменьшение частоты и выраженности симптомов КС у пациенток, принимавших экстракт СR (климадинон) в дозе 40 мг в сутки, по сравнению с клиническими проявлениями КС у больных 2-й группы. О положительной динамике симптомов при приеме активного препарата свидетельствовало достоверное снижение значений ММИ через 3 и 6 мес приема экстракта СR (p<0,05). Во 2-й группе женщин, принимавших плацебо, через 3 мес терапии наблюдалось повышение значений ММИ (p>0,05), что нами расценено как отрицательная динамика симптомов КС. Этим пациенткам в последующем назначался активный препарат.
К 12-му месяцу лечения климадиноном значения ММИ возвращались к исходному уровню у 74% (n=21) пациенток, только у 26% (n=8) пациенток эффективность терапии сохранялась в течение 12 мес.
Статистически достоверные различия значений ММИ в 1-й и 2-й группах пациенток установлены через 3 мес терапии (табл. 1).

При построении таблиц сопряженности установлено, что наибольшее положительное влияние прием экстракта CR оказывал на проявления нейровегетативных симптомов, которые в процессе 3-месячной терапии достоверно уменьшались по сравнению с таковыми у женщин 2-й группы. Наибольший эффект был достигнут в отношении «классических» эстрогендефицитных проявлений: «приливов» — у 59% пациенток 1-й группы (у 42,9% больных, принимавших плацебо) и потливости — у 54% пациенток 1-й группы (у 3,6% — 2-й группы).
Дополнительно эффективность экстракта CR проявилась в купировании головной боли — у 51,4% пациенток 1-й группы (у 10,7% — 2-й группы), сердцебиений — у 60% пациенток 1-й группы и у 21,4% пациенток, принимавших плацебо, сонливости — у 83 и 14,3%, сухости кожи — у 94 и 10,7%, нарушения сна — у 68 и 7,1%, отечности — у 40 и 3,6%, снижении АД — у 28,5 и 7,1% больных 1-й и 2-й групп соответственно. В меньшей степени прием препарата оказывал влияние на повышенную утомляемость, снижение памяти и либидо, которые традиционно относят к андрогензависимым расстройствам. Практически не менялась степень выраженности метаболических симптомов.
При анализе полученных результатов гормонального исследования крови достоверных различий уровней основных гонадотропинов на фоне приема климадинона в сравнении с приемом плацебо не выявлено. Через 3 мес терапии уровень пролактина достоверно снизился (p<0,001) в 1-й группе (группа приема экстракта CR), что соответствовало возрастной норме.
В 1-й группе пациенток уровень эстрадиола через 3-12 мес терапии не изменился, однако при его сравнении с таковым во 2-й группе (прием плацебо) выявлены достоверные различия (р=0,01). Возможно, данные результаты свидетельствуют о прогрессировании возрастных изменений во 2-й группе пациенток.
Учитывая отсутствие влияния приема климадинона на уровни половых и гонадотропных гормонов, особый интерес представило изучение изменения уровней основных моноаминов.
Нами установлено достоверное повышение уровня серотонина в плазме крови в первые 3 мес приема экстракта CR (р=0,01). Однако к 12-му месяцу терапии уровень серотонина снизился, что совпало со снижением эффективности лечения. Возможно, именно увеличение уровня серотонина при приеме экстракта цимицифуги рацимозы лежит в основе его эффективности при лечении КС (табл. 2).

Аналогичным образом менялись показатели серотонина в моче.
При сравнении динамики уровня серотонина в плазме крови у пациенток обеих групп выявлена достоверная разница через 3 мес терапии (табл. 3).

Достоверных изменений уровней серотонина в крови и моче на фоне приема плацебо не было выявлено (p>0,05).
В 1-й группе пациенток, принимавших экстракт CR, через 3 мес лечения выявлено достоверное снижение уровня дофамина в плазме крови (р=0,0001).
Динамика содержания дофамина в моче в обеих группах достоверно не отличалась.
При сравнении изменений уровней норадреналина в плазме крови и моче в 1-й и 2-й группах через 3 мес терапии мы получили достоверные отличия (табл. 4, 5).


Данные современной литературы о влиянии применения климадинона на соотношение липидов весьма разноречивы. При изучении динамики ЛПВП достоверных изменений не выявлено. Однако на фоне терапии экстрактом СR в течение 12 мес достоверно снизился уровень холестерина (р<0,05), ЛПНП (p<0,05), КА (p<0,05), что было расценено как дополнительный положительный эффект терапии климадиноном у больных с КС.
При анализе колебаний показателей биохимических параметров в крови, уровней триглицеридов, мочевины, креатинина, прямого билирубина, щелочной фосфатазы, γ-глутаминтрансферазы отмечалась тенденция к их увеличению, не превышавшая референсных значений. Содержание общего белка, глюкозы, общего билирубина, АЛТ крови у пациенток, принимавших климадинон, не менялось на протяжении всего времени наблюдения. Полученные данные свидетельствуют о безопасности применения экстракта CR для печеночного метаболизма и отсутствии токсичности препарата при приеме в течение года.
Анализируя данные УЗИ в течение всего года приема экстракта CR, авторы выявили достоверное увеличение толщины эндометрия через 3 мес терапии (р<0,05), однако эти значения не выходили за пределы референсных. К концу 12-го месяца терапии климадиноном толщина эндометрия, по данным УЗИ, возвращалась к первоначальным значениям (р>0,05). При анализе данных УЗИ на фоне приема плацебо значимого изменения толщины эндометрия выявлено не было.
Данные патоморфологического исследования свидетельствовали об отсутствии отрицательного влияния приема экстракта CR на эндометрий.
Всем больным проводилось маммографическое исследование с определением плотности молочной железы по J. Wolfe (1976). В результате одного года наблюдения маммографическая плотность у пациенток 1-й группы в большинстве случаев не изменялась, либо отмечалось ее снижение, что совпадает с данными современной литературы.
Обсуждение
Бесспорным является положительное влияние современной ГТ на различные аспекты климактерических расстройств, в том числе и симптомы КС. Вместе с тем не менее 1/3 женщин имеют противопоказания или ограничения к назначению классической ГТ. В последнее десятилетие широкое распространение, особенно для лечения симптомов КС, получили растительные препараты. Однако между сторонниками ЗГТ и сторонниками альтернативной терапии продолжаются яростные споры. Сторонники ЗГТ явно преуменьшают эффективность растительных препаратов и сравнивают их эффективность с плацебо, а сторонники альтернативной терапии преувеличивают возможные риски ЗГТ, что вносит неразбериху в умы как врачей так и их пациенток. В представленном плацебо-контролируемом исследовании у пациенток с КС средней степени тяжести показано, что эффективность применения экстракта Cimicifuga racemosa достоверно превышает таковую плацебо. При этом уровни эстрадиола и основных гонадотропинов не менялись, а достоверное снижение уровня эстрадиола в группе принимавших плацебо мы можем объяснить возрастными изменениями. По нашему мнению, эффективность терапии климадиноном больных с КС связана, в основном, с достоверным повышением уровней серотонина и снижением содержания норадреналина как в крови, так и в моче. Изменения уровней этих нейротрансмиттеров могут раскрывать патогенетические аспекты проявлений КС. Указанные параметры у пациенток в группе плацебо не менялись.
Существует патогенетическое обоснование возможности влияния уровней нейротрансмиттеров на проявления КС. В настоящее время рассматривают три теории патогенеза возникновения «приливов» при климактерическом синдроме: теория вегетативных нарушений, абстинентная и гормонально-нейротрансмиттерная. Эти подходы отображают многообразие социальных, психологических и эндокринных факторов, вносящих свой вклад в появление «приливов». «Приливы» рассматриваются как проявление своеобразной «абстиненции» эстрогенчувствительных нейрональных систем, находившихся долгое время в условиях высокого содержания половых гормонов, и нарушения их адаптации к новым условиям дефицита эстрогенов. Гипоталамус обеспечивает функционирование сложнейшего взаимодействия между нервной и эндокринной системами. Эта область мозга реагирует на нейрональные сигналы от других систем организма (длительность светового дня, обонятельные рецепторы, стресс, температура), а также на многочисленные гормональные и другие стимулы, переносимые с кровью (стероидные гормоны, кортикостероиды, ангиотензин, инсулин, концентрация глюкозы). В медиальной преоптической области гипоталамуса содержится терморегуляторное ядро, активирующее механизмы поддержания температуры тела в нормальном диапазоне, называемом «терморегуляторной зоной» (R. Casper, S. Gen, 1985). У женщин с «приливами» может иметь место сужение границ терморегуляторной зоны по сравнению с женщинами, не страдающими приливами [5]. Сужение терморегуляторной зоны может быть обусловлено избытком синтеза норадреналина и недостатком серотонина в головном мозге. Норадреналин считается основным нейротрансмиттером, ответственным за сужение терморегуляторной зоны гипоталамуса [2]. Во время «приливов» отмечается корреляция резкого подъема уровней метаболитов норадреналина с повышением температуры тела и теплоотдачи (R. Freedman и соавт., 1995). Полагают, что синтез и секреция норадреналина в терморегуляторном ядре гипоталамуса полностью ингибируются эндорфинами и катехол-эстрогенами (B. Schurz и соавт., 1988). Очевидно, при недостатке последних развивается нарушение терморегуляции. Серотонин — еще один вероятный нейротрансмиттер, участвующий в механизме «приливов». Снижение уровней серотонина происходит параллельно со снижением уровней эстрогенов у женщин в периоде менопаузы, у пациенток с хирургической аменореей и после перенесенной овариэктомии (G. Gonzales, C. Carrillo, 1993). Высказано предположение, что определенные типы рецепторов серотонина имеют отношение к нарушениям терморегуляции при «приливах» [3]. Таким образом, полученные нами данные подтверждают нейротрансмиттерную теорию возникновения «приливов» и, по-видимому, объясняют механизм действия экстракта CR на симптомы КС.
Выводы
1. Установлено достоверное уменьшение частоты и выраженности симптомов климактерического синдрома у пациенток, принимавших экстракт Cimicifuga racemosa (климадинона) в течение 6 мес, к 12-му месяцу лечения значения ММИ возвращались к исходному уровню.
2. На фоне лечения пациенток с климактерическим синдромом климадиноном выявлены дополнительные положительные изменения липидного спектра крови и отсутствие гепатотоксичности препарата.
3. Через 3 мес лечения климадиноном выявлено увеличение уровня серотонина (p<0,05), снижение содержания норадреналина в крови и моче (p<0,05), что может раскрывать патогенетические аспекты проявлений климактерического синдрома.
Мы используем файлы cооkies для улучшения работы сайта. Оставаясь на нашем сайте, вы соглашаетесь с условиями
использования файлов cооkies. Чтобы ознакомиться с нашими Положениями о конфиденциальности и об использовании
файлов cookie, нажмите здесь.

Я.А.Юцковская («Клиника профессора Юцковской». 105118, Россия, Москва, пр-т Буденного, д. 26, корп. 1);
А.С.Суханова (ГБОУ ВПО Российский национальный исследовательский медицинский университет им. Н.И.Пирогова Минздрава России. 117997, Россия, Москва, ул. Островитянова, д. 1)
Представлены результаты изучения эффективности и безопасности совместного применения лекарственного средства Ци-Клим (производитель фармацевтическая компания «Эвалар», Россия) и косметического средства Ци-Клим, содержащих экстракт цимицифуги, с целью коррекции структурно-функциональных изменений кожи у женщин в периоде перименопаузы, менопаузы и постменопаузы.
Материалы и методы. Под наблюдением находились 15 женщин в возрасте от 41 до 56 лет, имевшие какие-либо признаки климактерического синдрома. Проводились исследование морфофункциональных характеристик кожи (в том числе измерение толщины дермы и эпидермиса с помощью ультразвука, характеристика структуры, влажности, эластичности и внешнего вида кожи), а также оценка качества жизни с помощью опросника SF-36. Лекарственное средство Ци-Клим назначалось по 1 таблетке 2 раза в сутки внутрь во время приема пищи в течение 12 мес, крем Ци-Клим рекомендовалось наносить на кожу лица по 1 мл 2 раза в день ежедневно в течение 12 мес. Повторные осмотры проводились ежемесячно, оценка морфофункциональных характеристик кожи – через 6 и 12 мес.
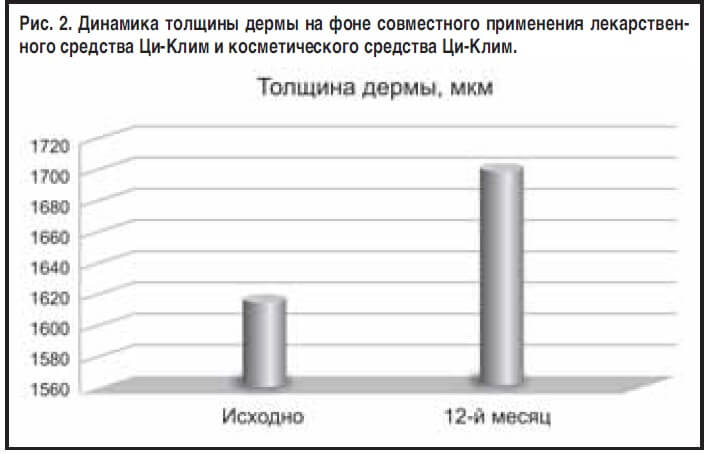
Результаты. Через 6 и 12 мес у пациенток отмечались значимое уменьшение толщины эпидермиса и увеличение толщины дермы, повышение увлажненности и эластичности кожи. Улучшались внешние характеристики кожи и как результат – качество жизни женщин.
Вывод. Совместное применение лекарственного средства Ци-Клим и косметического средства Ци-Клим на основе растительного сырья – высокоэффективно, отличается безопасностью и хорошей переносимостью, позволяет добиться хорошего результата в лечении инволюционных изменений кожи, улучшает психоэмоциональное состояние и качество жизни женщин.
Ключевые слова: климактерический синдром, кожа, цимицифуга, фитоэстрогены, лекарственное средство Ци-Клим.
yutskovskaya@yandex.ru
Опубликовано в издании “Гинекология”. 2015; 17 (6): 4–10.
Ya.A.Yutskovskaya (Clinic professor Yutskovskaya. 105118, Russian Federation, Moscow, pr-t Budennogo, d. 26, korp. 1);
A.S.Sukhanova (N.I.Pirogov Russian National Research Medical University of the Ministry of Health of the Russian Federation. 117997, Russian Federation, Moscow, ul. Ostrovitianova, d. 1)
Results of studying of efficiency and safety of the combination of medicine Ci-Clim and cosmetic product Ci-Clim (JSC EVALAR, Russia), containing extract of cimicifuga racemosa, for the purpose of correction of structural and functional changes of skin of women in the perimenopausal, menopausal and postmenopausal period are presented.
Materials and methods. Under supervision there were 15 women aged from 41 till 56 years, who had any signs of a climacteric syndrome. Research of the morphologic and functional skin characteristics (including measurement of thickness of derma and epidermis by means of ultrasound, the characteristic of structure, humidity, elasticity and visual appearance of skin), and also an assessment of quality of life by means of SF-36 questionnaire was conducted. Patients were treated with combination of medicine Ci-Clim 1 tablet 2 times per day during meal within 12 months, and cosmetic product Ci-Clim on the face (1 ml 2 times a day) daily within 12 months. Repeated visits were performed monthly, an assessment of the morphological and functional properties of the skin were done at 6 and 12 months.
Results. Significant reduction of thickness of epidermis and increase in thickness of derma, and also increase of skin humidity and elasticity were noted at 6 and 12 months. Visual characteristics of skin improved. Quality of life of postmenopausal women improved as well as the skin characteristics.
Conclusion. Application of the combination of medicine Ci-Clim and cosmetic product Ci-Clim, containing herbal extracts is highly effective, safe and well tolerated drug that allows to achieve effect in treatment of involutional changes of skin, improving an emotional state and quality of life of women.
Key words: Ci-Clim, climacteric syndrome, skin, cimicifuga, phytoestrogens.
yutskovskaya@yandex.ru
For citation: Yutskovskaya Ya.A., Sukhanova A.S. The results of the research on cimicifuga extract impact in systematic and local use on structural and functional skin rates in perimenopause, menopause and postmenopause. Gynecology. 2015; 17 (6): 4–10.
Кожа человека обеспечивает защиту от внедрения вирусов и бактерий, физических и химических агрессивных факторов внешней среды, предохраняет от потери влаги и тепла и выполняет ряд других жизненно важных функций. Кожа состоит из трех слоев: эпидермис, дерма и подкожно-жировая клетчатка. Эпидермис – тонкий наружный слой, непосредственно контактирующий с внешней средой. Дерма – основа кожи, содержит кровеносные и лимфатические сосуды, нервы, обеспечивающие кровоснабжение всех слоев кожи. Волокна (коллагеновые, эластиновые) соединительной ткани дермы, составляющие 80% ее сухой массы, обеспечивают, с одной стороны, ее прочность, с другой – упругость и эластичность. Помимо сети коллагеновых и эластиновых волокон дерма содержит клеточные элементы и основное вещество, представленное гликозаминогликанами, в том числе влияющими на степень гидратации кожи [1].
Старение кожи – естественный возрастной процесс. К факторам, ускоряющим дегенеративные процессы в тканях кожи, относятся помимо возраста перенесенные и сопутствующие заболевания, наследственность, воздействие ультрафиолета и инфракрасного излучения, образ жизни (диета, курение, употребление алкоголя, лекарственных препаратов), эндокринные дисфункции (нарушение гормонального фона, в том числе изменение уровня половых гормонов, гормонов щитовидной железы) и даже гравитация [2]. В процессе старения значительно замедляется обновление эпидермиса, уменьшается продукция пота и кожного сала, снижаются иммунная, барьерная и сенсорная функции кожи, ухудшается заживление ран, реактивность сосудов, падает продукция витамина D [3].
Важную роль в прогрессировании морфофункциональных изменений кожи, лежащих в основе ее старения, играет падение продукции эстрогенов у женщин в климактерическом периоде. Следствием этого являются снижение содержания коллагена и воды в коже, секреции кожного сала, эластичности, а также проявления гиперандрогении (в том числе избыточный рост волос на лице) [4]. Известна тесная зависимость между дефицитом эстрогенов и снижением содержания и нарушением структуры коллагена кожи [4–7]. В течение первых 15 лет постменопаузы происходит ежегодное снижение содержания коллагена в коже на 2,5%, этот процесс идет параллельно со снижением минеральной плотности костей [8]. У женщин с ранней менопаузой наблюдаются и дегенеративные изменения эластиновых волокон дермы [9].
Снижение содержания коллагена в коже можно предотвратить назначением эстрогенов [4, 7]. Показано повышение уровня коллагена при лечении топическими эстрогенами, а также после их назначения внутрь и подкожно [10–12]. Эстрогены могут увеличивать количество и толщину эластиновых волокон [13], повышать уровень гиалуроновой кислоты и мукополисахаридов, что приводит к уменьшению сухости кожи и нормализации ее толщины [14], способствовать увеличению слоя липидов на поверхности кожи [15]. За счет указанных механизмов терапия эстрогенами препятствует свойственному для старения истончению кожи [16], развитию морщин [17–19], повышает кровоснабжение кожи [20, 21]. Улучшение внешнего вида и свойств кожи на фоне терапии эстрогенами повышает самооценку и сексуальность женщин [1]. Таким образом, заместительная гормональная терапия (ЗГТ) в перименопаузе – один из наиболее эффективных методов не только профилактики и лечения общих климактерических симптомов, но и улучшения функции кожи и качества жизни женщин [4, 22–24].
Софи Лорен писала: «Зрелость тоже по-своему хороша, но совершенно иначе, чем молодость, и поэтому требует к себе иного подхода. Ей нужны забота и внимание, зато она изысканней, богаче и сложней, нежели нетронутая свежесть юности» [25]. Любая женщина хочет оставаться привлекательной как можно дольше, поэтому неудивительно, что рынок средств против старения кожи растет даже в условиях кризиса. По оценкам экспертов в 2005 г. в США на средства по уходу за кожей с антивозрастным эффектом покупатели потратили 664 млн дол. США, а с 2001 по 2005 г. этот рынок вырос на 33% [1]. По данным маркетингового исследования BBC, в 2018 г. оборот глобального рынка продуктов и услуг против старения составит 345,8 млрд дол. США [26]. Таким образом, существует очевидный спрос на новые лекарственные препараты, замедляющие процессы старения кожи. Альтернативой ЗГТ является применение фитоэстрогенов – препаратов растительного происхождения с эстрогеноподобным действием, но лишенных большого количества побочных эффектов, свойственных эстрогенам. В связи с этим особую актуальность приобретает изучение влияния на психоэмоциональный фон и морфофункциональные показатели кожи препаратов на основе фитоэстрогенов и растительных средств с эстрогеноподобным действием, в частности, на основе экстракта цимицифуги, а также оценка их клинической эффективности.
Цимицифуга – растение родом из Северной Америки, ее корневище традиционно использовалось в качестве лекарственного средства индейскими племенами (пенобскот, виннебаго, дакота) для лечения кашля, простуды, запоров, слабости, патологии суставов, а также усиления лактации. С 1832 г. настойка корневищ цимицифуги стала применяться для лечения дисменореи, а также боли и воспаления, связанных с эндометриозом [27]. Более 100 лет (с 1840 по 1946 г.) жидкий экстракт цимицифуги входил в национальный формуляр США. В настоящее время препараты на основе цимицифуги используются во всем мире для лечения менопаузальных симптомов [28].
Целью исследования явилась оценка влияния совместного применения лекарственного средства Ци-Клим и косметического средства Ци-Клим, содержащих экстракт цимицифуги, на структурно-функциональные показатели кожи женщин в периодах перименопаузы, менопаузы и постменопаузы при системном и местном применении, а также качества жизни до и после лечения и возможного влияния терапии на вазомоторную симптоматику климактерического синдрома.
Задачи: определить качественные и количественные изменения основных параметров кожи на основании изучения показателей рН, увлажненности, эластичности, ультразвукового сканирования и фотодокументирования, а также оценить удобство применения и степень удовлетворенности пациенток результатами терапии.
Материалы и методы
На базе Клиники профессора Юцковской (Москва) в период с января по декабрь 2014 г. (12 мес) под наблюдением находились 15 женщин в возрасте от 41 до 56 лет (средний возраст 47±4,4 года), имеющие те или иные признаки климактерического синдрома. Всем пациенткам назначалось лекарственное средство Ци-Клим по 1 таблетке 2 раза в сутки внутрь во время приема пищи в течение 12 мес, а также косметическое средство Ци-Клим – наружно на область лица по 1 мл 2 раза в день ежедневно в течение 12 мес. В рамках настоящего исследования проводились ежемесячные визиты, предусматривающие следующие процедуры: сбор жалоб и мнения пациентки о динамике климактерических симптомов, оценка общего состояния, осмотр косметологом с визуальной оценкой кожи лица, количественные характеристики кожи (увлажненность, жирность, эластичность, pH, биологический возраст по отношению к возрастному диапазону). На визите включения, визитах через 6 и 12 мес помимо указанных процедур проводились фотодокументирование, ультразвуковое исследование кожи с оценкой количественных параметров (толщина эпидермиса и дермы), а также структуры эпидермиса и дермы (расположение волокон, дифференцировка эпидермиса и дермы, железы, сосуды), осмотр гинекологом с оценкой тяжести течения климактерического синдрома по шкале Купермана. Помимо этого для оценки влияния проводимого лечения на качество жизни пациентки на скрининговом визите, а также через 6 и 12 мес заполняли опросник SF-36. Для оценки качественных и количественных показателей кожи использовались аппарат «Soft Plus Callegari S.P.A.» (Италия), метод ультразвукового дермасканирования с помощью портативного высокочастотного прибора «DUB – Digital Ultraschall Bildsystem-tpm» и «ПО DUB-SkinScanver.3.2» (Германия), а для визуальной оценки состояния кожи применялся метод фотоанализа на аппарате «Reveal Imager» (США).
Статистический анализ проводился с использованием статистической программы Stata 13. Нормальность распределения признаков оценивалась с помощью критерия Шапиро–Уилка. При описании нормально распределенных переменных указывалось среднее и стандартное отклонение (M±s), переменные с отличным от нормального распределением описывались с указанием медианы и интерквартильного размаха [Ме (25%; 75%)]. Сравнение переменных в динамике для нормально распределенных количественных признаков проводилось с использованием t-критерия для зависимых выборок, динамика переменных с распределением, отличным от нормального, оценивалась с помощью критерия Вилкоксона.
Результаты
Все 15 женщин прошли полный курс запланированного приема лекарственного средства Ци-Клим и косметического средства Ци-Клим наружного применения. За время исследования не было зарегистрировано ни одного нежелательного явления, что подтверждает хорошую переносимость совместного применения лекарственного средства Ци-Клим и косметического средства Ци-Клим. При анализе фотографий пациенток до лечения и после 6 и 12 мес во всех случаях отмечались улучшение текстуры кожи, ее цвета, уменьшение видимого шелушения.

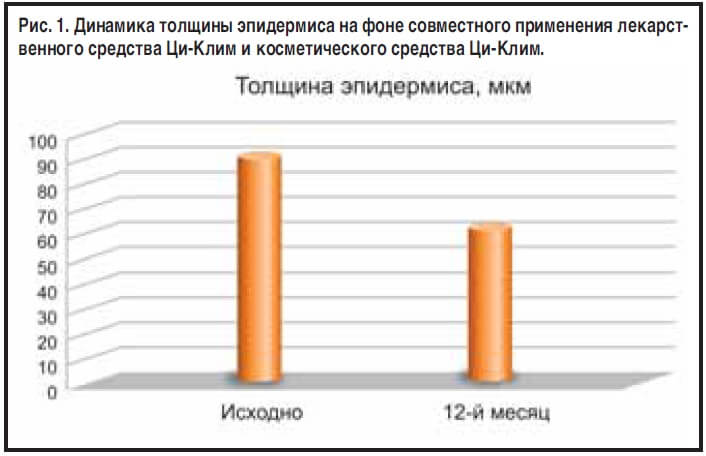
Визуально оцениваемые результаты подтверждаются изменениями объективных параметров, характеризующих состояние кожи. Так, уже к 6-му месяцу достоверно улучшились эластические свойства кожи (от 38±6 у.е. исходно, что является нижней границей нормы этого показателя для данной возрастной группы, до 40,2±4,7 у.е.; p<0,05). Продолжение терапии в течение еще полугода привело к дальнейшему повышению эластичности (41,9±4,7 у.е. к 12-му месяцу; p<0,05). Степень гидратации кожи на фоне совместного применения лекарственного средства Ци-Клим и косметического средства Ци-Клим значимо увеличилась к 6-му месяцу (от 52,3±19,8 до 61,1±16,5 у.е.; p<0,05) и в еще большей степени – к 12-му (64,5±15 у.е., p<0,05); см. таблицу. У 86,6% женщин нормализовался рН до 4,5–5,5.
Позитивные сдвиги наблюдались и при морфометрическом анализе. Толщина эпидермиса (рис. 1) уменьшилась с 95 (92,4–97,4) мкм исходно до 71,4 (67,5–78,4) мкм к 6-му месяцу (p=0,012) и 66,5 (64,7–70,8) мкм – к 12-му (p=0,01), при этом распространение эхосигнала стало более равномерным. У всех пациенток с плохо видимой границей эпидермиса и дермы дифференцировка к 6 и 12-му месяцам лечения стала четкой.
Толщина дермы (рис. 2) повысилась к 12-му месяцу до 1707,7 (1677,9–1783,5) мкм (p=0,000982). Вследствие синтеза основных белков межклеточного матрикса эхогенность дермы повысилась.
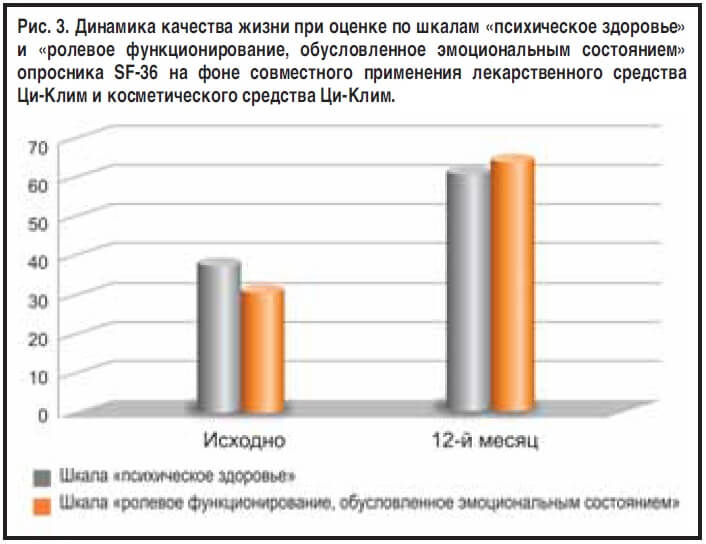
При оценке психоэмоциональной сферы по международному опроснику SF-36 в процессе проводимой терапии было отмечено улучшение показателей по шкале «психическое здоровье» [базально 40 (40–48) баллов, в конце курса лечения 64 (62–74) балла; p<0,05] и «ролевое функционирование, обусловленное эмоциональным состоянием» [базально 33 (33–50) баллов, через год терапии 67 (50–67) баллов; p<0,05]. Наглядно указанные изменения представлены на рис. 3.
Анализ данных по шкале Купермана показал, что у всех женщин с исходно среднетяжелым или тяжелым течением климактерического синдрома (n=6) произошло уменьшение его тяжести и, как следствие, улучшение качества жизни пациенток. Участницы исследования отмечали уменьшение частоты приливов, нормализацию сна, улучшение настроения.
Удовлетворенность лечением отметили подавляющее большинство женщин (13 из 15, или 86,6%). Из них 80% выразили желание рекомендовать аналогичную терапию родным и знакомым.
Обсуждение
Знание физиологии и патологии менопаузального перехода и периода менопаузы, а также возможных методов коррекции негативных последствий возрастных изменений становится особенно актуальным в свете глобальной демографической ситуации в XXI в. В соответствии с данными Всемирной организации здравоохранения, средняя
ожидаемая продолжительность жизни женщин в развитых странах составляет приблизительно 80 лет. Даже в развивающихся странах, таких как Гватемала и Коста-Рика, этот показатель составляет 69 и 70 лет соответственно, а в России он по прогнозам к 2020 г. будет равен 77,3 года [29]. Учитывая, что средний возраст наступления менопаузы в США составляет 52 года, в странах Центральной Америки –
42–44 года, на постменопаузу у большинства женщин приходится больше 1/3 жизни. По данным статистики, к 2030 г. во всем мире будет приблизительно 1,2 млрд женщин в постменопаузальном периоде. Приведенные данные подчеркивают необходимость поиска средств, повышающих качество жизни женщин в постменопаузе [28].
Менопаузальная гормональная терапия является стандартом лечения климактерического синдрома, особенно средней и тяжелой степени. В то же время к ЗГТ имеется ряд противопоказаний, для нее характерны побочные эффекты, среди которых наиболее опасно повышение риска тромбообразования, развития онкологических заболеваний. В соответствии с действующими современными клиническими рекомендациями, при наличии у пациентки легкого или умеренно выраженного климактерического синдрома, абсолютном противопоказании гормональной терапии или вызываемых ею побочных эффектах, наличии онкологических заболеваний половых органов в анамнезе, высоком риске рака молочных желез либо отказе пациентки от гормонотерапии целесообразно применение в качестве альтернативы ЗГТ лекарственных средств растительного происхождения на основе экстракта цимицифуги [23].
Как средство облегчения климакса экстракт цимицифуги используется более 100 лет. Препараты цимицифуги сертифицированы в Германии, США, России для лечения климактерических нейровегетативных симптомов. Клинические исследования демонстрируют эффективность экстракта этого растения в уменьшении частоты и силы приливов, снижении потливости, нормализации сердечного ритма, уменьшении степени тревоги и депрессии, нормализации настроения, улучшении метаболизма костной ткани. Отмечены положительные эффекты экстракта цимицифуги в отношении не только вазомоторных жалоб, но и маркеров костного метаболизма [28, 30].
W.Stoll и соавт. провели двойное слепое плацебо-контролируемое исследование эффективности сухого экстракта цимицифуги, стандартизованного по содержанию тритерпенов (1 г на 20 г экстракта), в сравнении с конъюгированными эстрогенами в отношении купирования климактерических симптомов и атрофии влагалища [31]. В исследование включили 18 женщин в возрасте от 45 до 58 лет, которые получали либо плацебо, либо экстракт цимицифуги в дозе 8 мг (соответствует 48–140 мг сухого сырья), либо конъюгированные эстрогены в дозе 0,625 мг/сут в течение 3 мес. К концу периода лечения во всех 3 группах отмечалось уменьшение выраженности климактерических симптомов, однако значимые результаты были достигнуты в группе лечения экстрактом цимицифуги, что проявилось в снижении индекса Купермана с 34 до 14 (p<0,0001) и свидетельствовало о купировании вазомоторных симптомов, а также в уменьшении уровня тревожности по шкале Гамильтона. Кроме того, на фоне лечения экстрактом цимицифуги выявлено улучшение пролиферации влагалищного эпителия, что объясняется эстрогеноподобным действием экстракта.
Влияние такого же экстракта цимицифуги на течение климактерического синдрома оценивалось в исследовании E.Lehmann-Willenbrock и соавт. [32]. В это рандомизированное сравнительное исследование вошли 16 женщин моложе 40 лет, у которых менопауза была индуцирована гистерэктомией с сохранением одного яичника. Больных распределяли в одну из следующих групп лечения: эстриол в дозе 1 мг/сут, конъюгированные эстрогены (1,25 мг/сут), комбинированная терапия эстроген/прогестаген (эстрадиол 2 мг/норэтистерона ацетат 1 мг) или экстракт цимицифуги 8 мг/сут в течение 6 мес. Эффективность (динамика модифицированного индекса Купермана, уровней фолликулостимулирующего – ФСГ и лютеинизирующего – ЛГ гормонов) оценивали через 4, 8, 12 и 24 нед. Во всех группах отмечалось статистически значимое снижение тяжести климактерических симптомов. Комбинация эстроген/прогестаген и монотерапия конъюгированными эстрогенами оказывала несколько больший эффект, чем экстракт цимицифуги, однако различие не достигало статистической достоверности. Сывороточные уровни ФСГ и ЛГ оставались неизменными на протяжении всего исследования.
Оценка эффективности спиртового экстракта цимицифуги в лечении климактерического синдрома проводилась в исследовании G.Warnecke [33]. Женщинам в возрасте 40–60 лет (n=60) назначался один из вариантов терапии: 80 капель 60% спиртового экстракта цимицифуги, 0,625 мг конъюгированного эстрогена или диазепам 2 мг в течение 12 нед. Во всех 3 группах к концу периода лечения отмечались снижение выраженности климактерических симптомов (приливы жара, потливость, невротические реакции, головные боли, ощущение сердцебиения) при оценке по индексу Купермана, уменьшение тревожности (шкала Гамильтона) и симптомов депрессии (шкала самооценки депрессии). Кроме того, в группах лечения экстрактом цимицифуги и конъюгированным эстрогеном уменьшалась выраженность атрофии эпителия влагалища. При этом лечение экстрактом цимицифуги сопровождалось наиболее выраженными положительными сдвигами в состоянии больных.
E.Liske и соавт. изучали эффективность двух разных дозировок экстракта цимицифуги. Женщины в периоде пери- и постменопаузы были разделены на 2 группы: прием препарата в дозе 39 или 127 мг/сут в течение 6 мес [34]. Снижение индекса Купермана происходило в равной степени в обеих группах уже через 2 нед лечения. К концу 6-го месяца терапии подавляющее большинство женщин (около 90% в обеих группах) ответили на терапию (индекс Купермана 15 и менее). Не наблюдалось изменения уровней ЛГ, ФСГ, связывающего половые гормоны глобулина, пролактина, эстрадиола, также не менялись цитологические характеристики влагалищного эпителия.
Имеются сообщения и о неконтролируемых исследованиях. Так, назначение экстракта цимицифуги в дозе 80 мг/сут в течение 12 нед женщинам (n=36) с климактерическими симптомами приводило к значимому снижению индекса Купермана, также достоверно уменьшалась тяжесть симптомов при оценке по шкале Clinical Global Impressions Scale [35]. В другое открытое исследование вошли 50 женщин, ранее по поводу климактерических расстройств получавшие внутримышечные инъекции эстрадиола валерата 4 мг + прастерона энантата 200 мг каждые 4–6 нед. Они были переведены на прием экстракта цимицифуги 80 мг/сут в течение 6 мес. У 41 пациентки результаты лечения были расценены как хорошие или очень хорошие. Необходимость в продолжении инъекций отпала у 28 (56%) женщин, у 21 (44%) снизилась потребность в инъекциях до 1 раза в 6 мес, достоверное снижение индекса Купермана менее 15 также свидетельствовало об успехе терапии [36].
J.Chen и соавт. назначали экстракт цимицифуги по 20 мг 2 раза в сутки (n=56) либо тиболон (эстроген-гестагенный препарат) в дозе 2,5 мг ежедневно в течение 3 мес для коррекции менопаузальных расстройств больным, получавшим лечение гонадотропин-рилизинг-гормоном после оперативного лечения по поводу эндометриоза. Экстракт цимицифуги показал равную тиболону эффективность при значительно меньшем количестве побочных эффектов [37]. Экстракт цимицифуги при комбинации с пароксетином уменьшает выраженность постменопаузальной депрессии и количество побочных эффектов антидепрессанта [38]. В последние годы проведено большое количество исследований, подтвердивших ранее полученные данные об эффективности и безопасности применения экстракта цимицифуги для лечения перименопаузальных расстройств [39–41].
Интересно, что, несмотря на эстрогеноподобное действие, цимицифуга не снижает уровень ФСГ, за счет чего сохраняется естественная стимуляция яичников женщины и поддерживается выработка собственных эстрогенов [42, 43]. Долгое время считалось, что компоненты экстракта цимицифуги стимулируют рецепторы эстрогенов [44], однако недавно полученные данные позволяют утверждать, что механизм действия цимицифуги может быть связан с воздействием на дофаминовые, серотониновые [45], а также опиатные [46] рецепторы.
Медицинская литература богата публикациями, посвященными проблеме лечения климактерических расстройств фитоэстрогенами, проведено множество клинических исследований, в том числе в России, в которых показана эффективность данных препаратов [47, 48]. Опубликованы большие обзоры на тему клинического применения фитоэстрогенов для предупреждения и купирования менопаузальных симптомов [49, 50]. В данных обзорах постулируются безопасность и положительные результаты лечения фитоэстрогенами. В то же время специальных исследований, посвященных влиянию этих препаратов на состояние кожи, относительно немного.
Лекарственное средство Ци-Клим содержит обладающий эстрогеноподобным действием сухой экстракт цимицифуги с содержанием суммы тритерпеновых сапонинов, в пересчете на безводный эсцин не менее 2,5% – 20 мг [51]. В нашем исследовании совместное применение лекарственного средства Ци-Клим (по 1 таблетке 2 раза в сутки, т.е. 40 мг/сут) и косметического средства Ци-Клим у женщин в перименопаузальном, менопаузальном и постменопаузальном периодах сопровождалось визуальным улучшением состояния кожи, позитивными морфологическими и функциональными изменениями. Уменьшалась толщина эпидермиса, в то время как толщина дермы увеличивалась, что может объясняться повышением содержания коллагеновых, эластиновых волокон и основного вещества. Это предположение подтверждается тем, что после 6-месячного и годового курса терапии увеличивались гидратация и эластичность кожи. Также отмечалось улучшение качества жизни пациенток за счет уменьшения выраженности характерных для климакса расстройств. Бесспорным преимуществом совместного применения лекарственного средства Ци-Клим и косметического средства Ци-Клим является их безопасность. В течение года ни у одной из 15 женщин не отмечалось побочных эффектов.
В I фазе исследования M.Ehrlich и соавт. [52] 12 пациенток с морщинами лица были рандомизированы на применение крема, содержащего экстракт цимицифуги, на левую или правую половину лица и комбинированного крема, содержащего тот же экстракт с L-аскорбиновой кислотой, – на противоположную половину лица 2 раза в день в течение 3 мес. Во II фазе исследования 20 женщин рандомизировали на применение крема с экстрактом цимицифуги на левую или правую половину лица и «питательный восстанавливающий ткани комплекс», содержащий разнообразные ростовые факторы (фактор роста эндотелия сосудов, тромбоцитарный фактор роста, фактор роста гепатоцитов, интерлейкин-6 и 8, трансформирующий фактор роста β), – на противоположную сторону лица 2 раза в день в течение 3 мес. Оценка результатов проводилась по цифровым фотографиям, «заслепленным» врачом-исследователем, также участниц просили высказать мнение о динамике состояния кожи в конце исследования по сравнению с его началом. Все три состава кремов переносились удовлетворительно. По оценке врачей, на стороне лица, на которую наносился крем, содержащий экстракт цимицифуги, отмечалось уменьшение выраженности морщин по специально разработанной шкале на 21,7%. Так же, как в нашем исследовании, большинство участниц исследования остались довольны применением крема с экстрактом цимицифуги. По самооценке пациенток состояние кожи при использовании такого крема улучшилось в 18 случаях, при этом больные предпочитали крем с экстрактом цимицифуги крему с ростовыми факторами.
Выводы
Совместное применение лекарственного средства Ци-Клим и косметического средства Ци-Клим, содержащих экстракт цимицифуги, для коррекции климактерических расстройств и возрастных изменений кожи является высокоэффективной альтернативой в лечении менопаузального старения, отличается безопасностью и хорошей переносимостью. Такой метод терапии позволяет добиться эффекта в лечении инволюционных изменений кожи, устраняя вазомоторные расстройства и улучшая качество жизни женщин.
Литература/References
1. Calleja-Agius J, Muscat-Baron Y, Brincat MP. Skin ageing. Menopause Int. 2007; 13 (2): 60–4.
2. Brincat MP. Hormone Replacement Therapy and the Skin. Lancaster: Parthenon, 2001.
3. Hall GK, Phillips TJ. Skin and hormone therapy. Clin Obstet Gynecol 2004; 47: 437–49.
4. Brincat MP, Baron YM, Galea R. Estrogens and the skin. Climacteric 2005; 8 (2): 110–23.
5. Brincat M, Moniz CF, Kabalan S et al. Decline in skin collagen content and metacarpal index after the menopause and its prevention with sex hormone replacement. Br J Obstet Gynaecol 1987; 94 (2): 126–9.
6. Castelo-Branco C, Duran M, González-Merlo J. Skin collagen changes related to age and hormone replacement therapy. Maturitas 1992; 15 (2): 113–9.
7. Shah MG, Maibach HI. Estrogen and skin. An overview. Am J Clin Dermatol 2001; 2 (3): 143–50.
8. Shuster S. Osteoporosis, a unitary hypothesis of collagen loss in skin and bone. Med Hypotheses 2005; 65 (3): 426–32.
9. Bolognia JL, Braverman IM, Rousseau ME, Sarrel PM. Skin changes in menopause.Maturitas 1989; 11 (4): 295–304.
10. Savvas M, Bishop J, Laurent G et al. Type III collagen content in the skin of postmenopausal women receiving oestradiol and testosterone implants. Br J Obstet Gynaecol 1993; 100 (2): 154–6.
11. Schmidt JB, Binder M, Demschik G et al. Treatment of skin aging with topical estrogens.Int J Dermatol 1996; 35 (9): 669–74.
12. Varila E, Rantala I, Oikarinen A et al. The effect of topical oestradiol on skin collagen of postmenopausal women. Br J Obstet Gynaecol 1995; 102 (12): 985–9.
13. Punnonen R, Vaajalahti P, Teisala K. Local oestriol treatment improves the structure of elastic fibers in the skin of postmenopausal women Ann Chir Gynaecol Suppl 1987; 202: 39–41.
14. Waller JM, Maibach HI. Age and skin structure and function, a quantitative approach (II): protein, glycosaminoglycan, water, and lipid content and structure. Skin Res Technol 2006; 12 (3): 145–54.
15. Sator PG, Schmidt JB, Sator MO et al. The influence of hormone replacement therapy on skin ageing: a pilot study. Maturitas 2001; 39 (1): 43–55.
16. Maheux R, Naud F, Rioux M et al. A randomized, double-blind, placebo-controlled study on the effect of conjugated estrogens on skin thickness. Am J Obstet Gynecol 1994; 170 (2): 642–9.
17. Sumino H, Ichikawa S, Abe M et al. Effects of aging, menopause, and hormone replacement therapy on forearm skin elasticity in women. J Am Geriatr Soc 2004; 52 (6): 945–9.
18. Piérard GE, Letawe C, Dowlati A, Piérard-Franchimont C. Effect of hormone replacement therapy for menopause on the mechanical properties of skin. J Am Geriatr Soc 1995; 43 (6): 662–5.
19. Castelo-Branco C, Figueras F, de Osaba MJM, Vanrell JA. Facial wrinkling in postmenopausal women. Effects of smoking status and hormone replacement therapy. Maturitas 1998; 29 (1): 75–86.
20. Haenggi W, Linder HR, Birkhaeuser MH, Schneider H. Microscopic findings of the nail-fold capillaries – dependence on menopausal status and hormone replacement therapy. Maturitas. 199; 22 (1): 37–46.
21. Arora S, Veves A, Caballaro AE et al. Estrogen improves endothelial function. J Vasc Surg 1998; 27 (6): 1141–6; discussion 1147.
22. Nair PA. Dermatosis associated with menopause. J Midlife Health 2014; 5 (4): 168–75.
23. Клинические рекомендации. Акушерство и гинекология. Под ред. В.Н.Серова, Г.Т.Сухих. Изд. 4-е, перераб. и доп. М.: ГЭОТАР-Медиа, 2014. / Klinicheskie rekomendacii. Akusherstvo i ginekologija. Pod red. V.N.Serova, G.T.Suhih. Izd. 4-e, pererab. i dop. M.: GJeOTAR-Media, 2014. [in Russian]
24. Wines N, Willsteed E. Menopause and the skin. Australas J Dermatol 2001; 42 (3): 149–8; quiz. 159.
25. Лорен С. Женщины и красота. М.: Вагриус, 2001. / Loren S. Zhenshchiny i krasota. M.: Vagrius, 2001. [in Russian]
26. Antiaging Products and Services: The Global Market. BCC Research, 2013 – 164 pages. Интернет-ресурс http://www.bccresearch.com/market-research/healthcare/antiaging-products-serviceshlc060b.html. Дата обращения 21.06.2015. / Antiaging Products and Services: The Global Market. BCC Research, 2013 – 164 pages. Internet resource http://www.bccresearch.com/market-research/healthcare/antiaging-products-services-hlc060b.html. Date accessed 21 Jun 2015. [in Russian]
27. Foster S. Black cohosh: Cimicifuga racemosa: a literature review. Herbalgram. 1999; 45: 35–49.
28. Mahady GB. Black cohosh (Actaea/Cimicifuga racemosa): review of the clinical data for safety and efficacy in menopausal symptoms. Treat Endocrinol 2005; 4 (3): 177–84.
29. Грицюк М. 50 плюс новая жизнь. «Российская газета» – Федеральный вып. №5622 (246) Интернет-ресурс http://www.rg.ru/2011/11/02/trud.html. Дата обращения 21.06.2015. / Gricjuk M. 50 pljus novaja zhizn’. «Rossijskaja gazeta» – Federal’nyj vyp. №5622
(246) Internet-resource http://www.rg.ru/2011/11/02/trud.html.Date accessed 21 Jun 2015. [in Russian]
30. García-Pérez MA, Pineda B, Hermenegildo C et al. Isopropanolic Cimicifuga racemosa is favorable on bone markers but neutral on an osteoblastic cell line. Fertil Steril. 2009; 91 (Suppl. 4): 1347–50.
31. Stoll W. Phytotherapeutikum beeinflusst atrophisches Vaginalepithel: Doppelblind-versuch Cimicifuga vs. Ostrogenpraparat. Therapeutikon 1987; 1: 23–31.
32. Lehmann-Willenbrock E, Riedel HH. Clinical and endocrinologic studies of the treatment of ovarian insufficiency manifestations following hysterectomy with intact adnexa. Zentralbl Gynakol 1988; 110 (10): 611–8.
33. Warnecke G. Influencing menopausal symptoms with a phytotherapeutic agent. Med Welt 1985; 36: 871–4.
34. Liske E, Hänggi W, Henneicke-von Zepelin HH et al. Physiological investigation of a unique extract of black cohosh (Cimicifugae racemosae rhizoma): a 6-month clinical study demonstrates no systemic estrogenic effect. J Womens Health Gend Based Med 2002; 11 (2): 163–74.
35. Daiber W. Klimakterische beschwerden: ohne hormone zum erfolg. Ӓrztliche Praxis 1983; 35: 1946–7.
36. Pethӧ A. Klimakterische beschwerden: umstellung einer hormonbehandlung auf ein pflanzliches gynӓkologikum mӧglich? Ӓrztliche Praxis 1987; 38: 1551–3
37. Chen J, Gao H, Li Q et al. Efficacy and safety of remifemin on perimenopausal symptoms induced by post-operative GnRH-a therapy for endometriosis: a randomized study versus tibolone. Zhonghua Yi Xue Za Zhi 2013; 93 (8): 600–2.
38. Huang YX, Song L, Zhang X et al. Clinical study of combined treatment of remifemin and paroxetine for perimenopausal depression. Zhonghua Yi Xue Za Zhi 2013; 93 (8): 600–2.
39. Juliá Mollá MD, García-Sánchez Y, Romeu Sarri A et al. Cimicifuga racemosa treatment and health related quality of life in postmenopausal Spanish women. Gynecol Endocrinol 2009; 25 (1): 21–6.
40. Ross SM. Menopause: a standardized isopropanolic black cohosh extract (remifemin) is found to be safe and effective for menopausal symptoms. Holist Nurs Pract 2012; 26 (1): 58–61.
41. Drewe J, Zimmermann C, Zahner C. The effect of a Cimicifuga racemosa extracts Ze 450 in the treatment of climacteric complaints – an observational study. Phytomedicine. 2013; 20 (8–9): 659–66.
42. Ayres DC, Loike JD. Lignans. Chemical, biological and clinical properties. Eds. J.D.Phillllipson, D.C.Ayres, H.Baxter. Chemistry & Pharmacology of Natural Products. Cambridge: University Press, 1990.
43. Ботоева Е.А. К вопросу о фитоэстрогенах (обзор литературы). Бюллетень ВСНЦ СО РАМН. 2010. Гинекология. 2013; 15 (1): 85–92. / Botoeva E.A. K voprosu o fitojestrogenah (obzor literatury). Bjulleten’ VSNC SO RAMN. 2010. Gynecology. 2013; 15 (1): 85–92. [in
Russian]
44. Кузнецова И.В. Растительные препараты в климактерии: многообразие и разумный выбор. Эффективная фармакотерапия. 2011; 2: 50–4. / Kuznecova I.V. Rastitel’nye preparaty v klimakterii:mnogoobrazie i razumnyj vybor. Jeffektivnaja farmakoterapija. 2011;
2: 50-4. [in Russian]
45. Кузнецова И.В., Успенская Ю.Б. Применение фитоэстрогенов у женщин в период менопаузального перехода и постменопаузе. Эффективная фармакотерапия. 2013; 52: 44–51. / Kuznecova I.V., Uspenskaja Ju.B. Primenenie fitojestrogenov u zhenshhin v period menopauzal’nogo perehoda i postmenopauze. Jeffektivnaja farmakoterapija. 2013; 52: 44–51. [in Russian]
46. Reame NE, Lukacs JL, Padmanabhan V et al. Black cohosh has central opioid activity in postmenopausal women: evidence from naloxone blockade and positron emission tomography neuroimaging. Menopause 2008; 15 (5): 832–40.
47. Иванова О.В., Усольцева Е.Н., Брюхина Е.В. Клиническая эффективность и динамика качества жизни у женщин с климактерическим синдромом, принимающих фитоэстрогены. Мед. наука и образ. Урала; 2013. 14 (1): 22–5. / Ivanova O.V., Usol’ceva E.N., Brjuhina E.V. Klinicheskaja jeffektivnost’ i dinamika kachestva zhizni u zhenshhin s klimaktericheskim sindromom, prinimajushhih fitojestrogeny. Med. nauka i obraz. Urala; 2013. 14 (1): 22–5. [in Russian]
48. Татарова Н.А., Линде В.А., Жидкова Е.В., Сохадзе Х.С. Негормональная коррекция климактерических расстройств в пери- и пост-менопаузе. Эффективная фармакотерапия. 2009; 17: 12–5. / Tatarova N.A., Linde V.A., Zhidkova E.V., Sohadze H.S. Negormonal’naja korrekcija klimaktericheskih rasstrojstv v peri- i postmenopauze. Jeffektivnaja farmakoterapija. 2009; 17: 12–5. [in Russian]
49. Moreira AC, Silva AM, Santos MS, Sardão VA. Phytoestrogens as alternative hormone replacement therapy in menopause: What is real, what is unknown. J Steroid Biochem Mol Biol 2014; 143: 61–71.
50. Chen MN, Lin CC, Liu CF. Efficacy of phytoestrogens for menopausal symptoms: a meta-analysis and systematic review. Climacteric 2015; 18 (2): 260–9.
51. Инструкция по медицинскому применению препарата Ци-клим, ЗАО «Эвалар», Россия. Регистрационное удостоверение № ЛСР-006592/09.
52. Ehrlich M, Rao J, Pabby A, Goldman MP. Improvement in the appearance of wrinkles with topical transforming growth factor beta(1) and l-ascorbic acid. Dermatol Surg 2006; 32 (5): 618–25.
СВЕДЕНИЯ ОБ АВТОРАХ
Юцковская Яна Александровна – д-р мед. наук, проф., «Клиника профессора Юцковской». E-mail: yutskovskaya@yandex.ru
Суханова Александра Сергеевна – врач-интерн ФДПО ГБОУ ВПО РНИМУ им. Н.И.Пирогова
