Двусторонний и односторонний блефароспазм, гемифациальный спазм
Содержимое флакона 300 ЕД разводят в 1.5 мл 0.9% раствора натрия хлорида для инъекций, содержимое флакона 500 ЕД разводят в 2.5 мл 0.9% раствора натрия хлорида для инъекций. 1 мл и того и другого раствора содержит 200 ЕД препарата Диспорт®.
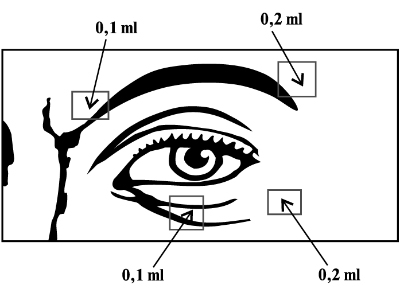
Для взрослых и пациентов пожилого возраста для лечения двустороннего блефароспазма рекомендуемая начальная доза составляет 120 ЕД на каждый глаз. Препарат вводят п/к в объеме 0.1 мл (20 ЕД) медиально, в объеме 0.2 мл (40 ЕД) — латерально в соединение между пресептальной и глазничной частями верхней и нижней частей круговой мышцы (m.orbicularis oculi) пораженного глаза. Для проведения инъекций в верхнее веко иглу следует направлять в сторону от центра, чтобы не задеть мышцу, поднимающую верхнее веко (m.levator palpebrae superioris). Ниже приведена схема, показывающая места проведения инъекций.
Проявление клинического эффекта можно ожидать в течение 2-4 дней, максимальный лечебный эффект развивается в течение 2 недель.
Инъекции следует повторять каждые 12 недель или по показаниям для предупреждения рецидива симптомов. При каждом последующем введении дозу препарата следует уменьшать до 80 ЕД на глаз. Например, 0.1 мл (20 ЕД) медиально и 0.1 мл (20 ЕД) латерально над глазом и ниже глаза. В дальнейшем доза препарата может быть снижена до 60 ЕД на глаз, за счет исключения введения препарата медиально в нижнее веко. Последующие дозы врач определяет в соответствии с полученным эффектом.
При одностороннем блефароспазме инъекции следует ограничить областью пораженного глаза. Аналогичное лечение проводят при гемифациальном спазме.
Спастическая кривошея
Содержимое флакона 300 ЕД разводят в 0.6 мл 0.9% раствора натрия хлорида для инъекций, а флакона 500 ЕД в 1 мл 0.9% раствора натрия хлорида для инъекций. 1 мл и того и другого раствора содержит 500 ЕД препарата Диспорт®.
Дозы, рекомендуемые для лечения кривошеи, применяют у взрослых всех возрастов, имеющих нормальную массу тела и удовлетворительное развитие мышц шеи. Снижение дозы препарата возможно при значимом дефиците массы тела или у лиц пожилого возраста, со сниженной мышечной массой тела.
Для лечения спастической кривошеи начальная суммарная разовая доза составляет 500 ЕД. Данная доза распределяется между 2 или 3 наиболее активными мышцами шеи.
При ротационной кривошее препарат в дозе 500 ЕД вводят следующим образом: 350 ЕД в ременную мышцу головы (m. splenius capitis), ипсилатерально направлению ротации головы и 150 ЕД в грудино-ключично-сосцевидную мышцу (m. sternocleidomastoideus), контрлатеральную ротации.
При латероколлисе (наклоне головы к плечу) дозу препарата 500 ЕД распределяют следующим образом: 350 ЕД вводят ипсилатерально в ременную мышцу головы (m.splenius capitis) и 150 ЕД — ипсилатерально в грудино-ключично-сосцевидную мышцу (m. sternocleidomastoideus). В случаях, сопровождающихся поднятием плеча за счет трапециевидной мышцы (m.trapezius) или мышцы, поднимающей лопатку (m.levator scapulae), может потребоваться лечение в соответствии с видимой гипертрофией мышц или по данным электромиографии.
Когда требуется введение препарата в 3 мышцы, доза 500 ЕД распределяется следующим образом: 300 ЕД вводят в ременную мышцу головы (m.splenius capitis), 100 ЕД — в грудино-ключично-сосцевидную мышцу (m.sternocleidomastoideus), 100 ЕД — в третью мышцу (трапециевидную мышцу или мышцу, поднимающую лопатку).
При антероколлисе (наклоне головы вперед) вводят по 150 ЕД в обе грудино-ключично-сосцевидные мышцы (m. sternocleidomastoideus).
При ретроколлисе (наклоне головы назад) дозу 500 ЕД распределяют следующим образом: вводят по 250 ЕД в каждую ременную мышцу головы (m.splenius capitis). В случае недостаточного клинического эффекта после инъекции можно через 6 недель ввести препарат в трапециевидные мышцы (m.trapezius) билатерально (в дозе до 250 ЕД на каждую мышцу). Двусторонние инъекции в ременные мышцы (m.splenius capitis) могут повысить риск развития слабости мышц шеи.
При последующем назначении препарата дозы могут быть адаптированы в соответствии с клиническим эффектом и возникшими побочными эффектами. Рекомендуемые суммарные дозы составляют 250-1000 ЕД. Применение препарата в более высоких дозах может сопровождаться увеличением частоты побочных эффектов, в частности дисфагии.
Клиническое улучшение при спастической кривошее отмечается в течение 1 недели после инъекции. Инъекции следует повторять каждые 8-12 недель или по мере необходимости.
Для лечения других форм кривошеи большое значение имеет применение электромиографии (ЭМГ) для выявления и введения препарата в наиболее активные мышцы. ЭМГ следует использовать для диагностики всех сложных форм кривошеи или при повторном обследовании пациентов с отсутствием положительной динамики после введения препарата, для проведения инъекций в глубокие мышцы и у пациентов с избыточной массой тела и трудно пальпируемыми мышцами шеи.
Спастичность руки после инсульта у взрослых
Определение показаний для введения препарата Диспорт® при лечении спастичности руки после инсульта производится неврологом через 3 месяца после перенесенного инсульта.
Во флакон с препаратом, содержащий 300 ЕД, вводят 0.6 мл 0.9% раствора натрия хлорида, а во флакон с препаратом, содержащий 500 ЕД, вводят 1 мл 0.9% раствора натрия хлорида. В обоих случаях получая раствор, содержащий 500 ЕД препарата Диспорт® в 1 мл.
Максимальная суммарная разовая доза составляет 1000 ЕД, которую распределяют между следующими 5 мышцами: глубоким сгибателем пальцев (m.flexor digitorum profundus), поверхностным сгибателем пальцев (m.flexor digitorum superficialis), локтевым сгибателем запястья (m.flexor carpi ulnaris), лучевым сгибателем запястья (m.flexor carpi radialis) и двуглавой мышцей плеча (m.biceps brachii).
При выборе места инъекции следует руководствоваться стандартным точками ЭМГ, а непосредственное место инъекции определяется пальпацией. Во все мышцы, кроме двуглавой мышцы плеча (m.biceps brachii), инъекции проводят в одну точку. В двуглавую мышцу плеча (m.biceps brachii) инъекцию проводят в 2 точках. Рекомендуемое распределение дозы между мышцами приведено в таблице.
Начальная суммарная доза препарата может быть снижена до 500 ЕД для предотвращения излишней слабости инъецируемых мышц в тех случаях, когда мышцы-мишени малы по объему, когда инъекция в двуглавую мышцу плеча (m.biceps brachii) не проводится, или когда пациентам инъекция делается в несколько точек одной мышцы.
Клиническое улучшение наступает в течение 2 недель после инъекции. Инъекции можно повторять примерно каждые 16 недель или по необходимости для поддержания эффекта, но не чаще, чем каждые 12 недель.
Гиперкинетические складки (мимические морщины) лица
Основной областью применения препарата Диспорт® с целью косметической коррекции является верхняя половина лица. Нижняя половина лица и шея подвергаются коррекции путем введения ботулинического токсина гораздо реже.
Содержимое флакона 300 ЕД разводят 1.5 мл 0.9% раствора натрия хлорида для инъекций, а содержимое флакона 500 ЕД разводят 2.5 мл 0.9% раствора натрия хлорида для инъекций. При данном разведении 1 мл и того и другого раствора содержит 200 ЕД препарата Диспорт®.
Суммарная рекомендуемая доза при однократном введении во все четыре области (межбровная область, область лба, наружного угла глаза и спинки носа) не должна превышать 200 ЕД препарата Диспорт®.
Для коррекции вертикальных складок в межбровной области инъекции препарата производятся в мышцу, сморщивающую бровь (m.corrugator supercilii), по 8-10 ЕД на 2-4 точки и мышцу гордецов (m.procerus) по 5-10 ЕД в 2 точки. Общая доза составляет от 42 до 100 ЕД.
Устранение гиперкинетических складок в области лба производится путем введения препарата в область максимального напряжения лобной мышца (m.frontalis). Количество точек введения может быть произвольным. Все они должны располагаться на 2 см выше линии бровей на одной линии или V-образно. Оптимальная суммарная доза препарата Диспорт® в этой области составляет 30-40 ЕД (максимальная — 90 ЕД) из расчета по 5-15 ЕД на одну точку, общее количество точек 4-6.
Коррекция складок в области наружного угла глаза («гусиные лапки») осуществляется п/к введением в точки, расположенные на 1 см латеральнее от наружного угла глаза, из расчета 5-15 ЕД препарата Диспорт® на одну точку введения. Количество точек — от 2 до 4 на каждый глаз. Максимальная рекомендуемая суммарная доза на обе стороны составляет 120 ЕД.
Частота повторных инъекций зависит от сроков восстановления мимической активности мышц. Длительность эффекта составляет 3-4 мес.
Если во время первой инъекции была введена адекватная доза препарата, то при проведении второй и последующих инъекций суммарная доза препарата Диспорт® может быть уменьшена на 15-20 ЕД для соответствующих областей. При этом возможно увеличение интервала между инъекциями препарата до 6-9 мес. Если первоначальная доза препарата была недостаточной, то при повторных инъекциях ее следует увеличить.
Для коррекции морщин в области спинки носа инъекции осуществляются в середину брюшка носовых мышц. Доза распределяется по 5-10 ЕД на 1-2 точки в каждую мышцу.
Миорелаксирующее действие препарата Диспорт® на мимические мышцы лица клинически проявляется на 2-3 день после введения и достигает максимума на 14-15 день.
Рекомендуемые дозы препарата Диспорт®, используемые в эстетической медицине, не вызывают системных побочных эффектов.
Динамическая деформация стопы, вызванная спастичностью при ДЦП у детей в возрасте 2 лет и старше
Содержимое флакона 300 ЕД растворяют в 0.6 мл 0.9% раствора натрия хлорида для инъекций, а содержимое флакона 500 ЕД в 1 мл 0.9% раствора натрия хлорида для инъекций, получая и в том и в другом случае раствор, содержащий 500 ЕД в 1 мл.
Препарат вводят в/м в икроножные мышцы (m. gastrocnemius). Начальная рекомендуемая доза составляет 20 ЕД/кг массы тела и делится поровну между икроножными мышцами (m. gastrocnemius). При поражении одной икроножной мышцы (m.gastrocnemius) препарат вводят в дозе 10 ЕД/кг. Оптимальная доза определяется индивидуально, последующее лечение следует планировать после оценки результатов применения начальной дозы. Во избежание развития побочных эффектов не следует превышать максимальную дозу 1000 ЕД. Препарат преимущественно вводят в икроножную мышцу (m.gastrocnemius), однако возможно введение в камбаловидную мышцу (m.soleus) и заднюю большеберцовую мышцу (m.tibialis posterior). Для определения наиболее активных мышц можно использовать метод электромиографии.
В случаях, когда мышцы-мишени пациента малы по объему, начальную дозу препарата следует снизить для предотвращения развития их излишней слабости. Клиническое улучшение наступает в течение 2 недель после введения препарата. Инъекции повторяют по мере необходимости с интервалами не менее 12 недель, при этом вводимая доза может варьировать от 10 до 30 ЕД на 1 кг массы тела в зависимости от эффекта предыдущей инъекции.
Лечение гипергидроза подмышечной области
Содержимое флакона 300 ЕД разводят 1.5 мл 0.9% раствора натрия хлорида для инъекций, а содержимое флакона 500 ЕД разводят 2.5 мл 0.9% раствора натрия хлорида для инъекций, получая и в том и в другом случае раствор, содержащий 200 ЕД в 1 мл.
Рекомендуемая начальная доза — 100 ЕД на одну подмышечную область. Если желаемый эффект не достигается, то возможно последующее увеличение дозы до 200 ЕД.
Область введения препарата определяют пробой Минора. Проба проводится до лечения и, при необходимости, в динамике, при комнатной температуре (22-24°С) после 15-минутного отдыха пациента. Для проведения пробы необходимо: 5% спиртовой раствор йода; картофельный крахмал; маркер; антисептик; кисточка; марлевые салфетки.
Пациент находится в положении лежа, руки под головой. Область потоотделения обрабатывают 5% спиртовым раствором йода и через 1 мин на эту зону салфеткой или кисточкой наносят тонким слоем картофельный крахмал. Результаты теста оценивают через 5 мин. При наличии потоотделения визуально наблюдается окрашивание обработанной поверхности в синий цвет. Интенсивность окраски (от бледно-синего до сине-черного) коррелирует с активностью потоотделения. После проведенной пробы площадь гипергидроза отмечают маркером, затем крахмал смывают спиртом или другим антисептиком.
Внутрикожные инъекции проводят в десять точек в каждой аксиллярной области, в каждую точку вводят по 10 ЕД препарата в объеме 0.05 мл, 100 ЕД на одну область. Максимальный терапевтический эффект развивается в течение 2 недель. В большинстве случаев рекомендуемая начальная доза подавляет потоотделение на срок до 48 недель. Периодичность повторных инъекций определяют индивидуально при восстановлении исходного уровня потоотделения, но не чаще, чем раз в 12 недель. Если есть какие-либо доказательства кумулятивного эффекта при повторных инъекциях, сроки проведения повторных инъекций для каждого пациента определяют индивидуально.
Правила приготовления раствора для инъекций
С флакона удаляют защитную пластмассовую крышку контроля первого вскрытия.
При разведении препарата запрещается открывать флакон, удаляя пробку. Непосредственно перед разведением содержимого флакона центральная часть пробки должна быть обработана спиртом. Лиофилизат разводят, вводя во флакон регламентированный объем 0.9% раствора натрия хлорида для инъекций, путем прокола пробки стерильной иглой размера 23 или 25. Полученный раствор представляет собой бесцветную прозрачную жидкость. Поскольку препарат не содержит консерванта, рекомендуется его использовать сразу же после растворения. Разведенный препарат может храниться не более 8 ч при температуре от 2° до 8°С.
Правила обработки инструментов и уничтожения отходов
Сразу же после проведения инъекции оставшийся раствор во флаконе или в шприце следует инактивировать разбавленным раствором натрия гипохлорита, содержащим 1% активного хлора. Все вспомогательные материалы, находившиеся в контакте с препаратом, следует утилизировать в соответствии со стандартной больничной практикой.
Пролитый препарат следует удалить абсорбирующей салфеткой, смоченной в 1% растворе натрия гипохлорита.
Миорелаксант.
Противопоказано при беременности.
П/к, в/м.
Двусторонний и односторонний блефароспазм, гемифациальный спазм
Для взрослых и пожилых пациентов для лечения двустороннего блефароспазма рекомендуемая начальная доза — 120 ЕД на каждый глаз. Препарат вводят п/к в объеме 0,1 мл (20 ЕД) медиально, в объеме 0,2 мл (40 ЕД) латерально в соединение между пресептальной и глазничной частями как нижней, так и верхней орбитальной мышц каждого глаза. Для проведения инъекций в верхнее веко иглу следует направлять в сторону от центра, чтобы не задеть мышцу, поднимающую верхнее веко. На рисунке 1 показаны места введения препарата.
Рисунок 1. Места проведения инъекций препарата Диспорт®.
Проявление клинического эффекта можно ожидать в течение 2–4 дней, максимальный лечебный эффект развивается в течение 2 нед.
Для профилактики рецидива введение препарата следует повторять каждые 8 нед или в зависимости от клинической ситуации. При каждом последующем введении дозу следует уменьшать до 80 ЕД на глаз. Например — 0,1 мл (20 ЕД) медиально и 0,1 мл (20 ЕД) латерально выше и ниже глаза по способу, представленному выше. В дальнейшем доза препарата может быть снижена до 60 ЕД на глаз за счет исключения введения медиально в нижнее веко. Последующие дозы определяются в зависимости от полученного эффекта.
При одностороннем блефароспазме инъекции следует ограничить областью пораженного глаза. Аналогичное лечение проводят при гемифациальном спазме.
Спастическая кривошея
Содержимое флакона разводят 1 мл 0,9% раствора натрия хлорида для инъекций. 1 мл данного раствора содержит 500 ЕД Диспорта®. Дозы, рекомендуемые для лечения кривошеи, применяют у взрослых, имеющих нормальную массу тела и удовлетворительное развитие мышц шеи. Снижение дозы препарата возможно при выраженном похудании или у лиц пожилого возраста со сниженной мышечной массой тела.
Для лечения спастической кривошеи начальная рекомендуемая разовая доза — 500 ЕД, препарат вводят частями в 2 или 3 наиболее активные мышцы шеи.
При ротационной кривошее 500 ЕД препарата вводят следующим образом: 350 ЕД в ременную мышцу головы ипсилатерально направлению ротации головы и 150 ЕД в грудино-ключично-сосцевидную мышцу, контрлатеральную ротации.
При латероколлисе (наклоне головы к плечу) дозу препарата 500 ЕД распределяют следующим образом: 350 ЕД вводят ипсилатерально в ременную мышцу головы и 150 ЕД — ипсилатерально в грудино-ключично-сосцевидную мышцу. В случаях, сопровождающихся поднятием плеча за счет трапециевидной мышцы или мышцы, поднимающей лопатку, может потребоваться лечение в соответствии с видимой гипертрофией мышц или по данным электромиографии.
При введении препарата в 3 мышцы доза 500 ЕД распределяется следующим образом: 300 ЕД вводят в ременную мышцу, 100 ЕД — в грудино-ключично-сосцевидную мышцу, 100 ЕД — в третью мышцу.
При антероколлисе (наклоне головы вперед) вводят по 150 ЕД в обе грудино-ключично-сосцевидные мышцы.
При ретроколлисе (наклоне головы назад) дозу 500 ЕД распределяют следующим образом: вводят по 250 ЕД в каждую ременную мышцу головы. Затем могут следовать инъекции препарата билатерально в трапециевидные мышцы (до 250 ЕД на мышцу). Повторные инъекции могут быть сделаны спустя 6 нед, если не отмечается достаточного эффекта.
Следует учитывать, что двусторонние инъекции в ременные мышцы могут повысить риск развития слабости мышц шеи.
При последующем введении препарата в соответствии с клиническим эффектом и отмечаемыми побочными эффектами дозы можно довести до оптимальных. Рекомендуются дозы — 250–1000 ЕД. При применении препарата в дозе более 1000 ЕД увеличивается риск развития побочных эффектов, особенно дисфагии. Поэтому применение препарата в дозе более 1000 ЕД не рекомендуется.
Клиническое улучшение при спастической кривошее отмечается в течение 1 нед после инъекции. Рекомендуется повторное введение препарата каждые 8–12 нед или по необходимости для предупреждения рецидивов.
Лечение всех других форм кривошеи проводится по индивидуальным схемам, которые подбирает врач с учетом данных электромиографии (ЭМГ) относительно наиболее активных мышц. ЭМГ следует применять для диагностики всех сложных форм кривошеи или при обследовании пациентов с отсутствием положительной динамики после введения препарата. ЭМГ также используют при введении Диспорта® в глубокие мышцы или у пациентов с избыточной массой тела при слабо пальпируемых мышцах шеи.
Спастичность руки после инсульта у взрослых
Во флакон с препаратом вводят 1 мл 0,9% раствор натрия хлорида, получая раствор, содержащий 500 ЕД Диспорта® в 1 мл. Максимальная доза — 1000 ЕД, которую необходимо распределить между следующими 5 мышцами: m.flexor digitorum profundus, m.flexor digitorum superfacialis, m.flexor carpi ulnaris, m.flexor carpi radialis, m.biceps brachii.
При выборе места инъекции следует ориентироваться на стандартные точки ЭМГ, а непосредственное место инъекции определять пальпацией. Во все мышцы, кроме biceps brachii, инъекции проводят в одну точку. M.biceps brachii инъецируют в 2 точках. Рекомендуемое распределение дозы между мышцами приведено в таблице.
| Мышцы | Количество единиц препарата |
| m.biceps brachii | 300–400 |
| m.flexor digitorum profundus | 150 |
| m.flexor digitorum superficialis | 150–250 |
| m.flexor carpi ulnaris | 150 |
| m.flexor carpi radialis | 150 |
| Общая доза | 1000 |
Начальная доза препарата может быть снижена до 500 ЕД для предотвращения излишней слабости инъецируемых мышц в тех случаях, когда мышцы-мишени малы по объему, инъекция в m.biceps brachii не проводится или делается в несколько точек одной мышцы.
Клиническое улучшение наступает в течение 2 нед. Инъекции можно повторять примерно каждые 16 нед или по необходимости, для поддержания эффекта, но не чаще чем каждые 8 нед.
Лечение гиперкинетических складок (мимических морщин) лица
Основной областью применения препарата с целью косметической коррекции является верхняя половина лица. Нижняя половина лица и шея подвергаются коррекции путем введения ботулинического токсина гораздо реже (в данных областях предпочтительно использовать другие методы).
Содержимое флакона разводят 2,5 мл 0,9% раствора натрия хлорида для инъекций. При данном разведении 1 мл раствора содержит 200 ЕД Диспорта®.
Суммарная рекомендуемая доза при однократном инъецировании всех четырех областей (межбровная область, область лба, наружного угла глаза и спинки носа) не должна превышать 200 ЕД Диспорта®.
Межбровная область. Для коррекции вертикальных складок в межбровной области инъекции препарата производятся в m.corrugator supercilii по 10–20 ЕД на 2–4 точки и m.procerus по 5–10 ЕД в 1–2 точки. Общая доза — от 30 до 100 ЕД.
Область лба. Устранение гиперкинетических складок в области лба производится путем введения препарата в область максимального напряжения m.frontalis. Количество точек введения может быть произвольным. Все они должны располагаться на 2 см выше линии бровей на одной линии или V-образно. Инъекции производятся в общей дозе 20–90 ЕД Диспорта® из расчета по 5–15 ЕД на одну точку, общее количество точек 4–6.
Область наружного угла глаза. Коррекция складок в области наружного угла глаза («гусиные лапки») осуществляется п/к введением в точки, расположенные на 1 см латеральнее от наружного угла глаза, из расчета 5–15 ЕД Диспорта® на одну точку введения. Количество точек от 2 до 4 на каждый глаз. Максимальная рекомендуемая суммарная доза на обе стороны — 120 ЕД.
Частота повторных инъекций зависит от сроков восстановления мимической активности мышц. Длительность эффекта — 3–4 мес. Если во время первой инъекции была введена адекватная доза препарата, то при проведении второй и последующих инъекций суммарная доза Диспорта® может быть уменьшена на 15–20 ЕД для соответствующих областей. При этом возможно увеличение периода действия препарата до 6–9 мес. Если первоначальная доза препарата была недостаточной, то при повторных инъекциях ее следует увеличить.
Область спинки носа. Для коррекции морщин в области спинки носа инъекции осуществляются в середину брюшка носовых мышц. Доза распределяется по 5–10 ЕД на 1–2 точки в каждую мыщцу.
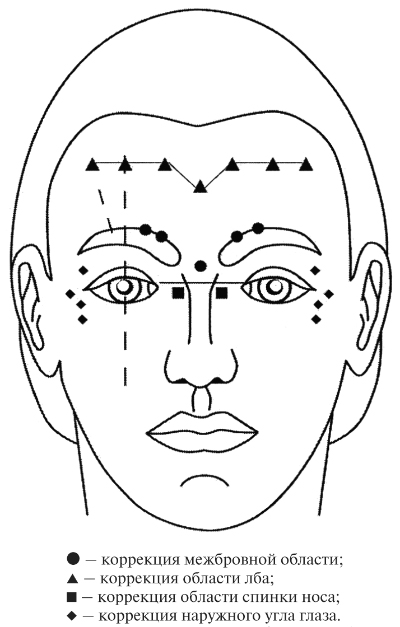
Точки введения препарата показаны на рисунке 2.
Рисунок 2. Точки введения Диспорта® с целью косметической коррекции, где 1 — точки коррекции области лба; 2 — точки коррекции межбровной области; 3 — точки коррекции области спинки носа; 4 — точки коррекции наружного угла глаза.
Миорелаксирующее действие Диспорта® на мимические мышцы лица клинически проявляется на 2–3-й день после введения и достигает максимума на 14–15-й день. Дозы Диспорта®, используемые в эстетической медицине, не оказывают системных побочных эффектов.
Динамическая деформация стопы, вызванная спастичностью при ДЦП у детей старше 2 лет
Содержимое флакона растворяют в 1 мл 0,9% раствора натрия хлорида для инъекций, получая раствор, содержащий 500 ЕД в 1 мл.
Препарат вводят в/м в икроножные мышцы. Начальная рекомендуемая доза составляет 20 ЕД/кг, она делится поровну между икроножными мышцами. При поражении только одной икроножной мышцы препарат вводят в дозе 10 ЕД/кг. Оптимальная доза определяется индивидуально, и последующее лечение следует планировать после оценки результатов применения начальной дозы. Во избежание развития побочных эффектов суммарная доза не должна превышать 1000 ЕД. Преимущественно препарат вводят в m.gastrocnemius, однако возможно введение в m.soleus и m.tibialis posterior. Для определения наиболее активных мышц можно использовать метод ЭМГ. Начальную дозу препарата снижают для предотвращения излишней слабости инъецируемых мышц в тех случаях, когда мышцы-мишени пациента малы по объему или требуется введение препарата в дополнительные мышечные группы. В ходе последующей оценки результатов лечения вводимая доза может варьировать от 10 до 30 ЕД/кг и распределяться между мышцами обеих ног. Клиническое улучшение наступает в течение 2 нед после введения препарата. Инъекции можно повторять примерно каждые 16 нед или по необходимости, для поддержания эффекта, но не чаще чем через 8 нед.
Правила приготовления раствора для инъекций
С флакона удаляют защитную пластмассовую крышку контроля первого вскрытия.
При разведении препарата запрещается открывать флакон, удаляя пробку. Непосредственно перед разведением содержимого флакона центральная часть пробки должна быть обработана спиртом. Лиофилизат разводят, вводя во флакон нужный объем 0,9% раствора натрия хлорида для инъекций путем прокола пробки стерильной иглой размера 23 или 25. Полученный раствор представляет собой бесцветную прозрачную жидкость. Поскольку препарат не содержит консерванта, рекомендуется его использовать сразу же после растворения. Препарат может храниться не более 8 ч при температуре от 2 до 8 °C после растворения, при условии, что растворение проводилось в асептических условиях.
Правила обработки инструментов и уничтожения отходов
Сразу же после проведения инъекции оставшийся во флаконе или в шприце раствор следует инактивировать разбавленным раствором натрия гипохлорита, содержащим 1% активного хлора. Все вспомогательные материалы, находившиеся в контакте с препаратом, должны быть утилизированы в соответствии со стандартной больничной практикой. Пролитый препарат должен быть удален абсорбирующей салфеткой, смоченной в растворе натрия гипохлорита.
Блефароспазм и гемифациальный спазм. Побочное действие может иметь место при несоблюдении врачом правил выполнения инъекции (разведения, точного расчета вводимой дозы, правильного выбора точек введения, направления иглы и глубины введения) и связанной с этим излишней диффузией препарата в близлежащие к месту инъекции группы мышц. Необходимо также учитывать анатомо-физиологические особенности инъецируемых мышц пациента. Наиболее часто встречается блефароптоз. У нескольких пациентов отмечались диплопия или симптомы, свидетельствующие о распространении миорелаксирующего действия на соседние мышцы лица (эти явления проходят в течение 2–4 нед после произведенной инъекции). Возможно появление сухости глаз и развитие кератита вследствие уменьшения частоты моргания (в этих случаях показано применение искусственной слезы), появление гематомы и отечности век кратковременного характера, а также возникновение обратимой наружной офтальмоплегии при применении препарата в высоких дозах.
Инъекции могут сопровождаться чувством жжения в месте введения препарата, которое длится в течение 1–2 мин.
Крайне редко отмечаются аллергические реакции в виде кожной сыпи и гриппоподобных симптомов.
Спастическая кривошея. Побочное действие развивается в результате проведения глубокой инъекции или инъекции в неправильно выбранные мышцы и точки, что ведет к избыточной слабости близлежащих мышц. Инъекции могут сопровождаться чувством жжения в месте введения препарата, которое длится в течение 1–2 мин.
Наиболее часто встречается дисфагия. В двойном слепом плацебо-контролируемом исследовании препарата дисфагия отмечалась у 29% больных, которым назначали Диспорт® в дозе 500 ЕД, и у 10% больных, получавших плацебо. Дисфагия носит дозозависимый характер и отмечается наиболее часто при введении препарата в грудино-ключично-сосцевидную мышцу. При развитии дисфагии необходимо воздерживаться от употребления грубой пищи до исчезновения симптомов. У пациентов с выраженной дисфагией при ларингоскопии отмечалось скопление слюны. В редких случаях у таких пациентов может потребоваться аспирация слюны, особенно при нарушениях проходимости дыхательных путей.
Возможно развитие слабости мышц шеи, сухости во рту, изменение голоса.
В редких случаях отмечались общая слабость, нарушения зрения (включая диплопию и нечеткость зрения), затруднение дыхания (при применении препарата в высоких дозах).
Эти побочные эффекты проходят в течение 2–4 нед. Могут развиваться аллергические реакции в виде кожной сыпи и гриппоподобных симптомов.
Образование противоботулинических антител отмечено у небольшого числа пациентов, которым проводили терапию Диспортом® при лечении кривошеи. Клинически это проявлялось снижением терапевтического эффекта, что требовало постоянного повышения доз препарата.
Спастичность руки у взрослых после инсульта. Наиболее часто развивается слабость близлежащих к месту инъекции мышц, гриппоподобные симптомы (6,1%), сухость во рту, боль в месте инъекции, фарингит, общая слабость, запор, диарея, сонливость (каждая побочная реакция отмечалась не более чем у 4,1% пациентов). Бóльшая часть этих побочных эффектов исчезает в течение 2 нед.
Динамическая деформация стопы, вызванная спастичностью при ДЦП, у детей старше 2 лет. Может развиваться боль в ноге, фарингит (до 8%), слабость мышц, приводящая к случайным травмам (падениям) (до 7%), бронхит и лихорадка (до 6%).
С частотой от 1 до 5% могут проявляться вирусная инфекция, инфекции верхних дыхательных путей, астения, астма, ринит, судороги, кашель, рвота, насморк, диарея, недержание мочи, аномальная походка, гастроэнтерит, ларингит и сонливость. Частота многих из этих реакций (фарингит, бронхит, лихорадка, вирусные инфекции, ринит, инфекции верхних дыхательных путей, кашель, рвота, насморк) аналогична той, которая отмечалась у больных, получавших плацебо.
Астения и недержание мочи возникали при введении Диспорта® в высоких дозах (20–30 ЕД/кг) и могли быть результатом системного воздействия токсина.
Коррекция гиперкинетических складок (мимических морщин) лица. Возможно возникновение обратимого птоза верхнего века (3%), болезненности в месте инъекции, головной боли (1,3%), гематомы в месте инъекции (3–10%), опущение или подъем бровей (<1%). Диплопия встречается крайне редко. Наиболее серьезное осложнение — птоз верхнего века. Вероятной причиной его развития является диффузия препарата в мышцу, поднимающую верхнее веко, при коррекции вертикальных складок над переносицей или горизонтальных морщин на лбу. Птоз носит обратимый характер и исчезает к концу 3–4-й нед после инъекции. Свести к минимуму вероятность возникновения и выраженность данных побочных эффектов можно путем строгого соблюдения методик введения препарата Диспорт® при коррекции гиперкинетических складок (мимических морщин) лица и учета анатомо-физиологических особенностей каждого конкретного пациента.
При одновременном применении с препаратами, влияющими на нервно-мышечную передачу, такими как антибиотики группы аминогликозидов, требуется осторожность.
2 года.
Не применять по истечении срока годности, указанного на упаковке.
Активное вещество:
ботулинический токсин типа a (botulinum A toxin) Ph.Eur. Европейская Фармакопея
Лекарственные формы
| Диспорт® |
Лиофилизат д/пригот. р-ра д/инъекций 300 ЕД: фл. 1 шт.
рег. №: ЛП-001486 от 08.02.12 — ДействующееДата перерегистрации: 30.03.15 |
|
|
Лиофилизат д/пригот. р-ра д/инъекций 500 ЕД: фл. 1 шт.
рег. №: П N011520/01 от 15.08.11 — БессрочноДата перерегистрации: 01.04.15 |
Форма выпуска, упаковка и состав препарата Диспорт®
| Лиофилизат для приготовления раствора для инъекций | 1 фл. |
| комплекс ботулинический токсин типа A — гемагглютинин | 300 ЕД* |
Вспомогательные вещества: альбумин человека — 125 мкг, лактоза — 2.5 мг.
Флаконы стеклянные (1) в держателе из картона — пачки картонные.
* ЕД — единица активности фирмы.
Клинико-фармакологическая группа:
Миорелаксант. Ингибитор высвобождения ацетилхолина
Фармако-терапевтическая группа:
МИБП
Фармакологическое действие
Миорелаксант периферического действия. Действующим началом является токсин Clostridium botulinum типа А, который блокирует высвобождение ацетилхолина в нервно-мышечном соединении, что приводит к снятию мышечного спазма в области введения препарата. Восстановление передачи нервного импульса происходит постепенно, по мере образования новых нервных окончаний и восстановления контактов с постсинаптической моторной концевой пластинкой.
Фармакокинетика
Данных о фармакокинетике препарата Диспорт® не имеется.
Показания препарата Диспорт®
- блефароспазм, гемифациальный спазм, спастическая кривошея, спастичность мышц руки после инсульта, гиперкинетические складки (мимические морщины) лица у взрослых;
- динамическая деформация стопы, вызванная спастичностью, при ДЦП у детей в возрасте 2 лет и старше;
- гипергидроз подмышечной области.
| Код МКБ-10 | Показание |
| G24.3 | Спастическая кривошея |
| G24.5 | Блефароспазм |
| G80 | Церебральный паралич |
| R25.2 | Судорога и спазм |
| R61 | Гипергидроз |
Режим дозирования
Двусторонний и односторонний блефароспазм, гемифациальный спазм
Содержимое флакона 300 ЕД разводят в 1.5 мл 0.9% раствора натрия хлорида для инъекций, содержимое флакона 500 ЕД разводят в 2.5 мл 0.9% раствора натрия хлорида для инъекций. 1 мл и того и другого раствора содержит 200 ЕД препарата Диспорт®.
Для взрослых и пациентов пожилого возраста для лечения двустороннего блефароспазма рекомендуемая начальная доза составляет 120 ЕД на каждый глаз. Препарат вводят п/к в объеме 0.1 мл (20 ЕД) медиально, в объеме 0.2 мл (40 ЕД) — латерально в соединение между пресептальной и глазничной частями верхней и нижней частей круговой мышцы (m.orbicularis oculi) пораженного глаза. Для проведения инъекций в верхнее веко иглу следует направлять в сторону от центра, чтобы не задеть мышцу, поднимающую верхнее веко (m.levator palpebrae superioris). Ниже приведена схема, показывающая места проведения инъекций.
Проявление клинического эффекта можно ожидать в течение 2-4 дней, максимальный лечебный эффект развивается в течение 2 недель.
 Инъекции следует повторять каждые 12 недель или по показаниям для предупреждения рецидива симптомов. При каждом последующем введении дозу препарата следует уменьшать до 80 ЕД на глаз. Например, 0.1 мл (20 ЕД) медиально и 0.1 мл (20 ЕД) латерально над глазом и ниже глаза. В дальнейшем доза препарата может быть снижена до 60 ЕД на глаз, за счет исключения введения препарата медиально в нижнее веко. Последующие дозы врач определяет в соответствии с полученным эффектом.
Инъекции следует повторять каждые 12 недель или по показаниям для предупреждения рецидива симптомов. При каждом последующем введении дозу препарата следует уменьшать до 80 ЕД на глаз. Например, 0.1 мл (20 ЕД) медиально и 0.1 мл (20 ЕД) латерально над глазом и ниже глаза. В дальнейшем доза препарата может быть снижена до 60 ЕД на глаз, за счет исключения введения препарата медиально в нижнее веко. Последующие дозы врач определяет в соответствии с полученным эффектом.
При одностороннем блефароспазме инъекции следует ограничить областью пораженного глаза. Аналогичное лечение проводят при гемифациальном спазме.
Спастическая кривошея
Содержимое флакона 300 ЕД разводят в 0.6 мл 0.9% раствора натрия хлорида для инъекций, а флакона 500 ЕД в 1 мл 0.9% раствора натрия хлорида для инъекций. 1 мл и того и другого раствора содержит 500 ЕД препарата Диспорт®.
Дозы, рекомендуемые для лечения кривошеи, применяют у взрослых всех возрастов, имеющих нормальную массу тела и удовлетворительное развитие мышц шеи. Снижение дозы препарата возможно при значимом дефиците массы тела или у лиц пожилого возраста, со сниженной мышечной массой тела.
Для лечения спастической кривошеи начальная суммарная разовая доза составляет 500 ЕД. Данная доза распределяется между 2 или 3 наиболее активными мышцами шеи.
При ротационной кривошее препарат в дозе 500 ЕД вводят следующим образом: 350 ЕД в ременную мышцу головы (m. splenius capitis), ипсилатерально направлению ротации головы и 150 ЕД в грудино-ключично-сосцевидную мышцу (m. sternocleidomastoideus), контрлатеральную ротации.
При латероколлисе (наклоне головы к плечу) дозу препарата 500 ЕД распределяют следующим образом: 350 ЕД вводят ипсилатерально в ременную мышцу головы (m.splenius capitis) и 150 ЕД — ипсилатерально в грудино-ключично-сосцевидную мышцу (m. sternocleidomastoideus). В случаях, сопровождающихся поднятием плеча за счет трапециевидной мышцы (m.trapezius) или мышцы, поднимающей лопатку (m.levator scapulae), может потребоваться лечение в соответствии с видимой гипертрофией мышц или по данным электромиографии.
Когда требуется введение препарата в 3 мышцы, доза 500 ЕД распределяется следующим образом: 300 ЕД вводят в ременную мышцу головы (m.splenius capitis), 100 ЕД — в грудино-ключично-сосцевидную мышцу (m.sternocleidomastoideus), 100 ЕД — в третью мышцу (трапециевидную мышцу или мышцу, поднимающую лопатку).
При антероколлисе (наклоне головы вперед) вводят по 150 ЕД в обе грудино-ключично-сосцевидные мышцы (m. sternocleidomastoideus).
При ретроколлисе (наклоне головы назад) дозу 500 ЕД распределяют следующим образом: вводят по 250 ЕД в каждую ременную мышцу головы (m.splenius capitis). В случае недостаточного клинического эффекта после инъекции можно через 6 недель ввести препарат в трапециевидные мышцы (m.trapezius) билатерально (в дозе до 250 ЕД на каждую мышцу). Двусторонние инъекции в ременные мышцы (m.splenius capitis) могут повысить риск развития слабости мышц шеи.
При последующем назначении препарата дозы могут быть адаптированы в соответствии с клиническим эффектом и возникшими побочными эффектами. Рекомендуемые суммарные дозы составляют 250-1000 ЕД. Применение препарата в более высоких дозах может сопровождаться увеличением частоты побочных эффектов, в частности дисфагии.
Клиническое улучшение при спастической кривошее отмечается в течение 1 недели после инъекции. Инъекции следует повторять каждые 8-12 недель или по мере необходимости.
Для лечения других форм кривошеи большое значение имеет применение электромиографии (ЭМГ) для выявления и введения препарата в наиболее активные мышцы. ЭМГ следует использовать для диагностики всех сложных форм кривошеи или при повторном обследовании пациентов с отсутствием положительной динамики после введения препарата, для проведения инъекций в глубокие мышцы и у пациентов с избыточной массой тела и трудно пальпируемыми мышцами шеи.
Спастичность руки после инсульта у взрослых
Определение показаний для введения препарата Диспорт® при лечении спастичности руки после инсульта производится неврологом через 3 месяца после перенесенного инсульта.
Во флакон с препаратом, содержащий 300 ЕД, вводят 0.6 мл 0.9% раствора натрия хлорида, а во флакон с препаратом, содержащий 500 ЕД, вводят 1 мл 0.9% раствора натрия хлорида. В обоих случаях получая раствор, содержащий 500 ЕД препарата Диспорт® в 1 мл.
Максимальная суммарная разовая доза составляет 1000 ЕД, которую распределяют между следующими 5 мышцами: глубоким сгибателем пальцев (m.flexor digitorum profundus), поверхностным сгибателем пальцев (m.flexor digitorum superficialis), локтевым сгибателем запястья (m.flexor carpi ulnaris), лучевым сгибателем запястья (m.flexor carpi radialis) и двуглавой мышцей плеча (m.biceps brachii).
При выборе места инъекции следует руководствоваться стандартным точками ЭМГ, а непосредственное место инъекции определяется пальпацией. Во все мышцы, кроме двуглавой мышцы плеча (m.biceps brachii), инъекции проводят в одну точку. В двуглавую мышцу плеча (m.biceps brachii) инъекцию проводят в 2 точках. Рекомендуемое распределение дозы между мышцами приведено в таблице.
| Мышцы | Диспорт® (ЕД) |
| Двуглавая мышца плеча | 300-400 |
| Глубокий сгибатель пальцев | 150 |
| Поверхностный сгибатель пальцев | 150-250 |
| Локтевой сгибатель запястья | 150 |
| Лучевой сгибатель запястья | 150 |
| Общая доза | 1000 |
Начальная суммарная доза препарата может быть снижена до 500 ЕД для предотвращения излишней слабости инъецируемых мышц в тех случаях, когда мышцы-мишени малы по объему, когда инъекция в двуглавую мышцу плеча (m.biceps brachii) не проводится, или когда пациентам инъекция делается в несколько точек одной мышцы.
Клиническое улучшение наступает в течение 2 недель после инъекции. Инъекции можно повторять примерно каждые 16 недель или по необходимости для поддержания эффекта, но не чаще, чем каждые 12 недель.
Гиперкинетические складки (мимические морщины) лица
Основной областью применения препарата Диспорт® с целью косметической коррекции является верхняя половина лица. Нижняя половина лица и шея подвергаются коррекции путем введения ботулинического токсина гораздо реже.
Содержимое флакона 300 ЕД разводят 1.5 мл 0.9% раствора натрия хлорида для инъекций, а содержимое флакона 500 ЕД разводят 2.5 мл 0.9% раствора натрия хлорида для инъекций. При данном разведении 1 мл и того и другого раствора содержит 200 ЕД препарата Диспорт®.
Суммарная рекомендуемая доза при однократном введении во все четыре области (межбровная область, область лба, наружного угла глаза и спинки носа) не должна превышать 200 ЕД препарата Диспорт®.
 Для коррекции вертикальных складок в межбровной области инъекции препарата производятся в мышцу, сморщивающую бровь (m.corrugator supercilii), по 8-10 ЕД на 2-4 точки и мышцу гордецов (m.procerus) по 5-10 ЕД в 2 точки. Общая доза составляет от 42 до 100 ЕД.
Для коррекции вертикальных складок в межбровной области инъекции препарата производятся в мышцу, сморщивающую бровь (m.corrugator supercilii), по 8-10 ЕД на 2-4 точки и мышцу гордецов (m.procerus) по 5-10 ЕД в 2 точки. Общая доза составляет от 42 до 100 ЕД.
Устранение гиперкинетических складок в области лба производится путем введения препарата в область максимального напряжения лобной мышца (m.frontalis). Количество точек введения может быть произвольным. Все они должны располагаться на 2 см выше линии бровей на одной линии или V-образно. Оптимальная суммарная доза препарата Диспорт® в этой области составляет 30-40 ЕД (максимальная — 90 ЕД) из расчета по 5-15 ЕД на одну точку, общее количество точек 4-6.
Коррекция складок в области наружного угла глаза («гусиные лапки») осуществляется п/к введением в точки, расположенные на 1 см латеральнее от наружного угла глаза, из расчета 5-15 ЕД препарата Диспорт® на одну точку введения. Количество точек — от 2 до 4 на каждый глаз. Максимальная рекомендуемая суммарная доза на обе стороны составляет 120 ЕД.
Частота повторных инъекций зависит от сроков восстановления мимической активности мышц. Длительность эффекта составляет 3-4 мес.
Если во время первой инъекции была введена адекватная доза препарата, то при проведении второй и последующих инъекций суммарная доза препарата Диспорт® может быть уменьшена на 15-20 ЕД для соответствующих областей. При этом возможно увеличение интервала между инъекциями препарата до 6-9 мес. Если первоначальная доза препарата была недостаточной, то при повторных инъекциях ее следует увеличить.
Для коррекции морщин в области спинки носа инъекции осуществляются в середину брюшка носовых мышц. Доза распределяется по 5-10 ЕД на 1-2 точки в каждую мышцу.
Миорелаксирующее действие препарата Диспорт® на мимические мышцы лица клинически проявляется на 2-3 день после введения и достигает максимума на 14-15 день.
Рекомендуемые дозы препарата Диспорт®, используемые в эстетической медицине, не вызывают системных побочных эффектов.
Динамическая деформация стопы, вызванная спастичностью при ДЦП у детей в возрасте 2 лет и старше
Содержимое флакона 300 ЕД растворяют в 0.6 мл 0.9% раствора натрия хлорида для инъекций, а содержимое флакона 500 ЕД в 1 мл 0.9% раствора натрия хлорида для инъекций, получая и в том и в другом случае раствор, содержащий 500 ЕД в 1 мл.
Препарат вводят в/м в икроножные мышцы (m. gastrocnemius). Начальная рекомендуемая доза составляет 20 ЕД/кг массы тела и делится поровну между икроножными мышцами (m. gastrocnemius). При поражении одной икроножной мышцы (m.gastrocnemius) препарат вводят в дозе 10 ЕД/кг. Оптимальная доза определяется индивидуально, последующее лечение следует планировать после оценки результатов применения начальной дозы. Во избежание развития побочных эффектов не следует превышать максимальную дозу 1000 ЕД. Препарат преимущественно вводят в икроножную мышцу (m.gastrocnemius), однако возможно введение в камбаловидную мышцу (m.soleus) и заднюю большеберцовую мышцу (m.tibialis posterior). Для определения наиболее активных мышц можно использовать метод электромиографии.
В случаях, когда мышцы-мишени пациента малы по объему, начальную дозу препарата следует снизить для предотвращения развития их излишней слабости. Клиническое улучшение наступает в течение 2 недель после введения препарата. Инъекции повторяют по мере необходимости с интервалами не менее 12 недель, при этом вводимая доза может варьировать от 10 до 30 ЕД на 1 кг массы тела в зависимости от эффекта предыдущей инъекции.
Лечение гипергидроза подмышечной области
Содержимое флакона 300 ЕД разводят 1.5 мл 0.9% раствора натрия хлорида для инъекций, а содержимое флакона 500 ЕД разводят 2.5 мл 0.9% раствора натрия хлорида для инъекций, получая и в том и в другом случае раствор, содержащий 200 ЕД в 1 мл.
Рекомендуемая начальная доза — 100 ЕД на одну подмышечную область. Если желаемый эффект не достигается, то возможно последующее увеличение дозы до 200 ЕД.
Область введения препарата определяют пробой Минора. Проба проводится до лечения и, при необходимости, в динамике, при комнатной температуре (22-24°С) после 15-минутного отдыха пациента. Для проведения пробы необходимо: 5% спиртовой раствор йода; картофельный крахмал; маркер; антисептик; кисточка; марлевые салфетки.
Пациент находится в положении лежа, руки под головой. Область потоотделения обрабатывают 5% спиртовым раствором йода и через 1 мин на эту зону салфеткой или кисточкой наносят тонким слоем картофельный крахмал. Результаты теста оценивают через 5 мин. При наличии потоотделения визуально наблюдается окрашивание обработанной поверхности в синий цвет. Интенсивность окраски (от бледно-синего до сине-черного) коррелирует с активностью потоотделения. После проведенной пробы площадь гипергидроза отмечают маркером, затем крахмал смывают спиртом или другим антисептиком.
Внутрикожные инъекции проводят в десять точек в каждой аксилярной области, в каждую точку вводят по 10 ЕД препарата в объеме 0.05 мл, 100 ЕД на одну область. Максимальный терапевтический эффект развивается в течение 2 недель. В большинстве случаев рекомендуемая начальная доза подавляет потоотделение на срок до 48 недель. Периодичность повторных инъекций определяют индивидуально при восстановлении исходного уровня потоотделения, но не чаще, чем раз в 12 недель. Если есть какие-либо доказательства кумулятивного эффекта при повторных инъекциях, сроки проведения повторных инъекций для каждого пациента определяют индивидуально.
Правила приготовления раствора для инъекций
С флакона удаляют защитную пластмассовую крышку контроля первого вскрытия.
При разведении препарата запрещается открывать флакон, удаляя пробку. Непосредственно перед разведением содержимого флакона центральная часть пробки должна быть обработана спиртом. Лиофилизат разводят, вводя во флакон регламентированный объем 0.9% раствора натрия хлорида для инъекций, путем прокола пробки стерильной иглой размера 23 или 25. Полученный раствор представляет собой бесцветную прозрачную жидкость. Поскольку препарат не содержит консерванта, рекомендуется его использовать сразу же после растворения. Разведенный препарат может храниться не более 8 ч при температуре от 2° до 8°С.
Правила обработки инструментов и уничтожения отходов
Сразу же после проведения инъекции оставшийся раствор во флаконе или в шприце следует инактивировать разбавленным раствором натрия гипохлорита, содержащим 1% активного хлора. Все вспомогательные материалы, находившиеся в контакте с препаратом, следует утилизировать в соответствии со стандартной больничной практикой.
Пролитый препарат следует удалить абсорбирующей салфеткой, смоченной в 1% растворе натрия гипохлорита.
Побочное действие
Во время проведения различных клинических исследований препарата Диспорт® с участием около 7800 пациентов побочные реакции развивались со следующей частотой: очень часто (≥1/10), часто (≥1/100, до <1/10), нечасто (≥1/1000, до <1/100), редко (<1/1000), очень редко (≤1/10 000).
Общие побочные эффекты
Со стороны нервной системы: редко — невралгическая амиотрофия.
Дерматологические реакции: редко — кожная сыпь.
Местные реакции: часто — боль и гематома в месте введения; нечасто — раздражение, чувство жжения в месте инъекции, которое длится 1-2 мин.
Общие реакции: часто — общая слабость, утомляемость, гриппопободный синдром.
Спастичность руки у взрослых после инсульта
Побочные реакции зарегистрированы в 14 клинических исследованиях с участием 141 пациента.
Со стороны пищеварительной системы: часто — дисфагия (была зарегистрирована когда были использованы дозы превышающие 2700 ЕД, введенные в одну точку или распределенные между несколькими точками введения).
Со стороны костно-мышечной системы: часто — слабость мышц руки.
Прочие: часто — случайная травма/падение.
Динамическая деформация стопы, вызванная спастичностью у детей с церебральным параличом
Побочные реакции зарегистрированы в 14 клинических исследованиях с участием около 900 пациентов.
Со стороны пищеварительной системы: часто — диарея.
Со стороны костно-мышечной системы: часто — слабость мышц ноги.
Со стороны мочевыделительной системы: часто — недержание мочи.
Прочие: часто — случайная травма вследствие падения и аномальная походка, которые являются следствием чрезмерной слабости мышц и/или распространением действия токсина на другие, близлежащие к месту инъекции, мышцы, вовлеченные или участвующие в определенном двигательном акте и в поддержании равновесия тела пациента в положении стоя и при ходьбе.
Спастическая кривошея
Побочные реакции зарегистрированы в 21 клиническом исследовании с участием около 4100 пациентов.
Со стороны нервной системы: часто — дисфония; нечасто — головная боль.
Со стороны органа зрения: нечасто — диплопия, нарушение аккомодации.
Со стороны дыхательной системы: редко — респираторные расстройства.
Со стороны пищеварительной системы: очень часто — дисфагия; нечасто — сухость во рту.
Дисфагия носит дозозависимый эффект и происходит наиболее часто при введении препарата в грудино-ключично-сосцевидную мышцу. Может потребоваться диета с исключением грубой пищи до исчезновения симптомов
Блефароспазм и гемифациальный спазм
Побочные реакции зарегистрированы в 13 клинических исследованиях с участием около 1400 пациентов.
Со стороны нервной системы: часто — слабость мышц лица; нечасто — парез мышц лица.
Со стороны органов зрения: очень часто — птоз; часто — диплопия, сухость глаз, слезоотделение; редко — офтальмоплегия.
Дерматологические реакции: часто — отек век; редко — заворот века.
Побочное действие может иметь место при несоблюдении врачом правил выполнения инъекции (разведения, точного расчета вводимой дозы, правильного выбора точек введения, направления иглы и глубины введения) и связанной с этим излишней диффузией препарата и временным параличом близлежащих к месту инъекции группы мышц.
Подмышечный гипергидроз
Побочные реакции зарегистрированы в 4 клинических исследованиях с участием около 217 пациентов.
Дерматологические реакции: часто — компенсаторное потоотделение.
Гиперкинетические складки (мимические морщины) лица
Зарегистрированы следующие побочные реакции (обычно от легкой до умеренной интенсивности).
Со стороны органа зрения: часто — отек век и слизистой оболочки глаза; нечасто — сухость слизистой оболочки глаза (сухой кератоконъюнктивит).
Со стороны костно-мышечной системы: часто — слабость соседних к месту введения мышц, что также часто приводит к птозу век, астенопии (слабость зрения) или, нечасто, к парезу мышц лица и расстройствам зрения.
Со стороны нервной системы: очень часто — головная боль (также часто наблюдаемая в группе плацебо).
Дерматологические реакции: нечасто — сыпь, кожный зуд; редко — крапивница.
Местные реакции: очень часто — боль, гематома, кожный зуд, парестезии, эритема, сыпь в месте введения препарата (которые также часто отмечались и в группе плацебо).
Пострегистрационный опыт применения
Большинство побочных эффектов являются умеренными и преходящими.
Редко: расстройства пищеварения, кожные аллергические реакции, головокружение, головные боли.
Очень редко (1/10 000): выраженная мышечная слабость, дисфагия, аспирационная пневмония, которая может вызвать летальный исход.
Противопоказания к применению
- острые заболевания (введение препарата осуществляют после выздоровления);
- беременность;
- период лактации (грудного вскармливания);
- повышенная чувствительность к компонентам препарата.
Применение при беременности и кормлении грудью
Диспорт® противопоказан к применению при беременности и в период лактации (грудного вскармливания).
Исследований влияния препарата Диспорт® на репродуктивность и тератогенность не проводилось. Безопасность применения препарата Диспорт® при беременности и в период грудного вскармливания не подтверждена.
Применение у пожилых пациентов
Возможно снижение дозы препаратау лиц пожилого возраста со сниженной мышечной массой тела.
Особые указания
Лечение препаратом Диспорт® должны проводить специалисты, имеющие опыт диагностики и лечения данных заболеваний и прошедшие подготовку по проведению лечения этим препаратом.
С особой осторожностью следует повторно вводить препарат больным, у которых отмечены аллергические реакции на предыдущую инъекцию.
Были зарегистрированы побочные эффекты, возникающие в результате действия токсина на мышцы, отдаленные от места введения препарата. Пациенты, получающие Диспорт® в терапевтических дозах, могут испытывать общую мышечную слабость. Риск возникновения подобных побочных эффектов может быть уменьшен при соблюдении рекомендаций по дозированию препарата и применении препарата в минимальных эффективных дозах.
С осторожностью и под строгим медицинским контролем назначают препарат пациентам с субклиническими или клиническими проявлениями поражений нервно-мышечной передачи (например, бульбоспинальный паралич). Такие пациенты могут иметь повышенную чувствительность к препаратам ботулинического токсина, которые могут вызвать у них резко выраженную мышечную слабость.
С осторожностью следует вводить Диспорт® пациентам с нарушениями функций глотания и дыхания, т.к. данные нарушения могут быть усугублены вследствие распространенного действия токсина на соответствующие мышцы.
У пациентов, страдающих хроническими респираторными заболеваниями, в редких случаях возможно развитие аспирации.
При терапии ботулиническими токсинами типа А и В были зарегистрированы единичные случаи летального исхода, вызванные дисфагией (нарушение глотания), пневмопатией или у пациентов со значительной астенией.
Больные и лица, осуществляющие уход за ними, должны быть предупреждены о необходимости срочного обращения к врачу в случаях возникновений нарушений глотания, речи и нарушениях дыхания.
Образование противоботулинических антител отмечено у небольшого числа больных, которым проводили терапию препаратом Диспорт®. Клинически это проявлялось снижением терапевтического эффекта, что требовало постоянного повышения доз препарата.
У пациентов с замедленным временем свертываемости крови и при воспалении в предполагаемом месте введения Диспорт® следует применять в случаях крайней необходимости.
Единицы действия препарата Диспорт® являются специфическими и не могут сравниваться с таковыми других препаратов, содержащих ботулотоксин.
Влияние на способность к вождению автотранспорта и управлению механизмами
Данные о влиянии препарата на способность к вождению автотранспорта и управление механизмами отсутствуют.
Передозировка
Симптомы: генерализованная мышечная слабость.
Лечение: показана поддерживающая терапия, ИВЛ при параличе дыхательных мышц. При передозировке введение антитоксина (противоботулинической сыворотки) целесообразно в течение первых 3 ч. Как правило, лечение передозировки направленно на общую поддерживающую терапию при постоянном наблюдении за больным.
Лекарственное взаимодействие
При одновременном применении с препаратами, влияющими на нервно-мышечную передачу, такими как антибиотики группы аминогликозидов, требуется осторожность.
Условия хранения препарата Диспорт®
Препарат следует хранить и транспортировать всеми видами крытого транспорта при температуре от 2° до 8°С; не замораживать. Срок годности — 2 года.
Диспорт® хранят в отдельной закрытой промаркированной коробке в холодильнике лечебного учреждения, где осуществляется проведение инъекций препарата.
Диспорт® нельзя выдавать на хранение пациенту.
Хранить в недоступном для детей месте.
Срок годности препарата Диспорт®
Срок годности — 2 года. Диспорт® хранят в отдельной закрытой промаркированной коробке в холодильнике лечебного учреждения, где осуществляется проведение инъекций препарата. Диспорт® нельзя выдавать на хранение пациенту. Хранить в недоступном для детей месте.
Лечение блефароспазма, гемифациального спазма, спастической кривошеи, спастичности руки после инсульта, гиперкинетических складок (мимических морщин) лица у взрослых.
Лечение динамической деформации стопы, вызванной спастичностью, у детей с церебральным параличом с 2-х летнего возраста.
Лечение гипергидроза аксилярной области.
Правила приготовления раствора для инъекций
С флакона удаляют защитную пластмассовую крышку контроля первого вскрытия.
При разведении препарата запрещается открывать флакон, удаляя пробку. Непосредственно перед разведением содержимого флакона центральная часть пробки должна быть обработана спиртом. Лиофилизат разводят, вводя во флакон нужный объем 0,9 % раствора натрия хлорида для инъекций, путем прокола пробки стерильной иглой размера 23 или 25. Полученный раствор представляет собой бесцветную прозрачную жидкость. Поскольку препарат не содержит консерванта, рекомендуется его использовать сразу же после растворения. Разведенный препарат может храниться не более 8 ч при температуре от 2 ° до 8 °С .
Способ применения и дозировка
Двусторонний и односторонний блефароспазм, гемифациальный спазм
Содержимое флакона разводят 2,5 мл 0,9 % раствора натрия хлорида для инъекций. 1 мл данного раствора содержит 200 ЕД Диспорта®.
Рекомендуемые дозы применяются у взрослых любого возраста, включая пожилых пациентов. Рекомендованной начальной дозой лечения двустороннего блефароспазма доза в 120 единиц на каждый глаз. Подкожную инъекцию в объеме 0,1 мл (20 единиц) следует провести медиально и в объеме 0,2 мл (40 единиц) латерально в соединение между пресептальной и глазничной частями как нижней, так и верхней орбитальной мышцами пораженного глаза. Для проведения инъекций в верхнее веко иглу следует направлять в сторону от центра, чтобы не задеть мышцу, поднимающую верхнее веко. Ниже приведена схема, показывающая места проведения инъекций.
Проявление эффекта можно ожидать в течение 2-4 дней, а максимальный лечебный эффект развивается в течение двух недель.
Инъекции следует повторять приблизительно каждые 12 недель или по показаниям для предупреждения рецидива симптомов. При каждом последующем введении препарата суммарную дозу следует уменьшать до 80 единиц на глаз. Например, 0,1 мл (20 единиц) медиально и ОД мл (20 единиц) латерально над глазом и ниже его. Доза в дальнейшем может быть снижена до 60 единиц на глаз, за счет исключения введения препарата медиально в нижнее веко. В дальнейшем дозу препарата определяет врач в соответствии с полученным эффектом.
В случае одностороннего блефароспазма инъекции следует ограничить областью пораженного глаза.
Больные, страдающие гемифациальным спазмом, должны лечиться так же, как пациенты с односторонним блефароспазмом.
Спастическая кривошея
Содержимое флакона разводят 1,0 мл 0,9 % раствора натрия хлорида для инъекций. 1 мл данного раствора содержит 500 ЕД Диспорта®. Дозы, рекомендуемые для лечения кривошеи, применяются у взрослых больных всех возрастов, имеющих нормальную массу тела и удовлетворительное развитие мышц шеи. Снижение дозы препарата возможно при значимом дефиците веса пациента или у лиц пожилого возраста, со сниженной мышечной массой тела.
Начальная суммарная разовая доза препарата для лечения спастической кривошеи составляет 500 единиц. Данная доза распределяется между двумя-тремя наиболее активными мышцами шеи.
При ротационной кривошее 500 единиц вводят следующим образом: 350 единиц в ременную мышцу головы, ипсилатерально направлению ротации головы и 150 единиц в грудино-ключично-сосцевидную мышцу, контрлатеральную ротации.
При латероколлисе (наклону головы к плечу) дозу препарата (500 единиц) распределяют следующим образом: 350 единиц вводят ипсилатерально в ременную мышцу головы и 150 единиц ипсилатерально в грудино-ключично-сосцевидную мышцу. В случаях, сопровождающихся поднятием плеча за счет трапециевидной мышцы или мышцы, поднимающей лопатку, может потребоваться лечение в соответствии с видимой гипертрофией мышц или по данным электромиографического обследования. Когда требуется введение в три мышцы, то доза в 500 единиц распределяется следующим образом: 300 единиц препарата вводят в ременную мышцу, 100 единиц — в грудино-ключично-сосцевидную мышцу и 100 единиц — в третью мышцу.
При антероколлисе (наклоне головы вперед) вводят по 150 ЕД в обе грудинно-ключично-сосцевидные мышцы.
При ретроколлисе (наклоне головы назад), дозу в 500 единиц препарата распределяют следующим образом: по 250 единиц в каждую ременную мышцу головы. В случае недостаточного клинического ответа на инъекцию возможно по прошествии 6 недель ввести препарат в трапециевидные мышцы билатерально (в дозе до 250 единиц на каждую мышцу). Двусторонние инъекции в ременные мышцы могут повысить риск появления слабости мышц шеи.
При последующем назначении препарата дозы могут быть адаптированы в соответствии с полученным эффектом и зарегистрированными побочными эффектами. Рекомендуемые суммарные дозы находятся в пределах от 250 до 1000 единиц. Применение более высоких доз может сопровождаться увеличением частоты побочных эффектов, в частности дисфагии.
Улучшение симптоматики при спастической кривошее проявляется в течение первой недели после инъекции. Инъекции следует повторять каждые 8-12 недель или по мере необходимости.
Для лечения других форм кривошеи большое значение имеет применение электромиографии (ЭМГ) для выявления и введения препарата в наиболее активные мышцы. ЭМГ следует использовать для диагностики всех сложных форм кривошеи или при повторном обследовании пациентов с отсутствием положительной динамики после введения препарата, для проведения инъекций в глубокие мышцы и у пациентов с избыточной массой тела и трудно пальпируемыми мышцами шеи.
Спастичность руки у взрослых после инсульта
Определение показаний для введения Диспорта при лечении спастичности руки после инсульта производится неврологом через 3 месяца после перенесенного инсульта.
Во флакон с препаратом вводят 1,0 мл 0,9 % раствора натрия хлорида для инъекций, получая раствор, содержащий 500 единиц Диспорта в 1,0 мл.
Максимальная суммарная разовая доза составляет 1000 ЕД, распределенных между следующими пятью мышцами: m. flexor digitorum profundus (FDP), т. flexor digitorum superficialis (FDS), m. flexor carpi ulnaris (FCU), m. flexor carpi radialis (FCR) и biceps brachii (BB).
При выборе места инъекции следует руководствоваться стандартными точками электромиографии, а непосредственное место инъекции определяется пальпацией. Все мышцы, кроме biceps brachii, подвергаются инъекции в одной точке. Мышцу biceps brachii инъецируют в двух точках. Рекомендуемое распределение дозы между мышцами приводится ниже.
| Мышца | ВВ | FDP | FDS | FCU | FCR | Общая доза |
| Диспорт® (единицы) | 300-400 | 150 | 150-250 | 150 | 150 | 1000 |
Начальная суммарная доза препарата может быть снижена до 500 ЕД для предотвращения излишней слабости инъецируемых мышц в тех случаях, когда мышцы-мишени пациента малы по объему, когда инъекция в мышцу ВВ не вводится, или когда пациентам инъекция делается в несколько точек одной мышцы. Клиническое улучшение наступает в течение двух недель после инъекций. Инъекции можно повторять примерно каждые 16 недель или по необходимости для поддержания эффекта, но не чаще чем каждые 12 недель.
Гиперкинетические складки (мимические морщины) лица
Основной областью применения Диспорта® с целью косметической коррекции является верхняя половина лица. Нижняя половина лица и шея подвергаются коррекции путем введения ботулинического токсина гораздо реже.
Содержимое флакона разводят 2,5 мл 0,9 % раствора хлорида натрия для инъекций. При данном разведении 1 мл раствора содержит 200 ЕД Диспорта®.
Суммарная рекомендуемая доза при однократном инъецировании всех четырех областей (межбровная область, область лба, наружного угла глаза и спинки носа) не должна превышать 200 ЕД.
Межбровная область
Для коррекции вертикальных складок в межбровной области инъекции препарата производятся в m. corrugator supercilii по 8-10 ЕД на 2-4 точки и в m. Procerus по 5-10 ЕД в 2 точки. Суммарная доза составляет от 42 до 100 ЕД.
Область лба
Устранение гиперкинетических складок в области лба производится путем введения препарата в область максимального напряжения m. frontalis. Количество точек введения может быть произвольным. Все они должны располагаться на 2 см выше линии бровей на одной линии или V-образно. Оптимальная суммарная доза Диспорта® в этой области составляет 30-40 ЕД из расчета по 5-15 ЕД на одну точку, общее количество точек 4-6.
Область наружного угла глаза
Коррекция складок в области наружного угла глаза («гусиные лапки») осуществляется подкожным введением в точки, расположенные на 1 см латеральнее от наружного угла глаза, из расчета 5-15 ЕД Диспорта® на одну точку введения. Количество точек от 2 до 4 на каждый глаз. Максимальная рекомендуемая суммарная доза на обе стороны составляет 120 ЕД.
Частота повторных инъекций зависит от сроков восстановления мимической активности мышц. Длительность эффекта составляет 3-4 месяца.
Если во время первой инъекции была введена адекватная доза препарата, то при проведении второй и последующих инъекций суммарная доза Диспорта® может быть уменьшена на 15-20 ЕД для соответствующих областей. При этом возможно увеличение интервала между инъекциями препарата до 6-9 месяцев. Если первоначальная доза препарата была недостаточной, то при повторных инъекциях ее следует увеличить.
Область спинки носа
Для коррекции морщин в области спинки носа инъекции осуществляются в середину брюшка носовых мышц. Доза распределяется по 5-10 единиц на 1-2 точки в каждую мышцу.
Точки введения
? — коррекция межбровной области
^ — коррекция области лба
¦ — коррекция области спинки носа
¦ — коррекция наружного угла глаза
Миорелаксирующее действие Диспорта® на мимические мышцы лица клинически проявляется на 2-3 день после введения и достигает максимума на 14-15 день. Рекомендуемые дозы Диспорта® для использования в эстетической медицине не вызывают системных побочных эффектов.
Динамическая деформация стопы, вызванная спастичностью у детей с церебральным параличом
Содержимое флакона растворяют в 1 мл 0,9 % раствора натрия хлорида для инъекций, получая раствор, содержащий 500 ЕД в 1 мл.
Препарат вводят внутримышечно в икроножные мышцы. Начальная рекомендуемая доза — 20 единиц на 1 кг массы тела ребенка делится поровну между икроножными мышцами. При поражении только одной икроножной мышцы в нее вводят дозу из расчета 10 единиц на 1 кг массы тела. Оптимальная доза индивидуальна, последующее лечение должно планироваться после оценки результатов применения начальной дозы. Для предупреждения побочных эффектов суммарная доза не должна превышать 1000 ЕД. Препарат вводят преимущественно в m.gastrocnemius, однако возможно введение в m.soleus и m.tibialis posterior. Для определения наиболее активных мышц можно использовать метод электромиографии.
В случаях, когда мышцы-мишени пациента малы по объему, начальную дозу следует снизить для предотвращения развития их излишней слабости. Клиническое улучшение наступает в течение 2-х недель после введения препарата. Инъекции повторяют по мере необходимости с интервалами не менее 12 недель, при этом вводимая доза может варьировать в пределе от 10 — 30 ЕД на кг массы тела в зависимости от эффекта предыдущей инъекции.
Лечение гипергидроза аксилярной области.
Содержимое флакона разводят 2,5 мл 0,9 % раствором натрия хлорида для инъекций, получая раствор, содержащий 200 ЕД в 1 мл. Рекомендуемой начальной дозой лечения аксилярного гипергидроза является 100 ЕД на одну аксилярную область. Если желаемый эффект не достигается, то возможно последующее увеличение дозы до 200 ЕД Диспорта®.
Область введения препарата определяют пробой Минора. Проба проводится до лечения и, при необходимости, в динамике, при комнатной температуре (22 — 24 °С) после 15 — минутного отдыха пациента. Для проведения пробы необходимо:
- 5 % спиртовой раствор йода;
- картофельный крахмал;
- маркер;
- антисептик;
- кисточка;
- марлевые салфетки.
Пациент находится в положении лежа, руки под головой. Область потоотделения обрабатывают 5 % — ным спиртовым раствором йода и через 1 мин. на эту зону салфеткой или кисточкой наносят тонким слоем картофельный крахмал. Результаты теста оценивают через 5 мин. При наличии потоотделения визуально наблюдается окрашивание обработанной поверхности в синий цвет. Интенсивность окраски (от бледно-синего до сине-черного) коррелирует с активностью потоотделения. После проведенной пробы площадь гипергидроза отмечают маркером, затем крахмал смывают спиртом или другим антисептиком.
Внутрикожные инъекции проводят в десять точек в каждой аксилярной области, в каждую точку вводят по 10 ЕД препарата в объеме 0,05 мл, 100 ЕД на одну область. Максимальный терапевтический эффект развивается в течение двух недель. В большинстве случаев рекомендуемая начальная доза подавляет потоотделение на срок до 48 недель. Периодичность повторных инъекций определяют индивидуально при восстановлении исходного уровня потоотделения, но не чаще, чем раз в 12 недель. Если есть какие либо доказательства кумулятивного эффекта при повторных инъекциях, сроки проведения повторных инъекций для каждого пациента определяют индивидуально.
МНН: Гемагглютинин — комплекс ботулинического токсина типа А
Производитель: ИПСЕН Биофарм Лтд
Анатомо-терапевтическо-химическая классификация: Botulinum toxin
Номер регистрации в РК:
№ РК-БП-5№020468
Информация о регистрации в РК:
17.06.2019 — бессрочно
- Скачать инструкцию медикамента
Торговое название
Диспорт®
Международное непатентованное название
Нет
Лекарственная форма
Лиофилизат для приготовления раствора для внутримышечного и подкожного введения, 300 ЕД
Состав
Один флакон содержит
активное вещество — комплекс ботулинический токсин типа А – гемагглютинин 300 ЕД*,
вспомогательные вещества: альбумин человека, лактозы моногидрат, вода для инъекций**
* — одна единица (ЕД) эквивалентна LD50 дозы для мышей при внутрибрюшинном введении
** — вода для инъекций удаляется в процессе лиофилизации
Описание
Белый лиофилизированный порошок, свободный от видимых частиц. Восстановленный раствор – прозрачный бесцветный раствор, свободный от твердых частиц.
Фармакотерапевтическая группа
Миорелаксанты. Миорелаксанты периферического действия. Миорелаксанты периферического действия другие. Ботулинический токсин
Код АТХ М03АХ01
Фармакологические свойства
Фармакокинетика
Исследование фармакокинетики ботулинического токсина у животных затруднено в связи с его высокой активностью, низкими дозами, большой молекулярной массой, а также трудностью в нанесении радиоактивной метки для получения достаточно высокой специфической активности. Исследования с токсином, меченным I125, показали, что связывание c рецепторами является специфичным и прочным, кроме того, высокая плотность рецепторов к токсину является фактором, способствующим высокой нейротропности. Доза и время наступления результата у обезьян показали, что при низких дозах время задержки реакции составляет 2–3 дня, а максимальный эффект отмечался на 5-6 день после введения препарата. Продолжительность действия, измеряемая изменениями мышц глаза при косоглазии, варьировала от 2-х недель до 8 месяцев. Данное явление также наблюдалось у человека и относится к процессу связывания, интернализации и изменений в нервно-мышечном соединении.
Фармакодинамика
Комплекс ботулинический токсин типа А — гемагглютинин блокирует периферическую холинергическую передачу в нервно-мышечном соединении посредством пресинаптического действия в месте проксимального высвобождения ацетилхолина. Токсин действует внутри нервного окончания, нарушая Ca2+-зависимые механизмы, которые завершаются высвобождением нейромедиаторов. Токсин не влияет на постганглионарную холинергическую передачу или постганглионарную симпатическую передачу.
Действие токсина включает в себя обязательный начальный этап, на котором токсин быстро прикрепляется к пресинаптической мембране нервного окончания. Второй этап – интернализация: токсин проникает через пресинаптическую мембрану, не вызывая возникновения паралича. Наконец, токсин ингибирует высвобождение ацетилхолина, нарушая Ca2+-опосредованный механизм высвобождения ацетилхолина, тем самым уменьшая потенциал концевой пластинки и вызывая паралич.
Восстановление передачи нервного импульса происходит постепенно, по мере образования новых нервных окончаний и восстановления контактов с постсинаптической моторной концевой пластинкой, процесс занимает 6-8 недель у экспериментальных животных.
Показания к применению
— спастичность руки в сочетании с физиотерапией
— динамическая деформация стопы, вызванная спастичностью, у детей с церебральным параличом с 2-х летнего возраста
— спастическая кривошея у взрослых
— блефароспазм у взрослых
— гемифациальный спазм у взрослых
— подмышечный гипергидроз
— временное улучшение внешнего вида умеренных и выраженных мимических морщин у взрослых пациентов до 65 лет, если выраженность этих линий оказывает серьезное психологическое влияние на пациента
Способ применения и дозы
Единицы измерения активности Диспорта® являются специфическими для этого препарата и не могут сравниваться с другими препаратами ботулинического токсина.
Диспорт® должен вводиться только соответствующим образом обученными врачами.
Компания Ipsen может оказать содействие в обучении введению Диспорта®.
Спастичность руки
Во флакон с препаратом вводят 0.6 мл 0.9% раствора натрия хлорида для инъекций, получая раствор, содержащий 500 ЕД Диспорта® в 1.0 мл. Диспорт вводится внутримышечно в пять мышц, описанных ниже.
Рекомендуемая доза составляет 1000 ЕД, распределенных между следующими пятью мышцами: m. biceps brachii (BB) (двуглавая мышца плеча), m. flexor digitorum profundus (FDP) (глубокий сгибатель пальцев), m. flexor digitorum superficialis (FDS) (поверхностный сгибатель пальцев), m. flexor carpi ulnaris (FCU) (сгибатель локтевой), m. flexor carpi radialis (FCR) (сгибатель лучевой):
|
Мышца |
ВВ |
FDP |
FDS |
FCU |
FCR |
Общая доза |
|
Диспорт® |
300-400 ЕД |
150 ЕД |
150-250 ЕД |
150 ЕД |
150 ЕД |
1000 ЕД |
При выборе места инъекции следует руководствоваться стандартными точками электромиографии, а непосредственное место инъекции определяется пальпацией. Все мышцы, кроме двуглавой мышцы плеча, подвергаются инъекции в одной точке. Двуглавую мышцу плеча инъецируют в 2-х точках. Максимальная доза не должна превышать 1000 ЕД.
Начальная доза препарата должна быть уменьшена, если есть признаки, что данная доза может привести к избыточной слабости инъецируемых мышц, например если мышцы-мишени пациента малы по объему, когда инъекция в мышцу ВВ не вводится, или когда пациентам производятся сопутствующие инъекции в другие группы мышц. Клиническое улучшение наступает в течение двух недель после инъекции. Инъекции можно повторять примерно каждые 16 недель или при необходимости для поддержания эффекта, но не чаще, чем каждые 12 недель.
Дети: Безопасность и эффективность Диспорта® при лечении спастичности руки у детей не установлены.
Динамическая деформация стопы, вызванная спастичностью у детей с церебральным параличом
Содержимое флакона растворяют в 0.6 мл 0.9% раствора натрия хлорида для инъекций, получая раствор, содержащий 500 ЕД в мл.
Препарат вводят внутримышечно в икроножные мышцы.
Начальная доза 20 ЕД на 1 кг массы тела делится поровну между икроножными мышцами. При поражении только одной икроножной мышцы вводят дозу 10 единиц на 1 кг массы тела. Требуется рассмотреть необходимость уменьшения начальной дозы, если есть признаки, что данная доза может привести к избыточной слабости инъецируемых мышц, например, если мышцы-мишени пациента малы по объему, или когда пациентам производятся сопутствующие инъекции в другие группы мышц.
Оптимальная доза индивидуальна, и последующее лечение должно планироваться после оценки результатов применения начальной дозы. Последующие дозы препарата могут колебаться в пределах 10–30 ЕД/кг, распределенных для мышц обеих ног Для предупреждения побочных эффектов максимальная доза не должна превышать30 ЕД/кг или 1000 ЕД (в зависимости от того, что будет меньшим).
Препарат преимущественно вводят в икроножную мышцу, однако возможно введение в камбаловидную мышцу (m. soleus) и заднюю большеберцовую мышцу.
Применение электромиографии (ЭМГ) не является обычной лечебной практикой, но может помочь в определении наиболее активных мышц.
Клиническое улучшение наступает в течение 2-х недель после инъекции. Инъекции можно повторять примерно каждые 16 недель или при необходимости для поддержания эффекта, но не чаще, чем каждые 12 недель.
Спастическая кривошея
Препарат разводят в 0.6 мл 0.9% раствора натрия хлорида для инъекций, получая раствор, содержащий 500 ЕД в мл. Дозы, рекомендуемые для лечения кривошеи, применяются у взрослых больных всех возрастов, имеющих нормальную массу тела и удовлетворительное развитие мышц шеи. Снижение дозы препарата возможно при заметном похудании или у лиц пожилого возраста, когда возможно снижение мышечной массы.
Начальной рекомендуемой разовой дозой препарата для лечения спастической кривошеи является доза в 500 ЕД, которую вводят частями в две или три наиболее активные мышцы шеи.
При вращательной кривошее 500 ЕД вводят следующим образом: 350 ЕД в ременную мышцу головы, ипсилатерально в направлении вращения подбородок/голова и 150 ЕД в грудино-ключично-сосцевидную мышцу, контрлатерально вращению.
При боковой кривошее дозу препарата в 500 ЕД распределяют следующим образом: 350 ЕД вводят ипсилатерально в ременную мышцу головы и 150 ЕД ипсилатерально в грудино-ключично-сосцевидную мышцу. В случаях, сопровождающихся поднятием плеча за счет трапециевидной мышцы или мышцы, поднимающей лопатку, может потребоваться лечение в соответствии с видимой гипертрофией мышц или по данным электромиографического обследования.
Когда требуется введение в три мышцы, то доза в 500 ЕД распределяется следующим образом: 300 ЕД препарата вводят в ременную мышцу, 100 ЕД – в грудино-ключично-сосцевидную мышцу и 100 ЕД – в третью мышцу.
При ретроколлисе дозу в 500 ЕД распределяют следующим образом: по 250 ЕД в каждую ременную мышцу головы. Двусторонние инъекции в ременные мышцы могут повысить риск возникновения слабости мышц шеи.
Лечение всех других форм кривошеи непосредственно связано со знаниями специалиста и данными электромиографии (ЭМГ) для выявления и введения препарата в наиболее активные мышцы. ЭМГ следует использовать для диагностики всех сложных форм кривошеи или при повторном обследовании пациентов с отсутствием положительной динамики после введения препарата, для проведения инъекций в глубокие мышцы и у пациентов с избыточной массой тела и трудно пальпируемыми мышцами шеи.
При последующем введении препарата дозы могут доводиться до оптимальных в соответствии с клиническим эффектом и отмечаемыми побочными действиями препарата. Для введения рекомендуются дозы препарата в пределах 250 – 1000 ЕД, хотя применяют и более высокие дозы, но они могут сопровождаться увеличением числа побочных эффектов, и, в особенности, появлением дисфагии. Максимальная применяемая доза не должна превышать 1000 ЕД.
Улучшение симптоматики при спастической кривошее проявляется в течение одной недели после инъекции. Инъекции следует повторять каждые 16 недель или по мере необходимости для предотвращения рецидивов симптоматики, но не чаще, чем каждые 12 недель.
Дети: Безопасность и эффективность Диспорта® при лечении спастической кривошеи у детей не установлены.
Блефароспазм, гемифациальный спазм.
Содержимое флакона разводят 1.5 мл 0.9% раствора натрия хлорида для инъекций. 1 мл данного раствора содержит 200 ЕД Диспорта®.
В клинических испытаниях при определении дозы Диспорта® для лечения доброкачественного эссенциального блефароспазма доза в 40 ЕД на каждый глаз была значительно эффективной. Дозы по 80 и 120 ЕД на каждый глаз привели к более длительному эффекту. Тем не менее, частота местных побочных эффектов, в частности птоз, была дозозависимой. При лечении блефароспазма и гемифациального спазма максимальная доза Диспорта® не должна в общей сложности превышать 120 ЕД на каждый глаз.
Препарат в дозе 10 ЕД (0,05 мл) медиально и 10 ЕД (0,05 мл) латерально вводят в соединение между пресептальной и глазничной частями как верхней (3 и 4), так и нижней круговой мышц (m. orbicularis oculi) (5 и 6) каждого глаза. Для снижения риска птоза, необходимо избегать инъекций около мышцы, поднимающей верхнее веко (m. levator palpebrae superioris).
Для проведения инъекций в верхнее веко иглу следует направлять в сторону от центра, чтобы не задеть мышцу, поднимающую верхнее веко (m.levator palpebrae superioris). Приведена схема, показывающая места проведения инъекций.
Инъекции следует повторять каждые 12 недель или по показаниям для предупреждения рецидива симптомов, но не чаще чем каждые 12 недель. При каждом последующем введении, если результат от первоначальной дозы считается недостаточным, доза может быть увеличена до 60 ЕД: 10 ЕД (0,05 мл) медиально и 20 ЕД (0,1мл) латерально, 80 ЕД: 20 ЕД (0,1 мл) медиально и 20 ЕД (0,1 мл) латерально или до 120 ЕД: 20 ЕД (0,1 мл) медиально и 40 ЕД (0,2 мл) латерально выше и ниже глаза по схеме, указанной выше. В дополнительные места лобной мышцы над бровью (1 и 2) вводятся инъекции, если спазмы в них мешают зрению.
При одностороннем блефароспазме лечение ограничивается областью пораженного глаза. При гемифациальном спазме лечение такое же, как и при одностороннем блефароспазме.
Рекомендуемые дозы применяются у взрослых любого возраста, включая пожилых пациентов.
Дети: Безопасность и эффективность Диспорта® при лечении блефароспазма и гемифациального спазма у детей не установлены.
Подмышечный гипергидроз
Содержимое флакона разводят 1.5 мл 0.9% раствора натрия хлорида для инъекций. 1 мл данного раствора содержит 200 ЕД Диспорта®. Рекомендуемые дозы применяются у взрослых любого возраста, включая пожилых пациентов. Рекомендуемая начальная доза составляет 100 ЕД на каждую подмышечную область. Если ожидаемый эффект не достигается, при последующих инъекциях может применяться до 200 ЕД на каждую подмышечную область. Область, подлежащая инъецированию, должна быть предварительно определена путем проведения пробы Минора (йодно-крахмальной пробы). Обе подмышечные области должны быть очищены и продезинфицированы. Применяются внутрикожные инъекции в десяти точках, по 10 ЕД на каждую точку, по 100 ЕД на каждую подмышечную область. Максимальный терапевтический эффект наблюдается на второй неделе после инъекции. В большинстве случаев рекомендуемая доза обеспечивает адекватную супрессию потоотделения в течение приблизительно 48 недель. Периодичность повторных инъекций определяют индивидуально при восстановлении исходного уровня потоотделения, но не чаще, чем через каждые 12 недель. Имеются некоторые данные о кумулятивном эффекте повторных доз, таким образом, сроки проведения повторных инъекций для каждого пациента определяют индивидуально.
Дети: Безопасность и эффективность Диспорта® при лечении подмышечного гипергидроза у детей не установлены.
Мимические морщины (вертикальные складки в межбровной области)
Содержимое флакона разводят 1.5 мл 0.9 % раствора натрия хлорида для инъекций. При данном разведении 1 мл раствора содержит 200 ЕД Диспорта®.
Следует удалить макияж и дезинфицировать кожу местным антисептиком.
Рекомендуемая доза составляет 50 ЕД (0,25 мл), которые распределяют на 5 точек введения. По 10 ЕД (0,05 мл) вводят внутримышечно в каждую из 5 точек: по 2 инъекции в каждую m. corrugator supercilii (мышца, сморщивающая бровь) и одна инъекция в m. procerus (мышца гордецов) около назофронтального угла, как показано на схеме, приведенной ниже:
Анатомические ориентиры могут быть определены путем осмотра и пальпации при максимальном нахмуривании. Перед инъекцией плотно прижмите большой или указательный палец ниже края орбиты, чтобы предотвратить кровоизлияние ниже края глазницы. Внутримышечные инъекции должны быть выполнены под прямым углом к коже с помощью стерильной иглы размером 29-30. Во время инъекции игла должна быть направлена вверх и медиально. В целях уменьшения риска птоза следует избегать проведения инъекций близко к m. levator palpebrae superioris (мышца, поднимающая верхнее веко), особенно у пациентов с выраженными мышцами, опускающими брови (m. depressor supercilii). Инъекции в m. corrugator supercilii должны проводиться в центральную часть данной мышцы, по меньшей мере, на 1 см выше края орбиты.
Интервалы между курсами лечения зависят от индивидуальной реакции пациента. Курсы лечения не должны быть чаще одного раза в три месяца.
Дети: Использование препарата при коррекции мимических морщин у пациентов моложе 18 лет не рекомендуется.
Правила приготовления раствора для инъекций
С флакона удаляют защитную пластмассовую крышку контроля первого вскрытия. При разведении препарата запрещается открывать флакон, удаляя пробку. Непосредственно перед разведением содержимого флакона центральная часть пробки должна быть обработана спиртом. Лиофилизат разводят, вводя во флакон нужный объем 0.9% раствора натрия хлорида для инъекций, путем прокола пробки стерильной иглой размера 23 или 25. Полученный раствор представляет собой бесцветную прозрачную жидкость. Поскольку препарат не содержит консерванта, рекомендуется использовать его сразу же после растворения. Хранить разведенный препарат можно в асептических условиях при температуре от 2 ˚С до 8 ˚С не более 8 часов.
Побочные действия
Классификация побочных реакций: очень часто ˃1/10; часто ˃ 1/100 , < 1/10; нечасто ˃ 1/1000 ,< 1/100; редко ˃ 1/10000, ˃ 1/1000; очень редко ˃ 1/10000.
Сообщалось о побочных явлениях связанных с отдаленным распространением действия токсина от места введения (резко выраженная мышечная слабость, дисфагия, аспирация / аспирационная пневмония, со смертельным исходом в очень редких случаях).
Общие побочные эффекты
В ходе программы клинического исследования приблизительно 28% пациентов, получающих лечение Диспортом®, испытали побочные эффекты.
Следующие нежелательные воздействия наблюдались у пациентов, проходивших лечение по различным показаниям, включая блефароспазм, гемифациальный спазм, кривошея и спастичность, связанная с церебральным параличом или инсультом.
Со стороны нервной системы
Редко: невралгическая амиотрофия
Со стороны кожи и подкожных тканей
Нечасто: зуд
Очень редко: кожная сыпь
Осложнения общего характера и реакции в месте введения
Часто: общая слабость, утомляемость, гриппопободный синдром, боль/ гематома в месте введения
Спастичность руки
Нарушения со стороны желудочно-кишечного тракта
Часто: дисфагия
Нарушения со стороны опорно-двигательного аппарата и соединительной ткани
Часто: слабость мышц руки
Травмы, отравления и осложнения процедур
Часто: случайная травма/падение
Динамическая деформация стопы, вызванная спастичностью у детей с церебральным параличом
Нарушения со стороны желудочно-кишечного тракта
Часто: диарея
Нарушения со стороны опорно-двигательного аппарата и соединительной ткани
Часто: слабость мышц ноги, мышечная боль
Нарушения со стороны почек и мочевыделительной системы
Часто: недержание мочи
Осложнения общего характера и реакции в месте введения
Часто: аномальная походка
Травмы, отравления и осложнения процедур
Часто: случайная травма вследствие падения.
Случайная травма вследствие падения и аномальная походка могут быть следствием избыточной слабости мышц и/или распространением действия Диспорта® на другие мышцы, участвующие в определенном двигательном акте и в поддержании равновесия тела.
Спастическая кривошея
Нарушения со стороны нервной системы
Часто: головная боль, головокружение, парез мышц лица
Нарушения со стороны органов зрения
Часто: нечеткость зрения, снижение остроты зрения
Нечасто: диплопия, птоз
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения
Часто: дисфония, диспноэ
Очень редко: аспирация
Нарушения со стороны желудочно-кишечного тракта
Очень часто: дисфагия, сухость во рту
Нарушения со стороны опорно-двигательного аппарата и соединительной ткани
Очень часто: мышечная слабость
Часто: боль в шее, костно-мышечная боль, миалгия, боль в конечностях, костно-мышечной скованность
Нечасто: мышечная атрофия, расстройство со стороны челюсти
Дисфагия носит дозозависимый характер и встречается наиболее часто при введении препарата в грудино-сосцевидную мышцу. Может потребоваться диета с исключением грубой пищи до исчезновения симптомов.
Данные нежелательные явления исчезают в течение двух-четырех недель.
Блефароспазм и гемифациальный спазм
Нарушения со стороны нервной системы
Часто: слабость мышц лица
Нечасто: парез мышц лица
Нарушения со стороны органов зрения
Очень часто: птоз
Часто: диплопия, сухость глаз, слезоотделение
Редко: офтальмоплегия
Нарушения со стороны кожи и подкожных тканей
Часто: отек век
Редко: энтропион (заворот века)
Побочные действия могут иметь место при несоблюдении точек введения и глубины введения Диспорта®, временно парализующего близлежащие к месту инъекции группы мышц.
Подмышечный гипергидроз
Нарушения со стороны кожи и подкожных тканей
Часто: компенсаторная потливость
Мимические морщины
Нарушения со стороны нервной системы
Очень часто: головная боль
Часто: парез лица (преимущественно парез бровей)
Нечасто: головокружение
Нарушения со стороны органа зрения
Часто: астенопия, птоз, отек век, повышение слезотечения, сухость глаз, подергивание мышц вокруг глаз
Нечасто: зрительные нарушения, нечеткость зрения, диплопия
Редко: нарушения движения глаз
Нарушения со стороны кожи и подкожной ткани
Нечасто: кожная сыпь, зуд
Редко: крапивница
Осложнения общего характера и реакции в месте введения
Очень часто: реакции в месте введения (эритема, отек, раздражение, сыпь, зуд, парестезия, боль, дискомфорт, жжение и кровоподтек)
Нарушения со стороны иммунной системы
Нечасто: гиперчувствительность
Пострегистрационный опыт применения
Профиль нежелательных реакций, сообщенный компании во время пострегистрационного применения, отражает фармакологию продукта и соответствует тем, которые наблюдались во время клинических исследований. Кроме того, реакций о гиперчувствительности не поступало.
Противопоказания
— повышенная чувствительность к какому-либо компоненту препарата
— период лактации
— наличие инфекционного процесса в предполагаемом месте инъекции
— миастения гравис, синдром Ламберта-Итона, боковой амиотрофический склероз
— детский возраст до 2-х лет при лечении спастичности, обусловленной детским церебральным параличом
— детский возраст до 18 лет при всех остальных показаниях
Лекарственные взаимодействия
Воздействие ботулинического токсина может быть усилено лекарственными препаратами, взаимодействующими прямо или косвенно с нервно-мышечной функцией (например, аминогликозиды, кураре-подобные недеполяризующие блокаторы). Такие препараты следует назначать с осторожностью пациентам, проходящим лечение ботулиническим токсином.
Особые указания
Единицы Диспорта® являются специфическими для этого препарата и не могут сравниваться с другими препаратами ботулинического токсина.
Диспорт® должен вводиться только соответствующим образом обученными врачами.
Компания Ipsen может оказать содействие в обучении введению Диспорта®.
Сообщалось о побочных явлениях, связанных с отдаленным распространением действия токсина от места введения (усиленная мышечная слабость, дисфагия, аспирация / аспирационная пневмония, со смертельным исходом в очень редких случаях).
Пациенты, получающие Диспорт® в терапевтических дозах, могут испытывать чрезмерную мышечную слабость. Риск возникновения подобных побочных эффектов может быть уменьшен при соблюдении рекомендаций по дозированию препарата и применении минимальных эффективных доз препарата.
Диспорт® должен применяться с осторожностью и под пристальным медицинским наблюдением только у пациентов с субклиническими или клиническими признаками нарушения нервно-мышечной передачи (например, миастения гравис). Такие пациенты могут иметь повышенную чувствительность к препаратам ботулинического токсина, которые в терапевтических дозах могут вызвать у них резко выраженную мышечную слабость. Пациенты с сопутствующими неврологическими расстройствами подвергаются повышенному риску данного побочного эффекта.
На фоне проводимой терапии ботулиническим токсином типа А или В были зарегистрированы единичные случаи смерти, вызванные дисфагией (нарушением глотания), пневмопатией и/или у пациентов со значительно выраженной астенией. Пациенты с нарушениями нервно-мышечной передачи, затруднением глотания или дыхания имеют больший риск возникновения этих побочных эффектов. Лечение таких пациентов должно осуществляться под контролем специалиста и только тогда, когда ожидаемая польза лечения превышает риск.
Диспорт® должен применяться с осторожностью у пациентов с имеющимися нарушениями глотания или дыхания, поскольку проявления этих нарушений могут ухудшиться в случае распространения действия токсина на соответствующие мышцы. Аспирация отмечалась в редких случаях, и это является фактором риска при лечении больных, имеющих хронические дыхательные расстройства.
Рекомендованные дозы и кратность введения не должны превышаться.
Пациенты и лица, осуществляющие уход за ними, должны быть предупреждены о необходимости срочного обращения к врачу в случаях возникновений нарушений глотания, речи и нарушениях дыхания.
Диспорт® не должен применяться для лечения спастичности у пациентов, которые имеют устойчивую контрактуру.
Как и при любой внутримышечной инъекции, Диспорт® должен использоваться только в случае крайней необходимости у пациентов с длительными кровотечениями, инфекцией или воспалением на предполагаемом участке инъекции.
Диспорт® должен применяться для лечения одного пациента за одну сессию. Особые меры предосторожности должны приниматься в ходе подготовки к инъекции и при введении препарата, а так же при инактивации и утилизации оставшегося разведенного раствора.
Диспорт® содержит небольшое количество человеческого альбумина. Нельзя с абсолютной уверенностью исключить риск передачи вирусной инфекции после использования человеческой крови или продуктов на основе крови.
Образование антител к ботулиническому токсину отмечалось редко у больных, получавших лечение препаратом Диспорт®. Клинически наличие нейтрализующих антител выражалось в значительном ухудшении реакции на проводимое лечение и в необходимости постоянного увеличения дозы.
При применении Диспорта® для коррекции мимических морщин необходимо предварительно изучить анатомию лица пациента. Асимметрия лица, птоз, выраженный дерматохалазис, рубцы и любые анатомические повреждения вследствие предшествовавших хирургических вмешательств должны быть приняты во внимание. Особые меры предосторожности должны быть предприняты, если в мышцах, в которые предполагается провести инъекции, наблюдается чрезмерная слабость или атрофия.
Эффекты от применения различных ботулинических нейротоксинов во время курса лечения Диспортом® неизвестны, следует избегать подобных ситуаций.
Применение в педиатрии
Для лечения детского церебрального паралича Диспорт® может применяться только у детей в возрасте старше 2-х лет. Лечение детей с церебральным параличом проводится только в специализированных учреждениях с персоналом, прошедшим соответствующую подготовку При других показаниях безопасность и эффективность Диспорта® не была продемонстрирована.
Беременность и период лактации
Имеются ограниченные данные по применению комплекса ботулинический токсин типа А-гемагглютинин у беременных женщин. Исследования на животных показали репродуктивную токсичность в дозах, вызывающих токсичное действие на материнский организм.
Диспорт® следует применять во время беременности только в том случае, если польза оправдывает любой потенциальный риск для плода. Следует соблюдать осторожность при назначении беременным женщинам.
Не имеется данных о том, проникает ли комплекс ботулинический токсин типа А-гемагглютинин в грудное молоко. Не проводилось исследований на животных о выделении комплекса ботулинический токсин типа А-гемагглютинин в грудное молоко. Поэтому применение препарата в период кормления грудью не рекомендуется.
Особенности влияния лекарственного средства на способность управлять транспортным средством или потенциально опасными механизмами
Имеется потенциальный риск мышечной слабости и нарушения зрения, которые могут временно ухудшить способность управлять транспортным средством и работать с потенциально опасными механизмами.
Специальные указания по обработке остатков раствора препарата
Сразу же после проведения инъекции оставшийся во флаконе или в шприце раствор следует инактивировать разбавленным раствором гипохлорита натрия (содержащим 1% активного хлора). Все вспомогательные материалы, находившиеся в контакте с препаратом, должны быть утилизированы в соответствии со стандартной больничной практикой.
Пролитый раствор Диспорта® следует вытереть абсорбирующей салфеткой, смоченной раствором гипохлорита натрия.
Передозировка
Чрезмерные дозы могут вызвать отдаленный и глубокий нервно-мышечный паралич. Передозировка может привести к повышению риска попадания нейротоксина в системный кровоток, что может вызвать осложнения, связанные с проявлениями перорального ботулинического отравления (например, дисфагия и дисфония). Может потребоваться проведение искусственной вентиляции легких при передозировке, приведшей к параличу дыхательных мышц. Не имеется определенного антидота; Введение антитоксина неэффективно и лечение передозировки должно быть направлено на поддерживающую терапию. В случае передозировки пациент должен находиться под медицинским наблюдением на наличие признаков и/или симптомов избыточной мышечной слабости или паралича мышц. В случае необходимости провести симптоматическое лечение.
Симптомы передозировки могут проявиться не сразу после передозировки. Если произошло случайное введение инъекции или пероральное попадания пациент должен находиться под медицинским наблюдением в течение нескольких недель на наличие признаков и/или симптомов избыточной мышечной слабости или паралича мышц.
Форма выпуска и упаковка
Лиофилизат помещают во флакон нейтрального стекла типа 1, вместимостью 3 мл, укупоренный пробкой из хлорбутила, зафиксированной алюминиевым ободком с отверстием в центре, поверх которого имеется крышечка контроля первого вскрытия из пластика.
Флакон, зафиксированный в держателе из картона, вместе с инструкцией по медицинскому применению на русском и государственном языках помещается в пачку картонную.
Условия хранения
Хранить при температуре от 2 ˚С до 8 ˚С. Не замораживать.
Хранить в недоступном для детей месте!
Срок хранения
2 года
Не применять по истечении срока годности, указанного на упаковке.
После разведения препарат может храниться не более 8 ч при температуре от 2 ˚С до 8 ˚С
Условия отпуска из аптек
По рецепту
Препарат нельзя выдавать на хранение пациенту
Производитель
Ипсен Биофарм Лимитед, Великобритания
IPSEN Biopharm Limited — Ash Road, Wrexham Industrial Estate,
Wrexham, CLWYD, LL 13 9UF, U.K.
Владелец регистрационного удостоверения
Ипсен Биофарм Лимитед, Великобритания
IPSEN Biopharm Limited – 190 Bath Road, Slough, Berkshire, SL1 3XE, U.K.
Адрес организации, принимающей на территории Республики Казахстан претензии от потребителей по качеству продукции (товара):
Представительство АО IPSEN PHARMA (Ипсен Фарма) в РК
050040 г. Алматы, пр. Аль-Фараби, 45, оф. 2
Тел./факс: 8 (727) 2646448, 2646620, 2646715
Адрес электронной почты: aigul.ismagulova@ipsen.kz
| 950446201477976788_ru.doc | 157 кб |
| 170800851477977962_kz.doc | 203.5 кб |
Отправить прикрепленные файлы на почту
Национальный центр экспертизы лекарственных средств, изделий медицинского назначения и медицинской техники
