Дуаклир Дженуэйр — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер:
ЛП-003844
Торговое наименование:
Дуаклир Дженуэйр
Группировочное наименование:
аклидиния бромид + формотерол
Лекарственная форма:
порошок для ингаляций дозированный
СОСТАВ
Одна отмеренная доза содержит:
Активныевещества: аклидиния бромид микронизированный (в расчете на аклидиний) 0,400 мг (0,343 мг)* и формотерола фумарата дигидрат микронизированный 0,012 мг**.
Вспомогательное вещество: лактозы моногидрат 11,588 мг.
* доставленная доза аклидиния бромида – 396 мкг, что соответствует 340 мкг аклидиния.
** доставленная доза формотерола фумарата дигидрата – 11,8 мкг.
Описание
Ингалятор: Ингалятор белого цвета с оранжевым защитным колпачком, с оранжевой дозирующей кнопкой и закрепленной сдвигающейся крышкой с картриджем, содержащим 60 доз препарата и счетчиком доз.
Содержимое картриджа: Белый или почти белый мелкодисперсный, легкосыпучий порошок, не содержащий видимых конгломератов или посторонних частиц.
Фармакотерапевтическая группа:
бронходилатирующее средство комбинированное (β2-адреномиметик селективный+м-холиноблокатор)
Код АТХ: R03AL05
ФАРМАКОЛОГИЧЕСКИЕ СВОЙСТВА
Механизм действия
Препарат Дуаклир Дженуэйр содержит два бронходилататора: аклидиний, антагонист мускариновых рецепторов длительного действия (также называемый антихолинергик), и формотерол, длительно действующий агонист β2-адренергических рецепторов. Комбинация этих веществ с разными механизмами действия обеспечивает аддитивный эффект по сравнению с применением отдельных компонентов. Вследствие различия плотности мускариновых и β2-адренорецепторов в центральных и периферических дыхательных путях, антагонисты мускариновых рецепторов более эффективны в расслаблении центральных дыхательных путей, а агонисты β2-адренергических рецепторов – периферических дыхательных путей; таким образом, применение комбинированной терапии может усиливать благоприятное воздействие на функцию легких.
Аклидиний является конкурентным, селективным антагонистом мускариновых рецепторов с более длительным временем связывания с M3-рецепторами, чем с M2-рецепторами. M3-рецепторы служат посредниками при сокращении гладкой мускулатуры дыхательных путей. Вдыхаемый аклидиния бромид действует местно
в легких в качестве антагониста M3-рецепторов гладкой мускулатуры дыхательных путей и вызывает бронходилатацию. Применение аклидиния у пациентов с хронической обструктивной болезнью легких (ХОБЛ) вызывает также снижение выраженности симптомов, улучшение связанного с заболеванием состояния
здоровья, снижение частоты обострений и улучшение переносимости физической нагрузки. Поскольку аклидиния бромид быстро разрушается в плазме крови, количество системных антихолинергических побочных эффектов является низким.
Формотерол является мощным селективным агонистом β2-адренорецепторов.
Бронходилатация достигается за счет расслабления гладкой мускулатуры дыхательных путей вследствие повышения уровня циклического аденозинмонофосфата после активации аденилатциклазы. Помимо улучшения функции легких, формотерол уменьшает выраженность симптомов и повышает качество жизни у пациентов с ХОБЛ.
Фармакодинамика
Клинические исследования показали, что препарат Дуаклир Дженуэйр обеспечивает клинически значимое улучшение функции легких (оцениваемое по объему форсированного выдоха за 1 секунду (ОФВ1)) в течение более 12 часов после приема.
Препарат Дуаклир Дженуэйр обладает быстрым началом действия – в течение 5 минут после первой ингаляции по сравнению с плацебо. Начало действия препарата Дуаклир Дженуэйр было сравнимо с эффектом быстродействующего агониста β2-адренорецепторов, формотерола, в дозе 12 мкг. Максимальная бронходилатация (максимальный ОФВ1) по сравнению с исходным уровнем достигалась с первого дня (304 мл) и поддерживалась в течение всего периода терапии длительностью более 6 месяцев (326 мл).
Электрофизиология сердца
Не было выявлено клинически значимого влияния препарата Дуаклир Дженуэйр на параметры электрокардиограммы (ЭКГ), включая интервал QT, по сравнению с аклидинием, формотеролом и плацебо, а также на сердечный ритм при проведении суточного мониторирования по Холтеру.
Клиническая эффективность
Программа клинических исследований III фазы с участием приблизительно 4000 пациентов с клиническим диагнозом ХОБЛ средней или тяжелой степени включала два 6-месячных рандомизированных исследования с плацебо и активным контролем (ACLIFORM-COPD и AUGMENT), 6-месячную продленную фазу исследования AUGMENT, а также дополнительное 12-месячное рандомизированное, контролируемое исследование.
В долгосрочных исследованиях безопасности препарат Дуаклир Дженуэйр показал стойкую эффективность при длительности применения более 1 года, без признаков тахифилаксии.
Влияние на функцию легких
Препарат Дуаклир Дженуэйр (340 мкг + 11,8 мкг/доза 2 раза в сутки) обеспечивал клинически значимое улучшение функции легких (оцениваемое по ОФВ1, форсированной жизненной емкости легких и емкости вдоха) по сравнению с плацебо. Клинически значимый бронходилатирующий эффект достигался в течение 5 минут после приема первой дозы препарата и поддерживался в течение всего междозового интервала.
В исследовании ACLIFORM-COPD препарат Дуаклир Дженуэйр обеспечивал улучшение ОФВ1 через 1 час после приема дозы по сравнению с плацебо и аклидинием, на 299 мл и 125 мл, соответственно (p<0,0001 в обоих сравнениях), и улучшение остаточного ОФВ1 по сравнению с плацебо и формотеролом, на 143 мл и 85 мл, соответственно (p<0,0001 в обоих сравнениях). В исследовании AUGMENT улучшение ОФВ1 через 1 час после приема дозы по сравнению с плацебо и аклидинием, составило 284 мл и 108 мл, соответственно (p<0,0001 в обоих сравнениях), а улучшение остаточного ОФВ1 по сравнению с плацебо и формотеролом составило 130 мл (p<0,0001) и 45 мл (p=0,01), соответственно.
Облегчениесимптомовиулучшениесостоянияздоровья, обусловленного заболеванием
Одышка и другие симптомы
Препарат Дуаклир Дженуэйр обеспечивал клинически значимое улучшение в отношении одышки (оценивалось с помощью транзиторного индекса одышки (TDI)), с повышением индекса TDI через 6 месяцев терапии по сравнению с плацебо на 1,29 единиц в исследовании ACLIFORM-COPD (p<0,0001) и на 1,44 единицы – в исследовании AUGMENT (p<0,0001).
Объединенный анализ этих двух исследований показал, что применение препарата Дуаклир Дженуэйр ассоциируется со статистически значимым большим улучшением индекса TDI по сравнению с аклидинием (на 0,4 единицы; p=0,016) или формотеролом (на 0,5 единиц; p=0,009).
Препарат Дуаклир Дженуэйр улучшал дневную симптоматику ХОБЛ, в частности одышку, симптомы со стороны грудной клетки, кашель и отделение мокроты (оценивалась с помощью общего индекса E-RS), а также общую выраженность ночных симптомов, ранних утренних симптомов и симптомов, ограничивающих активность в ранние утренние часы, по сравнению с плацебо, аклидинием и формотеролом, однако данное улучшение не всегда было статистически значимым. Комбинация аклидиния/формотерола не показала статистически значимого снижения среднего количества ночных пробуждений, обусловленных ХОБЛ, по сравнению с плацебо или формотеролом.
Качество жизни, обусловленное состоянием здоровья В исследовании AUGMENT препарат Дуаклир Дженуэйр обеспечивал статистически значимое улучшение состояния здоровья, обусловленного заболеванием (оценивалось с помощью Респираторного опросника больницы Святого Георгия (SGRQ)), с улучшением общего индекса SGRQ на -4,35 единицы по сравнению с плацебо (p<0,0001). В исследовании ACLIFORM-COPD наблюдалось лишь небольшое снижение общего индекса SGRQ по сравнению с плацебо вследствие неожиданно выраженного ответа на терапию плацебо (p=0,598), и процент пациентов, достигших клинически значимого улучшения относительно исходного уровня, составил 55,3% в группе препарата Дуаклир Дженуэйр и 53,2% – в группе плацебо (p=0,669).
Объединенный анализ данных этих двух исследований показал большее улучшение общего индекса SGRQ при применении препарата ДуаклирДженуэйр по сравнению с формотеролом (-1,7 единиц; p=0,018) или аклидинием (-0,79 единиц; p=0,273).
Снижение частоты обострений ХОБЛ
В рамках объединенного анализа эффективности двух исследований длительностью 6 месяцев было продемонстрировано статистически значимое снижение на 29% частоты обострений средней или тяжелой степени (требующих терапии антибиотиками или кортикостероидами, или приводящих к госпитализации) на фоне терапии препаратом Дуаклир Дженуэйр по сравнению с плацебо (частота на пациента в год: 0,29 против 0,42, соответственно; p=0,036), а также увеличение времени до первого обострения средней или тяжелой степени по сравнению с плацебо (соотношение рисков 0,70; p=0,027).
Применение препаратов экстренной терапии
Препарат Дуаклир Дженуэйр снижал потребность в препарате экстренной терапии на протяжении более 6 месяцев по сравнению с плацебо (на 0,9 ингаляций/сутки (p<0,0001)), аклидинием (на 0,4 ингаляции/сутки (p<0,001)) и формотеролом (на 0,2 ингаляции/сутки (p=0,062)).
Фармакокинетика
Параметры фармакокинетики аклидиния и формотерола при ингаляционном применении в комбинации существенно не отличались от наблюдаемых при применении отдельных компонентов. Абсорбция
После однократной ингаляции препарата Дуаклир Дженуэйр, аклидиний и формотерол быстро абсорбировались в плазму крови с достижением максимальной концентрации в течение 5 минут после ингаляции у здоровых добровольцев и в течение 24 минут после ингаляции у пациентов с ХОБЛ. Максимальные равновесные концентрации аклидиния и формотерола у пациентов с ХОБЛ, получавших препарат Дуаклир Дженуэйр 2 раза в сутки в течение 5 дней, достигались в течение 5 минут после ингаляции и составляли 128 пг/мл и 17 пг/мл, соответственно.
Распределение
Общее количество попадающего в легкие через ингалятор Дженуэйр аклидиния составило приблизительно 30% отмеренной дозы. Связывание аклидиния с белками плазмы in vitro вероятнее всего соответствует связыванию метаболитов с белками, вследствие быстрого гидролиза аклидиния в плазме крови. Связывание с белками плазмы крови составило 87% для метаболита карбоновой кислоты и 15% для спиртового метаболита. Основным белком плазмы крови, который связывает аклидиний, является альбумин.
Связывание формотерола с белками плазмы крови составляет 61% — 64% (34% – преимущественно с альбумином). Не отмечено насыщения центров связывания в диапазоне концентраций, достигающихся при применении препарата в терапевтических дозах.
Биотрансформация
Аклидиний быстро и интенсивно гидролизуется до фармакологически неактивных спиртового производного и производного карбоновой кислоты. Происходит химический (неферментативный) и ферментативный гидролиз под действием эстераз. Основной эстеразой, вовлеченной в гидролиз у человека, является бутирилхолинэстераза. Концентрация кислотного метаболита в плазме крови после ингаляции приблизительно в 100 раз выше, чем концентрация спиртового метаболита и неизмененного активного вещества.
Низкая абсолютная биодоступность аклидиния при ингаляционном введении (<5%) обусловлена его интенсивным системным и пресистемным гидролизом как при нахождении в легких, так и при приеме внутрь. Биотрансформация с участием изоферментов цитохрома P450 (CYP450) играет незначительную роль в общем метаболическом клиренсе аклидиния. Исследования invitroпоказали, что аклидиний в терапевтической дозе или его метаболиты не ингибируют или не индуцируют какие-либо изоферменты CYP450 и не ингибируют эстеразы (карбоксилэстеразу, ацетилхолинэстеразу и бутирилхолинэстеразу). Также in vitro установлено, что аклидиний или его метаболиты не являются субстратами или ингибиторами P-гликопротеина.
Формотерол выводится преимущественно посредством метаболизма. Основным путем является прямая глюкуронизация с O-деметилированием с последующей конъюгацией с глюкуронидом. В O-деметилировании формотерола участвуют изоферменты CYP2D6, CYP2C19, CYP2C9 и CYP2A6. В терапевтически значимых концентрациях формотерол не ингибирует изоферменты CYP450.
Выведение
После ингаляции препарата Дуаклир Дженуэйр 340 мкг + 11,8 мкг/доза конечный период полувыведения аклидиния и формотерола составляет приблизительно 5 ч и 8 ч, соответственно.
После внутривенного введения 400 мкг меченого радиоактивным изотопом аклидиния здоровым добровольцам около 1% введенной дозы выводилось в неизмененном виде с мочой. До 65% дозы препарата выводилось в виде метаболитов с мочой и до 33% – в виде метаболитов с фекалиями. После ингаляции 200 мкг и 400 мкг аклидиния здоровыми добровольцами и пациентами с ХОБЛ выведение неизмененного аклидиния с мочой было очень низким (приблизительно 0,1% введенной дозы), что свидетельствует о том, что почечный клиренс играет незначительную роль в общем клиренсе аклидиния из плазмы крови.
Основная часть введенной дозы формотерола подвергалась метаболизму в печени с последующим выведением почками. После ингаляции 6% — 9% доставленной дозы формотерола выводится с мочой в неизмененном виде или в виде конъюгатов формотерола.
Особые популяции пациентов
Пожилые пациенты
Исследования фармакокинетики комбинации аклидиния/формотерола у пациентов пожилого возраста не проводились. Поскольку пожилым пациентам не требуется коррекции дозы препаратов аклидиния или формотерола, при применении комбинации аклидиния/формотерола корректировать дозу также не требуется.
Пациенты с нарушением функции почек и печени
Данные об особенностях применения комбинации аклидиния/формотерола у пациентов с нарушением функции почек или печени отсутствуют. Поскольку у пациентов с нарушением функции почек или печени не требуется коррекции дозы препаратов аклидиния или формотерола, при применении комбинации аклидиния/формотерола корректировать дозу также не требуется.
ПОКАЗАНИЯ К ПРИМЕНЕНИЮ
Препарат Дуаклир Дженуэйр показан в качестве поддерживающей бронходилатирующей терапии с целью облегчения симптомов хронической обструктивной болезни легких у взрослых.
ПРОТИВОПОКАЗАНИЯ
- Повышенная чувствительность к аклидиния бромиду, формотеролу или лактозе.
- Детский возраст до 18 лет (эффективность и безопасность не установлены).
- Непереносимость галактозы, дефицит лактазы или глюкозо-галактозная мальабсорбция.
С ОСТОРОЖНОСТЬЮ
Инфаркт миокарда, перенесенный в течение предшествующих 6 месяцев,
нестабильная стенокардия, впервые выявленная аритмия в течение предшествующих 3 месяцев, госпитализация в течение предшествующих 12 месяцев по поводу сердечной недостаточности III и IV функциональных классов по классификации NYHA или другие тяжелые сердечно-сосудистые заболевания, интервал QTc (по методу Базетта) > 470 мс, сопутствующая терапия лекарственными препаратами, удлиняющими интервал QTc, судорожные расстройства, тиреотоксикоз, феохромоцитома, симптоматическая гиперплазия предстательной железы, задержка мочи, закрытоугольная глаукома, гипокалиемия.
ПРИМЕНЕНИЕ В ПЕРИОД БЕРЕМЕННОСТИ И ГРУДНОГО ВСКАРМЛИВАНИЯ
Беременность
Данные о применении препарата Дуаклир Дженуэйр у беременных женщин отсутствуют.
В исследованиях на животных отмечена фетотоксичность только в дозах, значительно превышающих максимальную дозу аклидиния у человека, и нежелательные эффекты в исследованиях репродуктивной токсичности только при очень высокой системной экспозиции формотерола.
Во время беременности препарат Дуаклир Дженуэйр следует применять только в тех случаях, когда ожидаемая польза превосходит потенциальные риски.
Период грудного вскармливания
Неизвестно, выделяется ли аклидиний (и/или его метаболиты) или формотерол с грудным молоком. Поскольку доклинические исследования показали, что небольшие количества аклидиния (и/или его метаболиты) и формотерола проникают в молоко, в период грудного вскармливания препарат Дуаклир Дженуэйр следует применять только в случаях, когда ожидаемая польза для женщины превосходит потенциальный риск для младенца.
Фертильность
Доклинические исследования выявили небольшое снижение фертильности только при применении в дозах, значительно превышающих максимальные дозы аклидиния и формотерола у человека. Считается маловероятным, что применение препарата Дуаклир Дженуэйр в рекомендуемой дозе будет влиять на фертильность у человека.
СПОСОБ ПРИМЕНЕНИЯ И ДОЗЫ
Для ингаляционного применения.
Рекомендуемая доза – одна ингаляция препарата Дуаклир Дженуэйр 340 мкг + 11,8 мкг/доза 2 раза в сутки.
В случае пропуска приема дозы пропущенную дозу необходимо принять как можно скорее, а следующую дозу принять в обычное время. Не следует принимать двойную дозу с целью компенсации пропущенной.
Пожилые пациенты
Коррекции дозы препарата у пожилых пациентов не требуется (см. раздел «Фармакокинетика»).
Нарушение функции почек
Коррекции дозы препарата у пациентов с нарушением функции почек не требуется (см. раздел «Фармакокинетика»).
Нарушение функции печени
Коррекции дозы препарата у пациентов с нарушением функции печени не требуется (см. раздел «Фармакокинетика»).
Дети
Препарат Дуаклир Дженуэйр не предназначен для применения у детей и подростков младше 18 лет при ХОБЛ.
Способ применения
Пациенты должны быть обучены принципам правильного применения препарата.
Инструкция для правильного применения препарата Дуаклир Дженуэйр
Перед первым применением вскройте запечатанный пакет по линии стрелок, извлеките ингалятор Дженуэйр и ознакомьтесь с его составными частями. Пакет и пакетик-саше с десикантом подлежат утилизации.
Защитный колпачок -Индикатор доз — Оранжевая кнопка — Окно цветового контроля — Мундштук

Перед применением ингалятора Дженуэйр внимательно прочитайте инструкцию.
Как использовать Дуаклир Дженуэйр Общие сведения
Для использования ингалятора Дженуэйр после снятия колпачка Вам необходимо сделать 2 шага:
Шаг 1: Нажать и ОТПУСТИТЬ оранжевую кнопку и полностью выдохнуть, но не в ингалятор.
Шаг 2: Плотно обхватить губами мундштук и СИЛЬНО и ГЛУБОКО вдохнуть через ингалятор.
После ингаляции не забудьте надеть защитный колпачок.
Начало применения
•Когда Вы собираетесь принять дозу лекарственного препарата, снимите защитный колпачок, слегка сжав стрелки на каждой стороне и потянув колпачок наружу (см. рисунок 1).

РИСУНОК 1
• Убедитесь в том, что мундштук ничто не блокирует.
• Держите ингалятор Дженуэйр горизонтально мундштуком по направлению к Вам, с оранжевой кнопкой, обращенной прямо вверх (см. рисунок 2).
Держите ингалятор оранжевой кнопкой, обращенной прямо вверх. НЕ НАКЛОНЯЙТЕ ЕГО.
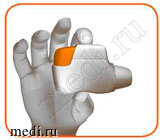
РИСУНОК 2
ШАГ 1: НАЖМИТЕ оранжевую кнопку на всю глубину и затем ОТПУСТИТЕ ее (см. рисунки 3 и 4).
НЕ УДЕРЖИВАЙТЕ ОРАНЖЕВУЮ КНОПКУ НАЖАТОЙ.
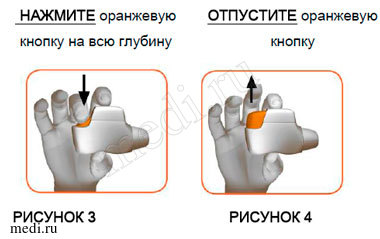
Остановитесь и проверьте: убедитесь, что доза готова для ингаляции
• Убедитесь, что окно цветового контроля стало зеленым (см. рисунок 5).
• Зеленый цвет окна контроля подтверждает, что лекарственный препарат готов для ингаляции.
Готов к применению
ЗЕЛЕНЫЙ

ЕСЛИ ОКНО ЦВЕТОВОГО КОНТРОЛЯ ОСТАЕТСЯ КРАСНЫМ, НАЖМИТЕ И ОТПУСТИТЕ ОРАНЖЕВУЮ КНОПКУ ЕЩЕ РАЗ (СМ. ШАГ 1).
•Перед тем, как поднести ингалятор ко рту, полностью выдохните. Не выдыхайте в ингалятор.
ШАГ 2:
•Плотно обхватите губами мундштук ингалятора Дженуэйр и СИЛЬНОи ГЛУБОКО вдохните через мундштук (см. рисунок 6).
— Такой сильный, глубокий вдох доставляет лекарственный препарат через ингалятор в легкие.
ВНИМАНИЕ! НЕ УДЕРЖИВАЙТЕ ОРАНЖЕВУЮ КНОПКУ НАЖАТОЙ ВО ВРЕМЯ ИНГАЛЯЦИИ.
ПРАВИЛЬНО / НЕПРАВИЛЬНО

РИСУНОК 6
•Во время вдоха Вы услышите «ЩЕЛЧОК», указывающий на правильное применение ингалятора Дженуэйр.
•Для того, чтобы принять всю дозу, продолжайте вдыхать даже после того, как
услышали «ЩЕЛЧОК» ингалятора.
•Выньте ингалятор Дженуэйр изо рта и задержите дыхание так долго, чтобы было комфортно, затем медленно выдохните через нос.
Примечание. Некоторые пациенты, в зависимости от индивидуальных особенностей, могут ощущать легкий сладковатый или горьковатый вкус при ингаляции препарата. Не принимайте дополнительную дозу, если Вы не почувствовали никакого вкуса после ингаляции.
Остановитесь и проверьте: убедитесь, что Вы правильно провели ингаляцию
•Убедитесь, что окно контроля стало красным (см. рисунок 7). Это подтверждает
то, что Вы правильно провели ингаляцию полной дозы.
Ингаляция проведена правильно
КРАСНЫЙ

РИСУНОК 7
ЕСЛИ ОКНО ЦВЕТОВОГО КОНТРОЛЯ ОСТАЕТСЯ ЗЕЛЕНЫМ, НЕОБХОДИМО ВНОВЬ СИЛЬНО И ГЛУБОКО ВДОХНУТЬ ЧЕРЕЗ МУНДШТУК (СМ. ШАГ 2).
•Если окно контроля все еще не изменяет цвет на красный, то возможно, Вы
забыли отпустить оранжевую кнопку перед ингаляцией или могли неправильно вдохнуть. Если это так, попробуйте вновь.
Убедитесь, что Вы ОТПУСТИЛИ оранжевую кнопку, исделайте СИЛЬНЫЙ глубокий вдох через мундштук.
Примечание. Если после нескольких попыток Вам так и не удалось правильно провести ингаляцию, обратитесь к лечащему врачу.
•Как только окно контроля стало красным, наденьте защитный колпачок на мундштук (см. рисунок 8).
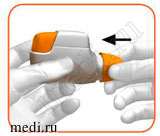
РИСУНОК 8
Когда Вам необходим новый ингалятор Дженуэйр?
• Ингалятор Дженуэйр оборудован индикатором доз, показывающим, сколько примерно доз осталось в ингаляторе. Индикатор доз медленно опускается, отражая интервалы по 10 (60, 50, 40, 30, 20, 10, 0) (см. рисунок A). Каждый ингалятор Дженуэйр содержит по меньшей мере 60 доз препарата.
Когда на индикаторе доз появится лента с красными полосками (см. рисунок А), это означает, что препарат заканчивается и необходимо приобрести новый ингалятор Дженуэйр.
Индикатор доз снижается с интервалами по 10: 60, 50, 40, 30, 20, 10, 0.
Индикатор доз
Лента с красными полосками

РИСУНОК А
Примечание. Если Ваш ингалятор Дженуэйр окажется поврежден или потерян колпачок, необходимо заменить ингалятор. Ингалятор Дженуэйр чистить НЕ НУЖНО. Однако, в случае необходимости, это надо делать с помощью сухой ткани или бумажной салфетки снаружи мундштука.
НИКОГДА не используйте воду для чистки ингалятора Дженуэйр, поскольку это может повредить лекарственный препарат.
Как узнать, что Ваш ингалятор Дженуэйр пуст?
• Когда в середине индикатора доз появится цифра 0 (ноль), необходимо продолжить применение всех остающихся в ингаляторе Дженуэйр доз.
• Когда для ингаляции будет подготовлена последняя доза, оранжевая кнопка не вернется полностью в свое верхнее положение, а останется заблокирована в среднем положении (см. рисунок B).
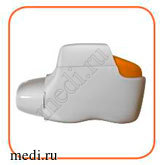
Заблокирована
Даже когда оранжевая кнопка заблокирована, Вы, тем не менее, сможете принять последнюю дозу. После этого ингалятор Дженуэйр не может быть использован вновь, и Вам необходимо будет начать использовать новый ингалятор Дженуэйр.
ПОБОЧНОЕ ДЕЙСТВИЕ
Представленные ниже сведения по безопасности основаны на опыте применения препарата Дуаклир Дженуэйр (в рекомендуемой терапевтической дозе до 12 месяцев) и его отдельных компонентов.
Обзор профиля безопасности
Нежелательные реакции, связанные с применением препарата Дуаклир Дженуэйр, схожи с наблюдавшимися при применении его отдельных компонентов. Поскольку препарат Дуаклир Дженуэйр содержит аклидиний и формотерол, то на фоне его применения можно ожидать нежелательные реакции, описанные для этих компонентов.
Наиболее часто отмечавшимися нежелательными реакциями при применении препарата Дуаклир Дженуэйр являлись назофарингит (7,9%) и головная боль (6,8%).
Список нежелательных реакций в виде таблицы
Частота нежелательных реакций основана на оценке общих коэффициентов возникновения реакций, наблюдаемых при применении препарата Дуаклир
Дженуэйр 340 мкг + 11,8 мкг/доза в рамках объединенного анализа рандомизированных, плацебо-контролируемых клинических исследований III фазы длительностью не менее 6 месяцев.
Частота нежелательных реакций представлена с использованием следующих обозначений: очень часто (≥ 1/10); часто (≥ 1/100 до < 1/10); нечасто (≥ 1/1000 до < 1/100); редко (≥ 1/10000 до < 1/1000); очень редко (< 1/10000) и неуточненной частоты (невозможно оценить по доступным данным).
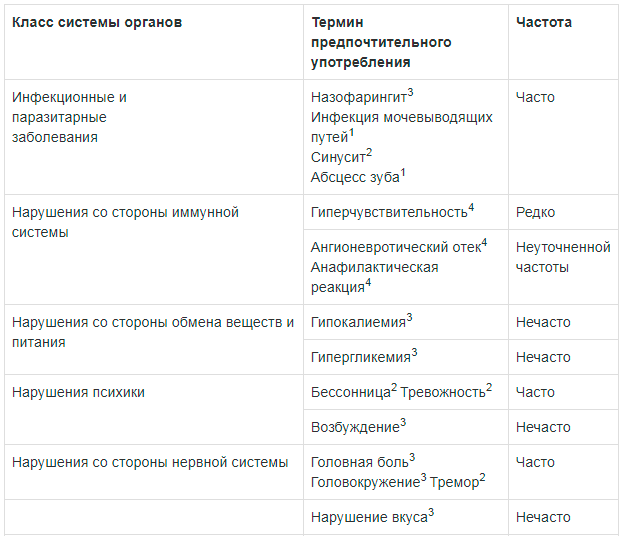

1 Нежелательные реакции, наблюдавшиеся при применении препарата Дуаклир
Дженуэйр, но не указанные в инструкциях на его отдель
ные компоненты.
2 Нежелательные реакции, наблюдавшиеся при применении препарата Дуаклир
Дженуэйр, и указанные в инструкции хотя бы одного из его отдельных компонентов.
3 Нежелательные реакции, указанные в инструкции хотя бы одного из отдельных
компонентов, но при применении препарата Дуаклир Дженуэйр 340 мкг + 11,8
мкг/доза наблюдавшиеся с более низкой или сопоставимой частотой, чем при
применении плацебо.
4 Нежелательные реакции, указанные в инструкции хотя бы одного из отдельных
компонентов, но не наблюдавшиеся при применении препарата Дуаклир Дженуэйр
340 мкг + 11,8 мкг/доза; категория частоты развития указана в соответствии с
разделом «Побочное действие» инструкции на отдельные компоненты.
ПЕРЕДОЗИРОВКА
Опыт лечения передозировки препарата Дуаклир Дженуэйр ограничен. Высокие дозы препарата Дуаклир Дженуэйр могут приводить к усилению симптомов и проявлений антихолинергического и/или β2-адренергического действия; наиболее частыми из которых являются: нечеткость зрения, сухость во рту, тошнота, мышечный спазм, тремор, головная боль, ощущение сердцебиения и артериальная гипертензия.
В случае передозировки следует прекратить применение препарата Дуаклир Дженуэйр. Показана поддерживающая и симптоматическая терапия.
ВЗАИМОДЕЙСТВИЕ С ДРУГИМИ ЛЕКАРСТВЕННЫМИ СРЕДСТВАМИ И ДРУГИЕ ВИДЫ ЛЕКАРСТВЕННОГО ВЗАИМОДЕЙСТВИЯ
Лекарственные средства для лечения ХОБЛ
Совместное применение препарата Дуаклир Дженуэйр с другими антихолинергическими средствами и/или агонистами β2-адренергических рецепторов длительного действия не изучалось и не рекомендуется.
Хотя формальных исследований лекарственных взаимодействий препарата Дуаклир Дженуэйр in vivo не проводилось, он применялся одновременно с другими лекарственными средствами для терапии ХОБЛ, включая агонисты β2-адренергических рецепторов короткого действия, метилксантины, а также пероральные и ингаляционные глюкокортикостероиды, без клинических признаков лекарственного взаимодействия.
Метаболические взаимодействия
В исследованиях in vitro было установлено, что не ожидается взаимодействия аклидиния в терапевтической дозе или его метаболитов с субстратами P-гликопротеина (P-gp) и лекарственными средствами, метаболизируемыми изоферментами цитохрома P450 (CYP450), и эстеразами. В терапевтически значимых концентрациях формотерол не ингибирует изоферменты CYP450 (см. раздел «Фармакокинетика»).
Препараты, вызывающие гипокалиемию
Сопутствующее применение производных метилксантина, стероидов или калийнесберегающих диуретиков, может усиливать возможный гипокалиемический эффект агонистов β2-адренорецепторов, поэтому следует соблюдать осторожность при совместном применении с этими препаратами (см. раздел «Особые указания»).
Блокаторы β-адренергических рецепторов
Блокаторы β-адренергических рецепторов могут ослаблять или нивелировать эффект агонистов β2-адренергических рецепторов. При необходимости применения блокаторов β-адренергических рецепторов (в том числе в виде глазных капель) предпочтительнее назначение кардиоселективных блокаторов β-адренергических рецепторов, хотя и они должны применяться с осторожностью.
Другие фармакодинамические взаимодействия
Следует с осторожностью применять препарат Дуаклир Дженуэйр у пациентов, получающих лекарственные препараты, удлиняющие интервал QTc, такие как ингибиторы моноаминоксидазы, трициклические антидепрессанты, антигистаминные средства или макролиды, поскольку они могут потенцировать влияние формотерола на сердечно-сосудистую систему. Лекарственные препараты, удлиняющие интервал QTc, повышают риск развития желудочковой аритмии.
ОСОБЫЕ УКАЗАНИЯ
Бронхиальная астма
Препарат Дуаклир Дженуэйр не должен применяться при бронхиальной астме; клинические исследования препарата Дуаклир Дженуэйр при бронхиальной астме не проводились.
Парадоксальный бронхоспазм
В клинических исследованиях не отмечены случаи парадоксального бронхоспазма на фоне применения препарата Дуаклир Дженуэйр в рекомендуемой дозе. Однако парадоксальный бронхоспазм наблюдали при проведении другой ингаляционной терапии. В случае его возникновения следует прекратить применение лекарственного препарата и рассмотреть возможность альтернативной терапии.
Препарат не предназначен для купирования острых приступов
Препарат Дуаклир Дженуэйр не показан для лечения острых приступов бронхоспазма.
Влияние на сердечно-сосудистую систему
Препарат Дуаклир Дженуэйр следует применять с осторожностью у пациентов, перенесших инфаркт миокарда в течение предшествующих 6 месяцев, у пациентов с нестабильной стенокардией, впервые выявленной аритмией в течение предшествующих 3 месяцев, с интервалом QTc (рассчитанного по методу Базетта) > 470 мс или госпитализировавшихся в течение предшествующих 12 месяцев по поводу сердечной недостаточности III и IV функциональных классов по классификации NYHA, поскольку эти пациенты не включались в клинические исследования.
У отдельных пациентов агонисты β2-адренорецепторов могут вызывать повышение частоты пульса и артериального давления, изменения на ЭКГ в виде уплощения зубца Т, депрессии сегмента ST и удлинения интервала QTc. В случае развития данных эффектов может потребоваться досрочное прекращение терапии. Агонисты β2-адренорецепторов длительного действия следует применять с осторожностью у пациентов с удлинением интервала QTc в настоящее время или в анамнезе, либо получающих лекарственные препараты, влияющие на длительность интервала QTc (см. раздел «Взаимодействие с другими лекарственными средствами и другие виды лекарственного взаимодействия»).
Системные эффекты
Препарат Дуаклир Дженуэйр следует применять с осторожностью у пациентов с тяжелыми нарушениями со стороны сердечно-сосудистой системы, судорожными расстройствами, тиреотоксикозом и феохромоцитомой.
При применении высоких доз агонистов β2-адренорецепторов возможно развитие метаболических эффектов в виде гипергликемии и гипокалиемии. В клинических исследованиях III фазы частота значимого повышения концентрации глюкозы в крови на фоне применения препарата Дуаклир Дженуэйр была низкой (0,1%) и схожей с группой плацебо. Гипокалиемия обычно транзиторная и не требует дополнительной терапии. У пациентов с тяжелой ХОБЛ гипокалиемия может потенцироваться гипоксией и сопутствующей терапией (см. раздел
«Взаимодействие с другими лекарственными средствами и другие виды лекарственного взаимодействия»). Гипокалиемия может увеличить риск развития аритмии.
Вследствие антихолинергической активности препарат Дуаклир Дженуэйр следует применять с осторожностью при симптоматической гиперплазии предстательной железы, задержке мочи или закрытоугольной глаукоме (несмотря на то, что непосредственный контакт препарата с глазами очень маловероятен). Сухость во рту, отмечавшаяся на фоне антихолинергической терапии, при сохранении в течение длительного времени может привести к кариесу зубов.
ВЛИЯНИЕ НА СПОСОБНОСТЬ УПРАВЛЯТЬ ТРАНСПОРТНЫМИ СРЕДСТВАМИ И ДРУГИМИ МЕХАНИЗМАМИ
Препарат Дуаклир Дженуэйр не влияет или в незначительной степени влияет на способность управлять транспортом и механизмами. Развитие нечеткости зрения или головокружения может оказать влияние на способность к управлению транспортными средствами или работе с механизмами.
ФОРМА ВЫПУСКА
Порошок для ингаляций дозированный, 340 мкг + 11,8 мкг/доза. По 60 доз порошка для ингаляций в ингалятор.
По 1 ингалятору в пакет из ламинированной алюминиевой фольги, содержащий пакетик-саше с десикантом. По 1 пакету с инструкцией по применению в картонную пачку с контролем первого вскрытия.
УСЛОВИЯ ХРАНЕНИЯ
При температуре не выше 30 °С. Хранить в недоступном для детей месте.
СРОК ГОДНОСТИ
2 года.
После первого вскрытия пакета – 60 дней.
Не применять по истечении срока годности, указанного на упаковке.
УСЛОВИЯ ОТПУСКА ИЗ АПТЕК
По рецепту.
НАИМЕНОВАНИЕ И АДРЕС ЮРИДИЧЕСКОГО ЛИЦА, НА ИМЯ КОТОРОГО ВЫДАНО РЕГИСТРАЦИОННОЕ УДОСТОВЕРЕНИЕ
АстраЗенека ЮК Лимитед, Великобритания
2 Кингдом Стрит, Лондон W2 6BD, Великобритания
AstraZeneca UK Limited, United Kingdom
2 Kingdom Street, London W2 6BD, United Kingdom
ПРОИЗВОДИТЕЛЬ,ФАСОВЩИК (ПЕРВИЧНАЯУПАКОВКА),УПАКОВЩИК (ВТОРИЧНАЯ (ПОТРЕБИТЕЛЬСКАЯ) УПАКОВКА), ВЫПУСКАЮЩИЙ КОНТРОЛЬ КАЧЕСТВА
Индустриас Фармасеутикас Альмиралль С.А., Испания
Ктра. Насьональ II, км 593
08740 Сант Андреу де ла Барка, Барселона, Испания
Industrias Farmaceuticas Almirall SA
Ctra. Nacional II, km 593
08740 Sant Andreu de la Barca, Barcelona, Spain
Дополнительная информация предоставляется по требованию:
Представительство АстраЗенека ЮК Лимитед, Великобритания, в г. Москве и ООО АстраЗенека Фармасьютикалз 125284 Москва, ул. Беговая д. 3, стр. 1
Купить Дуаклир Дженуэйр в planetazdorovo.ru
*Цена в Москве. Точная цена в Вашем городе будет указана на сайте аптеки.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Фармакологическое действие
Механизм действия
Препарат содержит два бронходилататора: аклидиния бромид, антагонист мускариновых рецепторов длительного действия, и формотерол, длительно действующий агонист β2-адренорецепторов. Комбинация этих веществ с разными механизмами действия обеспечивает аддитивный эффект по сравнению с применением отдельных компонентов. Вследствие различия плотности мускариновых и β2-адренорецепторов в центральных и периферических дыхательных путях антагонисты мускариновых рецепторов более эффективны в расслаблении центральных дыхательных путей, а агонисты β2-адренорецепторов — периферических дыхательных путей; таким образом, применение комбинированной терапии может усиливать благоприятное воздействие на функцию легких.
Аклидиния бромид является конкурентным, селективным антагонистом мускариновых рецепторов с более длительным временем связывания с М3-рецепторами, чем с М2-рецепторами. М3-рецепторы служат посредниками при сокращении гладкой мускулатуры дыхательных путей. Вдыхаемый аклидиния бромид действует местно в легких в качестве антагониста М3-рецепторов гладкой мускулатуры дыхательных путей и вызывает бронходилатацию. Применение аклидиния бромида у пациентов с ХОБЛ вызывает также снижение выраженности симптомов, улучшение связанного с заболеванием состояния здоровья, снижение частоты обострений и улучшение переносимости физической нагрузки. Поскольку аклидиния бромид быстро разрушается в плазме крови, количество системных антихолинергических побочных эффектов является низким.
Формотерол является мощным селективным агонистом β2-адренорецепторов. Бронходилатация достигается за счет расслабления гладкой мускулатуры дыхательных путей вследствие повышения уровня циклического аденозинмонофосфата после активации аденилатциклазы. Помимо улучшения функции легких формотерол уменьшает выраженность симптомов и повышает качество жизни у пациентов с ХОБЛ.
Фармакодинамика
Клинические исследования показали, что препарат обеспечивает клинически значимое улучшение функции легких (оцениваемое по объему форсированного выдоха за 1 секунду (OФВ1)) в течение более 12 ч после приема.
Препарат обладает быстрым началом действия — в течение 5 мин после первой ингаляции по сравнению с плацебо. Начало действия препарата было сравнимо с эффектом быстродействующего агониста β2-адренорецепторов, формотерола, в дозе 12 мкг. Максимальная бронходилатация (максимальный ОФВ1) по сравнению с исходным уровнем достигалась с первого дня (304 мл) и поддерживалась в течение всего периода терапии длительностью более 6 месяцев (326 мл).
Электрофизиология сердца
Не было выявлено клинически значимого влияния препарата на параметры ЭКГ, включая интервал QT, по сравнению с аклидинием, формотеролом и плацебо, а также на сердечный ритм при проведении суточного мониторирования по Холтеру.
Клиническая эффективность
Программа клинических исследований III фазы с участием приблизительно 4000 пациентов с клиническим диагнозом ХОБЛ средней или тяжелой степени включала два 6-месячных рандомизированных исследования с плацебо и активным контролем (ACLIFORM-COPD и AUGMENT), 6-месячную продленную фазу исследования AUGMENT, а также дополнительное 12-месячное рандомизированное, контролируемое исследование.
В долгосрочных исследованиях безопасности препарат показал стойкую эффективность при длительности применения более 1 года, без признаков тахифилаксии.
Влияние на функцию легких
Препарат в дозе 340 мкг+11.8 мкг/доза 2 раза/сут обеспечивал клинически значимое улучшение функции легких (оцениваемое по ОФВ1, форсированной жизненной емкости легких и емкости вдоха) по сравнению с плацебо. Клинически значимый бронходилатирующий эффект достигался в течение 5 мин после приема первой дозы препарата и поддерживался в течение всего междозового интервала.
В исследовании ACLIFORM-COPD препарат обеспечивал улучшение OOB1 через 1 ч после приема дозы по сравнению с плацебо и аклидинием, на 299 мл и 125 мл, соответственно (р<0.0001 в обоих сравнениях), и улучшение остаточного ОФВ1 по сравнению с плацебо и формотеролом, на 143 мл и 85 мл. соответственно (р<0.0001 в обоих сравнениях). В исследовании AUGMENT улучшение ОФВ1 через 1 ч после приема дозы по сравнению с плацебо и аклидинием, составило 284 мл и 108 мл, соответственно (р<0.0001 в обоих сравнениях), а улучшение остаточного ОФВ1 по сравнению с плацебо и формотеролом составило 130 мл (р<0.0001) и 45 мл (р=0.01), соответственно.
Облегчение симптомов и улучшение состояния здоровья, обусловленного заболеванием
Одышка и другие симптомы. Препарат обеспечивал клинически значимое улучшение в отношении одышки (оценивалось с помощью транзиторного индекса одышки (TDI)), с повышением индекса TDI через 6 месяцев терапии по сравнению с плацебо на 1.29 единиц в исследовании ACLIFORM-COPD (р<0.0001) и на 1.44 единицы — в исследовании AUGMENT (р<0.0001).
Объединенный анализ этих двух исследований показал, что применение препарата ассоциируется со статистически значимым большим улучшением индекса TDI по сравнению с аклидинием (на 0.4 единицы; р=0,016) или формотеролом (на 0,5 единиц: р=0.009).
Препарат улучшал дневную симптоматику ХОБЛ, в частности одышку, симптомы со стороны грудной клетки, кашель и отделение мокроты (оценивалась с помощью общего индекса E-RS), а также общую выраженность ночных симптомов, ранних утренних симптомов и симптомов, ограничивающих активность в ранние утренние часы, по сравнению с плацебо, аклидинием и формотеролом, однако данное улучшение не всегда было статистически значимым. Комбинация аклидиния/формотерола не показала статистически значимого снижения среднего количества ночных пробуждений, обусловленных ХОБЛ, по сравнению с плацебо или формотеролом.
Качество жизни, обусловленное состоянием здоровья. В исследовании AUGMENT препарат обеспечивал статистически значимое улучшение состояния здоровья, обусловленного заболеванием (оценивалось с помощью Респираторного опросника больницы Святого Георгия (SGRQ)), с улучшением общего индекса SGRQ на -4.35 единицы по сравнению с плацебо (р<0.0001). В исследовании ACLIFORM-COPD наблюдалось лишь небольшое снижение общего индекса SGRQ по сравнению с плацебо вследствие неожиданно выраженного ответа на терапию плацебо (р=0.598), и процент пациентов, достигших клинически значимого улучшения относительно исходного уровня, составил 55.3% в группе комбинированного препарата и 53.2% — в группе плацебо (р=0.669).
Объединенный анализ данных этих двух исследований показал большее улучшение общего индекса SGRQ при применении препарата по сравнению с формотеролом (-1.7 единиц; р=0.018) или аклидинием (-0.79 единиц; р=0.273).
Снижение частоты обострении ХОБЛ
В рамках объединенного анализа эффективности двух исследований длительностью 6 месяцев было продемонстрировано статистически значимое снижение на 29% частоты обострений средней или тяжелой степени (требующих терапии антибиотиками или кортикостероидами, или приводящих к госпитализации) на фоне терапии препаратом по сравнению с плацебо (частота на пациента в год: 0.29 против 0.42, соответственно; р=0.036), а также увеличение времени до первого обострения средней или тяжелой степени по сравнению с плацебо (соотношение рисков 0.70; р=0.027).
Применение препаратов экстренной терапии
Препарат снижал потребность в препарате экстренной терапии на протяжении более 6 месяцев по сравнению с плацебо (на 0.9 ингаляций/сут (p<0.0001)), аклидинием (на 0.4 ингаляции/сут (р<0.001)) и формотеролом (на 0.2 ингаляции/сут (р=0.062)).
Фармакокинетика
Параметры фармакокинетики аклидиния и формотерола при ингаляционном применении в комбинации существенно не отличались от наблюдаемых при применении отдельных компонентов.
После однократной ингаляции препарата аклидиний и формотерол быстро абсорбировались в плазму крови с достижением Cmax в течение 5 мин после ингаляции у здоровых добровольцев и в течение 24 мин после ингаляции у пациентов с ХОБЛ. Cmax аклидиния и формотерола в равновесном состоянии у пациентов с ХОБЛ, получавших препарат 2 раза/сут в течение 5 дней, достигались в течение 5 мин после ингаляции и составляли 128 пг/мл и 17 пг/мл соответственно.
Общее количество попадающего в легкие через ингалятор аклидиния составило приблизительно 30% отмеренной дозы. Связывание аклидиния с белками плазмы in vitro вероятнее всего соответствует связыванию метаболитов с белками, вследствие быстрого гидролиза аклидиния в плазме крови. Связывание с белками плазмы крови составило 87% для метаболита карбоновой кислоты и 15% для спиртового метаболита. Основным белком плазмы крови, который связывает аклидиний, является альбумин.
Связывание формотерола с белками плазмы крови составляет 61-64% (34% — преимущественно с альбумином). Не отмечено насыщения центров связывания в диапазоне концентраций, достигающихся при применении препарата в терапевтических дозах.
Аклидиний быстро и интенсивно гидролизуется до фармакологически неактивных спиртового производного и производного карбоновой кислоты. Происходит химический (неферментативный) и ферментативный гидролиз под действием эстераз. Основной эстеразой, вовлеченной в гидролиз у человека, является бутирилхолинэстераза. Концентрация кислотного метаболита в плазме крови после ингаляции приблизительно в 100 раз выше, чем концентрация спиртового метаболита и неизмененного активного вещества.
Низкая абсолютная биодоступность аклидиния при ингаляционном введении (<5%) обусловлена его интенсивным системным и пресистемным гидролизом как при нахождении в легких, так и при приеме внутрь. Биотрансформация с участием изоферментов цитохрома Р450 (CYP450) играет незначительную роль в общем метаболическом клиренсе аклидиния. Исследования in vitro показали, что аклидиний в терапевтической дозе или его метаболиты не ингибируют или не индуцируют какие-либо изоферменты CYP450 и не ингибируют эстеразы (карбоксилэстеразу, ацетилхолинэстеразу и бутирилхолинэстеразу). Также in vitro установлено, что аклидиний или его метаболиты не являются субстратами или ингибиторами Р-гликопротеина.
Формотерол выводится преимущественно посредством метаболизма. Основным путем является прямая глюкуронизация с O-деметилированием с последующей конъюгацией с глюкуронидом. В O-деметилировании формотерола участвуют изоферменты CYP2D6, CYP2C19, CYP2C9 и CYP2A6. В терапевтически значимых концентрациях формотерол не ингибирует изоферменты CYP450.
После ингаляции препарата в дозе 340 мкг+11.8 мкг/доза конечный Т1/2 аклидиния и формотерола составляет приблизительно 5 ч и 8 ч соответственно. После в/в введения 400 мкг меченого радиоактивным изотопом аклидиния здоровым добровольцам около 1% введенной дозы выводилось в неизмененном виде с мочой. До 65% дозы препарата выводилось в виде метаболитов с мочой и до 33% — в виде метаболитов с фекалиями. После ингаляции 200 мкг и 400 мкг аклидиния здоровыми добровольцами и пациентами с ХОБЛ выведение неизмененного аклидиния с мочой было очень низким (приблизительно 0.1% введенной дозы), что свидетельствует о том, что почечный клиренс играет незначительную роль в общем клиренсе аклидиния из плазмы крови. Основная часть введенной дозы формотерола подвергалась метаболизму в печени с последующим выведением почками. После ингаляции 6-9% доставленной дозы формотерола выводится с мочой в неизмененном виде или в виде конъюгатов формотерола.
Показания активных веществ препарата
Дуаклир Дженуэйр
В качестве поддерживающей бронходилатирующей терапии с целью облегчения симптомов ХОБЛ у взрослых.
Режим дозирования
Способ применения и режим дозирования конкретного препарата зависят от его формы выпуска и других факторов. Оптимальный режим дозирования определяет врач. Следует строго соблюдать соответствие используемой лекарственной формы конкретного препарата показаниям к применению и режиму дозирования.
Для ингаляционного применения.
Рекомендуемая доза — 1 ингаляция препарата (340 мкг+11.8 мкг/доза) 2 раза/сут.
В случае пропуска приема дозы пропущенную дозу необходимо принять как можно скорее, а следующую дозу принять в обычное время. Не следует принимать двойную дозу с целью компенсации пропущенной.
Коррекции дозы препарата у пациентов пожилого возраста не требуется.
Коррекции дозы препарата у пациентов с нарушением функции почек и печени не требуется.
Препарат не предназначен для применения у детей и подростков в возрасте до 18 лет при ХОБЛ.
Побочное действие
Представленные ниже сведения по безопасности основаны на опыте применения препарата (в рекомендуемой терапевтической дозе до 12 месяцев) и его отдельных компонентов.
Нежелательные реакции, связанные с применением препарата, схожи с наблюдавшимися при применении его отдельных компонентов. Поскольку препарат содержит аклидиния бромид и формотерол, на фоне его применения можно ожидать нежелательные реакции, описанные для этих компонентов.
Наиболее часто отмечавшимися нежелательными реакциями при применении препарата являлись назофарингит (7.9%) и головная боль (6.8%).
Частота нежелательных реакций основана на оценке общих коэффициентов возникновения реакций, наблюдаемых при применении препарата 340 мкг+11.8 мкг/доза в рамках объединенного анализа рандомизированных, плацебо-контролируемых клинических исследований III фазы длительностью не менее 6 месяцев.
Частота нежелательных реакций представлена с использованием следующих обозначений: очень часто (≥1/10); часто (≥1/100 до <1/10); нечасто (≥1/1000 до <1/100); редко (≥1/10 000 до <1/1000); очень редко (<1/10 000) и неуточненной частоты (невозможно оценить по доступным данным).
Инфекционные и паразитарные заболевания: часто — назофарингит3, инфекция мочевыводящих путей1, синусит2, абсцесс зуба1.
Со стороны иммунной системы: редко — гиперчувствительность4; неуточненной частоты — ангионевротический отек4, анафилактическая реакция4.
Со стороны обмена веществ и питания: нечасто — гипокалиемия3, гипергликемия3.
Нарушения психики: часто — бессонница2, тревожность2; нечасто — возбуждение3.
Со стороны нервной системы: часто — головная боль3, головокружение3, тремор2; нечасто — нарушение вкуса3.
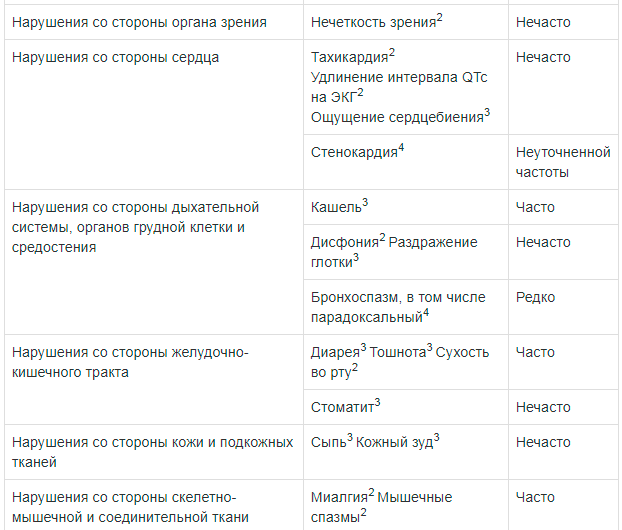
Со стороны органа зрения: нечасто — нечеткость зрения2.
Со стороны сердечно-сосудистой системы: нечасто — повышение АД3, тахикардия2, удлинение интервала QTc на ЭКГ2, ощущение сердцебиения3; неуточненной частоты — стенокардия4.
Со стороны дыхательной системы: часто — кашель3; нечасто — дисфония2, раздражение глотки3; редко — бронхоспазм, в т.ч. парадоксальный4.
Со стороны пищеварительной системы: часто — диарея3, тошнота3, сухость во рту2; нечасто — стоматит3.
Со стороны кожи и подкожно-жировой клетчатки: нечасто — сыпь3, зуд3.
Со стороны костно-мышечной системы: часто — миалгия2, мышечные спазмы2.
Со стороны мочевыделительной системы: нечасто — задержка мочи3.
Прочие: часто — периферический отек3.
Лабораторные и инструментальные данные: часто — повышение активности КФК1.
1 Нежелательные реакции, наблюдавшиеся при применении препарата, но не указанные в инструкциях на его отдельные компоненты.
2 Нежелательные реакции, наблюдавшиеся при применении препарата, указанные в инструкции хотя бы одного из его отдельных компонентов.
3 Нежелательные реакции, указанные в инструкции хотя бы одного из отдельных компонентов, но при применении комбинированного препарата 340 мкг+11.8 мкг/доза наблюдавшиеся с более низкой или сопоставимой частотой, чем при применении плацебо.
4 Нежелательные реакции, указанные в инструкции хотя бы одного из отдельных компонентов, но не наблюдавшиеся при применении комбинированного препарата 340 мкг+11.8 мкг/доза; категория частоты развития указана в соответствии с разделом «Побочное действие» инструкции на отдельные компоненты.
Противопоказания к применению
Возраст до 18 лет (эффективность и безопасность не установлены); непереносимость галактозы, дефицит лактазы или глюкозо-галактозная мальабсорбция; повышенная чувствительность к аклидиния бромиду, формотеролу или лактозе.
С осторожностью: инфаркт миокарда, перенесенный в течение предшествующих 6 месяцев; нестабильная стенокардия, впервые выявленная аритмия в течение предшествующих 3 месяцев; госпитализация в течение предшествующих 12 месяцев по поводу сердечной недостаточности III и IV ФК по классификации NYHA или другие тяжелые сердечно-сосудистые заболевания; интервал QTc (по методу Базетта) >470 мс; сопутствующая терапия лекарственными препаратами, удлиняющими интервал QTc; судорожные расстройства; тиреотоксикоз; феохромоцитома; симптоматическая гиперплазия предстательной железы; задержка мочи; закрытоугольная глаукома; гипокалиемия.
Применение при беременности и кормлении грудью
Беременность
Данные о применении препарата у беременных женщин отсутствуют. В исследованиях на животных отмечена фетотоксичность только в дозах, значительно превышающих максимальную дозу аклидиния у человека, и нежелательные эффекты в исследованиях репродуктивной токсичности только при очень высокой системной экспозиции формотерола.
Во время беременности препарат следует применять только в тех случаях, когда ожидаемая польза превосходит потенциальные риск.
Период грудного вскармливания
Неизвестно, выделяется ли аклидиний (и/или его метаболиты) или формотерол с грудным молоком. Поскольку доклинические исследования показали, что небольшие количества аклидиния (и/или его метаболиты) и формотерола проникают в молоко, в период грудного вскармливания препарат следует применять только в случаях, когда ожидаемая польза для женщины превосходит потенциальный риск для младенца.
Фертильность
Доклинические исследования выявили небольшое снижение фертильности только при применении в дозах, значительно превышающих максимальные дозы аклидиния и формотерола у человека. Считается маловероятным, что применение препарата в рекомендуемой дозе будет влиять на фертильность у человека.
Применение при нарушениях функции печени
Коррекции дозы препарата у пациентов с нарушением функции печени не требуется.
Применение при нарушениях функции почек
Коррекции дозы препарата у пациентов с нарушением функции почек не требуется.
Применение у детей
Противопоказано применение препарата в возрасте до 18 лет (эффективность и безопасность не установлены).
Применение у пожилых пациентов
Коррекции дозы препарата у пациентов пожилого возраста не требуется.
Особые указания
Препарат не следует применять при бронхиальной астме; клинические исследования препарата при бронхиальной астме не проводились.
Препарат не показан для лечения острых приступов бронхоспазма.
Парадоксальный бронхоспазм
В клинических исследованиях не отмечены случаи парадоксального бронхоспазма на фоне применения препарата в рекомендуемой дозе. Однако парадоксальный бронхоспазм наблюдали при проведении другой ингаляционной терапии. В случае его возникновения следует прекратить применение лекарственного препарата и рассмотреть возможность альтернативной терапии.
Влияние на сердечно-сосудистую систему
У отдельных пациентов агонисты β2-адренорецепторов могут вызывать повышение частоты пульса и АД, изменения на ЭКГ в виде уплощения зубца Т, депрессии сегмента ST и удлинения интервала QTc. В случае развития данных эффектов может потребоваться досрочное прекращение терапии. Агонисты β2-адренорецепторов длительного действия следует применять с осторожностью у пациентов с удлинением интервала QTc в настоящее время или в анамнезе, либо получающих лекарственные препараты, влияющие на длительность интервала QTc.
Системные эффекты
При применении высоких доз агонистов β2-адренорецепторов возможно развитие метаболических эффектов в виде гипергликемии и гипокалиемии. В клинических исследованиях III фазы частота значимого повышения концентрации глюкозы в крови на фоне применения комбинированного препарата была низкой (0.1%) и схожей с группой плацебо. Гипокалиемия обычно транзиторная и не требует дополнительной терапии. У пациентов с тяжелой ХОБЛ гипокалиемия может потенцироваться гипоксией и сопутствующей терапией. Гипокалиемия может увеличить риск развития аритмии.
Вследствие антихолинергической активности препарат следует применять с осторожностью при симптоматической гиперплазии предстательной железы, задержке мочи или закрытоугольной глаукоме (несмотря на то, что непосредственный контакт препарата с глазами очень маловероятен). Сухость во рту, отмечавшаяся на фоне антихолинергической терапии, при сохранении в течение длительного времени может привести к кариесу зубов.
Влияние на способность к управлению транспортными средствами и механизмами
Препарат не влияет или в незначительной степени влияет на способность управлять транспортом и механизмами. Развитие нечеткости зрения или головокружения может оказать влияние на способность к управлению транспортными средствами или работе с механизмами.
Лекарственное взаимодействие
Совместное применение препарата с другими антихолинергическими средствами и/или агонистами β2-адренорецепторов длительного действия не рекомендуется.
Препарат применялся одновременно с другими лекарственными средствами для терапии ХОБЛ, включая агонисты β2-адренорецепторов короткого действия, метилксантины, а также пероральные и ингаляционные ГКС, без клинических признаков лекарственного взаимодействия.
В исследованиях in vitro было установлено, что не ожидается взаимодействия аклидиния бромида в терапевтической дозе или его метаболитов с субстратами Р-гликопротеина (P-gp) и лекарственными средствами, метаболизируемыми изоферментами цитохрома Р450 (CYP450), и эстеразами. В терапевтически значимых концентрациях формотерол не ингибирует изоферменты CYP450.
Сопутствующее применение производных метилксантина, стероидов или калийнесберегающих диуретиков может усиливать возможный гипокалиемический эффект агонистов β2-адренорецепторов, поэтому следует соблюдать осторожность при совместном применении с этими препаратами.
Блокаторы β2-адренорецепторов могут ослаблять или нивелировать эффект агонистов β2-адренорецепторов. При необходимости применения бета-адреноблокаторов (в т.ч. в виде глазных капель) предпочтительнее назначение кардиоселективных бета-адреноблокаторов, хотя и они должны применяться с осторожностью.
Следует с осторожностью применять препарат у пациентов, получающих лекарственные средства, удлиняющие интервал QTc, такие как ингибиторы МАО, трициклические антидепрессанты, антигистаминные средства или макролиды, поскольку они могут потенцировать влияние формотерола на сердечно-сосудистую систему. Лекарственные препараты, удлиняющие интервал QTc, повышают риск развития желудочковой аритмии.
Состав
В каждой таблетке активного компонента нафтидрофурила оксалата — 50, 100 или 200 мг, а также дополнительные ингредиенты: кремния диоксид, лактоза, МКЦ, крахмал пшеничный, карбоксиметилкрахмал натрия, тальк, коповидон, кросповидон, магния стеарат.
В пленочную оболочку таблетки включены: дибутил фталат, тальк, макрогол, метакриловая кислота, краситель солнечный закат желтый, метилакрилат сополимер.
Форма выпуска
Препарат выпускается в виде круглых двояковыпуклых таблеток, имеющих оранжевую пленочную оболочку в дозировке по 50, 100 или 200 мг.
Таблетки упакованы в блистеры по 10 шт.
Упаковка содержит 3, 6 или 9 блистеров.
Фармакологическое действие
Препарат является периферическим вазодилататором. Действующее вещество — нафтидрофурил, оказывает сосудорасширяющий эффект, за счет которого улучшается кровоснабжение периферических тканей и головного мозга. Устраняет ишемию в зонах сосудистой патологии при этом не влияя на интактные сосуды. Положительно влияет на гемодинамические показатели: увеличивает минутный объём сердца (объём крови, выталкиваемый каждым желудочком сердца за минуту) и снижает общее периферическое сопротивление, при этом не изменяя частоту сердечных сокращений и уровень артериального давления.
Фармакодинамика и фармакокинетика
Препарат блокирует активацию специфических рецепторов 5НТ2 и предотвращает их активацию тромбоцитарным серотонином, что приводит к снижению агрегации тромбоцитов и устранению локального спазма сосудов. Активное вещество действует целенаправленно на зоны ишемии в сетчатке глаза, головном мозге и периферических тканях, при этом не повышая риск системной гипотонии и не провоцируя синдром обкрадывания. Препарат повышает устойчивость тканей к кислородному голоданию, уменьшает агрегацию тромбоцитов, что приводит к улучшению текучести крови. В результате курсового лечения у пациентов с нарушением кровообращения в мозговых сосудах уменьшаются проявления депрессии и тревоги. Терапевтические дозы нафтидрофурила способствуют улучшению когнитивных функций, качества сна, уменьшают частоту приступов головокружения и головных болей.
| Всасывание | Практически полностью при пероральном приёме |
| Время наступления максимальной концентрации в плазме крови | 1 час |
| Связь с белками крови | 80% |
| Гематоэнцефалический барьер | Проникает |
| Время наступления максимальной концентрации в тканях головного мозга | 1 час |
| Метаболизм | Печень |
| Прохождение через плаценту и грудное молоко | Информация отсутствует |
| Период полувыведения | От 1 до 3,5 часов |
| Выведение | Кишечник, почки |
Особенности фармакокинетики у определенных категорий пациентов
Пожилой возраст: возрастные особенности не влияет на всасывание и распределение препарата в организме.
Пациенты с нарушением работы почек и печени: информация о скорости выведения препарата из организма отсутствует.
Показания к применению
Препарат показан при:
- заболеваниях, сопровождающиеся расстройством периферического кровоснабжения: синдром и болезнь Рейно (спазм сосудов кистей), синдром «перемежающейся» хромоты (боли в ногах при ходьбе), нарушении чувствительности тканей, болезненных ощущениях в ногах, акроцианозе конечностей, судорогах в икроножных мышцах;
- заболеваниях, связанных с расстройством кровообращения в сосудах в головного мозга: атеросклероз и церебральная сосудистая недостаточность;
- трофических изменениях в виде диабетической ретинопатии и длительно не заживающих трофических язв.
Противопоказания
Препарат имеет следующие ограничения к применению:
- хроническая сердечная недостаточность II – III степени;
- артериальная гипотензия;
- эпилепсия;
- индивидуальная непереносимость компонентов препарата;
- гипероксалурия и мочекаменная болезнь в анамнезе;
- инфаркт миокарда в острый период;
- детский возраст до 18 лет;
- геморрагический инсульт в острый период;
- нарушения сердечного ритма, сопровождающиеся учащенным сердцебиением;
- повышенная судорожная готовность.
У пациентов с аденомой простаты и закрытоугольной глаукомой препарат назначают с осторожностью.
Побочные действия
Пероральный приём таблеток Дузофарм в терапевтических дозировках переносится без серьёзных побочных эффектов.
В некоторых случаях могут наблюдаться:
- со стороны кожных покровов: появление сыпи;
- со стороны нервной системы: приступы головой боли и головокружения;
- со стороны психики: расстройство сна;
- со стороны печени и желчевыводящих путей: повышение в крови уровня печеночных ферментов;
- со стороны пищеварительной системы: боли в области эпигастрия, язвенные поражения слизистой оболочки желудка, диспепсические расстройства (рвота, тошнота), снижение аппетита, кишечные колики. Зарегистрированы случаи локального воспаления слизистой оболочки пищевода при приёме препарата без достаточного объёма жидкости;
- со стороны иммунной системы: повышенная чувствительность;
- со стороны почечно-выделительной системы: образование кальциево-оксалатных камней.
Дузофарм, инструкция по применению (Способ и дозировка)
Таблетки необходимо принимать внутрь не разжевывая и запивая достаточным объёмом (не менее стакана) питьевой воды.
Дозировка и длительность лечения подбирается врачом с учетом особенностей клинического случая.
Режим дозирования
При расстройствах периферического кровообращения: суточная дозировка 300 – 600 мг разделенная на три приёма, разовая дозировка 100 мг.
При расстройствах мозгового кровообращения: суточная дозировка 400 – 600 мг, разовая дозировка 100 мг.
Препарат показан для длительного лечения.
Режим дозирования у пациентов с нарушением работы печени и почек коррекции не требует.
Передозировка
При превышении рекомендуемой дозировки возможно развитие следующих симптомов:
- угнетение сердечной проводимости;
- нарушение сердечного ритма;
- усиление выраженности побочных действий;
- уменьшение частоты сердечных сокращений;
- беспокойство.
- судороги.
Лечебные мероприятия: промывание желудка, прием сорбентов и слабительных препаратов, медикаментозное лечение, контроль жизненно важных показателей организма, проведение диализа.
Взаимодействие
При совместном приёме нафтидрофурила с препаратами, понижающими артериальное давление, возможно усиление их действия. Поэтому в начале лечения необходим постоянный контроль за уровнем артериального давления.
Условия продажи
Отпускается в аптеках по рецепту врача.
Условия хранения
Таблетки необходимо хранить при температурном режиме не более 25°С.
Срок годности
Препарат хранится в течение 2 лет. Применять по окончанию срока годности запрещено.
Особые указания
При проведении терапии лекарством Дузофарм необходимо учитывать:
- В начале терапии необходим контроль уровня артериального давления ввиду возможного развития артериальной гипотензии у некоторых пациентов.
- Пациентам страдающим целиакией необходимо учитывать, что состав препарата включен пшеничный крахмал.
- Препарат не оказывает влияния на концентрацию внимания и способность управлять транспортом.
- Во время терапии препаратом возможно изменение состава мочи и формирование оксалатных камней в почках.
- Выявлены случаи повреждения печени. При появлении симптомов, указывающих на нарушения в работе печени терапию препаратом следует отменить.
- В период терапии необходимо соблюдать водно-питьевой режим.
- Таблетки содержат лактозы моногидрат, в связи с этим больным с галактоземией, глюкозно-галактозным синдромом мальабсорбции и лактазной недостаточностью следует соблюдать осторожность при его приёме.
- Принимать препарат необходимо запивая необходимым объёмом воды, так как в противном случае возможно развитие локального воспаления слизистой оболочки пищевода.
Аналоги Дузофарма
Совпадения по коду АТХ 4-го уровня:
Полных аналогов данного лекарственного препарата на фармацевтическом рынке не существует. Групповые аналоги со схожим механизмом действия представлены следующими препаратами: Билобил, Вазонит, Танакан, Гинкоум, Бетасерк, Трентал.
Данные лекарственные препараты так же выпускаются в таблетках , оказывают сосудорасширяющее действие и могут быть назначены взамен препарата Дузофарм после консультации специалиста.
Дешевые аналоги представлены препаратами Пентоксифиллин, Бетагистин, Дипиридамол. Однако следует отметить, что данные лекарственные средства могут иметь менее выраженную эффективность, а также большее количество побочных эффектов.
Цена аналогов препарата составляет в среднем от 100 до 2000 рублей.
Детям
Препарат противопоказан к назначению у детей ввиду отсутствия информации о его безопасности и эффективности применения в данной возрастной группе.
При беременности и лактации
Препарат может применяться у беременных и в период грудного вскармливания только в тех ситуациях, когда польза лечения матери превосходит потенциальный риск для плода виду отсутствия информации об исследованиях безопасности у беременных. Отрицательного влияния на развитие плода не оказывает.
Отзывы о Дузофарме
Отзывы врачей говорят эффективности и высоком профиле безопасности препарата при лечении патологий мозговых и периферических сосудов. По мнению специалистов Дузофарм уменьшает частоту и выраженность приступов у пациентов с синдромом Рейно, нормализует когнитивные функции при сосудистой деменции, оказывает положительный эффект у пациентов с диабетической полинейропатией. Согласно отзывам пациентов, принимавших таблетки Дузофарм курсом препарат уменьшает выраженность симптомов болезни: снижается частота приступов головных болей, спазмов, судорог, устраняется шум в ушах. Пациенты отмечают улучшение качества жизни, а также отсутствие серьезных побочных эффектов.
Цена Дузофарма, где купить
Купить Дузофарм в аптеках Москвы можно по средней цене от 400 рублей.
- Интернет-аптеки РоссииРоссия
ЗдравСити
-
Дузофарм таблетки п/о плен. 50мг 30штUnipharm AD
-
Дузофарм таблетки п/о плен. 50мг 60штUnipharm AD
-
Дузофарм таблетки п/о плен. 50мг 90штUnipharm AD
Аптека Диалог
-
Дузофарм (таб.п.пл/об.50мг №30)Unipharm
-
Дузофарм (таб.п.пл/об.50мг №90)Unipharm
-
Дузофарм (таб.п.пл/об.50мг №60)Unipharm
показать еще
3-й мкр, 12, Московский, Москва
Новая Жизнь ул, 1, Красноармейск, МО
Чкалова ул, 7, Красноармейск, МО
Сергиев Посад-6, 1А, Сергиево-Посадский р-н, МО (на въезде в Военный городок, на территории рынка)
Юшуньская малая. ул, 3, Москва
Братиславская ул, 18к1, Москва
Снайперская ул, 9А, Москва
Вучетича ул, 22, Москва
Загородное ш, 6к1, Москва
40 Лет Октября пр, 4 к 2, Москва
Б. Учительская ул, 4, Родники дп, Раменское, МО
Жилино-1 п, 2/1, го Люберцы, МО (магазин Дикси)
Тихонравова ул, 28Б с 2, Юбилейный мкр, Королев, МО
Лешково д, 107, Истра го, МО
Молодежная ул, 15А, Заря мкр, Балашиха, МО
Советская ул, 9, Балашиха, МО
Усачева ул, 29к1, Москва
Рижское ш, 41А, Волоколамск, МО
Ласточкин пр-д, 16, Балашиха, МО
Маршала Жукова пр, 49, Москва
