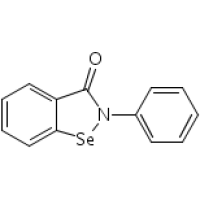
Эбселен
Ebselen
Фармакологическое действие
Эбселен — синтетический селенорганический препарат, обладает противовоспалительным, антиоксидантным, антиатеросклеротическим, нейропротективным и цитопротекторным действием. Повышает эффективность глутатиона, обладает сильным нейтрализующим действием против радикалов пероксинитрита.
Показания
Эбселен исследуется на предмет эффективности, переносимости и безопасности при лечении пациентов с инсультом, нарушением или потерей слуха, шумом в ушах, болезнью Меньера, биполярным расстройством, сердечно-сосудистыми заболеваниями, артритом, атеросклерозом, раком.
Эбселен показал эффективность при лечении Clostridium difficile, активен в отношении Aspergillus fumigatus.
Потенциальная активность против COVID-19
Предварительные исследования демонстрируют потенциальную ингибирующую активность эбселена против COVID-19 в клеточных анализах. Эффект был приписан необратимому ингибированию основной протеазы через образование ковалентной связи с тиоловой группой цистеина активного центра (Cys-145).
Протеаза Mpro — ключевой фермент COVID-19, участвующий в транскрипции РНК, позволяет реплицировать свой геном в заражённой клетке. Эбселен может снижать активность Mpro двумя способами: связывается с каталитическим сайтом фермента или с удалённым участком, который влияет на активность молекулы.
Подробнее о лечении COVID-19
Временные методические рекомендации профилактики, диагностики и лечения новой коронавирусной инфекции (COVID-19)*
В список возможных к назначению лекарственных средств для лечения COVID-19 у взрослых включены:
- Фавипиравир,
- Молнупиравир,
- Нирматрелвир + Ритонавир,
- Ремдесивир,
- Синтетическая малая интерферирующая рибонуклеиновая кислота (миРНК) [двуцепочечная],
- Иммуноглобулин человека против COVID-19,
- Интерферон-альфа (IFN-α),
- Интерферон альфа-2b (IFN-α2b)
- Умифеновир,
- Имидазолилэтанамид пентандиовой кислоты,
- Касиривимаб + имдевимаб,
- Бамланивимаб + этесевимаб,
- Сотровимаб,
- Регданвимаб.
В список препаратов упреждающей противовоспалительной терапии COVID-19 у взрослых включены:
- Барицитиниб,
- Тофацитиниб,
- Упадацитиниб,
- Олокизумаб,
- Левилимаб,
- Тоцилизумаб,
- Сарилумаб,
- Канакинумаб,
- Анакинра,
- Метилпреднизолон,
- Дексаметазон,
- Гидрокортизон,
- Будесонид.
В список возможных к назначению антикоагулянтов для лечения COVID-19 у взрослых включены:
1) антикоагулянты для парентерального введения:
- нефракционированный гепарин: нефракционированный гепарин.
- низкомолекулярные гепарины: далтепарин натрия, надропарин кальция, эноксапарин натрия, парнапарин натрия, бемипарин натрия.
- синтетические антикоагулянты: фондапаринукс натрия.
- ривароксабан, апиксабан, дабигатрана этексилат.
2) пероральные антикоагулянты:
По процедуре регистрации препаратов, предназначенных для применения в условиях угрозы возникновения, возникновения и ликвидации чрезвычайных ситуаций зарегистрирован ряд препаратов и вакцин, рекомендованных к применению для лечения, профилактики и терапии последствий новой коронавирусной инфекции (COVID-19).
Смотрите также код МКБ 10:
- U07.1 КОВИД-19 (COVID-19), вирус идентифицирован
* См. Версия 17 (14.12.2022) — Временные методические рекомендации профилактики, диагностики и лечения новой коронавирусной инфекции (COVID-19) — Минздрав России.
Информация о действующем веществе Эбселен предназначена для медицинских и фармацевтических специалистов, исключительно в справочных целях. Инструкция не предназначена для замены профессиональной медицинской консультации, диагностики или лечения. Содержащаяся здесь информация может меняться с течением времени. Наиболее точные сведения о применении препаратов, содержащих активное вещество Эбселен, содержатся в инструкции производителя, прилагаемой к упаковке.
126 306 руб.
Наличие: Срок поставки 60-90 дней
- Производитель: Acros Organics
- Каталожный номер: 300572500
- CAS номер : 60940-34-3
Краткое описание
Ebselen… Читать далее →
Характеристики реактива
Melting Point (°C)
178 — 181
Molecular Formula
C13 H9 N O Se
…
Вконтакте
Google+
- Описание
- Характеристики
| Product | 30057 Ebselen,99% |
General Product Data
|
| Product Specifications | |||||||||||
|
| Характеристики реактива | |
| Melting Point (°C) | 178 — 181 |
| Molecular Formula | C13 H9 N O Se |
| Molecular weight | 274.18 |
| StockUnit | |
| Фасовка | 250 мг |
Нормативные показатели
Информация о растворимости
Растворим в этаноле, метаноле, ацетоне, ацетонитриле.
Ключ ИнЧИ (InChI)
DYEFUKCXAQOFHX-UHFFFAOYSA-N
Молекулярная масса (г/моль)
274.19
Молекулярная формула
C13H9NOSe
Номер в леях
MFCD00210937
Температура плавления
180°C до 181°C
Технические характеристики
Отзывов: 0
Средняя оценка: 0
Доставка заказов осуществляется в любые регионы Российской Федерации и страны СНГ.
Цены на нашем сайте указаны с учетом НДС (20% либо 10%).
Оплата заказов производится только в безналичной форме на расчетный счет в рублях Российской Федерации на основании выставленного Счета.
Для бюджетных организаций и государственных структур предусмотрены особые условия оплаты.
Постоянным клиентам предоставляются скидки и индивидуальный порядок расчетов.
Внимание! В связи с нестабильным курсом валют и изменением цен у производителей, просим окончательную стоимость продукции уточнять у наших менеджеров.
Варианты доставки:
Самовывоз со склада в городе Клин
Адрес выдачи: Московская область, г. Клин, ул. Захватаева, д. 4, офис 101
Контактный телефон: +7 (977) 407-05-96
Доставка по Клину и Клинскому району – бесплатно
Доставка по Москве – 1 500 рублей
Доставка любыми транспортными компаниями, службами экспресс-доставки. Стоимость рассчитывается индивидуально для каждого заказа в соответствии с установленными тарифами транспортной компании. Все грузы застрахованы.
Эзиклен® (Eziclen) инструкция по применению
📜 Инструкция по применению Эзиклен®
💊 Состав препарата Эзиклен®
✅ Применение препарата Эзиклен®
📅 Условия хранения Эзиклен®
⏳ Срок годности Эзиклен®
Описание лекарственного препарата
Эзиклен®
(Eziclen)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для печатного издания справочника Видаль 2023 года.
Дата обновления: 2022.11.11
Код ATX:
A06AD10
(Минеральные соли в комбинации)
Активные вещества
-
безводный сульфат натрия
(sodium sulphate, anhydrous)
Ph.Eur.
Европейская Фармакопея -
магния сульфат
(magnesium sulphate)
Ph.Eur.
Европейская Фармакопея -
калия сульфат
(potassium sulphate)
Ph.Eur.
Европейская Фармакопея
Лекарственная форма
| Эзиклен® |
Концентрат д/пригот. р-ра д/приема внутрь 17.51 г+3.276 г+3.13 г/1 фл.: фл. 176 мл 2 шт. в компл. с мерн. стаканом рег. №: ЛП-004957 |
Форма выпуска, упаковка и состав
препарата Эзиклен®
Концентрат для приготовления раствора для приема внутрь в виде прозрачной или слегка опалесцирующей жидкости с фруктовым запахом.
Вспомогательные вещества: натрия бензоат — 0.098 г/1 фл. (0.196 г/2 фл.), лимонная кислота безводная — 0.315 г/1 фл. (0.63 г/2 фл.), яблочная кислота — 0.315 г/1 фл. (0.63 г/2 фл.), сукралоза — 0.3025 г/1 фл. (0.605 г/2 фл.), ароматизатор плодово-ягодный коктейль* — 0.7875 г/1 фл. (1.575 г/2 фл.), вода очищенная — 169.641 г/1 фл. (339.282 г/2 фл.).
* Ароматизатор плодово-ягодный коктейль состоит из смеси натуральных и синтетических ароматизаторов, пропиленгликоля (Е1520), этилового спирта, уксусной кислоты и бензойной кислоты (Е210).
176 мл — флаконы прозрачные из полиэтилентерефталата темно-коричневого цвета вместимостью 180 мл (2) в комплекте с полипропиленовым мерным стаканом — пачки картонные.
Фармакологическое действие
Механизм действия препарата в первую очередь обусловлен ограниченным по насыщаемости процессом активного транспорта сульфатов. При достижении порога насыщения всасывания сульфаты остаются в просвете кишечника.
Осмотический эффект неабсорбированных сульфатов и прием внутрь значительного объема воды вызывает задержку воды в кишечнике, что обеспечивает слабительное действие, вызывая обильную водянистую диарею, и приводит к очищению кишечника.
Фармакокинетика
Абсорбция сульфатов представляет собой ограниченный по насыщаемости процесс активного транспорта. Абсорбированные сульфаты выводятся преимущественно почками. В клинических исследованиях после приема препарата, сходного по содержанию сульфатов с препаратом Эзиклен®, у 6 здоровых добровольцев (в режиме дробного применения, т.е. прием 2 доз с перерывом в 12 ч) Сmax сульфатов в сыворотке наблюдалась приблизительно через 16 ч после приема 1-й дозы и через 5 ч после приема 2-й дозы и составила 499.5 мкмоль/л, по сравнению с исходным значением 141-467 мкмоль/л, в среднем — 335 мкмоль/л. Затем сывороточная концентрация сульфатов снижалась с Т1/2 8.5 ч.
Основным путем выведения сульфатов является выведение кишечником (около 70% от принятого количества).
Системная экспозиция сульфатов: AUC и Сmax после приема препарата Эзиклен® были изучены в ходе сравнительного исследования у здоровых добровольцев, у 6 пациентов с нарушением функции почек средней степени тяжести (КК от 30 до 49 мл/мин) и у 6 пациентов с нарушением функции печени легкой или средней степени тяжести (по шкале Чайлд-Пью: А (N=5) и В (N=1), соответственно). Нарушение функции почек приводило к снижению количества сульфатов, выводимых почками. Средние значения AUC и Сmax сульфатов были приблизительно на 50% выше у пациентов с нарушением функции почек по сравнению со здоровыми добровольцами. Системное воздействие препарата на концентрацию сульфатов не зависело от нарушения функции печени. Во всех 3 исследуемых группах концентрация сульфатов в сыворотке вернулась к исходному значению на 6-й день после приема препарата Эзиклен®. В данном исследовании прием препарата Эзиклен® не привел к клинически значимому повышению концентрации сульфатов в крови у пациентов с нарушением функции печени или почек.
Показания препарата
Эзиклен®
Очищение толстой кишки у взрослых пациентов при подготовке к:
- эндоскопическому и радиологическому исследованию толстой кишки;
- хирургическим вмешательствам, требующим отсутствия содержимого в толстой кишке.
Режим дозирования
Принимают внутрь.
Препарат можно применять только у взрослых пациентов.
Для надлежащего очищения кишечника требуется прием 2 флаконов препарата Эзиклен®.
Перед приемом содержимое каждого флакона необходимо развести водой. Пациент должен выпить полученный разведенный раствор и еще две чашки, наполненные до метки водой или разрешенной прозрачной жидкостью (т.е. приблизительно 1 л), в течение следующих 2 часов, как описано ниже в разделах «Режим применения» и «Схема разведения и применения».
Разрешенными прозрачными жидкостями являются: вода, чай или кофе (без молока или немолочных сливок), газированные (обогащенные углекислым газом) или негазированные легкие напитки, осветленные фруктовые соки (без мякоти, не красные и не фиолетовые), бульоны или процеженные от твердых ингредиентов супы.
В общей сложности для очистки кишечника перед проведением процедуры необходимо выпить не менее 3 л жидкости.
Раствор после разведения должен быть использован незамедлительно.
Режим применения
Препарат принимают либо в режиме дробного применения (1-й флакон принимается вечером накануне процедуры, а 2-й — на следующее утро), либо в режиме единовременного применения (прием накануне процедуры).
Подходящий режим приема препарата Эзиклен® может быть определен врачом.
Если позволяет время назначенной процедуры, то режим дробного применения предпочтительнее, чем режим единовременного приема накануне процедуры. Режим единовременного применения накануне процедуры потенциально подходит в качестве альтернативного режима.
Режим дробного применения
День перед процедурой
Необходимо следовать следующим инструкциям:
- содержимое одного флакона препарата Эзиклен® следует вылить в прилагаемый мерный стакан и развести водой до метки (т.е. до объема 0.5 л);
- в течение последующих 2 часов пациент должен выпить полученный раствор и дополнительно 2 мерных стакана воды или прозрачной жидкости (т.е. около 1 л).
День процедуры
В день процедуры (через 10-12 ч после приема первого флакона препарата) необходимо повторить действия, согласно инструкциям для предыдущего дня:
- содержимое 2-го флакона препарата Эзиклен® следует вылить в прилагаемый мерный стакан и развести водой до метки (т.е. до объема 0.5 л);
- в течение последующих 2 часов пациент должен выпить полученный раствор и дополнительно 2 мерных стакана воды или прозрачной жидкости (т.е. около 1 л).
Прием полного объема разведенного раствора препарата Эзиклен® и дополнительного количества воды или прозрачной жидкости должен быть закончен как минимум за 2 часа и не позднее 4 часов до начала процедуры.
Точный режим и время приема препарата Эзиклен® определяется врачом.
Режим единовременного применения
(режим применения для использования в зависимости от индивидуальных потребностей пациента, а также в зависимости от времени проведения процедуры).
Одноэтапная вечерняя схема
Время исследования — до 14.00.
Вечер перед процедурой:
- содержимое одного флакона препарата Эзиклен® следует вылить в прилагаемый мерный стакан и развести водой до метки (т.е. до объема 0.5 л);
- в течение последующих 2 часов пациент должен выпить полученный раствор и дополнительно 2 мерных стакана воды или прозрачной жидкости (т.е. около 1 л).
Приблизительно через 2 ч после начала приема 1-й дозы:
- содержимое 2-го флакона препарата Эзиклен® следует вылить в прилагаемый мерный стакан и развести водой до метки (т.е. до объема 0.5 л);
- в течение последующих 2 часов пациент должен выпить полученный раствор и дополнительно 2 мерных стакана воды или прозрачной жидкости (т.е. около 1 л).
Прием полного объема разведенного раствора препарата Эзиклен® и дополнительного количества воды или прозрачной жидкости должен быть закончен как минимум за 2 часа и не позднее 4 часов до начала процедуры.
Одноэтапная утренняя схема
Время исследования — 14.00 и позже.
Перед процедурой:
- содержимое одного флакона препарата Эзиклен® следует вылить в прилагаемый мерный стакан и развести водой до метки (т.е. до объема 0.5 л);
- в течение последующих 2 часов пациент должен выпить полученный раствор и дополнительно 2 мерных стакана воды или прозрачной жидкости (т.е. около 1 л).
Приблизительно через 2 ч после начала приема 1-й дозы:
- содержимое 2-го флакона препарата Эзиклен® следует вылить в прилагаемый мерный стакан и развести водой до метки (т.е. до объема 0.5 л);
- в течение последующих 2 часов пациент должен выпить полученный раствор и дополнительно 2 мерных стакана воды или прозрачной жидкости (т.е. около 1 л).
Прием полного объема разведенного раствора препарата Эзиклен® и дополнительного количества воды или прозрачной жидкости должен быть закончен как минимум за 2 часа и не позднее 4 часов до начала процедуры.
В случае проведения процедур под общей анестезией
При двухэтапной, одноэтапной утренней и одноэтапной вечерней схемах дозирования прием препарата Эзиклен® и других жидкостей (согласно списку разрешенных — см. выше) необходимо прекратить не менее чем за 2 часа до начала процедуры.
В случае проведения процедур без анестезии
При двухэтапной, одноэтапной утренней и одноэтапной вечерней схемах дозирования прием препарата Эзиклен® и других жидкостей (согласно списку разрешенных — см. выше) необходимо прекратить не менее чем за 1 час до начала процедуры.
Схема разведения и приема препарата:
- открыть флакон, нажав на крышку и поворачивая ее против часовой стрелки;
- вылить содержимое одного флакона в прилагаемый мерный стакан;
- развести препарат водой до метки (т.е. до объема 0.5 л);
- медленно выпить всю жидкость из стакана, в течение 30-60 мин;
- важно: необходимо выпить еще 2 мерных стакана воды или прозрачной жидкости, каждый раз наполняя стакан до метки;
- медленно выпить жидкость из каждого стакана в течение 30 мин (2 х 30 мин).
Выполнение вышеперечисленных этапов занимает около 2 часов.
Следует повторить все этапы со 2-м флаконом препарата Эзиклен®.
После процедуры
Для того чтобы восполнить потерянную в процессе подготовки к процедуре жидкость, пациенты должны выпить достаточное ее количество, чтобы поддержать соответствующий уровень гидратации.
Ограничения в питании
В день накануне процедуры допускается легкий завтрак. Далее пациент может употреблять только прозрачные жидкости в качестве приема пищи вплоть до процедуры. Следует избегать приема жидкостей красного и фиолетового цвета, молока и алкогольных напитков.
Особые группы пациентов
Пожилые пациенты
В ходе клинических исследований препарата не было выявлено разницы в эффективности и безопасности препарата Эзиклен® у пожилых пациентов и пациентов других возрастных групп. Для пожилых пациентов не требуется коррекция дозы, однако следует соблюдать осторожность при применении препарата у таких пациентов, как и в любой другой популяции высокого риска.
Пациенты с нарушением функции почек
Существуют ограниченные данные по этой группе пациентов. Не требуется коррекции дозы для пациентов с нарушением функции почек легкой или средней степени тяжести, однако следует соблюдать осторожность при применении препарата у таких пациентов, как и в любой другой популяции высокого риска. Препарат Эзиклен® противопоказан пациентам с нарушением функции почек тяжелой степени.
Пациенты с нарушением функции печени
Существуют ограниченные данные по этой группе пациентов. Не требуется коррекция дозы для пациентов с нарушением функции печени, однако следует соблюдать осторожность при применении препарата у таких пациентов, как и в любой другой популяции высокого риска.
Детская популяция
Безопасность и эффективность препарата Эзиклен® у пациентов в возрасте до 18 лет пока не установлены. Данные отсутствуют.
Побочное действие
Диарея, возникающая после приема препарата Эзиклен®, является ожидаемым эффектом при очищении кишечника в ходе подготовки перед процедурами и возникает у большинства пациентов. Наиболее частыми сообщаемыми побочными реакциями в клинических исследованиях и пострегистрационном наблюдении были: дискомфорт, вздутие живота, боль в животе, тошнота и рвота.
Во время клинических исследований сообщения о рвоте поступали с большей частотой при использовании режима единовременного применения, чем при использовании режима дробного применения.
Частота побочных реакций при применении препарата Эзиклен® классифицирована следующим образом: очень часто (≥1/10), часто (от ≥1/100 до <1/10), нечасто (от ≥1/1000 до <1/100), редко (от ≥1/10000 до <1/1000), очень редко (<1/10000), неизвестно (невозможно оценить на основании имеющихся данных).
Дополнительная информация для особых групп пациентов
Во время клинических исследований было обнаружено временное повышение концентрации мочевой кислоты. Для пациентов, у которых в анамнезе имеются клинические проявления подагры или гиперурикемии, см. информацию в разделе «Особые указания».
В ходе клинических исследований не было обнаружено разницы в безопасности приема препарата Эзиклен® у пожилых пациентов и пациентов других возрастных групп. Следует соблюдать осторожность при применении препарата у таких пациентов, как и в любой другой популяции высокого риска (см. раздел «Особые указания»).
Противопоказания к применению
- повышенная чувствительность к действующим веществам или к любому из компонентов препарата;
- желудочно-кишечная обструкция или подозрение на желудочно- кишечную обструкцию или стеноз;
- известная или предполагаемая перфорация стенки кишечника (перфорация кишечника);
- нарушения опорожнения желудка (в т.ч. гастропарез, гастростаз);
- кишечная непроходимость (илеус);
- токсический колит или токсический мегаколон;
- тошнота и рвота;
- серьезное ухудшение здоровья (такое как дегидратация тяжелой степени);
- застойная сердечная недостаточность;
- асцит;
- тяжелая почечная недостаточность (СКФ<30 мл/мин/1.73м2);
- активная фаза воспалительных заболеваний кишечника (таких как болезнь Крона, язвенный колит);
- острые заболевания брюшной полости, требующие хирургического вмешательства (например, острый аппендицит);
- беременность;
- период грудного вскармливания;
- возраст до 18 лет.
С осторожностью:
- пожилой возраст;
- нарушение функции почек легкой или средней степени тяжести;
- нарушение функции печени;
- одновременное применение препаратов, влияющих на концентрацию электролитов (блокаторы кальциевых каналов, диуретики, препараты лития или другие препараты подобного действия);
- одновременное применение препаратов, удлиняющих интервал QT;
- снижение моторики ЖКТ (в т. ч. в анамнезе), наличие хирургических вмешательств на ЖКТ, которые привели к нарушению моторики;
- у пациентов с нарушенным рвотным рефлексом, со склонностью к регургитации и аспирации;
- у истощенных, ослабленных пациентов;
- у пациентов с клинически значимыми нарушениями функции сердца;
- у пациентов, имеющих высокий риск развития водно-электролитных нарушений (включая гипонатриемию и гипокалиемию), проявления подагры или гиперурикемию.
Применение при беременности и кормлении грудью
Беременность
Исследования репродуктивной функции у животных с применением сульфатов натрия, магния и калия не проводились.
Данные по применению препарата Эзиклен® у беременных женщин отсутствуют.
Применение препарата Эзиклен® при беременности не рекомендуется.
Грудное вскармливание
Неизвестно, выделяется ли препарат Эзиклен® в грудное молоко.
Нельзя исключать риск для новорожденного/младенца.
Следует прекратить грудное вскармливание на период приема препарата Эзиклен® и вплоть до 48 часов после приема второй дозы.
Фертильность
Данные о влиянии на фертильность отсутствуют.
Применение при нарушениях функции печени
С осторожностью применять у пациентов с нарушением функции печени, коррекции дозы не требуется.
Применение при нарушениях функции почек
С осторожностью применять у пациентов с нарушением функции почек легкой или средней степени тяжести, коррекции дозы не требуется. Препарат Эзиклен® противопоказан пациентам с тяжелой почечной недостаточностью (СКФ<30 мл/мин/1.73м2).
Применение у детей
Противопоказано применение препарата у детей и подростков до 18 лет.
Применение у пожилых пациентов
Для пожилых пациентов не требуется коррекция дозы, однако следует соблюдать осторожность при применении препарата у этой категории пациентов.
Особые указания
Препарат Эзиклен® не применяется для лечения запоров.
Электролитные расстройства и дегидратация
Учитывая потенциальный риск развития серьезных электролитных нарушений, необходимо тщательно оценить соотношение польза/риск, прежде чем применять препарат Эзиклен® в группах высокого риска. Перед применением препарата Эзиклен® должны быть исключены противопоказания для его назначения. Особое внимание необходимо уделить применению специальных мер предосторожности, включая необходимость поддержания соответствующей гидратации.
Все пациенты должны быть предупреждены о необходимости поддержания адекватного уровня гидратации до, во время и после приема препарата Эзиклен®. Если у пациента развивается обильная рвота или признаки дегидратации после приема препарата, должны быть приняты меры по регидратации во избежание потенциального риска серьезных осложнений, связанных с нарушением водно-электролитного баланса (такими как судороги и аритмия сердца). Кроме того, рекомендуется проведение предварительных лабораторных анализов (определение концентрации электролитов, креатинина и азота мочевины крови). Пациентам необходимо рекомендовать пить как можно больше воды или прозрачных жидкостей для поддержания соответствующего уровня гидратации.
Пациенты группы высокого риска
У истощенных, ослабленных пациентов, пожилых пациентов, пациентов с клинически значимыми нарушениями функции почек, печени или сердца, а также у пациентов, имеющих высокий риск развития электролитных нарушений, необходимо провести биохимические анализы с определением сывороточной концентрации электролитов и оценить функцию почек перед началом и после применения препарата.
Пациентам с дегидратацией или нарушениями водно-электролитного баланса необходимо провести соответствующую терапию для их устранения до приема препарата для очищения кишечника. Кроме того, следует соблюдать осторожность при использовании препарата у пациентов с патологическими состояниями или у пациентов, принимающих препараты, которые увеличивают риск появления нарушений водно-электролитного баланса (включая гипонатриемию и гипокалиемию) или повышают риск потенциальных осложнений. Необходимо наблюдение за такими пациентами.
Существует теоретический риск удлинения интервала QT, которое может произойти в результате электролитных нарушений.
Необходимо соблюдать осторожность при использовании препарата у следующих групп пациентов:
- препарат должен применяться с осторожностью и только под наблюдением медицинского персонала у пациентов с нарушенным рвотным рефлексом и у пациентов со склонностью к регургитации и аспирации;
- снижение моторики ЖКТ, в том числе наличие в анамнезе хирургических вмешательств на ЖКТ, которые привели к снижению моторики.
Гиперурикемия
Прием препарата Эзиклен® может вызвать временное легкое или умеренное повышение концентрации мочевой кислоты. Возможность повышения концентрации мочевой кислоты должна учитываться до назначения препарата пациентам с проявлениями подагры или гиперурикемией.
Ишемический колит
Осмотические слабительные могут вызвать афтозные язвы слизистой оболочки толстой кишки. Сообщалось о пострегистрационных редких случаях ишемического колита, в т.ч. серьезных, требующих госпитализации. Этот диагноз следует рассматривать в случае возникновения боли в животе с прокторрагией (ректальными кровотечениями) или без нее после приема лекарственного препарата Эзиклен®. Препарат Эзиклен® следует применять с осторожностью у пациентов с известными факторами риска ишемического колита. При возникновении симптомов, указанных выше, следует незамедлительно обратиться к врачу.
Дополнительная информация
Перед приемом препарат необходимо развести водой. Прием неразбавленного раствора может увеличить риск тошноты, рвоты, дегидрации и электролитных нарушений. Каждый флакон препарата необходимо разводить водой, а также употреблять рекомендуемое дополнительное количество воды для обеспечения хорошей переносимости препарата у пациента.
Лекарственный препарат содержит 247.1 ммоль (или 5.684 г) натрия на флакон. Это необходимо принимать во внимание у пациентов, которые находятся на диете с контролем потребления натрия.
Лекарственный препарат содержит 35.9 ммоль (или 1.405 г) калия на флакон. Это необходимо принимать во внимание у пациентов со сниженной функцией почек или у пациентов, которые находятся на диете с контролем потребления калия.
После вскрытия флакона и/или разведения водой раствор должен быть использован незамедлительно.
Влияние на способность к управлению транспортными средствами и механизмами
Прием препарата Эзиклен® не оказывает влияния на способность управлять автомобилем и работать с механизмами.
Передозировка
В случае передозировки или неправильного применения (например, применение неразведенного препарата и/или прием недостаточного объема воды) возможно возникновение тошноты, рвоты, диареи и электролитных нарушений. Обычно в этом случае применяется симптоматическая терапия, в том числе прием жидкости внутрь. В редких случаях передозировки, сопровождающихся тяжелыми метаболическими нарушениями, рекомендуется проведение внутривенной регидратации.
Лекарственное взаимодействие
С осторожностью применять у пациентов, получающих терапию препаратами, оказывающими влияние на концентрацию электролитов (например, блокаторы медленных кальциевых каналов, диуретики, препараты лития или другие препараты подобного действия).
Следует соблюдать осторожность при одновременном приеме препаратов, удлиняющих интервал QT.
Диарея является ожидаемым эффектом, прием внутрь других лекарственных препаратов в течение 1-3 ч после начала приема препарата Эзиклен® и до окончания процесса очищения кишечника может привести к вымыванию их из ЖКТ и нарушению абсорбции. Может быть изменен терапевтический эффект препаратов, применяемых регулярно внутрь, имеющих узкий терапевтический диапазон или короткий Т1/2 (например, пероральные контрацептивы, противоэпилептические препараты, гипогликемические препараты, антибиотики, левотироксин натрия, дигоксин и т.д.).
Условия хранения препарата Эзиклен®
Препарат следует хранить в недоступном для детей месте при температуре не выше 25°С.
Срок годности препарата Эзиклен®
Срок годности — 3 года.
После вскрытия флакона и/или разведения водой раствор должен быть использован незамедлительно.
Не применять по истечении срока годности.
Условия реализации
Препарат отпускают без рецепта.
Контакты для обращений
ИПСЕН КОНСЬЮМЕР ХЕЛСКЕА САС
(Франция)

|
|
Организация, принимающая претензии потребителей: |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
From Wikipedia, the free encyclopedia
|
|

|
|

|
|
| Names | |
|---|---|
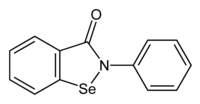
| Preferred IUPAC name
2-Phenyl-1,2-benzoselenazol-3(2H)-one |
|
| Identifiers | |
|
CAS Number |
|
|
3D model (JSmol) |
|
| ChEBI |
|
| ChEMBL |
|
| ChemSpider |
|
| ECHA InfoCard | 100.132.190 |
|
PubChem CID |
|
| UNII |
|
|
CompTox Dashboard (EPA) |
|
|
InChI
|
|
|
SMILES
|
|
| Properties | |
|
Chemical formula |
C13H9NOSe |
| Molar mass | 274.17666 |
|
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
Infobox references |
Ebselen (also called PZ 51, DR3305, and SPI-1005), is a synthetic organoselenium drug molecule with anti-inflammatory, anti-oxidant and cytoprotective activity. It acts as a mimic of glutathione peroxidase and can also react with peroxynitrite.[1] It is being investigated as a possible treatment for reperfusion injury and stroke,[2][3] Ménière’s disease,[4][5] hearing loss and tinnitus,[6][7] and bipolar disorder.[8][9]
Additionally, ebselen may be effective against Clostridioides difficile infections[10] and has been shown to have antifungal activity against Aspergillus fumigatus.[11]
Ebselen is a potent scavenger of hydrogen peroxide as well as hydroperoxides including membrane bound phospholipid and cholesterylester hydroperoxides. Several ebselen analogs have been shown to scavenge hydrogen peroxide in the presence of thiols.[12]
Possible anti-COVID-19 activity[edit]
Preliminary studies demonstrate that Ebselen exhibits promising inhibitory activity against COVID-19 in cell-based assays.[13][14][15] The effect was attributed to irreversible inhibition of the main protease via a covalent bond formation with the thiol group of the active center’s cysteine (Cys-145).[13]
Synthesis[edit]
Generally, synthesis of the characteristic scaffold of ebselen, the benzoisoselenazolone ring system, can be achieved either through reaction of primary amines (RNH2) with 2-(chloroseleno)benzoyl chloride (Route I),[16] by ortho-lithiation of benzanilides followed by oxidative cyclization (Route II) mediated by cupric bromide (CuBr2),[17] or through the efficient Cu-catalyzed selenation / heterocyclization of o-halobenzamides, a methodology developed by Kumar et al.[18] (Route III).

History[edit]
The first patent for 2-Phenyl-1,2-benzoselenazol-3(2H)-one was filed in 1980 and granted in 1982.[19]
References[edit]
- ^ Schewe T (October 1995). «Molecular actions of ebselen—an antiinflammatory antioxidant». General Pharmacology. 26 (6): 1153–69. doi:10.1016/0306-3623(95)00003-J. PMID 7590103.
- ^ Parnham M, Sies H (March 2000). «Ebselen: prospective therapy for cerebral ischaemia». Expert Opinion on Investigational Drugs. 9 (3): 607–19. doi:10.1517/13543784.9.3.607. PMID 11060699. S2CID 42599736.
- ^ Yamaguchi T, Sano K, Takakura K, Saito I, Shinohara Y, Asano T, Yasuhara H (January 1998). «Ebselen in acute ischemic stroke: a placebo-controlled, double-blind clinical trial. Ebselen Study Group». Stroke. 29 (1): 12–7. doi:10.1161/01.STR.29.1.12. PMID 9445321.
- ^ «SPI-1005 for the Treatment of Meniere’s Disease». Sound Pharmaceuticals. Retrieved 7 November 2022.
- ^ «Sound Pharma initiates enrollment in pivotal Phase 3 clinical trial of SPI-1005 for the treatment of hearing loss and tinnitus in Meniere’s disease». Sound Pharmaceuticals. 2022-07-28. Retrieved 7 November 2022.
- ^ Kil J, Pierce C, Tran H, Gu R, Lynch ED (April 2007). «Ebselen treatment reduces noise induced hearing loss via the mimicry and induction of glutathione peroxidase». Hearing Research. 226 (1–2): 44–51. doi:10.1016/j.heares.2006.08.006. PMID 17030476. S2CID 39896274.
- ^ Kil, Jonathan; Harruff, E. Emily; Longenecker, Ryan J. (2022). «Development of ebselen for the treatment of sensorineural hearing loss and tinnitus». Hearing Research. Elsevier BV. 413: 108209. doi:10.1016/j.heares.2021.108209. ISSN 0378-5955. PMID 33678494. S2CID 231956488.
- ^ Singh N, Halliday AC, Thomas JM, Kuznetsova OV, Baldwin R, Woon EC, et al. (2013). «A safe lithium mimetic for bipolar disorder». Nature Communications. 4: 1332. Bibcode:2013NatCo…4.1332S. doi:10.1038/ncomms2320. PMC 3605789. PMID 23299882.
- ^ «New drug for bipolar disorder may offer fewer side effects». University of Oxford Latest News. 2013-01-08. Retrieved 12 January 2013.
- ^ «Drug disarms deadly C. difficile bacteria without destroying healthy gut flora». Medical Express.
- ^ Marshall AC, Kidd SE, Lamont-Friedrich SJ, Arentz G, Hoffmann P, Coad BR, Bruning JB (March 2019). «Structure, Mechanism, and Inhibition of Aspergillus fumigatus Thioredoxin Reductase». Antimicrobial Agents and Chemotherapy. 63 (3): e02281-18. doi:10.1128/AAC.02281-18. PMC 6395915. PMID 30642940.
- ^ Satheeshkumar K, Mugesh G (April 2011). «Synthesis and antioxidant activity of peptide-based ebselen analogues». Chemistry: A European Journal. 17 (17): 4849–57. doi:10.1002/chem.201003417. PMID 21400619.
- ^ a b Jin Z, Du X, Xu Y, Deng Y, Liu M, Zhao Y, et al. (June 2020). «Structure of Mpro from SARS-CoV-2 and discovery of its inhibitors». Nature. 582 (7811): 289–293. Bibcode:2020Natur.582..289J. doi:10.1038/s41586-020-2223-y. PMID 32272481.
- ^ Weglarz-Tomczak E, Tomczak JM, Talma M, Burda-Grabowska M, Giurg M, Brul S (February 2021). «Identification of ebselen and its analogues as potent covalent inhibitors of papain-like protease from SARS-CoV-2». Scientific Reports. 11 (1): 3640. Bibcode:2021NatSR..11.3640W. doi:10.1038/s41598-021-83229-6. PMC 7878891. PMID 33574416.
- ^ Xiang R, Yu Z, Wang Y, Wang L, Huo S, Li Y, et al. (July 2021). «Recent advances in developing small-molecule inhibitors against SARS-CoV-2». Acta Pharmaceutica Sinica B. 12 (4): 1591–1623. doi:10.1016/j.apsb.2021.06.016. PMC 8260826. PMID 34249607.
- ^ Kamigata N, Iizuka H, Izuoka A, Kobayashi M (July 1986). «Photochemical Reaction of 2-Aryl-1, 2-benzisoselenazol-3 (2 H)-ones». Bulletin of the Chemical Society of Japan. 59 (7): 2179–83. doi:10.1246/bcsj.59.2179.
- ^ Engman L, Hallberg A (1989-06-01). «Expedient synthesis of ebselen and related compounds». The Journal of Organic Chemistry. 54 (12): 2964–2966. doi:10.1021/jo00273a035. ISSN 0022-3263.
- ^ Balkrishna SJ, Bhakuni BS, Chopra D, Kumar S (December 2010). «Cu-catalyzed efficient synthetic methodology for ebselen and related Se-N heterocycles». Organic Letters. 12 (23): 5394–7. doi:10.1021/ol102027j. PMID 21053969.
- ^ DE3027073A1, Etschenberg, Eugen Dr; Renson, Marcel Prof Dipl-Chem Jupille & Winkelmann, Johannes Dr 5000 Köln, «2-phenyl-1,2-benzisoselenazol-3(2h)-on enthaltende pharmazeutische praeparate und ihre verwendung», issued 1982-02-18
