Галвус® (Galvus®)
💊 Состав препарата Галвус®
✅ Применение препарата Галвус®
Описание активных компонентов препарата
Галвус®
(Galvus®)
Приведенная научная информация является обобщающей и не может быть использована для принятия
решения о возможности применения конкретного лекарственного препарата.
Дата обновления: 2020.03.25
Владелец регистрационного удостоверения:
Код ATX:
A10BH02
(Вилдаглиптин)
Лекарственная форма
| Галвус® |
Таб. 50 мг: 14, 28, 56, 84, 112 или 168 шт. рег. №: ЛП-(000761)-(РГ-RU) Предыдущий рег. №: ЛСР-008119/08 |
Форма выпуска, упаковка и состав
препарата Галвус®
Таблетки от белого до светло-желтого цвета, круглые, гладкие, со скошенными краями, с гравировкой «NVR» на одной стороне и «FB» на другой стороне.
Вспомогательные вещества: целлюлоза микрокристаллическая, лактоза, карбоксиметилкрахмал натрия, магния стеарат.
7 шт. — блистеры (2) — пачки×.
7 шт. — блистеры (4) — пачки×.
7 шт. — блистеры (8) — пачки×.
7 шт. — блистеры (12) — пачки×.
14 шт. — блистеры (2) — пачки×.
14 шт. — блистеры (4) — пачки×.
14 шт. — блистеры (8) — пачки×.
14 шт. — блистеры (12) — пачки×.
× допускается наличие контроля первичного вскрытия на картонной пачке.
Фармакологическое действие
Гипогликемическое средство. Вилдаглиптин — представитель класса стимуляторов островкового аппарата поджелудочной железы, селективно ингибирует фермент дипептидилпептидазу-4 (ДПП-4). Быстрое и полное ингибирование активности ДПП-4 (> 90%) вызывает повышение как базальной, так и стимулированной приемом пищи секреции глюкагоноподобного пептида 1 типа (ГПП-1) и глюкозо-зависимого инсулинотропного полипептида (ГИП) из кишечника в системный кровоток в течение всего дня.
Увеличивая уровни ГПП-1 и ГИП, вилдаглиптин вызывает повышение чувствительности β-клеток поджелудочной железы к глюкозе, что приводит к улучшению глюкозозависимой секреции инсулина. При применении вилдаглиптина в дозе 50-100 мг/сут у больных с сахарным диабетом 2 типа отмечается улучшение функции β-клеток поджелудочной железы. Степень улучшения функции β-клеток зависит от степени их исходного повреждения; так у лиц, не страдающих сахарным диабетом (с нормальным уровнем глюкозы в плазме крови) вилдаглиптин не стимулирует секрецию инсулина и не снижает уровень глюкозы.
Повышая уровни эндогенного ГПП-1, вилдаглиптин увеличивает чувствительность α-клеток к глюкозе, что приводит к улучшению глюкозозависимой регуляции секреции глюкагона. Снижение уровня избыточного глюкагона во время еды, в свою очередь, вызывает уменьшение инсулинорезистентности.
Увеличение соотношения инсулин/глюкагон на фоне гипергликемии, обусловленное повышением уровней ГПП-1 и ГИП, вызывает уменьшение продукции глюкозы печенью как в прандиальный период, так и после приема пищи, что приводит к снижению уровня глюкозы в плазме крови.
Кроме того, на фоне применения вилдаглиптина отмечается снижение уровня липидов в плазме крови, однако этот эффект не связан с его действием на ГПП-1 или ГИП и улучшением функции β-клеток поджелудочной железы.
Известно, что повышение уровня ГПП-1 может приводить к замедлению опорожнения желудка, однако на фоне применения вилдаглиптина подобного эффекта не наблюдается.
При применении вилдаглиптина у 5795 больных с сахарным диабетом 2 типа в течение от 12 до 52 недель в качестве монотерапии или в комбинации с метформином, производными сульфонилмочевины, тиазолидиндионом, или инсулином отмечается достоверное длительное снижение концентрации гликированного гемоглобина (HbA1с) и глюкозы крови натощак.
Фармакокинетика
Вилдаглиптин быстро абсорбируется при приеме внутрь с абсолютной биодоступностью 85%. В терапевтическом диапазоне доз увеличение Cmax вилдаглиптина в плазме и AUC практически прямо пропорционально повышению дозы.
После приема внутрь натощак время достижения Cmax вилдаглиптина в плазме крови составляет 1 ч 45 мин. При одновременном приеме с пищей скорость абсорбции снижается незначительно: отмечается уменьшение Cmax на 19% и увеличение времени ее достижения до 2 ч 30 мин. Однако прием пищи не оказывает влияния на степень абсорбции и AUC.
Связывание вилдаглиптина с белками плазмы низкое (9.3%). Эквивалентно распределяется между плазмой и эритроцитами. Распределение вилдаглиптина происходит предположительно экстраваскулярно, Vd в равновесном состоянии после в/в введения составляет 71 л.
Биотрансформация является основным путем выведения вилдаглиптина. В организме у человека подвергается превращению 69%. Основной метаболит — LAY151 (57% дозы) фармакологически неактивен и является продуктом гидролиза циано-компонента. Около 4% подвергается амидному гидролизу. В экспериментальных исследованиях отмечается положительное влияние ДПП-4 на гидролиз активного вещества. Вилдаглиптин не метаболизируется при участии изоферментов цитохрома Р450, не является субстратом, не ингибирует и не индуцирует данные изоферменты.
После приема внутрь около 85% выводится почками и 15% — через кишечник, почечная экскреция неизмененного вилдаглиптина составляет 23%. T1/2 после приема внутрь составляет около 3 ч независимо от дозы.
Показания активных веществ препарата
Галвус®
Сахарный диабет 2 типа: в качестве монотерапии в сочетании с диетотерапией и физическими упражнениями; в составе двухкомпонентной комбинированной терапии с метформином, производными сульфонилмочевины, тиазолидиндионом или с инсулином в случае неэффективности диетотерапии, физических упражнений и монотерапии этими препаратами.
Режим дозирования
Способ применения и режим дозирования конкретного препарата зависят от его формы выпуска и других факторов. Оптимальный режим дозирования определяет врач. Следует строго соблюдать соответствие используемой лекарственной формы конкретного препарата показаниям к применению и режиму дозирования.
Режим дозирования устанавливают индивидуально в зависимости эффективности, переносимости и схемы терапии.
Разовая доза — 50 мг, суточная доза — 100 мг (по 50 мг 2 раза/сут).
Побочное действие
Со стороны пищеварительной системы: иногда — запоры; редко — нарушения функции печени (включая гепатит) бессимптомного течения; при комбинации с инсулином часто — тошнота, метеоризм, ГЭРБ.
Со стороны ЦНС: часто — тремор, головокружение, головная боль.
Со стороны обмена веществ: часто — гипогликемия, увеличение массы тела.
Аллергические реакции: редко — ангионевротический отек (чаще при комбинации с ингибиторами АПФ).
Прочие: часто — астения, периферические отеки.
Противопоказания к применению
Повышенная чувствительность к вилдаглиптину.
Применение при беременности и кормлении грудью
Адекватных и строго контролируемых клинических исследований безопасности применения вилдаглиптина при беременности и в период лактации не проводилось, поэтому не следует применять вилдаглиптин при беременности и в период грудного вскармливания.
При нарушениях обмена глюкозы у беременных женщин отмечается повышение риска развития врожденных аномалий, а также частоты неонатальной заболеваемости и смертности.
Неизвестно, выделяется ли вилдаглиптин с грудным молоком у человека.
Применение при нарушениях функции печени
Не рекомендуется применять у пациентов с тяжелыми нарушениями функции печени, в т.ч. при повышении активности АЛТ или АСТ > 2.5 раза выше ВГН.
Перед началом лечения, а также регулярно (1 раз в 3 месяца) в ходе первого года лечения, рекомендуется определять биохимические показатели функции печени. В случае выявления повышенной активности аминотрансфераз, этот результат следует подтвердить повторным исследованием, а затем регулярно проводить определение биохимических показателей функции печени до тех пор, пока они не нормализуются. Если превышение активности АСТ или АЛТ в 3 раза и более ВГН подтверждено повторным исследованием, то вилдаглиптин рекомендуется отменить.
При развитии желтухи или других признаков нарушения функции печени терапию вилдаглиптином следует немедленно прекратить. После нормализации показателей функции печени лечение возобновлять нельзя.
Применение при нарушениях функции почек
Не рекомендуется применять у пациентов с умеренными или тяжелыми нарушениями функции почек (включая терминальную стадию почечной недостаточности и необходимостью проведения гемодиализа), т.к. данные о безопасности применения у данной категории пациентов ограничены.
Применение у детей
Эффективность и безопасность применения вилдаглиптина у детей и подростков в возрасте до 18 лет не установлены.
Особые указания
Не рекомендуется применять у пациентов с тяжелыми нарушениями функции печени, в т.ч. при повышении активности АЛТ или АСТ > 2.5 раза выше ВГН.
Не рекомендуется применять у пациентов с умеренными или тяжелыми нарушениями функции почек (включая терминальную стадию почечной недостаточности и необходимостью проведения гемодиализа), т.к. данные о безопасности применения у данной категории пациентов ограничены.
Перед началом лечения, а также регулярно (1 раз в 3 месяца) в ходе первого года лечения, рекомендуется определять биохимические показатели функции печени. В случае выявления повышенной активности аминотрансфераз, этот результат следует подтвердить повторным исследованием, а затем регулярно проводить определение биохимических показателей функции печени до тех пор, пока они не нормализуются. Если превышение активности АСТ или АЛТ в 3 раза и более ВГН подтверждено повторным исследованием, то вилдаглиптин рекомендуется отменить.
При развитии желтухи или других признаков нарушения функции печени терапию вилдаглиптином следует немедленно прекратить. После нормализации показателей функции печени лечение возобновлять нельзя.
При необходимости инсулинотерапии вилдаглиптин применяют только в комбинации с инсулином.
Вилдаглиптин не следует применять для лечения сахарного диабета 1 типа или для лечения диабетического кетоацидоза.
Использование в педиатрии
Эффективность и безопасность применения вилдаглиптина у детей и подростков в возрасте до 18 лет не установлены.
Влияние на способность к управлению транспортными средствами и механизмами
При развитии головокружения на фоне лечения препаратом пациентам не следует заниматься потенциально опасными видами деятельности (в т.ч. управлением транспортными средствами).
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код

ИМЕЮТСЯ ПРОТИВОПОКАЗАНИЯ. ВОЗМОЖНЫ ПОБОЧНЫЕ ЭФФЕКТЫ. НЕОБХОДИМА КОНСУЛЬТАЦИЯ СПЕЦИАЛИСТА.При диабете
Автор статьи
Подойницына Алёна Андреевна
,
Диплом о фармацевтическом образовании: 105924 3510722 рег. номер 31917
Все авторы
Содержание статьи
- Галвус: состав
- Галвус: таблетки от чего
- Галвус: до еды или после еды принимать
- Галвус: противопоказания
- Галвус: побочные действия
- Галвус или Випидия: что лучше
- Кселевия или Галвус: что лучше
- Форсига или Галвус: что лучше
- Краткое содержание
- Задайте вопрос эксперту по теме статьи
Сахарный диабет – это заболевание, при котором поджелудочная железа вырабатывает малое количество инсулина или организм теряет к нему восприимчивость. Согласно статистике Всемирной организации здравоохранения (ВОЗ), за время с 1980 по 2014 год количество пациентов с диабетом выросло со 108 миллионов до 422 миллионов человек. Рост численности пациентов связывают с неправильным питанием, малоподвижным образом жизни, избыточным весом и генетической предрасположенностью. Международная федерация диабета (International Diabetes Federation, IDF) считает, что к 2045 году ожидается рост числа диабетиков до 629 миллионов.
Провизор расскажет о препарате Галвус: ознакомит с его составом, показаниями к применению, противопоказаниями и побочными действиями, а также сравнит с аналогами.
Галвус: состав
Таблетки Галвус – гипогликемическое средство. Простыми словами, это препарат, действие которого направлено на снижение уровня глюкозы в крови. За оказание нужного эффекта отвечает действующее вещество Галвус – вилдаглиптин, принадлежащее к инновационному классу активных соединений.
Выпускается также комбинированная форма – Галвус Мет. В его составе присутствует два действующих вещества для оказания более выраженного гипогликемического действия: вилдаглиптин и метформин.
Галвус: таблетки от чего
Галвус – лекарство от диабета второго типа. Согласно инструкции, препарат назначается в сочетании с диетой и физическими упражнениями для монотерапии или в комплексе с другими медикаментами. Например, метформином. Чтобы понять, как работает Галвус, нужно разобраться с двумя веществами – инсулином и глюкагоном:
- Инсулин – это вещество, которое помогает сбалансировать уровень глюкозы в крови, в особенности после еды;
- Глюкагон – это вещество, которое стимулирует синтез глюкозы в печени, повышая ее уровень в крови.
Оба вещества синтезируются в поджелудочной железе. Так вот, Галвус помогает органу вырабатывать больше инсулина и меньше глюкагона, таким образом, контролируя уровень глюкозы в крови.
Галвус: до еды или после еды принимать
Лекарство Галвус можно принимать во время еды или вне приема пищи. Дозировка Галвус устанавливается врачом, в зависимости от действенности и переносимости препарата. Для удобства дозирования в аптеке присутствует:
- Галвус 50 мг;
- Галвус Мет 50+500 мг;
- Галвус Мет 50+850 мг;
- Галвус Мет 50+1000 мг.
Галвус: противопоказания
- Повышенная чувствительность к компонентам препарата;
- Сахарный диабет первого типа;
- Нарушение почечных функций;
- Хроническая сердечная недостаточность;
- Острый или хронический кетоацидоз, лактоацидоз;
- Наследственная непереносимость галактозы, недостаточность лактазы, глюкозо-галактозная мальабсорбция;
- Период беременности и грудного вскармливания;
- Детский возраст до 18 лет.
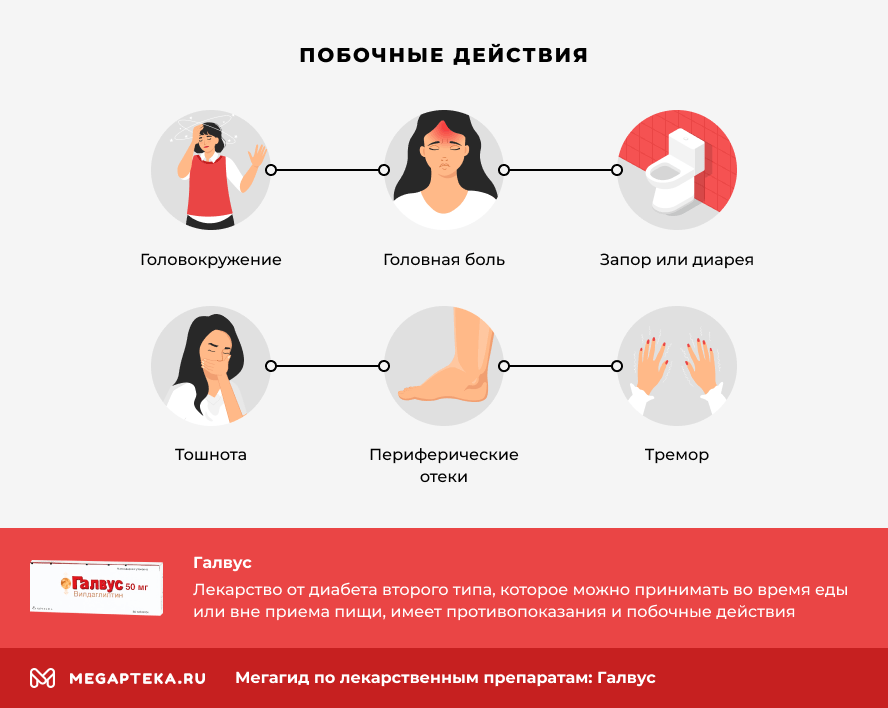
Галвус: побочные действия
С полным списком нежелательных реакций можно ознакомиться в инструкции к препарату, включая побочные действия Галвус Мет. Неблагоприятные реакции на действие рассматриваемых лекарств, как правило, выражены слабо и носят временный характер. Тем не менее при их возникновении рекомендуется обратиться к врачу.
Побочные действия Галвус и комбинации с другими препаратами:
- Головокружение;
- Головная боль;
- Тошнота;
- Запор или диарея;
- Периферические отеки;
- Тремор;
- Утомляемость;
- Чрезмерное снижение уровня сахара;
- Другие.
Галвус или Випидия: что лучше
Випидия и Галвус – современные средства для лечения сахарного диабета, которые принадлежат к одной группе и работают по схожему механизму. Эффективность препаратов является сопоставимой. Врач выбирает между Випидией и Галвусом на основе индивидуальных особенностей пациента.
Кселевия или Галвус: что лучше
В основе препарата Кселевия лежит ситаглиптин – первое лекарство рассматриваемой группы, одобренное для лечения сахарного диабета второго типа еще в 2006 году. После его успешного применения в практику было введено еще несколько препаратов данной группы, включая вилдаглиптин (Галвус).
Кселевия и Галвус сопоставимы по эффективности. Решение о назначении того или иного препарата принимает врач на основе индивидуальных характеристик пациента.
Форсига или Галвус: что лучше
Форсига – лекарство для терапии сахарного диабета второго типа. Помимо основного действия, препарат способствует снижению артериального давления и нагрузки на сердце, а также сохранению функции почек. В связи с этим Форсига чаще назначается пациентам, у которых сахарный диабет второго типа сочетается с сердечно-сосудистыми рисками и хронической сердечной недостаточностью.
Выбор между Форсига и Галвус остается за врачом. Только специалист, знакомый с историей болезни пациента, может грамотно подобрать препарат под персональные особенности больного.
Краткое содержание
- Таблетки Галвус – гипогликемическое средство.
- Галвус – лекарство от диабета второго типа.
- Лекарство Галвус можно принимать во время еды или вне приема пищи.
- Галвус имеет противопоказания и побочные действия.
- Випидия и Галвус – современные средства для лечения сахарного диабета, которые принадлежат к одной группе и работают по схожему механизму.
- В основе препарата Кселевия лежит ситаглиптин – первое лекарство рассматриваемой группы, одобренное для лечения сахарного диабета второго типа еще в 2006 году.
- Форсига чаще назначается пациентам, у которых сахарный диабет второго типа сочетается с сердечно-сосудистыми рисками и хронической сердечной недостаточностью.
Задайте вопрос эксперту по теме статьи
Остались вопросы? Задайте их в комментариях ниже – наши эксперты ответят вам. Там же вы можете поделиться своим опытом с другими читателями Мегасоветов.
Поделиться мегасоветом
Понравилась статья? Расскажите маме, папе, бабушке и тете Гале из третьего подъезда
Галвус
Galvus
Регистрационный номер
Торговое наименование
Галвус
Международное непатентованное наименование
Лекарственная форма
таблетки
Состав
Описание
От белого до светло-жёлтого цвета, круглые, гладкие таблетки со скошенными краями, с гравировкой «NVR» на одной стороне и «FB» на другой стороне.
Фармакотерапевтическая группа
Код АТХ
Фармакологические свойства
Механизм действия
Вилдаглиптин — представитель класса стимуляторов островкового аппарата поджелудочной железы, селективно ингибирует фермент дипептидилпептидазу-4 (ДПП-4). Быстрое и полное ингибирование активности ДПП-4 (>90 %) вызывает повышение как базальной, так и стимулированной приёмом пищи секреции глюкагоноподобного пептида 1 типа (ГПП-1) и глюкозозависимого инсулинотропного полипептида (ГИП) из кишечника в системный кровоток в течение всего дня.
Повышая концентрацию ГПП-1 и ГИП, вилдаглиптин вызывает повышение чувствительности β-клеток поджелудочной железы к глюкозе, что приводит к улучшению глюкозозависимой секреции инсулина.
Фармакодинамика
При применении вилдаглиптина в дозе 50–100 мг в сутки у пациентов с сахарным диабетом 2 типа (СД 2 типа) отмечается улучшение функции β-клеток поджелудочной железы. Степень улучшения функции β-клеток зависит от степени их исходного повреждения; так у лиц без СД (с нормальной концентрацией глюкозы в плазме крови) вилдаглиптин не стимулирует секрецию инсулина и не снижает концентрацию глюкозы.
Повышая концентрацию эндогенного ГПП-1, вилдаглиптин увеличивает чувствительность α-клеток к глюкозе, что приводит к улучшению глюкозозависимой регуляции секреции глюкагона. Снижение повышенной концентрации глюкагона во время еды, в свою очередь, вызывает уменьшение инсулинорезистентности.
Увеличение соотношения инсулин/глюкагон на фоне гипергликемии, обусловленное повышением концентрации ГПП-1 и ГИП, вызывает уменьшение продукции глюкозы печенью как во время, так и после приёма пищи, что приводит к снижению концентрации глюкозы в плазме крови.
Кроме того, на фоне применения вилдаглиптина отмечается снижение концентрации липидов в плазме крови после приёма пищи, однако этот эффект не связан с его действием на ГПП-1 или ГИП и улучшением функции островковых клеток поджелудочной железы.
Известно, что повышение концентрации ГПП-1 может приводить к замедлению опорожнения желудка, однако на фоне применения вилдаглиптина подобного эффекта не наблюдается.
При применении вилдаглиптина у 5795 пациентов с СД 2 типа в течение 52 недель в монотерапии или в комбинации с метформином, производными сульфонилмочевины, тиазолидиндионом, или инсулином отмечалось достоверное длительное снижение концентрации гликированного гемоглобина (HbA1c) и глюкозы крови натощак.
При применении комбинации вилдаглиптина и метформина в качестве начальной терапии у пациентов с сахарным диабетом 2 типа в течение 24 недель отмечалось дозозависимое снижение концентрации HbA1c в сравнении с монотерапией данными препаратами. Случаи развития гипогликемии были минимальны в обеих группах терапии.
При применении вилдаглиптина в дозе 50 мг 1 раз в сутки в течение 6 месяцев у пациентов с СД 2 типа с нарушением функции почек средней (скорость клубочковой фильтрации (СКФ) ≥30, <50 мл/мин/1,73 м2) или тяжёлой (СКФ <30 мл/мин/1,73 м2) степени отмечалось клинически значимое снижение концентрации HbA1c по сравнению с плацебо.
При применении вилдаглиптина в дозе 50 мг 2 раза в сутки в комбинации с/без метформина и инсулином (средняя доза 41 ЕД/сут) было продемонстрировано снижение показателя HbA1c на 0,77 % от исходного среднего значения 8,8 % со статистически достоверной разницей с плацебо 0,72 %. Частота гипогликемии в группе вилдаглиптина сравнима с таковой в группе плацебо. При применении вилдаглиптина в дозе 50 мг 2 раза в сутки в комбинации с метформипом (≥1500 мг/сут) и глимепиридом (≥4 мг/сут) было показано статистически значимое снижение уровня HbA1c на 0,76 % от исходного среднего значения 8,8 %.
Фармакокинетика
Всасывание
При приёме внутрь натощак вилдаглиптин быстро всасывается, а его максимальная концентрация в плазме крови (Сmax) достигается через 1,75 часа после приёма. При одновременном приёме с пищей скорость абсорбции вилдаглиптина снижается незначительно: отмечается уменьшение Сmax на 19 % и увеличение времени её достижения до 2,5 часов. Однако приём пищи не оказывает влияния на степень абсорбции и площадь под кривой «концентрация–время» (AUC).
Вилдаглиптин быстро всасывается, а его абсолютная биодоступность после приёма внутрь составляет 85 %. Сmax и AUC в терапевтическом диапазоне доз увеличиваются примерно пропорционально дозе.
Распределение
Степень связывания вилдаглиптина с белками плазмы крови низкая (9,3 %). Вилдаглиптин распределяется равномерно между плазмой крови и эритроцитами. Распределение вилдаглиптина происходит, предположительно, экстраваскулярно, объём распределения в равновесном состоянии после внутривенного введения (Vss) составляет 71 л.
Метаболизм
Основным путём выведения вилдаглиптина является биотрансформация. В организме человека 69 % дозы препарата подвергается биотрансформации. Основной метаболит — LAY151 (57 % дозы) фармакологически неактивен и является продуктом гидролиза цианокомпонента. Около 4 % дозы препарата подвергаются амидному гидролизу.
В доклинических исследованиях отмечается положительное влияние ДПП-4 на гидролиз вилдаглиптина. Вилдаглиптин метаболизируется без участия изоферментов цитохрома P450. Вилдаглиптин не является субстратом изоферментов P450 (CYP), не ингибирует и не индуцирует изоферменты цитохрома P450.
Выведение
После приёма препарата внутрь около 85 % дозы выводится почками и 15 % — через кишечник. Почечная экскреция неизменённого вилдаглиптина составляет 23 %. При внутривенном введении средний период полувыведения достигает 2 часов, общий плазменный клиренс и почечный клиренс вилдаглиптина составляют 41 л/ч и 13 л/ч соответственно. Период полувыведения (T½) после приёма внутрь составляет около 3 часов, независимо от дозы.
Фармакокинетика в особых случаях
Пол, индекс массы тела и этническая принадлежность не оказывают влияния на фармакокинетику вилдаглиптина.
Пациенты с нарушением функции печени
У пациентов с нарушением функции печени лёгкой и средней степеней тяжести (6–9 баллов по шкале Чайлд-Пью) после однократного применения препарата отмечается снижение биодоступности вилдаглиптина на 20 % и 8 % соответственно. У пациентов с нарушением функции печени тяжёлой степени (10–12 баллов по шкале Чайлд-Пью) биодоступность вилдаглиптина повышается на 22 %. Увеличение или уменьшение максимальной биодоступности вилдаглиптина, не превышающее 30 %, не является клинически значимым. Корреляции между степенью тяжести нарушений функции печени и биодоступностью препарата не выявлено.
Пациенты с нарушением функции почек
У пациентов с нарушением функции почек лёгкой, средней или тяжёлой степени AUC вилдаглиптина увеличивалась по сравнению со здоровыми добровольцами в 1,4, 1,7 и 2 раза соответственно. AUC метаболита LAY151 увеличивалась в 1,6, 3,2, и 7,3 раза, а метаболита BQS867 — в 1,4, 2,7, и 7,3 раза у пациентов с нарушением функции почек лёгкой, средней и тяжёлой степеней соответственно. Ограниченные данные у пациентов с терминальной стадией хронической болезни почек (ХБП) указывают на то, что показатели данной группы схожи с таковыми у пациентов с нарушением функции почек тяжёлой степени. Концентрация метаболита LAY151 у пациентов с терминальной стадией ХБП увеличивалась в 2–3 раза по сравнению с концентрацией у пациентов с нарушением функции почек тяжёлой степени.
При применении препарата у пациентов с нарушением функции почек может потребоваться коррекция дозы.
Выведение вилдаглиптина при гемодиализе ограничено (через 4 часа после однократного приёма составляет 3 % при длительности процедуры более 3–4 часов).
Применение у пациентов в возрасте ≥65 лет
Максимальное увеличение биодоступности препарата на 32 % (увеличение Сmах на 18 %) у пациентов старше 70 лет не является клинически значимым и не влияет на ингибирование ДПП-4.
Применение у пациентов в возрасте ≤18 лет
Фармакокинетические особенности вилдаглиптина у детей и подростков младше 18 лет не установлены.
Показания
Сахарный диабет 2 типа (в сочетании с диетотерапией и физическими упражнениями):
- в качестве монотерапии в случае неэффективности диетотерапии и физических упражнений у пациентов с противопоказанием к применению метформина или в случае неэффективности метформина;
- в комбинации с метформином в качестве начальной медикаментозной терапии при недостаточной эффективности диетотерапии и физических упражнений;
- в составе двухкомпонентной комбинированной терапии с метформином, производным сульфонилмочевины, тиазолидиндионом или с инсулином в случае неэффективности диетотерапии, физических упражнений и монотерапии этими препаратами;
- в составе тройной комбинированной терапии: в комбинации с производными сульфонилмочевины и метформином, у пациентов, ранее получавших терапию производными сульфонилмочевины и метформином на фоне диетотерапии и физических упражнений и не достигших адекватного контроля гликемии;
- в составе тройной комбинированной терапии: в комбинации с инсулином и метформином, у пациентов, ранее получавших инсулин и метформин на фоне диетотерапии и физических упражнений и не достигших адекватного контроля гликемии.
Противопоказания
- Повышенная чувствительность к вилдаглиптину и любым другим компонентам препарата;
- наследственная непереносимость галактозы, недостаточность лактазы, глюкозо-галактозная мальабсорбция;
- беременность, грудное вскармливание (в связи с недостатком соответствующих данных);
- сахарный диабет 1 типа;
- острый или хронический метаболический ацидоз (включая диабетический кетоацидоз в сочетании с комой или без таковой). Диабетический кетоацидоз должен корректироваться инсулинотерапией. Лактоацидоз (в том числе и в анамнезе);
- нарушения функции печени, включая пациентов с повышенной активностью «печёночных» ферментов (аланинаминотрансферазы (АЛТ) или аспартатаминотрансферазы (ACT) в 3 и более раз выше верхней границы нормы, (3 × ВГН);
- хроническая сердечная недостаточность (ХСН) IV функционального класса (ФК) по функциональной классификации Нью-Йоркской кардиологической ассоциации (NYHA) (ввиду отсутствия данных клинических исследований о применении вилдаглиптина у этой группы пациентов);
- детский возраст до 18 лет (эффективность и безопасность применения препарата не установлены).
С осторожностью
Рекомендуется с осторожностью применять препарат Галвус у пациентов с острым панкреатитом в анамнезе.
Поскольку опыт применения препарата Галвус у пациентов с терминальной стадией ХБП, находящихся на гемодиализе или проходящих процедуру гемодиализа, ограничен, препарат рекомендуется применять с осторожностью у данной категории пациентов. Поскольку данные о применении вилдаглиптина у пациентов с ХСН III ФК по классификации NYHA ограничены и не позволяют сделать окончательный вывод, рекомендуется с осторожностью применять препарат Галвус у пациентов данной категории.
Применение при беременности и в период грудного вскармливания
Достаточных данных по применению препарата Галвус у беременных нет, в связи с чем препарат противопоказан во время беременности. В доклинических исследованиях была выявлена репродуктивная токсичность при применении в высоких дозах, потенциальный риск для человека неизвестен.
Препарат Галвус противопоказан в период грудного вскармливания, поскольку неизвестно, проникает ли вилдаглиптин в грудное молоко у человека.
Способ применения и дозы
Дозу препарата Галвус следует подбирать индивидуально в зависимости от эффективности и переносимости.
Рекомендуемая доза препарата Галвус 50 мг 1 или 2 раза в день. Максимальная суточная доза препарата составляет 100 мг.
Дозу 50 мг/сут следует принимать 1 раз в день утром, дозу 100 мг/сут следует делить на 2 приёма — по 50 мг утром и вечером. В случае пропуска приёма препарата следует принять пропущенную дозу как можно скорее. При этом следует избегать принятия удвоенной дозы в один день.
Препарат Галвус принимают внутрь независимо от приёма пищи.
Рекомендуемая доза препарата в монотерапии или в составе комбинированной терапии с метформином, тиазолидиндионом или инсулином (в комбинации с метформином или без метформина), составляет 50 мг или 100 мг в сутки.
Рекомендуемая доза препарата Галвус в составе двойной комбинированной терапии с препаратами сульфонилмочевины составляет 50 мг 1 раз в сутки утром. В этой популяции пациентов эффективность препарата Галвус в дозе 100 мг в сутки была сходной с таковой в дозе 50 мг в сутки.
Рекомендованная доза препарата Галвус в составе тройной комбинированной терапии (вилдаглиптин + производные сульфонилмочевины + метформин) составляет 100 мг в сутки.
Если цели гликемического контроля не достигнуты на фоне применения максимальной суточной дозы 100 мг, следует рассмотреть возможность добавления к терапии препаратом Галвус других гипогликемических препаратов, таких, как метформин, производные сульфонилмочевины, тиазолидиндион или инсулин.
Пациенты с нарушениями функции почек
У пациентов с нарушением функции почек лёгкой степени (СКФ ≥60 мл/мин/1,73 м2) и средней степени с СКФ 50–60 мл/мин/1,73 м2 не требуется коррекции режима дозирования препарата. У пациентов с нарушением функции почек средней степени с СКФ 30–50 мл/мин/1,73 м2 и тяжёлой степени (СКФ <30 мл/мин/1,73 м2), включая терминальную стадию ХБП у пациентов, находящихся на гемодиализе или проходящих процедуру гемодиализа, препарат следует применять в дозе 50 мг 1 раз в сутки.
Пациенты в возрасте ≥65 лет
У пациентов пожилого возраста не требуется коррекции режима дозирования препарата Галвус.
Пациенты в возрасте ≤18 лет
Поскольку опыта применения препарата Галвус у детей и подростков младше 18 лет нет, не рекомендуется применять препарат у пациентов данной категории.
Побочное действие
При применении препарата Галвус в монотерапии или в комбинации с другими препаратами большинство нежелательных реакций были слабо выражены, имели временный характер и не требовали отмены терапии. Корреляции между частотой нежелательных явлений (НЯ) и возрастом, полом, этнической принадлежностью, продолжительностью применения или режимом дозирования не выявлено.
Частота развития ангионевротического отёка на фоне терапии препаратом Галвус составляла ≥1/10 000, <1/1 000 (градация «редко») и была сходной с таковой в контрольной группе. Наиболее часто случаи ангионевротического отёка отмечались при применении препарата в комбинации с ингибиторами ангиотензинпревращающего фермента. В большинстве случаев ангионевротический отёк был средней степени тяжести и разрешался самостоятельно в ходе продолжения терапии вилдаглиптином.
На фоне терапии препаратом Галвус редко отмечались нарушения функции печени (включая гепатит) бессимптомного течения. В большинстве случаев данные нарушения и отклонения показателей функции печени от нормы разрешились самостоятельно без осложнений после прекращения терапии препаратом. При применении препарата Галвус в дозе 50 мг 1 или 2 раза в сутки частота увеличения активности «печёночных» ферментов (АЛТ или ACT ≥3 × ВГН) составляла 0,2 % или 0,3 % соответственно (по сравнению с 0,2 % в контрольной группе). Увеличение активности «печёночных» ферментов в большинстве случаев было бессимптомным, не прогрессировало и не сопровождалось холестазом или желтухой.
НЯ сгруппированы в соответствии с классификацией органов и систем органов MedDRA. В пределах каждой группы органов и систем органов НЯ перечислены в порядке уменьшения частоты встречаемости. В пределах каждой группы частоты встречаемости НЯ указаны в порядке уменьшения тяжести.
Для оценки частоты встречаемости нежелательных явлений использовались следующие критерии: очень часто (≥1/10), часто (≥1/100, <1/10), нечасто (≥1/1 000, <1/100), редко (≥1/10 000, <1/1 000), очень редко (<1/10 000), отдельные сообщения (частота неизвестна).
При применении препарата Галвус в монотерапии
При применении препарата Галвус в дозе 50 мг 1 или 2 раза в сутки частота отмены терапии в связи с развитием нежелательных реакций (0,2 % или 0,1 % соответственно) была не выше таковой в группе плацебо (0,6 %) или препарата сравнения (0,5 %).
На фоне монотерапии препаратом Галвус в дозе 50 мг 1 или 2 раза в сутки частота развития гипогликемии без увеличения степени тяжести состояния составляла 0,5 % (2 пациента из 409) и 0,3 % (4 из 1082) соответственно, что сопоставимо с препаратом сравнения и плацебо (0,2 %).
Инфекционные и паразитарные заболевания: очень редко — инфекции верхних дыхательных путей, назофарингит.
Нарушения со стороны нервной системы: часто — головокружение; нечасто — головная боль.
Нарушения со стороны желудочно-кишечного тракта: нечасто — запор.
Нарушения со стороны сосудов: нечасто — периферические отёки.
Долгосрочные клинические исследования продолжительностью до 2 лет не выявили каких-либо дополнительных отклонений профиля безопасности или непредвиденных рисков при применении вилдаглиптина в монотерапии.
При применении препарата Галвус в дозе 50 мг 1 или 2 раза в сутки в комбинации с метформином
При применении препарата Галвус в дозе 50 мг/сут в комбинации с метформином частота отмены терапии в связи с развитием нежелательных реакций составляла 0,4 % (в группах вилдаглиптин (50 мг 2 раза в сутки) + метформин и плацебо + метформин случаев отмены терапии в связи с развитием нежелательных реакций не отмечалось).
При применении препарата Галвус в дозе 50 мг 1 или 2 раза в сутки в комбинации с метформином гипогликемия отмечалась в 0,9 % и 0,5 % случаев соответственно (в группе плацебо + метформин — 0,4 %). В группе применения препарата Галвус не наблюдалось развития гипогликемии тяжёлой степени.
Комбинированная терапия вилдаглиптин + метформин не влияла на массу тела пациентов.
Нарушения со стороны нервной системы: часто — тремор, головокружение, головная боль.
Нарушения со стороны желудочно-кишечного тракта: часто — тошнота.
Долгосрочные клинические исследования продолжительностью до 2 лет не выявили каких-либо дополнительных отклонений профиля безопасности или непредвиденных рисков при применении вилдаглиптина в комбинации с метформином.
Изучение применения комбинации вилдаглиптина и метформина в качестве стартовой терапии при сахарном диабете 2 типа не выявило отклонений профиля безопасности или непредвиденных рисков.
При применении препарата Галвус в дозе 50 мг/сут в комбинации с производными сульфонилмочевины
При применении препарата Галвус в дозе 50 мг/сут в комбинации с глимепиридом частота отмены терапии в связи с развитием нежелательных реакций составляла 0,6 % (по сравнению с 0 % в группе глимепирид + плацебо).
Частота развития гипогликемии у пациентов, получавших препарат Галвус в дозе 50 мг/сут вместе с глимепиридом, составила 1,2 % (по сравнению с 0,6 % в группе плацебо + глимепирид). В группе применения препарата Галвус не наблюдалось развития гипогликемии тяжёлой степени.
При применении препарата Галвус в рекомендованной дозе (50 мг/сут) в комбинации с глимепиридом не отмечалось увеличения массы тела.
Инфекционные и паразитарные заболевания: очень редко — назофарингит.
Нарушения со стороны желудочно-кишечного тракта: нечасто — запор.
Нарушения со стороны нервной системы: часто — тремор, головокружение, головная боль, астения.
При применении препарата Галвус в дозе 50 мг 1 или 2 раза в сутки в комбинации с производными тиазолидиндиона
При применении препарата Галвус в дозе 50 мг/сут в комбинации с пиоглитазоном частота отмены терапии в связи с развитием нежелательных реакций составляла 0,7 % (в группах вилдаглиптин 100 мг/сут + пиоглитазон и плацебо + пиоглитазон случаев отмены терапии в связи с развитием нежелательных реакций не отмечалось).
При применении препарата Галвус в дозе 50 мг/сут в комбинации с пиоглитазоном в дозе 45 мг развития гипогликемии не отмечалось; в группе вилдаглиптин (в дозе 50 мг 2 раза в сутки) + пиоглитазон (в дозе 45 мг) отмечалось развитие гипогликемии в 0,6 % случаев, а у пациентов, получавших плацебо + пиоглитазон в дозе 45 мг, — в 1,9 % случаев.
В группе применения препарата Галвус не наблюдалось развития гипогликемии тяжёлой степени. Среднее увеличение массы тела по сравнению с плацебо у пациентов, получавших препарат Галвус в дозе 50 мг 1 или 2 раза в сутки вместе с пиоглитазоном, составляло +0,1 кг или +1,3 кг соответственно.
При добавлении препарата Галвус в дозе 50 мг 1 или 2 раза в сутки к пиоглитазону в дозе 45 мг/сут частота развития периферических отёков составляла 8,2 % и 7% соответственно (по сравнению с 2,5 % на фоне монотерапии пиоглитазоном). Однако при начальной комбинированной терапии вилдаглиптином в дозе 50 мг 1 или 2 раза в сутки вместе с пиоглитазоном в дозе 45 мг/сут развитие периферических отёков наблюдалось у 3,5 % или 6,1 % пациентов соответственно (по сравнению с 9,3 % на фоне монотерапии пиоглитазоном в дозе 30 мг/сут).
Нарушения со стороны сосудов: часто — периферические отёки.
Нарушения со стороны обмена веществ и питания: часто — увеличение массы тела.
При применении препарата Галвус в дозе 50 мг 2 раза в сутки в комбинации с инсулином (с метформином или без него)
При применении препарата в комбинации с инсулином (в комбинации с метформином или без метформина) частота отмены терапии вследствие развития побочных эффектов была равна 0,3 %, в группе терапии вилдаглиптином, в группе плацебо случаев отмены терапии не было.
При применении препарата в комбинации с инсулином (в комбинации с метформином или без метформина) не отмечалось увеличения риска развития гипогликемии по сравнению с комбинацией плацебо + инсулин (14 % в группе вилдаглиптина и 16,4 % в группе плацебо). У 2 пациентов в группе вилдаглиптина и у 6 пациентов в группе плацебо развилась гипогликемия тяжёлой степени.
На момент завершения исследования препарат не оказывал влияния на среднюю массу тела (масса тела увеличена на +0,6 кг по сравнению с исходной в группе вилдаглиптина, а в группе плацебо осталась неизменной).
Нарушения со стороны нервной системы: часто — головная боль, неизвестно — астения.
Нарушения со стороны желудочно-кишечного тракта: часто — тошнота, гастроэзофагеальный рефлюкс; нечасто — диарея, метеоризм.
Общие расстройства и нарушения в месте введения: часто — озноб.
Нарушения со стороны обмена веществ и питания: часто — гипогликемия.
При применении препарата Галвус в дозе 50 мг два раза в день в комбинации с препаратами сульфонилмочевины и метформином
Случаев отмены препарата, связанных с НЯ в группе комбинированной терапии вилдаглиптином, метформином и глимепиридом, отмечено не было. В группе комбинированной терапии плацебо, метформином и глимепиридом частота НЯ составила 0,6 %.
Гипогликемия отмечалась часто в обеих группах (5,1 % в группе комбинированной терапии вилдаглиптином, метформином и глимепиридом и 1,9 % в группе комбинированной терапии плацебо, метформином и глимепиридом). В группе вилдаглиптина отмечен один эпизод гипогликемии тяжёлой степени.
На момент завершения исследования значимого влияния на массу тела выявлено не было (+0,6 кг в группе вилдаглиптина и -0,1 кг в группе плацебо).
Нарушения со стороны нервной системы: часто — головокружение, тремор, астения.
Нарушения со стороны обмена веществ и питания: часто — гипогликемия.
Нарушения со стороны кожи и подкожных тканей: часто — гипергидроз.
Пострегистрационные исследования
Во время проведения пострегистрационных исследований были выявлены следующие побочные реакции (поскольку сообщения получены в добровольном порядке от популяции неопределённого размера, достоверно определить частоту развития данных НЯ не представляется возможным, в связи с чем они классифицированы как частота неизвестна): гепатит (обратим при прекращении терапии), крапивница, панкреатит, буллезное и эксфолиативное поражение кожи, артралгия, в редких случаях выраженная, миалгия, повышение активности «печёночных» ферментов.
Если любые из указанных в инструкции побочных эффектов усугубляются, или Вы заметили любые другие побочные эффекты, не указанные в инструкции, сообщите об этом врачу.
Передозировка
Вилдаглиптин хорошо переносится при применении в дозе до 200 мг/сут.
При применении препарата в дозе 400 мг/сут может наблюдаться боль в мышцах, редко — лёгкие и транзиторные парестезии, лихорадка, отёки и транзиторное повышение активности липазы (выше ВГН в 2 раза). При увеличении дозы вилдаглиптина до 600 мг/сут возможно развитие отёков конечностей, сопровождающихся парестезиями и повышением активности креатинфосфокиназы, С-реактивного белка и миоглобина, активности ACT. Все симптомы передозировки и изменения лабораторных показателей обратимы после прекращения применения препарата.
Выведение препарата из организма с помощью диализа маловероятно. Однако основной гидролизный метаболит вилдаглиптина (LAY151) может быть удалён из организма путём гемодиализа.
Взаимодействие с другими лекарственными средствами
Вилдаглиптин обладает низким потенциалом лекарственного взаимодействия.
Поскольку вилдаглиптин не является субстратом ферментов цитохрома P450 (CYP), а также не ингибирует и не индуцирует эти ферменты, взаимодействие вилдаглиптина с лекарственными препаратами, которые являются субстратами, ингибиторами или индукторами P450 (CYP), маловероятно. При одновременном применении вилдаглиптин также не влияет на скорость метаболизма препаратов, являющихся субстратами ферментов: CYP1A2, CYP2C8, CYP2C9, CYP2C19, CYP2D6, CYP2E1 и CYP3A4/5.
Клинически значимого взаимодействия вилдаглиптина с препаратами, наиболее часто используемыми при лечении СД 2 типа (глибенкламидом, пиоглитазоном, метформином) или обладающими узким терапевтическим диапазоном (амлодипином, дигоксином, рамиприлом, симвастатином, валсартаном, варфарином) не установлено.
Тиазиды, глюкокортикостероиды, препараты гормонов щитовидной железы, симпатомиметики могут снижать гипогликемическое действие вилдаглиптина, как и других пероральных противодиабетических препаратов.
Частота развития ангионевротического отёка была выше при одновременном применении вилдаглиптина с ингибиторами ангиотензинпревращающего фермента, при этом была сходной с таковой в контрольной группе. В большинстве случаев ангионевротический отёк был средней степени тяжести и разрешался самостоятельно в ходе продолжения терапии вилдаглиптином.
Особые указания
В доклинических исследованиях при применении в дозах, в 200 раз превышающих рекомендуемые для человека, препарат не вызывал нарушений фертильности.
При необходимости инсулинотерапии препарат Галвус применяют только в комбинации с инсулином. Препарат противопоказан у пациентов с сахарным диабетом 1 типа или для лечения диабетического кетоацидоза.
Сердечная недостаточность
Поскольку данные о применении вилдаглиптина у пациентов с ХСН III ФК по классификации NYHA (см. Таблицу 1, приведённую ниже) ограничены и не позволяют сделать окончательный вывод, рекомендуется с осторожностью применять препарат Галвус у пациентов данной категории.
Не рекомендуется применение вилдаглиптина у пациентов с ХСН IV ФК по классификации NYHA, ввиду отсутствия данных клинических исследований о применении вилдаглиптина у пациентов этой группы.
Таблица 1. Нью-Йоркская классификация функционального состояния пациентов с хронической сердечной недостаточностью (в модификации), NYHA, 1964.
| Функциональный класс (ФК) | Ограничение физической активности и клинические проявления |
|---|---|
| I ФК | Ограничений в физической активности нет. Обычная физическая нагрузка не вызывает выраженного утомления, слабости, одышки или сердцебиения. |
| II ФК | Умеренное ограничение физической активности. В покое какие-либо патологические симптомы отсутствуют. Обычная физическая нагрузка вызывает слабость, утомляемость, сердцебиение, одышку и другие симптомы. |
| III ФК | Выраженное ограничение физической активности. Больной комфортно чувствует себя только в состоянии покоя, но малейшие физические нагрузки приводят к появлению слабости, сердцебиения, одышки и т. п. |
| IV ФК | Невозможность выполнять какие-либо нагрузки без появления дискомфорта. Симптомы сердечной недостаточности имеются в покое и усиливаются при любой физической нагрузке |
Нарушения функции печени
Поскольку в редких случаях при применении вилдаглиптина отмечалось повышение активности аминотрансфераз (как правило, без клинических проявлений), перед применением препарата Галвус, а также и регулярно в ходе первого года применения препарата (1 раз в 3 месяца), рекомендуется определять биохимические показатели функции печени. При выявлении повышения активности аминотрансфераз следует провести повторное исследование с целью подтверждения результата, а затем регулярно проводить определение биохимических показателей функции печени до их нормализации. Если превышение активности ACT или АЛТ в 3 или более раз выше ВГН подтверждено повторным исследованием, препарат рекомендуется отменить.
При развитии желтухи или других признаков нарушения функции печени на фоне применения препарата Галвус терапию препаратом следует немедленно прекратить. После нормализации показателей функции печени лечение препаратом возобновлять нельзя.
Гипогликемия
Известно, что препараты сульфонилмочевины могут провоцировать развитие гипогликемии. Существует риск развития гипогликемии при одновременном применении вилдаглиптина с препаратами сульфонилмочевины. При необходимости следует рассмотреть возможность снижения дозы препаратов сульфонилмочевины с целью минимизировать риск развития гипогликемии.
Острый панкреатит
Применение вилдаглиптина связано с риском развития острого панкреатита. Следует проинформировать пациента о симптомах, характерных для острого панкреатита. При подозрении на острый панкреатит вилдаглиптин следует отменить. Не следует возобновлять терапию вилдаглиптином, если острый панкреатит был подтверждён. У пациентов с острым панкреатитом в анамнезе применять вилдаглиптин следует с осторожностью.
Влияние на способность управлять транспортными средствами, механизмами
Исследования влияния препарата Галвус на способность управлять транспортными средствами или работать с механизмами не проводились. При развитии головокружения на фоне применения препарата пациентам не следует управлять транспортными средствами или работать с механизмами.
Форма выпуска
Таблетки, 50 мг.
По 7 или 14 шт. в блистере.
По 2, 4, 8, 12 блистеров вместе с инструкцией по применению в картонной пачке.
Хранение
В оригинальной упаковке, при температуре не выше 30 °C.
Хранить в недоступном для детей месте.
Срок годности
3 года.
Не применять по истечении срока годности.
Условия отпуска из аптек
Отпускают по рецепту
Производитель
 |
Международное непатентованное название? Вилдаглиптин |
 |
Действующее вещество: вилдаглиптин — 50,0мг; вспомогательные вещества: целлюлоза микрокристаллическая — 95,68мг; лактоза — 47,82мг; карбоксиметилкрахмал натрия — 4,0мг; магния стеарат — 2,5мг. |
 |
Противодиабетические средства — ингибиторы дипептидилпептидазы-4 |
 |
ПроизводителиНовартис Нева(Россия), Новартис Фармасьютика(Испания), Новартис Фарма Штейн(Швейцария) |
 |
Показания к применению Галвус таблетки 50мгСахарный диабет 2 типа (в сочетании с диетотерапией и физическими упражнениями): в качестве монотерапии в случае неэффективности диетотерапии и физических упражнений у пациентов с противопоказанием к применению метформина или в случае неэффективности метформина; в комбинации с метформином в качестве начальной медикаментозной терапии при недостаточной эффективности диетотерапии и физических упражнений; в составе двухкомпонентной комбинированной терапии с метформином, производным сульфонилмочевины, тиазолидиндионом или с инсулином в случае неэффективности диетотерапии, физических упражнений и монотерапии этими препаратами; в составе тройной комбинированной терапии: в комбинации с производными сульфонилмочевины и метформином, у пациентов, ранее получавших терапию производными сульфонилмочевины и метформином на фоне диетотерапии и физических упражнений и не достигших адекватного контроля гликемии; в составе тройной комбинированной терапии: в комбинации с инсулином и метформином, у пациентов, ранее получавших инсулин и метформин на фоне диетотерапии и физических упражнений и не достигших адекватного контроля гликемии. |
 |
Способ применения и дозировка Галвус таблетки 50мгДозу препарата следует подбирать индивидуально в зависимости от эффективности и переносимости.Рекомендуемая доза 50мг 1 или 2 раза в день. Максимальная суточная доза составляет 100мг.Дозу 50мг/сутки следует принимать 1 раз в день утром, дозу 100мг/сутки следует делить на 2 приема — по 50мг утром и вечером. В случае пропуска приема препарата следует принять пропущенную дозу как можно скорее. При этом следует избегать принятия удвоенной дозы в один день.Препарат Галвус принимают внутрь независимо от приема пищи.Рекомендуемая доза препарата в монотерапии или в составе комбинированной терапии с метформином, тиазолидиндионом или инсулином (в комбинации с метформином или без метформина), составляет 50мг или 100мг в сутки.Рекомендуемая доза Галвуса в составе двойной комбинированной терапии с препаратами сульфонилмочевины составляет 50мг 1 раз в сутки утром. В этой популяции пациентов эффективность препарата в дозе 100мг в сутки была сходной с таковой в дозе 50мг в сутки.Рекомендованная доза препарата в составе тройной комбинированной терапии (вилдаглиптин + производные сульфонилмочевины + метформин) составляет 100мг в сутки.Если цели гликемического контроля не достигнуты на фоне применения максимальной суточной дозы 100мг, следует рассмотреть возможность добавления к терапии препаратом других гипогликемических препаратов, таких, как метформин, производные сульфонилмочевины, тиазолидиндион или инсулин.Пациенты с нарушениями функции почек: у пациентов с нарушением функции почек легкой степени (СКФ более 60мл/мин/1,73м2) и средней степени с СКФ 50-60мл/мин/1,73м2 не требуется коррекции режима дозирования препарата. У пациентов с нарушением функции почек средней степени с СКФ 30- 50мл/мин/1,73м2 и тяжелой степени (СКФ менее 30мл/мин/1,73м2), включая терминальную стадию ХБП у пациентов, находящихся на гемодиализе или проходящих процедуру гемодиализа, препарат следует применять в дозе 50мг 1 раз в сутки.Пациенты в возрасте старше 65 лет: у пациентов пожилого возраста не требуется коррекции режима дозирования препарата.Пациенты в возрасте менее 18 лет: поскольку опыта применения препарата у детей и подростков младше 18 лет нет, не рекомендуется применять препарат у пациентов данной категории. |
 |
Противопоказания Галвус таблетки 50мгПовышенная чувствительность к вилдаглиптину и любым другим компонентам препарата.Наследственная непереносимость галактозы, недостаточность лактазы, глюкозо-галактозная мальабсорбция.Беременность, грудное вскармливание (в связи с недостатком соответствующих данных).Сахарный диабет 1 типа.Острый или хронический метаболический ацидоз (включая диабетический кетоацидоз в сочетании с комой или без таковой). Диабетический кетоацидоз должен корректироваться инсулинотерапией. Лактоацидоз (в том числе и в анамнезе).Нарушения функции печени, включая пациентов с повышенной активностью «печеночных» ферментов (аланинаминотрансферазы (АЛТ) или аспартатаминотрансферазы (ACT) в 3 и более раз выше верхней границы нормы.Хроническая сердечная недостаточность (ХСН) IV функционального класса (ФК) по функциональной классификации Нью-Йоркской кардиологической ассоциации (NYHA) (ввиду отсутствия данных клинических исследований о применении вилдаглиптина у этой группы пациентов).Детский возраст до 18 лет (эффективность и безопасность применения препарата не установлена).С осторожностью: рекомендуется с осторожностью применять препарат у пациентов с острым панкреатитом в анамнезе.Поскольку опыт применения препарата у пациентов с терминальной стадией ХБП, находящихся на гемодиализе или проходящих процедуру гемодиализа, ограничен, препарат рекомендуется применять с осторожностью у данной категории пациентов. Поскольку данные о применении вилдаглиптина у пациентов с ХСН III ФК по классификации NYHA ограничены и не позволяют сделать окончательный вывод, рекомендуется с осторожностью применять препарат Галвус у пациентов данной категории.Применение при беременности и в период грудного вскармливания: достаточных данных по применению препарата у беременных нет, в связи, с чем препарат противопоказан во время беременности. В доклинических исследованиях была выявлена репродуктивная токсичность при применении в высоких дозах, потенциальный риск для человека неизвестен.Препарат Галвус противопоказан в период грудного вскармливания, поскольку неизвестно, проникает ли вилдаглиптин в грудное молоко у человека. |
 |
Фармакологическое действиеВилдаглиптин — представитель класса стимуляторов островкового аппарата поджелудочной железы, селективно ингибирует фермент дипептидилпептидазу-4 (ДПП-4). Быстрое и полное ингибирование активности ДПП-4 (более 90%) вызывает повышение как базальной, так и стимулированной приемом пищи секреции глюкагоноподобного пептида 1 типа (ГПП-1) и глюкозозависимого инсулинотропного полипептида (ГИП) из кишечника в системный кровоток в течение всего дня.Повышая концентрацию ГПП-1 и ГИП, вилдаглиптин вызывает повышение чувствительности бета-клеток поджелудочной железы к глюкозе, что приводит к улучшению глюкозозависимой секреции инсулина. Фармакодинамика: при применении вилдаглиптина в дозе 50-100мг в сутки у пациентов с сахарным диабетом 2 типа (СД 2 типа) отмечается улучшение функции бета-клеток поджелудочной железы. Степень улучшения функции бета-клеток зависит от степени их исходного повреждения; так у лиц без СД (с нормальной концентрацией глюкозы в плазме крови) вилдаглиптин не стимулирует секрецию инсулина и не снижает концентрацию глюкозы. Повышая концентрацию эндогенного ГПП-1, вилдаглиптин увеличивает чувствительность альфа-клеток к глюкозе, что приводит к улучшению глюкозозависимой регуляции секреции глюкагона. Снижение повышенной концентрации глюкагона во время еды, в свою очередь, вызывает уменьшение инсулинорезистентности.Увеличение соотношения инсулин/глюкагон на фоне гипергликемии, обусловленное повышением концентрации ГПП-1 и ГИП, вызывает уменьшение продукции глюкозы печенью как во время, так и после приема пищи, что приводит к снижению концентрации глюкозы в плазме крови.Кроме того, на фоне применения вилдаглиптина отмечается снижение концентрации липидов в плазме крови после приема пищи, однако этот эффект не связан с его действием на ГПП-1 или ГИП и улучшением функции островковых клеток поджелудочной железы.Известно, что повышение концентрации ГПП-1 может приводить к замедлению опорожнения желудка, однако на фоне применения вилдаглиптина подобного эффекта не наблюдается.При применении вилдаглиптина у 5795 пациентов с СД 2 типа в течение 52 недель в монотерапии или в комбинации с метформином, производными сульфонилмочевины, тиазолидиндионом, или инсулином отмечалось достоверное длительное снижение концентрации гликированного гемоглобина (HbAlc) и глюкозы крови натощак.При применении комбинации вилдаглиптина и метформина в качестве начальной терапии у пациентов с сахарным диабетом 2 типа в течение 24 недель отмечалось дозозависимое снижение концентрации HbAlc в сравнении с монотерапией данными препаратами. Случаи развития гипогликемии были минимальны в обеих группах терапии.При применении вилдаглиптина в дозе 50мг 1 раз в сутки в течение 6 месяцев у пациентов с СД 2 типа с нарушением функции почек средней (скорость клубочковой фильтрации (СКФ) от 30 до 50мл/мин/1,73м2) или тяжелой (СКФ менее 30мл/мин/1,73м2) степени отмечалось клинически значимое снижение концентрации HbAlc по сравнению с плацебо.При применении вилдаглиптина в дозе 50мг 2 раза в сутки в комбинации с/без метформина и инсулином (средняя доза 41ЕД/сутки) было продемонстрировано снижение показателя HbAlc на 0,77% от исходного среднего значения 8,8% со статистически достоверной разницей с плацебо 0,72%. Частота гипогликемии в группе вилдаглиптина сравнима с таковой в группе плацебо. При применении вилдаглиптина в дозе 50мг 2 раза в сутки в комбинации с метформином (более 1500мг/сутки) и глимепиридом (более 4мг/сутки) было показано статистически значимое снижение уровня HbAlc на 0,76% от исходного среднего значения 8,8%.Фармакокинетика: при приеме внутрь натощак вилдаглиптин быстро всасывается, а его максимальная концентрация в плазме крови (Cmax) достигается через 1,75 часа после приема. При одновременном приеме с пищей скорость абсорбции вилдаглиптина снижается незначительно: отмечается уменьшение Cmax на 19% и увеличение времени ее достижения до 2,5 часов. Однако прием пищи не оказывает влияния на степень абсорбции и площадь под кривой «концентрация-время» (AUC).Вилдаглиптин быстро всасывается, а его абсолютная биодоступность после приема внутрь составляет 85%. Cmax и AUC в терапевтическом диапазоне доз увеличиваются примерно пропорционально дозе.Степень связывания вилдаглиптина с белками плазмы крови низкая (9,3%). Вилдаглиптин распределяется равномерно между плазмой крови и эритроцитами. Распределение вилдаглиптина происходит, предположительно, экстраваскулярно, объем распределения в равновесном состоянии после внутривенного введения (Vss) составляет 71л.Основным путем выведения вилдаглиптина является биотрансформация. В организме человека 69% дозы препарата подвергается биотрансформации. Основной метаболит — LAY151 (57% дозы) фармакологически неактивен и является продуктом гидролиза циано- компонента. Около 4% дозы препарата подвергаются амидному гидролизу.В доклинических исследованиях отмечается положительное влияние ДПП-4 на гидролиз вилдаглиптина. Вилдаглиптин метаболизируется без участия изоферментов цитохрома Р450. Вилдаглиптин не является субстратом изоферментов Р450 (CYP), не ингибирует и не индуцирует изоферменты цитохрома Р450.После приема препарата внутрь около 85% дозы выводится почками и 15% — через кишечник. Почечная экскреция неизмененного вилдаглиптина составляет 23%. При внутривенном введении средний период полувыведения достигает 2 часов, общий плазменный клиренс и почечный клиренс вилдаглиптина составляют 41л/ч и 13л/ч соответственно. Период полувыведения (T1/2) после приема внутрь составляет около 3 часов, независимо от дозы.Пол, индекс массы тела и этническая принадлежность не оказывают влияния на фармакокинетику вилдаглиптина.Пациенты с нарушением функции печени: у пациентов с нарушением функции печени легкой и средней степеней тяжести (6-9 баллов по шкале Чайлд-Пью) после однократного применения препарата отмечается снижение биодоступности вилдаглиптина на 20% и 8% соответственно. У пациентов с нарушением функции печени тяжелой степени (10-12 баллов по шкале Чайлд-Пью) биодоступность вилдаглиптина повышается на 22%. Увеличение или уменьшение максимальной биодоступности вилдаглиптина, не превышающее 30%, не является клинически значимым. Корреляции между степенью тяжести нарушений функции печени и биодоступностью препарата не выявлено.Пациенты с нарушением функции почек: у пациентов с нарушением функции почек легкой, средней или тяжелой степени AUC вилдаглиптина увеличивалась по сравнению со здоровыми добровольцами в 1,4, 1,7 и 2 раза соответственно. AUC метаболита LAY151 увеличивалась в 1,6, 3,2, и 7,3 раза, а метаболита BQS867 — в 1,4, 2,7, и 7,3 раза у пациентов с нарушением функции почек легкой, средней и тяжелой степеней соответственно. Ограниченные данные у пациентов с терминальной стадией хронической болезни почек (ХБП) указывают на то, что показатели данной группы схожи с таковыми у пациентов с нарушением функции почек тяжелой степени. Концентрация метаболита LAY151 у пациентов с терминальной стадией ХБП увеличивалась в 2-3 раза по сравнению с концентрацией у пациентов с нарушением функции почек тяжелой степени.При применении препарата у пациентов с нарушением функции почек может потребоваться коррекция дозы.Выведение вилдаглиптина при гемодиализе ограничено (через 4 часа после однократного приема составляет 3% при длительности процедуры более 3-4 часов).Применение у пациентов в возрасте старше 65 лет: максимальное увеличение биодоступности препарата на 32% (увеличение Cmax на 18%) у пациентов старше 70 лет не является клинически значимым и не влияет на ингибирование ДПП-4.Применение у пациентов в возрасте младше 18 лет: фармакокинетические особенности вилдаглиптина у детей и подростков младше 18 лет не установлены. |
 |
Побочное действие Галвус таблетки 50мгПри применении препарата в монотерапии или в комбинации с другими препаратами большинство нежелательных реакций были слабо выражены, имели временный характер и не требовали отмены терапии. Корреляции между частотой нежелательных реакций (HP) и возрастом, полом, этнической принадлежностью, продолжительностью применения или режимом дозирования не выявлено.Частота развития ангионевротического отека на фоне терапии препаратом составляла более 1/10000, но менее 1/1000 (градация «редко») и была сходной с таковой в контрольной группе. Наиболее часто случаи ангионевротического отека отмечались при применении препарата в комбинации с ингибиторами ангиотензинпревращающего фермента. В большинстве случаев ангионевротический отек был средней степени тяжести и разрешался самостоятельно в ходе продолжения терапии вилдаглиптином.На фоне терапии препаратом редко отмечались нарушения функции печени (включая гепатит) бессимптомного течения. В большинстве случаев данные нарушения и отклонения показателей функции печени от нормы разрешились самостоятельно без осложнений после прекращения терапии. При применении препарата в дозе 50мг 1 или 2 раза в сутки частота увеличения активности «печеночных» ферментов (АЛТ или ACT выше в 3 раза ВГН) составляла 0,2% или 0,3% соответственно (по сравнению с 0,2% в контрольной группе). Увеличение активности «печеночных» ферментов в большинстве случаев было бессимптомным, не прогрессировало и не сопровождалось холестазом или желтухой. HP сгруппированы в соответствии с классификацией органов и систем органов MedDRA. В пределах каждой группы органов и систем органов HP перечислены в порядке уменьшения частоты встречаемости. В пределах каждой группы частоты встречаемости HP указаны в порядке уменьшения тяжести.Для оценки частоты встречаемости нежелательных реакций использовались следующие критерии: очень часто (более 1/10), часто (более 1/100, но менее 1/10), нечасто (более 1/1000, но менее 1/100), редко (более 1/10000, но менее 1/1000), очень редко (менее 1/10000), частота неизвестна (поскольку сообщения получены в добровольном порядке от популяции неопределенного размера, достоверно определить частоту развития данных HP не представляется возможным, в связи, с чем они классифицированы как частота неизвестна).При применении препарата в монотерапии: при применении препарата в дозе 100мг в сутки частота отмены терапии в связи с развитием нежелательных реакций (0,3%) была не выше таковой в группе плацебо (0,6%) или препарата сравнения (0,5%).На фоне монотерапии препаратом в дозе 100мг в сутки частота развития гипогликемии без увеличения степени тяжести состояния составляла 0,4%, что сопоставимо с препаратом сравнения и плацебо (0,2%).Масса тела не изменялась по сравнению с исходной в клинических исследованиях, когда вилдаглиптин 100мг в сутки применяли в качестве монотерапии (-0,3кг и -1,3кг в группах препарата Галвус и плацебо соответственно).Инфекционные и паразитарные заболевания: очень редко — инфекции верхних дыхательных путей, назофарингит. Нарушения со стороны обмена веществ и питания: нечасто — гипогликемия. Нарушения со стороны нервной системы: часто — головокружение; нечасто — головная боль.Нарушения со стороны желудочно-кишечного тракта: нечасто — запор. Нарушения со стороны сосудов: нечасто — периферические отеки.Нарушения со стороны скелетно-мышечной и соединительной ткани: нечасто — артралгия.Долгосрочные клинические исследования продолжительностью до 2 лет не выявили каких-либо дополнительных отклонений профиля безопасности или непредвиденных рисков при применении вилдаглиптина в монотерапии.При применении препарата Галвус в дозе 100мг в сутки в комбинации с метформином: при применении препарата в дозе 100мг/сутки в комбинации с метформином или плацебо в сочетании с метформином случаев отмены терапии в связи с развитием нежелательных реакций не отмечалось.При применении препарата в дозе 100мг в сутки в комбинации с метформином гипогликемия отмечалась в 1% случаев (в группе плацебо + метформин — нечасто (0,4%)) в группе применения препарата не наблюдалось развития гипогликемии тяжелой степени.Масса тела не изменялась по сравнению с исходной в клинических исследованиях при применении комбинации препарата 100мг в сутки и метформина (+0,2 кг и -1,0 кг в группах препарата Галвус и плацебо соответственно). Нарушения со стороны обмена веществ и питания: часто — гипогликемия.Нарушения со стороны нервной системы: часто — тремор, головная боль, головокружение; нечасто — повышенная утомляемость.Нарушения со стороны желудочно-кишечного тракта: часто — тошнота. Долгосрочные клинические исследования продолжительностью до 2 лет не выявили каких-либо дополнительных отклонений профиля безопасности или непредвиденных рисков при применении вилдаглиптина в комбинации с метформином.Изучение применения комбинации вилдаглиптина и метформина в качестве стартовой терапии при сахарном диабете 2 типа не выявило отклонений профиля безопасности или непредвиденных рисков. При применении препарата Галвус в дозе 50мг/сутки в комбинации с производными сульфонилмочевины: при применении препарата в дозе 50мг/сутки в комбинации с глимепиридом частота отмены терапии в связи с развитием нежелательных реакций составляла 0,6% (по сравнению с 0% в группе глимепирид + плацебо).Частота развития гипогликемии у пациентов, получавших препарат в дозе 50мг/сутки вместе с глимепиридом, составила 1,2% (по сравнению с 0,6% в группе плацебо + глимепирид). В группе применения препарата Галвус не наблюдалось развития гипогликемии тяжелой степени.Масса тела не изменялась по сравнению с исходной в клинических исследованиях когда препарат в дозе 50мг один раз в сутки добавляли к глимепириду (-0,1кг и -0,4кг в группах препарата Галвус и плацебо соответственно). Инфекционные и паразитарные заболевания: очень редко — назофарингит. Нарушения со стороны обмена веществ и питания: часто — гипогликемия. Нарушения со стороны желудочно-кишечного тракта: нечасто — запор. Нарушения со стороны нервной системы: часто — тремор, головокружение, головная боль, астения.При применении препарата в дозе 100мг в сутки в комбинации с тиазолидиндионом: при применении препарата в дозе 100мг/сутки + тиазолидиндион и плацебо + тиазолидиндион случаев отмены терапии в связи с развитием нежелательных реакций не отмечалось.При применении препарата Галвус в дозе 100мг в сутки + пиоглитазон отмечалось развитие гипогликемии в 0,6% случаев, а у пациентов, получавших плацебо + пиоглитазон, — в 1,9% случаев. В группе применения препарата не наблюдалось развития гипогликемии тяжелой степени.В исследовании применения препарата Галвус в качестве дополнительной терапии к пиоглитазону абсолютное увеличение массы тела в группе плацебо и препарата Галвус 100мг в сутки составило 1,4 и 2,7кг соответственно.При добавлении препарата Галвус в дозе 100мг в сутки к пиоглитазону в дозе 45мг/сутки частота развития периферических отеков составляла 7% (по сравнению с 2,5% на фоне монотерапии пиоглитазоном).Нарушения со стороны сосудов: часто — периферические отеки.Нарушения со стороны обмена веществ и литания: часто — увеличение массы тела; нечасто — гипогликемия.Нарушения со стороны нервной системы: нечасто — головная боль, астения.При применении препарата Галвус в дозе 50мг 2 раза в сутки в комбинации с инсулином (с метформином или без него): при применении препарата в комбинации с инсулином (в комбинации с метформином или без метформина) частота отмены терапии вследствие развития побочных эффектов была равна 0,3%, в группе терапии вилдаглиптином, в группе плацебо случаев отмены терапии не было.При применении препарата в комбинации с инсулином (в комбинации с метформином или без метформина) не отмечалось увеличения риска развития гипогликемии по сравнению с комбинацией плацебо + инсулин (14% в группе вилдаглиптина и 16,4% в группе плацебо). У 2 пациентов в группе вилдаглиптина и у 6 пациентов в группе плацебо развилась гипогликемия тяжелой степени.На момент завершения исследования препарат не оказывал влияния на среднюю массу тела (масса тела увеличилась на +0,6кг по сравнению с исходной в группе вилдаглиптина, а в группе плацебо осталась неизменной).Нарушения со стороны нервной системы: часто — головная боль, озноб.Нарушения со стороны желудочно-кишечного тракта: часто — тошнота, гастроэзофагеальный рефлюкс; нечасто -диарея, метеоризм.Нарушения со стороны обмена веществ и питания: часто — гипогликемия.При применении препарата Галвус в дозе 50мг два раза в день в комбинации с препаратами сульфонилмочевины и метформином: случаев отмены препарата, связанных с HP в группе комбинированной терапии вилдаглиптином, метформином и глимепиридом, отмечено не было. В группе комбинированной терапии плацебо, метформином и глимепиридом частота отмены препарата, связанной с HP, составила 0,6%.Гипогликемия отмечалась часто в обеих группах (5,1% в группе комбинированной терапии вилдаглиптином, метформином и глимепиридом и 1,9% в группе комбинированной терапии плацебо, метформином и глимепиридом). В группе вилдаглиптина отмечен один эпизод гипогликемии тяжелой степени.На момент завершения исследования значимого влияния на массу тела выявлено не было (+0,6кг в группе вилдаглиптина и -0,1кг в группе плацебо).Нарушения си стороны нервной системы: часто — головокружение, тремор.Нарушения со стороны обмена веществ и питания: часто — гипогликемия.Нарушения со стороны кожи и подкожных тканей: часто — гипергидроз.Общие расстройства и нарушения в месте введения: часто — астения. Пострегистрационные исследования: во время проведения пострегистрационных исследований были выявлены следующие побочные реакции (поскольку сообщения получены в добровольном порядке от популяции неопределенного размера, достоверно определить частоту развития данных HP не представляется возможным, в связи с чем они классифицированы как «частота неизвестна»).Нарушения со стороны желудочно-кишечного тракта: частота неизвестна — панкреатит.Нарушения со стороны печени и желчевыводящих путей: частота неизвестна — гепатит (разрешившийся самостоятельно после отмены лекарственного препарата), повышение активности «печеночных» ферментов (разрешившееся самостоятельно после отмены лекарственного препарата). Нарушения со стороны скелетно-мышечной и соединительной ткани: частота неизвестна — миалгия.Нарушения со стороны кожи и подкожных тканей: частота неизвестна — крапивница, эксфолиативное и буллезное поражения кожи, включая буллезный пемфигоид.Если любые из указанных в инструкции побочных эффектов усугубляются, или Вы заметили любые другие побочные эффекты, не указанные в инструкции, сообщите об этом врачу. |
 |
ПередозировкаВилдаглиптин хорошо переносится при применении в дозе до 200мг/сутки.При применении препарата в дозе 400мг/сутки может наблюдаться боль в мышцах, редко — легкие и транзиторные парестезии, лихорадка, отеки и транзиторное повышение активности липазы (выше ВГН в 2 раза). При увеличении дозы вилдаглиптина до 600мг/сутки возможно развитие отеков конечностей, сопровождающихся парестезиями и повышением активности креатинфосфокиназы, С-реактивного белка и миоглобина, активности ACT. Все симптомы передозировки и изменения лабораторных показателей обратимы после прекращения применения препарата.Выведение препарата из организма с помощью диализа маловероятно. Однако основной гидролизный метаболит вилдаглиптина (LAY151) может быть удален из организма путем гемодиализа. |
 |
Взаимодействие Галвус таблетки 50мгВилдаглиптин обладает низким потенциалом лекарственного взаимодействия.Поскольку вилдаглиптин не является субстратом ферментов цитохрома Р450 (CYP), а также не ингибирует и не индуцирует эти ферменты, взаимодействие вилдаглиптина с лекарственными препаратами, которые являются субстратами, ингибиторами или индукторами Р450 (CYP), маловероятно. При одновременном применении вилдаглиптин также не влияет на скорость метаболизма препаратов, являющихся субстратами ферментов: CYP1А2, CYP2C8, CYP2C9, CYP2C19, CYP2D6, CYP2E1 и CYP3A4/5. Клинически значимого взаимодействия вилдаглиптина с препаратами, наиболее часто используемыми при лечении СД 2 типа (глибенкламидом, пиоглитазоном, метформином) или обладающими узким терапевтическим диапазоном (амлодипином, дигоксином, рамиприлом, симвастатином, валсартаном, варфарином) не установлено.Тиазиды, глюкокортикостероиды, препараты гормонов щитовидной железы, симпатомиметики могут снижать гипогликемическое действие вилдаглиптина, как и других пероральных противодиабетических препаратов.Частота развития ангионевротического отека была выше при одновременном применении вилдаглиптина с ингибиторами ангиотензинпревращающего фермента, при этом была сходной с таковой в контрольной группе. В большинстве случаев ангионевротический отек был средней степени тяжести и разрешался самостоятельно в ходе продолжения терапии вилдаглиптином. |
 |
Особые указанияВ доклинических исследованиях при применении в дозах, в 200 раз превышающих рекомендуемые для человека, препарат не вызывал нарушений фертильности.При необходимости инсулинотерапии препарат применяют только в комбинации с инсулином. Препарат противопоказан у пациентов с сахарным диабетом 1 типа или для лечения диабетического кетоацидоза.Сердечная недостаточность: поскольку данные о применении вилдаглиптина у пациентов с ХСН III ФК по классификации NYHA ограничены и не позволяют сделать окончательный вывод, рекомендуется с осторожностью применять препарат у пациентов данной категории.Не рекомендуется применение вилдаглиптина у пациентов с ХСН IV ФК по классификации NYHA, ввиду отсутствия данных клинических исследований о применении вилдаглиптина у пациентов этой группы.Нью-Йоркская классификация функционального состояния пациентов с хронической сердечной недостаточностью (в модификации), NYHA, 1964: ФК I — ограничений в физической активности нет. Обычная физическая нагрузка не вызывает выраженного утомления, слабости, одышки или сердцебиения.ФК II — умеренное ограничение физической активности. В покое какие-либо патологические симптомы отсутствуют. Обычная физическая нагрузка вызывает слабость, утомляемость, сердцебиение, одышку и др. симптомы.ФК III — выраженное ограничение физической активности. Больной комфортно чувствует себя только в состоянии покоя, но малейшие физические нагрузки приводят к появлению слабости, сердцебиения, одышки и т.п.ФК IV — невозможность выполнять какие-либо нагрузки без появления дискомфорта. Симптомы сердечной недостаточности имеются в покое и усиливаются при любой физической нагрузкеНарушения функции печени: поскольку в редких случаях при применении вилдаглиптина отмечалось повышение активности аминотрансфераз (как правило, без клинических проявлений), перед применением препарата, а так же и регулярно в ходе первого года применения препарата (1 раз в 3 месяца), рекомендуется определять биохимические показатели функции печени. При выявлении повышения активности аминотрансфераз следует провести повторное исследование с целью подтверждения результата, а затем регулярно проводить определение биохимических показателей функции печени до их нормализации. Если превышение активности ACT или АЛТ в 3 или более раз выше ВГН подтверждено повторным исследованием, препарат рекомендуется отменить.При развитии желтухи или других признаков нарушения функции печени на фоне применения препарата терапию препаратом следует немедленно прекратить. После нормализации показателей функции печени лечение препаратом возобновлять нельзя. Гипогликемия: известно, что препараты сульфонилмочевины могут провоцировать развитие гипогликемии. Существует риск развития гипогликемии при одновременном применении вилдаглиптина с препаратами сульфонилмочевины. При необходимости следует рассмотреть возможность снижения дозы препаратов сульфонилмочевины с целью минимизировать риск развития гипогликемии.Острый панкреатит: применение вилдаглиптина связано с риском развития острого панкреатита. Следует проинформировать пациента о симптомах, характерных для острого панкреатита. При подозрении на острый панкреатит вилдаглиптин следует отменить. Не следует возобновлять терапию вилдаглиптином, если острый панкреатит был подтвержден. У пациентов с острым панкреатитом в анамнезе применять вилдаглиптин следует с осторожностью.Влияние на способность управлять транспортными средствами и механизмами: исследования влияния препарата на способность управлять транспортными средствами или работать с механизмами не проводились. При развитии головокружения на фоне применения препарата пациентам не следует управлять транспортными средствами или работать с механизмами. |
 |
Условия храненияХранить в недоступном для детей месте при температуре не выше 30°C в оригинальной упаковке. |
Состав
В таблетках содержится активное вещество вилдаглиптин – 50 мг.
Дополнительные компоненты: МКЦ, лактоза безводная, карбоксиметилкрахмал натрия, магния стеарат.
Форма выпуска
Выпускается Galvus в форме круглых гладких таблеток светлого оттенка с маркировками «NVR» и «FB».
Расфасованы таблетки в блистеры по 7 или 14 штук, по 2, 4, 8, 12 блистеров в упаковке.
Фармакологическое действие
Препарат обладает гипогликемическим действием.
Фармакодинамика и фармакокинетика
Вещество вилдаглиптин является стимулятором островкового аппарата поджелудочной железы, способным селективно ингибировать фермент дипептидилпептидазу-4. Полноценность этого процесса повышает базальную и стимулированную приёмом пищи секрецию глюкагоноподобного пептида 1-го типа и глюкозозависимого инсулинотропного полипептида из кишечника в системный кровоток. При этом увеличивается концентрация данных компонентов и чувствительность β-клеток поджелудочной железы к глюкозе, улучшающие глюкозозависимую секрецию инсулина.
Повышенный уровень глюкагоноподобного пептида 1-го типа может вызвать замедление опорожнения желудка, но при лечении вилдаглиптином такого эффекта не отмечено.
Монотерапия Галвусом или комбинированный прием с Метформином, тиазолидиндионом, производными сульфонилмочевины или инсулином на длительное время понижает концентрацию гликированного гемоглобина и глюкозы крови. Также подобное лечение сводит к минимуму случаи возникновения гипогликемии.
При приёме внутрь абсорбция вилдаглиптина происходит достаточно быстро. Абсолютная биодоступность вещества составляет 85%. Концентрация активного компонента в плазме зависит от назначенной дозировки.
После приёма лекарства натощак его присутствие в плазме крови обнаруживается спустя 1 ч 45 мин. Приём пищи оказывает незначительное влияние на действие препарата. Внутри организма основная часть Галвуса преобразуется в метаболиты, выведение которых преимущественно осуществляется при помощи почек.
Показания к применению
Основным показанием к назначению Галвуса является лечение сахарного диабета типа 2 в моно- или различных формах комбинированной терапии, например, с Метформином, Тиазолидиндионом производными сульфонилмочевины или инсулином в вариациях, установленных лечащим врачом.
Противопоказания к применению
Данное лекарство не рекомендуется принимать при:
- чувствительности к вилдаглиптину и другим составляющим препарата;
- наследственной непереносимости галактозы, недостаточности лактазы глюкозо-галактозной мальабсорбции;
- некоторых случаях хронической сердечной недостаточности;
- возрасте до 18 лет.
С осторожностью назначается лечение пациентам, страдающим тяжёлыми нарушениями функций печени и почечной недостаточности.
Побочные эффекты
Обычно при лечении Галвусом не возникает тяжёлых нежелательных реакций, требующих отмены препарата.
Однако не следует исключать развития аллергических проявлений, особенно в виде отёчности. Возможно нарушение функций печени, отклонения в показателях нормальной деятельности данного органа. Также сохраняется вероятность возникновения гипогликемии, головных болей, головокружения, нарушений пищеварения и общих расстройств организма.
Инструкция на Галвус (Способ и дозировка)
Данное лекарство предназначено для приёма внутрь и не зависит от употребления еды. Дозировка препарата подбирается индивидуально, с учётом эффективности и особенностей организма.
Как сообщает инструкция по применению Галвуса, при проведении монотерапии, а также в двухкомпонентной комбинированной терапии с тиазолидиндионом, метформином или инсулином назначают суточную дозу 50-100мг. У пациентов с тяжёлой формой сахарного диабета типа 2, получающих инсулин, суточная доза таблеток Галвус составляет 100мг.
Назначение тройной комбинированной терапии, то есть: вилдаглиптин + метформин + производные сульфонилмочевины предполагает приём 100мг в сутки. При этом обычно принимают по 50мг – утром и вечером.
Двухкомпонентная комбинированная терапия с производными сульфонилмочевины включает суточную дозировку Галвуса, составляющую 50мг, которую принимают с утра. Возможно увеличение суточной дозы до 100 мг, но обычно этого не требуется.
Если наблюдается недостаточный клинический эффект при приёме максимальной суточной дозировки 100 мг, то чтобы контролировать развитие гликемии дополнительно, можно принимать другие гипогликемические средства, например: метформин, тиазолидиндион, производные сульфонилмочевины или инсулин.
Передозировка
Как правило, пациенты хорошо переносят Галвус при назначении суточной дозировки до 200 мг.
При назначении суточной дозы 400 мг возможно развитие мышечных болей, лихорадки, отёчности и других нежелательных симптомов.
Увеличение суточной дозы до 600 мг может вызвать развитие отёчности конечностей, значительное повышение концентрации АЛТ, КФК, С-реактивного белка и миоглобина. Обычно после прекращения приёма лекарства все симптомы передозировки устраняются.
Взаимодействие
Установлено, что для Галвуса характерен низкий потенциал лекарственного взаимодействия. Поэтому допускается его приём одновременно субстратами, ингибиторами, индукторами цитохрома Р450 и различными ферментами.
Возможно значимое взаимодействие данного лекарства с препаратами, также назначаемыми при сахарном диабете типа 2, например: Глибенкламидом, Метформином, Пиоглитазоном. Результаты одновременного применения с лекарственными средствами, имеющими узкий терапевтический диапазон – Амлодипином, Дигоксином, Рамиприлом, Симвастатином, Валсартаном, Варфарином не установлено, поэтому подобную комбинированную терапию следует проводить с осторожностью.
Условия продажи
Препарат отпускают по рецепту.
Условия хранения
Для хранения Галвуса предназначено сухое место, не доступное для детей, при температуре до 30 C.
Срок годности
3 года.
Аналоги
Совпадения по коду АТХ 4-го уровня:
Основные аналоги представлены препаратами Галвус Мет и Вилдаглиптин.
Отличие Галвус и Галвус Мет
Важным отличием Галвус Мет от Галвуса является то, что в его состав включено вещество – метформин. При этом многочисленные исследования показали, что эффективность лечения при приёме этого препарата и по отдельности таблеток Метформина и Вилдаглиптина значительно выше и достаточно удобно. Кроме того, пациенты, принимающие комбинированное лекарство не отмечают случаев тяжёлой гипогликемии.
Алкоголь и Галвус
Во время лечения данным препаратом необходимо отказаться от употребления спиртного, так как это может вызвать развитие нежелательных симптомов и осложнение течения заболевания.
Отзывы о Галвусе
Как показывают отзывы о Галвусе на форумах, посвящённых медицинской тематике, данный препарат является одним из первых, который назначают при постановке диагноза сахарный диабет. Возможно, по этой причине пациенты не знают точно, как правильно принимать лекарство, чтобы терапия оказалась эффективной.
Кроме того, на начальной стадии течения заболевания далеко не все пациенты серьёзно относятся к другим рекомендациям специалиста: соблюдение диеты, контроль массы тела и так далее, поэтому часто подобные назначения просто не выполняются. В результате, люди начинают ощущать нежелательные симптомы и «скачки» уровня сахара, пытаясь всё это нормализовать только приёмом лекарственного средства.
Те, кто сразу серьёзно отнёсся к лечению, отмечают хорошую эффективность Галвуса. Пациенты рассказывают, что им пришлось изменить некоторые привычки, но на качестве жизни это особо не отразилось. Другой проблемой является высокая стоимость препарата, из-за чего больные вынуждены искать ему замену.
Известно, что нормальное самочувствие пациентов, страдающих сахарным диабетом, требует определённых усилий от самого человека. Только благодаря комплексному подходу к своему здоровью можно хорошо себя чувствовать и не допустить или существенно замедлить развитие нарушений в работе нервной и сердечно-сосудистой системы, которые, к сожалению, часто сопровождают диабетиков.
Цена Галвуса, где купить
Цена Галвус 50 мг, 28 штук, в аптеках Москвы варьируется в пределах 720-800 руб.
- Интернет-аптеки РоссииРоссия
ЗдравСити
-
Галвус таблетки 50мг 28штООО Новартис Нева
-
Галвус Мет таблетки п/о плён. 50мг+850мг 30штООО Новартис Нева
-
Галвус Мет таблетки п/о плён. 50мг+1000мг 30штООО Новартис Нева
-
Галвус Мет таблетки п/о плён. 50мг+500мг 30штООО Новартис Нева
Аптека Диалог
-
Галвус Мет таблетки 50мг+1000мг №30Новартис Нева ООО
-
Галвус Мет таблетки 50+500мг №30Novartis
-
Галвус таблетки 50мг №28Novartis/Новартис Нева
-
Галвус Мет таблетки 50мг+1000мг №30Novartis
-
Галвус Мет таблетки 50+850мг №30Novartis Farma/Новартис Нева ООО
показать еще
