
Приготовление буферных растворов — распространенная процедура в химических и биохимических лабораториях. Буферный раствор — это смесь слабой кислоты и сопряженного с ней основания или слабого основания и сопряженной с ним кислоты. Буферные растворы позволяют поддерживать стабильный уровень pH другого раствора, смешанного с буферным. Если в раствор попадает небольшое количество другой кислоты или щелочи или они образуются в ходе химической реакции, буферный раствор не допустит изменения значения pH всего раствора. Поэтому буферы очень полезны в разных задачах, где требуется поддержание стабильного уровня pH. Другие названия буферных растворов — также pH-буферы, водород-ионные буферы или просто буферы.
Например, в крови человека содержатся естественные буферы для поддержания рН в диапазоне от 7,35 до 7,45 — именно при таком уровне могут нормально действовать энзимы. Поскольку активность энзимов зависит от pH, при проведении биохимических анализов необходимо поддержание этого параметра на постоянном уровне. Буферные растворы применяются в шампунях для предотвращения раздражения кожи, в детских лосьонах для противодействия росту бактерий, а также в растворах для контактных линз, чтобы уровень pH жидкости оставался совместимым с уровнем рН глаз.
Приготовление буферного раствора состоит из нескольких этапов: взвешивание компонентов, растворение компонентов, корректировка pH и дополнение до заданного объема. Поскольку итоговое значение pH в буфере зависит от соотношения кислоты и основания, чрезвычайно важно взвешивать компоненты с высокой точностью. Все используемое оборудование (весы, пипетки и рН-метр) должно быть правильно откалибровано и иметь достаточную точность.
Видео: приготовление буферного раствора — простота, удобство и точность
Для приготовления буферного раствора нужны время и особая тщательность, иначе раствор не будет действовать так, как требуется. Если качество продукции или биохимических анализов зависит от качества буферных растворов, ошибки при приготовлении буферов недопустимы.
Посмотрите видео и узнайте, как можно сэкономить время и силы, если готовить буферные растворы с помощью технических весов и рН-метров МЕТТЛЕР ТОЛЕДО.
Перейдите в один из следующих разделов, чтобы узнать больше:
- Как готовить буферные растворы? Стандартная процедура.
- Секреты работы с буферными растворами
- Как действуют буферные растворы?
- Разновидности буферных растворов
- На что следует обращать внимание при приготовлении буферного раствора
- Преимущества универсальных буферных растворов
- Дополнительные советы по приготовлению и использованию буферных растворов
- Запросить консультацию по процедурам приготовления буферных растворов
- Сложности при приготовлении буферных растворов
- Специальное решение МЕТТЛЕР ТОЛЕДО для точного и удобного приготовления буферного раствора
- Руководство по эффективному взвешиванию
- Приготовление буферных растворов: оптимизированный рабочий процесс с комплексным управлением данными
- Как обеспечить правильную калибровку pH-метра
- Часто задаваемые вопросы о приготовлении буферных растворов
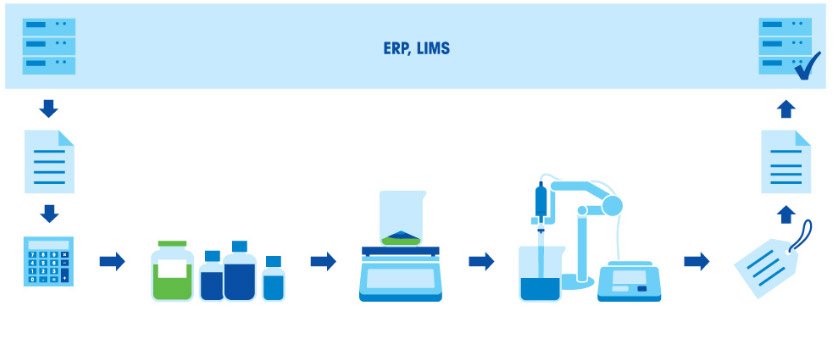
Как готовить буферные растворы? Стандартная процедура
Приготовление буферного раствора состоит из нескольких этапов: расчет концентрации и количества компонентов в соответствии с назначением и нужным объемом раствора; взвешивание компонентов; растворение компонентов; корректировка pH; дополнение до заданного объема; маркировка и документирование; использование раствора или его сохранение для применения в будущем.
- Выберите рецептуру из базы данных.
- Рассчитайте количество компонентов, указанных в рецептуре, в соответствии с требуемым объемом буферного раствора.
- Взвесьте компоненты и поместите их в сосуд.
- Растворите компоненты в подходящем растворителе (обычно в воде).
- С помощью рН-метра проверьте и скорректируйте значение pH.
- Долейте раствор до необходимого объема.
- Переместите раствор в бутыль для хранения и нанесите на нее соответствующую маркировку.
- Задокументируйте результаты.

Нужна помощь?
Буферные растворы чрезвычайно важны для решения многих практических задач. Однако приготовление буферного раствора требует много времени и сил и должно производиться тщательно, чтобы избежать ошибок. Если вам нужна помощь в приготовлении буферных растворов или при подборе весов с требуемым уровнем точности, проконсультируйтесь с экспертами МЕТТЛЕР ТОЛЕДО. В случае сомнений обратитесь к специалистам.

Сложности при приготовлении буферных растворов
Хотя простейший буферный раствор состоит только из кислоты, основания и воды, лаборантам часто приходится готовить по несколько буферных растворов в день. Обычно буферы состоят из 2–5 компонентов, но иногда их количество достигает 20. В обычной лаборатории может быть более 20 рецептур, рассчитанных на приготовление одного литра буферного раствора.
Расчеты буферных растворов
Если в базе данных содержится несколько десятков рецептур для буферных растворов, лаборанту нужно сначала удостовериться, что рецептура выбрана правильно. Если нужный объем буферного раствора отличается от одного литра, необходимо пересчитать количество всех компонентов и записать в журнал новые значения. Ошибки в вычислениях или при записи новых значений могут привести к неправильному уровню pH в буферном растворе. При ручной системе записи данных риск ошибок выше.
Взвешивание и запись результатов взвешивания
При взвешивании компонентов буферного раствора необходимо строго следить за соответствием типа и количества компонентов. Фактическую массу всех компонентов нужно записывать в журнал. Если запись результатов выполняется вручную или вводом значений в компьютер, необходимо внимательно следить за отсутствием ошибок.
Возможно, придется использовать несколько весов в зависимости от требуемой массы компонентов буферного раствора и минимальной массы, с которой могут работать весы. Это усложняет процесс и снижает эффективность.
Правильная работа с рН-метрами
Проверка уровня pH буферного раствора чрезвычайно важна. Но если рН-метр не откалиброван и не поддерживается в надлежащем состоянии, измерения рН могут быть неточными. Использование буферного раствора с неправильным pH может серьезно повлиять на последующий анализ или качество продукта.
Документация
Полученный буферный раствор должен быть правильно промаркирован. На этикетке нужно указать все данные, необходимые для предотвращения ошибок. Важно знать срок годности, чтобы буферный раствор сохранял эффективность. Все данные, связанные с приготовлением буферного раствора, нужно внести в журнал. Эта информация должна храниться для справки и обеспечения прослеживаемости.

Специальное решение МЕТТЛЕР ТОЛЕДО для точного и удобного приготовления буферного раствора
Технические весы МЕТТЛЕР ТОЛЕДО XSR упрощают приготовление буферных растворов и значительно снижают нагрузку на лаборантов.
Хранение рецептур
Непосредственно на весах можно хранить до 50 рецептур буферных растворов в виде методов взвешивания. Сохранив на весах наиболее часто используемые рецептуры буферных растворов, можно быстро найти нужный метод и начать работу. Весы выдают пошаговые инструкции, поэтому лаборантам легко следить за тем, на каком этапе приготовления буферного раствора они находятся.
Автоматические расчеты и подсказки по взвешиванию
При запуске метода вводится требуемый объем буферного раствора, и массы компонентов рассчитываются автоматически. В ходе взвешивания компонентов на индикаторе SmartTrac графически отображается соответствие фактической массы целевому значению. Цветная полоска становится зеленой, как только масса добавляемого компонента войдет в заданный диапазон допусков. Это позволяет специалистам быстрее и точнее дозировать компоненты.
Эффективные процессы и автоматическая регистрация данных
После добавления каждого компонента весы регистрируют фактический результат взвешивания, а затем выполняют автоматическое тарирование. Записывать результаты вручную не нужно, поэтому эффективность работы повышается. Весы можно настроить на автоматическую печать результатов взвешивания после добавления всех компонентов.
Удобное измерение pH
pH-метры SevenExcellence МЕТТЛЕР ТОЛЕДО — лучший выбор для точного измерения pH. В этих удобных приборах с сенсорным управлением предусмотрена возможность прямого измерения одним нажатием кнопки и реализована технология цифрового управления датчиками (ISM).
Точность измерения рН определяется качеством буферных растворов, используемых для калибровки. МЕТТЛЕР ТОЛЕДО предлагает большой выбор калибровочных буферных растворов высокого качества для самых разных задач.

Guide: Biological Buffer Preparation
Discover how you can make your buffer preparation process easy and reliable.
Download the guide and get useful tips and hints to help improve the productivity of your preparation process, ensure quality standards and traceability for buffer solutions.
- Step-by-step SOP user guidance and accessible buffer recipes directly on the balance screen improves workflows
- Accurate weighing in compounds is vital for the quality of buffer solutions
- Exact and reliable pH measurement is important for the correct preparation of buffers
- Using and operating pipettes the correct way helps to ensure that pH buffer is properly adjusted
- Automatic calculation, labeling and reporting ensure safe data transfer and data traceability

Приготовление буферных растворов: оптимизированный рабочий процесс с комплексным управлением данными
Технические весы МЕТТЛЕР ТОЛЕДО Excellence (XPR и XSR) и pH-метры SevenExcellence можно подключить к фирменному лабораторному ПО LabX и создать полностью оптимизированную систему, обладающую рядом важных преимуществ:
- Автоматические расчеты и документирование
- Все результаты сохраняются в защищенной базе данных.
- Полная прослеживаемость
- Централизованное управление задачами, пользователями и приборами.
Соответствие требованиям части 11 раздела 21 CFR (Свода федеральных постановлений США)
LabX обеспечивает полное управление данными, практически исключая их ручную регистрацию. В автоматическом режиме можно даже печатать этикетки с подробной информацией. Благодаря централизованной базе данных все подключенные пользователи и приборы имеют доступ к одним и тем же сохраненным СОП для приготовления буферных растворов. Таким образом, все лаборанты будут выполнять приготовление буферных растворов с одними и теми же настройками и параметрами. Все результаты и метаданные процесса автоматически сохраняются в защищенной базе данных, что обеспечивает полную прослеживаемость.

Как обеспечить правильную калибровку pH-метра
Для точной калибровки рН-метра нужны качественные калибровочные буферные растворы с известным уровнем рН. МЕТТЛЕР ТОЛЕДО предлагает ряд качественных буферных растворов, в том числе максимально точные растворы, соответствующие требованиям NIST/DIN.
Буферные растворы поставляются с сертификатами испытаний, которые помогут обеспечить соответствие нормативным требованиям и прослеживаемость. В ассортименте МЕТТЛЕР ТОЛЕДО найдутся буферные растворы для любых задач — как технические буферы, так и растворы, сертифицированные аккредитованными организациями.
Часто задаваемые вопросы о приготовлении буферных растворов
Выберите вопрос:
- Что такое анализатор влажности?
- Как работает анализатор влажности?
- Какой анализатор влажности лучше всего подойдет для моих задач?
- Что необходимо учитывать при выборе анализатора влажности?
- Почему при выборе анализатора влажности важно учитывать тип образца?
1. Как повысить эффективность взвешивания при приготовлении буферных растворов?
Пользователи могут сохранять собственные методы взвешивания на весах МЕТТЛЕР ТОЛЕДО XPR/XSR. Для приготовления буферных растворов подходит метод «Простое взвешивание по рецептурам с шаблоном». На весах в виде рецептуры хранятся данные о всех компонентах раствора с заданной массой и интервалом допуска. После запуска метода весы будут выдавать указания по каждому этапу процедуры. Не нужно постоянно сверяться с рецептурой, а этапы процедуры невозможно перепутать. Результаты взвешивания сохраняются автоматически и в конце могут быть распечатаны. Можно сэкономить время, избавившись от необходимости записывать все результаты взвешивания вручную.
2. Какие весы лучше всего подходят для приготовления буферных растворов?
Выбор весов зависит от индивидуальных требований. Нужно знать минимальную и максимальную массу взвешиваемых компонентов, а также требуемую точность взвешивания (допуски или допустимые погрешности). МЕТТЛЕР ТОЛЕДО предлагает бесплатную услугу по подбору весов с учетом специфики применения. Бесплатную рекомендацию по весам можно получить у местного представителя МЕТТЛЕР ТОЛЕДО. В рамках этой же услуги можно определить, соответствуют ли требованиям имеющиеся весы.
- GWP Recommendation
3. При приготовлении буферного раствора нужно записывать очень много данных. Как избежать ошибок? Нужно найти безошибочное решение.
Прежде всего подключите к весам сканер штрихкодов. Это позволит в электронном виде регистрировать идентификаторы образцов, номера партий, номера заказов и т. д. Во-вторых, подключите к весам принтер. В конце процедуры взвешивания принтеры МЕТТЛЕР ТОЛЕДО P-5x могут автоматически распечатывать результаты, метаданные, а также дату и время. Другой вариант — подключить весы к лабораторному программному обеспечению LabX, которое обеспечивает комплексное управление данными, включая создание настраиваемых отчетов, которые можно отправлять прямо в системы LIMS или ERP.
4. Как обеспечить надежность при измерении pH буферного раствора?
Показания рН-метра будут точными, если прибор регулярно проходит калибровку и проверку. Ознакомьтесь с руководством МЕТТЛЕР ТОЛЕДО и решениями для калибровки рН-метров. Посмотрите видео «Калибровка pH-метров — удобное руководство».
5. Что делать, если компонент был добавлен в большем объеме, чем нужно?
Если вы случайно добавили слишком большое количество какого-то компонента, необязательно выбрасывать всю смесь. Можно добавить к ней дополнительное количество других компонентов. Но при ручном расчете объемов это может быть непросто, и риск ошибок высок. Не исключено также, что потребуется добавить очень небольшое количество вещества, и имеющиеся весы не подойдут для его взвешивания. Могут потребоваться вторые весы с более высокой точностью и меньшей минимальной массой. Если весы подключены к LabX, то ПО сможет выполнить все необходимые перерасчеты и проследить за ходом процедуры.
- Apteka.uz
- Лекарства
- БЛОКИУМ
БЛОКИУМ
Цены БЛОКИУМ в аптеках
Информация, опубликованная на сайте, предназначена для специалистов. Не занимайтесь самолечением. Обязательно проконсультируйтесь со специалистом, чтобы не нанести вред своему здоровью!
Информация о доставке:
Аптеки, предлагающие услуги доставки, выделены в каталоге обозначением «Доставка».
Свяжитесь по контактному телефону с аптекой, помеченной таким образом, и уточните стоимость и срок доставки заказа.
Как правило, аптека отправляет заказ в течение 1 часа.
БЛОКИУМ инструкция
Фармакотерапевтическая группа:
— Нестероидное противовоспалительное средство
Показания к применению
Острый «кризис воспалительного ревматизма. Воспаление в поясничном отделе. Невралгия в шейном отделе и множественные нейрорадиколиты.
Все показания к применению
Противопоказания
— гиперчувствительность к активным компонентам.
— гиперчувствительность к аспирину и другим НПВС.
— активная гастродуоденальная язва,
— серьезная почечная недостаточность,
— тяжелая печеночная недостаточность,
— декомпенсаторная сердечная недостаточность, серьезная гипертония,
— системный микоз,
— активный туберкулез,
— подагра,
— гепатит А, В и не-А не-В и другие вирусные болезни,
— лечение антикоагулянтами,
— беременность и кормление грудью.
Все противопоказания
Диклофенак выводится путем метаболизма в печени. Выводится с мочой (65 %) и желчью (35 %), как метаболиты, соединенные с серой или глюкуронидом. Никакие изменения в фармакокинетике не были обнаружены в гериатрии или у пациентов с печеночной или почечной недостаточностью. Бетаметазон’циркулирует в связанном состоянии с плазменными белками (64 %), и его период полураспада — 5.6 часов.
Витамин В12 в основном распределяется в клетках паренхимы печени, которые составляют его основное место хранения.
Блокиум В12 содержит диклофенак, поэтому он должен применяться с осторожностью пациентами с почечными, сердечными или печеночными нарушениями и пациентами, которые подвергались серьезным операциям или сниженным ОЦК, Диклофенак может обострять картину у пациентов с порфирией печени, а также может обострять картину у пациентов, которые страдают от бронхиальной астмы.
Медицинское наблюдение необходимо у пациентов c дуоденальной язвой, язвенным колитом или болезнью Крона.
Пациенты с нарушениями свертывающей системы крови или те, кто принимает оральные антикоагулянты, должны также быть под контролем.
Также Блокиум В12 содержит бетаметазон, он должен применяться с осторожностью пациентами с дивертикулитом, кишечным анастомозом, язвой желудка, язвенным колитом, нарывами или другими гнойными заболеваниями, гипертонией, остеопоро^ом и миастенией Гравис.
Он должен также использоваться с осторожностью пациентами с глазным простым герпесом, эмоциональной нестабильностью или психотическими тенденциями, и гипертиреоидизмом.
При длительной терапии с Блокиум В12 необходимо проверить кровь, функции почек и печени.
Пожилые пациенты должны принимать самую низкую эффективную дозу Блокиум В12.
Блокиум В12 содержит диклофенак, и подобно любому другому нестероидному противовоспалительному препарату, он может привести, в любое время во время лечения к кровотечению из ЖКТ. Это, вероятнее всего, может случиться у пожилых пациентов. Диклофенак редко приводит к серьезной анафилактической или анафилактоидной аллергической реакции. *
Бетаметазон может маскировать некоторые признаки инфекции.
Пациенты при лечении с Блокиум В12 не должны подвергнуться процедурам иммунизации из-за изменения иммунного ответа. Он также с осторожностью должен применяться пациентами с подозрением на инфекцию из-за странгилоидоза, поскольку он может предрасполагать к распространению признаков, и может быть опасным для жизни.
Пациенты со скрытым туберкулезом или реактивностью к туберкулину должны быть тщательно проверены, так как болезнь может начаться. Эти пациенты должны получить хемопрофилактику в течение долгосрочного лечения.
Кортикоидная терапия в течение больше чем двух недель несет риск недостаточности надпочечников из-за ингибирования АКТГ, что может привести к атрофии надпочечника. В этих случаях, недостаточность надпочечника может быть вызвана стрессами (операция, серьезный травматизм, серьезные инфекции) или как последствие внезапного прерывания лечения стероидами. В этих ситуациях, быстрое применение кортикостероидов предотвратит недостаточность надпочечников. Если долгосрочное кортикостероидное лечение должно быть прервано, рекомендуется уменьшать дозу постепенно.
Блокиум В12 не должен быть предписан в течение беременности, если нет обязательных причин, особенно в течение последних трех месяцев беременности, так как диклофенак может приостанавливать утробные сокращения и вызывать раннее закрытие артериального канала. Кортикостероиды частично задерживаются в грудном молоке.
В/м введение: по 3-6 мл (1 или 2 флакона растворенный растворителем) ежедневно, через глубокое в/м введение.
Блокиум В12 может вызывать различные неблагоприятные реакции в следующих системах:
Желудочно-кишечный тракт: эпигастральная боль, тошнота, рвота, диарея, брюшная дистензия, желудочные кровотечения, желудочная или дуоденальная язва с или без кровоизлияния или перфорация.
Центральная нервная система: конвульсии, увеличенное внутричерепное давление, головокружение, мигрень и сонливость.
Печень: иногда, увеличение трансам иназ и редко гепатит с или без желтухи.
Кожа: иногда, эритема и сыпь кожи. Редко крапивница. Описаны изолированные случаи синдрома Стевенса Джонсона, многообразная эритема и токсический эпидермолиз. Задержка рубцевания ран, хрупкость кожи, петехии и экхимозы, покраснение лица. Некоторые неблагоприятные реакции зависят от его парентерального применения: гиперпигментация или гипорпигментация, кожная и подкожная атрофия, абсцесс.
Почка: изолированные случаи острой почечной недостаточности, гематурия и протеурия
Система кроветворения: Изолированные случаи лейкопении, гемолитическая анемия и агранулоцитоз.
Сердечно-сосудистая система: Артериальная гипертония, сердечная недостаточность и трепетание.
Водно-электролитические нарушения: задержание натрия, отек, потеря калия и гипокалиемический алкалоз.
Костно-мышечная система: мышечная слабость, стероидная миопатия, потеря мышечной массы, остеопороз, компрессионные переломы позвоночника, некроз головки бедренной кости и/или патологический перелом длинных костей.
Эндокринная система: нарушения менструаций, болезнь Иценко — Кушинга, прерывание роста у детер, надпочечниковая недостаточность, особенно в случаях травматизма, операций, системных болезней. Уменьшение толерантности к углеводам и увеличение потребности в инсулине и оральных сахаропонижающих препаратов у диабетических пациентов.
Органы чувств: субкапсулярная катаракта, повышение внутриглазного давления, глаукома, боль при ярком освещении и звон в ушах.
Метаболизм: отрицательный баланс азота из-за белкового катаболизма.
Совместное применение блокиум В12 с другими систематическими нестероидными противовоспалительными лекарствами может привести к появлению неблагоприятных эффектов.
Рекомендуется строгий контроль над показателями свертываемости крови у пациентов, принимающих оральные антикоагулянты.
Блокиум В12 может ингибировать фармакологическое действие диуретиков. Он может также увеличивать задержку калия из-за ингибирования диуретиков.
Следует с осторожностью назначать препарат, за 24 часа или после дозы метотрексата, так как это может увеличивать его уровень в крови и его токсичность.
Совместное применение Блокиум В12 и солей лития может увеличивать уровень в крови последнего без признаков передозировки.
Блокиум В12 содержит стероид (бетаметазон), в последующем это необходимо учитывать.
Препятствующиеся ассоциации: в/в эритромицин, астемизол, бепридил, галофантрин, пентамидин, терфенадин, сультоприд, винкамин — риск трепетания, мерцания желудочков (гипокалием1р , брадикардия, и удлинение QT интервала увеличивает риск развития этой аритмии).
Ассоциации, которые требуют осторожного использования: антиаритмические препараты которые располагают к развитию трепетания, мерцания желудочков, такие как: амиодарон, брителий, дизо пирам ид, квинидин, соталол. Дигиталы увеличивают риск токсических явлений в случае гипокалиемии. Вещества, которые приводят к гипокалиемии при в/в введении — это амфотерицин В, тиазидные диуретики и слабительные.
Ацетилсалициловая кислота: кортикостероиды увеличивают выведение салицилата. Поэтому, существует риск передозировки салицилата после прерывания лечения с кортикостероидами. Рекомендует приспособить дозу салицилата после прекращения лечения кортикостероидами.
Оральные антикоагулянты и парентеральный гепарин: в этих случаях рекомендуется усилить наблюдение за пациентом, так как кортикостероиды увеличивают риск кровоизлияния. Этот эффект может быть заметным, когда высокие дозы кортикостероидов принимаются в течение периодов больше, чем десять дней.
Инсулин, метформин, сульфаниламиды, снижающие уровень глюкозы в крови: в этих случаях рекомендуется усилить наблюдение за уровнем глюкозы у пациента и регулировать дозу антидиабетических препаратов во время и после лечения кортикостероидами.
Изониазид: уровень изониазида в крови уменьшается, когда изиниазид применяется совместно с кортикостероидами. В этих случаях рекомендуется клинический и микробиологический контроль.
Фенобарбитал, фенитоин, примидон, карбамазепин, рифабутин, рифампицин: все они — энзимные индукторы, которые уменьшают эффективность кортикостероидов. Поэтому, рекомендуется регулировать дозу препарата в течение и после лечения с этими лекарствами.
Ассоциации, которые следует принять во внимание:
Антигипертензивные препараты: кортикостероиды уменьшают их терапевтические эффекты.
Альфа интерферон: кортикостероиды могут прерывать его терапевтическое действие.
Вакцины с уменьшенными живущими микробами: там существует риск развития системных заболеваний, которые могут, в конечном счете, быть смертельными. Риск будет больший у пациентов предварительно иммуннодепрессированных, как последствие основной болезни. Предпочтительно использовать вакцины с бездействующими микроорганизмами.
Форма выпуска: Контейнеры по 3 и 5 флаконов + 3 и 5 ампул с растворителем.
Лекарственная форма: Лиофилизат для приготовления раствора для инъекций N3; N5 (флаконы) в комплекте с растворителем 3 мл N3; N5 (ампулы).
СОСТАВ:
Каждая ампула с растворителем содержит:
Активные вещества: Диклофенак натрия 75 мг Бетаметазона натрия фосфат 2,63 мг
Вспомогательные вещества: Бензиловый спирт 0,06 г Динатрия фосфат, безводный 0,98 мг Натрия гидроксид q.s. рН 8,4 Метипарабен 2,40 мг Пропилпарабен 0,45 мг Пропиленгликоль 576,00 мг Дистиллированная вода q.s. 3,0 мл
Каждый флакон с лиофилизатом содержит: Гидроксокобаламин 10,00 мг
Вспомогательные вещества: Маннитол 87,00 мг
Диклофенак — нестероидный противовоспалительный препарат, чей механизм действия подобен таковому же у НПВС, не полностью выяснен. Он способен ингибировать синтез простогландинов — это часть его фармакологического действия.
Бетаметазон — глюкокортикоид, который подавляет воспаление через несколько механизмов: ингибирует образование различных факторов воспалительной реакции, среди них, вазоактивные и хемотактические факторы. Он уменьшает секрецию липофильных и ‘протеолитических ферментов, уменьшает выброс лейкоцитов к участкам повреждения и уменьшает фиброз; наконец, он также влияет на количество и иммунные реакции, которые зависят от лимфоцитов.
Витамин В12 необходим для клеточного роста и репродукции. Его производный, метилкобаламин, требуется для формирования метионина и S-аденозилметионина из гомоцистеина. Дефицит витамина В12 может причинять необратимый вред нервной системе, с прогрессивной опухолью нейрона, демиелонизацией и смерти на нервной почве.
Хранить в сухом и вентилируемом месте, при температуре 15 и 30°С Хранить в недоступном для детей месте.
СРОК ГОДНОСТИ:
24 месяца. Не использовать после истечения срока годности, указанного на упаковке.
В случае передозировки желудок должен быть освобожден, вызывая рвоту или путем промывания желудка. Прием активизированного угля, чтобы уменьшить поглощение или прервать внутрипеченочный цикл диклофенака. Применение антиацидных или других подщелачивающих веществ мочи, таких как дифунисал или сулиндак, усиливают выведение нестероидных противовоспалительных веществ.
Гемодиализ, который необходим в некоторых случаях лечения вторичного почечного воспаления при интоксикации нестероидными противовоспалительными веществами, может ускорять выведение диклофенака.
При появлении конвульсий, диазепам или другие бензодиазепины назначаются внутривенно. Кровоизлияние или язва желудка должны приниматься во внимание. Витамин К назначается в случае гипопротромбинемии.
В случае передозировки, следует обратиться в ближайший госпиталь или токсикологический центр.
Формы выпуска

Цены: от 550 000 сум
Цены: от 1 сум


Зарегистрирован ли препарат БЛОКИУМ в реестре препаратов Узбекистана?
Да, препарат зарегистирован в реестре препаратов Узбекистана.
Кто производитель препарата БЛОКИУМ и какая страна происхождения?
Препарат БЛОКИУМ производится в стране Аргентина производителем Laboratorios Casasco S.A.I.C..
Для лечения чего используется данный препарат?
Описание препарата «БЛОКИУМ» на сайте Apteka.uz может быть упрощенной или дополненной версией официальной инструкции по применению.
Перед покупкой и использованием препарата вам необходимо проконсультироваться с врачом и ознакомиться с утверждённой производителем аннотацией.
- А
- Б
- В
- Г
- Д
- Е
- Ё
- Ж
- З
- И
- Й
- К
- Л
- М
- Н
- О
- П
- Р
- С
- Т
- У
- Ф
- Х
- Ц
- Ч
- Ш
- Щ
- Э
- Ю
- Я
- A-Z
- 0-9
Существует
два способа приготовления буферных
растворов:
1) смешение
растворов сопряжённых кислоты и
основания.
2) частичная нейтрализация слабой кислоты
— щёлочью или слабого основания – сильной
кислотой.
Второй способ широко используется в
лабораторной практике при приготовлении
буферных смесей с использованием рН –
метров, когда нейтрализацию ведут до
нужного значения рН, величину которого
контролируют по прибору.
1) Приготовить фосфатный буфер объемом
Vбуф. с данным значением рН методом
смешения растворов дигидрофосфата и
гидрофосфата натрия:






Схема смешения.
Определим объемы Vк и V0
исходных растворов сопряжённых кислоты
и основания, если известны их концентрации
Ск(нач) и С0(нач) .
Для расчёта необходимо составить два
уравнения, первое из которых очевидно
Vбуф = V0 + Vк ,
(6)
а второе получим на основе уравнения
(4).
Поскольку количества солей в буферном
растворе равно их количеству в
соответствующих объёмах исходных
растворов, то n0
/ в буферном растворе = С0(нач)
×
V0
nк
/ в буферном растворе = Ск(нач)
×
Vк
Подставляя эти величины в уравнение
(4), находим второе уравнение связи между
искомыми объёмами:

Решая систему из двух уравнений (6 — 7)
или (6 – 8), находим объёмы растворов Vк
и V0, при смешении которых образуется
буферный раствор с заданным значением
рН.
2) Этот же буферный раствор можно
приготовить путём частичной нейтрализации
фосфорной кислоты щёлочью, например
NaOH.
Пусть в растворе фосфорной кислоты
объёмом V литров и молярной концентрацией
С (Н3РО4) моль/л содержится
n
(Н3РО4) = С×V
= а моль Н3РО4. Фосфатный
буфер содержит смесь двух солей NaH2PO4
/ Na2HPO4, поэтому расчет
нейтрализации кислоты проводят в два
этапа: перевод а моль фосфорной
кислоты в дигидрофосфат – ион (I этап)
и далее частичный перевод дигидрофосфат-иона
в гидрофосфат-ион до нужного значения
рН (II этап):

Необходимое количество щёлочи х
для осуществления второго этапа
определяют по уравнению (4):
рН = рК2 + lg (n0/nк)
= рК2 + lg (x/(a-x)).
Общее количество NaOH равно nобщ.(I+II
этапы) = а + х, и если в исходныйраствор
фосфорной кислоты добавляют кристаллический
NaOH, то его масса равна m (NaOH) = (a+x) ×
M (NaOH), а если добавляют раствор щёлочи,
то его объём равен Vщёлочи =
(а-х) / С (NaOH).
V. Расчёт изменения рН при добавлении к фосфатному буферному раствору небольших добавок сильной кислоты или щёлочи, а также при его разбавлении.
Пусть исходный буферный раствор объёмом
V содержит nк
моль кислоты и n0
моль сопряжённого основания, тогда в
соответствии с уравнением (4): рН(нач.)
= рК2 + lg (n0/nк).
а) добавка сильной кислоты НnX:
n
(Н+) = С (1/nНnX) ×
Vдоб. = х моль и согласно (1)
конечные количества компонентов буферной
смеси равны: n0(кон.)
= n0
– х
nк(кон.)
= nк
+ х .
Величина рН конечного состояния
рассчитывается по формуле:
рН(кон.) = рК2 + lg [(n0
— x)/(nк
+ х)] (9)
причём происходит небольшой сдвиг в
кислую область рН(нач.) >
рН(кон.).
б) добавка щёлочи M(OH)n: n(ОН—)
= С(1/n M(OH)n) ×
Vдоб. = х моль и согласно (2)
конечные количества компонентов буферной
смеси равны: n0(кон.)
= n0
+ х
nк(кон.)
= nк
— х
Величина рН конечного состояния
рассчитывается по формуле:
рН(кон.) = рК2 + lg [(n0
+ x)/(nк
— х)] (10)
причём происходит небольшой сдвиг в
щелочную область рН(нач.) <
рН(кон.).
Замечание: n0
и nк
относятся к объёму буферного раствора,
в который сделаны добавки.
в) При разбавлении буферного раствора
водой исходные концентрации его
компонентов С0 и Ск уменьшаются
в одинаковое число раз, поэтому их
отношение в уравнении (3) остаётся
неизменным и, следовательно, величина
рН сохраняется.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Сегодня имеется масса самых разных измерительных устройств, которые призваны помогать в контроле смесей, жидкой продукции и даже домашних пищевых продуктов. Для того чтобы можно было правильно настроить все это многообразие приборов, как раз и используются так называемые калибровочные буферные растворы.
Сами по себе, они представлены в виде растворов, имеющих определенную устойчивую концентрацию ионов водорода. При этом уровень рН их практически остается неизменным после добавления в них небольшого количества сильного основания или сильных кислот, либо при концентрировании или разбавлении.
При всем многообразии, буферные растворы (они же составы, смеси и системы) принято разделять на два основных типа:
- Из слабых кислот или их солей, образованных сильными основаниями;
- Из слабых оснований и их солей, образованных сильными кислотами.
Выбор того или иного варианта буферной системы будет зависеть от типа измерительного прибора, от поставленных задач.
Использование
В водохранилищах, аквариумах, в бассейнах, пищепроме и многих других сферах активно сегодня используются солемерные устройства, которые призваны выявлять степень минерализации жидких составов, уровень их кислотности, определять температуру. Таким образом можно всегда подкорректировать состав воды или иного раствора, улучшить потребительские показатели, вкусовые характеристики и т.д.
Чтобы TDS-метры работали корректно, прибегают к специальным растворам, которые носят название буферных. Они отличаются всегда стабильным содержанием ионов. Рекомендуется проводить с их помощью калибровку измерительного оборудования перед каждым сеансом замера. В этом случае можно получить максимально точный результат.
Большинство пользователей предпочитают для проведения калибрования рН-метров приобретать готовые составы. Они могут предлагаться как в жидком концентрированном, так и в разведенном виде, а также порошками. Следует для получения раствора использовать только дистиллированную воду, поскольку она лишена примесей и минералов, способных повредить точности замеров. Рекомендуется также строго следовать инструкции от производителя буферного раствора.
Рекомендации по использованию калибровочных растворов
Приведенные ниже рекомендации помогут с максимальной эффективностью использовать калибровочные составы:
- Использовать состав следует по возможности сразу же после вскрытия упаковки. Только свежий раствор гарантирует высокую точность замеров;
- После того, как упаковка была вскрыта, следует записать на ней точное время вскрытия;
- Флакон следует плотно закрывать, если в нем остался состав. Строго запрещается возвращать раствор обратно во флакон, даже если он не был использован;
- Также строго нужно следить за тем, чтобы в калибровочные составы не проникали никакие посторонние примеси и тем более – загрязнение;
- Хранение буферных калибровочных растворов нужно осуществлять в условиях комнатной температуры и без доступа прямых солнечных лучей;
- Перед тем, как провести замер, нужно тщательно промыть все датчики. Саму калибровку запрещается проводить в исходном флаконе с составом. Исключение допустимо лишь в том случае, если того требует инструкция от производителя;
- Недопустимо использование загрязненных растворов и с истекшим сроком хранения;
- Калибровку рН-электродов следует проводить не просто регулярно, а ежедневно – перед тем, как приступить к их использованию;
- Если электроды долгое время не использовались или были подвергнуты чистке – их также следует откалибровать;
- Во время проведения калибровки следует уточнить показатели углового коэффициента и нулевой точки электрода;
- Калибровка осуществляется как минимум по двум точкам. Если нужно получить более широкий диапазон замеров, то калибровка осуществляется по трем точкам и больше.
Общей рекомендацией будет – приобретать калибровочные растворы только у проверенных продавцов и производителей, которые уже получили хорошую репутацию на рынке.
Растворы слабой кислоты и ее соли (или слабого основания и его соли), концентрация водородных ионов в которых почти не меняется при введении в них сильней кислоты или сильного основания, называются буферными растворами. Они играют большую роль в регулировании жизненных процессов в организмах животных и растений, широко применяются в лабораторной практике. [c.257]
Буферные растворы широко используются в научно-исследовательской практике и технологии. Они служат для поддержания постоянного значения pH среды при проведении процессов, направление и скорость которых зависят от pH. Регулирование pH растворов позволяет направлять различного рода процессы в желаемую сторону и синтезировать вещества с заданными свойствами. [c.324]
Часто в буферный раствор для регулирования силы подвижной фазы добавляют нейтральные соли. Особой популярностью пользуется нитрат натрия, поскольку он не вызывает коррозии аппаратуры. Галогенид-ионы оказывают вредное влияние на нержавеющую сталь, и поэтому их лучше не применять. [c.39]
На панели лабораторного рН-метра установлены три, а иногда четыре ручки управления 1) переключатель положений Выключено и Включено 2) регулятор калибровки или стандартизации для установки на нуль, чтобы рН-метр показывал правильную величину, когда электроды погружены в стандартный буферный раствор 3) температурный компенсатор для регулирования чувствительности согласно зависимости потенциала от температуры. Некоторые рН-метры имеют также переключатель шкалы, что позволяет прибору давать показания во всем интервале шкалы pH (обычно от О до 14) или в огра- [c.105]
При проведении качественных реакций большое значение имеет регулирование и поддержание определенных значений pH. Для определения pH раствора наносят стеклянной палочкой каплю анализируемого раствора на универсальную индикаторную бумагу и сравнивают появившуюся окраску с цветной шкалой. В зависимости от необходимого значения pH в анализируемый раствор по каплям при перемешивании вносят раствор кислоты, основания, гидролизующейся соли, буферный раствор и другие компоненты, контролируя значение pH. [c.126]
Если буферный раствор должен быть наиболее эффективным в отношении регулирования кислотности, его pH должен не только мало зависеть от добавления небольших количеств сильной кислоты или сильного основания, но и быть мало чувствительным к изменениям общей концентрации компонентов буфера. Эффект разбавления можно выразить подобно тому, как это сделано для буферного действия, в количественной форме. [c.99]
Если желательно измерить pH с точностью, большей, чем 0,01 ед. pH, то необходимо обратить особое внимание на а) регулирование температуры, особенно поддержание одинаковой температуры в гальваническом элементе б) на составляющую стеклянного электрода в э.д.с. элемента, которая меняется в зависимости от взятых электродов (см. главу X) в) на изменение диффузионного потенциала. Изменения, приписываемые остаточному диффузионному потенциалу, проявляются тогда, когда стандартный и исследуемый растворы содержат различные виды ионов и имеют разную ионную силу. Например, при 38° С наблюдается кажущееся расхождение на 0,01 ед. pH между стандартными фосфатным (1 1) и 0,01 т боратным буферными растворами (см. стр. 86). Эти данные иллюстрируют трудности, которые возникают при определении значений pH с использованием лучших современных приборов. [c.356]
Рефрактометрия широко используется в производстве сахара с целью измерения концентрации растворов сахарозы [54]. За последнее время были описаны многочисленные примеры применения в гель-проникающей хроматографии дифференциальных, автоматических регистрирующих рефрактометров [39]. Дифференциальный рефрактометр также использовался для регулирования режима разделения нейтральных сахаров в виде бо-ратных комплексов при ионообменной хроматографии [55]. Однако чувствительность прибора к изменениям концентрации буферного раствора, наряду с наличием ложных пиков, вызывает некоторые затруднения при его широкой эксплуатации. [c.72]
С целью регулирования pH в конденсационную смесь добавляются вещества, образующие так называемые буферные растворы, т. е. растворы, в которых pH автоматически поддерживается в требуемых пределах. В качестве такой буферной добавки обычно применяются щавелевая, лимонная, уксусная и фосфорная кислоты, соли которых дают буферные растворы. [c.268]
Регулирование pH среды в щелочном растворе. Если среда исследуемого раствора щелочная, а требуется довести ее до нейтральной или кислой, то к раствору по каплям прибавляют соляную, азотную, уксусную кислоты, хлорид аммония, нитрат аммония или другие соли, образованные слабыми основаниями и сильными кислотами, или соответствующие определенным значениям pH буферные растворы. Если раствор сильно щелочной, его предварительно нейтрализуют сильными кислотами, а затем прибавляют к нему буферный раствор. [c.174]
Растворимость гидроксидов, гидратированных оксидов и кислот разных элементов заметно различается. Кроме того, концентрацию ионов водорода и гидроксида можно изменять в 10 раз и больше и легко регулировать при помощи буферов. Поэтому разделения, основанные на регулировании значения pH, легко осуществимы. На практике эти методы можно разделить на три группы 1) разделения в относительно концентрированных растворах сильных кислот, 2) разделения в присутствии буферных растворов с промежуточными значениями pH и 3) разделения в относительно концентрированных растворах гидроксидов калия или натрия. [c.242]
Проверку стеклянных электродов, которые используются для контроля и регулирования pH рассола, лучше проводить на солевых буферных растворах. Эти растворы отличаются от обычных тем, что в них добавляют твердый, химически чистый хлористый натрий с таким расчетом, чтобы его концентрация составляла [c.161]
В нижеприведенных методиках йодометрического определения пенициллина нужное течение реакции учтено определенной концентрацией реагентов — пенициллина, щелочи, кислоты, йода, а также регулированием времени, в течение которого взаимодействуют указанные вещества. Разработана методика, где для создания более постоянного pH йодометрическое определение проводят в присутствии буферных растворов (ацетатного, фталатного или фосфатного) в концентрации 0,3 М. [c.224]
При титровании гипохлоритом растворов, полученных после разложения в запаянных пробирках, оказалось довольно трудно отрегулировать оптимальное значение pH раствора. Титрование гипохлоритом было эффективным только в области pH 7,5—9,6. Органические индикаторы реагировали с гипохлоритом, и поэтому результаты холостых опытов не были постоянными. Удалось установить, что индикатором [14] может служить соль ртути (П) осаждение окиси ртути указывало на достижение конечной точки, и для окончательного регулирования добавляли буферный раствор бикарбоната натрия. Некоторые, однако, предпочитают регулировать pH, осторожно добавляя твердый бикарбонат натрия (Замечание 3, стр. 46). [c.36]
На скорость и направление реакции существенное влияние оказывает pH среды. Для поддержания щелочной среды применяют специальные буферные растворы, например тринатрийфосфат. Для регулирования средней молекулярной массы [c.375]
Описан способ отделения церия от других редкоземельных металлов осаждением в виде основного бромата при регулировании концентрации ионов водорода в растворе буферным раствором, состоящим из пиридина и его хлористоводородной соли. Автор указывает, что однократным осаждением достигается достаточно четкое разделение. Доп. перев. [c.573]
Определение pH. Пользуясь стеклянной палочкой, наносят каплю анализируемого раствора на универсальную индикаторную бумагу, сравнивают окраску пятна со стандартной шкалой. Для регулирования pH среды в анализируемый раствор по каплям при перемешивании, в зависимости от цели, вносят раствор либо кислоты, либо основания, либо гидролизующейся соли, либо буферный раствор, постоянно контролируя значение pH. [c.161]
Одним из вариантов метода постоянной ионной силы является метод буферных растворов. Растворы сильных электролитов, применяемые для разбавления при получении стандартной серии, могут быть заменены так называемыми буферными растворами для регулирования общей ионной силы (БРОИС) или, иначе говоря, рХ-буфер-ными растворами (X — определенный вид ионов). Действие рХ-буфера обеспечивается соответствующими равновесиями, устанавливающимися в реакциях осаждения или комплексообразования. Например, р1- или pAg-буфер может быть приготовлен на основе раствора, насыщенного относительно Agi или КС1, для которого справедливо следующее равновесие с константой K = aija [c.113]
Методика опыта. В кюветы наливают требуемый буферный раствор. Жидкость кювет приводят к одш1аковому уровню сифоном, наполненным буферным раствором. На перекладину кладут полоски хроматографической бумаги для установления электрической связи между кюветами. В камеру укладывают обычно до б полос бумаги. Полосы должны лежать горизонтально и не провисать (для регулирования и пользуется пружина). Полосы бумаги берут чистым пинцетом или руками в резиновых перчатках. Размеры бумажных полос обычно 2,0 X 2,5. [c.31]
В приборе предусмотрена как работа с ручным управлением электромагнитным клапаном бюретка (ключ К4), так и с автоматическим (ключ /Сз). Регулировка компенсирующего напряжения измерительной схемы осуществляется при помощи градуированного переменного сопротивления Рь имеющего намотку значительной длины и специальное устройство для обеспечения линейной зависимости его сопротивления от угла поворота. Для установки нуля служат сопротивления Ps (грубо) и Ps (точно). Коррекция диапазона шкалы производится сопротивлением Ri. Настройка измерительной схемы по стандартным буферным растворам выполняется при помощи сопротивления Рз (при работе с титровальным стендом, подключенным к разъему UIP2) и Рг (при работе со стендом, подключенным к разъему ШР ). Для регулирования ширины полосы замедления скорости подачи титранта в пределах О—300 мв служит сопротивление Ру. [c.176]
Зависимость высоты кинетической волны от периода капания для определения константы скорости предшествуюш,ей реакции использовал Д. Вольф [179, 180]. Регулирование периода капания в его опытах достигалось с помощью периодического удара молоточка по концу капилляра. Скорость истечения ртути при таком способе изменения периода капания сохранялась практически постоянной. Значение константы скорости находилось из величины наклона графика, построенного по экспериментальным значениям токов в координатах — iap/t по уравнению (33), в котором для данных условий опыта (т = onst) х = kt f . Полученное таким образом значение константы скорости нротонизации аниона пировиноградной кислоты в цитратном буферном растворе оказалось близким величине, найденной Г. Штреловым и М. Беккером [181, 182]. [c.35]
Метод несколько усовершенствовали Дёринг [4] и другие [1, 13, 33]. Бромид окисляют до бромата гипохлоритом в слабокислом растворе, содержащем большие количества хлорида натрия. Уиллард и Хейн [33] изучали пределы pH для выполнения реакции и пришли к заключению, что она количественно протекает при pH 5,5—7,0. Для регулирования pH можно применять фосфатные, ацетатные буферные растворы или борную кислоту. Однако удовлетворительные результаты получаются и при простом методе контроля pH, предложенном Дёрингом и состоящем в добавлении небольшого избытка карбоната кальция к слабокислому раствору. [c.201]
Далее был установлен круг ионов, реагирующих с исследуемыми красителяг.ш. Для регулирования pH применяли хлопцд-но-ацетатные, ацетатные и ацетатно-аммиачные буферные растворы [28, 29], величину pH которых контролировали электрометрически. [c.102]
Проверку стеклянных электродов, которые используют для контроля и регулирования pH рассола, лучше проводить, применяя солевые буферные растворы. Эти растворы отличаются от обычных тем, что в них добавляют твердый, химически чистый хлористый натрий с таким расчетом, чтобы его концентрация составляла примерно 300—305 г/л Na l. Опыты показали, что повышение концентрации поваренной соли от 300 до 350 г/л уже не оказывает влияния на pH буферных растворов. [c.139]
На панели лабораторного рН-метра установлены три, а иногда четыре ручки управления 1) переключатель положений выключено и включено 2) регулятор калибровки или стандартизации для установки на нуль, чтобы рН-метр показывал правильную величину, когда электроды погружены в стандартный буферный раствор 3) температурный компенсатор для регулирования чувствительности согласно нернстов-ской зависимости потенциала от температуры. Некоторые рН-метры имеют также переключатель шкалы, что позволяет прибору давать показания во всем интервале шкалы pH (обычно от О до 14) или в ограниченном интервале этой шкалы, возможно в 2 или 3 единицы pH приборы такого типа называют рН-метрами с растянутыми шкалами. [c.327]
Буферные свойства растворам придает наличие в них веществ Слабой кислоты и одной из ее солей или слабого основания и одной из его солей (например, бикарбонаты, фосфаты, уксуснокислые соли). Эти вещества оказывают буферное действие в определенных пределах шкалы pH и поэтому любой буферный раствор является буферным в своем ужом пределе pH. При раз рабоже системы автоматического регулирования технологического процесса по значению pH необходимо знать, обладает ли реакционный раствор буферными овойствами и а каком интервале pH эти свойства проявляются. Если раствор имеет буферные овойства в области регулируемых значений pH, то технологический процесс нельзя регулировать по рН, так как при добавлении к раство1ру реагента pH не будет изменяться или будет изменяться незначительно. [c.415]
Таким образом, способ очистки ТФК в ацетатно-буферном растворе позволяет получать продукт высокой степени чистоты, не отличающийся от стадартных образцов по цветности и содержанию наиболее вредной примеси — п-карбоксибензальдегида. Очистка эффективна лишь с применением окислителя — перманганата калия и адсорбента — активированного угля. Регулирование гидродинамики и пересыщения при кристаллизации ТФК из раствора также оказывает влияние а чистоту продукта. Однако таким образом не удается очистить ТФК от п-толуило-вой кислоты, поэтому поступающий на очистку продукт не должен содержать эту примесь более 0,02%. Это, очевидно, должно быть достигнуто на стадии получения ТФК из л-ксилола [13]. [c.12]
Буферным действием обладают растворы, содержащие кислую и среднюю соль слабой кислоты, например НаНСОз и Ыа СОз (карбонатный буферный раствор), или растворы двух кислых солей, например ЫаН2Р04 и Мз2НР04 (фосфатный буферный раствор). Карбонатный и фосфатный буферные растворы играют определенную роль в регулировании процессов в организмах, обеспечивая устойчивость реакций физиологических жидкостей (кровь, молоко, клеточный сок растений и др.). [c.155]
Часто гидролиз удается предотвратить, используя буферные растворы или добавляя в раствор слабое основание, например аммиак. Если для регулирования pH в раствор вводят аммиак, то может произойти аминный обмен. Например, взаимодействие быс-ацетилацетонтриметилендиамина с ионом меди в присутствии большого избытка аммиака приводит к образованию [41 быс-(4-аминонентан-2-оно)-меди(И). [c.72]
В хроматографии на неполярных стационарных фазах осно-Бу подвижной фазы составляет вода, к которой с целью регулирования полярности добавляют метанол или ацетонитрил или тетрагидрофуран. При разделении ионогенных веществ методом хроматографии ионных пар в подвижную фазу добавляют соли гидрофобных ионов. В хроматографии сильных кислот и их солей часто используют тетрабутила.ммонийфосфат или гек-садецилтриметиламмонийхлорид в хроматографии сильных оснований и их солей применяют натриевые соли s— s алкил-сульфоновых кислот. Для разделения слабых кислот бывает достаточно подавить их диссоциацию. Для этого регулируют pH подвижной фазы путем добавления фосфатных или ацетатных буферных растворов или уксусной кислоты. [c.248]
Буферные растворы играют большую роль в аналитической химии. Осаждение, например, часто должно проводиться при определенном значении pH раствора. Этот pH устанавливают прибавлением подходящей буферной с.меси. Так, буферное действие смеси КНо+КН С используется для осаждения гидроокиси алюминия, которая при применении одного аммиака частично растворяется в его избытке, образуя алю.минат. Эта же буферная смесь применяется в случае необходимости удержать гидроокись магния в растворе (стр. 264). Ацетатный буфер ( Ho OOH+ Hз OONa) или формиатный (НСООН+НСОбЫа) используются при осаждении ионов цинка сероводородом. Многие цветные реакции с органическими реактивами могут быть успешно применены только при поддержании определенно- о значения pH раствора. Наконец, дифференциальное выделение сульфидов различных ионов осуществляется посредством регулирования pH раствора. [c.94]
Курс аналитической химии. Кн.1 (1968) — [
c.201
]
Курс аналитической химии Книга 1 1964 (1964) — [
c.172
]
Основы аналитической химии Книга 1 (1961) — [
c.173
,
c.174
]
Курс аналитической химии Издание 3 (1969) — [
c.201
]
Курс аналитической химии Издание 5 (1981) — [
c.172
]
