Исентресс® (Isentress) инструкция по применению
📜 Инструкция по применению Исентресс®
💊 Состав препарата Исентресс®
✅ Применение препарата Исентресс®
📅 Условия хранения Исентресс®
⏳ Срок годности Исентресс®
Описание лекарственного препарата
Исентресс®
(Isentress)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для электронного издания справочника Видаль 2017
года, дата обновления: 2021.07.02
Код ATX:
J05AJ01
(Ралтегравир)
Лекарственная форма
| Исентресс® |
Таб., покр. пленочной оболочкой, 400 мг: 60 шт. рег. №: ЛСР-007737/08 |
Форма выпуска, упаковка и состав
препарата Исентресс®
Таблетки, покрытые пленочной оболочкой розового цвета, овальные, двояковыпуклые, с гравировкой «227» на одной стороне и гладкие на другой.
Вспомогательные вещества: целлюлоза микрокристаллическая — 169.4 мг, лактозы моногидрат — 26.06 мг, кальция гидрофосфат — 69.5 мг, гипромеллоза 2208 — 43.44 мг, полоксамер 407 (содержит 0.01% бутилгидрокситолуола в качестве антиоксиданта) — 104.3 мг, натрия стеарилфумарат — 8.688 мг, магния стеарат — 13.03 мг.
Состав пленочного покрытия: краситель Опадрай II розовый (85F94224) — 26.06 мг.
Состав пленочной оболочки: поливиниловый спирт — 44.75%, макрогол — 22%, тальк — 21.415%, титана диоксид — 11.32%, краситель железа оксид красный — 0.495%, краситель железа оксид черный — 0.02%.
60 шт. — флаконы из полиэтилена высокой плотности (1) — пачки картонные.
Фармакологическое действие
Ралтегравир ингибирует каталитическую активность ВИЧ интегразы — фермента, участвующего в репликации вируса ВИЧ. Ингибирование интегразы предотвращает ковалентное введение (интеграцию) генома ВИЧ в геном клетки хозяина на ранних стадиях развития инфекции. Не включенные в ДНК человека геномы ВИЧ не способны индуцировать продукцию новых вирусных частиц, поэтому подавление процесса интеграции предотвращает распространение вирусной инфекции в организме. Ингибирующая способность ралтегравира в отношении фосфотрансфераз человека, включая ДНК-полимеразы α, β и γ, выражена незначительно.
Микробиология
При плазменной концентрации 31±20 нмоль/л ралтегравир обеспечивал подавление репликации вируса на 95% (95% ингибирующая концентрация, ИК95) в клеточных культурах человеческих Т-лимфоцитов, инфицированных адаптированным к культурам клеток вариантом H9IIIB ВИЧ-1 по сравнению с контрольной вирус-инфицированной культурой клеток. ИК95 достигалась в концентрациях от 6 до 50 нмоль/л в культурах человеческих митоген-активированных мононуклеаров периферической крови, инфицированных различными первичными клиническими штаммами ВИЧ-1, включая штаммы 5 не-В подтипов ВИЧ-1, а также штаммы, резистентные к ингибиторам обратной транскриптазы и ингибиторам протеазы ВИЧ.
При анализе одного цикла инфекции ралтегравир подавлял инфицирование, вызванное 23 штаммами ВИЧ, представляющими 5 не-В подтипов и 5 циркулирующих рекомбинантных форм, с ИК50 — 5-12 нмоль/л. Ралтегравир также подавлял репликацию штаммов ВИЧ-2 при тестировании на клетках линии СЕМх174 (ИК95 = 6 нмоль/л). При одновременном введении в культуру человеческих Т-лимфоцитов, инфицированных вариантом H9IIIB вируса ВИЧ-1, ралтегравира и нуклеозидных ингибиторов обратной транскриптазы (зидовудин, залцитабин, ставудин, абакавир, тенофовир, диданозин и ламивудин), ненуклеозидных ингибиторов обратной транскриптазы (эфавиренз, невирапин и делавирдин), ингибиторов протеазы ВИЧ (индинавир, саквинавир, ритонавир, ампренавир, лопинавир, нелфинавир и атазанавир) или ингибитора слияния (энфувиртид) наблюдалась антиретровирусная активность от аддитивной до синергичной.
Резистентность к препарату
Мутации интегразы ВИЧ-1, способствующие появлению резистентных к ралтегравиру штаммов вируса (развивались in vitro или у пациентов, принимавших ралтегравир), в основном включают замены в положениях 155 (N155 замена на Н), 148 (Q148 замена на Н, К или R) или 143 (Y143 замена на С, Н или R), в сочетании с одной или более дополнительными мутациями (например, L74M, E92Q, Т97А, Е138А/К, G140A/S, V151I, G163R, S230R).
Рекомбинантные вирусы с одной первичной мутацией (Q148H, К или R или N155H) отличались сниженной способностью к репликации и сниженной чувствительностью к ралтегравиру in vitro. Вторичные мутации вируса еще больше снижали чувствительность к ралтегравиру, иногда компенсируя сниженную способность вируса к репликации.
Мутации, ассоциированные с развитием резистентности к ралтегравиру, также могут приводить к формированию резистентности к другому ингибитору переноса цепи интегразой элвитегравиру. При замене в положении 143 чувствительность к ралтегравиру снижается в большей степени, чем чувствительность к элвитегравиру, тогда как мутации в E92Q вызывают большую резистентность к элвитегравиру, чем к ралтегравиру. У вирусов с мутацией в положении 148 в сочетании с одной и более дополнительными мутациями, вызывающими резистентность к ралтегравиру, также может наблюдаться клинически значимая резистентность к долутегравиру.
Влияние на электрофизиологическую активность сердца или на показатели ЭКГ
В плацебо-контролируемом клиническом исследовании с участием здоровых добровольцев однократный прием 1600 мг ралтегравира не оказывал влияния на продолжительность интервала QTc несмотря на то, что Cmax ралтегравира в плазме крови была в 4 раза больше, чем при однократном приеме ралтегравира в дозе 400 мг.
Фармакокинетика
У взрослых пациентов
Всасывание
Ралтегравир быстро всасывается после приема препарата натощак, Cmax в плазме крови определяется примерно через 3 часа. Значения AUC и Cmax ралтегравира увеличиваются пропорционально дозе в диапазоне доз от 100 до 1600 мг. Значения С12ч ралтегравира возрастают пропорционально дозе в диапазоне доз от 100 мг до 800 мг и возрастают в несколько меньшей степени — в диапазоне доз от 100 мг до 1600 мг.
При режиме приема препарата 2 раза/сут равновесное состояние достигается быстро, примерно в течение 2 дней после начала лечения. Значения AUC и Cmax свидетельствуют в пользу отсутствия или минимальной кумуляции препарата, значение С12ч — в пользу незначительной кумуляции препарата. В режиме монотерапии по 400 мг 2 раза/сут значение среднего геометрического для AUC0-12ч составляло 14.3 мкмоль/л х ч, значение С12ч — 142 нмоль/л.
Абсолютная биодоступность ралтегравира не установлена. Ралтегравир можно принимать вне зависимости от режима приема пищи.
Распределение
Примерно 83% ралтегравира связывается с белками плазмы в диапазоне концентраций от 2 до 10 мкмоль/л. Ралтегравир легко преодолевал плацентарный барьер в экспериментальных исследованиях на крысах, но не проникал через ГЭБ в заметной степени.
В двух клинических исследованиях с участием пациентов, инфицированных ВИЧ-1, которые принимали ралтегравир в дозе 400 мг 2 раза/сут, ралтегравир быстро определялся в спинномозговой жидкости. В первом исследовании средняя концентрация ралтегравира в спинномозговой жидкости составила 5.8% (в диапазоне от 1 до 53.5%) от соответствующей концентрации в плазме крови, а во втором исследовании — 3% (в диапазоне от 1 до 61%) от соответствующей концентрации в плазме крови. Медианы полученных значений были приблизительно в 3-6 раз ниже, чем концентрации свободной фракции ралтегравира в плазме крови.
Метаболизм и выведение
Исследования с использованием селективных ингибиторов к изоформе фермента уридиндифосфат-глюкуронилтрансферазы (УДФ-ГТ), полученной путем экспрессии комплементарной ДНК, показали, что УДФ-ГТ1А1 является основным ферментом, участвующим в образовании ралтегравир-глюкуронида. Эти данные показали, что основной путь метаболизма ралтегравира у человека представлен процессом глюкуронирования, опосредованного УДФ-ГТ1А1. T1/2 ралтегравира в конечной фазе составляет около 9 ч, большая часть AUC соответствует более короткой α-фазе кажущегося T1/2 ралтегравира (составляет примерно 1 ч). После приема внутрь радиоактивно меченого ралтегравира примерно 51% от принятой дозы выводилось через кишечник и 32% — через почки. В кале обнаруживался только ралтегравир, который, вероятно, образовывался путем гидролиза ралтегравир-глюкуронида, выделившегося с желчью. В моче определялись ралтегравир и ралтегравир-глюкуронид в количестве 9% и 23% от принятой дозы соответственно. В плазме крови основным циркулирующим радиоактивным компонентом был ралтегравир (примерно 70% от общей радиоактивности), в то время как на ралтегравир-глюкуронид приходилось только 30%.
Фармакокинетика у отдельных групп пациентов
Пол
Пол не оказывает клинически значимого влияния на фармакокинетические параметры ралтегравира. Коррекция дозы препарата в зависимости от пола пациента не требуется.
Пожилые пациенты
В исследованиях с участием пациентов в возрасте 18 лет и старше не было обнаружено значимой зависимости фармакокинетических параметров ралтегравира от возраста пациентов, поэтому коррекция дозы препарата в зависимости от возраста не требуется.
Подростки и дети
Дозы для подростков и детей старше 6 лет для лечения ВИЧ-1 инфекции рекомендованы на основании того, что фармакокинетические параметры ралтегравира сопоставимы с таковыми у взрослых пациентов.
Фармакокинетика ралтегравира у детей младше 2 лет не изучалась.
Пациенты из разных расово-этнических групп
Расово-этническая принадлежность не оказывала клинически значимого влияния на фармакокинетические параметры ралтегравира. Коррекция дозы не требуется.
Пациенты с различным индексом массы тела (ИМТ)
ИМТ не оказывал клинически значимого влияния на фармакокинетические параметры ралтегравира у взрослых пациентов. Коррекция дозы препарата в зависимости от ИМТ пациента не требуется.
Пациенты с печеночной недостаточностью
Ралтегравир выводится преимущественно путем глюкуронирования в печени. Фармакокинетика препарата была изучена у взрослых пациентов с печеночной недостаточностью средней степени тяжести, а также в комбинированном фармакокинетическом анализе. Клинически значимых отклонений фармакокинетических параметров у взрослых пациентов с печеночной недостаточностью средней степени тяжести по сравнению со здоровыми добровольцами не выявлено. Таким образом, коррекция дозы препарата при печеночной недостаточности легкой и средней степени тяжести не требуется. Влияние печеночной недостаточности тяжелой степени на фармакокинетические параметры ралтегравира не изучалось.
Пациенты с почечной недостаточностью
На почечный клиренс приходится незначительная доля в выведении ралтегравира из организма. Фармакокинетика препарата была изучена у взрослых пациентов с тяжелой степенью почечной недостаточности, а также в сложном фармакокинетическом анализе. Клинически значимых отклонений фармакокинетических параметров у пациентов с тяжелой степенью почечной недостаточности по сравнению со здоровыми добровольцами не выявлено. Таким образом, коррекции дозы препарата пациентам с тяжелой степенью почечной недостаточности не требуется. Поскольку эффективность диализа ралтегравира неизвестна, принимать препарат накануне сеанса диализа не рекомендуется.
Пациенты с полиморфизмом УДФ-ГТ1А1
Доказательства или какие-либо данные, свидетельствующие, что наличие полиморфизма у фермента УДФ-ГТ1А1 может оказывать клинически значимое влияние на фармакокинетические параметры ралтегравира, не были получены. По данным сравнительного исследования с участием 30 взрослых здоровых добровольцев с генетически-детерминированной сниженной активностью УДФ-ГТ1А1 и 27 взрослых здоровых добровольцев с неизмененным генотипом УДФ-ГТ1А1 отношение средних геометрических AUC ралтегравира составило 1.41 (90% доверительный интервал составил 0.96; 2.09).
Показания препарата
Исентресс®
- лечение ВИЧ-1 инфекции в комбинации с другими антиретровирусными препаратами у взрослых, подростков и детей, начиная с 6 лет и с массой тела не менее 25 кг, как ранее получавших, так и не получавших антиретровирусную терапию.
Режим дозирования
Внутрь. Таблетки препарата Исентресс® нельзя жевать, крошить, разламывать. Препарат применяется вне зависимости от приема пищи.
Лечение препаратом Исентресс® должен проводить врач, обладающий достаточным опытом терапии ВИЧ-инфекции.
Лечение препаратом Исентресс® проводят в комбинации с другими антиретровирусными препаратами.
Рекомендуемые дозы препарата Исентресс® для лечения ВИЧ-1 инфекции:
для взрослых — 400 мг 2 раза/сут;
для детей с массой тела не менее 25 кг — 400 мг 2 раза/сут.
Если пациенты детского возраста испытывают трудности при проглатывании таблеток, покрытых пленочной оболочкой, следует рассмотреть возможность приема препарата Исентресс® таблетки жевательные (см. инструкцию по применению препарата Исентресс® таблетки жевательные).
У пациентов пожилого возраста коррекция дозы не требуется.
У пациентов с нарушением функции почек коррекция дозы не требуется.
У пациентов с нарушением функции печени легкой и средней степени тяжести коррекция дозы не требуется.
Побочное действие
Профиль безопасности препарата Исентресс® основан на результатах обобщенных данных по безопасности, полученных в ходе клинических исследований с участием пациентов, ранее получавших антиретровирусную терапию (АРВТ), и пациентов, ранее не получавших АРВТ.
В объединенном анализе результатов клинических исследований антиретровирусной терапии у взрослых пациентов, ранее получавших АРВТ, частота отмены терапии по причине нежелательных реакций составила 3.9% в группе пациентов, принимавших препарат Исентресс® и оптимизированную дополнительную терапию (ОДТ), и 4.6% в группе пациентов, принимавших плацебо и ОДТ. Частота отмены терапии по причине нежелательных реакций у взрослых пациентов, ранее не получавших АРВТ, составила 5.0% в группе пациентов, принимавших препарат Исентресс® одновременно с эмтрицитабином и тенофовиром, и 10.0% в группе пациентов, принимавших одновременно эфавиренз, эмтрицитабин и тенофовир.
Ниже представлены данные о нежелательных явлениях, наблюдавшихся в клинических исследованиях, с различной степенью вероятности связанных с препаратом Исентресс® или его комбинацией с другой АРВТ.
Нежелательные явления перечислены в соответствии с системно-органными классами и классификацией по частоте: часто (≥1/100 и <1/10), нечасто (≥1/1000 и <1/100).
Инфекционные и паразитарные заболевания: нечастые — генитальный герпес, фолликулит, гастроэнтерит, простой герпес, герпетическая инфекция, опоясывающий лишай, грипп, абсцесс лимфоузла, контагиозный моллюск, назофарингит, инфекция верхних дыхательных путей.
Доброкачественные, злокачественные и неуточненные новообразования (включая кисты и полипы): нечастые — папилломатоз кожи.
Со стороны крови и лимфатической системы: нечастые — анемия, железодефицитная анемия, болезненность лимфоузлов, лимфаденопатия, нейтропения, тромбоцитопения1.
Со стороны иммунной системы: нечастые — синдром восстановления иммунитета, гиперчувствительность к препарату, реакции гиперчувствительности.
Со стороны обмена веществ: частые — снижение аппетита; нечастые — кахексия, сахарный диабет, дислипидемия, гиперхолестеринемия, гипергликемия, гиперлипидемия, гиперфагия, повышение аппетита, полидипсия, нарушение жирового обмена.
Нарушения психики: частые — необычные сновидения, бессонница, ночные кошмары, нарушение поведения2, депрессия; нечастые — психические расстройства, суицидальные попытки, чувство тревоги, спутанность сознания, подавленное настроение, большое депрессивное расстройство, бессонница середины ночи, изменения настроения, панические атаки, нарушения сна, суицидальные идеи1, суицидальное поведение1 (особенно у пациентов с психиатрическими заболеваниями в анамнезе).
Со стороны нервной системы: частые — головокружение, головная боль, психомоторная гиперреактивность2, нечастые — амнезия, синдром запястного канала, когнитивные расстройства, нарушения внимания, постуральное головокружение, дисгевзия, гиперсомния, гипестезия, летаргия, расстройство памяти, мигрень, периферическая невропатия, парестезии, сонливость, головная боль напряжения, тремор, снижение качества сна.
Со стороны органа зрения: нечастые — снижение остроты зрения.
Со стороны органа слуха и лабиринтные нарушения: частые — вертиго; нечастые — шум в ушах.
Со стороны сердечно-сосудистой системы: нечасто — ощущение сердцебиения, синусовая брадикардия, желудочковая экстрасистолия, приливы крови к коже лица с ощущением жара, артериальная гипертензия.
Со стороны дыхательной системы, органов грудной клетки и средостения: нечастые — дисфония, носовое кровотечение, заложенность носа.
Со стороны пищеварительной системы: частые — чувство распирания в животе, боль в животе, диарея, метеоризм, тошнота, рвота, диспепсия; нечастые — гастрит, ощущение дискомфорта в животе, боль в верхних отделах живота, болезненность в области живота, чувство дискомфорта в области заднего прохода, запор, сухость во рту, ощущение дискомфорта в эпигастральной области, эрозивный дуоденит, отрыжка, гастроэзофагеальный рефлюкс, гингивит, глоссит, болезненность при глотании, острый панкреатит, пептическая язва, ректальные кровотечения.
Со стороны печени и желчевыводящих путей: нечастые — гепатит, стеатоз печени, алкогольный гепатит, печеночная недостаточность1.
Со стороны кожи и подкожных тканей: частые — кожная сыпь; нечастые — акне, алопеция, угревидная сыпь, сухость кожи, эритема, липоатрофия лица, гипергидроз, липоатрофия, приобретенная липодистрофия, липогипертрофия, ночная потливость, пруриго, зуд (локальный и генерализованный), макулярная сыпь, макуло-папулезная сыпь, зудящая сыпь, крапивница, ксеродермия, другие поражения кожи, синдром Стивенса-Джонсона1, лекарственная сыпь с эозинофилией и системными симптомами (DRESS-синдром)1.
Со стороны костно-мышечной системы: нечастые — артралгия, артрит, боль в спине, боль в боку, миалгия, боль в области шеи, остеопения, боль в конечностях, остеопороз, полиартрит, тендинит, миопатия, рабдомиолиз1.
Со стороны почек и мочевыводящих путей: нечастые — почечная недостаточность, нефрит, нефролитиаз, никтурия, киста почки, нарушение функции почек, тубулоинтерстициальный нефрит.
Со стороны половых органов и молочной железы: нечастые — эректильная дисфункция, гинекомастия, симптомы менопаузы.
Общие расстройства: частые — астения, слабость, лихорадка; нечастые — дискомфорт в груди, озноб, отек лица, увеличение объема жировой ткани, состояние беспокойства, недомогание, подчелюстное новообразование, периферические отеки, боль.
Лабораторные и инструментальные данные: частые — повышение активности в плазме АЛТ, АСТ, липазы и амилазы поджелудочной железы, повышение концентрации триглицеридов и количества атипичных лимфоцитов; нечастые — снижение абсолютного числа нейтрофилов плазмы; повышение активности в плазме ЩФ, КФК, снижение концентрации альбумина; повышение концентрации билирубина, холестерина, креатинина, глюкозы (в т.ч. определяемой натощак), азота мочевины, холестерина ЛПВП, холестерина ЛПНП; повышение значения МНО; снижение количества тромбоцитов и лейкоцитов в крови; наличие глюкозы в моче, наличие эритроцитов в моче; увеличение окружности талии; увеличение или снижение массы тела.
Травмы, интоксикации и осложнения манипуляций: нечастые — непреднамеренная передозировка.
1Нежелательные явления, не связанные с применением препарата Исентресс®, которые наблюдались в пострегистрационном периоде и не наблюдались в ходе клинических исследований.
2У одного пациента детского возраста наблюдались связанные с приемом препарата нежелательные реакции: психомоторная гиперреактивность 3 степени и нарушение поведения; также у данного пациента наблюдалась бессонница.
В ходе клинических исследований у пациентов, ранее получавших и не получавших АРВТ, наблюдались случаи развития злокачественных новообразований при использовании комбинации препарата Исентресс® с другими антиретровирусными средствами. Характеристика и частота злокачественных новообразований соответствовали таковым для пациентов с тяжелым иммунодефицитом. Риск развития злокачественных новообразований в клинических исследованиях был одинаков как в группах пациентов, принимавших препарат Исентресс®, так и в группах пациентов, принимавших препараты сравнения.
У пациентов, принимавших препарат Исентресс®, наблюдалось повышение активности КФК 2-4 степени. Наблюдались случаи развития миопатии и рабдомиолиза. Пациентам с миопатией или рабдомиолизом в анамнезе, а также имеющим другие факторы риска (включая сопутствующую терапию), препарат следует назначать с осторожностью.
Сообщалось о случаях развития остеонекроза, особенно у пациентов с общепризнанными факторами риска, поздней стадией ВИЧ-заболевания или длительным воздействием комбинированной АРВТ. Частота его развития неизвестна.
В клинических исследованиях у пациентов, ранее получавших АРВТ, кожная сыпь, вне зависимости от этиологии, чаще наблюдалась при применении препарата Исентресс® одновременно с дарунавиром, чем при применении данных препаратов по отдельности. Тем не менее, частота развития кожной сыпи, связанной с приемом препаратов, была сопоставима в этих группах лечения. Кожная сыпь была легкой и умеренной степени тяжести и не влияла на продолжение АРВТ. У пациентов, ранее не принимавших АРВТ, при лечении препаратом Исентресс® в комбинации с эмтрицитабином и тенофовиром развитие сыпи наблюдалось реже, чем при лечении эфавирензом в комбинации с эмтрицитабином и тенофовиром.
Пациенты с ко-инфекцией гепатита В и/или гепатита С
В целом профиль безопасности препарата Исентресс® у пациентов, как ранее получавших, так и не получавших АРВТ, ко-инфицированных хроническим (но не острым) активным гепатитом В и/или гепатитом С, был аналогичен профилю безопасности у пациентов без ко-инфекции гепатита В и/или гепатита С, хотя частота отклонения активности АЛТ и ACT иногда была выше в группах с ко-инфекцией гепатита В и/или гепатита С.
Дети
По результатам клинических исследований по применению ралтегравира в рекомендованных дозах в комбинации с другими антиретровирусными лекарственными средствами у ВИЧ-1 инфицированных детей и подростков от 2 до 18 лет было установлено, что частота, тип и выраженность нежелательных реакций, связанных с приемом препарата, были сопоставимы с таковыми у взрослых пациентов. У одного пациента наблюдались связанные с приемом препарата нежелательные реакции: психомоторная гиперактивность 3 степени, нарушение поведения и бессонница. У другого пациента наблюдалась серьезная нежелательная реакция 2 степени — аллергическая сыпь. Еще у одного пациента наблюдалось повышение активности ACT 4 степени и АЛТ 3 степени, которое было расценено как серьезное.
Противопоказания к применению
- повышенная чувствительность к ралтегравиру и другим компонентам препарата;
- детский возраст до 6 лет;
- масса тела до 25 кг;
- беременность;
- период лактации (грудного вскармливания);
- непереносимость лактозы, дефицит лактазы или мальабсорбция глюкозы/галактозы.
С осторожностью:
- миопатия и рабдомиолиз (в т.ч. в анамнезе), наличие состояний и факторов, предрасполагающих к их развитию;
- печеночная недостаточность тяжелой степени;
- одновременное применение с сильными индукторами УДФ-ГТ1А1 (рифампицин);
- одновременное применение препарата Исентресс® с антацидами, содержащими алюминий или магний;
- депрессия, включая суицидальные идеи и поведение (наблюдалась в основном у пациентов с депрессией или психиатрическими заболеваниями в анамнезе). Следует соблюдать осторожность при назначении препарата Исентресс® пациентам с депрессией или психиатрическими заболеваниями в анамнезе;
- пожилой возраст (ввиду ограниченной информации о применении ралтегравира у пациентов старше 65 лет).
Применение при беременности и кормлении грудью
Контролируемых исследований препарата Исентресс® у беременных не проводилось, поэтому Исентресс® противопоказан к применению во время беременности.
Отсутствуют данные о поступлении ралтегравира в грудное молоко человека. Однако обнаружено поступление ралтегравира в молоко у лактирующих крыс: при введении препарата в суточной дозе 600 мг/кг концентрация ралтегравира в молоке превышала плазменную концентрацию примерно в 3 раза.
Грудное вскармливание не рекомендуется ВИЧ-инфицированным матерям во избежание постнатальной передачи ВИЧ детям. При необходимости применения препарата в период лактации рекомендуется прекратить грудное вскармливание.
Особые указания
Пациентов следует информировать о том, что современные антиретровирусные препараты не излечивают ВИЧ-инфекцию и не предотвращают передачу ВИЧ другим людям с кровью или при половых контактах. Во время лечения препаратом Исентресс® пациенты должны продолжать соблюдать соответствующие меры безопасности. Также пациенты должны быть проинформированы о том, что у них все еще могут развиться инфекции или другие состояния, распространенные среди ВИЧ-инфицированных пациентов (оппортунистические инфекции). Очень важно оставаться под наблюдением врача во время терапии препаратом Исентресс®.
Ралтегравир имеет относительно низкий генетический барьер к развитию резистентности, поэтому для повышения эффективности лечения и снижения риска развития резистентности к препарату ралтегравир необходимо назначать в комбинации с двумя другими активными антиретровирусными средствами, если это возможно. Важно объяснить пациентам необходимость изучить инструкцию по применению перед началом терапии препаратом Исентресс® и перечитывать се каждый раз при получении очередного рецепта от врача. Пациенты должны быть проинформированы о необходимости сообщать врачу о появлении каких-либо необычных симптомов, а также о сохранении или ухудшении любого известного симптома.
Синдром восстановления иммунитета
На начальных этапах комбинированной АРВТ у ВИЧ-инфицированных пациентов с тяжелым иммунодефицитом может развиться так называемый синдром восстановления иммунитета, т.е. воспалительная реакция на бессимптомно текущие или остаточные оппортунистические инфекции (цитомегаловирусный ретинит, пневмоцистная пневмония, вызванная Pneumocystis jirovecii, диссеминированные или очаговые микобактериальные инфекции и др.). Это может способствовать ухудшению клинического состояния и усилению имеющихся симптомов. Обычно такая реакция может наблюдаться в первые недели или месяцы после начала комбинированной терапии. Любые воспалительные симптомы должны быть оценены, и при необходимости назначено лечение.
При развитии синдрома восстановления иммунитета были описаны такие аутоиммунные расстройства, как Базедова болезнь. Тем не менее развитие таких нарушений может наблюдаться через много месяцев после начала лечения.
Остеонекроз
Несмотря на то, что этиология данного осложнения считается многофакторной (включая терапию ГКС, употребление алкоголя, тяжелый иммунодефицит, высокий индекс массы тела), описаны случаи развития остеонекроза, особенно на поздних стадиях ВИЧ-инфекции и/или при длительном приеме комбинированной АРВТ. Пациентам, у которых появились такие симптомы, как боль в суставах, скованность или ограничение подвижности, нужна срочная консультация специалиста.
Тяжелые реакции со стороны кожи и реакции гиперчувствительности
Получены данные о тяжелых (потенциально жизнеугрожающих) и фатальных нежелательных реакциях со стороны кожи у пациентов, принимавших препарат Исентресс® в составе комбинированной терапии с другими лекарственными средствами, ассоциирующимися с этими нежелательными реакциями, такими как синдром Стивенса-Джонсона и токсический эпидермальный некролиз. Также сообщалось о реакциях гиперчувствительности, которые проявлялись в виде сыпи генерализованного характера, и иногда органной дисфункции, включая печеночную недостаточность. Следует немедленно прекратить применение препарата Исентресс® и других препаратов, предположительно способных вызвать такие реакции, если появились признаки или симптомы тяжелых реакций со стороны кожи или реакции гиперчувствительности (включая тяжелую кожную сыпь или сыпь, сопровождающуюся лихорадкой, общее недомогание, слабость, боли в мышцах или суставах, появление волдырей на коже, повреждения в ротовой полости, конъюнктивит, отек лица, гепатит, эозинофилию, ангионевротический отек, но не ограничиваясь только ими). В этих случаях необходимо мониторировать клинический статус, включая активность печеночных аминотрансфераз, и начать соответствующую терапию. Несвоевременное прекращение терапии препаратом Исентресс® или другими лекарственными средствами, ассоциирующимися с этими нежелательными реакциями, после появления тяжелой сыпи может привести к жизнеугрожающим реакциям.
Миопатия и рабдомиолиз
Сообщалось о развитии миопатии и рабдомиолиза. Следует соблюдать осторожность при назначении препарата пациентам с миопатией и рабдомиолизом в анамнезе или с какими-либо факторами, предрасполагающими к их развитию, в частности, при сопутствующей терапии препаратами, способными вызвать эти нежелательные реакции.
Нарушение функции печени
Безопасность и эффективность препарата Исентресс® у пациентов с тяжелыми сопутствующими заболеваниями печени не установлена. Следует соблюдать осторожность при назначении препарата Исентресс® пациентам с тяжелыми нарушениями функции печени.
У пациентов с существующей дисфункцией печени, включая хронический гепатит, повышается частота нарушений функции печени на фоне комбинированной АРВТ, и они подлежат мониторингу в соответствии со стандартной практикой. При появлении у таких пациентов признаков ухудшения заболевания печени должен быть рассмотрен вопрос о прерывании или прекращении лечения.
Пациенты с хроническим гепатитом В или С, также получающие комбинированную АРВТ, входят в группу риска развития тяжелых и потенциально фатальных нежелательных явлений со стороны печени.
Кожная сыпь
У пациентов, ранее получавших АРВТ, при применении препарата Исентресс® одновременно с дарунавиром кожная сыпь наблюдается чаще, чем у пациентов, применяющих препараты по отдельности (см. раздел «Побочное действие»).
Депрессия
Депрессия, включая суицидальные идеи и поведение, наблюдалась в основном у пациентов с депрессией или психиатрическими заболеваниями в анамнезе. Следует соблюдать осторожность при назначении препарата Исентресс® пациентам с депрессией или психиатрическими заболеваниями в анамнезе.
Одновременное применение с другими лекарственными средствами
Сильные индукторы УДФ-ГТ1А1. Следует соблюдать осторожность при назначении препарата Исентресс® одновременно с сильными индукторами УДФ-ГT1A1, такими как рифампицин, вследствие вызываемого ими снижения плазменной концентрации ралтегравира. При необходимости проведения комбинированной терапии рифампицином и препаратом Исентресс® доза препарата Исентресс® должна быть увеличена в 2 раза у взрослых пациентов. Нет данных для корректировки доз препаратов при одновременном применении препарата Исентресс® и рифампицина у пациентов младше 18 лет.
Антациды. Одновременное применение препарата Исентресс® с антацидами, содержащими алюминий или магний, приводит к снижению концентрации ралтегравира в плазме крови.
Одновременное применение препарата Исентресс® с антацидами, содержащими алюминий или магний, не рекомендуется (см. раздел «Лекарственное взаимодействие»).
Влияние на способность к управлению транспортными средствами и механизмами
Исследования но изучению влияния на способность к управлению транспортными средствами и использованию механизмов не проводились. Учитывая возможность развития головокружения, слабости, сонливости и нечеткости зрения на фоне лечения препаратом Исентресс®, нужно проявлять особую осторожность при управлении автомобилем и работе с механизмами.
Передозировка
Специфических симптомов передозировки препарата Исентресс® не выявлено. Ралтегравир хорошо переносился здоровыми добровольцами в режиме 1600 мг 1 раз в сутки и 800 мг 2 раза в сутки, без каких-либо проявлений токсичности. Однократный прием дозы 1800 мг в сутки в исследованиях II/III фазы не оказывал токсического воздействия. На основании имеющихся данных можно заключить, что ралтегравир хорошо переносится в дозах до 800 мг два раза в сутки, а также при приеме с препаратами, увеличивающими его экспозицию на 50-70% (например, тенофовиром и атазанавиром). Ралтегравир имеет широкий терапевтический диапазон, поэтому потенциал токсического действия в результате передозировки ограничен.
Лечение: в случае передозировки необходимо следовать стандартным рекомендациям, таким, как удаление невсосавшегося препарата из желудочно-кишечного тракта, наблюдение за показателями жизнедеятельности, включая ЭКГ, назначение симптоматической терапии. Данных об эффективности диализа при передозировке препаратом Исентресс® нет.
Лекарственное взаимодействие
В исследованиях in vitro было показано, что ралтегравир не является субстратом изоферментов системы цитохрома Р450 и не ингибирует CYP1A2, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6 или CYP3A. Кроме этого, in vitro ралтегравир ие индуцирует CYP3A4 и не является ингибитором P-гликопротеин-опосредованного транспорта. На основании этих данных можно сделать вывод, что Исентресс® не влияет на фармакокинетические параметры лекарственных средств, которые являются субстратами указанных ферментов или Р-гликопротеина.
Как показали исследования in vitro и in vivo, ралтегравир выводится в основном посредством метаболизма (глюкуронирования) по УДФ-ГТ1А1-опосредованному пути. Хотя исследования in vitro показали, что ралтегравир не является ингибитором УДФ-ГТ1А1 и 2В7, в одном клиническом исследовании были выявлены некоторые признаки ингибирования УДФ-ГТ1А1 in vivo на основе наблюдаемого влияния на глюкуронирование билирубина. Тем не менее маловероятно, что данный эффект приводит к клинически значимому лекарственному взаимодействию.
В фармакокинетике ралтегравира наблюдалась значимая интер- и интраиндивидуальная изменчивость. Приведенная ниже информация о взаимодействии с лекарственными средствами основана на средних геометрических значениях; эффект у отдельного пациента точно предсказать нельзя.
Влияние ралтегравира на фармакокинетику других лекарственных средств
В исследованиях по изучению лекарственного взаимодействия ралтегравир не оказывал клинически значимого влияния на фармакокинетику этравирина, маравирока, тенофовира, гормональных контрацептивов, метадона и мидазолама.
В некоторых исследованиях при одновременном применении препарата Исентресс® с дарунавиром наблюдалось незначительное снижение концентрации дарунавира в плазме крови. Механизм данного явления неизвестен. Тем не менее, влияние ралтегравира на концентрацию дарунавира в плазме крови не считается клинически значимым.
Влияние других лекарственных средств на фармакокинетику ралтегравира
Следует соблюдать осторожность при одновременном применении препарата Исентресс® с сильными индукторами УДФ-ГТ1А1 (например, рифампицином), учитывая, что ралтегравир метаболизируется в основном посредством УДФ-ГТ1А1. Рифампицин снижает концентрации ралтегравира в плазме крови. Влияние на эффективность ралтегравира неизвестно. Тем не менее, если одновременного применения с рифампицином избежать невозможно, можно удвоить дозу препарата Исентресс® у взрослых. Данные по одновременному применению препарата Исентресс® и рифампицина у пациентов младше 18 лет отсутствуют.
Влияние других сильных индукторов изоферментов, метаболизирующих лекарственные средства, такие как фенитоин и фенобарбитал, на систему УДФ-ГТ1А1 неизвестно. Менее сильные индукторы (например, эфавиренз, невирапин, этравирин, рифабутин, ГКС, зверобой продырявленный, пиоглитазон) могут применяться одновременно с препаратом Исентресс® в рекомендованной дозе.
Одновременное применение препарата Исентресс® с сильными ингибиторами УДФ-ГТ1А1 (например, атазанавиром) может повысить концентрацию ралтегравира в плазме крови. Менее сильные ингибиторы УДФ-ГТ1А1 (например, индинавир и саквинавир) также могут повысить концентрацию ралтегравира в плазме крови, но в меньшей степени по сравнению с атазанавиром. Кроме того, тенофовир может повысить концентрацию ралтегравира в плазме крови, однако механизм этого влияния неизвестен.
Профиль безопасности, наблюдаемый у пациентов, получавших атазанавир и/или тенофовир, в целом идентичен профилю пациентов, которые не принимали данные препараты, поэтому коррекция дозы не требуется.
Одновременное применение препарата Исентресс® с антацидами, содержащими бивалентные ионы металлов, может снижать абсорбцию ралтегравира путем хелатирования, что приводит к снижению концентрации ралтегравира в плазме крови. Т.к. прием антацидов, содержащих алюминий или магний, через 6 часов после приема препарата Исентресс® приводит к значительному снижению концентрации ралтегравира в плазме крови, одновременное применение препарата Исентресс® и антацидов, содержащих алюминий или магний, не рекомендуется.
Одновременное применение препарата Исентресс® с антацидами, содержащими карбонат кальция, снижает концентрацию ралтегравира в плазме крови, однако данное взаимодействие не рассматривается как клинически значимое. Вследствие этого при одновременном применении препарата Исентресс® с антацидами, содержащими карбонат кальция, коррекция дозы не требуется.
Одновременное применение препарата Исентресс® с другими лекарственными средствами, повышающими значения рН желудочного сока (например, омепразол или фамотидин), может повысить скорость абсорбции ралтегравира и, соответственно, концентрацию ралтегравира в плазме крови. В клиническом исследовании профиль безопасности в подгруппе пациентов, принимавших ингибиторы протонного насоса или блокаторы гистаминовых Н2-рецепторов, был сопоставим с профилем безопасности в подгруппе пациентов, не принимавших данные лекарственные средства. Коррекция дозы препарата Исентресс® не требуется при одновременном применении с ингибиторами протонового насоса или блокаторами гистаминовых Н2-рецепторов.
Все исследования взаимодействия лекарственных средств проводились с участием взрослых пациентов.
Таблица 2. Данные по фармакокинетическому взаимодействию лекарственных средств у взрослых пациентов.
Условия хранения препарата Исентресс®
Препарат следует хранить в недоступном для детей месте при температуре не выше 25°С.
Срок годности препарата Исентресс®
Срок годности — 2.5 года. Не использовать по истечению срока годности, указанного на упаковке.
Условия реализации
Препарат отпускается по рецепту.
Контакты для обращений
МСД ФАРМАСЬЮТИКАЛС ООО
(Россия)

|
|
119021 Москва, |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Клинико-фармакологическая группа
Противовирусный препарат, активный в отношении ВИЧ
Действующее вещество
— ралтегравир (raltegravir)
Форма выпуска, состав и упаковка
Таблетки жевательные светло-желтого цвета с вкраплениями белого цвета, круглые, плоскоцилиндрические, со скошенными краями, с гравировкой логотипа компании [графический символ] на одной стороне и «473» на другой стороне.
| 1 таб. | |
| ралтегравир калия | 27.16 мг, |
| что соответствует содержанию ралтегравира | 25 мг |
Вспомогательные вещества: гипролоза — 2.362 мг, Опадрай бесцветный YS-1-19025-A1 — 1.771 мг, Surelease E-7-190402 — 2.657 мг, сукралоза — 2.334 мг, натрия сахаринат — 6.999 мг, натрия цитрата дигидрат — 1.167 мг, маннитол — 153.84 мг, краситель железа оксид желтый — 1.167 мг, аммония глицирризинат (Magnasweet 1353) — 2.334 мг, ароматизатор банановый натуральный WONF Durarome 501392 TD0991 — 4.667 мг, ароматизатор апельсиновый натуральный и искусственный 501331 TP0551 — 6.999 мг, ароматизатор маскирующий натуральный и искусственный 501482 TP04244 — 4.667 мг, кросповидон — 11.67 мг, магния стеарат — 1.167 мг, натрия стеарилфумарат — 2.334 мг.
60 шт. — флаконы из полиэтилена высокой плотности (1) — пачки картонные.
Таблетки жевательные светло-оранжевого цвета с вкраплениями белого цвета, овальные, двояковыпуклые, с гравировкой логотипа компании [графический символ] и «477», разделенных риской, на одной стороне и с риской на другой стороне.
| 1 таб. | |
| ралтегравир калия | 108.6 мг, |
| что соответствует содержанию ралтегравира | 100 мг |
Вспомогательные вещества: гипролоза — 9.448 мг, Опадрай бесцветный YS-1-19025-A1 — 7.085 мг, Surelease E-7-190402 — 10.63 мг, сукралоза — 4.667 мг, натрия сахаринат — 14 мг, натрия цитрата дигидрат — 2.333 мг, маннитол — 239.6 мг, краситель железа оксид красный — 0.28 мг, краситель железа оксид желтый — 2.333 мг, аммония глицирризинат (Magnasweet 1353) — 4.667 мг, ароматизатор банановый натуральный WONF Durarome 501392 TD0991 — 9.334 мг, ароматизатор апельсиновый натуральный и искусственный 501331 TP0551 — 14 мг, ароматизатор маскирующий натуральный и искусственный 501482 TP04244 — 9.334 мг, кросповидон — 23.34 мг, магния стеарат — 2.334 мг, натрия стеарилфумарат — 4.667 мг.
60 шт. — флаконы из полиэтилена высокой плотности (1) — пачки картонные.
1 — Опадрай бесцветный YS-1-19025-A состоит из гипромеллозы 2910/6cP и макрогола;
2 — Surelease E-7-19040 состоит из 25% водной суспензии этилцеллюлозы в воде очищенной,этилцеллюлозы 20сР, аммония гидроксида, триглицеридов среднецепочных и олеиновой кислоты;
3 — Magnasweet 135 состоит из экстракта солодки, сорбитола и фруктозы;
4 — содержит аспартам.
Фармакологическое действие
Ралтегравир ингибирует каталитическую активность ВИЧ интегразы — фермента, участвующего в репликации вируса ВИЧ. Ингибирование интегразы предотвращает ковалентное введение (интеграцию) генома ВИЧ в геном клетки хозяина на ранних стадиях развития инфекции. Не включенные в ДНК человека геномы ВИЧ не способны индуцировать продукцию новых вирусных частиц, поэтому подавление процесса интеграции предотвращает распространение вирусной инфекции в организме. Ингибирующая способность ралтегравира в отношении фосфотрансфераз человека, включая ДНК-полимеразы α, β и γ, выражена незначительно.
Микробиология
При плазменной концентрации 31±20 нмоль/л ралтегравир обеспечивал подавление репликации вируса на 95% (95% ингибирующая концентрация, ИК95) в клеточных культурах человеческих Т-лимфоцитов, инфицированных адаптированным к культурам клеток вариантом H9IIIB ВИЧ-1 по сравнению с контрольной вирус-инфицированной культурой клеток. ИК95 достигалась в концентрациях от 6 до 50 нмоль/л в культурах человеческих митоген-активированных мононуклеаров периферической крови, инфицированных различными первичными клиническими штаммами ВИЧ-1, включая штаммы 5 не-В подтипов ВИЧ-1, а также штаммы, резистентные к ингибиторам обратной транскриптазы и ингибиторам протеазы ВИЧ.
При анализе одного цикла инфекции ралтегравир подавлял инфицирование, вызванное 23 штаммами ВИЧ, представляющими 5 не-В подтипов и 5 циркулирующих рекомбинантных форм, с ИК50 — 5-12 нмоль/л. Ралтегравир также подавлял репликацию штаммов ВИЧ-2 при тестировании на клетках линии СЕМх174 (ИК95 = 6 нмоль/л). При одновременном введении в культуру человеческих Т-лимфоцитов, инфицированных вариантом H9IIIB вируса ВИЧ-1, ралтегравира и нуклеозидных ингибиторов обратной транскриптазы (зидовудин, залцитабин, ставудин, абакавир, тенофовир, диданозин и ламивудин), ненуклеозидных ингибиторов обратной транскриптазы (эфавиренз, невирапин и делавирдин), ингибиторов протеазы ВИЧ (индинавир, саквинавир, ритонавир, ампренавир, лопинавир, нелфинавир и атазанавир) или ингибитора слияния (энфувиртид) наблюдалась антиретровирусная активность от аддитивной до синергичной.
Резистентность к препарату
Мутации интегразы ВИЧ-1, способствующие появлению резистентных к ралтегравиру штаммов вируса (развивались in vitro или у пациентов, принимавших ралтегравир), в основном включают замены в положениях 155 (N155 замена на Н), 148 (Q148 замена на Н, К или R) или 143 (Y143 замена на С, Н или R), в сочетании с одной или более дополнительными мутациями (например, L74M, E92Q, Т97А, Е138А/К, G140A/S, V151I, G163R, S230R).
Рекомбинантные вирусы с одной первичной мутацией (Q148H, К или R или N155H) отличались сниженной способностью к репликации и сниженной чувствительностью к ралтегравиру in vitro. Вторичные мутации вируса еще больше снижали чувствительность к ралтегравиру, иногда компенсируя сниженную способность вируса к репликации.
Мутации, ассоциированные с развитием резистентности к ралтегравиру, также могут приводить к формированию резистентности к другому ингибитору переноса цепи интегразой элвитегравиру. При замене в положении 143 чувствительность к ралтегравиру снижается в большей степени, чем чувствительность к элвитегравиру, тогда как мутации в E92Q вызывают большую резистентность к элвитегравиру, чем к ралтегравиру. У вирусов с мутацией в положении 148 в сочетании с одной и более дополнительными мутациями, вызывающими резистентность к ралтегравиру, также может наблюдаться клинически значимая резистентность к долутегравиру.
Влияние на электрофизиологическую активность сердца или на показатели ЭКГ
В плацебо-контролируемом клиническом исследовании с участием здоровых добровольцев однократный прием 1600 мг ралтегравира не оказывал влияния на продолжительность интервала QTc несмотря на то, что Cmax ралтегравира в плазме крови была в 4 раза больше, чем при однократном приеме ралтегравира в дозе 400 мг.
Фармакокинетика
У взрослых пациентов
Всасывание
Ралтегравир быстро всасывается после приема препарата натощак, Cmax в плазме крови определяется примерно через 3 часа. Значения AUC и Cmax ралтегравира увеличиваются пропорционально дозе в диапазоне доз от 100 до 1600 мг. Значения С12ч ралтегравира возрастают пропорционально дозе в диапазоне доз от 100 мг до 800 мг и возрастают в несколько меньшей степени — в диапазоне доз от 100 мг до 1600 мг.
При режиме приема препарата 2 раза/сут равновесное состояние достигается быстро, примерно в течение 2 дней после начала лечения. Значения AUC и Cmax свидетельствуют в пользу отсутствия или минимальной кумуляции препарата, значение С12ч — в пользу незначительной кумуляции препарата. В режиме монотерапии по 400 мг 2 раза/сут значение среднего геометрического для AUC0-12ч составляло 14.3 мкмоль/л х ч, значение С12ч — 142 нмоль/л.
Абсолютная биодоступность ралтегравира не установлена. Ралтегравир можно принимать вне зависимости от режима приема пищи.
Распределение
Примерно 83% ралтегравира связывается с белками плазмы в диапазоне концентраций от 2 до 10 мкмоль/л. Ралтегравир легко преодолевал плацентарный барьер в экспериментальных исследованиях на крысах, но не проникал через гематоэнцефалический барьер в заметной степени.
В двух клинических исследованиях с участием пациентов, инфицированных ВИЧ-1, которые принимали ралтегравир в дозе 400 мг 2 раза/сут, ралтегравир быстро определялся в спинномозговой жидкости. В первом исследовании средняя концентрация ралтегравира в спинномозговой жидкости составила 5.8% (в диапазоне от 1 до 53.5%) от соответствующей концентрации в плазме крови, а во втором исследовании — 3% (в диапазоне от 1 до 61%) от соответствующей концентрации в плазме крови. Медианы полученных значений были приблизительно в 3-6 раз ниже, чем концентрации свободной фракции ралтегравира в плазме крови.
Метаболизм и выведение
Исследования с использованием селективных ингибиторов к изоформе фермента уридиндифосфат-глюкуронилтрансферазы (УДФ-ГТ), полученной путем экспрессии комплементарной ДНК, показали, что УДФ-ГТ1А1 является основным ферментом, участвующим в образовании ралтегравир-глюкуронида. Эти данные показали, что основной путь метаболизма ралтегравира у человека представлен процессом глюкуронирования, опосредованного УДФ-ГТ1А1. T1/2 ралтегравира в конечной фазе составляет около 9 ч, большая часть AUC соответствует более короткой α-фазе кажущегося T1/2 ралтегравира (составляет примерно 1 ч). После приема внутрь радиоактивно меченого ралтегравира примерно 51% от принятой дозы выводилось через кишечник и 32% — через почки. В кале обнаруживался только ралтегравир, который, вероятно, образовывался путем гидролиза ралтегравир-глюкуронида, выделившегося с желчью. В моче определялись ралтегравир и ралтегравир-глюкуронид в количестве 9% и 23% от принятой дозы соответственно. В плазме крови основным циркулирующим радиоактивным компонентом был ралтегравир (примерно 70% от общей радиоактивности), в то время как на ралтегравир-глюкуронид приходилось только 30%.
Фармакокинетика у отдельных групп пациентов
Пол
Пол не оказывает клинически значимого влияния на фармакокинетические параметры ралтегравира. Коррекция дозы препарата в зависимости от пола пациента не требуется.
Пожилые пациенты
В исследованиях с участием пациентов в возрасте 18 лет и старше не было обнаружено значимой зависимости фармакокинетических параметров ралтегравира от возраста пациентов, поэтому коррекция дозы препарата в зависимости от возраста не требуется.
Подростки и дети
По результатам сравнительного исследования у здоровых взрослых добровольцев таблетки жевательные обладают более высокой пероральной биодоступностью по сравнению с таблетками, покрытыми пленочной оболочкой, по 400 мг. В этом исследовании применение таблеток жевательных с пищей с высоким содержанием жиров, приводило к повышению AUC в среднем на 6%, снижению Cmax на 62% и повышению С12 ч на 188% по сравнению с приемом препарата натощак. Прием таблеток жевательных с пищей с высоким содержанием жиров не оказывал клинически значимого влияния на фармакокинетику ралтегравира, поэтому таблетки жевательные могут применяться независимо от приема пищи.
Дозы для подростков и детей старше 2 лет для лечения ВИЧ-1 инфекции рекомендованы на основании того, что фармакокинетические параметры ралтегравира сопоставимы с таковыми у взрослых пациентов, принимавших Исентресс, таблетки, покрытые пленочной оболочкой, по 400 мг 2 раза/сут.
Фармакокинетика ралтегравира в лекарственной форме таблетки жевательные у детей младше 2 лет не изучалась.
Пациенты из разных расово-этнических групп
Расово-этническая принадлежность не оказывала клинически значимого влияния на фармакокинетические параметры ралтегравира. Коррекция дозы не требуется.
Пациенты с различным индексом массы тела (ИМТ)
ИМТ не оказывал клинически значимого влияния на фармакокинетические параметры ралтегравира у взрослых пациентов. Коррекция дозы препарата в зависимости от ИМТ пациента не требуется.
Пациенты с печеночной недостаточностью
Ралтегравир выводится преимущественно путем глюкуронирования в печени. Фармакокинетика препарата была изучена у взрослых пациентов с печеночной недостаточностью средней степени тяжести, а также в комбинированном фармакокинетическом анализе. Клинически значимых отклонений фармакокинетических параметров у взрослых пациентов с печеночной недостаточностью средней степени тяжести по сравнению со здоровыми добровольцами не выявлено. Таким образом, коррекция дозы препарата при печеночной недостаточности легкой и средней степени тяжести не требуется. Влияние печеночной недостаточности тяжелой степени на фармакокинетические параметры ралтегравира не изучалось.
Пациенты с почечной недостаточностью
На почечный клиренс приходится незначительная доля в выведении ралтегравира из организма. Фармакокинетика препарата была изучена у взрослых пациентов с тяжелой степенью почечной недостаточности, а также в сложном фармакокинетическом анализе. Клинически значимых отклонений фармакокинетических параметров у пациентов с тяжелой степенью почечной недостаточности по сравнению со здоровыми добровольцами не выявлено. Таким образом, коррекции дозы препарата пациентам с тяжелой степенью почечной недостаточности не требуется. Поскольку эффективность диализа ралтегравира неизвестна, принимать препарат накануне сеанса диализа не рекомендуется.
Пациенты с полиморфизмом УДФ-ГТ1А1
Доказательства или какие-либо данные, свидетельствующие, что наличие полиморфизма у фермента УДФ-ГТ1А1 может оказывать клинически значимое влияние на фармакокинетические параметры ралтегравира, не были получены. По данным сравнительного исследования с участием 30 взрослых здоровых добровольцев с генетически-детерминированной сниженной активностью УДФ-ГТ1А1 и 27 взрослых здоровых добровольцев с неизмененным генотипом УДФ-ГТ1А1 отношение средних геометрических AUC ралтегравира составило 1.41 (90% доверительный интервал составил 0.96; 2.09).
Показания
- лечение ВИЧ-1 инфекции в комбинации с другими антиретровирусными препаратами у детей в возрасте 2-11 лет, как ранее получавших, так и не получавших антиретровирусную терапию.
Противопоказания
- повышенная чувствительность к ралтегравиру и другим компонентам препарата;
- детский возраст до 2 лет и масса тела менее 7 кг;
- беременность;
- период лактации;
- дефицит сахаразы/изомальтазы, непереносимость фруктозы, глюкозо-галактозная мальабсорбция;
- фенилкетонурия.
С осторожностью:
- миопатия и рабдомиолиз (в т.ч. в анамнезе), наличие состояний и факторов, предрасполагающих к их развитию;
- печеночная недостаточность тяжелой степени;
- одновременное применение с сильными индукторами УДФ-ГТ1А1 (рифампицин);
- одновременное применение препарата Исентресс с антацидами, содержащими алюминий или магний;
- депрессия, включая суицидальные идеи и поведение (наблюдалась в основном у пациентов с депрессией или психиатрическими заболеваниями в анамнезе). Следует соблюдать осторожность при назначении препарата Исентресс пациентам с депрессией или психиатрическими заболеваниями в анамнезе.
Дозировка
Внутрь. Таблетки жевательные препарата Исентресс назначают вне зависимости от приема пищи.
Лечение препаратом Исентресс должен проводить врач, обладающий достаточным опытом терапии ВИЧ-инфекции.
Т.к. лекарственные формы ралтегравира не являются биоэквивалентными, то таблетки жевательные не следует заменять таблетками, покрытыми пленочной оболочкой, по 400 мг. Исследований препарата Исентресс в форме таблеток жевательных у ВИЧ-инфицированных детей в возрасте от 12 до 18 лет и взрослых не проводилось.
Максимальная суточная доза таблеток жевательных составляет 300 мг 2 раза/сут.
Лечение препаратом Исентресс проводят в комбинации с другими антиретровирусными препаратами.
Рекомендуемые дозы препарата Исентресс в лекарственной форме таблетки жевательные для лечения ВИЧ-1 инфекции у детей в возрасте 2-11 лет рассчитывают по массе тела так, чтобы максимальная суточная доза ралтегравира не превышала 300 мг 2 раза в сутки (см. таблицу 1).
Таблица 1. Рекомендованные дозы* препарата Исентресс в лекарственной форме таблетки жевательные для детей в возрасте 2-11 лет.
| Масса тела, кг | Доза | Количество таблеток жевательных |
| от 7 до < 10 | 50 мг 2 раза/сут | 0.5 × 100 мг1 2 раза/сут |
| от 10 до < 14 | 75 мг 2 раза/сут | 3 × 25 мг 2 раза/сут |
| от 14 до < 20 | 100 мг 2 раза/сут | 1 × 100 мг 2 раза/сут |
| от 20 до < 28 | 150 мг 2 раза/сут | 1.5 × 100 мг1 2 раза/сут |
| от 28 до < 40 | 200 мг 2 раза/сут | 2 × 100 мг 2 раза/сут |
| не менее 40 | 300 мг 2 раза/сут | 3 × 100 мг 2 раза/сут |
*рекомендации доз по массе тела основаны ориентировочно на приеме 6 мг/кг/доза 2 раза/сут.
1таблетки жевательные по 100 мг — могут быть разделены на две половины. Тем не менее, следует по возможности избегать деления таблеток на две половины.
Необходимо строго соблюдать график дозирования, поскольку дозу препарата Исентресс следует корректировать по мере роста ребенка.
У взрослых и детей от 12 лет и массой тела не менее 25 кг следует использовать препарат Исентресс таблетки, покрытые оболочкой, 400 мг.
У пациентов с нарушением функции почек коррекция дозы не требуется.
У пациентов с нарушением функции печени легкой и средней степени тяжести коррекция дозы не требуется. Безопасность и эффективность применения ралтегравира у пациентов с нарушением функции печени тяжелой степени не установлены. Поэтому необходимо соблюдать осторожность при применении препарата Исентресс у пациентов с нарушением функции печени тяжелой степени (см. разделы «Фармакологическое действие», «Фармакокинетика», «Особые указания»). При появлении у таких пациентов признаков ухудшения заболевания печени следует рассмотреть вопрос о прерывании или прекращении лечения.
Побочные действия
Профиль безопасности препарата Исентресс основан на результатах обобщенных данных по безопасности, полученных в ходе клинических исследований с участием пациентов, ранее получавших антиретровирусную терапию (АРВТ), и пациентов, ранее не получавших АРВТ.
В объединенном анализе результатов клинических исследований антиретровирусной терапии у взрослых пациентов, ранее получавших АРВТ, частота отмены терапии по причине нежелательных реакций составила 3.9% в группе пациентов, принимавших препарат Исентресс и оптимизированную дополнительную терапию (ОДТ), и 4.6% в группе пациентов, принимавших плацебо и ОДТ. Частота отмены терапии по причине нежелательных реакций у взрослых пациентов, ранее не получавших АРВТ, составила 5.0% в группе пациентов, принимавших препарат Исентресс одновременно с эмтрицитабином и тенофовиром, и 10.0% в группе пациентов, принимавших одновременно эфавиренз, эмтрицитабин и тенофовир.
Ниже представлены данные о нежелательных явлениях, наблюдавшихся в клинических исследованиях, с различной степенью вероятности связанных с препаратом Исентресс или его комбинацией с другой АРВТ.
Нежелательные явления перечислены в соответствии с системно-органными классами и классификацией по частоте: часто (≥1/100 и <1/10), нечасто (≥1/1000 и <1/100).
Инфекционные и паразитарные заболевания: нечасто — генитальный герпес, фолликулит, гастроэнтерит, простой герпес, герпетическая инфекция, опоясывающий лишай, грипп, абсцесс лимфоузла, контагиозный моллюск, назофарингит, инфекция верхних дыхательных путей.
Доброкачественные, злокачественные и неуточненные новообразования (включая кисты и полипы): нечасто — папилломатоз кожи.
Со стороны системы кроветворения и лимфатической системы: нечасто — анемия, железодефицитная анемия, болезненность лимфоузлов, лимфаденопатия, нейтропения, тромбоцитопения1.
Со стороны иммунной системы: нечасто — синдром восстановления иммунитета, гиперчувствительность к препарату, реакции гиперчувствительности.
Со стороны обмена веществ: часто — снижение аппетита; нечастые — кахексия, сахарный диабет, дислипидемия, гиперхолестеринемия, гипергликемия, гиперлипидемия, гиперфагия, повышение аппетита, полидипсия, нарушение жирового обмена.
Нарушения психики: часто — необычные сновидения, бессонница, ночные кошмары, нарушение поведения2, депрессия; нечасто — психические расстройства, суицидальные попытки, чувство тревоги, спутанность сознания, подавленное настроение, большое депрессивное расстройство, бессонница середины ночи, изменения настроения, панические атаки, нарушения сна, суицидальные идеи1, суицидальное поведение1 (особенно у пациентов с психиатрическими заболеваниями в анамнезе).
Со стороны нервной системы: часто — головокружение, головная боль, психомоторная гиперреактивность2, нечасто — амнезия, синдром запястного канала, когнитивные расстройства, нарушения внимания, постуральное головокружение, дисгевзия, гиперсомния, гипестезия, летаргия, расстройство памяти, мигрень, периферическая невропатия, парестезии, сонливость, головная боль напряжения, тремор, снижение качества сна.
Со стороны органа зрения: нечасто — снижение остроты зрения.
Со стороны органа слуха и лабиринтные нарушения: часто — вертиго; нечастые — шум в ушах.
Со стороны сердечно-сосудистой системы: нечасто — ощущение сердцебиения, синусовая брадикардия, желудочковая экстрасистолия, приливы крови к коже лица с ощущением жара, артериальная гипертензия.
Со стороны дыхательной системы, органов грудной клетки и средостения: нечасто — дисфония, носовое кровотечение, заложенность носа.
Со стороны пищеварительной системы: часто — чувство распирания в животе, боль в животе, диарея, метеоризм, тошнота, рвота, диспепсия; нечасто — гастрит, ощущение дискомфорта в животе, боль в верхних отделах живота, болезненность в области живота, чувство дискомфорта в области заднего прохода, запор, сухость во рту, ощущение дискомфорта в эпигастральной области, эрозивный дуоденит, отрыжка, гастроэзофагеальный рефлюкс, гингивит, глоссит, болезненность при глотании, острый панкреатит, пептическая язва, ректальные кровотечения.
Со стороны печени и желчевыводящих путей: нечасто — гепатит, стеатоз печени, алкогольный гепатит, печеночная недостаточность1.
Со стороны кожи и подкожных тканей: часто — кожная сыпь; нечасто — акне, алопеция, угревидная сыпь, сухость кожи, эритема, липоатрофия лица, гипергидроз, липоатрофия, приобретенная липодистрофия, липогипертрофия, ночная потливость, пруриго, зуд (локальный и генерализованный), макулярная сыпь, макуло-папулезная сыпь, зудящая сыпь, крапивница, ксеродермия, другие поражения кожи, синдром Стивенса-Джонсона1, лекарственная сыпь с эозинофилией и системными симптомами (DRESS-синдром)1.
Со стороны костно-мышечной системы: нечасто — артралгия, артрит, боль в спине, боль в боку, миалгия, боль в области шеи, остеопения, боль в конечностях, остеопороз, полиартрит, тендинит, миопатия, рабдомиолиз1.
Со стороны почек и мочевыводящих путей: нечасто — почечная недостаточность, нефрит, нефролитиаз, никтурия, киста почки, нарушение функции почек, тубулоинтерстициальный нефрит.
Со стороны половых органов и молочной железы: нечасто — эректильная дисфункция, гинекомастия, симптомы менопаузы.
Общие расстройства: часто — астения, слабость, лихорадка; нечасто — дискомфорт в груди, озноб, отек лица, увеличение объема жировой ткани, состояние беспокойства, недомогание, подчелюстное новообразование, периферические отеки, боль.
Лабораторные и инструментальные данные: часто — повышение активности в плазме АЛТ, АСТ, липазы и амилазы поджелудочной железы, повышение концентрации триглицеридов и количества атипичных лимфоцитов; нечасто — снижение абсолютного числа нейтрофилов плазмы; повышение активности в плазме ЩФ, КФК, снижение концентрации альбумина; повышение концентрации билирубина, холестерина, креатинина, глюкозы (в т.ч. определяемой натощак), азота мочевины, холестерина ЛПВП, холестерина ЛПНП; повышение значения МНО; снижение количества тромбоцитов и лейкоцитов в крови; наличие глюкозы в моче, наличие эритроцитов в моче; увеличение окружности талии; увеличение или снижение массы тела.
Травмы, интоксикации и осложнения манипуляций: нечасто — непреднамеренная передозировка.
1Нежелательные явления, не связанные с применением препарата Исентресс, которые наблюдались в пострегистрационном периоде и не наблюдались в ходе клинических исследований.
2У одного пациента детского возраста наблюдались связанные с приемом препарата нежелательные реакции: психомоторная гиперреактивность 3 степени и нарушение поведения; также у данного пациента наблюдалась бессонница.
В ходе клинических исследований у пациентов, ранее получавших и не получавших АРВТ, наблюдались случаи развития злокачественных новообразований при использовании комбинации препарата Исентресс с другими антиретровирусными средствами. Характеристика и частота злокачественных новообразований соответствовали таковым для пациентов с тяжелым иммунодефицитом. Риск развития злокачественных новообразований в клинических исследованиях был одинаков как в группах пациентов, принимавших препарат Исентресс, так и в группах пациентов, принимавших препараты сравнения.
У пациентов, принимавших препарат Исентресс, наблюдалось повышение активности КФК 2-4 степени. Наблюдались случаи развития миопатии и рабдомиолиза. Пациентам с миопатией или рабдомиолизом в анамнезе, а также имеющим другие факторы риска (включая сопутствующую терапию), препарат следует назначать с осторожностью.
Сообщалось о случаях развития остеонекроза, особенно у пациентов с общепризнанными факторами риска, поздней стадией ВИЧ-заболевания или длительным воздействием комбинированной АРВТ. Частота его развития неизвестна.
В клинических исследованиях у пациентов, ранее получавших АРВТ, кожная сыпь, вне зависимости от этиологии, чаще наблюдалась при применении препарата Исентресс одновременно с дарунавиром, чем при применении данных препаратов по отдельности. Тем не менее, частота развития кожной сыпи, связанной с приемом препаратов, была сопоставима в этих группах лечения. Кожная сыпь была легкой и умеренной степени тяжести и не влияла на продолжение АРВТ. У пациентов, ранее не получавших АРВТ, при лечении препаратом Исентресс в комбинации с эмтрицитабином и тенофовиром развитие сыпи наблюдалось реже, чем при лечении эфавирензом в комбинации с эмтрицитабином и тенофовиром.
Пациенты с ко-инфекцией гепатита В и/или гепатита С
В целом профиль безопасности препарата Исентресс у пациентов, как ранее получавших, так и не получавших АРВТ, ко-инфицированных хроническим (но не острым) активным гепатитом В и/или гепатитом С, был аналогичен профилю безопасности у пациентов без ко-инфекции гепатита В и/или гепатита С, хотя частота отклонения активности АЛТ и ACT иногда была выше в группах с ко-инфекцией гепатита В и/или гепатита С.
Дети
По результатам клинических исследований по применению ралтегравира в рекомендованных дозах в комбинации с другими антиретровирусными лекарственными средствами у ВИЧ-1 инфицированных детей и подростков от 2 до 18 лет было установлено, что частота, тип и выраженность нежелательных реакций, связанных с приемом препарата, были сопоставимы с таковыми у взрослых пациентов. У одного пациента наблюдались связанные с приемом препарата нежелательные реакции: психомоторная гиперактивность 3 степени, нарушение поведения и бессонница. У другого пациента наблюдалась серьезная нежелательная реакция 2 степени — аллергическая сыпь. Еще у одного пациента наблюдалось повышение активности ACT 4 степени и АЛТ 3 степени, которое было расценено как серьезное.
Передозировка
Специфических симптомов передозировки препарата Исентресс не выявлено. Ралтегравир хорошо переносился здоровыми добровольцами в режиме 1600 мг 1 раз/сут и 800 мг 2 раза/сут, без каких-либо проявлений токсичности. Однократный прием дозы 1800 мг/сут в исследованиях II/III фазы не оказывал токсического воздействия. На основании имеющихся данных можно заключить, что ралтегравир хорошо переносится в дозах до 800 мг 2 раза/сут, а также при приеме с препаратами, увеличивающими его экспозицию на 50-70% (например, тенофовиром и атазанавиром). Ралтегравир имеет широкий терапевтический диапазон, поэтому потенциал токсического действия в результате передозировки ограничен.
Лечение: в случае передозировки необходимо следовать стандартным рекомендациям, таким, как удаление невсосавшегося препарата из ЖКТ, наблюдение за показателями жизнедеятельности, включая ЭКГ, назначение симптоматической терапии. Данных об эффективности диализа при передозировке препаратом Исентресс нет.
Лекарственное взаимодействие
В исследованиях in vitro было показано, что ралтегравир не является субстратом изоферментов системы цитохрома Р450 и не ингибирует CYP1A2, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6 или CYP3A. Кроме этого, in vitro ралтегравир ие индуцирует CYP3A4 и не является ингибитором P-гликопротеин-опосредованного транспорта. На основании этих данных можно сделать вывод, что Исентресс не влияет на фармакокинетические параметры лекарственных средств, которые являются субстратами указанных ферментов или Р-гликопротеина.
Как показали исследования in vitro и in vivo, ралтегравир выводится в основном посредством метаболизма (глюкуронирования) по УДФ-ГТ1А1-опосредованному пути. Хотя исследования in vitro показали, что ралтегравир не является ингибитором УДФ-ГТ1А1 и 2В7, в одном клиническом исследовании были выявлены некоторые признаки ингибирования УДФ-ГТ1А1 in vivo на основе наблюдаемого влияния на глюкуронирование билирубина. Тем не менее маловероятно, что данный эффект приводит к клинически значимому лекарственному взаимодействию.
В фармакокинетике ралтегравира наблюдалась значимая интер- и интраиндивидуальная изменчивость. Приведенная ниже информация о взаимодействии с лекарственными средствами основана на средних геометрических значениях; эффект у отдельного пациента точно предсказать нельзя.
Влияние ралтегравира на фармакокинетику других лекарственных средств
В исследованиях по изучению лекарственного взаимодействия ралтегравир не оказывал клинически значимого влияния на фармакокинетику этравирина, маравирока, тенофовира, гормональных контрацептивов, метадона и мидазолама.
В некоторых исследованиях при одновременном применении препарата Исентресс с дарунавиром наблюдалось незначительное снижение концентрации дарунавира в плазме крови. Механизм данного явления неизвестен. Тем не менее, влияние ралтегравира на концентрацию дарунавира в плазме крови не считается клинически значимым.
Влияние других лекарственных средств на фармакокинетику ралтегравира
Следует соблюдать осторожность при одновременном применении препарата Исентресс с сильными индукторами УДФ-ГТ1А1 (например, рифампицином), учитывая, что ралтегравир метаболизируется в основном посредством УДФ-ГТ1А1. Рифампицин снижает концентрации ралтегравира в плазме крови. Влияние на эффективность ралтегравира неизвестно. Тем не менее, если одновременного применения с рифампицином избежать невозможно, можно удвоить дозу препарата Исентресс у взрослых. Данные по одновременному применению препарата Исентресс и рифампицина у пациентов младше 18 лет отсутствуют.
Влияние других сильных индукторов изоферментов, метаболизирующих лекарственные средства, такие как фенитоин и фенобарбитал, на систему УДФ-ГТ1А1 неизвестно. Менее сильные индукторы (например, эфавиренз, невирапин, этравирин, рифабутин, ГКС, зверобой продырявленный, пиоглитазон) могут применяться одновременно с препаратом Исентресс в рекомендованной дозе.
Одновременное применение препарата Исентресс с сильными ингибиторами УДФ-ГТ1А1 (например, атазанавиром) может повысить концентрацию ралтегравира в плазме крови. Менее сильные ингибиторы УДФ-ГТ1А1 (например, индинавир и саквинавир) также могут повысить концентрацию ралтегравира в плазме крови, но в меньшей степени по сравнению с атазанавиром. Кроме того, тенофовир может повысить концентрацию ралтегравира в плазме крови, однако механизм этого влияния неизвестен.
Профиль безопасности, наблюдаемый у пациентов, получавших атазанавир и/или тенофовир, в целом идентичен профилю пациентов, которые не принимали данные препараты, поэтому коррекция дозы не требуется.
Одновременное применение препарата Исентресс с антацидами, содержащими бивалентные ионы металлов, может снижать абсорбцию ралтегравира путем хелатирования, что приводит к снижению концентрации ралтегравира в плазме крови. Т.к. прием антацидов, содержащих алюминий или магний, через 6 часов после приема препарата Исентресс приводит к значительному снижению концентрации ралтегравира в плазме крови, одновременное применение препарата Исентресс и антацидов, содержащих алюминий или магний, не рекомендуется.
Одновременное применение препарата Исентресс с антацидами, содержащими карбонат кальция, снижает концентрацию ралтегравира в плазме крови, однако данное взаимодействие не рассматривается как клинически значимое. Вследствие этого при одновременном применении препарата Исентресс с антацидами, содержащими карбонат кальция, коррекция дозы не требуется.
Одновременное применение препарата Исентресс с другими лекарственными средствами, повышающими значения рН желудочного сока (например, омепразол или фамотидин), может повысить скорость абсорбции ралтегравира и, соответственно, концентрацию ралтегравира в плазме крови. В клиническом исследовании профиль безопасности в подгруппе пациентов, принимавших ингибиторы протонового насоса или блокаторы гистаминовых Н2-рецепторов, был сопоставим с профилем безопасности в подгруппе пациентов, не принимавших данные лекарственные средства. Коррекция дозы препарата Исентресс не требуется при одновременном применении с ингибиторами протонового насоса или блокаторами гистаминовых Н2-рецепторов.
Все исследования взаимодействия лекарственных средств проводились с участием взрослых пациентов.
Таблица 2. Данные по фармакокинетическому взаимодействию лекарственных средств у взрослых пациентов.
| Лекарственное средство с учетом терапевтической области применения | Взаимодействие (механизм, если известен) | Рекомендации по коррекции режима дозирования |
| Антиретровирусные лекарственные средства | ||
| Ингибиторы протеазы | ||
| атазанавир/ритонавир (ралтегравир 400 мг 2 раза/сут) |
ралтегравир AUC↑ 41% ралтегравир C12ч ↑ 77% ралтегравир Cmax ↑ 24% (ингибирование УДФ-ГТ1А1) |
Коррекция дозы препарата Исентресс не требуется. |
| типранавир/ритонавир (ралтегравир 400 мг 2 раза/сут) | ралтегравир AUC↓ 24% ралтегравир C12ч ↓ 55% ралтегравир Cmax ↓ 18% (индукция УДФ-ГТ1А1) |
Коррекция дозы препарата Исентресс не требуется. |
| Ненуклеозидные ингибиторы обратной транскриптазы (ННИОТ) | ||
| эфавиренз (ралтегравир 400 мг 1 раз/сут) | ралтегравир AUC↓ 36% ралтегравир C12ч ↓ 21% ралтегравир Cmax ↓ 36% (индукция УДФ-ГТ1А1) |
Коррекция дозы препарата Исентресс не требуется. |
| этравирин (ралтегравир 400 мг 2 раза/сут) | ралтегравир AUC↓ 10% ралтегравир C12ч ↓ 34% ралтегравир Cmax ↓ 11% (индукция УДФ-ГТ1А1) этравирин AUC↑ 10% этравирин C12ч ↑ 17% этравирин Cmax ↑ 4% |
Коррекция доз препарата Исентресс или этравирина не требуется. |
| Нуклеозидные ингибиторы обратной транскриптазы (НИОТ) | ||
| тенофовир (ралтегравир 400 мг 2 раза/сут) | ралтегравир AUC↑ 49% ралтегравир C12ч ↑ 3% ралтегравир Cmax ↑ 64% (механизм взаимодействия неизвестен) тенофовир AUC ↓10% тенофовир C12ч ↓ 13% тенофовир Cmax ↓ 23% |
Коррекция доз препарата Исентресс или тенофовира дизопроксила фумарата не требуется. |
| Антагонисты хемокиновых рецепторов CCR5 | ||
| маравирок (ралтегравир 400 мг 2 раза/сут) | ралтегравир AUC↓ 37% ралтегравир C12ч ↓28% ралтегравир Cmax ↓ 33% (механизм взаимодействия неизвестен) маравирок AUC↓ 14% маравирок C12ч ↓ 10% маравирок Cmax ↓ 21% |
Коррекции доз препарата Исентресс или маравирока не требуется. |
| Лекарственные средства против вируса гепатита С | ||
| Ингибиторы протеазы NS3/4A вируса гепатита С | ||
| боцепревир (ралтегравир 400 мг 1 раз/сут) | ралтегравир AUC↑ 4% ралтегравир C12ч↓ 25% ралтегравир Cmax ↑ 11% (механизм взаимодействия неизвестен) |
Коррекция доз препарата Исентресс или боцепревира не требуется. |
| Противомикробные препараты | ||
| Противотуберкулезные препараты | ||
| рифампицин (ралтегравир 400 мг 1 раз/сут) | ралтегравир AUC↓ 40% ралтегравир C12ч ↓ 61% ралтегравир Cmax ↓ 38% (индукция УДФ-ГТ1А1) |
Рифампицин снижает концентрацию ралтегравира в плазме крови. Если комбинированной терапии с рифампицином избежать невозможно, необходимо рассмотреть возможность увеличения дозы препарата Исентресс в 2 раза. |
| Седативные препараты | ||
| мидазолам (ралтегравир 400 мг 2 раза/сут) | мидазолам AUC↓ 8% мидазолам Cmax↑ 3% |
Коррекция доз препарата Исентресс или мидазолама не требуется. Полученные данные указывают на то, что ралтегравир не является индуктором или ингибитором CYP3A4 и что ралтегравир не влияет на фармакокинетику лекарственных средств, являющихся субстратами CYP3A4. |
| Антациды | ||
| Антациды, содержащие алюминий или магний (ралтегравир 400 мг 2 раза/сут) | Одновременно с ралтегравиром ралтегравир AUC↓ 49% ралтегравир C12ч ↓63% ралтегравир Cmax ↓ 44% За 2 ч до приема ралтегравира ралтегравир AUC↓ 51% ралтегравир C12ч ↓56% ралтегравир Cmax ↓51% Через 2 ч после приема ралтегравира ралтегравир AUC↓ 30% ралтегравир C12ч ↓57% ралтегравир Cmax ↓22% За 6 ч до приема ралтегравира ралтегравир AUC↓ 13% ралтегравир C12ч ↓50% ралтегравир Cmax ↓10% Через 6 ч после приема ралтегравира ралтегравир AUC↓ 11% ралтегравир C12ч ↓49% ралтегравир Cmax ↓10% (хелатирование катионами металлов) |
Антациды, содержащие алюминий или магний, снижают концентрацию ралтегравира в плазме крови. Одновременное применение препарата Исентресс и антацидов, содержащих алюминий или магний, не рекомендовано. |
| Антациды, содержащие кальция карбонат (ралтегравир 400 мг 2 раза/сут) | ралтегравир AUC↓55% ралтегравир C12ч ↓32% ралтегравир Cmax ↓52% (хелатирование катионами металлов) |
Коррекция дозы препарата Исентресс не требуется. |
| Блокаторы гистаминовых H2-рецепторов и ингибиторы протонного насоса | ||
| омепразол (ралтегравир 400 мг 2 раза/сут) | ралтегравир AUC↑ 37% ралтегравир C12ч↑24% ралтегравир Cmax↑51% (увеличение растворимости) |
Коррекция дозы препарата Исентресс не требуется. |
| фамотидин (ралтегравир 400 мг 2 раза/сут) | ралтегравир AUC↑ 44% ралтегравир C12ч↑6% ралтегравир Cmax↑60% (увеличение растворимости) |
Коррекция дозы препарата Исентресс не требуется. |
| Гормональные контрацептивы | ||
| этинилэстрадиол норэлгестромин (ралтегравир 400 мг 2 раза/сут) | этинилэстрадиол AUC↓2% этинилэстрадиол Cmax↑6% норэлгестромин AUC↑ 14% норэлгестромин Cmax↑29% |
Коррекция доз препарата Исентресс или гормональных контрацептивов (эстроген- и/или прогестаген-содержащих) не требуется. |
| Опиоидные анальгетики | ||
| метадон (ралтегравир 400 мг 2 раза/сут) | метадон AUC ↔ метадон Cmax ↔ |
Коррекция доз препарата Исентресс или метадона не требуется. |
Особые указания
Пациентов следует информировать о том, что современные антиретровирусные препараты не излечивают ВИЧ-инфекцию и не предотвращают передачу ВИЧ другим людям с кровью или при половых контактах. Во время лечения препаратом Исентресс пациенты должны продолжать соблюдать соответствующие меры безопасности. Также пациенты должны быть проинформированы о том, что у них все еще могут развиться инфекции или другие состояния, распространенные среди ВИЧ-инфицированных пациентов (оппортунистические инфекции). Во время терапии препаратом Исентресс очень важно оставаться под наблюдением врача.
Ралтегравир имеет относительно низкий генетический барьер к развитию резистентности, поэтому для повышения эффективности лечения и снижения риска развития резистентности к препарату ралтегравир необходимо назначать в комбинации с двумя другими активными антиретровирусными средствами, если это возможно. Важно объяснить пациентам необходимость изучить инструкцию по применению перед началом терапии препаратом Исентресс и перечитывать се каждый раз при получении очередного рецепта от врача. Пациенты должны быть проинформированы о необходимости сообщать врачу о появлении каких-либо необычных симптомов, а также о сохранении или ухудшении любого известного симптома.
Синдром восстановления иммунитета
На начальных этапах комбинированной АРВТ у ВИЧ-инфицированных пациентов с тяжелым иммунодефицитом может развиться так называемый синдром восстановления иммунитета, т.е. воспалительная реакция на бессимптомно текущие или остаточные оппортунистические инфекции (в т.ч. цитомегаловирусный ретинит, пневмоцистная пневмония, вызванная Pneumocystis jirovecii, диссеминированные или очаговые микобактериальные инфекции). Это может способствовать ухудшению клинического состояния и усилению имеющихся симптомов. Обычно такая реакция может наблюдаться в первые недели или месяцы после начала комбинированной терапии. Любые воспалительные симптомы должны быть оценены, и при необходимости назначено лечение.
При развитии синдрома восстановления иммунитета были описаны такие аутоиммунные расстройства, как Базедова болезнь. Развитие таких нарушений может наблюдаться через много месяцев после начала лечения.
Остеонекроз
Несмотря на то, что этиология данного осложнения считается многофакторной (включая терапию ГКС, употребление алкоголя, тяжелый иммунодефицит, высокий индекс массы тела), описаны случаи развития остеонекроза, особенно на поздних стадиях ВИЧ-инфекции и/или при длительном приеме комбинированной АРВТ. Пациентам, у которых появились такие симптомы, как боль в суставах, скованность или ограничение подвижности, нужна срочная консультация специалиста.
Тяжелые реакции со стороны кожи и реакции гиперчувствительности
Получены данные о тяжелых (потенциально жизнеугрожающих) и фатальных нежелательных реакциях со стороны кожи у пациентов, принимавших препарат Исентресс в составе комбинированной терапии с другими лекарственными средствами, ассоциирующимися с этими нежелательными реакциями, такими как синдром Стивенса-Джонсона и токсический эпидермальный некролиз. Также сообщалось о реакциях гиперчувствительности, которые проявлялись в виде сыпи генерализованного характера, и иногда органной дисфункции, включая печеночную недостаточность. Следует немедленно прекратить применение препарата Исентресс и других препаратов, предположительно способных вызвать такие реакции, если появились признаки или симптомы тяжелых реакций со стороны кожи или реакции гиперчувствительности (включая тяжелую кожную сыпь или сыпь, сопровождающуюся лихорадкой, общее недомогание, слабость, боли в мышцах или суставах, появление волдырей на коже, повреждения в ротовой полости, конъюнктивит, отек лица, гепатит, эозинофилию, ангионевротический отек, но не ограничиваясь только ими). В этих случаях необходимо мониторировать клинический статус, включая активность печеночных аминотрансфераз, и начать соответствующую терапию. Несвоевременное прекращение терапии препаратом Исентресс или другими лекарственными средствами, ассоциирующимися с этими нежелательными реакциями, после появления тяжелой сыпи может привести к жизнеугрожающим реакциям.
Миопатия и рабдомиолиз
Сообщалось о развитии миопатии и рабдомиолиза. Следует соблюдать осторожность при назначении препарата пациентам с миопатией и рабдомиолизом в анамнезе или с какими-либо факторами, предрасполагающими к их развитию, в частности, при сопутствующей терапии препаратами, способными вызвать эти нежелательные реакции.
Нарушение функции печени
Безопасность и эффективность препарата Исентресс у пациентов с тяжелыми сопутствующими заболеваниями печени не установлены. Следует соблюдать осторожность при назначении препарата Исентресс пациентам с тяжелыми нарушениями функции печени.
У пациентов с существующей дисфункцией печени, включая хронический гепатит, повышается частота нарушений функции печени на фоне комбинированной АРВТ, и они подлежат мониторингу в соответствии со стандартной практикой. При появлении у таких пациентов признаков ухудшения заболевания печени должен быть рассмотрен вопрос о прерывании или прекращении лечения.
Пациенты с хроническим гепатитом В или С, также получающие комбинированную АРВТ, входят в группу риска развития тяжелых и потенциально фатальных нежелательных явлений со стороны печени.
Кожная сыпь
У пациентов, ранее получавших АРВТ, при применении препарата Исентресс одновременно с дарунавиром кожная сыпь наблюдается чаще, чем у пациентов, применяющих препараты по отдельности (см. раздел «Побочное действие»).
Депрессия
Депрессия, включая суицидальные идеи и поведение, наблюдалась в основном у пациентов с депрессией или психиатрическими заболеваниями в анамнезе. Следует соблюдать осторожность при назначении препарата Исентресс пациентам с депрессией или психиатрическими заболеваниями в анамнезе.
Одновременное применение с другими лекарственными средствами
Сильные индукторы УДФ-ГТ1А1. Следует соблюдать осторожность при назначении препарата Исентресс одновременно с сильными индукторами УДФ-ГT1A1, такими как рифампицин, вследствие вызываемого ими снижения плазменной концентрации ралтегравира. При необходимости проведения комбинированной терапии рифампицином и препаратом Исентресс доза препарата Исентресс должна быть увеличена в 2 раза у взрослых пациентов. Нет данных для корректировки доз препаратов при одновременном применении препарата Исентресс и рифампицина у пациентов младше 18 лет (см. раздел «Лекарственное взаимодействие»).
Антациды. Одновременное применение препарата Исентресс с антацидами, содержащими алюминий или магний, приводит к снижению концентрации ралтегравира в плазме крови.
Одновременное применение препарата Исентресс с антацидами, содержащими алюминий или магний, не рекомендуется (см. раздел «Лекарственное взаимодействие»).
Фруктоза и сорбитол
Препарат Исентресс в лекарственной форме таблетки жевательные содержит фруктозу и сорбитол. Пациентам с редкими наследственными нарушениями в виде непереносимости фруктозы не следует принимать препарат Исентресс.
Фенилкетонурия
Препарат Исентресс в лекарственной форме таблетки жевательные в составе ароматизатора маскирующего содержит фенилаланин как компонент аспартама. Каждая жевательная таблетка 25 мг препарата Исентресс содержит приблизительно 0.05 мг фенилаланина, а каждая жевательная таблетка 100 мг — приблизительно 0.10 мг фенилаланина. Фенилаланин может нанести вред пациентам с фенилкетонурией.
Влияние на способность к управлению транспортными средствами и механизмами
Исследования по изучению влияния на способность к управлению транспортными средствами и использованию механизмов не проводились. Учитывая возможность развития головокружения, слабости, сонливости и нечеткости зрения на фоне лечения препаратом Исентресс, нужно проявлять особую осторожность при управлении автомобилем и работе с механизмами.
Беременность и лактация
Контролируемых исследований препарата Исентресс у беременных не проводилось, поэтому Исентресс противопоказан к применению во время беременности.
Отсутствуют данные о поступлении ралтегравира в грудное молоко человека. Однако обнаружено поступление ралтегравира в молоко у лактирующих крыс: при введении препарата в суточной дозе 600 мг/кг концентрация ралтегравира в молоке превышала плазменную концентрацию примерно в 3 раза.
Грудное вскармливание не рекомендуется ВИЧ-инфицированным матерям во избежание постнатальной передачи ВИЧ детям. При необходимости применения препарата в период лактации рекомендуется прекратить грудное вскармливание.
Применение в детском возрасте
Возможно применение у детей старше 2 лет и с массой тела выше 7 кг по показаниям.
При нарушениях функции печени
С осторожностью: печеночная недостаточность тяжелой степени
Условия отпуска из аптек
Препарат отпускается по рецепту.
Условия и сроки хранения
Препарат следует хранить в недоступном для детей, сухом месте при температуре не выше 30°С в плотно закрытой оригинальной упаковке с влагопоглощающим агентом. Срок годности — 2 года. Не использовать по истечении срока годности, указанного на упаковке.
Описание препарата ИСЕНТРЕСС основано на официально утвержденной инструкции по применению и утверждено компанией–производителем.
Предоставленная информация о ценах на препараты не является предложением о продаже или покупке товара. Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в соответствии со статьей 55 ФЗ «Об обращении лекарственных средств».
Обнаружили ошибку? Выделите ее и нажмите Ctrl+Enter.
Синонимы, аналоги
Статьи
РЕГИСТРАЦИОННЫЙ НОМЕР:
ЛСР-007737/08
ТОРГОВОЕ НАЗВАНИЕ:
Иcентресс®
МЕЖДУНАРОДНОЕ НЕПАТЕНТОВАННОЕ НАЗВАНИЕ:
ралтегравир
ЛЕКАРСТВЕННАЯ ФОРМА:
таблетки покрытые пленочной оболочкой
СОСТАВ
1 таблетка покрытая пленочной оболочкой содержит:
активное вещество: ралтегравир калия 434,4 мг (эквивалентно 400 мг ралтегравира);
вспомогательные вещества: целлюлоза микрокристаллическая 169.4 мг. лактозы моногидрат 26,06 мг, кальция гидрофосфат 69,50 мг, гипромеллоза 2208 43,44 мг, полоксамер 407* 104,3 мг, натрия стсарилфумарат 8.688 мг, магния стеарат 13.03 мг;
пленочное покрытие: краситель Опадрай II розовый (85F94224) 26,06 мг;
состав пленочной оболочки: поливиниловый спирт 44,75%, макрогол 22,0%, тальк 21,415%, титана диоксид 11,32%, краситель железа оксид красный 0,495%. краситель железа оксид черный 0.02%.
* содержит 0,01% бутилгндрокситолуола в качестве антиоксиданта.
ОПИСАНИЕ
Овальные двояковыпуклые таблетки, покрытые пленочной оболочкой розового цвета, с гравировкой «227» на одной стороне и гладкие на другой.
ФАРМАКОТЕРАПЕВТИЧЕСКАЯ ГРУППА:
противовирусное (ВИЧ) средство
КОД ATX: J05AX08
ФАРМАКОЛОГИЧЕСКИЕ СВОЙСТВА
Фармакодинамика
Ралтегравир ингибирует каталитическую активность ВИЧ интегразы— фермента, участвующего в репликации вируса ВИЧ. Ингибирование питегразы предотвращает ковалентное введение (интеграцию) генома ВИЧ в геном клетки хозяина на ранних стадиях развития инфекции. Не включенные в ДНК человека геномы ВИЧ не способны индуцировать продукцию новых вирусных частиц, поэтому подавление процесса интеграции предотвращает распространение вирусной инфекции в организме.
Ингибирующая способность ралтегравира в отношении фосфотрансфераз человека, включая ДНК-полимеразы α, β и γ выражена незначительно.
Микробиология
При плазменной концентрации 31 ± 20 нмоль/л ралтегравир обеспечиват подавление репликации вируса на 95% (95% ингибирующая концентрация, ИК95) в клеточных культурах человеческих Т-лимфоцитов, инфицированных адаптированным к культурам клеток вариантом H9IIIB ВИЧ-1, но сравнению с контрольной вирус-инфицированной культурой клеток. ИК95 достигалась в концентрациях от 6 до 50 нмоль/л в культурах человеческих митоген-активированных мононуклеаров периферической крови. инфицированных различными первичными клиническими штаммами ВИЧ-1, включая штаммы 5 не-В подтипов ВИЧ-1, а также штаммы, резистентные к ингибиторам обратной транскриптазы и ингибиторам протеазы ВИЧ. При анализе одного цикла инфекции ралтегравир подавлял инфицирование, вызванное 23 штаммами ВИЧ, представляющими не-В подтипов и 5 циркулирующих рекомбинантных форм, с ИК50 при концентрации от до 12 нмоль/л. Ралтегравир также подавлял репликацию штаммов ВИЧ-2 при тестировании на клетках линии СЕМх174 (ИК95 = 6 нмоль/л). При одновременном введении в культуру человеческих Т-лимфоцитов, инфицированных вариантом H9IIIB вируса ВИЧ-1, ралтегравира и пуклеозидных ингибиторов обратной транскриптазы (зидовудин, зальцитабин, ставудин, абакавир, тенофовир. диданозин и ламнвудин). Ненуклеозидных ингибиторов обратной транскриптазы (эфавиренз, иевирапин и делавирдин), ингибиторов протеазы ВИЧ (индинавир, саквинавнр, ритонавир, амнренавир, лонинавир, нелфинавир и атазанавир) или ингибитора слияния (энфувиртид) наблюдалась антиретровирусная активность от аддитивной до синергичной.
Резистентность к препарату
Мутации ннтегразы ВИЧ-1, способствующие появлению резистентных к ралтегравиру штаммов вируса (развивались или in vitro, или у пациентов, принимавших ралтегравир), в основном включают замены в положениях 155 (N155 замена на Н), 148 (Q148 замена на H, K или R) или 143 (Y143 замена на С, H или R), в сочетании с одной или более дополнительными мутациями (например, L74M, E92Q, Т97А, Е138Л/К, G140A/S. V151I, G163R, S230R).
Рекомбинантные вирусы с одной первичной мутацией (Q148H, К или R или N15511) отличались сниженной способностью к репликации и сниженной чувствительностью к ралтегравиру in vitro. Вторичные мутации вируса еще больше снижали чувствительность к раттегравиру. иногда компенсируя сниженную способность вируса к репликации. Мутации, ассоциированные с развитием резистентности к ралтегравиру, также могут приводить к формированию устойчивости к другому ингибитору переноса цепи интегразой элвитегравиру. При замене в положении 143 чувствительность к ралтегравиру снижается в большей степени, чем чувствительность к элвитегравиру, тогда как мутации в E92Q- большую резистентность к элвитегравиру, чем к ралтегравиру. У вирусов с мутацией в положении 148 в сочетании с одной и более дополнительными мутациями, вызывающими резистентность к ралтегравиру, также может наблюдаться клинически значимая резистентность к долутегравиру.
Влияние на электрофизиологическую активность сердца или на показатели электрокардиограммы
В плацебо-контролируемом клиническом исследовании с участием здоровых добровольцев однократный прием 1600 мг ралтегравира не оказывал какого-либо влияния на продолжительность интервала QTc, несмотря на то, что максимальная концентрация (Сmах) ралтегравира в плазме крови была в 4 раза больше, чем при однократном приеме ралтегравира в дозе 400 мг.
Фармакокинетика
У взрослых пациентов
Всасывание
Ралтeгравир быстро всасывается после приема препарата натощак, Сmax в плазме крови определяется примерно через 3 часа. Площадь под кривой «концентрация — время» (AUC) и значение Сmax ралтегравира увеличиваются пропорционально дозе в диапазоне доз от 100 мг до 1600 мг. Значения Сmax ралтегравира возрастают пропорционально дозе в диапазоне доз от 100 мг до 800 мг и возрастают в несколько меньшей степени в диапазоне доз от 100 мг до 1600 мг. При режиме приема препарата 2 раза в сутки равновесное состояние достигается быстро, примерно в течение 2 дней после начала лечения. Значения AUC и Сmax свидетельствуют в пользу отсутствия или минимальной кумуляции препарата, значение С12ч в пользу незначительной кумуляции препарата. В режиме монотерапии по 400 мг 2 раза в сутки значение среднего геометрического для AUC0-12ч составляло 14,3 мкмоль/л х ч, значение С12ч — 14 нмоль/л.
Абсолютная биодоступность ралтегравира не установлена. Ралтегравир можно принимать вне зависимости от режима приема пищи.
Распределение
Примерно 83% ралтегравира связывается с белками плазмы в диапазоне концентраций от 2 до 10 мкмоль/л. Ралтегравир легко преодолевал плацентарный барьер в экспериментальных исследованиях на крысах, но не проникал через гематоэнцефалический барьер в заметной степени.
В двух клинических исследованиях с участием пациентов, инфицированных ВИЧ-1, которые принимали ралтегравир в дозе 400 мг 2 раза в сутки, ралтегравир быстро определялся в спинномозговой жидкости. В первом исследовании средняя концентрация ралтегравира в спинномозговой жидкости составила 5,8% (в диапазоне от 1 до 53,5%) от соответствующей концентрации в плазме крови. Во втором исследовании средняя концентрация ралтегравира в спинномозговой жидкости составила 3% (в диапазоне от 1 до 61%) от соответствующей концентрации в плазме крови. Медианы полученных значений были приблизительно в 3-6 раз ниже, чем концентрации свободной фракции ралтегравира в плазме крови.
Метаболизм и выведение
Исследования с использованием селективных ингибиторов изоформы фермента уридиндифосфат-глюкуронилтрансферазы (УДФ-ГТ). полученной путем экспрессии комплементарной ДНК. показали, что изоформа УДФ-ГТ1А1 является основным ферментом, участвующим в образовании ралтегравир-глюкуронида. Эти данные показали, что основной путь метаболизма ралтегравпра у человека представлен процессом глюкуроннрования, опосредованного УДФ-ГТ1А1. Длительность конечной фазы периода полувыведения ралтегравпра составляет около 9 часов, большая часть AUC соответствует более короткой а-фазе кажущегося периода полувыведения ралтегравира (составляет Примерно 1 час). После приема внутрь радиоактивно меченого ралтегравира примерно 51% от принятой дозы выводилось через кишечник и 32%— через почки. В кале обнаруживался только ралтегравир, который, вероятно, образовывался путем гидролиза ралтегравир-глюкуронида, выделившегося с желчью. В моче определялись ралтегравир и ралтегравнр-глюкуронид в количестве 9% и 23% от принятой дозы соответственно. В плазме крови основным циркулирующим радиоактивным компонентом был ралтегравир (примерно 70% от общей радиоактивности), в то время как на ралтегравир-глюкуронид приходилось только 30%.
Фармакокинепшка у отдельных групп пациентов
Пол
Пол не оказывает клинически значимого влияния на фармакокинсгические параметры ралтегравира. Коррекция дозы препарата в зависимости от пола пациента не требуется. Пожилые пациенты
В исследованиях на пациентах от 18 лет и старше не было обнаружено значимой зависимости фармакокинетических параметров ралтегравира от возраста пациентов, поэтому коррекция дозы препарата в зависимости от возраста не требуется.
Подростки и дети
Дозы для подростков и детей старше 6 лет для лечения ВИЧ-1 инфекции рекомендованы на основании того, что фармакокннетическис параметры ралтегравира сопоставимы с таковыми у взрослых пациентов. Фармакокинетпка ралтегравира у детей младше 2 лет не изучалась.
Пациенты из разных расово—этнических групп
Расово-этиическая принадлежность не оказывала клинически значимого влияния на фармакокннетическис параметры ралтегравира. Коррекция дозы не требуется.
Пациенты с различным индексом массы тела (ИМТ)
ИМТ не оказывал клинически значимого влияния на фармакокннетическис параметры ралтегравира у взрослых пациентов. Коррекция дозы препарата в зависимости от ИМТ пациента не требуется.
Пациенты с печеночной недостаточностью
Налтегравир выводится преимущественно путем глюкуронировапия и печени.
Фармакокинетика препарата была изучена у взрослых пациентов с печеночной недостаточностью средней степени тяжести, а также в комбинированном фармакокинетическом анализе. Клинически значимых отклонении фармакокинетических параметров у взрослых пациентов с печеночной недостаточностью средней степени тяжести по сравнению со здоровыми добровольцами не выявлено. Таким образом, коррекция дозы препарата при печеночной недостаточности легкой и средней степени тяжести не требуется. Влияние тяжелой степени печеночной недостаточности на фармакокинетические параметры ралтегравира не изучалось.
Пациенты с почечной недостаточностью
На почечный клиренс приходится незначительная доля в выведении ралтегравира из организма. Фармакокинетика препарата была изучена у взрослых пациентов с тяжелой степенью почечной недостаточности, а также в сложном фармакокинетнческом анализе.
Клинически значимых отклонений фармакокинетических параметров у пациентов с тяжелой степенью почечной недостаточности по сравнению со здоровыми добровольцами не выявлено. Таким образом, коррекции дозы препарата пациентам с тяжелой степенью почечной недостаточности не требуется. Поскольку эффективность диализа ралтегравира неизвестна, принимать препарат накануне сеанса диализа не рекомендуется.
Пациенты с полиморфизмом УДФ-ГТ1АI
Доказательства или какие-либо данные, свидетельствующие, что наличие полиморфизма у фермента УДФ-ГТ1А1 может оказывать клинически значимое влияние на фармакокннетические параметры ралтегравира, не были получены. По данным сравнительного исследования с участием 30 взрослых здоровых добровольцев с генетически детерминированной сниженной активностью УДФ-ГТ1А1 и 27 взрослых здоровых добровольцев с неизмененным генотипом УДФ-ГТ1А1 отношение средних геометрических AUC ралтегравира составило 1,41 (90% доверительный интервал составил 0.96; 2,09).
ПОКАЗАНИЯ К ПРИМЕНЕНИЮ
Лечение ВИЧ-1 инфекции в комбинации с другими антиретровирусными препаратами у взрослых, подростков и детей, начиная с 6 лет и с массой тела не менее 25 кг, как ранее получавших, так и не получавших аптирстровируспую терапию.
ПРОТИВОПОКАЗАНИЯ
- Повышенная чувствительность к ралтегравиру и другим компонентам препарата.
- Детский возраст до 6 лет.
- Масса тела до 25 кг.
- Переменность.
- Период лактации.
Препарат содержит лактозу. поэтому пациенты с редкой наследственной непереносимостью лактозы, дефицитом лактазы или нарушенным всасыванием глюкозо-галактозы не должны принимать препарат Исентресс .
С ОСТОРОЖНОСТЬЮ
Миопатия и рабдомиолиз (в том числе в анамнезе), наличие состояний и факторов, предрасполагающих к их развитию.
Печепочная недостаточность тяжелой степени.
Одновременное применение с сильными индукторами УДФ-ГТ1А1 (рифампицин).
Одновременное применение препарата Исентресс с антацидами, содержащими алюминий или магний.
Депрессия, включая супцидапьные идеи и поведение, наблюдалась в основном у шцпентов с депрессией или психиатрическими заболеваниями в анамнезе. Следует соблюдать осторожность при назначении препарата Исентресс пациентам с депрессией или психиатрическими заболеваниями в анамнезе.
Пожилой возраст (ввиду ограниченной информации о применении ралтегравира у пациентов старше 65 лет).
ПРИМЕНЕНИЕ ПРИ БЕРЕМЕННОСТИ И В ПЕРИОД ГРУДНОГО ВСКАРМЛИВАНИЯ
Контролируемых исследований препарата Исентресс у беременных не проводилось, поэтому препарат Исстрссс противопоказан к применению во время беременности.
Отсутствуют данные о поступлении ралтегравира в грудное молоко человека. Однако обнаружено поступление ралтегравира в молоко у крыс: при введении препарата в суточной дозе 600 мг/кг концентрация ралтегравира в молоке превышала плазменную концентрацию примерно в 3 раза. Грудное вскармливание не рекомендуется ВИЧ-инфицированным матерям во избежание постнатальной передачи ВИЧ-инфекции детям. При необходимости применения препарата в период лактации рекомендуется прекратить грудное вскармливание.
СПОСОБ ПРИМЕНЕНИЯ И ДОЗЫ
Внутрь. Таблетки препарата Исентресс нельзя жевать, крошить, разламывать. Препарат применяется вне зависимости от приема пищи.
Лечение препаратом Исентресс должен проводить врач, обладающий достаточным опытом терапии ВИЧ-инфекции. Лечение препаратом Исентресс проводят в комбинации с другими антиретровирусными препаратами.
Рекомендуемые дозы препарата Исентресс для лечения ВИЧ-1 инфекции:
— для взрослых: 400 мг х 2 раза в сутки;
— для детей с массой тела не менее 25 кг: 400 мг х 2 раза в сутки.
Если пациенты детского возраста испытывают трудности при проглатывании таблеток, покрытых пленочной оболочкой, следует рассмотреть возможность приема препарата Исентресс таблетки жевательные (смотри инструкцию по применению препарата Исентресс, таблетки жевательные).
Пожилые пациенты
Коррекция дозы у пожилых пациентов не требуется.
Пациенты с нарушением функции почек
Коррекция дозы у пациентов с нарушением функции почек не требуется.
Пациенты с нарушением функции печени
Коррекция дозы у пациентов с нарушением функции печени легкой и средней степени тяжести не требуется.
ПОБОЧНОЕ ДЕЙСТВИЕ
Профиль безопасности препарата Исентресс основан на результатах обобщенных данных о безопасности, полученных в ходе клинических исследований с участием пациентов, ранее получавших антиретровирусную терапию (АРВТ), и пациентов, ранее не получавших АРВТ.
В объединенном анализе результатов клинических исследований антиретровирусной терапии у взрослых пациентов, ранее получавших АРВТ, частота отмены терапии но причине нежелательных реакций составила 3,9% в группе пациентов, принимавших препарат Исентресс® и оптимизированную дополнительную терапию (ОДТ), и 4,6% в группе пациентов, принимавших плацебо и ОДТ. Частота отмены терапии по причине нежелательных реакций у взрослых пациентов, ранее не получавших АРВТ, составила 5,0% в группе пациентов, принимавших препарат Исентресс® одновременно с энтрицитабином и тенофовиром, и 10,0% в группе пациентов, принимавших одновременно эфавиренз, эмтрицитабин и тенофовир.
Ниже представлены данные о нежелательных явлениях, наблюдавшихся в клинических исследованиях, с различной степенью вероятности связанных с препаратом Исентресс® или его комбинацией с другой АРВТ. Нежелательные явления перечислены в соответствии с системно-органными классами и классификацией по частоте: «частые» (>1/100 и <1/10). «нечастые» (> 1/1000 и <1/100).
Инфекционные и паразитарные заболевания
Нечастые: гепитальный герпес, фолликулит, гастроэнтерит, простой герпес, герпетическая инфекция, опоясывающий лишай, грипп, абсцесс лимфоузла, контагиозный моллюск, назофарингит, инфекция верхних дыхательных путей.
Доброкачественные, злокачественные и неуточненные новообразования (включая кисты и полипы)
Нечастые: папилломатоз кожи.
Со стороны крови и лимфатической системы
Нечастые: анемия. железодефицитная анемия. болезненность лимфоузлов, лимфаденопатия, нейтропения, тромбоцитопения .
Со стороны иммунной системы
Нечастые: синдром восстановления иммунитета, гиперчувствительность к препарату, реакции гиперчувствительности.
Со стороны обмена веществ и питания
Частые: снижение аппетита.
Нечастые: кахексия, сахарный диабет, дислипидемия, гиперхолестеринемия, гипергликемия, гиперлипидемия, гиперфагия, повышение аппетита, полидипсия, нарушение жирового обмена.
Нарушения психики
Частые: необычные сновидения, бессонница, ночные кошмары, нарушение поведения, депрессия.
Нечастые: психические расстройства, суицидальные попытки, чувство тревоги, спутанность сознания, подавленное настроение, большое депрессивное расстройство, бессонница середины ночи, изменения настроения, панические атаки, нарушения сна, суицидальные идеи1, суицидальное поведение1 (особенно у пациентов с психиатрическими заболеваниями в анамнезе).
Со стороны нервной системы
Частые: головокружение, головная боль, психомоторная гиперреактивность2. Нечастые: амнезия, синдром запястного канала, когнитивные расстройства, нарушения внимания, постуральное головокружение, дисгевзпя, гиперсомния. гиисстезия, летаргия, расстройство памяти, мигрень, периферическая нейропатпя, парестезии, сонливость, головная боль напряжения, тремор, снижение качества сна.
Со стороны органа зрения
Нечастые: снижение остроты зрения.
Со стороны органа слуха н лабиринтные нарушения
Частые: вертиго. Нечастые: шум в ушах.
Со стороны сердца
Нечастые: ощущение сердцебиения, синусовая брадикардия, желудочковая экстрасистолия.
Со стороны сосудов
Нечастые: «приливы» крови к коже лица с ощущением жара, артериальная гипертензия.
Со стороны дыхательной системы, органов грудной клетки и средостения
Нечастые: дисфония. носовое кровотечение, заложенность носа.
Со стороны желудочно-кишечного тракта
Частые: чувство распирания в животе, боль в животе, диарея, метеоризм, тошнота, рвота, диспепсия.
Нечастые: гастрит, ощущение дискомфорта в животе, боль в верхних отделах живота, болезненность в области живота, чувство дискомфорта в области заднего прохода, запор, сухость во рту. ощущение дискомфорта в эпигастральной области, эрозивный дуоденит, отрыжка, гастроэзофагеальный рефлюкс, гингивит, глоссит, болезненность при глотании, острый панкреатит, пептическая язва, ректальные кровотечения.
Со стороны печени и желчквынодящих путей
Нечастые: гепатит, стеатоз печени, алкогольный гепатит, печеночная недостаточность .
Со стороны кожи и подкожных тканей
Частые: кожная сыпь.
Нечастые: акне, алопеция, угревидная сыпь, сухость кожи, эритема, липоатрофия лица, гипергидроз, липоатрофия, приобретенная липодистрофия, липогипертрофия, ночная потливость, пруриго, зуд (локальный и генерализованный), макулярная сыпь, макулопапуллезная сыпь, зудящая сыпь, крапивница, ксеродермия, другие поражения кожи, синдром Стивенса-Джонсона, лекарственная сыпь с эозинофилией и системными симптомами (DRESS-синдром)1.
Со стороны скелетно-мышечной и соединительной ткани
Нечастые: артралгия, артрит, боль в спине, боль в боку, скелетно-мышечная боль. миалгия, боль в области шеи. остеопения, боль в конечностях, остеопороз, полиартрит. тендинит, миопатия, рабдомиолиз .
Со стороны почек и мочевыводяпшх путей
Нечастые: почечная недостаточность, нефрит, нефролитиаз, никтурия, киста почки, нарушение функции почек, тубулоинтерстициальный нефрит.
Ср стороны половых органон и молочной железы
Нечастые: эректильная дисфункция, гинекомастия, симптомы менопаузы.
Общие расстройства и нарушения в месте введения
Частые: астения, слабость, лихорадка.
Нечастые: дискомфорт в груди, озноб, отек лица, увеличение объема жировой ткани, состояние беспокойства, недомогание, подчелюстное новообразование, периферические отеки. боль.
Лабораторные и инструментальные данные
Частые: повышение активности в плазме аланинаминотрансферазы (АЛТ). аспартатаминотрансферазы (ACT), липазы и амилазы поджелудочной железы, повышение концентрации триглицеридов и количества атипичных лимфоцитов.
Нечастые: снижение абсолютного числа нейтрофилов плазмы, повышение активности в плазме щелочной фосфатазы, амилазы, креатинфосфокиназы, снижение концентрации альбумина, повышение концентрации билирубина, холестерина, креатинина, глюкозы (в том числе определяемой натощак), азота мочевины, холестерина липопротеинов высокой плотности, холестерина липопротеинов низкой плотности, повышение значения международного нормализованного отношения, снижение количества тромбоцитов и лейкоцитов в крови, наличие глюкозы в моче, наличие эритроцитов в моче, увеличение окружности талии, увеличение или снижение массы тела.
Травмы, интоксикации и осложнения манипуляций
Нечастые: непреднамеренная передозировка.
Нежелательные явления без наличия причинно-следственной связи с применением препарата Исснтресс которые наблюдались в пострегистрационном периоде наблюдения и не наблюдались в ходе клинических исследований.
У одного пациента детского возраста наблюдались связанные с приемом препарата нежелательные реакции: психомоторная гиперреактивность 3 степени и нарушение поведения; также у данного пациента наблюдалась бессонница.
В ходе клинических исследований у пациентов, ранее получавших и ранее не получавших АРВТ, наблюдались случаи развития злокачественных новообразований при использовании комбинации препарата Исентресс с другими антиретровирусным и средствами. Характеристика и частота злокачественных новообразований соответствовали таковым для пациентов с тяжелым иммунодефицитом. Риск развития злокачественных новообразований в клинических исследованиях был одинаков как в группах пациентов, принимавших препарат Исентресс*, так и в группах пациентов, принимавших препараты сравнения.
У пациентов, принимавших препарат Исентресс, наблюдалось повышение активности креатинфосфокиназы 2-4 степени. Наблюдались случаи развития миопатии и рабдомиолиза. Пациентам с миопатией или рабдомиолизом в анамнезе, а также имеющим другие факторы риска (включая сопутствующую терапию), препарат следует назначать с осторожностью.
Сообщалось о случаях развития остеонекроза, особенно у пациентов с общепризнанными факторами риска, поздней стадией ВИЧ-заболевания или длительным воздействием комбинированной АРВТ. Частота его развития неизвестна.
В клинических исследованиях у пациентов, ранее получавших АРВТ, кожная сыпь, вне зависимости от этиологии, чаще наблюдалась при применении препарата Исентресс одновременно с дарупавиром, чем при применении данных препаратов по отдельности. Тем не менее частота развития кожной сыпи, связанной с приемом препаратов, была сопоставима во всех трех группах лечения. Кожная сыпь была легкой и умеренной Степени тяжести и не влияла на продолжение АРВТ. У пациентов, ранее не получавших АРВТ, при лечении препаратом Исентресс в комбинации с эмтрицитабином и тенофовиром, развитие сыпи наблюдалось реже, чем при лечении эфавирензом в комбинацни с эмтрицитабином и тенофовиром.
Пациенты с ко-инфекцией гепатита В и/или гепатита С
В целом профиль безопасности препарата Исентресс у пациентов, как ранее получавших, так и не получавших АРВТ, ко-инфицнрованных хроническим (но не острым) активным гепатитом В и/или гепатитом С, был аналогичен профилю безопасности у пациентов без ко-инфекции гепатита В и/или гепатита С, хотя частота отклонения активностей АЛТ и ACT иногда была выше в группах с ко-инфекцией гепатита В и/или гепатита С.
Дети
По результатам клинических исследований применения ралтегравира в рекомендованных дозах в комбинации с другими антиретровирусным и лекарственными средствами у ВИЧ-1 инфицированных детей и подростков от 2 до 18 лет было установлено, что частота, тип и выраженность нежелательных реакций, связанных с приемом препарата, были сопоставимы с таковыми у взрослых пациентов.
У одного Пациента наблюдались следующие связанные с приемом препарата нежелательные реакции: психомоторная гиперактивность 3 степени, нарушение поведения и бессонница. У другого пациента наблюдалась серьезная нежелательная реакция 2 степени — аллергическая сыпь.
Еще у одного пациента наблюдалось повышение активности ACT 4 степени и АЛТ 3 степени, которое было расценено как серьезное.
ПЕРЕДОЗИРОВКА
Специфических симптомов передозировки препарата Исентресс не выявлено. Ралтегравир хорошо переносился здоровыми добровольцами в режиме 1600 мг х 1 раз в сутки и 800 мг х 2 раза в сутки без каких-либо проявлений токсичности. Однократный прием дозы 1800 мг в сутки в исследованиях II/III фазы не оказывал токсического воздействия. На основании имеющихся данных можно заключить, что ралтегравир хорошо переносится в дозах до 800 мг два раза в сутки, а также при приеме с препаратами, увеличивающими его экспозицию на 50-70% (например, генофовиром и пазанавиром). Ралтегравир имеет широкий терапевтический диапазон, поэтому потенциал токсического действия в результате передозировки ограничен. В случае передозировки необходимо следовать стандартным рекомендациям, таким как удаление невсосавшегося препарата из желудочно-кишечного тракта, наблюдение за показателями жизнедеятельности, включая ЭКГ, назначение симптоматической терапии. Данных об эффективности диализа при передозировке препаратом Исентресс нет.
ВЗАИМОДЕЙСТВИЕ С ДРУГИМИ ЛЕКАРСТВЕННЫМИ СРЕДСТВАМИ
В исследованиях in vitroбыло показано, что ралтегравир не является субстратом изоферментов системы цитохрома Р450 и не ингибирует CYP1A2, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6 или CYP3A. Кроме этого, in
vitro ралтегравир не индуцирует CYP3A4 и не является ингибитором Р-гликопротеин-опосредованного транспорта. На основании этих данных можно сделать вывод, что Исентресс не влияет на фармакокинетические параметры лекарственных средств, которые являются субстратами указанных ферментов или Р-гликопротеина.
Как показали исследования in
vitroи in vivo, ралтегравир выводится в основном посредством метаболизма (глюкуронирования) но УДФ-ГТ1А1-опосредованному пути. Хотя исследования in
vitroпоказали, что ралтегравир не является ингибитором УДФ-ГТ1А1 и 2В7, в одном клиническом исследовании были выявлены некоторые признаки ингибирования УДФ-ГТ1А1 in vivo
на основе наблюдаемого влияния на глюкуронирование билирубина. Тем не менее маловероятно, что данный эффект приводит к клинически значимым межлекарственным взаимодействиям.
В фармакокинетике ралтегравира наблюдалась значимая интер- и интраиндивидуальная изменчивость. Приведенная ниже информация о взаимодействии с лекарственными средствами основана на средних геометрических значениях; эффект у отдельного пациента точно предсказать нельзя.
Влияние ралтегравира на фармакокинетику других лекарственных средств
В исследованиях по изучению лекарственного взаимодействия ралтегравир не оказывал клинически значимого влияния на фармакокинетику этравирина, маравирока, тенофовира, гормональных контрацептивов, метадона, мидазолама и боцепревира.
В некоторых исследованиях при одновременном применении препарата Исентресс® с дарунавнром наблюдалось незначительное снижение концентрации дарунавира в плазме крови. Механизм данного явления неизвестен. Тем не менее влияние ралтегравира на концентрацию дарунавира в плазме крови не считается клинически значимым.
Влияние других лекарственных средств на фармакокинетику ралтегравира
Следует соблюдать осторожность при одновременном применении препарата Исентресс с сильными индукторами УДФ-ГТ1Л1 (например, рифампицином), учитывая, что ралтегравир метаболизируется в основном посредством УДФ-ГТ1А1. Рифампицин снижает концентрации ралтегравира в плазме крови. Влияние на эффективность ралтегравира неизвестно. Тем не менее если одновременного применения с рифампицином избежать невозможно, можно удвоить дозу препарата Исентресс у взрослых. Данные по одновременному применению препарата Исентресс и рифампицина у пациентов младше 18 лет отсутствуют. Влияние других сильных индукторов изоферментов, метаболизирующих лекарственные средства, такие как фенитоин и фенобарбитал, на систему УДФ-ГТ1А1 неизвестно. Менее сильные индукторы (например, эфавиренз, невирапин, этравирин, рифабутин, глюкокортикостероиды, зверобой продырявленный, пиоглитазон) могут применяться одновременно с препаратом Исентресс в рекомендованной дозе.
Одновременное применение препарата Исентресс с сильными ингибиторами УДФ-ГТ1А1 (например, атазанавиром) может повысить концентрацию ралтегравира в плазме крови. Менее сильные ингибиторы УДФ-ГТ1А1 (например, индннавир и саквииавир) также могут повысить концентрацию ралтегравира в плазме крови, но в меньшей степени по сравнению с атазанавиром. Кроме того, тенофовир может повысить концентрацию ралтегравира в плазме крови, однако механизм этого влияния неизвестен. Профиль безопасности, наблюдаемый у пациентов, получавших атазанавир и/или
тенофовир, в целом идентичен профилю безопасности у пациентов, которые не принимали данные препараты, поэтому коррекция дозы не требуется. Одновременное применение препарата Исентресс с антацидами, содержащими бивалентные ионы металлов, может снижать абсорбцию ралтегравира путем хелатирования, что приводит к снижению концентрации ралтегравира в плазме крови. Так кг к прием антацидов, содержащих алюминий или магнии, через 6 часов после приема препарата Исентреес приводит к значительному снижению концентрации ралтегравира в плазме крови, одновременное применение препарата Исентреес и антацидов, содержащих алюминий или магнии, не рекомендуется.
Одновременное применение препарата Исентреес с антацидами, содержащими карбонат кальция, снижает концентрацию ралтегравира в плазме крови, однако данное взаимодействие не рассматривается как клинически значимое. Вследствие этого при одновременном применении препарата Исентресс с антацидами, содержащими карбонат кальция, коррекция дозы не требуется.
Одновременное применение препарата Исентрес
с с другими лекарственными средствами, повышающими значения рН желудочного сока (например, омепразол или фамотидин), может повысить скорость абсорбции ралтегравира и, соответственно, концентрацию ралтегравира в плазме крови. В клиническом исследовании профиль безопасности в подгруппе пациентов, принимавших ингибиторы протонного насоса или блокаторы Н2-гистаминовых рецепторов, был сопоставим с профилем безопасности в подгруппе пациентов, не принимавших данные лекарственные средства. Коррекция дозы препарата Исентресс не требуется при одновременном применении с ингибиторами фотонного насоса или блокаторами Н2-гистаминовых рецепторов.
Все исследования взаимодействия лекарственных средств проводились с участием взрослых пациентов.
Таблица 1. Данные по фармакокинетическому взаимодействию лекарственных средств у взрослых пациентов.
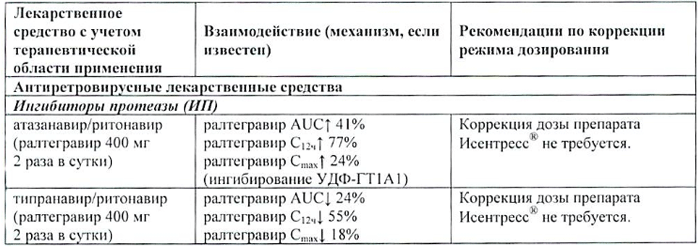
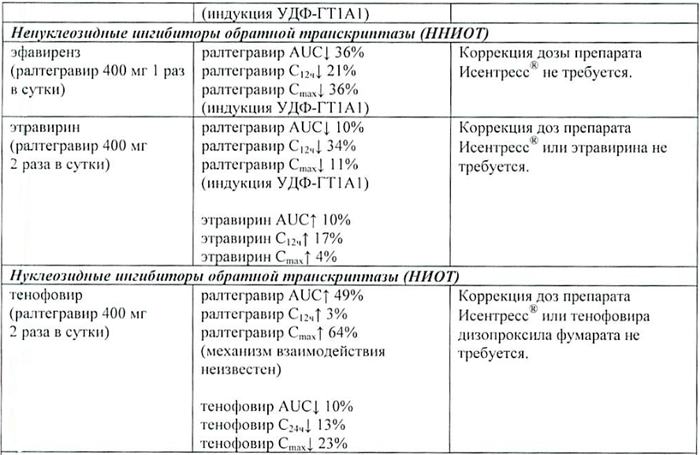
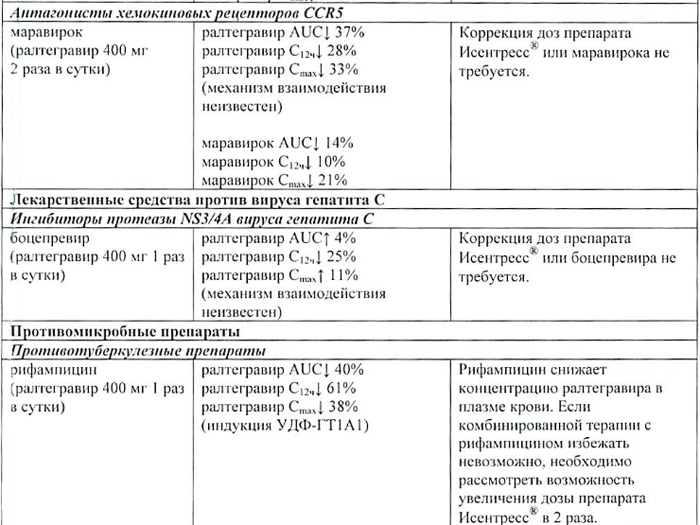

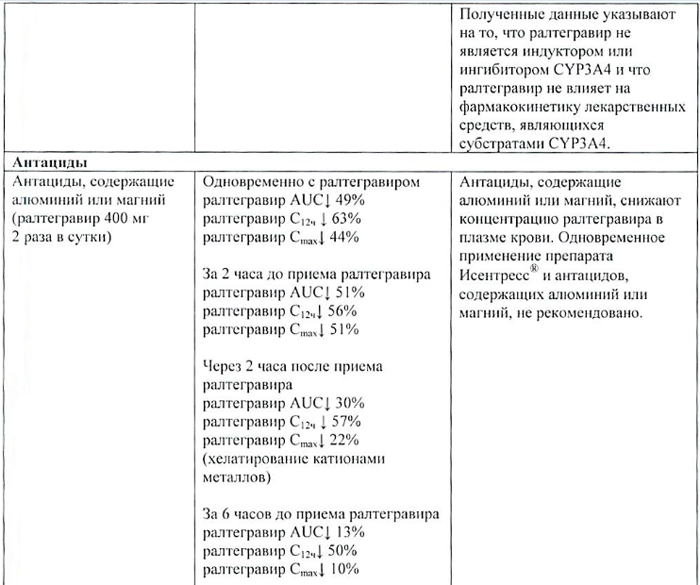
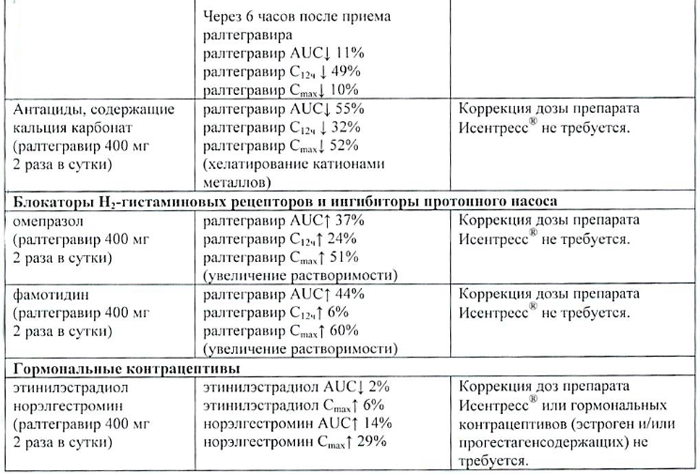

ОСОБЫЕ УКАЗАНИЯ
Пациентов следует информировать о том. что современные антиретровирусные препараты не излечивают ВИЧ-инфекцию и не предотвращают передачу ВИЧ другим людям с кровью или при половых контактах. Во время лечения препаратом Исентресс пациенты должны продолжать соблюдать соответствующие меры безопасности. Также пациенты должны быть проинформированы о том, что у них все еще могут развиться инфекции или другие состояния, распространенные среди ВИЧ-инфицнроваиных пациентов (оппортунистические инфекции). Во время терапии препаратом Исентресс очень важно оставаться под наблюдением врача. Ралтегравир имеет относительно низкий генетический барьер к развитию резистентности. Поэтому для повышения эффективности лечения и снижения риска развития резистентности к препарату ралтегравир необходимо назначать в комбинации с двумя другими активными антиретровирусными средствами, если это возможно. Важно объяснить пациентам необходимость изучить инструкцию по применению перед началом терапии препаратом Исентрссс и перечитывать ее каждый раз при получении очередного рецепта от врача. Пациенты должны быть проинформированы о необходимости сообщать врачу о появлении каких-либо необычных симптомов, либо сохранении или ухудшении любого известного симптома.
Синдром восстановления иммунитета
На начальных этапах комбинированной АРВТ у ВИЧ-инфицированных пациентов с тяжелым иммунодефицитом может развиться так называемый синдром восстановления иммунитета, то есть воспалительная реакция на бессимптомно текущие или остаточные оппортунистические инфекции (цитомегаловирусный ретинит, пневмоцистная пневмония, вызванная Pneumocystis jiroveci, диссеминированные или очаговые микобактериальные инфекции и др.). Это может способствовать ухудшению клинического состояния и усилению имеющихся симптомов. Обычно такая реакция может наблюдаться в первые недели или месяцы после начала комбинированной терапии. Любые воспалительные симптомы должны быть оценены и при необходимости назначено лечение. При развитии синдрома восстановления иммунитета были описаны такие аутоиммунные расстройства, как Базедова болезнь. Тем не менее, развитие таких нарушений может наблюдаться через много месяцев после начала лечения.
Остеонекроз
Несмотря на то, что этиология данного осложнения считается многофакторной (включая терапию кортикостероидами, употребление алкоголя, тяжелый иммунодефицит, высокий индекс массы тела), описаны случаи развития остеонекроза, особенно на поздних стадиях ВИЧ-инфекции и/или при длительном приеме комбинированной АРВТ. Пациентам, у которых появились такие симптомы, как боль в суставах, скованность или ограничение подвижности, нужна срочная консультация специалиста.
Тяжелые реакции со стороны кожи и реакции гиперчувствительности олучены данные о тяжелых (потенциально жизнеугрожающих) и фатальных нежелательных реакциях со стороны кожи у пациентов, принимавших препарат Исентресс в составе комбинированной терапии с другими лекарственными средствами, асоциирующимися с этими нежелательными реакциями, такими как синдром Стивенса-Джонсона и токсический эпидермальный некролиз. Также сообщалось о реакциях гиперчуветвительности, которые проявлялись в виде сыпи генерализованного характера, и иногда органной дисфункции, включая печеночную недостаточность. Следует немедленно прекратить применение препарата Исентресс и других препаратов, предположительно способных вызвать такие реакции, если появились признаки или симптомы тяжелых реакций со стороны кожи или реакции гиперчувствительности (включая тяжелую кожную сыпь или сыпь, сопровождающуюся лихорадкой, общее недомогание, слабость, боли в мышцах или суставах, появление волдырей на коже, повреждения в ротовой полости, конъюнктивит, отек лица, гепатит, эозинофилню, ангионевротический отек, но не ограничиваясь только ими).
В этих случаях необходимо мониторировать клинический статус, включая активность «печеночных» аминотрансфераз, и начать соответствующую терапию. Несвоевременное прекращение терапии препаратом Исентресс или другими лекарственными средствами, ассоциирующимися с этими нежелательными реакциями, после появления тяжелой сыпи может привести к жизнеугрожающим реакциям.
Миопатия и рабдомиолиз
Сообщалось о развитии миопатии и рабдомиолиза. Следует соблюдать осторожность при назначении препарата пациентам с миопатией и рабдомиолизом в анамнезе или с какими-либо факторами, предрасполагающими к их развитию, в частности, при сопутствующей терапии препаратами, способными вызвать эти нежелательные реакции.
Нарушение функции печени
Безопасность и эффективность препарата Исеитресс у пациентов с тяжелыми сопутствующими заболеваниями печени не установлены. Следует соблюдать осторожность при назначении препарата Исентреес пациентам с тяжелыми нарушениями функции печени.
У пациентов с существующей дисфункцией печени, включая хронический гепатит, повышается частота нарушений функции печени на фоне комбинированной АРВТ. и они подлежат мониторингу в соответствии со стандартной практикой. При появлении у таких пациентов признаков ухудшения заболевания печени должен быть рассмотрен вопрос о прерывании или прекращении лечения.
Пациенты с хроническим гепатитом В или С также получающие комбинированную АРВТ, входят в группу риска развития тяжелых и потенциально фатальных нежелательных явлений со стороны печени.
Кожная сыпь
У пациентов, ранее получавших АРВТ. при применении препарата Исентресс одновременно с дарунавпром кожная сыпь наблюдается чаще, чем у пациентов, применяющих препараты но отдельности (см. раздел ПОБОЧНОЕ ДЕЙСТВИЕ).
Депрессии
Депрессия, включая суицидальные идеи и поведение, наблюдалась в основном у пациентов с депрессией или психиатрическими заболеваниями в анамнезе. Следует соблюдать осторожность при назначении препарата Исентресс пациентам с депрессией тли психиатрическими заболеваниями в анамнезе.
Одновременное применение с другими лекарственными средствами
Сильные индукторы УДФ-ГТ1АI
Следует соблюдать осторожность при назначении препарата Исентресс одновременно с ильными индукторами УДФ-ГТ1А1, такими как рифампиции. вследствие вызываемого 1ми снижения плазменной концентрации ралтегравира. При необходимости проведения комбинированной терапии рифампицином и препаратом Исентресс доза препарата Исентресс должна быть увеличена в 2 раза у взрослых пациентов. Нет данных для возможности корректировки доз препаратов при одновременном применении препарата Исентресс и рифамппцина у пациентов младше 18 лет (см. раздел ВЗАИМОДЕЙСТВИЕ С ДРУГИМИ ЛЕКАРСТВЕННЫМИ СРЕДСТВАМИ).
Антациды
Одновременное применение препарата Исентресс с антацидами, содержащими алюминий или магний, приводит к снижению концентрации ралтегравира в плазме крови. Одновременное применение препарата Исентресс с антацидами, содержащими алюминий или магний, не рекомендуется (см. раздел ВЗАИМОДЕЙСТВИЕ С ДРУГИМИ ЛЕКАРСТВЕННЫМИ СРЕДСТВАМИ).
ВЛИЯНИЕ НА СПОСОБНОСТЬ УПРАВЛЯТЬ ТРАНСПОРТНЫМИ СРЕДСТВАМИ И РАБОТАТЬ С МЕХАНИЗМАМИ
Исследования по изучению влияния на способность к управлению транспортными средствами и использованию механизмов не проводились. Учитывая возможность развития на фоне лечения препаратом Исентресс головокружения, слабости, сонливости и нечеткости зрения, которые могут влиять на указанные способности, нужно проявлять особую осторожность при управлении автомобилем и работе с механизмами.
ФОРМА ВЫПУСКА
Таблетки покрытые пленочной оболочкой 400 мг.
Но 60 таблеток во флакон из полиэтилена высокой плотности, запаянный защитной мембраной и закрытый пластмассовой крышкой с устройством против вскрытия флакона детьми, и контейнер с силикагелем. По 1 флакону вместе с инструкцией по применению в картонную пачку.
УСЛОВИЯ ХРАНЕНИЯ
При температуре не выше 30С.
Хранить в недоступном для детей месте.
СРОК годности
2,5 года.
Не использовать по истечении срока годности, указанного на упаковке.
УСЛОВИЯ ОТПУСКА
По рецепту.
ЮРИДИЧЕСКОЕ ЛИЦО, НА ИМЯ КОТОРОГО ВЫДАНО РЕГИСТРАЦИОННОЕ УДОСТОВЕРЕНИЕ
Мерк Шарп и Доум Б.В., Нидерланды
ПРОИЗВОДИТЕЛЬ
Произведено:
МСД Интернэшнл ГмбХ (Сингапур Ьранч), Сингапур MSD International GmbH (Singapore Branch) 21 Tuas South Avenue 6, 637766, Singapore Упаковано /
Выпускающий контроль качества:
Мерк Шарп и Доум В.В., Нидерланды Merck Sharp & Dohme B.V.
Waarderweg 39, 2031 BN, Haarlem, the Netherlands
или
ЗАО «ОРТАТ», Россия
157092, Костромская обл., Сусанинский район, с. Северное, мкр-н Харитоново
ПРЕТЕНЗИИ ПОТРЕБИТЕЛЕЙ НАПРАВЛЯТЬ ПО АДРЕСУ
ООО «МСД Фармасыотикалс» Павловская, д. 7, стр. 1 Москва, Россия, 115093
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
1 таблетка, покрытая пленочной оболочкой, содержит:
активное вещество: ралтегравир калия 434,4 мг (эквивалентно 400 мг ралтегравира)
вспомогательные вещества: целлюлоза микрокристаллическая; лактозы моногидрат, кальция гидрофосфат, гипромеллоза 2208, полоксамер 407, натрия стеарилфумарат, магния стеарат.
Пленочное покрытие: краситель опадрай II серый (85F97553).
Пленочная оболочка: поливиниловый спирт, макрогол, тальк, титана диоксид, краситель железа оксид черный.
Овальные двояковыпуклые таблетки, покрытые пленочной оболочкой серого цвета с гравировкой «227» на одной стороне и гладкие на другой.
Ралтегравир ингибирует каталитическую активность ВИЧ интегразы — фермента, участвующего в репликации вируса. Ингибирование интегразы предотвращает ковалентное введение генома ВИЧ в геном клетки хозяина на ранних стадиях развития инфекции. Не включенные в ДНК человека геномы ВИЧ не способны индуцировать продукцию новых вирусных частиц, вследствие чего происходит подавление процесса интеграции и предотвращение дальнейшего распространения вирусной инфекции в организме. Ингибируюшая способность ралтегравира в отношении фосфотрансферазы человека, включая ДНК-полимеразы α, β и γ, выражена незначительно.
Микробиология
При значениях плазменных концентраций 31 ± 20 нмоль ралтегравир обеспечивал подавление распространения вируса на 95% (ПК95) в клеточных культурах человеческих Т-лимфоцитов, инфицированных адаптированным к культурам клеток вариантом H9IIIB ВИЧ-1, по сравнению с контрольной вирус-инфицированной культурой клеток. В концентрациях от 6 до 50 нмоль препарат демонстрировал ПК95 в культурах человеческих митоген-активированных мононуклеаров периферической крови, инфицированных различными первичными клиническими штаммами ВИЧ-1, включая штаммы, резистентные к ингибиторам обратной транскриптазы и ингибиторам протеазы. Ралтегравир также подавлял репликацию штаммов ВИЧ-2 в Т-лимфоцитах (ПК95 = 6 нмоль). При одновременном введении в культуру человеческих Т-лимфоцитов, инфицированных вариантом H9IIIB вируса ВИЧ-1, отмечена дополнительная синергичная активность ралтегравира с другими антиретровирусными препаратами, в том числе, нуклеозидными аналогами ингибиторов обратной транскриптазы (зидовудин, зальцитабин, ставудин, абакавир, тенофовир, диданозин и делавирдин), ингибиторами протеазы (индинавир, саквинавир, ритонавир, ампренавир, лопинавир и атазанавир) и ингибитором проникновения энфувиртидом.
Всасывание
Ралтегравир быстро всасывается после приема препарата натощак, максимальная концентрация (Стах) в плазме крови определяется примерно через 3 часа. Площадь под кривой «концентрация — время» (AUC) и значение Стах увеличиваются пропорционально дозе в диапазоне доз от 100 до 1600 мг. При режиме введения препарата 2 раза в сутки равновесное состояние достигается быстро, примерно в течение 2 дней после начала лечения. Значения AUC и Сmах свидетельствуют в пользу минимальной кумуляции препарата.
Абсолютная биодоступность ралтегравира не установлена.
Ралтегравир можно принимать вне зависимости от режима приема пищи.
Распределение
Примерно 83% ралтегравира связывается с белками плазмы в диапазоне концентраций от 2 до 10 мкмоль.
Ралтегравир легко преодолевал плацентарный барьер в экспериментальных исследованиях на крысах, но не проникал через гематоэнцефалический барьер.
Метаболизм и выведение
Основной путь метаболизма ралтегравира у человека представлен процессом уридин- дифосфат глюкуронозилтрансфераза (УДФ-ГТ)1А1 опосредованной глюкуронизации. После приема внутрь ралтегравира примерно 51% и 32% от общей дозы выделяется через кишечник и почки, соответственно. В кале обнаруживается только ралтегравир — продукт гидролиза ралтегравир-глюкуронида, секретируемого в желчь. В моче определяется ралтегравир и ралтегравир-глюкуронид в пропорциях, составляющих примерно 9 и 23% от введенной дозы, в то время как в плазме крови 70% составляет ралтегравир, а 30% — ралтегравир-глюкуронид.
Фармакокинетика у отдельных групп пациентов
Пол
Пол не оказывает клинически значимого влияния на фармакокинетические параметры ралтегравира. Коррекции дозы препарата в зависимости от пола пациента не требуется.
Пожилые пациенты
Не обнаружено зависимости фармакокинетических параметров ралтегравира от возраста пациентов, поэтому коррекции дозы препарата в зависимости от возраста не требуется.
Дети
Фармакокинетические параметры ралтегравира у детей не изучались.
Пациенты из разных расово-этнических групп
Расово-этническая принадлежность не оказывала клинически значимого влияния на фармакокинетические параметры ралтегравира. Коррекции дозы не требуется.
Пациенты с различным индексом массы тела (ИМТ)
ИМТ не оказывал клинически значимого влияния на фармакокинетические параметры ралтегравира. Коррекции дозы препарата в зависимости от ИМТ пациента не требуется.
Пациенты с печеночной недостаточностью
Ралтегравир метаболизируется преимущественно печенью и выводится через кишечник в виде конъюгата с глюкуронидом. Клинически значимых отклонений фармакокинетических параметров у пациентов с умеренной печеночной недостаточностью по сравнению со здоровыми добровольцами не выявили. Таким образом, коррекции дозы препарата при умеренной печеночной недостаточности не требуется. Влияние тяжелой печеночной недостаточности на фармакокинетические параметры ралтегравира не изучалось.
Пациенты с почечной недостаточностью
На почечный клиренс приходится незначительная доля в элиминации ралтегравира из организма. Фармакокинетика препарата была изучена у пациентов с тяжелой почечной недостаточностью, а также в сложном фармакокинетическом анализе. Клинически значимых отклонений фармакокинетических параметров у пациентов с тяжелой почечной недостаточностью по сравнению со здоровыми добровольцами не выявлено. Таким образом, коррекции дозы препарата пациентам с тяжелой почечной недостаточностью не требуется. Поскольку эффективность диализа препарата ИСЕНТРЕСС неизвестна, принимать препарат накануне сеанса диализа не рекомендуется.
Пациенты с полиморфизмом УДФ-ГТ1А1
По данным еще незавершенного клинического исследования полиморфизм УДФ-ГТ1А1 у пациентов не оказывает влияния на фармакокинетические параметры ралтегравира.
Лечение ВИЧ-1 инфекции в комбинации с другими антиретровирусными препаратами у взрослых пациентов, в том числе, при неэффективности предшествующей антиретровирусной терапии.
• Повышенная чувствительность к какому-либо из компонентов препарата.
• Детский возраст до 18 лет.
• Беременность.
• Период лактации.
ИСЕНТРЕСС содержит лактозу, поэтому пациенты с редкой наследственной непереносимостью лактозы, дефицитом лактазы или нарушенным всасыванием глюкозо-галактозы не должны принимать этот препарат.
Контролируемых исследований препарата ИСЕНТРЕСС у беременных не проводилось, поэтому, ИСЕНТРЕСС не рекомендуется назначать во время беременности. Отсутствуют данные о поступлении ралтегравира в грудное молоко человека. Однако обнаружена секреция ралтегравира в молоко у крыс. При введении препарата в суточной дозе 600 мг/кг концентрация ралтегравира в молоке превышала плазменную концентрацию примерно в 3 раза. Препарат ИСЕНТРЕСС не должен назначаться в период лактации. Кроме этого, грудное вскармливание не рекомендуется ВИЧ- инфицированным матерям во избежание постнатальной передачи ВИЧ детям.
Внутрь. Таблетки ИСЕНТРЕССа, которые нельзя жевать, крошить, разламывать, назначают вне зависимости от приема пищи.
Лечение препаратом ИСЕНТРЕСС должен проводить врач, обладающий достаточным опытом терапии ВИЧ-инфекции.
Рекомендуемая доза препарата ИСЕНТРЕСС для лечения ВИЧ-1- инфекции составляет 400 мг х 2 раза в сутки. Лечение препаратом ИСЕНТРЕСС проводят в комбинации с другими антиретровирусными препаратами.
Перечисленные ниже побочные реакции выявлены в ходе клинических многоцентровых плацебо контролируемых исследований, в которых сравнивали эффективность и безопасность комбинации ИСЕНТРЕСС (400 мг х 2 раза в день) и оптимизированной стандартной терапии (507 больных) и плацебо оптимизированной стандартной терапии (282 больных). С частотой > 2% наблюдались следующие побочные эффекты: диарея, тошнота, головная боль и повышение температуры.
Побочные эффекты, наблюдаемые с частотой < 2%, представлены по органам и системам в классификации «часто» (> 1/100<1/10) и «нечасто» (> 1/1000 <1/100) .
Со стороны системы крови и кроветворных органов Нечасто: анемия, в т.ч. макроцитарная анемия, нейтропения.
Со стороны сердечно-сосудистой системы
Нечасто: инфаркт миокарда, сердцебиение, желудочковая экстрасистолия.
Со стороны органов чувств
Часто: головокружение, нечеткость зрения.
Со стороны желудочно-кишечного тракта
Часто: боли в животе, метеоризм, запор.
Нечасто: рвота, ощущение дискомфорта и боль в верхних отделах живота, диспепсия, гастрит, глоссит, гастро-эзофагеальный рефлюкс.
Со стороны гепатобилиарной системы
Нечасто: гепатит, гепатомегалия.
Со стороны иммунной системы
Нечасто: аллергические реакции.
Инфекции и инвазии
Нечасто: флегмона, герпес simplex.
Со стороны обмена веществ
Нечасто: сахарный диабет, нарушение жирового обмена, дислипидемия, повышение аппетита, липоматоз, снижение или увеличение массы тела.
Со стороны опорно-двигательного аппарата
Часто: артралгия.
Нечасто: миалгия, боли в конечностях, боли в спине, мышечные спазмы, миозит, мышечная атрофия.
Со стороны нервной системы
Нечасто: периферическая нейропатия, парестезии, полинейропатия, сонливость, головная боль напряжения.
Со стороны органов дыхания
Нечасто: носовое кровотечение.
Со стороны почек и мочевыводящей системы
Нечасто: токсическая нефропатия, нефротический синдром, никтурия, поллакиурия, почечная недостаточность, тубулярный некроз.
Со стороны репродуктивных органов
Нечасто: эректильная дисфункция и гинекомастия.
Со стороны кожи и подкожно-жировой клетчатки
Часто: приобретенная липодистрофия, гипергидроз, зуд.
Психические расстройства
Нечасто: депрессия, бессонница, необычные сновидения, чувство тревоги.
Прочие
Часто: астения, слабость.
Нечасто: чувство дискомфорта в грудной клетке, озноб, жар, раздражительность.
Со стороны лабораторных показателей
Гипергликемия, лактацидемия, гиперлипидемия, гипертриглицеридемия, повышение в сыворотке крови уровня общего билирубина, ACT, AJIT, щелочной фосфатазы и креатинфосфокиназы.
Специфических симптомов передозировки препарата ИСЕНТРЕСС не выявлено. Клинический опыт показывает, что ралтегравир обладает широким терапевтическим диапазоном и вероятность токсических проявлений при передозировке очень низка. В случае передозировки необходимо следовать стандартным рекомендациям, таким как: удаление невсосавшегося препарата из желудочно-кишечного тракта, наблюдение за показателями жизнедеятельности, включая ЭКГ, назначение симптоматической терапии. Данных об эффективности диализа при передозировке препаратом ИСЕНТРЕСС нет.
Ралтегравир не является субстратом изоферментов системы цитохрома Р450 и не ингибирует (ПК50 > 100 мкмоль) CYP1A2, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6 или CYP3A in vitro. Кроме этого, ралтегравир не индуцирует in vitro CYP3A4. Исследование с мидазоламом продемонстрировало низкий потенциал влияния ралтегравира на фармакокинетические параметры лекарственных средств, метаболизируемых CYP3A4 in vivo.
Ралтегравир, также, не является ингибитором (ПК50 >50 мкмоль) УДФ-ГТ — УДФ- ГТ1А1, УДФ-ГТТ2В7 и р-гликопротеин-опосредованного транспорта. Следовательно, ИСЕНТРЕСС не оказывает влияния на фармакокинетические параметры препаратов, являющихся субстратами этих ферментов и р-гликопротеина (т.е., ингибиторов протеаз, метадона, ненуклеозидных ингибиторов обратной транскриптазы, опиоидных анальгетиков, статинов, противогрибковых азолов, ингибиторов протонной помпы, пероральных контрацептивов и препаратов для лечения эректильной дисфункции). Влияние мощных индукторов ферментов — таких как фенитоин, фенобарбитал, задействованных в метаболизме препарата, на УДФ-ГТ1А1, неизвестно. Другие менее мощные индукторы (эфавиренз, невирапин, рифабутин, глюкокортикостероиды, пиоглитазон, зверобой) могут назначаться одновременно с рекомендованными дозами препарата ИСЕНТРЕСС.
Одновременное назначение препарата ИСЕНТРЕСС с мощными ингибиторами УДФ- ГТ1А1 (т.е., атазанавир) сопровождается умеренным увеличением плазменной концентрации препарата ИСЕНТРЕСС. По данным клинических исследований комбинированная терапия двумя препаратами, в целом, хорошо переносилась пациентами, необходимости в коррекции дозы не потребовалось.
Пациентов нужно поставить в известность о том, что современные антиретровирусные препараты не излечивают ВИЧ-инфекцию и не предотвращают передачу ВИЧ другим людям с кровью или при половых контактах. Во время лечения препаратом ИСЕНТРЕСС пациенты должны продолжать соблюдать соответствующие меры безопасности.
Самые высокие показатели эффективности ИСЕНТРЕССА отмечались у пациентов с результатами генотипирования выше 0. Пациенты, у которых результаты генотипирования или фенотипирования равны нулю, имеют высокий риск развития резистентности к ралтегравиру. Для того, чтобы повысить эффективность лечения и снизить риск развития резистентности к препарату, ралтегравир необходимо назначать в комбинации хотя бы с одним активным противовирусным препаратом.
Синдром восстановления иммунитета
На начальных этапах комбинированной терапии антиретровирусными средствами у ВИЧ-инфицированных пациентов может развиться воспалительная реакция на бессимптомные или остаточные оппортунистические инфекции (цитомегаловирусный ретинит, пневмоцистная пневмонии, вызванная Pneumocystis jiroveci, туберкулез и др.) которая может проявляться в виде ухудшения клинического состояния и усиления имеющихся симптомов. Обычно такие реакции наблюдаются в первые недели или месяцы после начала терапии. В подобных случаях могут потребоваться дополнительные диагностические и лечебные мероприятия.
Остеонекроз
Описаны случаи развития остеонекроза, особенно при тяжелом течении ВИЧ инфекции и/или длительном приеме комбинированной противовирусной терапии. Пациентам, у которых появились такие симптомы как боль в суставах, скованность или ограничение подвижности, нужна срочная консультация специалиста.
Применение препарата ИСЕНТРЕСС у пациентов, инфицированных вирусами гепатита В и/или С.
У пациентов с хроническим активным гепатитом В и/или гепатитом С, получающих комбинированную противовирусную терапию, повышен риск развития тяжелых и иногда фатальных побочных эффектов.
ВЛИЯНИЕ НА СПОСОБНОСТЬ УПРАВЛЕНИЯ АВТОМОБИЛЕМ И РАБОТЫ С МЕХАНИЗМАМИ.
Исследования по изучению влияния на способность к управлению транспортными средствами и использованию механизмов не проводились. Учитывая возможность развития головокружения, слабости, сонливости и нечеткости зрения на фоне лечения препаратом ИСЕНТРЕСС, нужно проявлять особую осторожность при управлении ) автомобилем и работе с механизмами.
Взаимосвязь таких побочных эффектов, как миопатия, рабдомиолиз и увеличение концентрации креатинфосфокиназы в сыворотке крови с лечением препаратом ИСЕНТРЕСС не определена, поэтому следует соблюдать осторожность при назначении препарата пациентам с известным риском миопатии и рабдомиолиза, в частности, получающим сопутствующую терапию препаратами, способными вызвать эти побочные эффекты.
Следует соблюдать осторожность при назначении препарата ИСЕНТРЕСС одновременно с мощными индукторами УДФ-ГТ 1А1, такими как рифампицин, ввиду снижения ими плазменной концентрации ралтегравира. При необходимости проведения комбинированной терапии рифампицином и ИСЕНТРЕССОМ, доза ИСЕНТРЕССА должна быть увеличена в 2 раза.
Тяжелая печеночная недостаточность требует применения препарата с осторожностью. При нарастании печеночной недостаточности на фоне лечения препаратом ИСЕНТРЕСС необходим перерыв или остановка лечения.
Таблетки, покрытые пленочной оболочкой, 400 мг.
По 60 таблеток во флакон из полиэтилена высокой плотности, запаянный защитной мембраной и закрытый пластмассовой крышкой с устройством против вскрытия флакона детьми и контейнер с силикагелем.
По 1 флакону вместе с инструкцией по применению в картонной пачке.
При температуре не выше 30 °С. Хранить в недоступном для детей месте.
2 года.
Не использовать по истечении срока годности, указанного на упаковке.
Исентресс
Исентресс: инструкция по применению и отзывы
- 1. Форма выпуска и состав
- 2. Фармакологические свойства
- 3. Показания к применению
- 4. Противопоказания
- 5. Способ применения и дозировка
- 6. Побочные действия
- 7. Передозировка
- 8. Особые указания
- 9. Применение при беременности и лактации
- 10. Применение в детском возрасте
- 11. При нарушениях функции почек
- 12. При нарушениях функции печени
- 13. Применение в пожилом возрасте
- 14. Лекарственное взаимодействие
- 15. Аналоги
- 16. Сроки и условия хранения
- 17. Условия отпуска из аптек
- 18. Отзывы
- 19. Цена в аптеках
Латинское название: Isentress
Код ATX: J05AX08
Действующее вещество: ралтегравир (Raltegravir)
Производитель: МСД Интернешнл ГмбХ (Сингапур Бранч) [MSD International GmbH (Singapore Branch)] (Сингапур); МСД Интернэшнл ГмбХ (MSD International GmbH) (Ирландия/Нидерланды); Патеон Фармасьютикалс Инк. (Patheon Pharmaceuticals Inc.) (США); Р-Фарм АО (Россия)
Актуализация описания и фото: 28.10.2021

Исентресс – противовирусный препарат, активный в отношении вируса иммунодефицита человека (ВИЧ).
Форма выпуска и состав
Лекарственные формы препарата Исентресс:
- таблетки, покрытые пленочной оболочкой, дозировка 400 мг: двояковыпуклые, овальные, розового цвета, на одной из сторон нанесена гравировка «227»;
- таблетки, покрытые пленочной оболочкой, дозировка 600 мг: двояковыпуклые, овальные, желтого цвета, на одной из сторон нанесена гравировка логотипа компании Merck и «242»;
- таблетки жевательные, дозировка 25 мг: плоскоцилиндрические, со скошенными краями, круглые, бледно-желтого цвета с вкраплениями белого цвета, на одной из сторон нанесена гравировка логотипа компании Merck, а на другой – «473»;
- таблетки жевательные, дозировка 100 мг: двояковыпуклые, овальные, бледно-оранжевого цвета с вкраплениями белого цвета, на одной стороне нанесена разделительная риска, а на другой гравировка логотипа компании Merck и «477», разделенные риской.
Упаковка: по 60 шт. во флаконах из полиэтилена высокой плотности, в картонной пачке 1 флакон и инструкция по применению Исентресса.
В 1 таблетке, покрытой пленочной оболочкой, содержатся:
- действующее вещество: ралтегравир калия – 434,4 или 651,6 мг (эквивалентно ралтегравиру в количестве 400 и 600 мг);
- дополнительные компоненты: целлюлоза микрокристаллическая, магния стеарат; дополнительно для 400 мг – гипромеллоза 2208, лактозы моногидрат, кальция гидрофосфат, полоксамер 407 (включает в состав 0,01% бутилгидрокситолуола в качестве антиоксиданта), натрия стеарилфумарат; дополнительно для 600 мг – кроскармеллоза натрия, гипромеллоза 2910;
- пленочная оболочка: 400 мг – краситель Опадрай II розовый 85F94224 (макрогол, титана диоксид, поливиниловый спирт, тальк, краситель железа оксид красный и оксид черный); 600 мг – воск карнаубский, Опадрай II желтый 39К170005 (гипромеллоза 2910, лактозы моногидрат, триацетин, титана диоксид, краситель железа оксид желтый и оксид черный).
В 1 таблетке жевательной содержатся:
- действующее вещество: ралтегравир калия – 27,16 или 108,6 мг (эквивалентно ралтегравиру в количестве 25 и 100 мг);
- дополнительные компоненты: сукралоза, гипролоза, Опадрай бесцветный YS-1-19025-А*, натрия сахаринат, Surelease E-7-19040**, маннитол, натрия цитрата дигидрат, аммония глицирризинат (Magnasweet 135***), магния стеарат, кросповидон, натрия стеарилфумарат, краситель железа оксид желтый, ароматизатор апельсиновый натуральный и искусственный 501331 TP0551, ароматизатор банановый натуральный WONF Durarome 501392 TD0991, ароматизатор маскирующий натуральный и искусственный 501482 TP0424****; дополнительно для 100 мг – краситель железа оксид красный.
Примечания
* – содержит гипромеллозу 2910/6cP и макрогол
** – включает в состав 25% водной суспензии этилцеллюлозы в воде очищенной, аммония гидроксид, этилцеллюлозу 20сР, триглицериды среднецепочные, олеиновую кислоту
*** – состоит из экстракта солодки, фруктозы и сорбитола
**** – содержит аспартам
Фармакологические свойства
Фармакодинамика
Действующий компонент препарата Исентресс – ралтегравир, подавляет каталитическую активность фермента, принимающего участие в размножение (репликации) вируса ВИЧ – интегразы ВИЧ. При ингибировании последней предотвращается ковалентное введение, или интеграция в геном клетки хозяина генома ВИЧ на ранних этапах развития инфекции. Геномы ВИЧ, не введенные в ДНК человека, не могут продуцировать новые вирусные частицы, таким образом, угнетение процесса интеграции блокирует дальнейшее распространение в организме вирусной инфекции. По отношению к фосфотрансферазам человека, включая ДНК-полимеразы α, β и γ, ингибирующая активность ралтегравира выражена в слабой степени.
При содержании в плазме, составляющем 31±20 нмоль/л, ралтегравир подавлял репликацию вируса на 95% (ингибирующая концентрация 95% – ИК95) в клеточных культурах человеческих Т-лимфоцитов, которые были инфицированы вариантом H9IIIB ВИЧ-1, адаптированным к культурам клеток, при сравнении с контрольной вирус-инфицированной культурой клеток. В концентрациях действующего вещества от 6 до 50 нмоль/л была достигнута ИК95 в культурах человеческих митоген-активированных мононуклеаров периферической крови, зараженных различными первичными клиническими штаммами ВИЧ-1, в т. ч. штаммами 5 не-В подтипов, а также штаммами устойчивыми к ингибиторам протеазы ВИЧ и ингибиторам обратной транскриптазы.
В ходе анализа разового цикла инфекции ралтегравир ингибировал инфицирование, возбуждаемое 23 штаммами ВИЧ, являющимися 5 не-В подтипами и 5 циркулирующими рекомбинантными формами с ИК50 – 5–12 нмоль/л. Мутации интегразы ВИЧ-1, содействующие возникновению устойчивых к влиянию ралтегравира штаммов вируса (развивались у получавших препарат пациентов, или in vitro), преимущественно содержат замены в положениях 148 (Q148 замена на Н, К или R), 143 (Y143 замена на С, Н или R) или 155 (N155 замена на Н), в комбинации с не менее одной дополнительной мутацией (например, Т97А, E92Q, L74M, G140A/S, Е138А/К, V151I, S230R, G163R).
Рекомбинантные вирусы с включением одной первичной мутации (Q148H, К или R, или N155H) характеризовались сниженной способностью к репликации и слабой чувствительностью к ралтегравиру in vitro. Вторичные мутации вируса приводили к дальнейшему уменьшению чувствительности к активному веществу, в некоторых случаях компенсируя ослабленную способность вируса к репликации.
Ассоциированные с появлением резистентности к ралтегравиру мутации, также способны вызывать формирование резистентности к другому ингибитору переноса цепи интегразой – элвитегравиру.
В ходе плацебо-контролируемого клинического исследования, в котором принимали участие здоровые добровольцы, однократный прием препарата Исентресс в дозе 1600 мг не оказывал воздействия на длительность интервала QTc, невзирая на то, что в плазме крови его максимальная концентрация (Cmax) была в 4 раза больше, чем при однократном приеме в дозе 400 мг.
Фармакокинетика
У взрослых пациентов ралтегравир после перорального приема натощак быстро абсорбируется, плазменная Cmax в крови наблюдается приблизительно спустя 3 часа. Величина площади под кривой «концентрация – время» (AUC) и Cmax вещества возрастают пропорционально дозе в диапазоне доз от 100 до 1600 мг. Значения содержания ралтегравира в плазме крови через 12 часов после приема (С12ч) повышаются пропорционально дозе в диапазоне доз от 100 до 800 мг, и увеличиваются несколько меньше в диапазоне от 100 до 1600 мг.
При использовании Исентресса 2 раза в сутки равновесное состояние отмечается примерно на протяжении 2 дней после начала курса. Величины AUC и Cmax подтверждают отсутствие или минимальное накопление вещества, а величина С12ч свидетельствует о незначительном накоплении. При использовании ралтегравира в качестве препарата монотерапии 2 раза в сутки по 400 мг значение среднего геометрического для AUC в интервале от 0 до 12 часов (AUC0-12ч) составляло 14,3 мкмоль/л × ч, величина С12ч – 142 нмоль/л. Абсолютная биодоступность средства не определена.
С белками плазмы крови связывается в среднем 83% ралтегравира в диапазоне уровня содержания от 2 до 10 мкмоль. В процессе доклинических исследований установлено, что активное вещество легко проникало через плацентарный барьер у крыс, но в заметной степени не проходило через гематоэнцефалический барьер (ГЭБ).
При проведении двух клинических исследований с участием больных, инфицированных ВИЧ-1, которые получали 2 раза в сутки ралтегравир в дозе 400 мг, он быстро фиксировался в спинномозговой жидкости. В первом исследовании в спинномозговой жидкости средний уровень ралтегравира составил 5,8% (в диапазоне от 1 до 53,5%) от соответствующего уровня содержания в плазме крови, а во втором исследовании – 3% (в диапазоне от 1 до 61%) от соответствующего уровня в плазме крови. Медианы установленных значений были примерно в 3–6 раз ниже, чем уровни свободной фракции ралтегравира в плазме крови.
По результатам исследований, в которых применялись селективные ингибиторы к изоформе фермента уридиндифосфатглюкуронилтрансферазы (УДФГТ), произведенной посредством экспрессии комплементарной ДНК, УДФГТ1А1 относится к основным ферментам, отвечающим за образование ралтегравир-глюкуронида. Согласно этим результатам у человека главным путем метаболической трансформации ралтегравира является процесс глюкуронирования, опосредованный УДФГТ1А1. Продолжительность конечной фазы периода полувыведения (Т1/2) вещества равна примерно 9 часам, а большая часть AUC соответствует менее длительной α-фазе кажущегося Т1/2 активного вещества, составляющего в среднем 1 час.
После перорального приема радиоактивно меченого ралтегравира приблизительно 32% от полученной дозы экскретируется почками, и 51% – через кишечник. В каловых массах был определен только ралтегравир, вероятно сформированный посредством гидролиза ралтегравир-глюкуронида, который элиминировался с желчью. Ралтегравир и ралтегравир-глюкуронид обнаруживались в моче в количестве 9 и 23% от первоначальной дозы соответственно. Основным циркулирующим радиоактивным ингредиентом в плазме крови был ралтегравир, составляющий в среднем 70% от общей радиоактивности, остальные 30% приходились на ралтегравир-глюкуронид.
Пол, индекс массы тела (ИМТ) и расово-этническая принадлежность больных не оказывают клинически значимого воздействия на фармакокинетические параметры Исентресса и не требуют проведения коррекции дозы.
У детей до 2 лет фармакокинетика препарата не изучалась.
Для подростков и детей старше 2 лет (жевательные таблетки) и старше 6 лет (таблетки, покрытые пленочной оболочкой) дозы ралтегравира для терапии ВИЧ-1 инфекции рекомендованы на том основании, что его основные параметры фармакокинетики соизмеримы с таковыми у взрослых больных, получающих 2 раза в сутки таблетки, покрытые пленочной оболочкой в дозе 400 мг.
Показания к применению
Исентресс рекомендован к применению для лечения ВИЧ-1 инфекции в сочетании с другими антиретровирусными средствами:
- таблетки, покрытые пленочной оболочкой: у взрослых, подростков и детей от 6 лет и старше с весом тела не менее 25 кг (дозировка 400 мг) или с весом тела не менее 40 кг (дозировка 600 мг);
- таблетки жевательные: у детей в возрасте 2–11 лет, как ранее получавших, так и не получавших антиретровирусную терапию (АРВТ).
Противопоказания
Абсолютные:
- беременность и период кормления грудью;
- возраст до 6 лет и вес тела до 25 кг (400 мг) или вес тела до 40 кг (600 мг) – для таблеток, покрытых пленочной оболочкой; возраст до 2 лет и вес тела до 7 кг – для жевательных таблеток;
- дефицит сахаразы/изомальтазы, непереносимость фруктозы, глюкозо-галактозная мальабсорбция – для жевательных таблеток (содержат сорбитол и фруктозу);
- непереносимость лактозы, мальабсорбция глюкозы/галактозы или дефицит лактазы – для таблеток, покрытых пленочной оболочкой (содержат лактозу);
- фенилкетонурия – для жевательных таблеток т. к. они содержат фенилаланин в качестве компонента аспартама (0,05 мг в дозе 25 мг и примерно 0,1 мг – в 100 мг);
- гиперчувствительность к любому составляющему препарата.
Относительные (принимать таблетки Исентресс требуется с осторожностью):
- печеночная недостаточность тяжелой степени;
- миопатия и рабдомиолиз (включая данные в анамнезе), а также состояния и факторы, предрасполагающие к их развитию;
- одновременное использование с сильными индукторами УДФГТ1А1 (включая рифампицин) или с антацидами, содержащими магний/алюминий; дополнительно для 600 мг – с типранавиром/ритонавиром, атазанавиром;
- депрессия, в т. ч. наличие суицидальных идей и поведения (фиксировалась преимущественно у больных с указаниями в анамнезе на депрессию или психиатрические заболевания);
- пожилой возраст – для таблеток, покрытых пленочной оболочкой.
Исентресс, инструкция по применению: способ и дозировка
Таблетки Исентресс используют перорально, в комбинации с другими антиретровирусными средствами. Время приема не зависит от режима питания.
Назначать и проводить лечение препаратом должен врач, имеющий достаточный опыт терапии ВИЧ-инфекции.
Таблетки, покрытые пленочной оболочкой
Таблетки, покрытые пленочной оболочкой, следует проглатывать целиком, не разламывая, не измельчая и не разжевывая.
Взрослым, подросткам и детям с весом тела не менее 25 кг, Исентресс в дозировке 400 мг рекомендуют принимать 2 раза в сутки по 1 таблетке, суточная доза составляет 800 мг. При необходимости дальнейшего перехода на прием таблеток в дозировке 600 мг, пациентам, включая детей с весом тела не менее 40 кг, назначают препарат в дозе 1200 мг – 2 таблетки по 600 мг, принимаемые 1 раз в сутки.
Если у пациентов детского возраста возникают трудности с проглатыванием таблеток, покрытых оболочкой, можно рассмотреть возможность их перевода на прием жевательных таблеток Исентресс.
Таблетки жевательные
Максимально допустимая суточная доза жевательных таблеток составляет 300 мг 2 раза в сутки. Исследования терапии противовирусным препаратом в данной форме у ВИЧ-инфицированных взрослых и подростков от 12 до 18 лет не проводились.
Поскольку лекарственные формы Исентресса не являются биоэквивалентными, не следует заменять таблетки жевательные, таблетками, покрытыми пленочной оболочкой, в дозировке 400 мг.
Рекомендованные разовые дозы* жевательных таблеток для детей в возрасте от 2 до 11 лет в зависимости от веса тела (при кратности приема 2 раза в сутки):
- > 7, но < 10 кг: 50 мг – ½ таблетки по 100 мг1;
- ≥ 10, но < 14 кг: 75 мг – 3 таблетки по 25 мг;
- ≥ 14, но < 20 кг: 100 мг – 1 таблетка по 100 мг;
- ≥ 20, но < 28 кг: 150 мг – 1½ таблетки по 100 мг;
- ≥ 28, но < 40 кг: 200 мг – 2 таблетки по 100 мг;
- ≥ 40 кг: 300 мг – 3 таблетки по 100 мг.
Примечания
* – рекомендации доз по весу тела основаны приблизительно из расчета 6 мг/кг/доза 2 раза в сутки
1 – таблетки жевательные в дозировке 100 мг можно делить на две половины, однако по возможности следует избегать такого деления
Пациентам следует в точности соблюдать график дозирования, т. к. дозу ралтегравира требуется изменять по мере роста ребенка.
Взрослым и подросткам в возрасте от 12 лет с весом тела не менее 25 кг рекомендуется принимать Исентресс в форме таблеток, покрытых оболочкой в дозировке 400 мг.
Побочные действия
Нижеперечисленные нежелательные реакции были зафиксированы в ходе клинических исследований и связаны с различной степенью вероятности с использованием Исентресса или его сочетанием с другой АРВТ:
- инфекционные и паразитарные заболевания: нечасто – фолликулит, инфицирование верхних дыхательных путей, назофарингит, генитальный герпес, простой герпес, опоясывающий лишай, герпетическая инфекция, гастроэнтерит, абсцесс лимфоузла, грипп, контагиозный моллюск;
- иммунная система: нечасто – гиперчувствительность к препарату, синдром восстановления иммунитета, реакции гиперчувствительности;
- система кроветворения и лимфатическая система: нечасто – анемия, болезненность лимфоузлов, железодефицитная анемия, нейтропения, лимфаденопатия, тромбоцитопения1;
- обмен веществ: часто – снижение аппетита; нечасто – повышение аппетита, гиперфагия, гиперлипидемия, гипергликемия, гиперхолестеринемия, дислипидемия, сахарный диабет, кахексия, нарушение жирового обмена, полидипсия;
- неуточненные, доброкачественные и злокачественные новообразования (включая полипы и кисты): нечасто – папилломатоз кожи;
- нервная система: часто – головная боль, психомоторная гиперреактивность2, головокружение; нечасто – снижение качества сна, сонливость, тремор, головная боль напряжения, мигрень, гиперсомния, дисгевзия, постуральное головокружение, нарушение внимания, расстройство памяти, синдром запястного канала, гипестезия, летаргия, парестезии, периферическая невропатия, когнитивные расстройства, амнезия;
- нарушения психики: часто – бессонница, необычные сновидения, ночные кошмары, депрессия, нарушение поведения2; нечасто – нарушения сна, бессонница середины ночи, изменения настроения, чувство тревоги, подавленное настроение, психические расстройства, большое депрессивное расстройство, панические атаки, суицидальные попытки, суицидальное поведение1, суицидальные идеи1(особенно при наличии психиатрических заболеваний в анамнезе);
- орган слуха и лабиринтные нарушения: часто – вертиго; нечасто – шум в ушах;
- орган зрения: нечасто – снижение остроты зрения;
- дыхательная система, органы грудной клетки и средостения: нечасто – заложенность носа, носовое кровотечение, дисфония;
- сердечно-сосудистая система: нечасто – приливы крови к коже лица с чувством жара, ощущение сердцебиения, артериальная гипертензия, желудочковая экстрасистолия, синусовая брадикардия;
- печень и желчевыводящие пути: нечасто – стеатоз печени, гепатит, печеночная недостаточность1, алкогольный гепатит;
- половые органы и молочная железа: нечасто – симптомы менопаузы, гинекомастия, эректильная дисфункция;
- почки и мочевыводящие пути: нечасто – никтурия, нефролитиаз, нефрит, нарушение функции почек, киста почки, почечная недостаточность, тубулоинтерстициальный нефрит;
- кожа и подкожные ткани: часто – кожная сыпь; нечасто – сухость кожи, акне, угревидная сыпь, алопеция, липоатрофия лица, эритема, приобретенная липодистрофия, липоатрофия, липогипертрофия, ночная потливость, гипергидроз, зуд (локальный и генерализованный), пруриго, крапивница, зудящая сыпь, ксеродермия, макулопапулезная/макулярная сыпь, другие поражения кожи, лекарственная сыпь с эозинофилией и системными симптомами (DRESS-синдром)1, синдром Стивенса – Джонсона1;
- костно-мышечная система: нечасто – боль в боку, боль в спине, боль в конечностях, артрит, артралгия, миалгия, остеопения, боль в области шеи, тендинит, остеопороз, миопатия, полиартрит, рабдомиолиз1;
- пищеварительная система: часто – диспепсия, тошнота, рвота, чувство распирания/боль в животе, метеоризм, диарея; нечасто – болезненность при глотании, сухость во рту, отрыжка, боль в верхних отделах живота, ощущение дискомфорта в эпигастральной области/животе, болезненность в области живота, запор, ощущение дискомфорта в области заднего прохода, эрозивный дуоденит, глоссит, гингивит, гастроэзофагеальный рефлюкс, пептическая язва, острый панкреатит, ректальные кровотечения;
- интоксикации, травмы и осложнения манипуляций: нечасто – непроизвольная передозировка;
- лабораторные и инструментальные данные: часто – возрастание активности в плазме аспартатаминотрансферазы (АСТ), аланинаминотрансферазы (АЛТ), амилазы и липазы поджелудочной железы, повышение содержания триглицеридов и числа атипичных лимфоцитов; нечасто – понижение абсолютного количества нейтрофилов плазмы; повышение активности в плазме креатинфосфокиназы (КФК), щелочной фосфатазы (ЩФ), уменьшение содержания альбумина; возрастание уровня билирубина, креатинина, холестерина (ХС), азота мочевины, глюкозы (в т. ч. определяемой натощак), холестерина липопротеинов низкой плотности (ХС ЛПНП), холестерина липопротеинов высокой плотности (ХС ЛПВП); повышение значения международного нормализованного отношения (МНО), снижение числа лейкоцитов и тромбоцитов в крови, наличие в моче глюкозы, эритроцитов; увеличение/снижение веса тела, увеличение окружности талии;
- общие расстройства: часто – лихорадка, астения, слабость; нечасто – озноб, дискомфорт в груди, недомогание, состояние беспокойства, увеличение объема жировой ткани, отек лица, боль, периферические отеки, подчелюстное новообразование.
Примечания
1 – побочные эффекты, не вызванные использованием Исентресса, которые фиксировались в пострегистрационном периоде и не выявлялись в ходе клинических исследований
2 – связанные с использованием препарата нежелательные явления, отмеченные у одного ребенка: нарушение поведения и психомоторная гиперреактивность III степени, бессонница
Согласно данным клинических исследований при приеме ралтегравира в рекомендованных дозах в сочетании с другими антиретровирусными средствами у ВИЧ-1 инфицированных детей и подростков 2–18 лет выраженность, частота и тип побочных эффектов, обусловленных приемом Исентресса, были такими же, как и у взрослых.
Передозировка
На фоне передозировки Исентресса специфических симптомов не зафиксировано. При приеме здоровыми добровольцами ралтегравира в режиме 1 раз в сутки по 1600 мг и 2 раза в сутки по 800 мг отмечалась хорошая переносимость терапии без каких-либо признаков токсичности. В ходе исследований II/III фазы однократный прием препарата в суточной дозе 1800 мг не демонстрировал токсического воздействия. Согласно имеющихся данных можно сделать вывод, что препарат хорошо переносится при использовании 2 раза в сутки в дозах до 800 мг, а также в комбинации с лекарственными средствами, приводящими к увеличению его экспозиции на 50–70% (атазанавир, тенофовир и др.). Поскольку ралтегравир имеет широкий терапевтический диапазон, вследствие передозировки потенциал его токсического действия довольно ограничен.
При подозрении на передозировку рекомендуется проведение стандартных поддерживающих мероприятий, таких как эвакуация неадсорбированного препарата из пищеварительного тракта, мониторинг показателей жизнедеятельности (в т. ч. ЭКГ), симптоматическая терапия. Степень экскреции ралтегравира при диализе не установлена.
Особые указания
Пациенты должны быть осведомлены о том, что текущая комбинированная АРВТ не излечивает ВИЧ-инфекцию и не препятствует передаче ВИЧ при половых контактах или с кровью другим людям. В период лечения препаратом Исентресс необходимо продолжать соблюдать соответствующие меры безопасности в целях предупреждения передачи вируса. Во время терапии крайне важно находиться под наблюдением специалиста, поскольку в этот период все еще могут возникнуть инфекции или другие нежелательные состояния, характерные для ВИЧ- инфицированных больных (оппортунистические инфекции).
Ралтегравир отличается относительно низким генетическим барьером к появлению резистентности, вследствие этого для усиления эффекта терапии и уменьшения риска развития невосприимчивости к Исентрессу, его необходимо по возможности использовать в комбинации с двумя другими активными антиретровирусными средствами.
Врача требуется информировать о возникновении любых необычных симптомов, а также о сохранении или усугублении любой известной побочной реакции.
У ВИЧ-инфицированных пациентов, имеющих тяжелую форму иммунной недостаточности, на начальном этапе комбинированной АРВТ может возникнуть так называемый синдром восстановления иммунитета, представляющий собой воспалительную реакцию на бессимптомно текущие/остаточные оппортунистические инфекции – диссеминированные/очаговые микобактериальные инфекции; пневмоцистная пневмония, возбуждаемая Pneumocystis jirovecii; цитомегаловирусный ретинит и другие. Данное осложнение способно усилить выраженность имеющихся симптомов и привести к усугублению клинического состояния. Как правило, появление такой реакции возможно на протяжении первых недель или месяцев после начала комбинированного лечения. Следует оценивать любой воспалительный симптом и при необходимости проводить лечение.
На фоне развития синдрома восстановления иммунитета возможно появление таких аутоиммунных расстройств как Базедова болезнь. Однако развитие подобных явлений может фиксироваться спустя много месяцев после начала курса лечения.
Невзирая на то, что этиология остеонекроза считается многофакторной (включая тяжелый иммунодефицит, употребление алкоголя, терапию ГКС, высокий ИМТ) имеются сообщения о случаях развития данного осложнения, в особенности при длительной комбинированной АРВТ и/или на поздних стадиях ВИЧ-инфекции. При возникновении таких симптомов, как ограничение подвижности, скованность или боль в суставах, нужно незамедлительно проконсультироваться с врачом.
Если появились признаки/симптомы реакции гиперчувствительности или тяжелых дерматологических реакций, к которым могут относиться: слабость, общее недомогание, сыпь, сопровождающаяся лихорадкой или тяжелая кожная сыпь, появление волдырей на коже, боли в мышцах/суставах, повреждения в ротовой полости, отек лица, конъюнктивит, эозинофилия, гепатит, ангионевротический отек, необходимо срочно прекратить лечение препаратом Исентресс и другими средствами, способными вызвать такие состояния. В подобных случаях требуется тщательно мониторировать клинический статус, в т. ч. уровень печеночных аминотрансфераз, и провести соответствующее лечение. Несвоевременный отказ от терапии препаратом или другими средствами, предположительно связанными с этими осложнениями, после возникновения тяжелой сыпи может привести к развитию жизнеугрожающих реакций.
Влияние на способность к управлению автотранспортом и сложными механизмами
Влияние Исентресса на быстроту психомоторных реакций и способность к концентрации внимания не изучалось. Поскольку на фоне терапии возможно возникновение нечеткости зрения, сонливости и головокружения, управлять транспортными средствами и работать с другой сложной техникой пациентам следует с особой осторожностью.
Применение при беременности и лактации
Контролируемые исследования эффективности и безопасности применения Исентресса у беременных не проводились, вследствие этого прием препарата во время беременности противопоказан.
Данных о поступлении ралтегравира в материнское молоко человека не имеется. Однако в процессе исследований на животных выявлено проникновение активного вещества в молоко у лактирующих крыс – при использовании ралтегравира в суточной дозе 600 мг/кг его уровень в молоке превышал плазменный уровень в среднем в 3 раза.
Кормление грудью не рекомендовано ВИЧ-инфицированным матерям во избежание передачи вируса младенцам, Исентресс не должен использоваться в период лактации.
Применение в детском возрасте
Таблетки жевательные Исентресс противопоказано принимать детям в возрасте до 2 лет с весом тела менее 7 кг. Прием таблеток, покрытых пленочной оболочкой, противопоказан детям до 6 лет: в дозе 400 мг – с весом тела ребенка менее 25 кг, в дозе 600 мг – менее 40 кг.
При нарушениях функции почек
Пациентам с функциональными нарушениями почек индивидуальный подбор доз Исентресса не требуется. Ввиду того, что эффективность диализа ралтегравира не установлена, не рекомендуется принимать средство накануне сеанса диализа.
При нарушениях функции печени
Безопасность и эффективность лечения препаратом больных с тяжелыми сопутствующими болезнями печени не установлены. При наличии тяжелой печеночной недостаточности следует принимать Исентресс с особой осторожностью. У больных с дисфункцией печени, в т. ч. с хроническим гепатитом, на фоне комбинированной АРВТ возрастает частота нарушений деятельности печени, вследствие чего пациенты данной группы риска подлежат мониторингу в соответствии со стандартной практикой. В случае развития у них признаков усугубления заболевания печени требуется рассмотреть вопрос о временном прерывании или прекращении приема препарата.
У больных с хроническим гепатитом B или C, получающих также комбинированную АРВТ, возрастает риск возникновения выраженных и потенциально угрожающих жизни нежелательных реакций со стороны печени.
При имеющихся легких и умеренных функциональных нарушениях печени нет необходимости в проведении коррекции дозы Исентресса.
Применение в пожилом возрасте
Поскольку имеется ограниченная информация об использовании ралтегравира у больных старше 65 лет, лечение препаратом у пациентов этой возрастной группы следует проводить с осторожностью (для доз 400/600 мг). Изменять дозу Исентресса пожилым пациентам не требуется.
Лекарственное взаимодействие
Не обнаруживается влияние Исентресса на фармакокинетические параметры лекарственных средств, являющихся субстратами Р-гликопротеина или ферментов CYP2B6, CYP1A2, CYP2C8, CYP2D6, CYP2C9, CYP2C19, CYP3A или CYP3A4, поскольку ралтегравир не относится к субстратам изоферментов системы цитохрома Р450, а также к ингибиторам Р-гликопротеин-опосредованного транспорта.
Фармакокинетическое взаимодействие ралтегравира с другими лекарственными средствами/веществами:
- маравирок, этравирин, тенофовир, гормональные контрацептивы, мидазолам, метадон: не отмечается клинически значимого влияния ралтегравира на фармакокинетику данных средств; изменения доз этих препаратов не требуется;
- дарунавир: наблюдается незначительное снижение плазменного уровня этого вещества в крови, не считающееся клинически значимым;
- рифампицин (сильные индукторы УДФГТ1А1): снижается концентрация ралтегравира в плазме крови; при данной концентрации необходимо соблюдать осторожность, поскольку ралтегравир метаболизируется преимущественно при участии УДФГТ1А1; влияние на эффективность Исентресса не установлено, в случае необходимости подобной комбинации у взрослых допускается возможность увеличения дозы ралтегравира в 2 раза, однако комбинация последнего в суточной дозе 1200 мг с рифампицином не рекомендуется; данных по сочетанному использованию ралтегравира и рифампицина у пациентов до 18 лет не имеется;
- этравирин, невирапин, эфавиренз, ГКС, рифабутин, пиоглитазон, зверобой продырявленный (индукторы УДФГТ1А1): возможно сочетанное использование данных веществ с ралтегравиром в рекомендованных дозах;
- атазанавир, саквинавир, тенофовир, индинавир (ингибиторы УДФГТ1А1): повышается плазменная концентрация ралтегравира в крови; комбинация последнего в дозе 1200 мг с атазанавиром не рекомендуется; изменения дозы Исентресса при комбинации с атазанавиром и/или тенофовиром не требуется;
- антациды, содержащие бивалентные ионы металлов (алюминий/магний): возможно уменьшение абсорбции ралтегравира посредством хелатирования, что обуславливает снижение плазменной концентрации препарата в крови; данные комбинации не рекомендуются;
- антациды, содержащие карбонат кальция: снижается содержание ралтегравира в плазме, однако взаимодействие не является клинически значимым; не рекомендуется с этими лекарственными средствами принимать Исентресс в дозе 1200 мг в сутки, при использовании в суточной дозе 800 мг коррекция не проводится;
- фамотидин, омепразол, циметидин, ранитидин (лекарственные средства, повышающие значение pH желудочного сока, блокаторы Н2-гистаминовых рецепторов): возрастает незначительно скорость абсорбции ралтегравира и, как следствие, уровень его концентрации в плазме крови; изменения дозы Исентресса не требуется.
Фармакокинетические характеристики ралтегравира отличаются значимой интер- и интраиндивидуальной вариабельностью. Приведенная информация о лекарственном взаимодействии с другими средствами основана на среднестатистических геометрических данных. Предусмотреть реакцию отдельного пациента точно нельзя.
Аналоги
Аналогами Исентресса являются Абакавир, Дарунавир, Атазанавир, Зиаген, Комбивир, Зидовудин, Кемерувир, Тенофовир, Невирапин, Эпивир и др.
Сроки и условия хранения
Таблетки Исентресс, покрытые пленочной оболочкой, надлежит хранить в месте недоступном детям, при температуре до 25 °С.
Срок годности – 2,5 года.
Таблетки жевательные Исентресс надлежит хранить с влагопоглощающим агентом в плотно укупоренной оригинальной упаковке, в сухом месте недоступном детям, при температуре до 30 °С.
Срок годности – 2 года.
Условия отпуска из аптек
Отпускается по рецепту.
Отзывы об Исентрессе
Согласно немногочисленным отзывам, Исентресс, по мнению пациентов и специалистов, является достаточно безопасным и действенным противовирусным препаратом, применяемым для лечения ВИЧ-1 инфекции в составе комбинированной терапии. Исентресс быстро снижает вирусную нагрузку и способствует повышению уровня иммунокомпетентных клеток СД-4.
К недостаткам средства относят низкий порог резистентности, развитие побочных эффектов и его высокую стоимость.
Цена на Исентресс в аптеках
Цена на Исентресс за 60 шт. в упаковке может составлять:
- таблетки жевательные (100 мг) – 9900 руб.;
- таблетки, покрытые пленочной оболочкой (400 мг) – 13 500 руб.
Информация о препарате является обобщенной, предоставляется в ознакомительных целях и не заменяет официальную инструкцию. Самолечение опасно для здоровья!
