Квадрапарин®-СОЛОфарм (Quadraparin-SOLOpharm) инструкция по применению
📜 Инструкция по применению Квадрапарин®-СОЛОфарм
💊 Состав препарата Квадрапарин®-СОЛОфарм
✅ Применение препарата Квадрапарин®-СОЛОфарм
📅 Условия хранения Квадрапарин®-СОЛОфарм
⏳ Срок годности Квадрапарин®-СОЛОфарм

Описание лекарственного препарата
Квадрапарин®-СОЛОфарм
(Quadraparin-SOLOpharm)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для электронного издания справочника Видаль 2023
года, дата обновления: 2022.12.01
Владелец регистрационного удостоверения:
Контакты для обращений:
ГРОТЕКС ООО
(Россия)
Код ATX:
B01AB05
(Эноксапарин)
Лекарственные формы
| Квадрапарин®-СОЛОфарм |
Р-р д/инъекц. 2000 анти-Ха МЕ/0.2 мл: шприцы 2, 4, 6, 10 или 20 шт. или амп. 5, 10, 15 или 20 шт. рег. №: ЛП-(000924)-(РГ-RU) |
|
|
Р-р д/инъекц. 3000 анти-Ха МЕ/0.3 мл: шприцы 2, 4, 6, 10 или 20 шт. или амп. 5, 10, 15 или 20 шт. рег. №: ЛП-(000924)-(РГ-RU) |
||
|
Р-р д/инъекц. 4000 анти-Ха МЕ/0.4 мл: шприцы 2, 4, 6, 10 или 20 шт. или амп. 5, 10, 15 или 20 шт. рег. №: ЛП-(000924)-(РГ-RU) |
||
|
Р-р д/инъекц. 5000 анти-Ха МЕ/0.5 мл: шприцы 2, 4, 6, 10 или 20 шт. или амп. 5, 10, 15 или 20 шт. рег. №: ЛП-(000924)-(РГ-RU) |
||
|
Р-р д/инъекц. 6000 анти-Ха МЕ/0.6 мл: шприцы 2, 4, 6, 10 или 20 шт. или амп. 5, 10, 15 или 20 шт. рег. №: ЛП-(000924)-(РГ-RU) |
||
|
Р-р д/инъекц. 7000 анти-Ха МЕ/0.7 мл: шприцы 2, 4, 6, 10 или 20 шт. или амп. 5, 10, 15 или 20 шт. рег. №: ЛП-(000924)-(РГ-RU) |
||
|
Р-р д/инъекц. 8000 анти-Ха МЕ/0.8 мл: шприцы 2, 4, 6, 10 или 20 шт. или амп. 5, 10, 15 или 20 шт. рег. №: ЛП-(000924)-(РГ-RU) |
||
|
Р-р д/инъекц. 10000 анти-Ха МЕ/1 мл: шприцы 2, 4, 6, 10 или 20 шт. или амп. 5, 10, 15 или 20 шт. рег. №: ЛП-(000924)-(РГ-RU) |
Форма выпуска, упаковка и состав
препарата Квадрапарин®-СОЛОфарм
Раствор для инъекций в виде прозрачной, бесцветной или желтоватой, или коричневато-желтоватой жидкости.
Вспомогательные вещества: вода д/и — до 0.2 мл.
0.2 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (1) — пачки картонные.
0.2 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (2) — пачки картонные.
0.2 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (3) — пачки картонные.
0.2 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (5) — пачки картонные.
0.2 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (10) — пачки картонные.
0.2 мл — ампулы стеклянные (5) — упаковки ячейковые контурные×× (1) — пачки картонные.
0.2 мл — ампулы стеклянные (5) — упаковки ячейковые контурные×× (2) — пачки картонные.
0.2 мл — ампулы стеклянные (5) — упаковки ячейковые контурные×× (3) — пачки картонные.
0.2 мл — ампулы стеклянные (5) — упаковки ячейковые контурные×× (4) — пачки картонные.
0.2 мл — ампулы стеклянные (10) — упаковки ячейковые контурные×× (1) — пачки картонные.
0.2 мл — ампулы стеклянные (10) — упаковки ячейковые контурные×× (2) — пачки картонные.
Раствор для инъекций в виде прозрачной, бесцветной или желтоватой, или коричневато-желтоватой жидкости.
Вспомогательные вещества: вода д/и — до 0.3 мл.
0.3 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (1) — пачки картонные.
0.3 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (2) — пачки картонные.
0.3 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (3) — пачки картонные.
0.3 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (5) — пачки картонные.
0.3 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (10) — пачки картонные.
0.3 мл — ампулы стеклянные (5) — упаковки ячейковые контурные×× (1) — пачки картонные.
0.3 мл — ампулы стеклянные (5) — упаковки ячейковые контурные×× (2) — пачки картонные.
0.3 мл — ампулы стеклянные (5) — упаковки ячейковые контурные×× (3) — пачки картонные.
0.3 мл — ампулы стеклянные (5) — упаковки ячейковые контурные×× (4) — пачки картонные.
0.3 мл — ампулы стеклянные (10) — упаковки ячейковые контурные×× (1) — пачки картонные.
0.3 мл — ампулы стеклянные (10) — упаковки ячейковые контурные×× (2) — пачки картонные.
Раствор для инъекций в виде прозрачной, бесцветной или желтоватой, или коричневато-желтоватой жидкости.
Вспомогательные вещества: вода д/и — до 0.4 мл.
0.4 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (1) — пачки картонные.
0.4 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (2) — пачки картонные.
0.4 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (3) — пачки картонные.
0.4 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (5) — пачки картонные.
0.4 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (10) — пачки картонные.
0.4 мл — ампулы стеклянные (5) — упаковки ячейковые контурные×× (1) — пачки картонные.
0.4 мл — ампулы стеклянные (5) — упаковки ячейковые контурные×× (2) — пачки картонные.
0.4 мл — ампулы стеклянные (5) — упаковки ячейковые контурные×× (3) — пачки картонные.
0.4 мл — ампулы стеклянные (5) — упаковки ячейковые контурные×× (4) — пачки картонные.
0.4 мл — ампулы стеклянные (10) — упаковки ячейковые контурные×× (1) — пачки картонные.
0.4 мл — ампулы стеклянные (10) — упаковки ячейковые контурные×× (2) — пачки картонные.
Раствор для инъекций в виде прозрачной, бесцветной или желтоватой, или коричневато-желтоватой жидкости.
Вспомогательные вещества: вода д/и — до 0.5 мл.
0.5 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (1) — пачки картонные.
0.5 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (2) — пачки картонные.
0.5 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (3) — пачки картонные.
0.5 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (5) — пачки картонные.
0.5 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (10) — пачки картонные.
0.5 мл — ампулы стеклянные (5) — упаковки ячейковые контурные×× (1) — пачки картонные.
0.5 мл — ампулы стеклянные (5) — упаковки ячейковые контурные×× (2) — пачки картонные.
0.5 мл — ампулы стеклянные (5) — упаковки ячейковые контурные×× (3) — пачки картонные.
0.5 мл — ампулы стеклянные (5) — упаковки ячейковые контурные×× (4) — пачки картонные.
0.5 мл — ампулы стеклянные (10) — упаковки ячейковые контурные×× (1) — пачки картонные.
0.5 мл — ампулы стеклянные (10) — упаковки ячейковые контурные×× (2) — пачки картонные.
Раствор для инъекций в виде прозрачной, бесцветной или желтоватой, или коричневато-желтоватой жидкости.
Вспомогательные вещества: вода д/и — до 0.6 мл.
0.6 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (1) — пачки картонные.
0.6 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (2) — пачки картонные.
0.6 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (3) — пачки картонные.
0.6 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (5) — пачки картонные.
0.6 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (10) — пачки картонные.
0.6 мл — ампулы стеклянные (5) — упаковки ячейковые контурные×× (1) — пачки картонные.
0.6 мл — ампулы стеклянные (5) — упаковки ячейковые контурные×× (2) — пачки картонные.
0.6 мл — ампулы стеклянные (5) — упаковки ячейковые контурные×× (3) — пачки картонные.
0.6 мл — ампулы стеклянные (5) — упаковки ячейковые контурные×× (4) — пачки картонные.
0.6 мл — ампулы стеклянные (10) — упаковки ячейковые контурные×× (1) — пачки картонные.
0.6 мл — ампулы стеклянные (10) — упаковки ячейковые контурные×× (2) — пачки картонные.
Раствор для инъекций в виде прозрачной, бесцветной или желтоватой, или коричневато-желтоватой жидкости.
Вспомогательные вещества: вода д/и — до 0.7 мл.
0.7 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (1) — пачки картонные.
0.7 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (2) — пачки картонные.
0.7 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (3) — пачки картонные.
0.7 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (5) — пачки картонные.
0.7 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (10) — пачки картонные.
0.7 мл — ампулы стеклянные (5) — упаковки ячейковые контурные×× (1) — пачки картонные.
0.7 мл — ампулы стеклянные (5) — упаковки ячейковые контурные×× (2) — пачки картонные.
0.7 мл — ампулы стеклянные (5) — упаковки ячейковые контурные×× (3) — пачки картонные.
0.7 мл — ампулы стеклянные (5) — упаковки ячейковые контурные×× (4) — пачки картонные.
0.7 мл — ампулы стеклянные (10) — упаковки ячейковые контурные×× (1) — пачки картонные.
0.7 мл — ампулы стеклянные (10) — упаковки ячейковые контурные×× (2) — пачки картонные.
Раствор для инъекций в виде прозрачной, бесцветной или желтоватой, или коричневато-желтоватой жидкости.
Вспомогательные вещества: вода д/и — до 0.8 мл.
0.8 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (1) — пачки картонные.
0.8 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (2) — пачки картонные.
0.8 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (3) — пачки картонные.
0.8 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (5) — пачки картонные.
0.8 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (10) — пачки картонные.
0.8 мл — ампулы стеклянные (5) — упаковки ячейковые контурные×× (1) — пачки картонные.
0.8 мл — ампулы стеклянные (5) — упаковки ячейковые контурные×× (2) — пачки картонные.
0.8 мл — ампулы стеклянные (5) — упаковки ячейковые контурные×× (3) — пачки картонные.
0.8 мл — ампулы стеклянные (5) — упаковки ячейковые контурные×× (4) — пачки картонные.
0.8 мл — ампулы стеклянные (10) — упаковки ячейковые контурные×× (1) — пачки картонные.
0.8 мл — ампулы стеклянные (10) — упаковки ячейковые контурные×× (2) — пачки картонные.
Раствор для инъекций в виде прозрачной, бесцветной или желтоватой, или коричневато-желтоватой жидкости.
Вспомогательные вещества: вода д/и — до 1 мл.
1 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (1) — пачки картонные.
1 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (2) — пачки картонные.
1 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (3) — пачки картонные.
1 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (5) — пачки картонные.
1 мл — шприцы стеклянные× (2) — упаковки ячейковые контурные (10) — пачки картонные.
1 мл — ампулы стеклянные (5) — упаковки ячейковые контурные×× (1) — пачки картонные.
1 мл — ампулы стеклянные (5) — упаковки ячейковые контурные×× (2) — пачки картонные.
1 мл — ампулы стеклянные (5) — упаковки ячейковые контурные×× (3) — пачки картонные.
1 мл — ампулы стеклянные (5) — упаковки ячейковые контурные×× (4) — пачки картонные.
1 мл — ампулы стеклянные (10) — упаковки ячейковые контурные×× (1) — пачки картонные.
1 мл — ампулы стеклянные (10) — упаковки ячейковые контурные×× (2) — пачки картонные.
× с устройствами предохранительными или защитными этикетками для игл, или без устройств предохранительных или защитных этикеток для игл;
×× со скарификатором ампульным или без него.
Фармакологическое действие
Эноксапарин натрия — низкомолекулярный гепарин со средней молекулярной массой около 4500 дальтон: менее 2000 дальтон — <20%, от 2000 до 8000 дальтон — >68%, более 8000 дальтон — <18%. Эноксапарин натрия получают с помощью щелочной деполимеризации бензилового эфира гепарина, выделенного из слизистой оболочки тонкой кишки свиньи. Его структура характеризуется невосстанавливающимся фрагментом 2-O-сульфо-4-енпиразиносуроновой кислоты и восстанавливающимся фрагментом 2-N,6-O-дисульфо-D-глюкопиранозида. Структура эноксапарина натрия содержит около 20% (в пределах от 15 до 25%) 1,6-ангидропроизводного в восстанавливающемся фрагменте полисахаридной цепи.
Фармакодинамика
В очищенной системе in vitro эноксапарин натрия обладает высокой анти-Ха активностью (примерно 100 МЕ/мл) и низкой анти-IIа или антитромбиновой активностью (примерно 28 МЕ/мл). Эта антикоагулянтная активность действует через антитромбин III (АТ-III), обеспечивая антикоагулянтную активность у людей. Кроме анти-Ха/IIа активности также выявлены дополнительные антикоагулянтные и противовоспалительные свойства эноксапарина натрия как у человека, так и на моделях животных. Это включает АТ-III зависимое ингибирование других факторов свертывания, таких как фактор VIIa, активацию высвобождения ингибитора пути тканевого фактора (ПТФ), а также снижение высвобождения фактора Виллебранда из эндотелия сосудов в кровоток. Эти факторы обеспечивают антикоагулянтный эффект эноксапарина натрия в целом.
Применение препарата в профилактических дозах незначительно изменяет активированное частичное тромбопластиновое время (АЧТВ), практически не оказывает воздействия на агрегацию тромбоцитов и на степень связывания фибриногена с рецепторами тромбоцитов.
Фармакокинетика
Всасывание
Абсолютная биодоступность эноксапарина натрия при п/к введении, оцениваемая на основании анти-Ха активности, близка к 100%.
Средняя максимальная анти-Ха активность плазмы наблюдается через 3-5 ч после п/к введения препарата и составляет приблизительно 0.2; 0.4; 1.0 и 1.3 анти-Ха МЕ/мл после п/к введения 20 мг, 40 мг, 1 мг/кг и 1.5 мг/кг.
В/в болюсное введение препарата в дозе 30 мг, сопровождающееся незамедлительным п/к введением препарата в дозировке 1 мг/кг каждые 12 ч, обеспечивает начальную максимальную анти-Ха активность на уровне 1.16 МЕ/мл (n=16), средняя экспозиция препарата в крови составляет приблизительно 88% от равновесного состояния, которое достигается на 2-й день терапии.
Фармакокинетика эноксапарина натрия в указанных режимах дозирования носит линейный характер. Вариабельность внутри и между группами пациентов низкая. После повторного подкожного введения 40 мг эноксапарина натрия 1 раз/сут и п/к введения эноксапарина натрия в дозе 1.5 мг/кг массы тела 1 раз/сут у здоровых добровольцев Css достигается ко 2-му дню, причем значения AUC в среднем на 15% выше, чем после однократного введения. После повторных п/к введений эноксапарина натрия в суточной дозе 1 мг/кг массы тела 2 раза/сут Css достигается через 3-4 дня, причем значения AUC в среднем на 65% выше, чем после однократного введения, и средние значения Cmax составляют соответственно 1.2 МЕ/мл и 0.52 МЕ/мл.
Анти-IIа активность в плазме примерно в 10 раз ниже, чем анти-Ха активность. Средняя максимальная анти-IIа активность наблюдается примерно через 3-4 ч после п/к введения и достигает 0.13 МЕ/мл и 0.19 МЕ/мл после повторного введения 1 мг/кг массы тела при двукратном введении и 1.5 мг/кг массы тела при однократном введении соответственно.
Распределение
Vd анти-Ха активности эноксапарина натрия составляет примерно 4.3 л и приближается к ОЦК.
Метаболизм и выведение
Эноксапарин натрия является препаратом с низким клиренсом. После в/в введения в течение 6 ч в дозе 1.5 мг/кг массы тела среднее значение клиренса анти-Ха в плазме составляет 0.74 л/ч.
Выведение препарата носит монофазный характер с Т1/2 около 5 ч (после однократного п/к введения) и около 7 ч (после многократного введения препарата).
Эноксапарин натрия в основном метаболизируется в печени путем десульфатирования и/или деполимеризации с образованием низкомолекулярных веществ с очень низкой биологической активностью. Выведение через почки активных фрагментов препарата составляет примерно 10% от введенной дозы, и общая экскреция активных и неактивных фрагментов составляет примерно 40% от введенной дозы.
Особые группы пациентов
Пациенты пожилого возраста (старше 75 лет): фармакокинетический профиль эноксапарина натрия не отличается у пациентов пожилого возраста и более молодых пациентов при нормальной функции почек. Однако в результате снижения функции почек с возрастом может наблюдаться замедление выведения эноксапарина натрия у пациентов пожилого возраста.
Нарушения функции печени: в исследовании с участием пациентов с поздними стадиями цирроза печени, получавших эноксапарин натрия в дозе 4000 МЕ (40 мг) 1 раз/сут, снижение максимальной анти-Ха активности было связано с увеличением степени тяжести нарушения функции печени (с оценкой по шкале Чайлд-Пью). Это снижение, главным образом, было обусловлено снижением уровня АТ-III, вторичным по отношению к снижению синтеза АТ-III у пациентов с нарушением функции печени.
Нарушение функции почек: отмечено уменьшение клиренса эноксапарина натрия у пациентов с нарушениями функции почек. После повторного п/к введения 40 мг эноксапарина натрия 1 раз/сут происходит увеличение активности анти-Ха, представленной AUC у пациентов с нарушениями функции почек легкой (КК ≥ 50 и < 80 мл/мин) и умеренной степени тяжести (КК ≥ 30 и < 50 мл/мин). У пациентов с тяжелым нарушением функции почек (КК < 30 мл/мин) значения AUC в равновесном состоянии в среднем на 65% выше при повторном п/к введении 40 мг препарата 1 раз/сут.
Гемодиализ: фармакокинетика эноксапарина натрия сопоставима с показателями в контрольной популяции после однократных в/в введений в дозах 25 МЕ, 50 МЕ или 100 МЕ/кг (0.25, 0.50 или 1.0 мг/кг), однако значения AUC были в 2 раза выше, чем в контрольной популяции.
Масса тела: после повторных п/к введений в дозе 1.5 мг/кг 1 раз/сут средние значения AUC анти-Ха активности в равновесном состоянии незначительно выше у пациентов с избыточной массой тела (ИМТ 30-48 кг/м2) по сравнению с пациентами с обычной средней массой тела, в то время как максимальная анти-Ха активность плазмы крови не увеличивается. У пациентов с избыточной массой тела при п/к введении препарата клиренс несколько меньше. Если не делать поправку дозы с учетом массы тела пациента, то после однократного п/к введения 40 мг эноксапарина натрия анти-Ха активность будет на 52% выше у женщин с массой тела менее 45 кг и на 27% выше у мужчин с массой тела менее 57 кг по сравнению с пациентами с обычной средней массой тела.
Показания препарата
Квадрапарин®-СОЛОфарм
- профилактика венозных тромбозов и эмболий при хирургических вмешательствах у пациентов умеренного и высокого риска, особенно при ортопедических и общехирургических вмешательствах, включая онкологические;
- профилактика венозных тромбозов и эмболий у пациентов, находящихся на постельном режиме вследствие острых терапевтических заболеваний, включая острую сердечную недостаточность и декомпенсацию хронической сердечной недостаточности (III или IV класс NYHA), дыхательную недостаточность, а также при тяжелых инфекциях и ревматических заболеваниях при повышенном риске венозного тромбообразования (см. раздел «Особые указания»);
- лечение тромбоза глубоких вен с тромбоэмболией легочной артерии или без тромбоэмболии легочной артерии, кроме случаев тромбоэмболии легочной артерии, требующих тромбоэмболической терапии или хирургического вмешательства;
- профилактика тромбообразования в системе экстракорпорального кровообращения во время гемодиализа;
- острый коронарный синдром:
- лечение нестабильной стенокардии и инфаркта миокарда без подъема сегмента ST в сочетании с пероральным приемом ацетилсалициловой кислоты;
- лечение острого инфаркта миокарда с подъемом сегмента ST у пациентов, подлежащих медикаментозному лечению или последующему чрескожному коронарному вмешательству (ЧКВ).
Режим дозирования
Препарат Квадрапарин®-СОЛОфарм применяется для лечения взрослых пациентов.
Подкожно, за исключением особых случаев (см. ниже подразделы «Профилактика тромбообразования в системе экстракорпорального кровообращения при проведении гемодиализа» и «Лечение острого инфаркта миокарда с подъемом сегмента ST, медикаментозное или с помощью чрескожного коронарного вмешательства»).
Профилактика венозных тромбозов и эмболии при хирургических вмешательствах у пациентов умеренного и высокого риска
Пациентам с умеренным риском развития тромбозов и эмболий (например, абдоминальные операции) рекомендуемая доза препарата составляет 20 мг 1 раз/сут п/к.
Первую инъекцию следует сделать за 2 ч до хирургического вмешательства.
Пациентам с высоким риском развития тромбозов и эмболий (например, при ортопедических операциях, хирургических операциях в онкологии, пациентам с дополнительными факторами риска, не связанными с операцией, такими как врожденная или приобретенная тромбофилия, злокачественное новообразование, постельный режим более 3 суток, ожирение, венозный тромбоз в анамнезе, варикозное расширение вен нижних конечностей, беременность) препарат рекомендуется в дозе 40 мг 1 раз/сут п/к, с введением первой дозы за 12 ч до хирургического вмешательства. При необходимости более ранней предоперационной профилактики (например, у пациентов с высоким риском развития тромбозов и тромбоэмболий, ожидающих отсроченную ортопедическую операцию) последняя инъекция должна быть сделана за 12 ч до операции и через 12 ч после операции.
Длительность лечения препаратом в среднем составляет 7-10 дней. При необходимости терапию можно продолжать до тех пор, пока сохраняется риск развития тромбоза и эмболии, и до тех пор, пока пациент не перейдет на амбулаторный режим.
При крупных ортопедических операциях может быть целесообразно после начальной терапии продолжение лечения путем введения препарата в дозе 40 мг 1 раз/сут в течение 5 недель.
Для пациентов с высоким риском венозных тромбоэмболий, перенесших хирургическое вмешательство, абдоминальную и тазовую хирургию по причине онкологического заболевания, может быть целесообразно увеличение продолжительности введения препарата в дозе 40 мг 1 раз/сут в течение четырех недель.
Профилактика венозных тромбозов и эмболий у пациентов, находящихся на постельном режиме вследствие острых терапевтических заболеваний
Рекомендуемая доза препарата составляет 40 мг 1 раз/сут, п/к, как минимум в течение 6-14 дней. Терапию следует продолжать до полного перехода пациента на амбулаторный режим (максимально в течение 14 дней).
Лечение тромбоза глубоких вен с тромбоэмболией легочной артерии или без тромбоэмболии легочной артерии
Препарат вводится п/к из расчета 1.5 мг/кг массы тела 1 раз/сут или 1 мг/кг массы тела 2 раза/сут. Режим дозирования должен выбираться врачом на основе оценки риска развития тромбоэмболии и риска развития кровотечений. У пациентов без тромбоэмболических осложнений и с низким риском развития венозной тромбоэмболии препарат рекомендуется вводить п/к из расчета 1.5 мг/кг массы тела 1 раз/сут. У всех других пациентов, включая пациентов с ожирением, симптоматической тромбоэмболией легочных артерий, раком, повторной венозной тромбоэмболией и проксимальным тромбозом (в подвздошной вене) препарат рекомендуется применять в дозе 1 мг/кг 2 раза/сут.
Длительность лечения в среднем составляет 10 дней. Следует сразу же начать терапию непрямыми антикоагулянтами, при этом лечение препаратом необходимо продолжать до достижения терапевтического антикоагулянтного эффекта (значения МНО должны составлять 2.0-3.0).
Профилактика тромбообразования в системе экстракорпорального кровообращения во время гемодиализа
Рекомендуемая доза препарата составляет в среднем 1 мг/кг массы тела. При высоком риске развития кровотечения дозу следует снизить до 0.5 мг/кг массы тела при двойном сосудистом доступе или до 0.75 мг при одинарном сосудистом доступе.
При гемодиализе эноксапарин натрия следует вводить в артериальный участок шунта в начале сеанса гемодиализа. Одной дозы, как правило, достаточно для 4-часового сеанса, однако при обнаружении фибриновых колец при более продолжительном гемодиализе можно дополнительно ввести препарат из расчета 0.5-1 мг/кг массы тела. Данные в отношении пациентов, применяющих эноксапарин натрия для профилактики или лечения и во время сеансов гемодиализа, отсутствуют.
Лечение нестабильной стенокардии и инфаркта миокарда без подъема сегмента ST
Препарат вводится из расчета 1 мг/кг массы тела каждые 12 ч, п/к, при одновременном применении антитромбоцитарной терапии. Средняя продолжительность терапии составляет, как минимум, 2 дня и продолжается до стабилизации клинического состояния пациента. Обычно введение препарата продолжается от 2 до 8 дней.
Ацетилсалициловая кислота рекомендуется всем пациентам, не имеющим противопоказаний, с начальной дозой 150-300 мг внутрь с последующей поддерживающей дозой 75-325 мг 1 раз/сут.
Лечение острого инфаркта миокарда с подъемом сегмента ST, медикаментозное или с помощью чрескожного коронарного вмешательства
Лечение начинают с однократного внутривенного болюсного введения эноксапарина натрия в дозе 30 мг. Сразу же после него п/к вводят эноксапарин натрия в дозе 1 мг/кг массы тела. Далее препарат назначают п/к по 1 мг/кг массы тела каждые 12 ч (максимально 100 мг эноксапарина натрия для каждой из первых двух п/к инъекций, затем — по 1 мг/кг массы тела для оставшихся подкожных доз, то есть при массе тела более 100 кг разовая доза не может превышать 100 мг). Как можно скорее после выявления острого инфаркта миокарда с подъемом сегмента ST пациентам необходимо назначить одновременно ацетилсалициловую кислоту и, если нет противопоказаний, прием ацетилсалициловой кислоты (в дозах 75-325 мг) следует продолжать ежедневно в течение не менее 30 дней.
Рекомендуемая продолжительность лечения препаратом составляет 8 дней или до выписки пациента из стационара (если период госпитализации составляет менее 8 дней).
При комбинации с тромболитиками (фибрин-специфическими и фибрин-неспецифическими) эноксапарин натрия следует вводить в интервале от 15 мин до начала тромболитической терапии и до 30 мин после нее.
У пациентов в возрасте 75 лет и старше не применяется начальное в/в болюсное введение. Препарат вводят п/к в дозе 0.75 мг/кг каждые 12 ч (максимально 75 мг эноксапарина натрия для каждой из первых двух п/к инъекций, затем — по 0.75 мг/кг массы тела для оставшихся п/к доз, то есть при массе тела более 100 кг разовая доза не может превышать 75 мг).
У пациентов, которым проводится чрескожное коронарное вмешательство, в случае, если последняя п/к инъекция эноксапарина натрия была проведена менее чем за 8 ч до раздувания введенного в место сужения коронарной артерии баллонного катетера дополнительного введения эноксапарина натрия не требуется. Если же последняя п/к инъекция эноксапарина натрия проводилась более чем за 8 ч до раздувания баллонного катетера, следует произвести дополнительное в/в болюсное введение эноксапарина натрия в дозе 0.3 мг/кг.
Особенности введения препарата
Предварительно заполненный одноразовый шприц готов к применению.
Препарат нельзя вводить внутримышечно!
Подкожное введение
Инъекции желательно проводить в положении пациента «лежа». При использовании предварительно заполненных шприцев во избежание потери препарата перед инъекцией не надо удалять пузырьки воздуха из шприца. Инъекции следует проводить поочередно в левую или правую переднелатеральную или заднелатеральную поверхность живота.
Иглу необходимо вводить на всю длину вертикально (не сбоку) в кожную складку, собранную и удерживаемую до завершения инъекции между большим и указательным пальцами. Складку кожи отпускают только после завершения инъекции.
Не следует массировать место инъекции после введения препарата.
Внутривенное болюсное введение
В/в болюсное введение эноксапарина натрия следует проводить через венозный катетер. Эноксапарин натрия не должен смешиваться или вводиться вместе с другими лекарственными препаратами. Для того, чтобы избежать присутствия в инфузионной системе следов других лекарственных препаратов и их взаимодействия с эноксапарином натрия, венозный катетер следует промывать достаточным количеством 0.9% раствора натрия хлорида или 5% раствора декстрозы до и после в/в болюсного введения эноксапарина натрия. Эноксапарин натрия можно безопасно вводить с 0.9% раствором натрия хлорида и 5% раствором декстрозы.
Для проведения болюсного введения 30 мг эноксапарина натрия при лечении острого инфаркта миокарда с подъемом сегмента ST из стеклянных шприцев большего объема удаляют лишнее количество препарата с тем, чтобы в них оставалось только 30 мг (0.3 мл).
Дозу 30 мг можно непосредственно вводить в/в.
Для проведения в/в болюсного введения эноксапарина натрия через венозный катетер могут использоваться предварительно заполненные шприцы для п/к введения препарата 30 мг, 40 мг, 50 мг, 60 мг, 70 мг, 80 мг и 100 мг. Рекомендуется использовать шприцы 30 мг, 40 мг, 50 мг и 60 мг, т.к. это уменьшает количество удаляемого из шприца препарата. Шприцы 20 мг не используются, т.к. в них недостаточно препарата для болюсного введения 30 мг эноксапарина натрия.
Для повышения точности дополнительного в/в болюсного введения малых объемов в венозный катетер при проведении чрескожных коронарных вмешательств рекомендуется развести препарат до концентрации 3 мг/мл. Разведение раствора рекомендуется проводить непосредственно перед введением.
Для получения раствора эноксапарина натрия с концентрацией 3 мг/мл с помощью предварительно заполненного шприца 60 мг рекомендуется использовать емкость с инфузионным раствором 50 мл (т.е. с 0.9% раствором натрия хлорида или 5% раствором декстрозы). Из емкости с инфузионным раствором с помощью обычного шприца извлекается и удаляется 30 мл раствора. Эноксапарин натрия (содержимое шприца для п/к введения 60 мг) вводится в оставшиеся в емкости 20 мл инфузионного раствора. Содержимое емкости с разведенным раствором эноксапарина натрия осторожно перемешивается. Для введения с помощью шприца извлекается необходимый объем разведенного раствора эноксапарина натрия, который рассчитывается по формуле:
Объемы, которые вводят внутривенно после разведения до концентрации 3 мг/мл
Переключение между эноксапарином натрия и пероральными антикоагулянтами
Переключение между эноксапарином натрия и антагонистами витамина К (АВК)
Для мониторирования эффекта АВК необходимо наблюдение врача и проведение лабораторных исследований [протромбиновое время, представленное как МНО].
Т.к. для развития максимального эффекта АВК требуется время, терапия эноксапарином натрия должна продолжаться в постоянной дозе так долго, как необходимо для поддержания значений МНО (по данным двух последовательных определений) в желаемом терапевтическом диапазоне в зависимости от показаний.
Для пациентов, которые получают АВК, отмена АВК и введение первой дозы эноксапарина натрия должны проводиться после того, как МНО снизилось ниже границы терапевтического диапазона.
Переключение между эноксапарином натрия и пероральными антикоагулянтами прямого действия (ПОАК)
Отмена эноксапарина натрия и назначение ПОАК должны проводиться за 0-2 ч до момента очередного запланированного введения эноксапарина натрия в соответствии с инструкцией по применению пероральных антикоагулянтов.
Для пациентов, получающих ПОАК, введение первой дозы эноксапарина натрия и отмена пероральных антикоагулянтов прямого действия должны проводиться в момент времени, соответствующий очередному запланированному применению ПОАК.
Применение при спинальной/эпидуральной анестезии или люмбальной пункции
В случае применения антикоагулянтной терапии во время проведения эпидуральной или спинальной анестезии/анальгезии или люмбальной пункции необходимо проведение неврологического мониторирования вследствие риска развития нейроаксиальных гематом (см. раздел «Особые указания»).
Применение эноксапарина натрия в профилактических дозах
Установка или удаление катетера должно проводиться спустя как минимум 12 ч после последней инъекции профилактической дозы эноксапарина натрия.
При использовании непрерывной техники необходимо соблюдать по меньшей мере 12 ч интервал до удаления катетера.
У пациентов с КК ≥15 и <30 мл/мин следует рассмотреть вопрос об удвоении времени до момента пункции или введения/удаления катетера как минимум до 24 ч.
Предоперационное введение эноксапарина натрия за 2 ч до вмешательства в дозе 20 мг несовместимо с проведением нейроаксиальной анестезии.
Применение эноксапарина натрия в терапевтических дозах
Установка или удаление катетера должно проводиться спустя как минимум через 24 ч после последней инъекции терапевтической дозы эноксапарина натрия (см. раздел «Противопоказания»).
При использовании непрерывной техники необходимо соблюдать по меньшей мере 24 ч интервал до удаления катетера.
У пациентов с КК ≥15 и <30 мл/мин следует рассмотреть вопрос об удвоении времени до момента пункции или введения/удаления катетера как минимум до 48 ч.
Пациентам, получающим эноксапарин натрия в дозах 0.75 мг/кг или 1 мг/кг массы тела 2 раза/сут, не следует вводить вторую дозу препарата с целью увеличения интервала перед установкой или заменой катетера. Точно так же следует рассмотреть вопрос о возможности отсрочки введения следующей дозы препарата как минимум на 4 ч, исходя из оценки соотношения польза/риск (риск развития тромбоза и кровотечений при проведении процедуры с учетом наличия у пациентов факторов риска). В эти временные точки все еще продолжает выявляться анти-Ха активность препарата, и отсрочки по времени не являются гарантией того, что развития нейроаксиальной гематомы удастся избежать.
Режим дозирования у особых групп пациентов
Дети до 18 лет
Безопасность и эффективность применения эноксапарина натрия у детей не установлены.
Пациенты пожилого возраста (старше 75 лет)
За исключением лечения инфаркта миокарда с подъемом сегмента ST для всех других показаний снижения доз эноксапарина натрия у пациентов пожилого возраста при отсутствии нарушений функции почек не требуется.
Пациенты с нарушениями функции почек
Применение эноксапарина натрия не рекомендуется пациентам с терминальной стадией хронической болезни почек (КК <15 мл/мин) ввиду отсутствия данных, кроме случаев профилактики тромбообразования в системе экстракорпорального кровообращения во время гемодиализа.
У пациентов с тяжелыми нарушениями функции почек (КК ≥15 и <30 мл/мин) доза эноксапарина натрия снижается в соответствии с представленными ниже таблицами, т.к. у этих пациентов отмечается увеличение системной экспозиции (продолжительности действия) препарата.
При применении препарата в терапевтических дозах рекомендуется следующая коррекция режима дозирования:
При применении препарата с профилактической целью рекомендуется коррекция режима дозирования, представленная в таблице ниже:
Рекомендованная коррекция режима дозирования не применяется при гемодиализе.
Нарушения функции почек легкой (КК ≥50 и <80 мл/мин) и умеренной (КК ≥30 и <50 мл/мин) степени тяжести. Коррекции дозы не требуется, однако пациенты должны находиться под тщательным наблюдением врача.
Пациенты с нарушениями функции печени
В связи с отсутствием клинических исследований препарат следует применять с осторожностью у пациентов с нарушениями функции печени.
Инструкция по самостоятельному выполнению инъекции эноксапарина натрия
- Вымойте руки и участок кожи (место для инъекции), в который Вы будете вводить препарат, водой с мылом. Высушите их.
- Примите удобное положение «сидя» или «лежа» и расслабьтесь. Убедитесь, что Вы хорошо видите место, в которое собираетесь вводить препарат. Оптимально использовать кресло для отдыха, шезлонг или кровать, обложенную подушками для опоры.
- Выберите место для проведения инъекции в правой или левой части живота. Это место должно находиться на расстоянии как минимум 5 см от пупка или вокруг имеющихся рубцов и кровоподтеков. Чередуйте места инъекций в правой и левой частях живота в зависимости от того, куда Вы вводили препарат в предыдущий раз.
- Протрите место для инъекции тампоном, смоченным спиртом.
- Осторожно снимите колпачок с иглы шприца с препаратом. Отложите колпачок. Шприц предварительно заполнен и готов к использованию. Не нажимайте на поршень для вытеснения пузырьков воздуха до введения иглы в место инъекции. Это может привести к потере препарата. После удаления колпачка не допускайте прикосновения иглы к каким-либо предметам. Это необходимо для сохранения стерильности иглы.
Внимание: при наличии защитной этикетки для иглы — следуйте Инструкции по использованию защитной этикетки для иглы, приведенной ниже.
- Удерживайте шприц в одной руке так, как Вы держите карандаш, а другой рукой осторожно сожмите протертое спиртом место для введения препарата между большим и указательным пальцами так, чтобы образовать складку кожи. Удерживайте кожную складку все время, пока Вы вводите препарат.
- Удерживайте шприц таким образом, чтобы игла была направлена вниз (вертикально под углом 90°). Введите иглу на всю длину в кожную складку.
- Нажмите пальцем на поршень. Это обеспечит введение препарата в подкожную жировую ткань живота. Удерживайте кожную складку все время, пока вы вводите препарат.
- Извлеките иглу, потянув ее назад без отклонения от оси. Теперь можно прекратить удержание кожной складки.
Внимание: при наличии устройства предохранительного — следуйте Инструкции по использованию устройства предохранительного, приведенной ниже.
- В целях предотвращения образования кровоподтека не растирайте место инъекции после введения препарата.
- Утилизируйте использованный одноразовый шприц в мусорный контейнер
При применении препарата строго придерживайтесь рекомендаций, представленных в данной инструкции, а также указаний врача или провизора. При возникновении вопросов обратитесь к врачу или провизору
Инструкция по использованию защитной этикетки для иглы (при ее наличии)
Не вскрывая упаковку, проверьте целостность шприца, а также отсутствие жидкости в контурной ячейковой упаковке. Если Вы сомневаетесь в целостности шприца или его герметичности, возьмите другую упаковку.
Откройте контурную ячейковую упаковку.
Проверьте содержание препарата в шприце.
1.
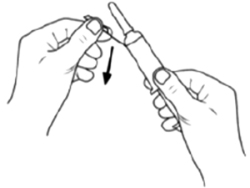
Внимание: не снимайте защитный колпачок до изгиба защитной этикетки!
Согните защитную этикетку для иглы в сторону приблизительно на 90°.
2.
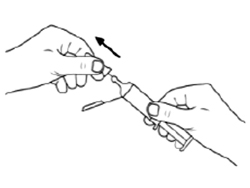
Снимите защитный колпачок.
3.
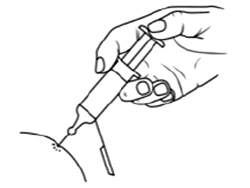
Сделайте инъекцию, как обычно.
4.
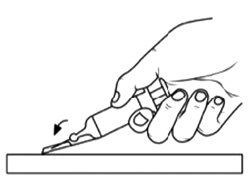
Внимание: не закрепляйте иглу в защитную этикетку пальцами!
Одной рукой закрепите иглу путем размещения защитной этикетки на жесткой устойчивой поверхности. Затем нажмите на защитную этикетку.
5.
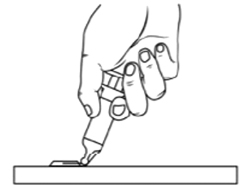
Согните защитную этикетку приблизительно на 90° до тех пор, пока игла со слышимым щелчком не окажется в пластиковой части защитной этикетки.
6.
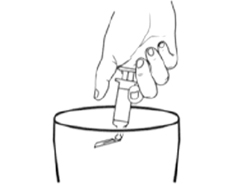
Утилизируйте одноразовый шприц с иглой в мусорный контейнер.
Инструкция по использованию устройства предохранительного
Внешний вид шприца перед применением
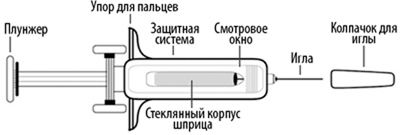
Внешний вид шприца после применения
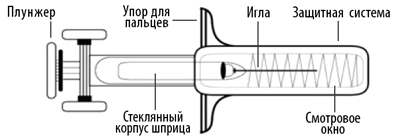
Не вскрывая упаковку, проверьте целостность шприца, а также отсутствие жидкости в контурной ячейковой упаковке. Если Вы сомневаетесь в целостности шприца или его герметичности, возьмите другую упаковку.
Откройте контурную ячейковую упаковку.
Проверьте содержание препарата в шприце.
1.
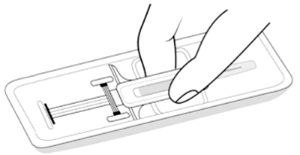
Внимание: вынимая шприц из упаковки, не тяните шприц за плунжер или колпачок для иглы. Выньте шприц из упаковки, как показано на рисунке.
2.
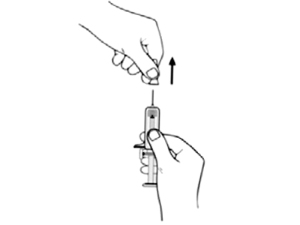
Внимание: не снимайте колпачок иглы, держась за плунжер или основание иглы.
Снимите колпачок иглы, как показано на рисунке, держась за защитную систему во избежание травмирования или изгиба иглы.
3.
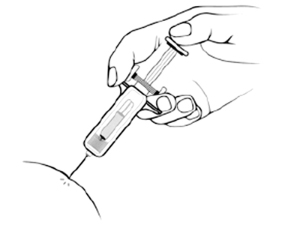
Сделайте инъекцию, как обычно.
4.
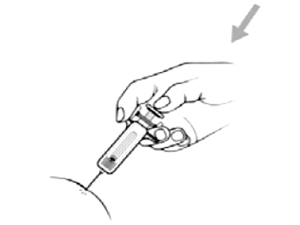
Зажав корпус шприца между указательным и средним пальцами, надавите на плунжер вниз до упора, чтобы ввести весь раствор.
Внимание: раствор должен быть введен полностью для срабатывания защитной системы.
5.
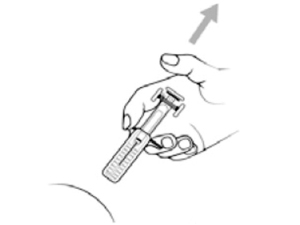
После завершения инъекции воспользуйтесь одним из предложенных вариантов:
1) Выньте иглу из места инъекции и отпустите плунжер. Дождитесь, пока защитная система полностью закроет иглу.
2) Не вынимая иглу из места инъекции, отпустите плунжер. Дождитесь, пока защитная система полностью закроет иглу.
Внимание: если защитная система не активировалась или активировалась частично — выбросите шприц с
незащищенной иглой. Т.к. игла не защищена, обратите особое внимание на то, чтобы избежать травм.
6.
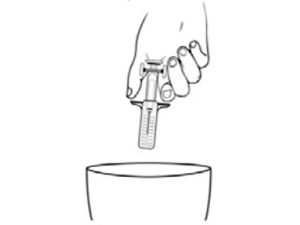
Выбросите шприц с защищенной иглой в мусорный контейнер.
Побочное действие
Изучение побочных эффектов эноксапарина натрия проводилось более чем у 15000 пациентов, участвовавших в клинических исследованиях, из них у 1776 пациентов — при профилактике венозных тромбозов и эмболий при общехирургических и ортопедических операциях; у 1169 пациентов — при профилактике венозных тромбозов и эмболий у пациентов, находящихся на постельном режиме вследствие острых терапевтических заболеваний; у 559 пациентов — при лечении тромбоза глубоких вен с тромбоэмболией легочной артерии или без тромбоэмболии легочной артерии; у 1578 пациентов — при лечении нестабильной стенокардии и инфаркта миокарда без зубца Q; у 10176 пациентов — при лечении инфаркта миокарда с подъемом сегмента ST.
Режим введения эноксапарина натрия отличался в зависимости от показаний. При профилактике венозных тромбозов и эмболий при общехирургических и ортопедических операциях или у пациентов, находящихся на постельном режиме, вводилось 40 мг п/к 1 раз/сут. При лечении тромбоза глубоких вен с тромбоэмболией легочной артерии или без нее, пациенты получали эноксапарин натрия из расчета 1 мг/кг массы тела п/к каждые 12 ч или 1.5 мг/кг массы тела п/к 1 раз/сут. При лечении нестабильной стенокардии и инфаркта миокарда без зубца Q доза эноксапарина натрия составляла 1 мг/кг массы тела п/к каждые 12 ч, а в случае инфаркта миокарда с подъемом сегмента ST проводилось в/в болюсное введение 30 мг с последующим введением 1 мг/кг массы тела п/к каждые 12 ч.
Частота возникновения нежелательных реакций определялась в соответствии с классификацией ВОЗ: очень часто (≥1/10); часто (≥1/100 и <1/10); нечасто (≥1/1000 и <1/100); редко (≥1/10000 и <1/1000); очень редко (<1/10000), частота неизвестна (не может быть подсчитана на основании имеющихся данных).
Нарушения со стороны сосудов
Кровотечения
В клинических исследованиях кровотечения были наиболее часто встречающимися нежелательными реакциями. К ним относились большие кровотечения, наблюдавшиеся у 4.2% пациентов (кровотечение считалось большим, если оно сопровождалось снижением содержания гемоглобина на 2 г/л и более, требовало переливания 2 или более доз компонентов крови, а также, если оно было забрюшинным или внутричерепным). Некоторые из этих случаев были летальными.
Как и при применении других антикоагулянтов при применении эноксапарина натрия возможно возникновение кровотечения, особенно при наличии факторов риска, способствующих развитию кровотечения, при проведении инвазивных процедур или применении препаратов, нарушающих гемостаз (см. разделы «Особые указания» и «Лекарственное взаимодействие»).
При описании кровотечений ниже знак «*» означает указание на следующие виды кровотечений: гематома, экхимозы (кроме развившихся в месте инъекции), раневые гематомы, гематурия, носовые кровотечения, желудочно-кишечные кровотечения.
Очень часто — кровотечения* при профилактике венозных тромбозов у хирургических пациентов и лечении тромбоза глубоких вен с тромбоэмболией или без нее; часто — кровотечения* при профилактике венозных тромбозов у пациентов, находящихся на постельном режиме, и при лечении нестабильной стенокардии, инфаркта миокарда без зубца Q и инфаркта миокарда с подъемом сегмента ST; нечасто — забрюшинные кровотечения и внутричерепные кровоизлияния у пациентов при лечении тромбоза глубоких вен с тромбоэмболией легочной артерии или без нее, а также при инфаркте миокарда с подъемом сегмента ST; редко — забрюшинные кровотечения при профилактике венозных тромбозов у хирургических пациентов и при лечении стенокардии, инфаркта миокарда без зубца Q.
Тромбоцитопения и тромбоцитоз
Очень часто — тромбоцитоз (количество тромбоцитов в периферической крови более 400 ×109/л) при профилактике венозных тромбозов у хирургических пациентов и лечении тромбоза глубоких вен с тромбоэмболией легочной артерии или без нее; часто — тромбоцитоз при лечении пациентов с острым инфарктом миокарда с подъемом сегмента ST, тромбоцитопения при профилактике венозных тромбозов у хирургических пациентов и лечении тромбоза глубоких вен с тромбоэмболией легочной артерии или без нее, а также при остром инфаркте миокарда с подъемом сегмента ST; нечасто — тромбоцитопения при профилактике венозных тромбозов у пациентов, находящихся на постельном режиме и при лечении нестабильной стенокардии, инфаркта миокарда без зубца Q; очень редко — аутоиммунная тромбоцитопения при лечении пациентов с острым инфарктом миокарда с подъемом сегмента ST.
Другие клинически значимые нежелательные реакции вне зависимости от показаний
Нежелательные реакции, представленные ниже, сгруппированы по системно-органным классам, даны с указанием определенной выше частоты их возникновения и в порядке уменьшения их тяжести.
Со стороны крови и лимфатической системы: часто — кровотечение, тромбоцитопения, тромбоцитоз; редко — случаи развития аутоиммунной тромбоцитопении с тромбозом; в некоторых случаях тромбоз осложнялся развитием инфаркта органов или ишемии конечностей (см. раздел «Особые указания», подраздел «Контроль количества тромбоцитов в периферической крови»).
Со стороны иммунной системы: часто — аллергические реакции.
Со стороны печени и желчевыводящих путей: очень часто — повышение активности печеночных ферментов, главным образом повышение активности трансаминаз, более чем в 3 раза превышающее ВГН.
Со стороны кожи и подкожных тканей: часто — крапивница, кожный зуд, эритема; нечасто — буллезный дерматит.
Общие расстройства и нарушения в месте введения: часто — гематома в месте инъекции, боль в месте инъекции, отек в месте инъекции, кровотечение, реакции повышенной чувствительности, воспаление, образование уплотнений в месте инъекции; нечасто — раздражение в месте инъекции, некроз кожи в месте инъекции.
Данные, полученные в пострегистрационный период
Следующие нежелательные реакции отмечались при постмаркетинговом применении препарата. Об этих побочных реакциях имелись спонтанные сообщения.
Со стороны иммунной системы: редко — анафилактические/анафилактоидные реакции, включая шок.
Со стороны нервной системы: часто — головная боль.
Со стороны сосудов: редко — при применении эноксапарина натрия на фоне спинальной/эпидуральной анестезии или спинальной пункции отмечались случаи развития спинальной гематомы (или нейроаксиальной гематомы). Эти реакции приводили к развитию неврологических нарушений различной степени тяжести, включая стойкий или необратимый паралич (см. раздел «Особые указания»»).
Со стороны крови и лимфатической системы: часто — геморрагическая анемия; редко — эозинофилия.
Со стороны кожи и подкожных тканей: редко — алопеция; в месте инъекции может развиться кожный васкулит, некроз кожи, которым обычно предшествует появление пурпуры или эритематозных папул (инфильтрированных и болезненных). В этих случаях терапию препаратом следует прекратить. Возможно образование твердых воспалительных узелков-инфильтратов в месте инъекции препарата, которые исчезают через несколько дней и не являются основанием для отмены препарата.
Со стороны печени и желчевыводящих путей: нечасто — гепатоцеллюлярное поражение печени; редко — холестатическое поражение печени.
Со стороны скелетно-мышечной системы и соединительной ткани: редко — остеопороз при длительной терапии (более 3 месяцев).
Лабораторные и инструментальные данные: редко — гиперкалиемия.
Противопоказания к применению
- повышенная чувствительность к эноксапарину натрия, гепарину или его производным, включая другие низкомолекулярные гепарины;
- активное клинически значимое кровотечение, а также состояния и заболевания, при которых имеется высокий риск развития кровотечения, включая недавно перенесенный геморрагический инсульт, острую язву ЖКТ, наличие злокачественного новообразования с высоким риском кровотечений, недавно перенесенные операции на головном и спинном мозге, офтальмологические операции, известное или предполагаемое наличие варикозного расширения вен пищевода, артериовенозные мальформации, сосудистые аневризмы, сосудистые аномалии спинного и головного мозга;
- спинальная или эпидуральная анестезия или локо-региональная анестезия, когда эноксапарин натрия применялся для лечения в предыдущие 24 ч;
- иммуноопосредованная гепарин-индуцированная тромбоцитопения (ГИТ) (в анамнезе) в течение 100 последних дней или наличие в крови циркулирующих антитромбоцитарных антител;
- детский возраст до 18 лет, т.к. эффективность и безопасность у данной категории пациентов не установлены (см. раздел «Особые указания»).
С осторожностью
Состояния, при которых имеется потенциальный риск развития кровотечения:
- нарушения гемостаза (в т.ч. гемофилия, тромбоцитопения, гипокоагуляция, болезнь Виллебранда), тяжелый васкулит;
- язвенная болезнь желудка или двенадцатиперстной кишки или другие эрозивно-язвенные поражения ЖКТ в анамнезе;
- недавно перенесенный ишемический инсульт;
- неконтролируемая тяжелая артериальная гипертензия;
- диабетическая или геморрагическая ретинопатия;
- тяжелый сахарный диабет;
- недавно перенесенная или предполагаемая неврологическая или офтальмологическая операция;
- проведение спинальной или эпидуральной анестезии (потенциальная опасность развития гематомы), спинномозговая пункция (недавно перенесенная);
- недавние роды;
- эндокардит бактериальный (острый или подострый);
- перикардит или перикардиальный выпот;
- почечная и/или печеночная недостаточность;
- внутриматочная контрацепция (ВМК);
- тяжелая травма (особенно ЦНС);
- открытые раны на больших поверхностях;
- одновременный прием препаратов, влияющих на систему гемостаза;
- гепарин-индуцированная тромбоцитопения без циркулирующих антител в анамнезе (более 100 дней).
Отсутствуют данные по клиническому применению эноксапарина натрия при следующих заболеваниях: активный туберкулез, лучевая терапия (недавно перенесенная).
Применение при беременности и кормлении грудью
Беременность
Сведений о том, что эноксапарин натрия проникает через плацентарный барьер во время беременности, нет. Т.к. отсутствуют адекватные и хорошо контролируемые исследования с участием беременных женщин, а исследования на животных не всегда прогнозируют реакцию на введение эноксапарина натрия во время беременности у человека, применять его во время беременности следует только в исключительных случаях, когда имеется настоятельная необходимость его применения, установленная врачом.
Рекомендуется проведение контроля за состоянием пациенток на предмет появления признаков кровотечения или чрезмерной антикоагуляции, пациентки должны быть предупреждены о риске возникновения кровотечений.
Нет данных о повышенном риске развития кровотечений, тромбоцитопении или остеопороза у беременных женщин, за исключением случаев, отмеченных у пациенток с искусственными клапанами сердца (см. раздел «Особые указания»).
При планировании эпидуральной анестезии рекомендуется перед ее проведением отменить эноксапарин натрия (см. раздел «Особые указания»).
Период грудного вскармливания
Неизвестно, экскретируется ли неизмененный эноксапарин натрия в грудное молоко. Всасывание эноксапарина натрия в ЖКТ у новорожденного маловероятно. Препарат может применяться в период грудного вскармливания.
Применение при нарушениях функции печени
В связи с отсутствием клинических исследований препарат следует применять с осторожностью у пациентов с нарушениями функции печени.
Применение при нарушениях функции почек
У пациентов с тяжелыми нарушениями функции почек (КК ≥15 и <30 мл/мин) требуется коррекция режима дозирования. При нарушении функции почек легкой (КК ≥50 и <80 мл/мин) и умеренной (КК ≥30 и <50 мл/мин) степени тяжести коррекции дозы не требуется, однако пациенты должны находиться под тщательным наблюдением врача.
Применение у детей
Противопоказание: детский возраст до 18 лет, т.к. эффективность и безопасность у данной категории пациентов не установлены
Применение у пожилых пациентов
За исключением лечения инфаркта миокарда с подъемом сегмента ST для всех других показаний снижения доз эноксапарина натрия у пациентов пожилого возраста при отсутствии нарушений функции почек не требуется.
Особые указания
Общие
Низкомолекулярные гепарины не являются взаимозаменяемыми, т.к. они различаются по процессу производства, молекулярной массе, специфической анти-Ха активности, единицам дозирования и режиму дозирования, с чем связаны различия в их фармакокинетике и биологической активности (антитромбиновая активность и взаимодействие с тромбоцитами). Поэтому требуется строго выполнять рекомендации по применению для каждого препарата, относящегося к классу низкомолекулярных гепаринов.
Кровотечение
Как и при применении других антикоагулянтов, при введении препарата возможно развитие кровотечений любой локализации (см. раздел «Побочное действие»). При развитии кровотечения необходимо найти его источник и назначить соответствующее лечение.
Эноксапарин натрия, как и другие антикоагулянты, следует применять с осторожностью при состояниях с повышенным риском кровотечения, таких как:
- нарушения гемостаза;
- язвенная болезнь в анамнезе;
- недавно перенесенный ишемический инсульт;
- тяжелая артериальная гипертензия;
- диабетическая ретинопатия;
- нейрохирургическое или офтальмологическое оперативное вмешательство;
- одновременное применение препаратов, влияющих на гемостаз (см. раздел «Лекарственное взаимодействие»).
Кровотечения у пациентов пожилого возраста
При применении препарата в профилактических дозах у пациентов пожилого возраста не отмечено увеличение риска развития кровотечений.
При применении препарата в терапевтических дозах у пациентов пожилого возраста (особенно в возрасте 80 лет и старше) существует повышенный риск развития кровотечений. Рекомендуется проведение тщательного наблюдения за состоянием таких пациентов (см. разделы «Фармакокинетика», «Режим дозирования», подраздел «Пациенты пожилого возраста»).
Одновременное применение других препаратов, влияющих на гемостаз
Применение препаратов, влияющих на гемостаз (салицилаты системного действия, в том числе ацетилсалициловая кислота в дозах, оказывающих противовоспалительное действие, НПВП, включая кеторолак, другие тромболитики (алтеплаза, ретеплаза, стрептокиназа. тенектеплаза, урокиназа)), рекомендуется отменить до начала лечения эноксапарином натрия за исключением случаев, когда их применение является необходимым. Если показаны комбинации эноксапарина натрия с этими препаратами, то следует проводить тщательное клиническое наблюдение и мониторинг соответствующих лабораторных показателей.
Почечная недостаточность
У пациентов с нарушением функции почек существует риск развития кровотечения в результате увеличения системной экспозиции эноксапарина натрия.
У пациентов с тяжелыми нарушениями функции почек (КК ≥15 и <30 мл/мин) отмечается значительное увеличение экспозиции эноксапарина натрия, поэтому рекомендуется проводить коррекцию дозы как при профилактическом, так и терапевтическом применении препарата. Хотя не требуется проводить коррекцию дозы у пациентов с легкими и умеренными нарушениями функции почек (КК 30-50 мл/мин или 50-80 мл/мин), рекомендуется проведение тщательного контроля состояния таких пациентов, и может рассматриваться проведение биологического мониторинга с измерением анти-Ха активности (см. разделы «Фармакокинетика» и «Режим дозирования», подраздел «Пациенты с нарушениями функции почек»). Применение эноксапарина натрия не рекомендуется пациентам с терминальной стадией хронической болезни ночек (КК <15 мл/мин) ввиду отсутствия данных, кроме случаев профилактики тромбообразования в системе экстракорпорального кровообращения во время гемодиализа.
Низкая масса тела
Отмечалось увеличение экспозиции эноксапарина натрия при его профилактическом применении у женщин с массой тела менее 45 кг и у мужчин с массой тела менее 57 кг, что может приводить к повышенному риску развития кровотечений. Рекомендуется проведение тщательного контроля состояния таких пациентов.
Пациенты с ожирением
Пациенты с ожирением имеют повышенный риск развития тромбозов и эмболий. Безопасность и эффективность применения эноксапарина натрия в профилактических дозах у пациентов с ожирением (ИМТ >30 кг/м2) до конца не определена и нет общего мнения по коррекции дозы. Этих пациентов следует внимательно наблюдать на предмет развития симптомов и признаков тромбозов и эмболий.
Контроль количества тромбоцитов в периферической крови
Риск развития антителоопосредованной гепарин-индуцированной тромбоцитопении существует и при применении низкомолекулярных гепаринов, при этом этот риск выше у пациентов, перенесших операции на сердце, и пациентов с онкологическими заболеваниями. Если развивается тромбоцитопения, то ее обычно выявляют между 5-м и 21-м днями после начала терапии эноксапарином натрия. В связи с этим рекомендуется регулярно контролировать количество тромбоцитов в периферической крови до начала лечения препаратом и во время его применения. Следует определять количество тромбоцитов в крови при наличии симптомов, указывающих на ГИТ (новый эпизод артериальных и/или венозных тромбоэмболических осложнений, болезненное поражение кожи в месте инъекции, аллергическая или анафилактическая реакция при лечении). При возникновении указанных симптомов следует проинформировать лечащего врача.
При наличии подтвержденного значительного снижения количества тромбоцитов (на 30-50% по сравнению с исходным показателем) необходимо немедленно отменить эноксапарин натрия и перевести пациента на другую антикоагулянтную терапию без применения гепаринов.
Спинальная/эпидуральная анестезия
Описаны случаи возникновения нейроаксиальных гематом при применении препарата при одновременном проведении спинальной/эпидуральной анестезии с развитием длительно существующего или необратимого паралича. Риск возникновения этих явлений снижается при применении препарата в дозе 40 мг или ниже. Риск повышается при применении более высоких доз препарата, а также при использовании постоянных катетеров после операции, или при одновременном применении дополнительных препаратов, влияющих на гемостаз, таких как НПВП (см. раздел «Лекарственное взаимодействие»). Риск также повышается при травматически проведенной или повторной спинномозговой пункции или у пациентов, имеющих в анамнезе указания на перенесенные операции в области позвоночника или деформацию позвоночника.
Для снижения возможного риска кровотечения, связанного с применением эноксапарина натрия и проведением эпидуральной или спинальной анестезии/анальгезии необходимо учитывать фармакокинетический профиль препарата (см. раздел «Фармакокинетика»). Установку или удаление катетера лучше проводить при низком антикоагулянтном эффекте эноксапарина натрия, однако точное время для достижения достаточного снижения антикоагулянтного эффекта у разных пациентов неизвестно. Следует дополнительно учитывать, что у пациентов с КК 15-30 мл/мин выведение эноксапарина натрия замедляется.
Если по назначению врача применяется антикоагулянтная терапия во время проведения эпидуральной/спинальной анестезии или люмбальной пункции, необходимо постоянное наблюдение за пациентом для выявления любых неврологических симптомов, таких как боли в спине, нарушение сенсорных и моторных функций (онемение или слабость в нижних конечностях), нарушение функции кишечника и/или мочевого пузыря. Пациента необходимо проинструктировать о необходимости немедленного информирования врача при возникновении вышеописанных симптомов. При подозрении на симптомы, характерные для гематомы спинного мозга, необходимы срочная диагностика и лечение, включая, при необходимости, декомпрессию спинного мозга.
Гепарин-индуцированная тромбоцитопения
Применение эноксапарина натрия у пациентов, имеющих в анамнезе указания на наличие гепарин-индуцированной тромбоцитопении в течение последних 100 дней или при наличии циркулирующих антител, противопоказано (см. раздел «Противопоказания»). Циркулирующие антитела могут персистировать несколько лет.
Эноксапарин натрия следует применять с особой осторожностью у пациентов, имеющих в анамнезе (более чем 100 дней) гепарин-индуцированную тромбоцитопению без циркулирующих антител. Решение о применении эноксапарина натрия в данной ситуации должно быть принято только после оценки соотношения польза/риск и при отсутствии безгепариновой (не содержащей гепарин) альтернативной терапии.
Чрескожная коронарная ангиопластика
С целью минимизации риска кровотечения, связанного с инвазивной сосудистой инструментальной манипуляцией при лечении нестабильной стенокардии и инфаркта миокарда без зубца Q и острого инфаркта миокарда с подъемом сегмента ST, эти процедуры следует проводить в интервалах между введением препарата. Это необходимо для того, чтобы достигнуть гемостаза в месте введения катетера после проведения чрескожного коронарного вмешательства. При использовании закрывающего устройства интродьюсер бедренной артерии может быть удален немедленно. При применении мануальной (ручной) компрессии интродьюсер бедренной артерии следует удалить через 6 ч после последней внутривенной или подкожной инъекции эноксапарина натрия. Если лечение эноксапарином натрия продолжается, то следующую дозу следует вводить не ранее, чем через 6-8 ч после удаления интродьюсера бедренной артерии. Необходимо следить за местом введения интродьюсера, чтобы своевременно выявить признаки кровотечения и образования гематомы.
Пациенты с механическими искусственными клапанами сердца
Применение препарата для профилактики тромбообразования у пациентов с механическими искусственными клапанами сердца изучено недостаточно. Имеются отдельные сообщения о развитии тромбоза клапанов сердца у пациентов с механическими искусственными клапанами сердца на фоне терапии эноксапарином натрия для профилактики тромбообразования. Ввиду недостаточности клинических данных и наличия неоднозначных факторов, включая основное заболевание, оценка таких сообщений затруднена.
Беременные женщины с механическими искусственными клапанами сердца
Применение препарата для профилактики тромбообразования у беременных женщин с механическими искусственными клапанами сердца изучено недостаточно. В клиническом исследовании беременных женщин с механическими искусственными клапанами сердца при применении эноксапарина натрия в дозе 1 мг/кг массы тела 2 раза/сут для уменьшения риска тромбозов и эмболий, у 2 из 8 женщин образовались тромбы, приведшие к блокированию клапанов сердца и к смерти матери и плода.
Имеются отдельные постмаркетинговые сообщения о тромбозе клапанов сердца у беременных женщин с механическими искусственными клапанами сердца, получавших лечение эноксапарином для профилактики тромбообразования.
Беременные женщины с механическими искусственными клапанами сердца имеют высокий риск развития тромбоза и эмболий.
Некроз кожи/кожный васкулит
Сообщалось о развитии некроза кожи и кожного васкулита при применении низкомолекулярных гепаринов. В случае развития некроза кожи/кожного васкулита применение препарата следует прекратить.
Острый инфекционный эндокардит
Применение гепарина не рекомендуется у пациентов с острым инфекционным эндокардитом вследствие риска развития геморрагического инсульта. В случае, если применение препарата считается абсолютно необходимым, решение следует принимать только после тщательной индивидуальной оценки соотношения пользы и риска.
Лабораторные тесты
В дозах, применяемых для профилактики тромбоэмболических осложнений, препарат существенно не влияет на время кровотечения и показатели свертывания крови, а также на агрегацию тромбоцитов или на связывание их с фибриногеном.
При повышении дозы может удлиняться АЧТВ и активированное время свертывания крови. Увеличение АЧТВ и активированного времени свертывания не находятся в прямой линейной зависимости от увеличения антикоагулянтной активности препарата, поэтому нет необходимости в их мониторинге.
Гиперкалиемия
Гепарины могут подавлять секрецию альдостерона надпочечниками, что приводит к развитию гиперкалиемии, особенно у пациентов с сахарным диабетом, хронической почечной недостаточностью, предшествующим метаболическим ацидозом, принимающих лекарственные препараты, повышающие содержание калия (см. раздел «Лекарственное взаимодействие»). Следует регулярно контролировать содержание калия в плазме крови, особенно у пациентов группы риска.
Профилактика венозных тромбозов и эмболий у пациентов с острыми терапевтическими заболеваниями, находящихся на постельном режиме
В случае развития острой инфекции, острых ревматических состояний профилактическое применение эноксапарина натрия оправдано только, если вышеперечисленные состояния сочетаются с одним из нижеперечисленных факторов риска венозного тромбообразования:
- возраст более 75 лет;
- злокачественные новообразования;
- тромбозы и эмболии в анамнезе;
- ожирение;
- гормональная терапия;
- сердечная недостаточность;
- хроническая дыхательная недостаточность.
Нарушение функции печени
Эноксапарин натрия следует с осторожностью применять у пациентов с нарушениями функции печени вследствие увеличения риска кровотечений. Коррекция дозы на основании мониторирования анти-Ха активности у пациентов с циррозом печени является ненадежной и не рекомендуется.
Натрий
Данный препарат содержит более 1 ммоль (23 мг) натрия на 150 мг эноксапарина натрия. Это необходимо учитывать пациентам, находящимся на диете с ограничением поступления натрия.
Влияние на способность к управлению транспортными средствами и механизмами
Эноксапарин натрия не оказывает влияния на способность управлять транспортными средствами и механизмами.
Передозировка
Симптомы: случайная передозировка препаратом при в/в, экстракорпоральном или п/к применении может привести к геморрагическим осложнениям. При приеме внутрь даже в больших дозах всасывание препарата маловероятно.
Лечение: антикоагулянтные эффекты можно в основном нейтрализовать путем медленного в/в введения протамина сульфата, доза которого зависит от дозы введенного препарата. Один мг (1 мг) протамина сульфата нейтрализует антикоагулянтный эффект одного мг (1 мг) препарата, если эноксапарин натрия вводился не более чем за 8 ч до введения протамина. 0.5 мг протамина нейтрализует антикоагулянтный эффект 1 мг препарата, если с момента введения последнего прошло более 8 ч или при необходимости введения второй дозы протамина. Если же после введения эноксапарина натрия прошло 12 ч и более, введения протамина не требуется. Однако даже при введении больших доз протамина сульфата, анти-Ха активность препарата полностью не нейтрализуется (максимально на 60%).
Лекарственное взаимодействие
Эноксапарин натрия нельзя смешивать с другими препаратами!
Нерекомендуемые комбинации
Препараты, влияющие на гемостаз (салицилаты системного действия, ацетилсалициловая кислота в дозах, оказывающих противовоспалительное действие, НПВП, включая кеторолак, другие тромболитики (алтеплаза, ретеплаза, стрептокиназа, тенектеплаза, урокиназа)), рекомендуется отменить до начала терапии эноксапарином натрия. При необходимости одновременного применения с эноксапарином натрия следует соблюдать осторожность и проводить тщательное клиническое наблюдение и мониторинг соответствующих лабораторных показателей.
Комбинации, требующие соблюдения осторожности
- Прочие лекарственные препараты, влияющие на гемостаз, такие как:
- ингибиторы агрегации тромбоцитов, включая ацетилсалициловую кислоту в дозах, оказывающих антиагрегантное действие (кардиопротекция), клопидогрел, тиклопидин и антагонисты гликопротеина IIb/IIIa рецепторов, показанные при остром коронарном синдроме, вследствие повышенного риска кровотечения;
- декстран с молекулярной массой 40 кДа; системные ГКС;
- системные ГКС.
- Лекарственные препараты, повышающие содержание калия.
При одновременном применении с лекарственными препаратами, повышающими содержание калия в сыворотке крови, следует проводить клинический и лабораторный контроль.
Условия хранения препарата Квадрапарин®-СОЛОфарм
Препарат следует хранить в недоступном для детей месте при температуре не выше 25°С.
Срок годности препарата Квадрапарин®-СОЛОфарм
Срок годности — 3 года.
Не применять после окончания срока годности.
Условия реализации
Отпускают по рецепту.
Контакты для обращений
ГРОТЕКС ООО
(Россия)

|
|
195279 Санкт-Петербург, Индустриальный пр-т, |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Обобщенные научные материалы по действующему веществу препарата Квадрапарин®-СОЛОфарм (раствор для инъекций, 10000 анти-Ха МЕ/мл)
Дата последней актуализации: 02.03.2021
Особые отметки:
Содержание
- Действующее вещество
- ATX
- Владелец РУ
- Условия хранения
- Срок годности
- Источники информации
- Фармакологическая группа
- Предупреждения
- Характеристика
- Фармакология
- Показания к применению
- Нозологическая классификация (МКБ-10)
- Противопоказания
- Применение при беременности и кормлении грудью
- Побочные действия
- Взаимодействие
- Передозировка
- Способ применения и дозы
- Меры предосторожности
- Заказ в аптеках Москвы
Действующее вещество
ATX
Владелец РУ
Гротекс ООО
Условия хранения
При температуре не выше 25 °C.
Хранить в недоступном для детей месте.
Срок годности
3 года.
Не применять по истечении срока годности, указанного на упаковке.
Источники информации
www.fda.gov и www.rxlist.com, 2021.
Фармакологическая группа
Предупреждения
Эпидуральные/спинальные гематомы
У пациентов, получающих низкомолекулярные гепарины или гепариноиды, при проведении нейроаксиальной анестезии или или спинномозговой пункции могут возникать эпидуральные или спинальные гематомы, которые могут привести к длительному или постоянному параличу. Необходимо учитывайть эти риски при назначении пациенту процедур на позвоночнике. Факторы, которые могут увеличить риск развития эпидуральной или спинальной гематомы, включают: использование постоянных эпидуральных катетеров; одновременное применение других ЛС, влияющих на гемостаз, таких как НПВП, антиагреганты и другие антикоагулянты; травматические или повторные эпидуральные или спинномозговые пункции в анамнезе; деформации позвоночника или операции на позвоночнике в анамнезе.
Оптимальное время между введением эноксапарина натрия и нейроаксиальными процедурами неизвестно.
Необходимо проводить частый мониторинг для выявления любых признаков и симптомов неврологических нарушений. При подозрении на неврологическое расстройство необходимо срочно провести диагностику и лечение.
Необходима тщательная оценка соотношения польза-риск перед нейроаксиальным вмешательством у пациентов, получающих антикоагулянт, или назначением антикоагулянта для тромбопрофилактики (см. Меры предосторожности).
Характеристика
Низкомолекулярный гепарин со средней молекулярной массой около 4500 Да. Эноксапарин натрия получают щелочной деполимеризацией бензилового эфира гепарина, полученного из слизистой оболочки кишечника свиней.
Фармакология
Фармакодинамика
У людей эноксапарин, вводимый п/к в дозе 1,5 мг/кг, характеризуется более высоким соотношением анти-Ха- к анти-IIa-активности (среднее значение ± стандартное отклонение, 14±3,1) (расчет по площади под кривой антифакторная активность-время) по сравнению с гепарином (среднее значение ± стандартное отклонение, 1,22±0,13). Повышение до 1,8 раза по сравнению с контрольными значениями наблюдалось для тромбинового времени и АЧТВ. Применение эноксапарина натрия в дозе 1 мг/кг (концентрация 100 мг/мл) п/к каждые 12 ч у пациентов в одном крупном клиническом исследовании привело к достижению значения АЧТВ 45 с или меньше у большинства пациентов (n=1607). В/в болюсное введение 30 мг эноксапарина натрия, сразу за которым следовало п/к введение в дозе 1 мг/кг, приводило к удлинению АЧТВ до 50 с после инъекции. Среднее удлинение АЧТВ в 1-й день было примерно на 16% больше, чем на 4-й день.
Фармакокинетика
Абсорбция
Изучение фармакокинетики эноксапарина натрия проводилось с использованием концентрации 100 мг/мл. Максимальная активность в отношении антифактора Ха и антитромбина (антифактор IIa) наблюдается через 3–5 ч после п/к инъекции эноксапарина натрия. Средняя максимальная анти-Ха-активность составляла 0,16 МЕ/мл (1,58 мкг/мл) и 0,38 МЕ/мл (3,83 мкг/мл) после п/к введения в дозе 20 и 40 мг соответственно. Средняя (n=46) максимальная анти-Ха-активность составляла 1,1 МЕ/мл в состоянии равновесия у пациентов с нестабильной стенокардией, получавших эноксапарин натрия 1 мг/кг п/к каждые 12 ч в течение 14 дней. Средняя абсолютная биодоступность эноксапарина натрия после п/к введения в дозе 1,5 мг/кг, оцененная на основе анти-Ха-активности, составляет приблизительно 100% у здоровых субъектов.
В/в болюсное введение эноксапарина натрия в дозе 30 мг с последующим немедленным п/к введением в дозе 1 мг/кг каждые 12 ч обеспечивало начальный максимальный уровень анти-Ха-активности 1,16 МЕ/мл (n=16) и среднюю экспозицию, соответствующую 84% от равновесного состояния. Равновесное состояние достигается на 2-й день лечения.
Фармакокинетика эноксапарина натрия близка к линейной в рекомендуемом диапазоне доз. После многократного п/к введения эноксапарина натрия в дозе 40 мг 1 раз в день и 1,5 мг/кг 1 раз в день у здоровых добровольцев равновесное состояние достигается на 2-й день со средней экспозицией примерно на 15% выше, чем после однократной дозы. Уровни активности эноксапарина в состоянии равновесия хорошо предсказываются по фармакокинетике однократной дозы. После многократного п/к введения в дозе 1 мг/кг 2 раза в день равновесное состояние достигается с 4-го дня со средней экспозицией примерно на 65% выше, чем после однократной дозы, и средними максимальными и минимальными уровнями активности примерно 1,2 и 0,52 МЕ/мл соответственно. Основываясь на фармакокинетике эноксапарина натрия, это различие в равновесном состоянии является ожидаемым и находится в пределах терапевтического диапазона.
Хотя клинические исследования не проводились, предполагается, что концентрация эноксапарина натрия 150 мг/мл приведет к антикоагулянтной активности, аналогичной наблюдаемой при концентрациях 100 и 200 мг/мл при той же дозе. При ежедневной п/к инъекции эноксапарина натрия в дозе 1,5 мг/кг 25 здоровым пациентам мужского и женского пола с использованием концентрации 100 или 200 мг/мл были получены следующие фармакокинетические профили (см. табл. 1).
Таблица 1
Фармакокинетические параметры1 через 5 дней п/к введения эноксапарина натрия в дозе 1,5 мг/кг 1 раз в день с использованием концентраций 100 или 200 мг/мл
| Параметр | Концентрация | Анти-Ха | Анти-IIa | Heptest | АЧТВ |
| Максимальная активность (МЕ/мл или Δ, с) | 100 мг/мл | 1,37 (±0,23) | 0,23 (±0,05) | 105 (±17) | 19 (±5) |
| 200 мг/мл | 1,45 (±0,22) | 0,26 (±0,05) | 111 (±17) | 22 (±7) | |
| 90% ДИ | 102–110% | 102–111% | |||
| Tmax2, ч | 100 мг/мл | 3 (2–6) | 4 (2–5) | 2,5 (2–4,5) | 3 (2–4,5) |
| 200 мг/мл | 3,5 (2–6) | 4,5 (2,5–6) | 3,3 (2–5) | 3 (2–5) | |
| AUCss, ч1·МЕ/мл или ч1·Δ, с | 100 мг/мл | 14,26 (±2,93) | 1,54 (±0,61) | 1321 (±219) | |
| 200 мг/мл | 15,43 (±2,96) | 1,77 (±0,67) | 1401 (±227) | ||
| 90% ДИ | 105–112% | 103–109% |
1 Среднее значение ± стандартное отклонение на 5-й день и 90% ДИ отношения.
2 Медиана (диапазон).
Распределение
Vd анти-Ха-активности составляет около 4,3 л.
Элиминация
После в/в введения общий клиренс эноксапарина натрия составляет 26 мл/мин. После в/в введения эноксапарина, меченного гамма-излучателем, 99mTc, 40% радиоактивности и от 8 до 20% анти-Ха-активности обнаруживались в моче через 24 ч. T1/2, на основании анти-Ха-активности, составлял от 4,5 ч после однократного п/к введения до примерно 7 ч после повторного введения. Значительная анти-Ха-активность сохраняется в плазме крови в течение примерно 12 ч после введения 40 мг п/к 1 раз в день. После п/к введения кажущийся клиренс (CL/F) эноксапарина натрия составляет примерно 15 мл/мин.
Метаболизм
Эноксапарин натрия в основном метаболизируется в печени путем десульфатирования и/или деполимеризации с образованием веществ с более низкой молекулярной массой и значительно сниженной биологической активностью. Почечный клиренс активных фрагментов составляет около 10% от введенной дозы, а общая почечная экскреция активных и неактивных фрагментов — 40% от дозы.
Особые группы пациентов
Пол. Кажущийся клиренс и максимальная активность, полученные на основе значений уровня антифактора Ха после однократного п/к введения (40 и 60 мг), были немного выше у мужчин, чем у женщин. Источник гендерных различий по этим параметрам окончательно не определен, однако таким фактором может быть масса тела.
Пожилой возраст. Кажущийся клиренс и максимальная активность, полученные на основе значений уровня антифактора Ха после однократного или многократного п/к введения у пожилых пациентов, были близки к таковым у молодых субъектов. После п/к введения 40 мг эноксапарина натрия 1 раз в день средняя AUC анти-Xa-активности на 10-й день была примерно на 15% больше, чем в 1-й день.
Почечная недостаточность. Наблюдалась линейная зависимость между клиренсом антифактора Ха из плазмы и Cl креатинина в равновесном состоянии, что указывает на уменьшение клиренса эноксапарина натрия у пациентов со сниженной функцией почек. Экспозиция антифактора Xa, представленная AUC, в равновесном состоянии незначительно увеличивается у пациентов с нарушением функции почек, имеющих Cl креатинина от 50 до 80 мл/мин и от 30 до <50 мл/мин, после повторных п/к введений в дозе 40 мг 1 раз в день. У пациентов с тяжелой почечной недостаточностью (Cl креатинина <30 мл/мин) AUC в равновесном состоянии значительно увеличивается, в среднем на 65%, после повторных п/к введений в дозе 40 мг 1 раз в день.
Гемодиализ. В одном исследовании скорость выведения была аналогичной, но AUC была в два раза выше, чем в контрольной популяции, после однократного в/в введения 0,25 или 0,5 мг/кг.
Печеночная недостаточность. Исследования эноксапарина натрия у пациентов с нарушением функции печени не проводились, и влияние нарушения функции печени на его воздействие неизвестно.
Масса тела. После многократного п/к введения в дозе 1,5 мг/кг 1 раз в сутки средняя AUC анти-Ха-активности незначительно выше в равновесном состоянии у здоровых добровольцев с ожирением (ИМТ 30–48 кг/м2) по сравнению с группой без ожирения, в то время как максимальная активность не увеличивается. При введении дозы без корректировки на массу тела было обнаружено, что после однократного п/к введения дозы 40 мг, экспозиция антифактора Ха выше на 52% у женщин с низким весом (<45 кг) и на 27% у мужчин с низким весом (<57 кг) по сравнению с пациентами с нормальной массой тела.
ФКВ
Не наблюдалось ФКВ эноксапарина натрия и других тромболитиков при одновременном применении.
Канцерогенность, мутагенность, влияние на фертильность
Долгосрочные исследования на животных для оценки канцерогенного потенциала эноксапарина натрия не проводились. Эноксапарин натрия не оказывал мутагенного действия в тестах in vitro, включая тест Эймса, тест на клетках лимфомы мышей, тест хромосомных аберраций в лимфоцитах крови человека и тест хромосомных аберраций в клетках костного мозга у крыс in vivo. Не обнаружено влияния эноксапарина натрия на фертильность или репродуктивную способность самцов и самок крыс при п/к введении в дозах до 20 мг/кг/сут или 141 мг/м2/сут. Максимальная доза для человека в клинических испытаниях составляла 2 мг/кг/сут или 78 мг/м2/сут (при средней массе тела 70 кг, росте 170 см и площади поверхности тела 1,8 м2).
Клинические исследования
Профилактика ТГВ после абдоминальной хирургии у пациентов с факторами риска развития тромбоэмболических осложнений
В абдоминальной хирургии в группу риска включают тех пациентов, кому старше 40 лет, кто страдает ожирением, подвергается операции под общей анестезией продолжительностью более 30 мин или имеет дополнительные факторы риска, такие как злокачественные новообразования, ТГВ в анамнезе или легочная эмболия.
В двойное слепое исследование с параллельными группами было вовлечено 1116 пациентов, перенесших плановую операцию по поводу рака ЖКТ или урогенитального тракта, и 1115 пациентов получили лечение. Возраст пациентов составлял от 32 до 97 лет (средний возраст 67 лет), 52,7% пациентов были мужчины и 47,3% — женщины. Среди пациентов 98% принадлежали к европеоидной расе, 1,1% были афроамериканцами, 0,4% — представителями монголоидной расы и 0,4% — других этнических групп. Эноксапарин натрия в дозе 40 мг, вводимый п/к 1 раз в день за 2 ч до операции и в течение максимум 12 дней после операции, сравнивался по снижению риска развития ТГВ с гепарином в дозе 5000 ЕД, вводимым каждые 8 ч п/к. Данные об эффективности представлены в таблице 2.
Таблица 2
Эффективность эноксапарина натрия в профилактике ТГВ после абдоминальной хирургии
| Показатель | Число пациентов, n (%) | |
| Эноксапарин натрия, 40 мг ежедневно, п/к | Гепарин, 5000 Ед, каждые 8 ч, п/к | |
| Всего пациентов, получавших профилактику | 555 (100) | 560 (100) |
| Всего венозных тромбоэмболических событий1 | 56 (10,1), 95% ДИ: 8–13 | 63 (11,3), 95% ДИ: 9–14 |
| Только ТГВ | 54 (9,7), 95% ДИ: 7–12 | 61 (10,9), 95% ДИ: 8–13 |
1 Венозные тромбоэмболические события включали ТГВ, легочную эмболию и смертельный исход по причине тромбоэмболического события.
Во втором двойном слепом исследовании с параллельными группами эноксапарин натрия в дозе 40 мг п/к 1 раз в день сравнивали с гепарином в дозе 5000 ЕД п/к каждые 8 ч у пациентов, перенесших колоректальную операцию (одна треть по поводу рака). В исследование были рандомизированы 1347 пациентов, все пациенты прошли лечение. Возраст пациентов составлял от 18 до 92 лет (средний возраст 50,1 года), из них 54,2% были мужчины и 45,8% — женщины. Лечение было начато примерно за 2 ч до операции и продолжалось примерно от 7 до 10 дней после операции. Данные об эффективности представлены в таблице 3.
Таблица 3
Эффективность эноксапарина натрия в профилактике ТГВ после колоректальной хирургии
| Показатель | Число пациентов, n (%) | |
| Эноксапарин натрия, 40 мг ежедневно, п/к | Гепарин, 5000 Ед, каждые 8 ч, п/к | |
| Всего пациентов, получавших профилактику | 673 (100) | 674 (100) |
| Всего венозных тромбоэмболических событий1 | 48 (7,1), 95% ДИ: 3–9 | 45 (6,7), 95% ДИ: 5–9 |
| Только ТГВ | 47 (7), 95% ДИ: 5–9 | 44 (6,5), 95% ДИ: 5–8 |
1 Венозные тромбоэмболические события включали ТГВ, легочную эмболию и смертельный исход по причине тромбоэмболического события.
Профилактика ТГВ после операции по замене тазобедренного или коленного сустава
Было показано, что эноксапарин натрия снижает риск развития послеоперационного ТГВ после операции по замене тазобедренного или коленного сустава. В двойном слепом исследовании сравнивали эноксапарин натрия (30 мг каждые 12 ч п/к) с плацебо у пациентов с заменой тазобедренного сустава. В исследование были рандомизированы 100 пациентов, все пациенты прошли лечение. Возраст пациентов варьировался от 41 до 84 лет (средний возраст 67,1 года), из них 45% были мужчины и 55% — женщины. После установления гемостаза лечение было начато через 12–24 ч после операции и продолжалось в течение 10–14 дней. Данные об эффективности представлены в таблице 4.
Таблица 4
Эффективность эноксапарина натрия в профилактике ТГВ после операции по замене тазобедренного сустава в сравнении с плацебо
| Показатель | Число пациентов, n (%) | |
| Эноксапарин натрия, 30 мг кажждые 12 ч, п/к | Плацебо, каждые 12 ч, п/к | |
| Всего пациентов после операции по замене тазобедренного сустава | 50 (100) | 50 (100) |
| Всего ТГВ | 5 (10)1 | 23 (46) |
| Проксимальный ТГВ | 1 (2)2 | 11 (22) |
1 p=0,0002 по сравнению с плацебо.
2 p=0,0134 по сравнению с плацебо.
В двойном слепом многоцентровом исследовании сравнивали три режима дозирования эноксапарина натрия у пациентов с заменой тазобедренного сустава. В исследование были рандомизированы 572 пациента, 568 пациентов прошли лечение. Возраст пациентов составлял от 31 до 88 лет (средний возраст 64,7 года), из них 63% были мужчины и 37% — женщины. Среди пациентов 93% принадлежали к европеоидной расе, 6% были афроамериканцами, менее 1% — представителями монголоидной расы и 1% — других этнических групп. Лечение было начато в течение двух дней после операции и продолжалось от 7 до 11 дней. Данные об эффективности представлены в таблице 5.
Таблица 5
Эффективность эноксапарина натрия в профилактике ТГВ после операции по замене тазобедренного сустава при разных режимах дозирования
| Показатель | Число пациентов, n (%) | ||
| Эноксапарин натрия, 10 мг ежедневно, п/к | Эноксапарин натрия, 30 мг кажждые 12 ч, п/к | Эноксапарин натрия, 40 мг ежедневно, п/к | |
| Всего пациентов, получавших профилактику | 161 (100) | 208 (100) | 199 (100) |
| Всего ТГВ | 40 (25) | 22 (11)1 | 27 (14) |
| Проксимальный ТГВ | 17 (11) | 8 (4)2 | 9 (5) |
1 p=0,0008 по сравнению с эноксапарином натрия в дозе 10 мг 1 раз в день.
2 p=0,0168 по сравнению с эноксапарином натрия в дозе 10 мг 1 раз в день.
Не наблюдалось значительных различий между режимами дозирования 30 мг каждые 12 ч и 40 мг 1 раз в день.
В двойном слепом исследовании у пациентов, перенесших операцию по замене коленного сустава, сравнивали применение эноксапарина натрия (п/к в дозе 30 мг каждые 12 ч) с плацебо. Всего 132 пациента были рандомизированы в исследование, 131 пациент прошел лечение, из которых 99 перенесли полную замену коленного сустава, а 32 — либо замену коленного сустава, либо остеотомию большеберцовой кости. 99 пациентов с тотальной заменой коленного сустава были в возрасте от 42 до 85 лет (средний возраст 70,2 года), из них 36,4% были мужчины и 63,6% — женщины. После установления гемостаза лечение было начато через 12–24 ч после операции и продолжалось до 15 дней. Частота случаев развития ТГВ, в т.ч. проксимального, была значительно ниже при применении эноксапарина натрия по сравнению с плацебо (табл. 6).
Таблица 6
Эффективность эноксапарина натрия в профилактике ТГВ после операции по замене коленного сустава
| Показатель | Число пациентов, n (%) | |
| Эноксапарин натрия, 30 мг кажждые 12 ч, п/к | Плацебо, каждые 12 ч, п/к | |
| Всего пациентов после операции по замене коленного сустава | 47 (100) | 52 (100) |
| Всего ТГВ | 5 (11)1, 95% ДИ: 1–21 | 23 (46), 95% ДИ: 47–76 |
| Проксимальный ТГВ | 0 (0)2, 95% выше предела достоверности: 5 | 11 (22), 95% ДИ: 3–24 |
1 p=0,0001 по сравнению с плацебо.
2 p=0,013 по сравнению с плацебо.
Кроме того, в открытом рандомизированном клиническом исследовании с параллельными группами эноксапарин натрия, вводимый п/к в дозе 30 мг каждые 12 ч у пациентов, перенесших операцию по замене коленного сустава, сравнивали с гепарином 5000 ЕД каждые 8 ч, п/к. В исследование были рандомизированы 453 пациента, все они прошли лечение. Возраст пациентов составлял от 38 до 90 лет (средний возраст 68,5 года), из них 43,7% были мужчин и 56,3% — женщины. Среди них 92,5% принадлежали к европеоидной расе, 5,3% были афроамериканцами и 0,6% — представителями других этнических групп. Лечение начиналось после операции и продолжалось до 14 дней. Частота развития ТГВ при применении эноксапарина натрия была ниже, чем при введении гепарина.
Расширенная профилактика ТГВ после операции по замене тазобедренного сустава
В исследовании расширенной профилактики пациенты, перенесшие операцию по замене тазобедренного сустава, получали эноксапарин натрия во время госпитализации в дозе 40 мг п/к за 12 ч до операции для профилактики послеоперационного ТГВ. В конце периоперационного периода всем пациентам была выполнена двусторонняя венография. Двойным слепым методом пациенты без признаков ВТЭ были рандомизированы для последующего получения либо эноксапарина натрия в дозе 40 мг п/к 1 раз в день (n=90), либо плацебо (n=89) в течение 3 нед. В эту фазу исследования было рандомизировано 179 пациентов, все пациенты прошли лечение. Возраст пациентов составлял от 47 до 87 лет (средний возраст 69,4 года), из них 57% были мужчины и 43% — женщины. В этой популяции пациентов частота развития ТГВ во время расширенной профилактики была значительно ниже в случае эноксапарина натрия по сравнению с плацебо. Данные об эффективности представлены в таблице 7.
Таблица 7
Эффективность эноксапарина натрия в расширенной профилактике ТГВ после операции по замене тазобедренного сустава
| Показатель | Число пациентов, n (%) | |
| Эноксапарин натрия, 40 мг ежедневно, п/к | Плацебо, ежедневно, п/к | |
| Всего пациентов в исследовании расширенной профилактики ТГВ | 90 (100) | 89 (100) |
| Всего ТГВ | 6 (7)1, 95% ДИ: 3–14 | 18 (20), 95% ДИ: 12–30 |
| Проксимальный ТГВ | 5 (6)2, 95% ДИ: 2–13 | 7 (8), 95% ДИ: 3–16 |
1 p=0,008 по сравнению с плацебо.
2 p=0,537 по сравнению с плацебо.
Во втором исследовании пациенты, перенесшие операцию по замене тазобедренного сустава, получали эноксапарин натрия в дозе 40 мг п/к за 12 ч до операции во время госпитализации. Все пациенты были обследованы на предмет клинических признаков и симптомов ВТЭ. Двойным слепым методом пациенты без клинических признаков и симптомов ВТЭ были рандомизированы для последующего получения либо эноксапарина натрия в дозе 40 мг п/к 1 раз в день (n=131), либо плацебо (n=131) в течение 3 нед. В эту фазу исследования были рандомизированы 262 пациента, все пациенты прошли лечение. Возраст пациентов составлял от 44 до 87 лет (средний возраст 68,5 года), из них 43,1% были мужчин и 56,9% — женщины. Как и в первом исследовании, частота развития ТГВ во время расширенной профилактики была значительно ниже в случае эноксапарина натрия по сравнению с плацебо со статистически значимой разницей как по общему числу случаев развития ТГВ (21 (16%) против 45 (34%); p=0,001), так и по числу случаев развития проксимального ТГВ (8 (6%) против 28 (21%); p=<0,001).
Профилактика ТГВ у пациентов с сильно ограниченной подвижностью при остром заболевании
В двойном слепом многоцентровом исследовании с параллельными группами сравнивали применение эноксапарина натрия (20 или 40 мг 1 раз в день п/к) с плацебо в профилактике ТГВ у пациентов с сильно ограниченной подвижностью во время острого заболевания (определяется как ходьба на расстояние до <10 м в течение ≤3 дней). В это исследование были включены пациенты с сердечной недостаточностью (классы III или IV по NYHA), острой дыхательной недостаточностью или осложненной хронической дыхательной недостаточностью (не требующей ИВЛ), острой инфекцией (за исключением септического шока) или острым ревматическим заболеванием (острая поясничная или седалищная боль, компрессия позвоночника из-за остеопороза или опухоли, эпизоды острого артрита нижних конечностей). Всего в исследование было включено 1102 пациента, 1073 пациента прошли лечение. Возраст пациентов составлял от 40 до 97 лет (средний возраст 73 года) с равным соотношением мужчин и женщин. Лечение продолжалось максимум 14 дней (средняя продолжительность 7 дней). При введении в дозе 40 мг 1 раз в день п/к эноксапарин натрия значительно снижал частоту развития ТГВ по сравнению с плацебо. Данные об эффективности представлены в таблице 8.
Таблица 8
Эффективность эноксапарина натрия в профилактике ТГВ у пациентов с сильно ограниченной подвижностью при остром заболевании
| Показатель | Число пациентов, n (%) | ||
| Эноксапарин натрия, 20 мг ежедневно, п/к | Эноксапарин натрия, 40 мг ежедневно, п/к | Плацебо | |
| Всего пациентов с острым заболеванием | 351 (100) | 360 (100) | 362 (100) |
| Всего венозных тромбоэмболических событий1 | 43 (12,3) | 16 (4,4) | 43 (11,9) |
| Всего ТГВ | 43 (12,3), 95% ДИ: 8,8–15,7 | 16 (4,4), 95% ДИ: 2,3–6,6 | 41 (11,3), 95% ДИ: 8,1–14,6 |
| Проксимальный ТГВ | 13 (3,7) | 5 (1,4) | 14 (3,9) |
1 Венозные тромбоэмболические события включали ТГВ, легочную эмболию и смертельный исход по причине тромбоэмболического события.
Примерно через 3 мес после включения в исследование частота развития ВТЭ оставалась ниже в группе получавших эноксапарин натрия в дозе 40 мг по сравнению с группой плацебо.
Лечение ТГВ с ТЭЛА или без нее
В многоцентровом исследовании с параллельными группами 900 пациентов с острым ТГВ нижних конечностей с ТЭЛА или без нее были рандомизированы для лечения в стационаре в группы, получавшие эноксапарин натрия п/к в дозе 1,5 мг/кг 1 раз в день, эноксапарин натрия п/к в дозе 1 мг/кг каждые 12 ч или гепарин (болюсное в/в введение в дозе 5000 МЕ с последующей непрерывной инфузией до достижения АЧТВ от 55 до 85 с). В исследование были рандомизированы 900 пациентов, все пациенты прошли лечение. Возраст пациентов составлял от 18 до 92 лет (средний возраст 60,7 года), из них 54,7% были мужчины и 45,3% — женщины. Все пациенты в пределах 72 ч после начала применения эноксапарина натрия или гепарина также получали варфарин натрия (доза скорректирована в соответствии с ПВ для достижения МНО от 2 до 3). Применение варфарина натрия продолжалось в течение 90 дней. Эноксапарин или стандартную гепариновую терапию назначали в течение минимум 5 дней и до достижения целевого МНО. Оба режима дозирования эноксапарина натрия были эквивалентны стандартной терапии гепарином в снижении риска рецидивов венозной тромбоэмболии (ТГВ и/или ТЭЛА). Данные по эффективности представлены в таблице 9.
Таблица 9
Эффективность эноксапарина натрия при лечении ТГВ с ТЭЛА или без нее
| Показатель | Число пациентов, n (%) | ||
| Эноксапарин натрия, 1,5 мг/кг ежедневно, п/к | Эноксапарин натрия, 1 мг/кг каждые 12 ч, п/к | Гепарин, в/в терапия с контролем АЧТВ | |
| Общее число пациентов с ТГВ сТЭЛА или без нее | 298 (100) | 312 (100) | 290 (100) |
| Всего венозных тромбоэмболических событий (ТГВ и/или ТЭЛА) | 13 (4,4)1 | 9 (2,9)1 | 12 (4,1) |
| Только ТГВ | 11 (3,7) | 7 (2,2) | 8 (2,8) |
| Проксимальный ТГВ | 9 (3) | 6 (1,9) | 7 (2,4) |
| ТЭЛА | 2 (0,7) | 2 (0,6) | 4 (1,4) |
1 95% ДИ для различных режимов дозирования составил: от −3,0 до 3,5 для эноксапарина натрия 1 раз в день по сравнению с гепарином и от −4,2 до 1,7 для эноксапарина натрия каждые 12 ч по сравнению с гепарином.
Аналогичным образом, в многоцентровом открытом исследовании с параллельными группами пациенты с острым проксимальным ТГВ были рандомизированы для получения эноксапарина натрия или гепарина. Пациенты, которые не могли получать амбулаторное лечение, исключались из исследования. Критерии исключения для амбулаторного лечения включали невозможность получить амбулаторную терапию гепарином из-за сопутствующих заболеваний или возможность несоблюдения режима лечения, а также невозможность последующих визитов в амбулаторных условиях из-за географической недоступности. Соответствующие условиям исследования пациенты могли лечиться в больнице, но только пациентам, получавшим эноксапарин натрия, разрешалось проходить лечение дома (72%). Всего в исследование был рандомизирован 501 пациент, все пациенты прошли лечение. Возраст пациентов варьировал от 19 до 96 лет (средний возраст 57,8 года), из них 60,5% были мужчины и 39,5% — женщины. Пациенты были рандомизированы для получения либо эноксапарина натрия (1 мг/кг каждые 12 ч п/к), либо гепарина (болюсное в/в введение в дозе 5000 МЕ с последующей непрерывной инфузией до достижения АЧТВ от 60 до 85 с в стационаре). Все пациенты также получали варфарин натрия, как описано в предыдущем исследовании. Эноксапарин натрия или стандартная терапия гепарином применялась в течение минимум 5 дней. Эноксапарин натрия был эквивалентен стандартной терапии гепарином в снижении риска рецидива ВТЭ. Данные по эффективности представлены в таблице 10.
Таблица 10
Эффективность эноксапарина натрия при лечении ТГВ
| Показатель | Число пациентов, n (%) | |
| Эноксапарин натрия, 1 мг/кг каждые 12 ч, п/к | Гепарин, в/в терапия с контролем АЧТВ | |
| Общее число пациентов с ТГВ | 247 (100) | 254 (100) |
| Всего венозных тромбоэмболических событий (ТГВ и/или ТЭЛА) | 13 (5,3)1 | 17 (6,7) |
| Только ТГВ | 11 (4,5) | 14 (5,5) |
| Проксимальный ТГВ | 10 (4) | 12 (4,7) |
| ТЭЛА | 2 (0,8) | 3 (1,2) |
1 95% ДИ для различных режимов дозирования составил: от −5,6 до 2,7 для эноксапарина натрия по сравнению с гепарином.
Профилактика ишемических осложнений при нестабильной стенокардии и инфаркте миокарда без зубца Q
В многоцентровом двойном слепом исследовании с параллельными группами пациенты, недавно перенесшие нестабильную стенокардию или инфаркт миокарда без зубца Q, были рандомизированы для получения либо эноксапарина натрия (1 мг/кг каждые 12 ч п/к), либо гепарина (болюсное в/в введение в дозе 5000 МЕ с последующей непрерывной инфузией до достижения АЧТВ от 60 до 85 с). В исследование был включен 3171 пациент, лечение прошли 3107 пациентов. Возраст пациентов составлял от 25 до 94 лет (средний возраст 64 года), из них 33,4% пациентов были женщины и 66,6% — мужчины. Среди них 89,8% были представителями европеоидной расы, 4,8% — афроамериканцы, 2% — монголоидной расы и 3,5% — других этнических групп. Все пациенты также получали ацетилсалициловую кислоту в дозе от 100 до 325 мг/сут. Лечение было начато в течение 24 ч после события и продолжалось до клинической стабилизации, процедур реваскуляризации или выписки из больницы с максимальной продолжительностью терапии 8 дней (медиана продолжительности 2,6 дня). Общая частота встречаемости комбинированной тройной конечной точки — смерти, инфаркта миокарда или рецидива стенокардии была ниже при использовании эноксапарина натрия по сравнению с терапией гепарином через 14 дней после начала лечения. Более низкая частота встречаемости тройной конечной точки сохранялась до 30 дней после начала лечения. Эти результаты наблюдались при анализе как у всех рандомизированных, так и всех получивших лечение пациентов (табл. 11).
Таблица 11
Эффективность эноксапарина натрия в профилактике ишемических осложнений при нестабильной стенокардии и инфаркте миокарда без зубца Q (комбинированная конечная точка — смерть, инфаркт миокарда или рецидив стенокардии)
| Показатель | Число пациентов, n (%) | Снижение, % | Значение p | |
| Эноксапарин натрия, 1 мг/кг каждые 12 ч, п/к | Гепарин, в/в терапия с контролем АЧТВ | |||
| Общее число пациентов, получивших лечение | 1578 (100) | 1529 (100) | ||
| Контрольный момент времени (с начала лечения) 48 ч | 96 (6,1) | 112 (7,3) | 1,2 | 0,12 |
| Контрольный момент времени (с начала лечения) 14 дней | 261 (16,5) | 303 (19,8) | 3,3 | 0,017 |
| Контрольный момент времени (с начала лечения) 30 дней | 313 (19,8) | 358 (23,4) | 3,6 | 0,014 |
Общая частота встречаемости смерти или инфаркта миокарда во все контрольные моменты времени была ниже при использовании эноксапарина натрия по сравнению со стандартной терапией гепарином, но это снижение не достигло статистической значимости (табл. 12).
Таблица 12
Эффективность эноксапарина натрия в профилактике ишемических осложнений при нестабильной стенокардии и инфаркте миокарда без зубца Q (комбинированная конечная точка — смерть или инфаркт миокарда)
| Показатель | Число пациентов, n (%) | Снижение, % | Значение p | |
| Эноксапарин натрия, 1 мг/кг каждые 12 ч, п/к | Гепарин, в/в терапия с контролем АЧТВ | |||
| Общее число пациентов, получивших лечение | 1578 (100) | 1529 (100) | ||
| Контрольный момент времени (с начала лечения) 48 ч | 16 (1) | 20 (1,3) | 0,3 | 0,126 |
| Контрольный момент времени (с начала лечения) 14 дней | 76 (4,8) | 93 (6,1) | 1,3 | 0,115 |
| Контрольный момент времени (с начала лечения) 30 дней | 96 (6,1) | 118 (7,7) | 1,6 | 0,069 |
Обследование, проведенное через год после лечения (информация была доступна для 92% включенных в исследование пациентов), показало, что общая частота встречаемости смерти, инфаркта миокарда или рецидива стенокардии оставалась ниже в группе пациентов, получавших эноксапарин натрия, по сравнению с применением гепарина (32 против 35,7%).
Срочные процедуры реваскуляризации выполнялись реже в группе пациентов, получавших эноксапарин натрия, по сравнению с применением гепарина: 6,3 против 8,2% в течение 30 дней (p=0,047).
Лечение острого инфаркта миокарда с подъемом сегмента ST
В многоцентровом двойном слепом плацебо-контролируемом исследовании с параллельными группами пациенты с острым инфарктом миокарда с подъемом сегмента ST, которые подлежали госпитализации в течение 6 ч после начала и подходили для получения фибринолитической терапии, были рандомизированы в группу в соотношении 1:1 для получения эноксапарина натрия или нефракционированного гепарина.
Применение исследуемого ЛС начинали в период между 15 мин до и 30 мин после начала фибринолитической терапии. Нефракционированный гепарин вводили начиная с в/в болюса 60 Ед/кг (максимум 4000 Ед), а затем в виде инфузии 12 Ед/кг/ч (начальный максимум 1000 Ед/ч), которую регулировали для поддержания АЧТВ в пределах 1,5–2 величин контрольного значения. Продолжительность в/в введения должна была составлять минимум 48 ч. Стратегию дозирования эноксапарина натрия корректировали в зависимости от возраста пациента и функции почек. Пациентам моложе 75 лет эноксапарин натрия вводили в виде однократного в/в болюса в дозе 30 мг плюс п/к доза 1 мг/кг с последующими п/к инъекциями 1 мг/кг каждые 12 ч. Пациентам старше 75 лет в/в болюс не вводили, а п/к доза была снижена до 0,75 мг/кг каждые 12 ч. Для пациентов с тяжелой почечной недостаточностью (расчетный Cl креатинина <30 мл/мин) дозу необходимо было изменять на 1 мг/кг каждые 24 ч. П/к инъекции эноксапарина натрия проводили до выписки из больницы или в течение максимум восьми дней (в зависимости от того, что наступало раньше). Средняя продолжительность применения эноксапарина натрия составляла 6,6 дня, нефракционированного гепарина — 54 ч.
Если в период применения исследуемого ЛС выполнялось чрескожное коронарное вмешательство, пациенты получали антитромботическую поддержку с применением замаскированного исследуемого препарата. Пациентам, получавшим эноксапарин натрия, чрескожное коронарное вмешательство должно было выполняться с применением эноксапарина натрия (без переключения) по ранее установленной схеме без дополнительного дозирования, если последнее п/к введение было менее чем за 8 ч до раздува катетера, и с в/в болюсным введением 0,3 мг/кг, если последнее п/к введение было более чем за 8 ч до раздува катетера. Все пациенты получали ацетилсалициловую кислоту минимум в течение 30 дней, 80% пациентов получали фибринспецифический тромболитик (19% тенектеплазу, 5% ретеплазу и 55% алтеплазу) и 20% пациентов получали стрептокиназу.
Средний возраст 20479 пациентов, получивших не менее одной дозы исследуемого ЛС, составлял 60 лет, 76% были мужчины, 87% являлись представителями европеоидной расы, 9,8% — монголоидной расы, 0,2% были афроамериканцами и 2,8% — представителями других этнических групп. Анамнез заболеваний включал перенесенный инфаркт миокарда (13%), гипертензию (44%), сахарный диабет (15%) и ангиографические доказательства ИБС (5%). Сопутствующими ЛС были ацетилсалициловая кислота (95%), бета-адреноблокаторы (86%), ингибиторы АПФ (78%), статины (70%) и клопидогрел (27%). Инфаркт миокарда по локализации был передним у 43%, непередним — у 56% и смешанным — у 1% пациентов.
Первичной конечной точкой эффективности являлась совокупность смерти от любой причины или повторный инфаркт миокарда в первые 30 дней после рандомизации. Последующее наблюдение продолжалось 1 год.
Доля первичной конечной точки эффективности (смерть или повторный инфаркт миокарда) составила 9,9% в группе пациентов, получавших эноксапарин натрия, и 12% у получавших нефракционированный гепарин, снижение относительного риска на 17% (p=0,000003) (табл. 13).
Таблица 13
Эффективность эноксапарина натрия в лечении острого инфаркта миокарда с подъемом сегмента ST
| Конечная точка | Эноксапарин натрия (n=10256) | Нефракционированный гепарин (n=10223) | Относительный риск (95% ДИ) | Значение p |
| Результат в течение 48 ч, n (%) | ||||
| Смерть или повторный инфаркт миокарда | 478 (4,7) | 531 (5,2) | 0,9 (0,8–1,01) | 0,08 |
| Смерть | 383 (3,7) | 390 (3,8) | 0,98 (0,85–1,12) | 0,76 |
| Повторный инфаркт миокарда | 102 (1) | 156 (1,5) | 0,65 (0,51–0,84) | <0,001 |
| Срочная реваскуляризация1 | 74 (0,7) | 96 (0,9) | 0,77 (0,57–1,04) | 0,09 |
| Смерть или повторный инфаркт миокарда или срочная реваскуляризация | 548 (5,3) | 622 (6,1) | 0,88 (0,79–0,98) | 0,02 |
| Результат в течение 8 дней, n (%) | ||||
| Смерть или повторный инфаркт миокарда | 740 (7,2) | 954 (9,3) | 0,77 (0,71–0,85) | <0,001 |
| Смерть | 559 (5,5) | 605 (5,9) | 0,92 (0,82–1,03) | 0,15 |
| Повторный инфаркт миокарда | 204 (2) | 379 (3,7) | 0,54 (0,45–0,63) | <0,001 |
| Срочная реваскуляризация1 | 145 (1,4) | 247 (2,4) | 0,59 (0,48–0,72) | <0,001 |
| Смерть или повторный инфаркт миокарда или срочная реваскуляризация | 874 (8,5) | 1181 (11,6) | 0,74 (0,68–0,8) | <0,001 |
| Результат в течение 30 дней, n (%) | ||||
| Первичная конечная точка эффективности (смерть или повторный инфаркт миокарда) | 1017 (9,9) | 1223 (12) | 0,83 (0,77–0,9) | 0,000003 |
| Смерть | 708 (6,9) | 765 (7,5) | 0,92 (0,84–1,02) | 0,11 |
| Повторный инфаркт миокарда | 352 (3,4) | 508 (5) | 0,69 (0,6–0,79) | <0,001 |
| Срочная реваскуляризация1 | 213 (2,1) | 286 (2,8) | 0,74 (0,62–0,88) | <0,001 |
| Смерть или повторный инфаркт миокарда или срочная реваскуляризация | 1199 (11,7) | 1479 (14,5) | 0,81 (0,75–0,87) | <0,001 |
1 Срочная реваскуляризация означает эпизоды рецидивирующей ишемии миокарда (без инфаркта), приводящие к клиническому решению о проведении коронарной реваскуляризации во время той же госпитализации.
Положительное действие эноксапарина натрия на первичную конечную точку отмечалось во всех ключевых подгруппах, включая возраст, пол, локализацию инфаркта, диабет в анамнезе, перенесенный инфаркт миокарда в анамнезе, введенный фибринолитик и время применения исследуемого препарата.
Положительное действие эноксапарина натрия на первичную конечную точку, наблюдаемое в течение первых 30 дней, сохранялось в течение 12-месячного периода наблюдения.
Частота развития серьезных кровотечений (определяемых как требующие 5 или более доз крови для переливания или снижение гематокрита на 15% или клинически очевидное кровотечение, включая внутричерепное кровоизлияние) в течение 30 дней составила 2,1% в группе пациентов, получавших эноксапарин натрия, и 1,4% при применении нефракционированного гепарина. Частота внутричерепных кровоизлияний в течение 30 дней в этих группах составила 0,8 и 0,7% соответственно. 30-дневное соотношение общей частоты встречаемости смерти, повторного инфаркта миокарда или показателя чистой клинической пользы было значительно ниже в группе пациентов, получавших эноксапарин натрия (10,1%) по сравнению с получавшими гепарин (12,2%).
Показания к применению
Профилактика тромбоза глубоких вен, который может привести к ТЭЛА у пациентов, подвергающихся абдоминальной хирургии, имеющих факторы риска развития тромбоэмболических осложнений, у пациентов, перенесших операцию по замене тазобедренного сустава, во время и после госпитализации, у пациентов, перенесших операцию по замене коленного сустава, а также у больных, которые подвержены риску развития тромбоэмболических осложнений из-за сильно ограниченной подвижности во время острого заболевания.
Лечение острого тромбоза глубоких вен:
— стационарное лечение острого тромбоза глубоких вен с легочной эмболией или без нее при введении в сочетании с варфарином;
— амбулаторное лечение острого тромбоза глубоких вен без легочной эмболии при введении в сочетании с варфарином.
Профилактика ишемических осложнений нестабильной стенокардии и инфаркта миокарда без зубца Q при одновременном применении с ацетилсалициловой кислотой.
Лечение острого инфаркта миокарда с подъемом сегмента ST. Было показано, что эноксапарин натрия при одновременном применении с ацетилсалициловой кислотой снижает риск комбинированной конечной точки, включающей повторный инфаркт миокарда или смертельный исход, у пациентов с острым инфарктом миокарда с подъемом сегмента ST, получающих тромболитическую терапию, или которым выполнено чрескожное коронарное вмешательство.
Противопоказания
Известная гиперчувствительность к эноксапарину натрия (например, зуд, крапивница, анафилактические/анафилактоидные реакции) (см. «Побочные действия») или к гепарину или продуктам из свинины; активное сильное кровотечение; иммуноопосредованная гепарининдуцированная тромбоцитопения (ГИТ) в анамнезе в течение последних 100 дней или наличие циркулирующих антител (см. «Меры предосторожности»).
Применение при беременности и кормлении грудью
В испытаниях, проведенных на животных, наблюдался плацентарный перенос эноксапарина натрия. Данные ретроспективного когортного исследования у женщин, включавшего 693 живорожденных, и данные, полученные в испытаниях на животных, позволяют предположить, что применение эноксапарина натрия не увеличивает риск серьезных аномалий развития плода.
Беременность, как состояние, создает повышенный риск развития тромбоэмболии, который еще выше у женщин с тромбоэмболическими заболеваниями и некоторыми сопутствующими состояниями с высокими факторами риска. Достаточных исследований не проводилось, но беременные женщины с механическими протезами клапанов сердца могут подвергаться еще более высокому риску развития тромбоза (см. «Меры предосторожности»).
Беременные женщины с тромбоэмболическими заболеваниями, в т.ч. с механическими протезами клапанов сердца, а также с наследственными или приобретенными тромбофилиями, имеют повышенный риск других материнских осложнений и потери плода независимо от типа используемого антикоагулянта.
Все пациенты, получающие антикоагулянты, в т.ч. беременные женщины, подвержены риску развития кровотечения. Беременные женщины, получающие эноксапарин натрия, должны находиться под тщательным наблюдением на предмет развития кровотечения или чрезмерной антикоагуляции. Следует использовать антикоагулянт с наиболее коротким действием. Кровоизлияние может произойти в любом месте и привести к смерти матери и/или плода.
Беременные женщины должны быть проинформированы о потенциальной опасности для плода и матери при применении эноксапарина натрия во время беременности.
Неизвестно, влияет ли мониторинг активности антифактора Ха и корректировка дозы (по масссе тела или активности антифактора Ха) эноксапарина натрия на его безопасность и эффективность применения во время беременности.
Адекватные и хорошо контролируемые исследования у беременных женщин не проводились. В ретроспективном исследовании были изучены данные о 604 женщинах, которые применяли эноксапарин натрия во время беременности. В общей сложности 624 беременности привели к появлению 693 живорожденных. У 63 женщин отмечено 72 геморрагических события (11 серьезных). Имелось 14 случаев неонатального кровотечения. Частота серьезных врожденных аномалий живорожденных младенцев (2,5%) была аналогична фоновой.
Имеются пострегистрационные сообщения о гибели плода при применении эноксапарина натрия у беременных женщин. Причинно-следственная связь в этих случаях не установлена. Оценку этих случаев усложняют недостаточные данные, наличие основного заболевания и возможность неадекватной антикоагуляции.
Имеются данные клинического исследования с применением эноксапарина натрия у беременных женщин с механическими протезами клапанов сердца (см. «Меры предосторожности»).
Тератологические исследования, проведенные на беременных крысах и кроликах при п/к дозах эноксапарина, которые в 15 раз превышают рекомендуемую дозу для человека (по сравнению с максимальной рекомендованной суточной дозой 2 мг/кг), показали отсутствие доказательств тератогенности или фетотоксичности эноксапарина натрия. Поскольку исследования репродукции животных не всегда позволяют прогнозировать реакцию человека, эноксапарин натрия следует использовать во время беременности только в случае крайней необходимости.
Неизвестно, выделяется ли эноксапарин натрия с грудным молоком. У кормящих крыс проникновение эноксапарина или его метаболитов с молоком очень ограничено. Нет информации о влиянии эноксапарина или его метаболитов на ребенка, находящегося на грудном вскармливании, или на выработку молока. Следует учитывать преимущества грудного вскармливания для развития и здоровья ребенка, а также клиническую потребность матери в эноксапарине натрия и любые возможные побочные действия у ребенка, находящегося на грудном вскармливании, возникшие от применения этого ЛС или из-за материнских заболеваний.
Побочные действия
Опыт клинических исследований
Поскольку клинические исследования проводятся в различных условиях, частота побочных реакций, наблюдаемая в клинических исследованиях какого-либо ЛС, не может напрямую сравниваться с частотой этих реакций в клинических исследованиях другого ЛС и может не отражать показатели, наблюдаемые в клинической практике.
Во время клинических исследований по одобренным показаниям эноксапарин натрия получали 15918 пациентов. Среди них 1228 пациентов с факторами риска развития тромбоэмболических осложнений получали эноксапарин для профилактики ТГВ после абдоминальных операций, 1368 — для профилактики ТГВ после операции по замене тазобедренного или коленного сустава, 711 — для профилактики ТГВ при сильно ограниченной подвижности во время острой болезни, 1578 — для профилактики ишемических осложнений при нестабильной стенокардии и инфаркта миокарда без зубца Q, 10176 — для лечения острого инфаркта миокарда с подъемом сегмента ST и 857 — для лечения ТГВ с ТЭЛА или без нее. Дозы эноксапарина в клинических исследованиях для профилактики ТГВ после операций на брюшной полости и по замене тазобедренного или коленного сустава или у больных с сильно ограниченной подвижностью во время острого заболевания варьировали от 40 мг п/к 1 раз в день до 30 мг п/к 2 раза в день. В клинических исследованиях по профилактике ишемических осложнений нестабильной стенокардии и инфаркта миокарда без зубца Q доза составляла 1 мг/кг каждые 12 ч, а в клинических исследованиях лечения острого инфаркта миокарда с подъемом сегмента ST дозы эноксапарина натрия составляли 30 мг в виде в/в болюсной инъекции с последующим п/к введением в дозе 1 мг/кг каждые 12 ч.
Геморрагия
Данные о случаях развития серьезных кровотечений в ходе клинических исследований эноксапарина натрия приведены в таблицах 14–19.
Таблица 14
Эпизоды серьезного кровотечения после абдоминальной и колоректальной хирургии1
| Показание | Режим дозирования | |
| Эноксапарин натрия, 40 мг ежедневно, п/к | Гепарин, 5000 МЕ, каждые 8 ч, п/к | |
| Абдоминальная хирургия | 23 (4%) (n=555) | 16 (3%) (n=560) |
| Колоректальная хирургия | 28 (4%) (n=673) | 21 (3%) (n=674) |
1 Осложнения, связанные с кровотечением, считались серьезными, если кровотечение вызвало значительное клиническое событие или оно сопровождалось снижением уровня Hb на ≥2 г/дл или переливанием 2 или более доз крови. Забрюшинные, внутриглазные и внутричерепные кровоизлияния всегда рассматривались как серьезные.
Таблица 15
Эпизоды серьезного кровотечения после операций по замене тазобедренного или коленного сустава1
| Показание | Режим дозирования | ||
| Эноксапарин натрия, 40 мг ежедневно, п/к | Эноксапарин натрия, 30 мг каждые 12 ч, п/к | Гепарин, 15000 МЕ/24 ч, п/к | |
| Замена тазобедренного сустава без профилактики2 | 31 (4%) (n=786) | 32 (6%) (n=541) | |
| Замена тазобедренного сустава с профилактикой: | |||
| — периоперационный период3 | 4 (2%) (n=288) | ||
| — период профилактики4 | 0 (0%) (n=221) | ||
| Замена коленного сустава без профилактики2 | 3 (1%) (n=294) | 3 (1%) (n=225) |
1 Осложнения, связанные с кровотечением, считались серьезными, если кровотечение вызвало значительное клиническое событие или оно сопровождалось снижением уровня Hb на ≥2 г/дл или переливанием 2 или более доз крови. Забрюшинные и внутричерепные кровоизлияния всегда рассматривались как серьезные. При операциях по замене коленного сустава внутриглазные кровотечения также рассматривались как серьезные.
2 Эноксапарин натрия, 30 мг каждые 12 ч п/к с началом введения через 12–24 ч после операции и в последующие 14 дней.
3 Эноксапарин натрия, 40 мг п/к 1 раз в день за 12 ч до операции и в течение 7 дней после операции.
4 Эноксапарин натрия, 40 мг п/к 1 раз в день в течение 21 дня после выписки.
Таблица 16
Эпизоды серьезного кровотечения у больных с сильно ограниченной подвижностью во время острого заболевания1
| Показание | Режим дозирования | ||
| Эноксапарин натрия2, 20 мг ежедневно, п/к | Эноксапарин натрия2, 40 мг ежедневно, п/к | Плацебо2 | |
| Малоподвижные больные в период острого заболевания | 1 (<1%) (n=351) | 3 (<1%) (n=360) | 2 (<1%) (n=362) |
1 Осложнения, связанные с кровотечением, считались серьезными, если кровоизлияние вызвало значимое клиническое событие, или оно вызвало снижение уровня Hb на ≥2 г/дл или переливание 2 или более доз крови. Забрюшинные и внутричерепные кровоизлияния всегда рассматривались как серьезные, хотя в ходе исследований о них не сообщалось.
2 Случаи развития серьезного кровотечения в течение 24 ч после введения последней дозы.
Таблица 17
Эпизоды серьезного кровотечения при ТГВ с легочной эмболией или без нее1
| Показание | Режим дозирования | ||
| Эноксапаран натрия, 1,5 мг/кг ежедневно, п/к | Эноксапарин натрия, 1 мг/кг каждые 12 ч, п/к | Гепарин, в/в терапия с контролем АЧТВ | |
| Лечение ТГВ и легочной эмболии | 5 (2%) (n=298) | 9 (2%) (n=559) | 9 (2%) (n=554) |
1 Осложнения, связанные с кровотечением, считались серьезными, если кровотечение вызвало значительное клиническое событие, или оно сопровождалось снижением уровня Hb на ≥2 г/дл или переливанием 2 или более доз крови. Забрюшинные, внутриглазные и внутричерепные кровоизлияния всегда рассматривались как серьезные.
2 После применения эноксапарина натрия или стандартной терапии гепарином все пациенты также получали варфарин натрия (доза, скорректированная в соответствии с ПВ для достижения МНО от 2 до 3), начиная в пределах 72 ч после окончания терапии и продолжая в течение до 90 дней.
Таблица 18
Эпизоды серьезного кровотечения при нестабильной стенокардии и инфаркте миокарда без зубца Q1
| Показание | Режим дозирования | |
| Эноксапарин натрия2, 1 мг/кг каждые 12 ч, п/к | Гепарин2, в/в терапия с контролем АЧТВ | |
| Нестабильная стенокардия и инфаркт миокарда без зубца Q3 | 17 (1%) (n=1578) | 18 (1%) (n=1529) |
1 Осложнения, связанные с кровотечением, считались серьезными, если кровотечение вызвало значимое клиническое событие, или оно сопровождалось снижением уровня Hb на ≥3 г/дл или переливанием 2 или более доз крови. Внутриглазные, забрюшинные и внутричерепные кровоизлияния всегда считались серьезными.
2 Случаи развития серьезного кровотечения в течение 12 ч после применения ЛС.
3 Одновременно назначалась ацетилсалициловая кислота в дозах от 100 до 325 мг/сут.
Таблица 19
Эпизоды серьезного кровотечения при остром инфаркте миокарда с подъемом сегмента ST
| Эпизод | Режим дозирования | |
| Эноксапарин натрия1, 1 мг/кг каждые 12 ч, п/к (n=10176) | Гепарин1, в/в терапия с контролем АЧТВ (n=10151) | |
| Серьезное кровотечение (включая внутричерепное кровоизлияние)2 | 211 (2,1%) | 138 (1,4%) |
| Внутричерепное кровоизлияние | 84 (0,8%) | 66 (0,7%) |
1 Случаи серьезного кровотечения (включая внутричерепное кровоизлияние), развившегося в период до 30 дней.
2 Кровотечение считалось серьезным, если оно вызывало значимое клиническое событие, связанное со снижением уровня Hb на ≥5 г/дл. Внутричерепное кровоизлияние всегда рассматривалось как серьезное.
Повышение уровня сывороточных аминотрансфераз
Бессимптомное повышение уровня АСТ и АЛТ более чем 3×ВГН лабораторного референсного диапазона было зарегистрировано у 6,1 и 5,9% пациентов соответственно во время применения эноксапарина натрия.
Так как определение уровня аминотрансфераз имеет большое значение в дифференциальной диагностике инфаркта миокарда, заболеваний печени и легочной эмболии, повышение, которое может быть связано с применением таких ЛС, как эноксапарин натрия, следует интерпретировать с осторожностью.
Реакции в месте введения
После п/к инъекции эноксапарина натрия могут возникать такие местные реакции, как раздражение, боль, гематома, экхимоз и эритема.
Побочные реакции у пациентов, получавших эноксапарин натрия для профилактики или лечения ТГВ, легочной эмболии
Ниже представлены другие побочные реакции, наблюдавшиеся с частотой не менее 2%, которые предположительно, возможно, или вероятно были связаны с применением эноксапарина натрия, гепарина или плацебо в клинических исследованиях с участием пациентов, перенесших операцию по замене тазобедренного или коленного сустава, абдоминальные или колоректальные операции или получивших лечение ТГВ (табл. 20–23).
Таблица 20
Побочные реакции, возникавшиие с частотой ≥2% у пациентов, получавших эноксапарин и перенесших абдоминальное или колоректальное хирургическое вмешательство
| Побочная реакция | Частота, % | |||
| Эноксапарин натрия, 40 мг ежедневно, п/к (n=1228) | Гепарин, 5000 МЕ каждые 8 ч, п/к (n=1234) | |||
| Серьезная | Всего | Серьезная | Всего | |
| Геморрагия | <1 | 7 | <1 | 6 |
| Анемия | <1 | 3 | <1 | 3 |
| Экхимоз | 0 | 3 | 0 | 3 |
Таблица 21
Побочные реакции, возникавшие с частотой ≥2% у пациентов, получавших эноксапарин и перенесших операцию по замене тазобедренного или коленного сустава
| Побочная реакция | Частота, % | |||||||||
| Эноксапарин натрия, 40 мг ежедневно, п/к | Эноксапарин натрия, 30 мг каждые 12 ч, п/к (n=1080) | Гепарин, 15000 МЕ/24 ч, п/к (n=766) | Плацебо, каждые 12 ч, п/к (n=115) | |||||||
| Периоперационный период (n=288)1 | Период профилактики (n=131)2 | |||||||||
| Серьезная | Всего | Серьезная | Всего | Серьезная | Всего | Серьезная | Всего | Серьезная | Всего | |
| Высокая температура | 0 | 8 | 0 | 0 | <1 | 5 | <1 | 4 | 0 | 3 |
| Кровоизлияние | <1 | 13 | 0 | 5 | <1 | 4 | 1 | 4 | 0 | 3 |
| Тошнота | <1 | 3 | <1 | 2 | 0 | 2 | ||||
| Анемия | 0 | 16 | 0 | <2 | <1 | 2 | 2 | 5 | <1 | 7 |
| Отек | <1 | 2 | <1 | 2 | 0 | 2 | ||||
| Периферический отек | 0 | 6 | 0 | 0 | <1 | 3 | <1 | 4 | 0 | 3 |
1 Данные получены при применении эноксапарина натрия в дозе 40 мг п/к 1 раз в день, начатом за 12 ч до операции, у 288 пациентов после операции по замене тазобедренного сустава, которые получали его в периоперационный период в одном открытом клиническом исследовании.
2 Данные получены при применении эноксапарина натрия в дозе 40 мг п/к 1 раз в день, вводимого в слепом режиме для профилактики в конце периоперационного периода, у 131 из всего 288 пациентов после операции по замене тазобедренного сустава в течение 21 дня в одном клиническом исследовании.
Таблица 22
Побочные реакции, возникавшие с частотой ≥2% у пациентов с сильно ограниченной подвижностью во время острого заболевания, получавших эноксапарин натрия
| Побочная реакция | Частота, % | |
| Эноксапарин натрия, 40 мг ежедневно, п/к (n=360) | Плацебо, ежедневно, п/к (n=362) | |
| Одышка | 3,3 | 5,2 |
| Тромбоцитопения | 2,8 | 2,8 |
| Спутанность сознания | 2,2 | 1,1 |
| Диарея | 2,2 | 1,7 |
| Тошнота | 2,5 | 1,7 |
Таблица 23
Побочные реакции, возникавшие с частотой ≥2% у пациентов, получавших эноксапарин натрия и проходящих лечение ТГВ с легочной эмболией или без нее
| Побочная реакция | Частота, % | |||||
| Эноксапарин натрия, 1,5 мг/кг ежедневно, п/к (n=298) | Эноксапарин натрия, 1 мг/кг каждые 12 ч, п/к (n=559) | Гепарин, в/в терапия с контролем АЧТВ (n=544) | ||||
| Серьезная | Всего | Серьезная | Всего | Серьезная | Всего | |
| Кровоизлияние в месте инъекции | 0 | 5 | 0 | 3 | <1 | <1 |
| Боль в месте инъекции | 0 | 2 | 0 | 2 | 0 | 0 |
| Гематурия | 0 | 2 | 0 | <1 | <1 | 2 |
Нежелательные реакции у пациентов с нестабильной стенокардией или инфарктом миокарда без зубца Q, получавших эноксапарин натрия
Сообщалось, что негеморрагические клинические события, связанные с применением эноксапарина натрия, встречались с частотой ≤1%. Незначительные геморрагические явления, в первую очередь экхимоз в месте инъекции и гематомы, чаще регистрировались у пациентов, получавших эноксапарин натрия п/к, чем у пациентов, получавших гепарин в/в. Ниже представлены серьезные нежелательные реакции при применении эноксапарина натрия или гепарина в клинических исследованиях у пациентов с нестабильной стенокардией или инфарктом миокарда без зубца Q, частота которых составляла не менее 0,5% в группе получавших эноксапарин натрия (табл. 24).
Таблица 24
Серьезные нежелательные реакции, возникавшие с частотой ≥0,5% у пациентов с нестабильной стенокардией или инфарктом миокарда без зубца Q, получавших эноксапарин натрия
| Нежелательная реакция | Число случаев (%) | |
| Эноксапарин натрия, 1 мг/кг каждые 12 ч, п/к (n=1578) | Гепарин, в/в терапия с контролем АЧТВ (n=1529) | |
| Мерцательная аритмия | 11 (0,7) | 3 (0,2) |
| Сердечная недостаточность | 15 (0,95) | 11 (0,72) |
| Отек легких | 11 (0,7) | 11 (0,72) |
| Пневмония | 13 (0,82) | 9 (0,59) |
Побочные реакции у пациентов с острым инфарктом миокарда с подъемом сегмента ST, получавших эноксапарин натрия
В клиническом исследовании у пациентов с острым инфарктом миокарда с подъемом сегмента ST частота тромбоцитопении составляла 1,5%.
Пострегистрационный опыт
Во время пострегистрационного применения эноксапарина натрия были выявлены следующие побочные реакции. Поскольку об этих реакциях сообщается в добровольном порядке от популяции неопределенного размера, не всегда возможно надежно оценить их частоту или установить причинно-следственную связь с действием ЛС.
Имелись сообщения об образовании эпидуральной или спинальной гематомы при одновременном применении эноксапарина натрия и спинальной/эпидуральной анестезии или выполнении спинальной пункции. Большинству пациентов был установлен постоянный эпидуральный катетер в послеоперационном периоде для обезболивания, или они получали дополнительные ЛС, влияющие на гемостаз, такие как НПВС. Многие эпидуральные или спинномозговые гематомы вызвали неврологические повреждения, включая долгосрочный или постоянный паралич.
Имеются сообщения о таких побочных реакциях, как местные реакции в месте инъекции (например, узелки, воспаление, мокнутие), системные аллергические реакции (например, зуд, крапивница, анафилактические/анафилактоидные реакции, включая шок), везикулобуллезная сыпь, случаи гиперчувствительности, кожный васкулит, пурпура, некроз кожи (возникающие в месте инъекции или на расстоянии от него), тромбоцитоз и тромбоцитопения с тромбозом (см. «Меры предосторожности»).
Сообщалось о случаях развития гиперкалиемии. Большинство этих случаев наблюдалось у пациентов, имевших также состояния, предрасполагающие к развитию гиперкалиемии (например, почечная дисфункция, применение сопутствующих калийсберегающих ЛС, дополнительное введение калия, гематома в тканях тела).
Сообщалось также об очень редких случаях развития гиперлипидемии; один случай гиперлипидемии с выраженной гипертриглицеридемией у беременной женщины с диабетом, причинно-следственная связь не установлена.
Сообщалось о случаях головной боли, геморрагической анемии, эозинофилии, алопеции, гепатоцеллюлярного и холестатического поражения печени.
Сообщалось также о развитии остеопороза после длительного лечения.
Взаимодействие
Реклама: ООО «ВЕДАНТА», ИНН 7714886235, erid 4CQwVszH9pUkKJ7jUDd
Реклама: ООО «РЛС-Библиомед» ИНН 7714758963
Реклама: ООО «ВЕДАНТА», ИНН 7714886235, erid 4CQwVszH9pUkKJ7jUDd
Реклама: ООО «РЛС-Библиомед» ИНН 7714758963
До начала применения эноксапарина натрия следует по возможности прекратить прием ЛС, которые могут повысить риск развития кровотечения. Такие ЛС включают антикоагулянты, ингибиторы агрегации тромбоцитов, включая ацетилсалициловую кислоту, салицилаты, НПВС (включая кеторолак), дипиридамол или сульфинпиразон. Если совместное применение необходимо, проводить его следует при тщательном клиническом и лабораторном мониторинге (см. «Меры предосторожности»).
Передозировка
Симптомы: случайная передозировка эноксапарина натрия может привести к геморрагическим осложнениям.
Лечение: инъекции эноксапарина натрия можно в значительной степени нейтрализовать медленным в/в введением протамина сульфата (1% раствор). Доза протамина сульфата должна быть равна дозе введенного эноксапарина натрия: следует ввести 1 мг сульфата протамина, чтобы нейтрализовать 1 мг эноксапарина натрия, если он применялся в предыдущие 8 ч. Инфузия 0,5 мг протамина на 1 мг эноксапарина натрия может быть введена, если эноксапарин натрия был введен более чем за 8 ч до протамина или если было определено, что требуется вторая доза протамина. Вторая инфузия 0,5 мг сульфата протамина на 1 мг эноксапарина натрия может быть назначена, если АЧТВ, измеренное через 2–4 ч после первой инфузии, остается продолжительным. Если с момента последней инъекции эноксапарина натрия прошло по крайней мере 12 ч, введение протамина может не потребоваться, однако даже при более высоких дозах протамина АЧТВ может оставаться выше, чем после введения гепарина. Во всех случаях активность антифактора Ха никогда полностью не нейтрализуется (максимум около 60%). Следует проявлять особую осторожность, чтобы избежать передозировки протамина сульфата. Применение протамина сульфата может вызвать тяжелые гипотензивные и анафилактоидные реакции. Поскольку сообщалось о фатальных реакциях, часто напоминающих анафилаксию, протамина сульфат следует назначать только тогда, когда доступны методы реанимации и лечения анафилактического шока.
Способ применения и дозы
Реклама: ООО «РЛС-Патент», ИНН 5044031277, erid=4CQwVszH9pUkpHxmQQo
Реклама: ООО «РЛС-Патент», ИНН 5044031277, erid=4CQwVszH9pUkpHxmQQo
В/в или п/к, режим дозирования зависит от показаний и индивидуальных особенностей пациента.
Меры предосторожности
Повышенный риск развития кровоизлияния
Сообщалось о случаях эпидурального или спинального кровоизлияния и развития последующих гематом при применении эноксапарина натрия и эпидуральной или спинальной анестезии/анальгезии или процедур спинномозговой пункции, что приводило к длительному или постоянному параличу. Риск этих событий выше при использовании послеоперационных постоянных эпидуральных катетеров с одновременным применением дополнительных ЛС, влияющих на гемостаз, таких как НПВС, при травматической или повторной эпидуральной или спинномозговой пункции или у пациентов с хирургическим вмешательством на позвоночнике или деформацией позвоночника (см. «Побочные действия» и «Взаимодействие»).
Чтобы снизить потенциальный риск развития кровотечения, связанного с одновременным использованием эноксапарина натрия и эпидуральной или спинальной анестезии/анальгезии или спинномозговой пункции, размещение или удаление эпидурального катетера или люмбальную пункцию лучше всего выполнять при низком антикоагулянтном эффекте эноксапарина натрия, однако точное время достижения такого эффекта у каждого пациента неизвестно.
Установку или удаление катетера следует отложить по крайней мере на 12 ч после применения более низких доз (30 мг 1 или 2 раза в день или 40 мг 1 раз в день) эноксапарина натрия и не менее чем на 24 ч после применения более высоких доз (0,75 мг/сут 2 раза в день в день, 1 мг/кг 2 раза в день или 1,5 мг/кг 1 раз в день). Уровень антиХа остается определяемым в эти временные точки, и эти отсрочки не являются гарантией того, что можно будет избежать нейроаксиальной гематомы. Пациенты, получающие дозу 0,75 мг/кг 2 раза в день или 1 мг/кг 2 раза в день, не должны получать вторую дозу эноксапарина натрия при схеме дозирования 2 раза в день, чтобы обеспечить более длительный интервал перед установкой или удалением катетера. Хотя конкретные рекомендации относительно времени введения следующей дозы эноксапарина натрия после удаления катетера не могут быть сделаны, аналогичным образом следует рассмотреть возможность отложить применение следующей дозы как минимум на 4 ч, что основано на оценке пользы и риска с учетом как риска развития тромбоза, так и кровотечения, принимая во внимание процедуру и факторы риска, имеющиеся у пациента. Для пациентов с Cl креатинина <30 мл/мин необходимо, учитывая более продолжительную элиминацию эноксапарина натрия, рассмотреть возможность удвоения сроков удаления катетера по крайней мере на 24 ч для более низкой предписанной дозы (30 мг 1 раз в день) и не менее 48 ч для более высокой (1 мг/кг/сут).
Если антикоагулянтная терапия назначается в условиях с применением эпидуральной или спинальной анестезии/анальгезии или спинномозговой пункции, необходимо проводить частый мониторинг для выявления любых признаков и симптомов неврологического нарушения, таких как боль в средней части спины, сенсорный и двигательный дефицит (онемение или слабость в нижних конечностях), а также дисфункция кишечника и/или мочевого пузыря. При появлении любого из вышеперечисленных признаков или симптомов пациент должен сообщить о них врачу. При подозрении на признаки или симптомы гематомы позвоночника необходимо срочно провести диагностику и лечение, включая декомпрессию спинного мозга, даже если такое лечение не может предотвратить или снять неврологические последствия.
Эноксапарин натрия следует применять с особой осторожностью в случаях повышенного риска развития кровоизлияния, таких как бактериальный эндокардит, врожденные или приобретенные нарушения свертываемости крови, активные язвенные и ангиодиспластические заболевания ЖКТ, геморрагический инсульт или вскоре после операции на головном мозге, позвоночнике или офтальмологической операции, а также у пациентов, получавших сопутствующее лечение с применением ингибиторов агрегации тромбоцитов.
Сообщалось о развитии больших кровоизлияний, включая забрюшинное и внутричерепное. Некоторые из этих случаев закончились смертельным исходом.
Во время применения эноксапарина натрия кровотечение может возникнуть в любом месте. Необъяснимое падение уровня гематокрита или АД должно стать основанием для поиска места кровотечения.
Повышенный риск развития кровотечения после процедур чрескожной коронарной реваскуляризации (ЧКРВ)
Чтобы свести к минимуму риск развития кровотечения после вмешательства на сосудах во время лечения нестабильной стенокардии, инфаркта миокарда без зубца Q и острого инфаркта миокарда с подъемом сегмента ST, необходимо точно соблюдать рекомендуемые интервалы между дозами эноксапарина натрия. После ЧКРВ важно добиться гемостаза в месте пункции.
При использовании устройства для закрытия сосуда интродьюсер можно удалить сразу. Удаление интродьюсера с последующей ручной компрессией следует проводить через 6 ч после последнего в/в или п/к введения эноксапарина натрия. Если применение эноксапарина натрия будет продолжено, следующую запланированную дозу следует ввести не раньше чем через 6–8 ч после удаления интродьюсера. Место процедуры следует наблюдать на предмет развития признаков кровотечения или образования гематомы.
Повышенный риск развития кровоизлияния у пациентов с сопутствующими заболеваниями
Эноксапарин натрия следует с осторожностью назначать пациентам с геморрагическим диатезом, неконтролируемой артериальной гипертензией или недавней язвой ЖКТ в анамнезе, диабетической ретинопатией, нарушением функции почек и геморрагией.
Риск развития ГИТ с тромбозом или без него
Эноксапарин натрия может вызывать ГИТ или гепарининдуцированную тромбоцитопению с тромбозом (ГИТТ). ГИТТ может привести к инфаркту органа, ишемии конечностей или смерти. Необходимо установить мониторинг тромбоцитопении любой степени.
Применение эноксапарина натрия у пациентов с историей иммуноопосредованной ГИТ в течение последних 100 дней или при наличии циркулирующих антител противопоказано (см. «Противопоказания»). Циркулирующие антитела могут сохраняться в течение нескольких лет.
Эноксапарин натрия можно применять у пациентов с ГИТ в анамнезе, только если с момента предыдущего эпизода ГИТ прошло более 100 дней и в крови отсутствуют антитела. Поскольку ГИТ все еще может возникать в этих обстоятельствах, решение об использовании эноксапарина натрия в таком случае должно быть принято только после тщательной оценки соотношения польза-риск и рассмотрения альтернативных методов лечения, не связанных с применением гепарина.
Тромбоцитопения
При применении эноксапарина натрия может развиться тромбоцитопения. Умеренная тромбоцитопения (количество тромбоцитов от 100000/мм3 до 50000/мм3) наблюдалась у 1,3% пациентов, получавших эноксапарин натрия, 1,2% пациентов, получавших гепарин, и 0,7% пациентов, получавших плацебо в клинических исследованиях. Количество тромбоцитов менее 50000/мм3 в тех же исследованиях наблюдалось у 0,1% пациентов, получавших эноксапарин натрия, у 0,2% пациентов, получавших гепарин, и 0,4% пациентов, получавших плацебо.
Следует внимательно следить за появлением тромбоцитопении любой степени. Если количество тромбоцитов становится ниже 100000/мм3, применение эноксапарина натрия следует прекратить.
Взаимозаменяемость с другими гепаринами
Эноксапарин натрия нельзя использовать взаимозаменяемо (по единицам измерения) с гепарином или другими низкомолекулярными гепаринами, поскольку они различаются по процессу производства, молекулярно-массовому распределению, анти-Ха- и анти-IIa-активности, единицам измерения и дозировке. У каждого из этих ЛС имеется собственная инструкция по применению.
Пациенты с механическими протезами клапанов сердца
Применение эноксапарина натрия для тромбопрофилактики у пациентов с механическими протезами сердечных клапанов изучено недостаточно, и отсутствуют адекватные иследования по его долгосрочному использованию в этой популяции пациентов. Сообщалось о единичных случаях тромбоза протеза клапана сердца у пациентов с механическими протезами клапанов сердца, получавших эноксапарин натрия для тромбопрофилактики.
Использование эноксапарина натрия для тромбопрофилактики у беременных женщин с механическими протезами клапанов сердца может привести к тромбозу протеза. В клиническом исследовании с участием беременных женщин с механическими протезами клапанов сердца, которые получали эноксапарин натрия (1 мг/кг 2 раза в день) для снижения риска развития тромбоэмболии, у 2 из 8 женщин образование сгустков привело к закупорке клапана и смерти матери и плода. Ни один из пациентов в группе получавших гепарин/варфарин (0 из 4 женщин) не умер. Также были отдельные пострегистрационные сообщения о развитии тромбоза протеза у беременных с механическими протезами клапанов сердца, получавших эноксапарин натрия для тромбопрофилактики. Женщины с механическими протезами клапанов сердца могут быть подвержены более высокому риску развития тромбоэмболии во время беременности и имеют более высокий уровень потери плода в результате мертворождения, самопроизвольного аборта и преждевременных родов. Следовательно, может потребоваться частый мониторинг максимального и минимального уровней антифактора Ха и корректировка дозы.
Особые группы пациентов
Дети. Безопасность и эффективность эноксапарина натрия в педиатрической практике не установлены. Эноксапарин натрия не одобрен для применения у новорожденных и младенцев.
Пожилой возраст. Более 2800 пациентов в возрасте 65 лет и старше получали эноксапарин натрия в ходе клинических исследований для профилактики ТГВ в хирургии бедра, колена и брюшной полости или лечения ТГВ, профилактики ишемических осложнений нестабильной стенокардии и инфаркта миокарда без зубца Q. Эффективность эноксапарина натрия в пожилом возрасте (≥65 лет) была аналогична таковой у более молодых пациентов (<65 лет). Частота развития кровотечений была сходной у пожилых и молодых пациентов, когда применялись дозы 30 мг каждые 12 ч или 40 мг 1 раз в день. Частота развития кровотечений у пожилых пациентов была выше по сравнению с более молодыми, когда эноксапарин натрия вводили в дозах 1,5 мг/кг 1 раз в день или 1 мг/кг каждые 12 ч. Риск развития кровотечения, связанного с применением эноксапарина натрия, увеличивается с возрастом. Серьезные побочные эффекты увеличивались с возрастом у пациентов, получавших эноксапарин натрия.
Другой клинический опыт (включая пострегистрационное наблюдение и отчеты) не выявил дополнительных различий в безопасности применения эноксапарина натрия у пожилых и более молодых пациентов. Рекомендуется внимательно следить за интервалами дозирования и приемом сопутствующих ЛС (особенно антиагрегантов). Эноксапарин натрия следует применять с осторожностью у пожилых пациентов, у которых может наблюдаться задержка выведения эноксапарина. Следует рассмотреть возможность наблюдения за пожилыми пациентами с низкой массой тела (<45 кг) и предрасположенными к снижению функции почек.
В клиническом исследовании лечения острого инфаркта миокарда с подъемом сегмента ST не выявлено различий в эффективности применения эноксапарина натрия у пациентов в возрасте ≥75 лет (n=1241) и моложе 75 лет (n=9015). Пациенты в возрасте ≥75 лет не получали 30 мг в/в болюсно до перехода к обычному режиму дозирования, а доза при п/к введении корректировалась до 0,75 мг/кг каждые 12 ч. Частота развития кровотечений была выше у пациентов в возрасте ≥65 лет по сравнению с пациентами более молодого возраста (<65 лет).
Почечная недостаточность. У пациентов с почечной недостаточностью увеличивается экспозиция эноксапарина натрия. За состоянием таких пациентов следует установить внимательное наблюдение на предмет развития признаков и симптомов кровотечения. Поскольку экспозиция эноксапарина натрия значительно увеличивается у пациентов с тяжелой почечной недостаточностью (Cl креатинина <30 мл/мин), рекомендуется корректировка терапевтических и профилактических доз. У пациентов с Cl креатинина от 30 до <50 мл/мин и от 50 до 80 мл/мин корректировка дозы не рекомендуется. У пациентов с почечной недостаточностью применение эноксапарина натрия было связано с развитием гиперкалиемии (см. «Побочные действия»).
Пациенты с низкой массой тела. У женщин и мужчин с низким весом (<45 и <57 кг соответственно) наблюдалось увеличение экспозиции эноксапарина натрия, применяемого в профилактических дозах (без корректировки в соответствии с массой тела). За состоянием таких пациентов следует установить внимательное наблюдение на предмет развития признаков и симптомов кровотечения.
Пациенты с ожирением. Пациенты с ожирением имеют более высокий риск развития тромбоэмболии. Безопасность и эффективность применения профилактических доз эноксапарина натрия у пациентов с ожирением (ИМТ >30 кг/м2) достаточно не установлены, и нет единого мнения о необходимости корректировки дозы. За состоянием таких пациентов следует установить внимательное наблюдение на предмет развития признаков и симптомов тромбоэмболии.
Представленная информация о ценах на препараты не является предложением о продаже или покупке товара.
Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в
соответствии со статьей 55 Федерального закона «Об обращении лекарственных средств» от 12.04.2010 № 61-ФЗ.
Квадрапарин-СОЛОфарм — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер:
ЛП-005947
Торговое наименование:
Квадрапарин®-СОЛОфарм
Международное непатентованное или группировочное наименование:
эноксапарин натрия
Лекарственная форма:
раствор для инъекций
Состав
1 шприц или ампула (0,2 мл) содержит:
действующее вещество: эноксапарин натрия 2000 анти-Ха ME (20 мг)
вспомогательное вещество: вода для инъекций – до 0,2 мл.
1 шприц или ампула (0,3 мл) содержит:
действующее вещество: эноксапарин натрия 3000 анти-Ха ME (30 мг)
вспомогательное вещество: вода для инъекций – до 0,3 мл.
1 шприц или ампула (0,4 мл) содержит:
действующее вещество: эноксапарин натрия 4000 анти-Ха ME (40 мг)
вспомогательное вещество: вода для инъекций – до 0,4 мл.
1 шприц или ампула (0,5 мл) содержит:
действующее вещество: эноксапарин натрия 5000 анти-Ха ME (50 мг)
вспомогательное вещество: вода для инъекций – до 0,5 мл.
1 шприц или ампула (0,6 мл) содержит:
действующее вещество: эноксапарин натрия 6000 анти-Ха ME (60 мг)
вспомогательное вещество: вода для инъекций – до 0,6 мл.
1 шприц или ампула (0,7 мл) содержит:
действующее вещество: эноксапарин натрия 7000 анти-Ха ME (70 мг)
вспомогательное вещество: вода для инъекций – до 0,7 мл.
1 шприц или ампула (0,8 мл) содержит:
действующее вещество: эноксапарин натрия 8000 анти-Ха ME (80 мг)
вспомогательное вещество: вода для инъекций – до 0,8 мл.
1 шприц или ампула (1 мл) содержит:
действующее вещество: эноксапарин натрия 10000 анти-Ха ME (100 мг)
вспомогательное вещество: вода для инъекций – до 1,0 мл.
Описание
Прозрачная бесцветная или желтоватая, или коричневато-желтоватая жидкость.
Фармакотерапевтическая группа
Антикоагулянтное средство прямого действия.
Код ATX:
В01АВ05
Фармакологические свойства
Эноксапарин натрия – низкомолекулярный гепарин со средней молекулярной массой около 4500 дальтон: менее 2000 дальтон – <20%, от 2000 до 8000 дальтон – >68%, более 8000 дальтон – <18%. Эноксапарин натрия получают с помощью щелочной деполимеризации бензилового эфира гепарина, выделенного из слизистой оболочки тонкой кишки свиньи. Его структура характеризуется невосстанавливающимся фрагментом 2-О-сульфо-4-енпиразиносуроновой кислоты и восстанавливающимся фрагментом 2-N,6-О-дисульфо-D-глюко-пиранозида. Структура эноксапарина натрия содержит около 20% (в пределах от 15 до 25%) 1,6-ангидропроизводного в восстанавливающемся фрагменте полисахаридной цепи.
Фармакодинамика
В очищенной системеin vitro эноксапарин натрия обладает высокой анти-Ха активностью (примерно 100 МЕ/мл) и низкой анти-IIа или антитромбиновой активностью (примерно 28 МЕ/мл). Эта антикоагулянтная активность действует через антитромбин III (АТ-III), обеспечивая антикоагулянтную активность у людей. Кроме анти-Ха/IIа активности также выявлены дополнительные антикоагулянтные и противовоспалительные свойства эноксапарина натрия как у человека, так и на моделях животных. Это включает АТ-III зависимое ингибирование других факторов свертывания, таких как фактор VIIa, активацию высвобождения ингибитора пути тканевого фактора (ПТФ), а также снижение высвобождения фактора Виллебранда из эндотелия сосудов в кровоток. Эти факторы обеспечивают антикоагулянтный эффект эноксапарина натрия в целом.
Применение препарата в профилактических дозах незначительно изменяет активированное частичное тромбопластиновое время (АЧТВ), практически не оказывает воздействия на агрегацию тромбоцитов и на степень связывания фибриногена с рецепторами тромбоцитов.
Фармакокинетика
Биодоступность и абсорбция
Абсолютная биодоступность эноксапарина натрия при подкожном (п/к) введении, оцениваемая на основании анти-Ха активности, близка к 100%.
Средняя максимальная анти-Ха активность плазмы наблюдается через 3-5 ч после п/к введения препарата и составляет приблизительно 0,2; 0,4; 1,0 и 1,3 анти-Ха МЕ/мл после п/к введения 20 мг, 40 мг, 1 мг/кг и 1,5 мг/кг.
Внутривенное болюсное введение препарата в дозировке 30 мг, сопровождающееся незамедлительным подкожным введением препарата в дозировке 1 мг/кг каждые 12 ч, обеспечивает начальную максимальную анти-Ха активность на уровне 1,16 МЕ/мл (n=16), средняя экспозиция препарата в крови составляет приблизительно 88% от равновесного состояния, которое достигается на второй день терапии.
Фармакокинетика эноксапарина натрия в указанных режимах дозирования носит линейный характер. Вариабельность внутри и между группами пациентов низкая. После повторного подкожного введения 40 мг эноксапарина натрия один раз в сутки и подкожного введения эноксапарина натрия в дозе 1,5 мг/кг массы тела один раз в сутки у здоровых добровольцев равновесная концентрация достигается ко второму дню, причем площадь под фармакокинетической кривой в среднем на 15% выше, чем после однократного введения. После повторных подкожных введений эноксапарина натрия в суточной дозе 1 мг/кг массы тела два раза в сутки равновесная концентрация достигается через 3-4 дня, причем площадь под кривой (AUC) в среднем на 65% выше, чем после однократного введения, и средние значения максимальных концентраций составляют соответственно 1,2 МЕ/мл и 0,52 МЕ/мл. Анти-IIa активность в плазме примерно в 10 раз ниже, чем анти-Ха активность. Средняя максимальная анти-IIа активность наблюдается примерно через 3-4 часа после подкожного введения и достигает 0,13 МЕ/мл и 0,19 МЕ/мл после повторного введения 1 мг/кг массы тела при двукратном введении и 1,5 мг/кг массы тела при однократном введении соответственно.
Распределение
Объем распределения анти-Ха активности эноксапарина натрия составляет примерно 4,3 л и приближается к объему циркулирующей крови.
Выведение
Эноксапарин натрия является препаратом с низким клиренсом. После внутривенного введения в течение 6 часов в дозе 1,5 мг/кг массы тела среднее значение клиренса анти-Ха в плазме составляет 0,74 л/час.
Выведение препарата носит монофазный характер с периодом полувыведения (Т1/2) около 5 часов (после однократного подкожного введения) и около 7 часов (после многократного введения препарата).
Эноксапарин натрия в основном метаболизируется в печени путем десульфатирования и/или деполимеризации с образованием низкомолекулярных веществ с очень низкой биологической активностью. Выведение через почки активных фрагментов препарата составляет примерно 10% от введенной дозы, и общая экскреция активных и неактивных фрагментов составляет примерно 40% от введенной дозы.
Особые группы пациентов
Пациенты пожилого возраста (старше 75 лет): фармакокинетический профиль эноксапарина натрия не отличается у пациентов пожилого возраста и более молодых пациентов при нормальной функции почек. Однако в результате снижения функции почек с возрастом может наблюдаться замедление выведения эноксапарина натрия у пациентов пожилого возраста.
Нарушения функции печени: в исследовании с участием пациентов с поздними стадиями цирроза печени, получавших эноксапарин натрия в дозировке 4000 ME (40 мг) один раз в сутки, снижение максимальной анти-Ха активности было связано с увеличением степени тяжести нарушения функции печени (с оценкой по шкале Чайлд-Пью). Это снижение, главным образом, было обусловлено снижением уровня AT-III, вторичным по отношению к снижению синтеза АТ-III у пациентов с нарушением функции печени.
Нарушение функции почек: отмечено уменьшение клиренса эноксапарина натрия у пациентов с нарушениями функции почек. После повторного подкожного введения 40 мг эноксапарина натрия один раз в сутки происходит увеличение активности анти-Ха, представленной площадью под фармакокинетической кривой (AUC) у пациентов с нарушениями функции почек легкой (клиренс креатинина ≥50 и <80 мл/мин) и умеренной степени и тяжести (клиренс креатинина ≥30 и <50 мл/мин). У пациентов с тяжелым нарушением функции почек (клиренс креатинина менее 30 мл/мин) AUC в состоянии равновесия в среднем на 65% выше при повторном подкожном введении 40 мг препарата один раз в сутки.
Гемодиализ: фармакокинетика эноксапарина натрия сопоставима с показателями в контрольной популяции после однократных внутривенных введений доз 25 ME, 50 ME или 100 МЕ/кг (0,25, 0,50 или 1,0 мг/кг), однако AUC была в два раза выше, чем в контрольной популяции.
Масса тела: после повторных подкожных введений в дозировке 1,5 мг/кг один раз в сутки средняя AUC анти-Ха активности в состоянии равновесия незначительно выше у пациентов с избыточной массой тела (ИМТ 30-48 кг/м²) по сравнению с пациентами с обычной средней массой тела, в то время как максимальная анти-Ха активность плазмы крови не увеличивается. У пациентов с избыточной массой тела при подкожном введении препарата клиренс несколько меньше. Если не делать поправку дозы с учетом массы тела пациента, то после однократного подкожного введения 40 мг эноксапарина натрия анти-Ха активность будет на 52% выше у женщин с массой тела менее 45 кг и на 27% выше у мужчин с массой тела менее 57 кг по сравнению с пациентами с обычной средней массой тела.
Показания к применению
- Профилактика венозных тромбозов и эмболий при хирургических вмешательствах у пациентов умеренного и высокого риска, особенно при ортопедических и общехирургических вмешательствах, включая онкологические;
- Профилактика венозных тромбозов и эмболий у пациентов, находящихся на постельном режиме вследствие острых терапевтических заболеваний, включая острую сердечную недостаточность и декомпенсацию хронической сердечной недостаточности (III или IV класс NYHA), дыхательную недостаточность, а также при тяжелых инфекциях и ревматических заболеваниях при повышенном риске венозного тромбообразования (см. раздел «Особые указания»);
- Лечение тромбоза глубоких вен с тромбоэмболией легочной артерии или без тромбоэмболии легочной артерии, кроме случаев тромбоэмболии легочной артерии, требующих тромбоэмболической терапии или хирургического вмешательства;
- Профилактика тромбообразования в системе экстракорпорального кровообращения во время гемодиализа;
- Острый коронарный синдром:
— лечение нестабильной стенокардии и инфаркта миокарда без подъема сегмента ST в сочетании с пероральным приемом ацетилсалициловой кислоты;
— лечение острого инфаркта миокарда с подъемом сегмента ST у пациентов, подлежащих медикаментозному лечению или последующему чрескожному коронарному вмешательству (ЧКВ).
Противопоказания
- повышенная чувствительность к эноксапарину натрия, гепарину или его производным, включая другие низкомолекулярные гепарины;
- активное клинически значимое кровотечение, а также состояния и заболевания, при которых имеется высокий риск развития кровотечения, включая недавно перенесенный геморрагический инсульт, острую язву желудочно-кишечного тракта (ЖКТ), наличие злокачественного новообразования с высоким риском кровотечений, недавно перенесенные операции на головном и спинном мозге, офтальмологические операции, известное или предполагаемое наличие варикозного расширения вен пищевода, артериовенозные мальформации, сосудистые аневризмы, сосудистые аномалии спинного и головного мозга;
- спинальная или эпидуральная анестезия или локо-региональная анестезия, когда эноксапарин натрия применялся для лечения в предыдущие 24 часа;
- иммуноопосредованная гепарин-индуцированная громбоцитопения (в анамнезе) в течение 100 последних дней или наличие в крови циркулирующих антитромбицитарных антител;
- детский возраст до 18 лет, так как эффективность и безопасность у данной категории пациентов не установлены (см. раздел «Особые указания»).
С осторожностью
Состояния, при которых имеется потенциальный риск развития кровотечения:
- нарушения гемостаза (в т.ч. гемофилия, тромбоцитопения, гипокоагуляция, болезнь Виллебранда и др.), тяжелый васкулит;
- язвенная болезнь желудка или двенадцатиперстной кишки или другие эрозивно-язвенные поражения желудочно-кишечного тракта в анамнезе;
- недавно перенесенный ишемический инсульт;
- неконтролируемая тяжелая артериальная гипертензия;
- диабетическая или геморрагическая ретинопатия;
- тяжелый сахарный диабет;
- недавно перенесенная или предполагаемая неврологическая или офтальмологическая операция;
- проведение спинальной или эпидуральной анестезии (потенциальная опасность развития гематомы), спинномозговая пункция (недавно перенесенная);
- недавние роды;
- эндокардит бактериальный (острый или подострый);
- перикардит или перикардиальный выпот;
- почечная и/или печеночная недостаточность;
- внутриматочная контрацепция (ВМК);
- тяжелая травма (особенно центральной нервной системы), открытые раны на больших поверхностях;
- одновременный прием препаратов, влияющих на систему гемостаза;
- гепарин-индуцированная тромбоцитопения без циркулирующих антител в анамнезе (более 100 дней).
Отсутствуют данные по клиническому применению эноксапарина натрия при следующих заболеваниях: активный туберкулез, лучевая терапия (недавно перенесенная).
Применение при беременности и в период грудного вскармливания
Беременность
Сведений о том, что эноксапарин натрия проникает через плацентарный барьер во время беременности, нет. Так как отсутствуют адекватные и хорошо контролируемые исследования с участием беременных женщин, а исследования на животных не всегда прогнозируют реакцию на введение эноксапарина натрия во время беременности у человека, применять его во время беременности следует только в исключительных случаях, когда имеется настоятельная необходимость его применения, установленная врачом.
Рекомендуется проведение контроля за состоянием пациенток на предмет появления признаков кровотечения или чрезмерной антикоагуляции, пациентки должны быть предупреждены о риске возникновения кровотечений.
Нет данных о повышенном риске развития кровотечений, тромбоцитопении или остеопороза у беременных женщин, за исключением случаев, отмеченных у пациенток с искусственными клапанами сердца (см. раздел «Особые указания»).
При планировании эпидуральной анестезии рекомендуется перед ее проведением отменить эноксапарин натрия (см. раздел «Особые указания»).
Период грудного вскармливания
Неизвестно, экскретируется ли неизмененный эноксапарин натрия в грудное молоко. Всасывание эноксапарина натрия в ЖКТ у новорожденного маловероятно. Препарат может применяться в период грудного вскармливания.
Способ применения и дозы
Подкожно, за исключением особых случаев (см. ниже подразделы «Профилактика тромбообразования в системе экстракорпорального кровообращения при проведении гемодиализа» и «Лечение острого инфаркта миокарда с подъемом сегмента ST, медикаментозное или с помощью чрескожного коронарного вмешательства»).
Профилактика венозных тромбозов и эмболии при хирургических вмешательствах у пациентов умеренного и высокого риска
Пациентам с умеренным риском развития тромбозов и эмболий (например, абдоминальные операции) рекомендуемая доза препарата составляет 20 мг один раз в сутки подкожно. Первую инъекцию следует сделать за 2 ч до хирургического вмешательства.
Пациентам с высоким риском развития тромбозов и эмболий (например, при ортопедических операциях, хирургических операциях в онкологии, пациентам с дополнительными факторами риска, не связанными с операцией, такими как врожденная или приобретенная тромбофилия, злокачественное новообразование, постельный режим более трех суток, ожирение, венозный тромбоз в анамнезе, варикозное расширение вен нижних конечностей, беременность) препарат рекомендуется в дозе 40 мг один раз в сутки подкожно, с введением первой дозы за 12 ч до хирургического вмешательства. При необходимости более ранней предоперационной профилактики (например, у пациентов с высоким риском развития тромбозов и тромбоэмболий, ожидающих отсроченную ортопедическую операцию) последняя инъекция должна быть сделана за 12 ч до операции и через 12 ч после операции.
Длительность лечения препаратом в среднем составляет 7-10 дней. При необходимости терапию можно продолжать до тех пор, пока сохраняется риск развития тромбоза и эмболии, и до тех пор, пока пациент не перейдет на амбулаторный режим.
При крупных ортопедических операциях может быть целесообразно после начальной терапии продолжение лечения путем введения препарата в дозе 40 мг один раз в сутки в течение пяти недель.
Для пациентов с высоким риском венозных тромбоэмболий, перенесших хирургическое вмешательство, абдоминальную и тазовую хирургию по причине онкологического заболевания, может быть целесообразно увеличение продолжительности введения препарата в дозе 40 мг один раз в сутки в течение четырех недель.
Профилактика венозных тромбозов и эмболий у пациентов, находящихся на постельном режиме вследствие острых терапевтических заболеваний
Рекомендуемая доза препарата составляет 40 мг один раз в сутки, подкожно, как минимум в течение 6-14 дней. Терапию следует продолжать до полного перехода пациента на амбулаторный режим (максимально в течение 14 дней).
Лечение тромбоза глубоких вен с тромбоэмболией легочной артерии или без тромбоэмболии легочной артерии
Препарат вводится подкожно из расчета 1,5 мг/кг массы тела один раз в сутки или 1 мг/кг массы тела два раза в сутки. Режим дозирования должен выбираться врачом на основе оценки риска развития тромбоэмболии и риска развития кровотечений. У пациентов без тромбоэмболических осложнений и с низким риском развития венозной тромбоэмболии препарат рекомендуется вводить подкожно из расчета 1,5 мг/кг массы тела один раз в сутки. У всех других пациентов, включая пациентов с ожирением, симптоматической тромбоэмболией легочных артерий, раком, повторной венозной тромбоэмболией и проксимальным тромбозом (в подвздошной вене) препарат рекомендуется применять в дозе 1 мг/кг два раза в сутки.
Длительность лечения в среднем составляет 10 дней. Следует сразу же начать терапию непрямыми антикоагулянтами, при этом лечение препаратом необходимо продолжать до достижения терапевтического антикоагулянтного эффекта (значения МНО [Международного Нормализованного Отношения] должны составлять 2,0-3,0).
Профилактика тромбообразования в системе экстракорпорального кровообращения во время гемодиализа
Рекомендуемая доза препарата составляет в среднем 1 мг/кг массы тела. При высоком риске развития кровотечения дозу следует снизить до 0,5 мг/кг массы тела при двойном сосудистом доступе или до 0,75 мг при одинарном сосудистом доступе.
При гемодиализе эноксапарин натрия следует вводить в артериальный участок шунта в начале сеанса гемодиализа. Одной дозы, как правило, достаточно для четырехчасового сеанса, однако при обнаружении фибриновых колец при более продолжительном гемодиализе можно дополнительно ввести препарат из расчета 0,5-1 мг/кг массы тела.
Данные в отношении пациентов, применяющих эноксапарин натрия для профилактики или лечения и во время сеансов гемодиализа, отсутствуют.
Лечение нестабильной стенокардии и инфаркта миокарда без подъема сегмента ST
Препарат вводится из расчета 1 мг/кг массы тела каждые 12 ч, подкожно, при одновременном применении антитромбоцитарной терапии. Средняя продолжительность терапии составляет, как минимум, 2 дня и продолжается до стабилизации клинического состояния пациента. Обычно введение препарата продолжается от 2 до 8 дней.
Ацетилсалициловая кислота рекомендуется всем пациентам, не имеющим противопоказаний, с начальной дозой 150-300 мг внутрь с последующей поддерживающей дозой 75-325 мг один раз в сутки.
Лечение острого инфаркта миокарда с подъемом сегмента ST, медикаментозное или с помощью чрескожного коронарного вмешательства
Лечение начинают с однократного внутривенного болюсного введения эноксапарина натрия в дозе 30 мг. Сразу же после него подкожно вводят эноксапарин натрия в дозе 1 мг/кг массы тела. Далее препарат назначают подкожно по 1 мг/кг массы тела каждые 12 ч (максимально 100 мг эноксапарина натрия для каждой из первых двух подкожных инъекций, затем – по 1 мг/кг массы тела для оставшихся подкожных доз, то есть при массе тела более 100 кг разовая доза не может превышать 100 мг). Как можно скорее после выявления острого инфаркта миокарда с подъемом сегмента ST пациентам необходимо назначить одновременно ацетилсалициловую кислоту и, если нет противопоказаний, прием ацетилсалициловой кислоты (в дозах 75-325 мг) следует продолжать ежедневно в течение не менее 30 дней.
Рекомендуемая продолжительность лечения препаратом составляет 8 дней или до выписки пациента из стационара (если период госпитализации составляет менее 8 дней).
При комбинации с тромболитиками (фибрин-специфическими и фибрин-неспецифическими) эноксапарин натрия должен вводиться в интервале от 15 мин до начала тромболитической терапии и до 30 минут после нее.
У пациентов в возрасте 75 лет и старше не применяется начальное внутривенное болюсное введение. Препарат вводят подкожно в дозе 0,75 мг/кг каждые 12 ч (максимально 75 мг эноксапарина натрия для каждой из первых двух подкожных инъекций, затем – по 0,75 мг/кг массы тела для оставшихся подкожных доз, то есть при массе тела более 100 кг разовая доза не может превышать 75 мг).
У пациентов, которым проводится чрескожное коронарное вмешательство, в случае, если последняя подкожная инъекция эноксапарина натрия была проведена менее чем за 8 ч до раздувания введенного в место сужения коронарной артерии баллонного катетера, дополнительного введения эноксапарина натрия не требуется. Если же последняя подкожная инъекция эноксапарина натрия проводилась более чем за 8 ч до раздувания баллонного катетера, следует произвести дополнительное внутривенное болюсное введение эноксапарина натрия в дозе 0,3 мг/кг.
Особенности введения препарата
Предварительно заполненный одноразовый шприц готов к применению.
Препарат нельзя вводить внутримышечно!
Подкожное введение
Инъекции желательно проводить в положении пациента «лежа». При использовании предварительно заполненных шприцев во избежание потери препарата перед инъекцией не надо удалять пузырьки воздуха из шприца. Инъекции следует проводить поочередно в левую или правую переднелатеральную или заднелатеральную поверхность живота.
Иглу необходимо вводить на всю длину вертикально (не сбоку) в кожную складку, собранную и удерживаемую до завершения инъекции между большим и указательным пальцами. Складку кожи отпускают только после завершения инъекции.
Не следует массировать место инъекции после введения препарата.
Внутривенное болюсное введение
Внутривенное болюсное введение эноксапарина натрия должно проводиться через венозный катетер. Эноксапарин натрия не должен смешиваться или вводиться вместе с другими лекарственными препаратами. Для того, чтобы избежать присутствия в инфузионной системе следов других лекарственных препаратов и их взаимодействия с эноксапарином натрия, венозный катетер должен промываться достаточным количеством 0,9% раствора натрия хлорида или 5% раствора декстрозы до и после внутривенного болюсного введения эноксапарина натрия. Эноксапарин натрия может безопасно вводиться с 0,9% раствором натрия хлорида и 5% раствором декстрозы.
Для проведения болюсного введения 30 мг эноксапарина натрия при лечении острого инфаркта миокарда с подъемом сегмента ST из стеклянных шприцев большего объема удаляют лишнее количество препарата с тем, чтобы в них оставалось только 30 мг (0,3 мл). Доза 30 мг может непосредственно вводиться внутривенно.
Для проведения внутривенного болюсного введения эноксапарина натрия через венозный катетер могут использоваться предварительно заполненные шприцы для подкожного введения препарата 30 мг, 40 мг, 50 мг, 60 мг, 70 мг, 80 мг и 100 мг. Рекомендуется использовать шприцы 30 мг, 40 мг, 50 мг и 60 мг, так как это уменьшает количество удаляемого из шприца препарата. Шприцы 20 мг не используются, так как в них недостаточно препарата для болюсного введения 30 мг эноксапарина натрия.
Для повышения точности дополнительного внутривенного болюсного введения малых объемов в венозный катетер при проведении чрескожных коронарных вмешательств рекомендуется развести препарат до концентрации 3 мг/мл. Разведение раствора рекомендуется проводить непосредственно перед введением.
Для получения раствора эноксапарина натрия с концентрацией 3 мг/мл с помощью предварительно заполненного шприца 60 мг рекомендуется использовать емкость с инфузионным раствором 50 мл (то есть с 0,9% раствором натрия хлорида или 5% раствором дектрозы). Из емкости с инфузионным раствором с помощью обычного шприца извлекается и удаляется 30 мл раствора. Эноксапарин натрия (содержимое шприца для подкожного введения 60 мг) вводится в оставшиеся в емкости 20 мл инфузионного раствора. Содержимое емкости с разведенным раствором эноксапарина натрия осторожно перемешивается. Для введения с помощью шприца извлекается необходимый объем разведенного раствора эноксапарина натрия, который рассчитывается по формуле:
Объем разведенного раствора = Масса тела пациента (кг) × 0,1,
или с помощью представленной ниже таблицы.
Объемы, которые должны вводиться внутривенно после разведения до концентрации 3 мг/мл
| Масса тела пациента (кг) | Необходимая доза (0,3 мг/кг) [мг] |
Необходимый для введения объем раствора, разведенного до концентрации 3 мг/мл [мл] |
| 45 | 13,5 | 4,5 |
| 50 | 15 | 5 |
| 55 | 16,5 | 5,5 |
| 60 | 18 | 6 |
| 65 | 19,5 | 6,5 |
| 70 | 21 | 7 |
| 75 | 22,5 | 7,5 |
| 80 | 24 | 8 |
| 85 | 25,5 | 8,5 |
| 90 | 27 | 9 |
| 95 | 28,5 | 9,5 |
| 100 | 30 | 10 |
| 105 | 31,5 | 10,5 |
| 110 | 33 | 11 |
| 115 | 34,5 | 11,5 |
| 120 | 36 | 12 |
| 125 | 37,5 | 12,5 |
| 130 | 39 | 13 |
| 135 | 40,5 | 13,5 |
| 140 | 42 | 14 |
| 145 | 43,5 | 14,5 |
| 150 | 45 | 15 |
Переключение между эноксапарином натрия и пероральными антикоагулянтами
Переключение между эноксапарином натрия и антагонистами витамина К (АВК)
Для мониторирования эффекта АВК необходимо наблюдение врача и проведение лабораторных исследований [протромбиновое время, представленное как МНО].
Так как для развития максимального эффекта АВК требуется время, терапия эноксапарином натрия должна продолжаться в постоянной дозе так долго, как необходимо для поддержания значений МНО (по данным двух последовательных определений) в желаемом терапевтическом диапазоне в зависимости от показаний.
Для пациентов, которые получают АВК, отмена АВК и введение первой дозы эноксапарина натрия должны проводиться после того, как МНО снизилось ниже границы терапевтического диапазона.
Переключение между эноксапарином натрия и пероральными антикоагулянтами прямого действия (ПОАК)
Отмена эноксапарина натрия и назначение ПОАК должны проводиться за 0-2 ч до момента очередного запланированного введения эноксапарина натрия в соответствии с инструкцией по применению пероральных антикоагулянтов.
Для пациентов, получающих ПОАК, введение первой дозы эноксапарина натрия и отмена пероральных антикоагулянтов прямого действия должны проводиться в момент времени, соответствующий очередному запланированному применению ПОАК.
Применение при спинальной/эпидуральной анестезии или люмбальной пункции
В случае применения антикоагулянтной терапии во время проведения эпидуральной или спинальной анестезии/анальгезии или люмбальной пункции необходимо проведение неврологического мониторирования вследствие риска развития нейроаксиальных гематом (см. раздел «Особые указания»).
Применение эноксапарина натрия в профилактических дозах
Установка или удаление катетера должно проводиться спустя как минимум 12 ч после последней инъекции профилактической дозы эноксапарина натрия.
При использовании непрерывной техники необходимо соблюдать по меньшей мере 12 ч интервал до удаления катетера.
У пациентов с клиренсом креатинина ≥15 и <30 мл/мин следует рассмотреть вопрос об удвоении времени до момента пункции или введения/удаления катетера как минимум до 24 ч.
Предоперационное введение эноксапарина натрия за 2 ч до вмешательства в дозировке 20 мг несовместимо с проведением нейроаксиальной анестезии.
Применение эноксапарина натрия в терапевтических дозах
Установка или удаление катетера должно проводиться спустя как минимум через 24 ч после последней инъекции терапевтической дозы эноксапарина натрия (см. раздел «Противопоказания»).
При использовании непрерывной техники необходимо соблюдать по меньшей мере 24 ч интервал до удаления катетера.
У пациентов с клиренсом креатинина ≥15 и <30 мл/мин следует рассмотреть вопрос об удвоении времени до момента пункции или введения/удаления катетера как минимум до 48 ч.
Пациентам, получающим эноксапарин натрия в дозах 0,75 мг/кг или 1 мг/кг массы тела 2 раза в сутки, не следует вводить вторую дозу препарата с целью увеличения интервала перед установкой или заменой катетера. Точно так же следует рассмотреть вопрос о возможности отсрочки введения следующей дозы препарата как минимум на 4 ч, исходя из оценки соотношения польза/риск (риск развития тромбоза и кровотечений при проведении процедуры с учетом наличия у пациентов факторов риска). В эти временные точки все еще продолжает выявляться анти-Ха активность препарата, и отсрочки по времени не являются гарантией того, что развития нейроаксиальной гематомы удастся избежать.
Режим дозирования у особых групп пациентов
Дети до 18 лет
Безопасность и эффективность применения эноксапарина натрия у детей не установлены.
Пациенты пожилого возраста (старше 75 лет)
За исключением лечения инфаркта миокарда с подъемом сегмента ST для всех других показаний снижения доз эноксапарина натрия у пациентов пожилого возраста при отсутствии нарушений функции почек не требуется.
Пациенты с нарушениями функции почек
Тяжелые нарушения функции почек (клиренс креатинина ≥15 и <30 мл/мин)
Применение эноксапарина натрия не рекомендуется пациентам с терминальной стадией хронической болезни почек (клиренс креатинина <15 мл/мин) ввиду отсутствия данных, кроме случаев профилактики тромбообразования в системе экстракорпорального кровообращения во время гемодиализа.
У пациентов с тяжелыми нарушениями функции почек (клиренс креатинина ≥15 и <30 мл/мин) доза эноксапарина натрия снижается в соответствии с представленными ниже таблицами, так как у этих пациентов отмечается увеличение системной экспозиции (продолжительности действия) препарата.
При применении препарата в терапевтических дозах рекомендуется следующая коррекция режима дозирования:
| Обычный режим дозирования | Режим дозирования при тяжелой почечной недостаточности |
| 1 мг/кг массы тела подкожно 2 раза в сутки | 1 мг/кг массы тела подкожно 1 раз в сутки |
| 1,5 мг/кг массы тела подкожно 1 раз в сутки | 1 мг/кг массы тела подкожно 1 раз в сутки |
| Лечение острого инфаркта миокарда с подъемом сегмента ST у пациентов моложе 75 лет | |
| Однократно внутривенное болюсное введение 30 мг плюс 1 мг/кг массы тела подкожно; с последующим подкожным введением в дозе 1 мг/кг массы тела 2 раза в сутки (максимально 100 мг для каждой из двух первых подкожных инъекций) | Однократно внутривенное болюсное введение 30 мг плюс 1 мг/кг массы тела подкожно; с последующим подкожным введением в дозе 1 мг/кг массы тела 1 раз в сутки (максимально 100 мг только для первой подкожной инъекции) |
| Лечение острого инфаркта миокарда с подъемом сегмента ST у пациентов в возрасте 75 лет и старше | |
| 0,75 мг/кг массы тела подкожно 2 раза в сутки без начального внутривенного болюсного введения (максимально 75 мг для каждой из двух первых подкожных инъекций) | 1 мг/кг массы тела подкожно 1 раз в сутки без начального внутривенного болюсного введения (максимально 100 мг только для первой подкожной инъекции) |
При применении препарата с профилактической целью рекомендуется коррекция режима дозирования, представленная в таблице ниже:
| Обычный режим дозирования | Режим дозирования при тяжелой почечной недостаточности |
| 40 мг подкожно 1 раз в сутки | 20 мг подкожно 1 раз в сутки |
| 20 мг подкожно 1 раз в сутки | 20 мг подкожно 1 раз в сутки |
Рекомендованная коррекция режима дозирования не применяется при гемодиализе.
Нарушения функции почек легкой (клиренс креатинина ≥50 и <80 мл/мин) и умеренной (клиренс креатинина ≥30 и <50 мл/мин) степени тяжести
Коррекции дозы не требуется, однако пациенты должны находиться под тщательным наблюдением врача.
Пациенты с нарушениями функции печени
В связи с отсутствием клинических исследований препарат следует применять с осторожностью у пациентов с нарушениями функции печени.
Инструкция по самостоятельному выполнению инъекции эноксапарина натрия
- Вымойте руки и участок кожи (место для инъекции), в который Вы будете вводить препарат, водой с мылом. Высушите их.
- Примите удобное положение «сидя» или «лежа» и расслабьтесь. Убедитесь, что Вы хорошо видите место, в которое собираетесь вводить препарат. Оптимально использовать кресло для отдыха, шезлонг или кровать, обложенную подушками для опоры.
- Выберите место для проведения инъекции в правой или левой части живота. Это место должно находиться на расстоянии как минимум 5 см от пупка или вокруг имеющихся рубцов и кровоподтеков. Чередуйте места инъекций в правой и левой частях живота в зависимости от того, куда Вы вводили препарат в предыдущий раз.
- Протрите место для инъекции тампоном, смоченным спиртом.
- Осторожно снимите колпачок с иглы шприца с препаратом. Отложите колпачок. Шприц предварительно заполнен и готов к использованию. Не нажимайте на поршень для вытеснения пузырьков воздуха до введения иглы в место инъекции. Это может привести к потере препарата. После удаления колпачка не допускайте прикосновения иглы к каким-либо предметам. Это необходимо для сохранения стерильности иглы.
Внимание: при наличии защитной этикетки для иглы – следуйте Инструкции по использованию защитной этикетки для иглы, приведенной ниже. - Удерживайте шприц в одной руке так, как Вы держите карандаш, а другой рукой осторожно сожмите протертое спиртом место для введения препарата между большим и указательным пальцами так, чтобы образовать складку кожи. Удерживайте кожную складку все время, пока Вы вводите препарат.
- Удерживайте шприц таким образом, чтобы игла была направлена вниз (вертикально под углом 90°). Введите иглу на всю длину в кожную складку.
- Нажмите пальцем на поршень. Это обеспечит введение препарата в подкожную жировую ткань живота. Удерживайте кожную складку все время, пока вы вводите препарат.
- Извлеките иглу, потянув ее назад без отклонения от оси. Теперь можно прекратить удержание кожной складки.
Внимание: при наличии устройства предохранительного – следуйте Инструкции по использованию устройства предохранительного, приведенной ниже. - В целях предотвращения образования кровоподтека не растирайте место инъекции после введения препарата.
- Утилизируйте использованный одноразовый шприц в мусорный контейнер.
При применении препарата строго придерживайтесь рекомендаций, представленных в данной инструкции, а также указаний врача или провизора. При возникновении вопросов обратитесь к врачу или провизору.
Инструкция по использованию защитной этикетки для иглы (при ее наличии)
Не вскрывая упаковку, проверьте целостность шприца, а также отсутствие жидкости в контурной ячейковой упаковке. Если Вы сомневаетесь в целостности шприца или его герметичности, возьмите другую упаковку.
Откройте контурную ячейковую упаковку.
Проверьте содержание препарата в шприце.
- Внимание: не снимайте защитный колпачок до изгиба защитной этикетки!
Согните защитную этикетку для иглы в сторону приблизительно на 90°.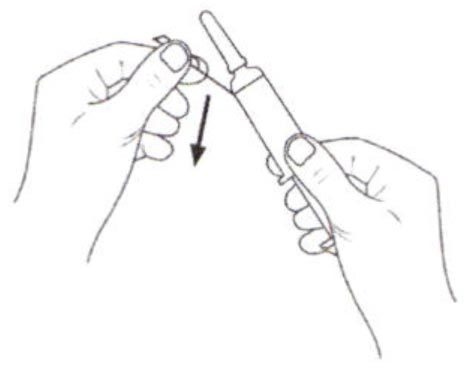
- Снимите защитный колпачок.
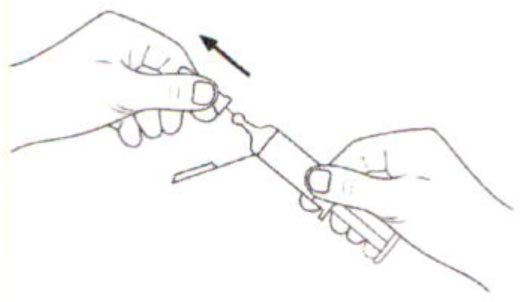
- Сделайте инъекцию, как обычно.
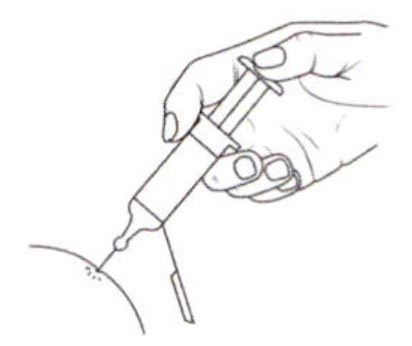
- Внимание: не закрепляйте иглу в защитную этикетку пальцами!
Одной рукой закрепите иглу путем размещения защитной этикетки на жесткой устойчивой поверхности. Затем нажмите на защитную этикетку.
- Согните защитную этикетку приблизительно на 90° до тех пор, пока игла со слышимым щелчком не окажется в пластиковой части защитной этикетки.
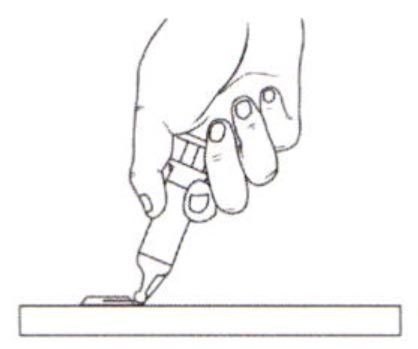
- Утилизируйте одноразовый шприц с иглой в мусорный контейнер.
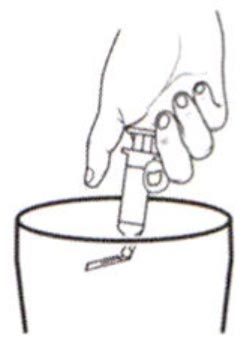
Инструкция по использованию устройства предохранительного
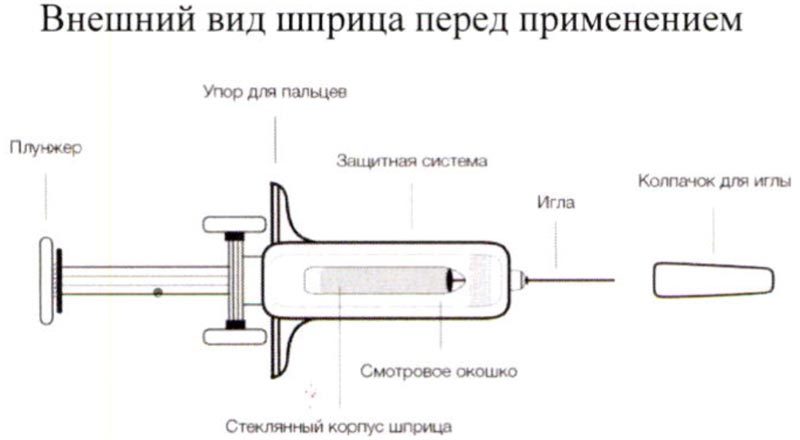
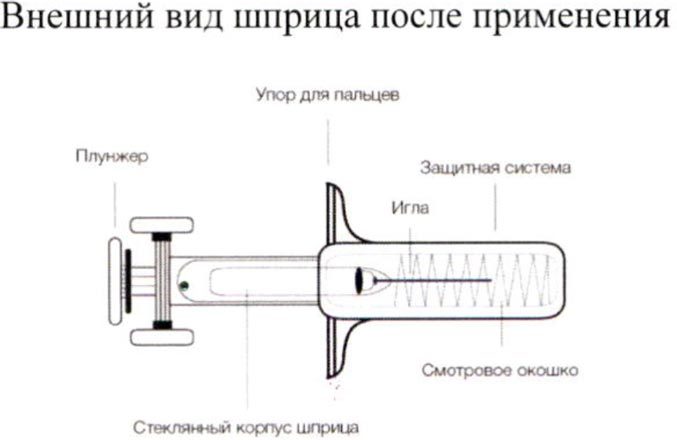
Не вскрывая упаковку, проверьте целостность шприца, а также отсутствие жидкости в контурной ячейковой упаковке. Если Вы сомневаетесь в целостности шприца или его герметичности, возьмите другую упаковку.
Откройте контурную ячейковую упаковку.
Проверьте содержание препарата в шприце.
- Внимание: Вынимая шприц из упаковки, не тяните шприц за плунжер или колпачок для иглы. Выньте шприц из упаковки, как показано на рисунке.

- Внимание: Не снимайте колпачок иглы, держась за плунжер или основание иглы.
Снимите колпачок иглы, как показано на рисунке, держась за защитную систему во избежание травмирования или изгиба иглы.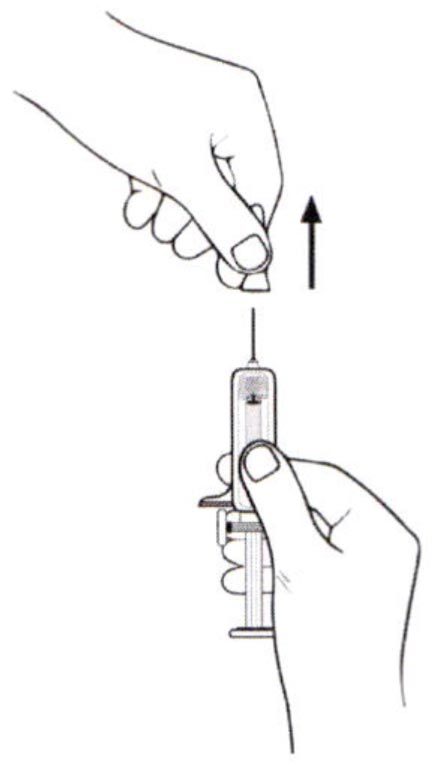
- Сделайте инъекцию, как обычно.
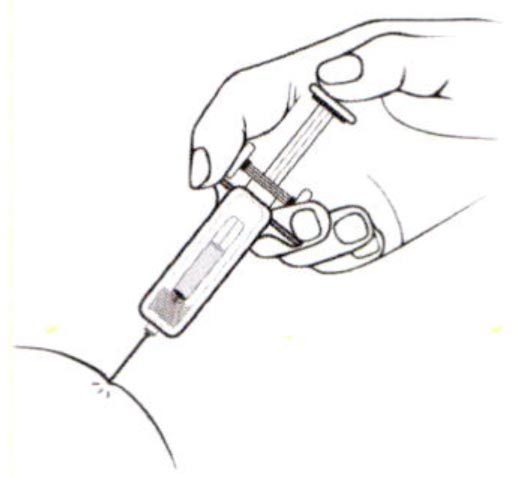
- Зажав корпус шприца между указательным и средним пальцами, надавите на плунжер вниз до упора, чтобы ввести весь раствор.
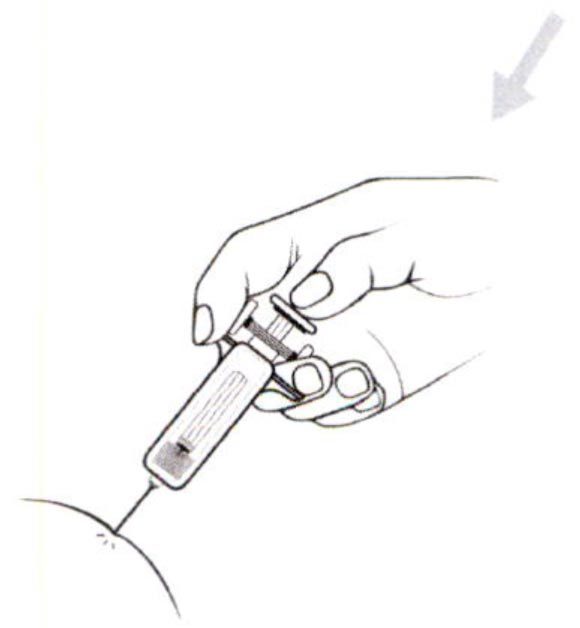
Внимание: Раствор должен быть введен полностью для срабатывания защитной системы. - После завершения инъекции воспользуйтесь одним из предложенных вариантов:
1) Выньте иглу из места инъекции и отпустите плунжер. Дождитесь пока защитная система полностью закроет иглу.
2) Не вынимая иглу из места инъекции, отпустите плунжер. Дождитесь пока защитная система полностью закроет иглу.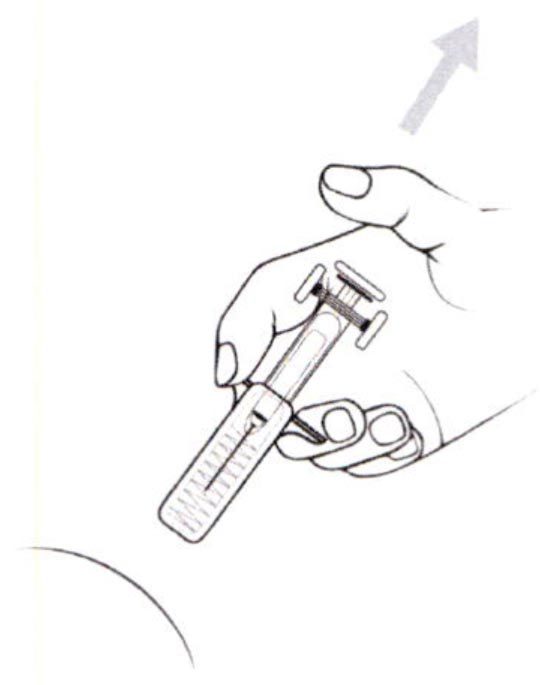
- Внимание: Если защитная система не активировалась или активировалась частично – выбросите шприц с незащищенной иглой. Т.к. игла не защищена, обратите особое внимание на то, чтобы избежать травм. Выбросите шприц с защищенной иглой в мусорный контейнер.
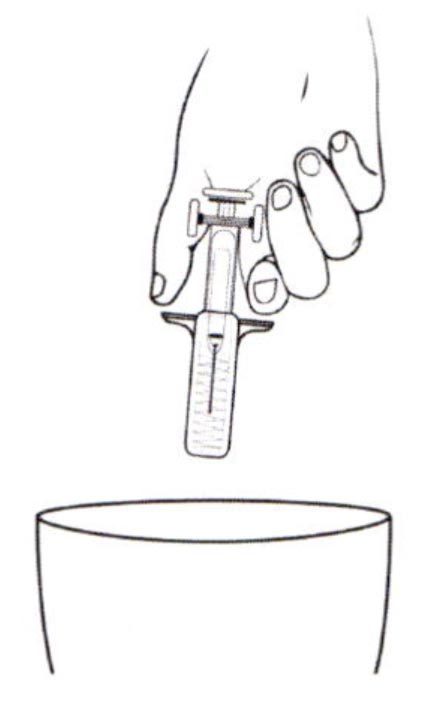
Побочное действие
Изучение побочных эффектов эноксапарина натрия проводилось более чем у 15000 пациентов, участвовавших в клинических исследованиях, из них у 1776 пациентов – при профилактике венозных тромбозов и эмболий при общехирургических и ортопедических операциях; у 1169 пациентов – при профилактике венозных тромбозов и эмболий у пациентов, находящихся на постельном режиме вследствие острых терапевтических заболеваний; у 559 пациентов – при лечении тромбоза глубоких вен с тромбоэмболией легочной артерии или без тромбоэмболии легочной артерии; у 1578 пациентов – при лечении нестабильной стенокардии и инфаркта миокарда без зубца Q; у 10176 пациентов – при лечении инфаркта миокарда с подъемом сегмента ST.
Режим введения эноксапарина натрия отличался в зависимости от показаний. При профилактике венозных тромбозов и эмболий при общехирургических и ортопедических операциях или у пациентов, находящихся на постельном режиме, вводилось 40 мг подкожно 1 раз в сутки. При лечении тромбоза глубоких вен с тромбоэмболией легочной артерии или без нее, пациенты получали эноксапарин натрия из расчета 1 мг/кг массы тела подкожно каждые 12 ч или 1,5 мг/кг массы тела подкожно 1 раз в сутки. При лечении нестабильной стенокардии и инфаркта миокарда без зубца Q доза эноксапарина натрия составляла 1 мг/кг массы тела подкожно каждые 12 ч, а в случае инфаркта миокарда с подъемом сегмента ST проводилось внутривенное болюсное введение 30 мг с последующим введением 1 мг/кг массы тела подкожно каждые 12 ч.
Частота возникновения нежелательных реакций определялась в соответствии с классификацией ВОЗ: очень часто (≥1/10); часто (≥1/100 и <1/10); нечасто (≥1/1000 и <1/100); редко (≥1/10000 и <1/1000); очень редко (<1/10000), частота неизвестна (не может быть подсчитана на основании имеющихся данных).
Нарушения со стороны сосудов:
Кровотечения
В клинических исследованиях кровотечения были наиболее часто встречающимися нежелательными реакциями. К ним относились большие кровотечения, наблюдавшиеся у 4,2% пациентов (кровотечение считалось большим, если оно сопровождалось снижением содержания гемоглобина на 2 г/л и более, требовало переливания 2 или более доз компонентов крови, а также, если оно было забрюшинным или внутричерепным). Некоторые из этих случаев были летальными.
Как и при применении других антикоагулянтов при применении эноксапарина натрия возможно возникновение кровотечения, особенно при наличии факторов риска, способствующих развитию кровотечения, при проведении инвазивных процедур или применении препаратов, нарушающих гемостаз (см. разделы «Взаимодействие с другими лекарственными средствами» и «Особые указания»).
При описании кровотечений ниже знак «*» означает указание на следующие виды кровотечений: гематома, экхимозы (кроме развившихся в месте инъекции), раневые гематомы, гематурия, носовые кровотечения, желудочно-кишечные кровотечения.
Очень часто – кровотечения* при профилактике венозных тромбозов у хирургических пациентов и лечении тромбоза глубоких вен с тромбоэмболией или без нее.
Часто – кровотечения* при профилактике венозных тромбозов у пациентов, находящихся на постельном режиме, и при лечении нестабильной стенокардии, инфаркта миокарда без зубца Q и инфаркта миокарда с подъемом сегмента ST.
Нечасто – забрюшинные кровотечения и внутричерепные кровоизлияния у пациентов при лечении тромбоза глубоких вен с тромбоэмболией легочной артерии или без нее, а также при инфаркте миокарда с подъемом сегмента ST.
Редко – забрюшинные кровотечения при профилактике венозных тромбозов у хирургических пациентов и при лечении стенокардии, инфаркта миокарда без зубца Q.
Тромбоцитопения и тромбоцитоз
Очень часто – тромбоцитоз (количество тромбоцитов в периферической крови более 400×109/л) при профилактике венозных тромбозов у хирургических пациентов и лечении тромбоза глубоких вен с тромбоэмболией легочной артерии или без нее.
Часто – тромбоцитоз при лечении пациентов с острым инфарктом миокарда с подъемом сегмента ST. Тромбоцитопения при профилактике венозных тромбозов у хирургических пациентов и лечении тромбоза глубоких вен с тромбоэмболией легочной артерии или без нее, а также при остром инфаркте миокарда с подъемом сегмента ST.
Нечасто – тромбоцитопения при профилактике венозных тромбозов у пациентов, находящихся на постельном режиме и при лечении нестабильной стенокардии, инфаркта миокарда без зубца Q.
Очень редко – аутоиммунная тромбоцитопения при лечении пациентов с острым инфарктом миокарда с подъемом сегмента ST.
Другие клинически значимые нежелательные реакции вне зависимости от показаний
Нежелательные реакции, представленные ниже, сгруппированы по системно-органным классам, даны с указанием определенной выше частоты их возникновения и в порядке уменьшения их тяжести.
Нарушения со стороны крови и лимфатической системы
Часто – кровотечение, тромбоцитопения, тромбоцитоз.
Редко – случаи развития аутоиммунной тромбоцитопении с тромбозом; в некоторых случаях тромбоз осложнялся развитием инфаркта органов или ишемии конечностей (см. раздел «Особые указания», подраздел «Контроль количества тромбоцитов в периферической крови»).
Нарушения со стороны иммунной системы
Часто – аллергические реакции.
Нарушения со стороны печени и желчевыводящих путей
Очень часто – повышение активности «печеночных» ферментов, главным образом повышение активности трансаминаз, более чем в три раза превышающее верхнюю границу нормы.
Нарушения со стороны кожи и подкожных тканей
Часто – крапивница, кожный зуд, эритема.
Нечасто – буллезный дерматит.
Общие расстройства и нарушения в месте введения
Часто – гематома в месте инъекции, боль в месте инъекции, отек в месте инъекции, кровотечение, реакции повышенной чувствительности, воспаление, образование уплотнений в месте инъекции.
Нечасто – раздражение в месте инъекции, некроз кожи в месте инъекции.
Данные, полученные в пострегистрационный период
Следующие нежелательные реакции отмечались при постмаркетинговом применении препарата. Об этих побочных реакциях имелись спонтанные сообщения.
Нарушения со стороны иммунной системы
Редко – анафилактические/анафилактоидные реакции, включая шок.
Нарушения со стороны нервной системы
Часто – головная боль.
Нарушения со стороны сосудов
Редко – при применении эноксапарина натрия на фоне спинальной/эпидуральной анестезии или спинальной пункции отмечались случаи развития спинальной гематомы (или нейроаксиальной гематомы). Эти реакции приводили к развитию неврологических нарушений различной степени тяжести, включая стойкий или необратимый паралич (см. раздел «Особые указания»).
Нарушения со стороны крови или лимфатической системы
Часто – геморрагическая анемия.
Редко – эозинофилия.
Нарушения со стороны кожи и подкожных тканей
Редко – алопеция; в месте инъекции может развиться кожный васкулит, некроз кожи, которым обычно предшествует появление пурпуры или эритематозных папул (инфильтрированных и болезненных). В этих случаях терапию препаратом следует прекратить.
Возможно образование твердых воспалительных узелков-инфильтратов в месте инъекции препарата, которые исчезают через несколько дней и не являются основанием для отмены препарата.
Нарушения со стороны печени и желчевыводящих путей
Нечасто – гепатоцеллюлярное поражение печени.
Редко – холестатическое поражение печени.
Нарушения со стороны скелетно-мышечной и соединительной ткани
Редко – остеопороз при длительной терапии (более трех месяцев).
Лабораторные и инструментальные данные
Редко – гиперкалиемия.
Передозировка
Случайная передозировка препаратом при внутривенном, экстракорпоральном или подкожном применении может привести к геморрагическим осложнениям. При приеме внутрь даже в больших дозах всасывание препарата маловероятно.
Антикоагулянтные эффекты можно в основном нейтрализовать путем медленного внутривенного введения протамина сульфата, доза которого зависит от дозы введенного препарата. Один мг (1 мг) протамина сульфата нейтрализует антикоагулянтный эффект одного мг (1 мг) препарата, если эноксапарин натрия вводился не более чем за 8 ч до введения протамина. 0,5 мг протамина нейтрализует антикоагулянтный эффект 1 мг препарата, если с момента введения последнего прошло более 8 ч или при необходимости введения второй дозы протамина. Если же после введения эноксапарина натрия прошло 12 ч и более, введения протамина не требуется. Однако даже при введении больших доз протамина сульфата, анти-Ха активность препарата полностью не нейтрализуется (максимально на 60%).
Взаимодействие с другими лекарственными средствами
Эноксапарин натрия нельзя смешивать с другими препаратами!
Нерекомендуемые комбинации
Препараты, влияющие на гемостаз (салицилаты системного действия, ацетилсалициловая кислота в дозах, оказывающих противовоспалительное действие, нестероидные противовоспалительные препараты, включая кеторолак, другие тромболитики (альтеплаза, ретеплаза, стрептокиназа, тенектеплаза, урокиназа)), рекомендуется отменить до начала терапии эноксапарином натрия. При необходимости одновременного применения с эноксапарином натрия следует соблюдать осторожность и проводить тщательное клиническое наблюдение и мониторинг соответствующих лабораторных показателей.
Комбинации, требующие соблюдения осторожности
• Прочие лекарственные препараты, влияющие на гемостаз, такие как:
— ингибиторы агрегации тромбоцитов, включая ацетилсалициловую кислоту в дозах, оказывающих антиагрегантное действие (кардиопротекция), клопидогрел, тиклопидин и антагонисты гликопротеина IIb/IIIа рецепторов, показанные при остром коронарном синдроме, вследствие повышенного риска кровотечения;
— декстран с молекулярной массой 40 кДа;
— системные глюкокортикостероиды.
• Лекарственные препараты, повышающие содержание калия
При одновременном применении с лекарственными препаратами, повышающими содержание калия в сыворотке крови, следует проводить клинический и лабораторный контроль.
Особые указания
Общие
Низкомолекулярные гепарины не являются взаимозаменяемыми, так как они различаются по процессу производства, молекулярной массе, специфической анти-Ха активности, единицам дозирования и режиму дозирования, с чем связаны различия в их фармакокинетике и биологической активности (антитромбиновая активность и взаимодействие с тромбоцитами). Поэтому требуется строго выполнять рекомендации по применению для каждого препарата, относящегося к классу низкомолекулярных гепаринов.
Кровотечение
Как и при применении других антикоагулянтов, при введении препарата возможно развитие кровотечений любой локализации (см. раздел «Побочное действие»). При развитии кровотечения необходимо найти его источник и назначить соответствующее лечение.
Эноксапарин натрия, как и другие антикоагулянты, следует применять с осторожностью при состояниях с повышенным риском кровотечения, таких как:
• нарушения гемостаза;
• язвенная болезнь в анамнезе;
• недавно перенесенный ишемический инсульт;
• тяжелая артериальная гипертензия;
• диабетическая ретинопатия;
• нейрохирургическое или офтальмологическое оперативное вмешательство;
• одновременное применение препаратов, влияющих на гемостаз (см. раздел «Взаимодействие с другими лекарственными средствами»).
Кровотечения у пациентов пожилого возраста
При применении препарата в профилактических дозах у пациентов пожилого возраста не отмечено увеличение риска развития кровотечений.
При применении препарата в терапевтических дозах у пациентов пожилого возраста (особенно в возрасте 80 лет и старше) существует повышенный риск развития кровотечений. Рекомендуется проведение тщательного наблюдения за состоянием таких пациентов (см. раздел «Фармакокинетика» и раздел «Способ применения и дозы», подраздел «Пациенты пожилого возраста»).
Одновременное применение других препаратов, влияющих на гемостаз
Применение препаратов, влияющих на гемостаз (салицилаты системного действия, в том числе ацетилсалициловая кислота в дозах, оказывающих противовоспалительное действие, нестероидные противовоспалительные препараты, включая кеторолак, другие тромболитики (альтеплаза, ретеплаза, стрептокиназа, тенектеплаза, урокиназа)), рекомендуется отменить до начала лечения эноксапарином натрия за исключением случаев, когда их применение является необходимым. Если показаны комбинации эноксапарина натрия с этими препаратами, то следует проводить тщательное клиническое наблюдение и мониторинг соответствующих лабораторных показателей.
Почечная недостаточность
У пациентов с нарушением функции почек существует риск развития кровотечения в результате увеличения системной экспозиции эноксапарина натрия.
У пациентов с тяжелыми нарушениями функции почек (клиренс креатинина ≥15 и <30 мл/мин) отмечается значительное увеличение экспозиции эноксапарина натрия, поэтому рекомендуется проводить коррекцию дозы как при профилактическом, так и терапевтическом применении препарата. Хотя не требуется проводить коррекцию дозы у пациентов с легкими и умеренными нарушениями функции почек (клиренс креатинина 30-50 мл/мин или 50-80 мл/мин), рекомендуется проведение тщательного контроля состояния таких пациентов, и может рассматриваться проведение биологического мониторинга с измерением анти-Ха активности (см. разделы «Фармакокинетика» и «Способ применения и дозы», подраздел «Пациенты с нарушениями функции почек»).
Применение эноксапарина натрия не рекомендуется пациентам с терминальной стадией хронической болезни почек (клиренс креатинина <15 мл/мин) ввиду отсутствия данных, кроме случаев профилактики тромбообразования в системе экстракорпорального кровообращения во время гемодиализа.
Низкая масса тела
Отмечалось увеличение экспозиции эноксапарина натрия при его профилактическом применении у женщин с массой тела менее 45 кг и у мужчин с массой тела менее 57 кг, что может приводить к повышенному риску развития кровотечений. Рекомендуется проведение тщательного контроля состояния таких пациентов.
Пациенты с ожирением
Пациенты с ожирением имеют повышенный риск развития тромбозов и эмболий. Безопасность и эффективность применения эноксапарина натрия в профилактических дозах у пациентов с ожирением (ИМТ более 30 кг/м²) до конца не определена и нет общего мнения по коррекции дозы. Этих пациентов следует внимательно наблюдать на предмет развития симптомов и признаков тромбозов и эмболий.
Контроль количества тромбоцитов в периферической крови
Риск развития антитело-опосредованной гепарин-индуцированной тромбоцитопении существует и при применении низкомолекулярных гепаринов, при этом этот риск выше у пациентов, перенесших операции на сердце, и пациентов с онкологическими заболеваниями. Если развивается тромбоцитопения, то ее обычно выявляют между 5-м и 21-м днями после начала терапии эноксапарином натрия. В связи с этим рекомендуется регулярно контролировать количество тромбоцитов в периферической крови до начала лечения препаратом и во время его применения. Следует определять количество тромбоцитов в крови при наличии симптомов, указывающих на ГИТ (новый эпизод артериальных и/или венозных тромбоэмболических осложнений, болезненное поражение кожи в месте инъекции, аллергическая или анафилактическая реакция при лечении). При возникновении указанных симптомов следует проинформировать лечащего врача.
При наличии подтвержденного значительного снижения количества тромбоцитов (на 30-50% по сравнению с исходным показателем) необходимо немедленно отменить эноксапарин натрия и перевести пациента на другую антикоагулянтную терапию без применения гепаринов.
Спинальная/эпидуральная анестезия
Описаны случаи возникновения нейроаксиальных гематом при применении препарата при одновременном проведении спинальной/эпидуральной анестезии с развитием длительно существующего или необратимого паралича. Риск возникновения этих явлений снижается при применении препарата в дозе 40 мг или ниже. Риск повышается при применении более высоких доз препарата, а также при использовании постоянных катетеров после операции, или при одновременном применении дополнительных препаратов, влияющих на гемостаз, таких как нестероидные противовоспалительные препараты (см. раздел «Взаимодействие с другими лекарственными средствами»). Риск также повышается при травматически проведенной или повторной спинномозговой пункции или у пациентов, имеющих в анамнезе указания на перенесенные операции в области позвоночника или деформацию позвоночника.
Для снижения возможного риска кровотечения, связанного с применением эноксапарина натрия и проведением эпидуральной или спинальной анестезии/анальгезии необходимо учитывать фармакокинетический профиль препарата (см. раздел «Фармакокинетика»). Установку или удаление катетера лучше проводить при низком антикоагулянтном эффекте эноксапарина натрия, однако точное время для достижения достаточного снижения антикоагулянтного эффекта у разных пациентов неизвестно. Следует дополнительно учитывать, что у пациентов с клиренсом креатинина 15-30 мл/мин выведение эноксапарина натрия замедляется.
Если по назначению врача применяется антикоагулянтная терапия во время проведения эпидуральной/спинальной анестезии или люмбальной пункции, необходимо постоянное наблюдение за пациентом для выявления любых неврологических симптомов, таких как боли в спине, нарушение сенсорных и моторных функций (онемение или слабость в нижних конечностях), нарушение функции кишечника и/или мочевого пузыря. Пациента необходимо проинструктировать о необходимости немедленного информирования врача при возникновении вышеописанных симптомов. При подозрении на симптомы, характерные для гематомы спинного мозга, необходимы срочная диагностика и лечение, включая, при необходимости, декомпрессию спинного мозга.
Гепарин-индуцированная тромбоцитопения
Применение эноксапарина натрия у пациентов, имеющих в анамнезе указания на наличие гепарин-индуцированной тромбоцитопении в течение последних 100 дней или при наличии циркулирующих антител, противопоказано (см. раздел «Противопоказания»). Циркулирующие антитела могут персистировать несколько лет.
Эноксапарин натрия следует применять с особой осторожностью у пациентов, имеющих в анамнезе (более чем 100 дней) гепарин-индуцированную тромбоцитопению без циркулирующих антител. Решение о применении эноксапарина натрия в данной ситуации должно быть принято только после оценки соотношения польза/риск и при отсутствии безгепариновой (не содержащей гепарин) альтернативной терапии.
Чрескожная коронарная ангиопластика
С целью минимизации риска кровотечения, связанного с инвазивной сосудистой инструментальной манипуляцией при лечении нестабильной стенокардии и инфаркта миокарда без зубца Q и острого инфаркта миокарда с подъемом сегмента ST, эти процедуры следует проводить в интервалах между введением препарата. Это необходимо для того, чтобы достигнуть гемостаза в месте введения катетера после проведения чрескожного коронарного вмешательства. При использовании закрывающего устройства интродьюсер бедренной артерии может быть удален немедленно. При применении мануальной (ручной) компрессии интродьюсер бедренной артерии следует удалить через 6 ч после последней внутривенной или подкожной инъекции эноксапарина натрия. Если лечение эноксапарином натрия продолжается, то следующую дозу следует вводить не ранее, чем через 6-8 ч после удаления интродьюсера бедренной артерии. Необходимо следить за местом введения интродьюсера, чтобы своевременно выявить признаки кровотечения и образования гематомы.
Пациенты с механическими искусственными клапанами сердца
Применение препарата для профилактики тромбообразования у пациентов с механическими искусственными клапанами сердца изучено недостаточно. Имеются отдельные сообщения о развитии тромбоза клапанов сердца у пациентов с механическими искусственными клапанами сердца на фоне терапии эноксапарином натрия для профилактики тромбообразования. Ввиду недостаточности клинических данных и наличия неоднозначных факторов, включая основное заболевание, оценка таких сообщений затруднена.
Беременные женщины с механическими искусственными клапанами сердца
Применение препарата для профилактики тромбообразования у беременных женщин с механическими искусственными клапанами сердца изучено недостаточно. В клиническом исследовании беременных женщин с механическими искусственными клапанами сердца при применении эноксапарина натрия в дозе 1 мг/кг массы тела 2 раза в сутки для уменьшения риска тромбозов и эмболий, у 2-х из 8-ми женщин образовались тромбы, приведшие к блокированию клапанов сердца и к смерти матери и плода.
Имеются отдельные постмаркетинговые сообщения о тромбозе клапанов сердца у беременных женщин с механическими искусственными клапанами сердца, получавших лечение эноксапарином для профилактики тромбообразования.
Беременные женщины с механическими искусственными клапанами сердца имеют высокий риск развития тромбоза и эмболий.
Некроз кожи/кожный васкулит
Сообщалось о развитии некроза кожи и кожного васкулита при применении низкомолекулярных гепаринов. В случае развития некроза кожи/кожного васкулита применение препарата следует прекратить.
Острый инфекционный эндокардит
Применение гепарина не рекомендуется у пациентов с острым инфекционным эндокардитом вследствие риска развития геморрагического инсульта. В случае, если применение препарата считается абсолютно необходимым, решение следует принимать только после тщательной индивидуальной оценки соотношения пользы и риска.
Лабораторные тесты
В дозах, применяемых для профилактики тромбоэмболических осложнений, препарат существенно не влияет на время кровотечения и показатели свертывания крови, а также на агрегацию тромбоцитов или на связывание их с фибриногеном.
При повышении дозы может удлиняться АЧТВ и активированное время свертывания крови. Увеличение АЧТВ и активированного времени свертывания не находятся в прямой линейной зависимости от увеличения антикоагулянтной активности препарата, поэтому нет необходимости в их мониторинге.
Гиперкалиемия
Гепарины могут подавлять секрецию альдостерона надпочечниками, что приводит к развитию гиперкалиемии, особенно у пациентов с сахарным диабетом, хронической почечной недостаточностью, предшествующим метаболическим ацидозом, принимающих лекарственные препараты, повышающие содержание калия (см. раздел «Взаимодействие с другими лекарственными препаратами»). Следует регулярно контролировать содержание калия в плазме крови, особенно у пациентов группы риска.
Профилактика венозных тромбозов и эмболий у пациентов с острыми терапевтическими заболеваниями, находящихся на постельном режиме
В случае развития острой инфекции, острых ревматических состояний профилактическое применение эноксапарина натрия оправдано только, если вышеперечисленные состояния сочетаются с одним из нижеперечисленных факторов риска венозного тромбообразования:
— возраст более 75 лет;
— злокачественные новообразования;
— тромбозы и эмболии в анамнезе;
— ожирение;
— гормональная терапия;
— сердечная недостаточность;
— хроническая дыхательная недостаточность.
Нарушение функции печени
Эноксапарин натрия следует с осторожностью применять у пациентов с нарушениями функции печени вследствие увеличения риска кровотечений. Коррекция дозы на основании мониторирования анти-Ха активности у пациентов с циррозом печени является ненадежной и не рекомендуется.
Влияние на способность управлять транспортными средствами и механизмами
Эноксапарин натрия не оказывает влияния на способность управлять транспортными средствами и механизмами.
Форма выпуска
Раствор для инъекций 10000 анти-Ха МЕ/мл.
По 0,2 мл (2000 анти-Ха ME), 0,3 мл (3000 анти-Ха ME), 0,4 мл (4000 анти-Ха ME), 0,5 мл (5000 анти-Ха ME), 0,6 мл (6000 анти-Ха ME), 0,7 мл (7000 анти-Ха ME), 0,8 мл (8000 анти-Ха ME) или 1,0 мл (10000 анти-Ха ME) в шприцы стеклянные стерильные, укомплектованные устройствами предохранительными и защитными этикетками для игл, или без устройств предохранительных и защитных этикеток для игл.
По 2 шприца в контурную ячейковую упаковку из пленки поливинилхлоридной или полиэтилентерефталатной с пленкой полимерной или фольгой алюминиевой лакированной, или без пленки полимерной и фольги алюминиевой лакированной.
По 1, 2, 3, 5 или 10 контурных ячейковых упаковок вместе с инструкцией по применению в пачке из картона.
По 0,2 мл (2000 анти-Ха ME), 0,3 мл (3000 анти-Ха ME), 0,4 мл (4000 анти-Ха ME), 0,5 мл (5000 анти-Ха ME), 0,6 мл (6000 анти-Ха ME), 0,7 мл (7000 анти-Ха ME), 0,8 мл (8000 анти-Ха ME) или 1,0 мл (10000 анти-Ха ME) в ампулы из бесцветного или темного стекла.
По 5 или 10 ампул из стекла в контурную ячейковую упаковку из пленки поливинилхлоридной или полиэтилентерефталатной с пленкой полимерной или фольгой алюминиевой лакированной, или без пленки полимерной и фольги алюминиевой лакированной, или в форму из картона.
По 1, 2, 3 или 4 контурные ячейковые упаковки или формы из картона с 5 ампулами или по 1 или 2 контурные ячейковые упаковки или формы из картона с 10 ампулами вместе с инструкцией по применению и скарификатором ампульным или без него в пачке из картона.
Условия хранения
При температуре не выше 25 °С.
Хранить в недоступном для детей месте.
Срок годности
3 года.
Не применять после окончания срока годности!
Условия отпуска
Отпускают по рецепту.
Владелец регистрационного удостоверения
ООО «Гротекс», Россия
195279, Санкт-Петербург. Индустриальный пр., д. 71, корп. 2, лит. А
Производитель/Организация, принимающая претензии
ООО «Гротекс», Россия
195279, Санкт-Петербург. Индустриальный пр., д. 71, корп. 2, лит. А
Купить Квадрапарин-СОЛОфарм в planetazdorovo.ru
*Цена в Москве. Точная цена в Вашем городе будет указана на сайте аптеки.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Квадрапарин®-СОЛОфарм
Quadraparin-SOLOpharm
Регистрационный номер
Торговое наименование
Квадрапарин®-СОЛОфарм
Международное непатентованное наименование
Лекарственная форма
раствор для инъекций
Состав
1 шприц или ампула (0,2 мл) содержит:
действующее вещество: эноксапарин натрия 2000 анти-Ха ME (20 мг)
вспомогательное вещество: вода для инъекций — до 0,2 мл.
1 шприц или ампула (0,3 мл) содержит:
действующее вещество: эноксапарин натрия 3000 анти-Ха ME (30 мг)
вспомогательное вещество: вода для инъекций — до 0,3 мл.
1 шприц или ампула (0,4 мл) содержит:
действующее вещество: эноксапарин натрия 4000 анти-Ха ME (40 мг)
вспомогательное вещество: вода для инъекций — до 0,4 мл.
1 шприц или ампула (0,5 мл) содержит:
действующее вещество: эноксапарин натрия 5000 анти-Ха ME (50 мг)
вспомогательное вещество: вода для инъекций — до 0,5 мл.
1 шприц или ампула (0,6 мл) содержит: действующее вещество: эноксапарин натрия 6000 анти-Ха ME (60 мг)
вспомогательное вещество: вода для инъекций — до 0,6 мл.
1 шприц или ампула (0,7 мл) содержит:
действующее вещество: эноксапарин натрия 7000 анти-Ха ME (70 мг)
вспомогательное вещество: вода для инъекций — до 0,7 мл.
1 шприц или ампула (0,8 мл) содержит:
действующее вещество: эноксапарин натрия 8000 анти-Ха ME (80 мг)
вспомогательное вещество: вода для инъекций — до 0,8 мл.
1 шприц или ампула (1 мл) содержит:
действующее вещество: эноксапарин натрия 10000 анти-Ха ME (100 мг)
вспомогательное вещество: вода для инъекций — до 1,0 мл.
Описание
Прозрачная бесцветная или желтоватая, или коричневато-желтоватая жидкость.
Фармакотерапевтическая группа
Код АТХ
Фармакологические свойства
Эноксапарин натрия — низкомолекулярный гепарин со средней молекулярной массой около 4500 дальтон: менее 2000 дальтон — <20 %, от 2000 до 8000 дальтон — >68 %, более 8000 дальтон — <18 %. Эноксапарин натрия получают с помощью щелочной деполимеризации бензилового эфира гепарина, выделенного из слизистой оболочки тонкой кишки свиньи. Его структура характеризуется невосстанавливающимся фрагментом 2-О-сульфо-4-енпиразиносуроновой кислоты и восстанавливающимся фрагментом 2-N,6-О-дисульфо-D-глюкопиранозида. Структура эноксапарина натрия содержит около 20 % (в пределах от 15 до 25%) 1,6-ангидропроизводного в восстанавливающемся фрагменте полисахаридной цепи.
Фармакодинамика
В очищенной системе in vitro эноксапарин натрия обладает высокой анти-Ха активностью (примерно 100 МЕ/мл) и низкой анти-IIа или антитромбиновой активностью (примерно 28 МЕ/мл). Эта антикоагулянтная активность действует через антитромбин III (АТ-III), обеспечивая антикоагулянтную активность у людей. Кроме анти-Ха/IIа активности также выявлены дополнительные антикоагулянтные и противовоспалительные свойства эноксапарина натрия как у человека, так и на моделях животных. Это включает АТ-III зависимое ингибирование других факторов свертывания, таких как фактор VIIa, активацию высвобождения ингибитора пути тканевого фактора (ПТФ), а также снижение высвобождения фактора Виллебранда из эндотелия сосудов в кровоток. Эти факторы обеспечивают антикоагулянтный эффект эноксапарина натрия в целом.
Применение препарата в профилактических дозах незначительно изменяет активированное частичное тромбопластиновое время (АЧТВ), практически не оказывает воздействия на агрегацию тромбоцитов и на степень связывания фибриногена с рецепторами тромбоцитов.
Фармакокинетика
Биодоступностъ и абсорбция
Абсолютная биодоступность эноксапарина натрия при подкожном (п/к) введении, оцениваемая на основании анти-Ха активности, близка к 100 %.
Средняя максимальная анти-Ха активность плазмы наблюдается через 3–5 ч после п/к введения препарата и составляет приблизительно 0,2; 0,4; 1,0 и 1,3 анти-Ха МЕ/мл после п/к введения 20 мг, 40 мг, 1 мг/кг и 1,5 мг/кг.
Внутривенное болюсное введение препарата в дозировке 30 мг, сопровождающееся незамедлительным подкожным введением препарата в дозировке 1 мг/кг каждые 12 ч, обеспечивает начальную максимальную анти-Ха активность на уровне 1,16 МЕ/мл (n=16), средняя экспозиция препарата в крови составляет приблизительно 88 % от равновесного состояния, которое достигается на второй день терапии.
Фармакокинетика эноксапарина натрия в указанных режимах дозирования носит линейный характер. Вариабельность внутри и между группами пациентов низкая. После повторного подкожного введения 40 мг эноксапарина натрия один раз в сутки и подкожного введения эноксапарина натрия в дозе 1,5 мг/кг массы тела один раз в сутки у здоровых добровольцев равновесная концентрация достигается ко второму дню, причём площадь под фармакокинетической кривой в среднем на 15 % выше, чем после однократного введения. После повторных подкожных введений эноксапарина натрия в суточной дозе 1 мг/кг массы тела два раза в сутки равновесная концентрация достигается через 3–4 дня, причём площадь под кривой (AUC) в среднем на 65 % выше, чем после однократного введения, и средние значения максимальных концентраций составляют соответственно 1,2 МЕ/мл и 0,52 МЕ/мл.
Анти-IIа активность в плазме примерно в 10 раз ниже, чем анти-Ха активность. Средняя максимальная анти-IIа активность наблюдается примерно через 3–4 часа после подкожного введения и достигает 0,13 МЕ/мл и 0,19 МЕ/мл после повторного введения 1 мг/кг массы тела при двукратном введении и 1,5 мг/кг массы тела при однократном введении соответственно.
Распределение
Объём распределения анти-Ха активности эноксапарина натрия составляет примерно 4,3 л и приближается к объёму циркулирующей крови.
Выведение
Эноксапарин натрия является препаратом с низким клиренсом. После внутривенного введения в течение 6 часов в дозе 1,5 мг/кг массы тела среднее значение клиренса анти-Ха в плазме составляет 0,74 л/час.
Выведение препарата носит монофазный характер с периодом полувыведения (T½) около 5 часов (после однократного подкожного введения) и около 7 часов (после многократного введения препарата). Эноксапарин натрия в основном метаболизируется в печени путём десульфатирования и/или деполимеризации с образованием низкомолекулярных веществ с очень низкой биологической активностью. Выведение через почки активных фрагментов препарата составляет примерно 10 % от введённой дозы, и общая экскреция активных и неактивных фрагментов составляет примерно 40 % от введённой дозы.
Особые группы пациентов
Пациенты пожилого возраста (старше 75 лет): фармакокинетический профиль эноксапарина натрия не отличается у пациентов пожилого возраста и более молодых пациентов при нормальной функции почек. Однако в результате снижения функции почек с возрастом может наблюдаться замедление выведения эноксапарина натрия у пациентов пожилого возраста.
Нарушения функции печени: в исследовании с участием пациентов с поздними стадиями цирроза печени, получавших эноксапарин натрия в дозировке 4000 ME (40 мг) один раз в сутки, снижение максимальной анти- Ха активности было связано с увеличением степени тяжести нарушения функции печени (с оценкой по шкале Чайлд-Пью). Это снижение, главным образом, было обусловлено снижением уровня АТ-III, вторичным по отношению к снижению синтеза АТ-III у пациентов с нарушением функции печени.
Нарушение функции почек: отмечено уменьшение клиренса эноксапарина натрия у пациентов с нарушениями функции почек. После повторного подкожного введения 40 мг эноксапарина натрия один раз в сутки происходит увеличение активности анти-Ха, представленной площадью под фармакокинетической кривой (AUC) у пациентов с нарушениями функции почек лёгкой (клиренс креатинина ≥50 и <80 мл/мин) и умеренной степени тяжести (клиренс креатинина ≥30 и <50 мл/мин). У пациентов с тяжелым нарушением функции почек (клиренс креатинина менее 30 мл/мин) AUC в состоянии равновесия в среднем на 65 % выше при повторном подкожном введении 40 мг препарата один раз в сутки.
Гемодиализ: фармакокинетика эноксапарина натрия сопоставима с показателями в контрольной популяции после однократных внутривенных введений доз 25 ME, 50 ME или 100 МЕ/кг (0,25, 0,50 или 1,0 мг/кг), однако AUC была в два раза выше, чем в контрольной популяции.
Масса тела: после повторных подкожных введений в дозировке 1,5 мг/кг один раз в сутки средняя AUC анти-Ха активности в состоянии равновесия незначительно выше у пациентов с избыточной массой тела (ИМТ 30–48 кг/м2) по сравнению с пациентами с обычной средней массой тела, в то время как максимальная анти-Ха активность плазмы крови не увеличивается. У пациентов с избыточной массой тела при подкожном введении препарата клиренс несколько меньше. Если не делать поправку дозы с учётом массы тела пациента, то после однократного подкожного введения 40 мг эноксапарина натрия анти-Ха активность будет на 52 % выше у женщин с массой тела менее 45 кг и на 27 % выше у мужчин с массой тела менее 57 кг по сравнению с пациентами с обычной средней массой тела.
Показания
- Профилактика венозных тромбозов и эмболий при хирургических вмешательствах у пациентов умеренного и высокого риска, особенно при ортопедических и общехирургических вмешательствах, включая онкологические;
- Профилактика венозных тромбозов и эмболий у пациентов, находящихся на постельном режиме вследствие острых терапевтических заболеваний, включая острую сердечную недостаточность и декомпенсацию хронической сердечной недостаточности (III или IV класс NYHA), дыхательную недостаточность, а также при тяжёлых инфекциях и ревматических заболеваниях при повышенном риске венозного тромбообразования (см. раздел «Особые указания»);
- Лечение тромбоза глубоких вен с тромбоэмболией лёгочной артерии или без тромбоэмболии лёгочной артерии, кроме случаев тромбоэмболии лёгочной артерии, требующих тромбоэмболической терапии или хирургического вмешательства;
- Профилактика тромбообразования в системе экстракорпорального кровообращения во время гемодиализа;
-
Острый коронарный синдром:
◦ лечение нестабильной стенокардии и инфаркта миокарда без подъёма сегмента ST в сочетании с пероральным приёмом ацетилсалициловой кислоты;
◦ лечение острого инфаркта миокарда с подъёмом сегмента ST у пациентов, подлежащих медикаментозному лечению или последующему чрескожному коронарному вмешательству (ЧКВ).
Противопоказания
- Повышенная чувствительность к эноксапарину натрия, гепарину или его производным, включая другие низкомолекулярные гепарины;
- активное клинически значимое кровотечение, а также состояния и заболевания, при которых имеется высокий риск развития кровотечения, включая недавно перенесённый геморрагический инсульт, острую язву желудочно-кишечного тракта (ЖКТ), наличие злокачественного новообразования с высоким риском кровотечений, недавно перенесённые операции на головном и спинном мозге, офтальмологические операции, известное или предполагаемое наличие варикозного расширения вен пищевода, артериовенозные мальформации, сосудистые аневризмы, сосудистые аномалии спинного и головного мозга;
- спинальная или эпидуральная анестезия или локо-региональная анестезия, когда эноксапарин натрия применялся для лечения в предыдущие 24 часа;
- иммуноопосредованная гепарин-индуцированная тромбоцитопения (в анамнезе) в течение 100 последних дней или наличие в крови циркулирующих антитромбоцитарных антител;
- детский возраст до 18 лет, так как эффективность и безопасность у данной категории пациентов не установлены (см. раздел «Особые указания»).
С осторожностью
Состояния, при которых имеется потенциальный риск развития кровотечения:
- нарушения гемостаза (в том числе гемофилия, тромбоцитопения, гипокоагуляция, болезнь Виллебранда и др.), тяжёлый васкулит;
- язвенная болезнь желудка или двенадцатиперстной кишки или другие эрозивно-язвенные поражения желудочно-кишечного тракта в анамнезе;
- недавно перенесённый ишемический инсульт;
- неконтролируемая тяжёлая артериальная гипертензия;
- диабетическая или геморрагическая ретинопатия;
- тяжёлый сахарный диабет;
- недавно перенесённая или предполагаемая неврологическая или офтальмологическая операция;
- проведение спинальной или эпидуральной анестезии (потенциальная опасность развития гематомы), спинномозговая пункция (недавно перенесённая);
- недавние роды;
- эндокардит бактериальный (острый или подострый);
- перикардит или перикардиальный выпот;
- почечная и/или печёночная недостаточность;
- внутриматочная контрацепция (ВМК);
- тяжёлая травма (особенно центральной нервной системы), открытые раны на больших поверхностях;
- одновременный приём препаратов, влияющих на систему гемостаза;
- гепарин-индуцированная тромбоцитопения без циркулирующих антител в анамнезе (более 100 дней).
Отсутствуют данные по клиническому применению эноксапарина натрия при следующих заболеваниях: активный туберкулёз, лучевая терапия (недавно перенесённая).
Применение при беременности и в период грудного вскармливания
Беременность
Сведений о том, что эноксапарин натрия проникает через плацентарный барьер во время беременности, нет. Так как отсутствуют адекватные и хорошо контролируемые исследования с участием беременных женщин, а исследования на животных не всегда прогнозируют реакцию на введение эноксапарина натрия во время беременности у человека, применять его во время беременности следует только в исключительных случаях, когда имеется настоятельная необходимость его применения, установленная врачом.
Рекомендуется проведение контроля за состоянием пациенток на предмет появления признаков кровотечения или чрезмерной антикоагуляции, пациентки должны быть предупреждены о риске возникновения кровотечений.
Нет данных о повышенном риске развития кровотечений, тромбоцитопении или остеопороза у беременных женщин, за исключением случаев, отмеченных у пациенток с искусственными клапанами сердца (см. раздел «Особые указания»).
При планировании эпидуральной анестезии рекомендуется перед её проведением отменить эноксапарин натрия (см. раздел «Особые указания»).
Период грудного вскармливания
Неизвестно, экскретируется ли неизменённый эноксапарин натрия в грудное молоко. Всасывание эноксапарина натрия в ЖКТ у новорождённого маловероятно. Препарат может применяться в период грудного вскармливания.
Способ применения и дозы
Подкожно, за исключением особых случаев (см. ниже подразделы «Профилактика тромбообразования в системе экстракорпорального кровообращения при проведении гемодиализа» и «Лечение острого инфаркта миокарда с подъемом сегмента ST, медикаментозное или с помощью чрескожного коронарного вмешательства»).
Профилактика венозных тромбозов и эмболии при хирургических вмешательствах у пациентов умеренного и высокого риска
Пациентам с умеренным риском развития тромбозов и эмболий (например, абдоминальные операции) рекомендуемая доза препарата составляет 20 мг один раз в сутки подкожно. Первую инъекцию следует сделать за 2 ч до хирургического вмешательства.
Пациентам с высоким риском развития тромбозов и эмболий (например, при ортопедических операциях, хирургических операциях в онкологии, пациентам с дополнительными факторами риска, не связанными с операцией, такими как врождённая или приобретённая тромбофилия, злокачественное новообразование, постельный режим более трёх суток, ожирение, венозный тромбоз в анамнезе, варикозное расширение вен нижних конечностей, беременность) препарат рекомендуется в дозе 40 мг один раз в сутки подкожно, с введением первой дозы за 12 ч до хирургического вмешательства. При необходимости более ранней предоперационной профилактики (например, у пациентов с высоким риском развития тромбозов и тромбоэмболий, ожидающих отсроченную ортопедическую операцию) последняя инъекция должна быть сделана за 12 ч до операции и через 12 ч после операции.
Длительность лечения препаратом в среднем составляет 7–10 дней. При необходимости терапию можно продолжать до тех пор, пока сохраняется риск развития тромбоза и эмболии, и до тех пор, пока пациент не перейдёт на амбулаторный режим.
При крупных ортопедических операциях может быть целесообразно после начальной терапии продолжение лечения путём введения препарата в дозе 40 мг один раз в сутки в течение пяти недель.
Для пациентов с высоким риском венозных тромбоэмболий, перенёсших хирургическое вмешательство, абдоминальную и тазовую хирургию по причине онкологического заболевания, может быть целесообразно увеличение продолжительности введения препарата в дозе 40 мг один раз в сутки в течение четырёх недель.
Профилактика венозных тромбозов и эмболий у пациентов, находящихся на постельном режиме вследствие острых терапевтических заболеваний
Рекомендуемая доза препарата составляет 40 мг один раз в сутки, подкожно, как минимум в течение 6–14 дней. Терапию следует продолжать до полного перехода пациента на амбулаторный режим (максимально в течение 14 дней).
Лечение тромбоза глубоких вен с тромбоэмболией лёгочной артерии или без тромбоэмболии лёгочной артерии
Препарат вводится подкожно из расчёта 1,5 мг/кг массы тела один раз в сутки или 1 мг/кг массы тела два раза в сутки. Режим дозирования должен выбираться врачом на основе оценки риска развития тромбоэмболии и риска развития кровотечений. У пациентов без тромбоэмболических осложнений и с низким риском развития венозной тромбоэмболии препарат рекомендуется вводить подкожно из расчёта 1,5 мг/кг массы тела один раз в сутки. У всех других пациентов, включая пациентов с ожирением, симптоматической тромбоэмболией лёгочных артерий, раком, повторной венозной тромбоэмболией и проксимальным тромбозом (в подвздошной вене) препарат рекомендуется применять в дозе 1 мг/кг два раза в сутки.
Длительность лечения в среднем составляет 10 дней. Следует сразу же начать терапию непрямыми антикоагулянтами, при этом лечение препаратом необходимо продолжать до достижения терапевтического антикоагулянтного эффекта (значения МНО [Международного Нормализованного Отношения] должны составлять 2,0-3,0).
Профилактика тромбообразования в системе экстракорпорального кровообращения во время гемодиализа
Рекомендуемая доза препарата составляет в среднем 1 мг/кг массы тела. При высоком риске развития кровотечения дозу следует снизить до 0,5 мг/кг массы тела при двойном сосудистом доступе или до 0,75 мг при одинарном сосудистом доступе.
При гемодиализе эноксапарин натрия следует вводить в артериальный участок шунта в начале сеанса гемодиализа. Одной дозы, как правило, достаточно для четырёхчасового сеанса, однако при обнаружении фибриновых колец при более продолжительном гемодиализе можно дополнительно ввести препарат из расчёта 0,5–1 мг/кг массы тела. Данные в отношении пациентов, применяющих эноксапарин натрия для профилактики или лечения и во время сеансов гемодиализа, отсутствуют.
Лечение нестабильной стенокардии и инфаркта миокарда без подъёма сегмента ST
Препарат вводится из расчёта 1 мг/кг массы тела каждые 12 ч, подкожно, при одновременном применении антитромбоцитарной терапии. Средняя продолжительность терапии составляет, как минимум, 2 дня и продолжается до стабилизации клинического состояния пациента. Обычно введение препарата продолжается от 2 до 8 дней.
Ацетилсалициловая кислота рекомендуется всем пациентам, не имеющим противопоказаний, с начальной дозой 150–300 мг внутрь с последующей поддерживающей дозой 75–325 мг один раз в сутки.
Лечение острого инфаркта миокарда с подъёмом сегмента ST, медикаментозное или с помощью чрескожного коронарного вмешательства
Лечение начинают с однократного внутривенного болюсного введения эноксапарина натрия в дозе 30 мг. Сразу же после него подкожно вводят эноксапарин натрия в дозе 1 мг/кг массы тела. Далее препарат назначают подкожно по 1 мг/кг массы тела каждые 12 ч (максимально 100 мг эноксапарина натрия для каждой из первых двух подкожных инъекций, затем — по 1 мг/кг массы тела для оставшихся подкожных доз, то есть при массе тела более 100 кг разовая доза не может превышать 100 мг). Как можно скорее после выявления острого инфаркта миокарда с подъемом сегмента ST пациентам необходимо назначить одновременно ацетилсалициловую кислоту и, если нет противопоказаний, приём ацетилсалициловой кислоты (в дозах 75–325 мг) следует продолжать ежедневно в течение не менее 30 дней.
Рекомендуемая продолжительность лечения препаратом составляет 8 дней или до выписки пациента из стационара (если период госпитализации составляет менее 8 дней).
При комбинации с тромболитиками (фибрин-специфическими и фибрин-неспецифическими) эноксапарин натрия должен вводиться в интервале от 15 мин до начала тромболитической терапии и до 30 минут после нее.
У пациентов в возрасте 75 лет и старше не применяется начальное внутривенное болюсное введение. Препарат вводят подкожно в дозе 0,75 мг/кг каждые 12 ч (максимально 75 мг эноксапарина натрия для каждой из первых двух подкожных инъекций, затем — по 0,75 мг/кг массы тела для оставшихся подкожных доз, то есть при массе тела более 100 кг разовая доза не может превышать 75 мг).
У пациентов, которым проводится чрескожное коронарное вмешательство, в случае, если последняя подкожная инъекция эноксапарина натрия была проведена менее чем за 8 ч до раздувания введённого в место сужения коронарной артерии баллонного катетера, дополнительного введения эноксапарина натрия не требуется. Если же последняя подкожная инъекция эноксапарина натрия проводилась более чем за 8 ч до раздувания баллонного катетера, следует произвести дополнительное внутривенное болюсное введение эноксапарина натрия в дозе 0,3 мг/кг.
Особенности введения препарата
Предварительно заполненный одноразовый шприц готов к применению.
Препарат нельзя вводить внутримышечно!
Подкожное введение
Инъекции желательно проводить в положении пациента «лёжа». При использовании предварительно заполненных шприцев во избежание потери препарата перед инъекцией не надо удалять пузырьки воздуха из шприца. Инъекции следует проводить поочередно в левую или правую переднелатеральную или заднелатеральную поверхность живота.
Иглу необходимо вводить на всю длину вертикально (не сбоку) в кожную складку, собранную и удерживаемую до завершения инъекции между большим и указательным пальцами. Складку кожи отпускают только после завершения инъекции.
Не следует массировать место инъекции после введения препарата.
Внутривенное болюсное введение
Внутривенное болюсное введение эноксапарина натрия должно проводиться через венозный катетер. Эноксапарин натрия не должен смешиваться или вводиться вместе с другими лекарственными препаратами. Для того, чтобы избежать присутствия в инфузионной системе следов других лекарственных препаратов и их взаимодействия с эноксапарином натрия, венозный катетер должен промываться достаточным количеством 0,9 % раствора натрия хлорида или 5 % раствора декстрозы до и после внутривенного болюсного введения эноксапарина натрия. Эноксапарин натрия может безопасно вводиться с 0,9 % раствором натрия хлорида и 5 % раствором декстрозы. Для проведения болюсного введения 30 мг эноксапарина натрия при лечении острого инфаркта миокарда с подъёмом сегмента ST из стеклянных шприцев большего объёма удаляют лишнее количество препарата с тем, чтобы в них оставалось только 30 мг (0,3 мл). Доза 30 мг может непосредственно вводиться внутривенно.
Для проведения внутривенного болюсного введения эноксапарина натрия через венозный катетер могут использоваться предварительно заполненные шприцы для подкожного введения препарата 30 мг, 40 мг, 50 мг, 60 мг, 70 мг, 80 мг и 100 мг. Рекомендуется использовать шприцы 30 мг, 40 мг, 50 мг и 60 мг, так как это уменьшает количество удаляемого из шприца препарата. Шприцы 20 мг не используются, так как в них недостаточно препарата для болюсного введения 30 мг эноксапарина натрия.
Для повышения точности дополнительного внутривенного болюсного введения малых объёмов в венозный катетер при проведении чрескожных коронарных вмешательств рекомендуется развести препарат до концентрации 3 мг/мл. Разведение раствора рекомендуется проводить непосредственно перед введением.
Для получения раствора эноксапарина натрия с концентрацией 3 мг/мл с помощью предварительно заполненного шприца 60 мг рекомендуется использовать ёмкость с инфузионным раствором 50 мл (то есть с 0,9 % раствором натрия хлорида или 5 % раствором дектрозы). Из ёмкости с инфузионным раствором с помощью обычного шприца извлекается и удаляется 30 мл раствора. Эноксапарин натрия (содержимое шприца для подкожного введения 60 мг) вводится в оставшиеся в ёмкости 20 мл инфузионного раствора. Содержимое ёмкости с разведённым раствором эноксапарина натрия осторожно перемешивается. Для введения с помощью шприца извлекается необходимый объём разведённого раствора эноксапарина натрия, который рассчитывается по формуле:
Объём разведённого раствора = Масса тела пациента (кг) × 0,1, или с помощью представленной ниже таблицы.
Объёмы, которые должны вводиться внутривенно после разведения до концентрации 3 мг/мл
|
Масса тела пациента (кг) |
Необходимая доза (0,3 мг/кг) [мг] |
Необходимый для введения объём раствора, разведённого до концентрации 3 мг/мл [мл] |
|
45 |
13,5 |
4,5 |
|
50 |
15 |
5 |
|
55 |
16,5 |
5,5 |
|
60 |
18 |
6 |
|
65 |
19,5 |
6,5 |
|
70 |
21 |
7 |
|
75 |
22,5 |
7,5 |
|
80 |
24 |
8 |
|
85 |
25,5 |
8,5 |
|
90 |
27 |
9 |
|
95 |
28,5 |
9,5 |
|
100 |
30 |
10 |
|
105 |
31,5 |
10,5 |
|
110 |
33 |
11 |
|
115 |
34,5 |
11,5 |
|
120 |
36 |
12 |
|
125 |
37,5 |
12,5 |
|
130 |
39 |
13 |
|
135 |
40,5 |
13,5 |
|
140 |
42 |
14 |
|
145 |
43,5 |
14,5 |
|
150 |
45 |
15 |
Переключение между эноксапарином натрия и пероральными антикоагулянтами
Переключение между эноксапарином натрия и антагонистами витамина К (АВК)
Для мониторирования эффекта АВК необходимо наблюдение врача и проведение лабораторных исследований [протромбиновое время, представленное как МНО]. Так как для развития максимального эффекта АВК требуется время, терапия эноксапарином натрия должна продолжаться в постоянной дозе так долго, как необходимо для поддержания значений МНО (по данным двух последовательных определений) в желаемом терапевтическом диапазоне в зависимости от показаний. Для пациентов, которые получают АВК, отмена АВК и введение первой дозы эноксапарина натрия должны проводиться после того, как МНО снизилось ниже границы терапевтического диапазона.
Переключение между эноксапарином натрия и пероральными антикоагулянтами прямого действия (ПОАК)
Отмена эноксапарина натрия и назначение ПОАК должны проводиться за 0-2 ч до момента очередного запланированного введения эноксапарина натрия в соответствии с инструкцией по применению пероральных антикоагулянтов.
Для пациентов, получающих ПОАК, введение первой дозы эноксапарина натрия и отмена пероральных антикоагулянтов прямого действия должны проводиться в момент времени, соответствующий очередному запланированному применению ПОАК.
Применение при спинальной/эпидуральной анестезии или люмбальной пункции
В случае применения антикоагулянтной терапии во время проведения эпидуральной или спинальной анестезии/анальгезии или люмбальной пункции необходимо проведение неврологического мониторирования вследствие риска развития нейроаксиальных гематом (см. раздел «Особые указания»).
Применение эноксапарина натрия в профилактических дозах
Установка или удаление катетера должно проводиться спустя как минимум 12 ч после последней инъекции профилактической дозы эноксапарина натрия.
При использовании непрерывной техники необходимо соблюдать по меньшей мере 12 ч интервал до удаления катетера.
У пациентов с клиренсом креатинина ≥15 и <30 мл/мин следует рассмотреть вопрос об удвоении времени до момента пункции или введения/удаления катетера как минимум до 24 ч.
Предоперационное введение эноксапарина натрия за 2 ч до вмешательства в дозировке 20 мг несовместимо с проведением нейроаксиальной анестезии.
Применение эноксапарина натрия в терапевтических дозах
Установка или удаление катетера должно проводиться спустя как минимум через 24 ч после последней инъекции терапевтической дозы эноксапарина натрия (см. раздел «Противопоказания»).
При использовании непрерывной техники необходимо соблюдать по меньшей мере 24 ч интервал до удаления катетера.
У пациентов с клиренсом креатинина ≥15 и <30 мл/мин следует рассмотреть вопрос об удвоении времени до момента пункции или введения/удаления катетера как минимум до 48 ч.
Пациентам, получающим эноксапарин натрия в дозах 0,75 мг/кг или 1 мг/кг массы тела 2 раза в сутки, не следует вводить вторую дозу препарата с целью увеличения интервала перед установкой или заменой катетера. Точно так же следует рассмотреть вопрос о возможности отсрочки введения следующей дозы препарата как минимум на 4 ч, исходя из оценки соотношения польза/риск (риск развития тромбоза и кровотечений при проведении процедуры с учётом наличия у пациентов факторов риска). В эти временные точки все ещё продолжает выявляться анти-Ха активность препарата, и отсрочки по времени не являются гарантией того, что развития нейроаксиальной гематомы удастся избежать.
Режим дозирования у особых групп пациентов
Дети до 18 лет
Безопасность и эффективность применения эноксапарина натрия у детей не установлены.
Пациенты пожилого возраста (старше 75 лет)
За исключением лечения инфаркта миокарда с подъёмом сегмента ST для всех других показаний снижения доз эноксапарина натрия у пациентов пожилого возраста при отсутствии нарушений функции почек не требуется.
Пациенты с нарушениями функции почек
Тяжёлые нарушения функции почек (клиренс креатинина ≥15 и <30 мл/мин) Применение эноксапарина натрия не рекомендуется пациентам с терминальной стадией хронической болезни почек (клиренс креатинина <15 мл/мин) ввиду отсутствия данных, кроме случаев профилактики тромбообразования в системе экстракорпорального кровообращения во время гемодиализа.
У пациентов с тяжёлыми нарушениями функции почек (клиренс креатинина ≥15 и <30 мл/мин) доза эноксапарина натрия снижается в соответствии с представленными ниже таблицами, так как у этих пациентов отмечается увеличение системной экспозиции (продолжительности действия) препарата.
При применении препарата в терапевтических дозах рекомендуется следующая коррекция режима дозирования:
|
Обычный режим дозирования |
Режим дозирования при тяжёлой почечной недостаточности |
|
1 мг/кг массы тела подкожно 2 раза в сутки |
1 мг/кг массы тела подкожно 1 раз в сутки |
|
1,5 мг/кг массы тела подкожно 1 раз в сутки |
1 мг/кг массы тела подкожно 1 раз в сутки |
|
Лечение острого инфаркта миокарда с подъёмом сегмента ST у пациентов моложе 75 лет |
|
|
Однократно внутривенное болюсное введение 30 мг плюс 1 мг/кг массы тела подкожно; с последующим подкожным введением в дозе 1 мг/кг массы тела 2 раза в сутки (максимально 100 мг для каждой из двух первых подкожных инъекций) |
Однократно внутривенное болюсное введение 30 мг плюс 1 мг/кг массы тела подкожно; с последующим подкожным введением в дозе 1 мг/кг массы тела 1 раз в сутки (максимально 100 мг только для первой подкожной инъекции) |
|
Лечение острого инфаркта миокарда с подъемом сегмента ST у пациентов в возрасте 75 лет и старше |
|
|
0,75 мг/кг массы тела подкожно 2 раза в сутки без начального внутривенного болюсного введения (максимально 75 мг для каждой из двух первых подкожных инъекций) |
1 мг/кг массы тела подкожно 1 раз в сутки без начального внутривенного болюсного введения (максимально 100 мг только для первой подкожной инъекции) |
При применении препарата с профилактической целью рекомендуется коррекция режима дозирования, представленная в таблице ниже:
|
Обычный режим дозирования |
Режим дозирования при тяжёлой почечной недостаточности |
|
40 мг подкожно 1 раз в сутки |
20 мг подкожно 1 раз в сутки |
|
20 мг подкожно 1 раз в сутки |
20 мг подкожно 1 раз в сутки |
Рекомендованная коррекция режима дозирования не применяется при гемодиализе.
Нарушения функции почек лёгкой (клиренс креатинина ≥50 и <80 мл/мин) и умеренной (клиренс креатинина ≥30 и <50 мл/мин) степени тяжести
Коррекции дозы не требуется, однако пациенты должны находиться под тщательным наблюдением врача.
Пациенты с нарушениями функции печени
В связи с отсутствием клинических исследований препарат следует применять с осторожностью у пациентов с нарушениями функции печени.
Инструкция по самостоятельному выполнению инъекции эноксапарина натрия
- Вымойте руки и участок кожи (место для инъекции), в который Вы будете вводить препарат, водой с мылом. Высушите их.
- Примите удобное положение «сидя» или «лёжа» и расслабьтесь. Убедитесь, что Вы хорошо видите место, в которое собираетесь вводить препарат. Оптимально использовать кресло для отдыха, шезлонг или кровать, обложенную подушками для опоры.
- Выберите место для проведения инъекции в правой или левой части живота. Это место должно находиться на расстоянии как минимум 5 см от пупка или вокруг имеющихся рубцов и кровоподтёков. Чередуйте места инъекций в правой и левой частях живота в зависимости от того, куда Вы вводили препарат в предыдущий раз.
- Протрите место для инъекции тампоном, смоченным спиртом.
-
Осторожно снимите колпачок с иглы шприца с препаратом. Отложите колпачок. Шприц предварительно заполнен и готов к использованию. Не нажимайте на поршень для вытеснения пузырьков воздуха до введения иглы в место инъекции. Это может привести к потере препарата. После удаления колпачка не допускайте прикосновения иглы к каким-либо предметам. Это необходимо для сохранения стерильности иглы.
Внимание: при наличии защитной этикетки для иглы — следуйте Инструкции по использованию защитной этикетки для иглы, приведённой ниже.
- Удерживайте шприц в одной руке так, как Вы держите карандаш, а другой рукой осторожно сожмите протертое спиртом место для введения препарата между большим и указательным пальцами так, чтобы образовать складку кожи. Удерживайте кожную складку все время, пока Вы вводите препарат.
- Удерживайте шприц таким образом, чтобы игла была направлена вниз (вертикально под углом 90°). Введите иглу на всю длину в кожную складку.
- Нажмите пальцем на поршень. Это обеспечит введение препарата в подкожную жировую ткань живота. Удерживайте кожную складку все время, пока вы вводите препарат.
-
Извлеките иглу, потянув её назад без отклонения от оси. Теперь можно прекратить удержание кожной складки.
Внимание: при наличии устройства предохранительного — следуйте Инструкции по использованию устройства предохранительного, приведённой ниже.
- В целях предотвращения образования кровоподтёка не растирайте место инъекции после введения препарата.
- Утилизируйте использованный одноразовый шприц в мусорный контейнер.
При применении препарата строго придерживайтесь рекомендаций, представленных в данной инструкции, а также указаний врача или провизора. При возникновении вопросов обратитесь к врачу или провизору.
Инструкция по использованию защитной этикетки для иглы (при её наличии)
Не вскрывая упаковку, проверьте целостность шприца, а также отсутствие жидкости в контурной ячейковой упаковке. Если Вы сомневаетесь в целостности шприца или его герметичности, возьмите другую упаковку.
Откройте контурную ячейковую упаковку.
Проверьте содержание препарата в шприце.
- Внимание: не снимайте защитный колпачок до изгиба защитной этикетки! Согните защитную этикетку для иглы в сторону приблизительно на 90°.
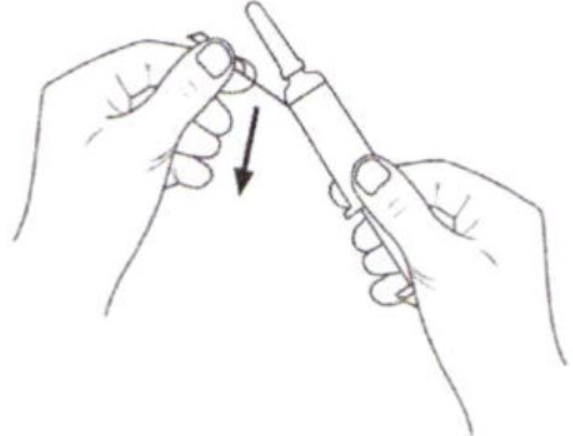
- Снимите защитный колпачок.
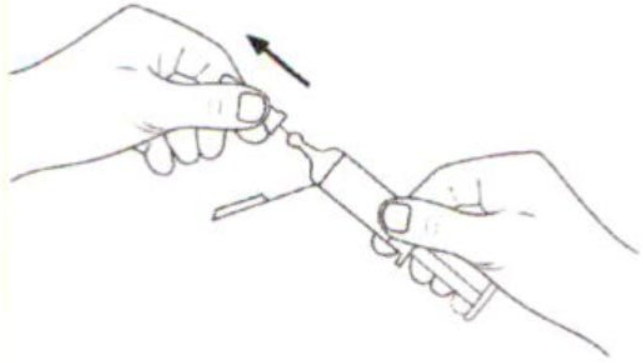
- Сделайте инъекцию, как обычно.
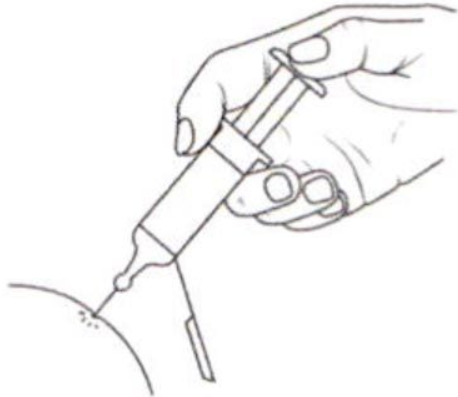
- Внимание: не закрепляйте иглу в защитную этикетку пальцами! Одной рукой закрепите иглу путём размещения защитной этикетки на жесткой устойчивой поверхности. Затем нажмите на защитную этикетку.
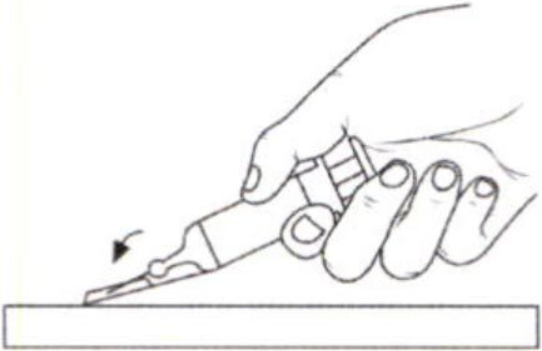
- Согните защитную этикетку приблизительно на 90° до тех пор, пока игла со слышимым щелчком не окажется в пластиковой части защитной этикетки.
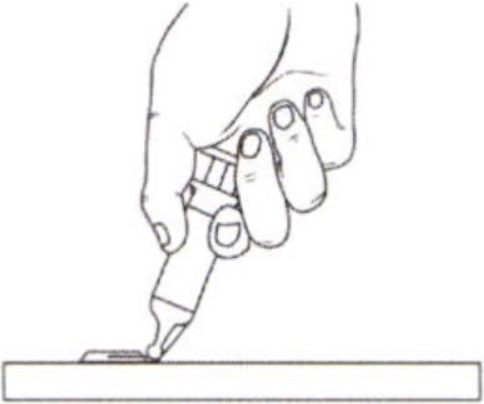
- Утилизируйте одноразовый шприц с иглой в мусорный контейнер.
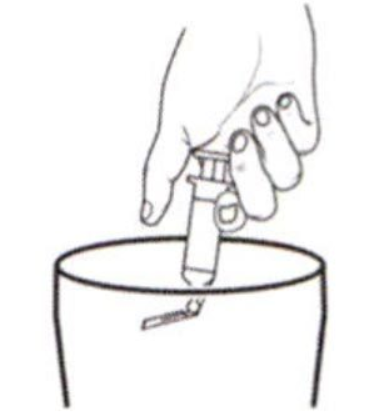
Инструкция по использованию устройства предохранительного
Внешний вид шприца перед его использованием
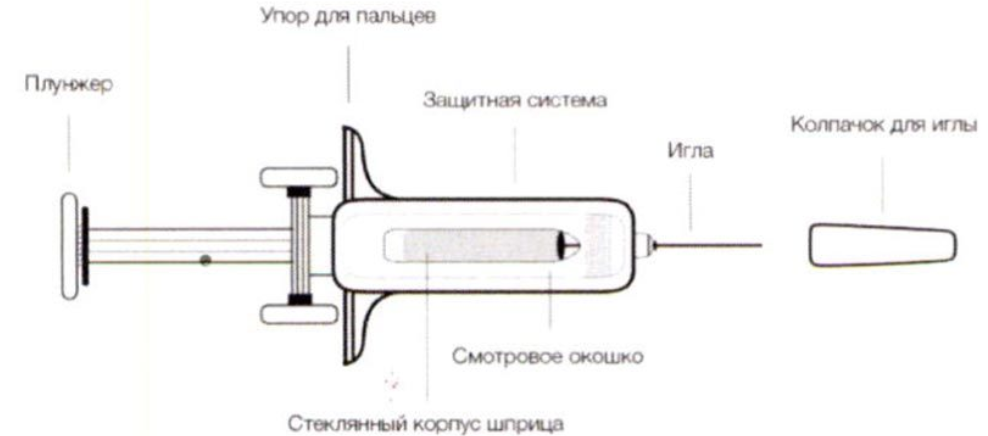
Внешний вид шприца после применения

Не вскрывая упаковку, проверьте целостность шприца, а также отсутствие жидкости в контурной ячейковой упаковке. Если Вы сомневаетесь в целостности шприца или его герметичности, возьмите другую упаковку. Откройте контурную ячейковую упаковку. Проверьте содержание препарата в шприце.
- Внимание: Вынимая шприц из упаковки, не тяните шприц за плунжер или колпачок для иглы. Выньте шприц из упаковки, как показано на рисунке.
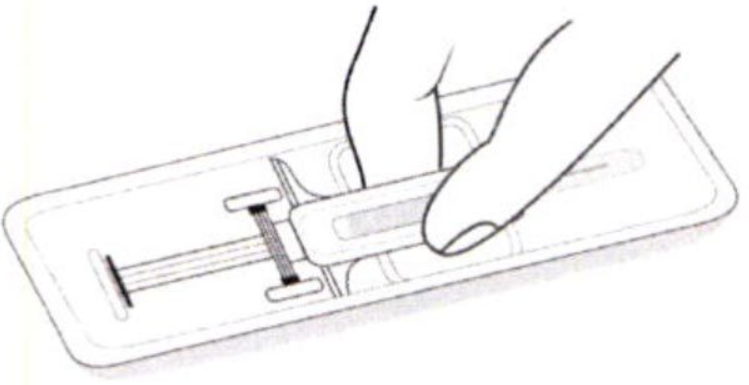
- Внимание: Не снимайте колпачок иглы, держась за плунжер или основание иглы. Снимите колпачок иглы, как показано на рисунке, держась за защитную систему во избежание травмирования или изгиба иглы.
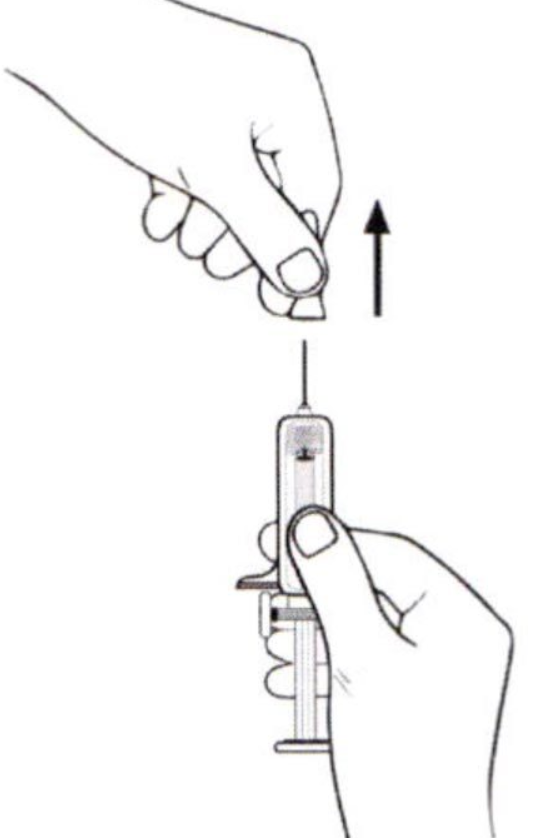
- Сделайте инъекцию, как обычно.
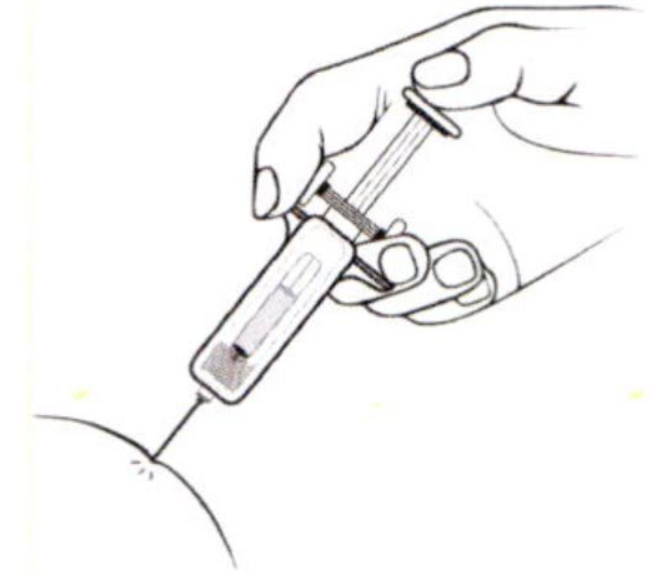
- Зажав корпус шприца между указательным и средним пальцами, надавите на плунжер вниз до упора, чтобы ввести весь раствор.
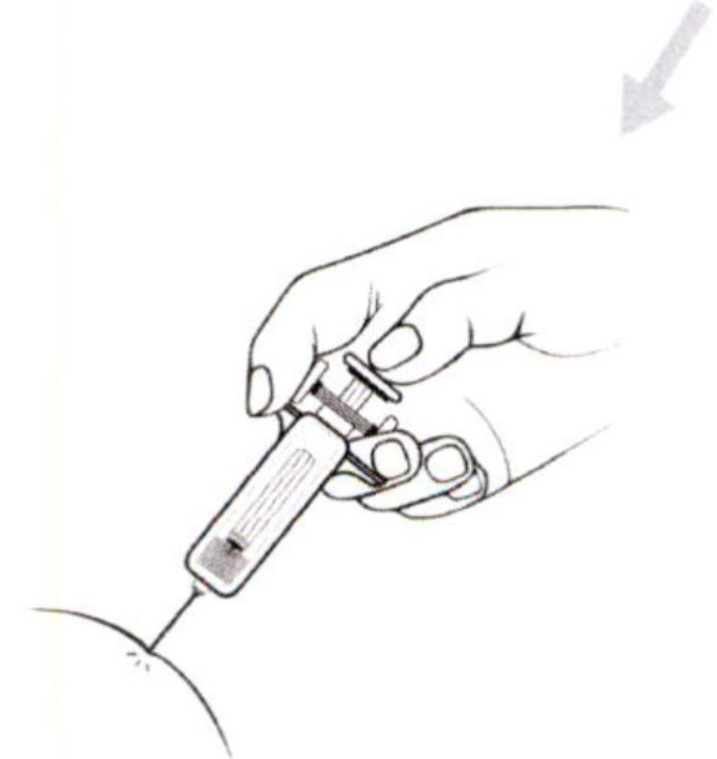 Внимание: Раствор должен быть введён полностью для срабатывания защитной системы.
Внимание: Раствор должен быть введён полностью для срабатывания защитной системы. - После завершения инъекции воспользуйтесь одним из предложенных вариантов: 1) Выньте иглу из места инъекции и отпустите плунжер. Дождитесь пока защитная система полностью закроет иглу. 2) Не вынимая иглу из места инъекции, отпустите плунжер. Дождитесь пока защитная система полностью закроет иглу.
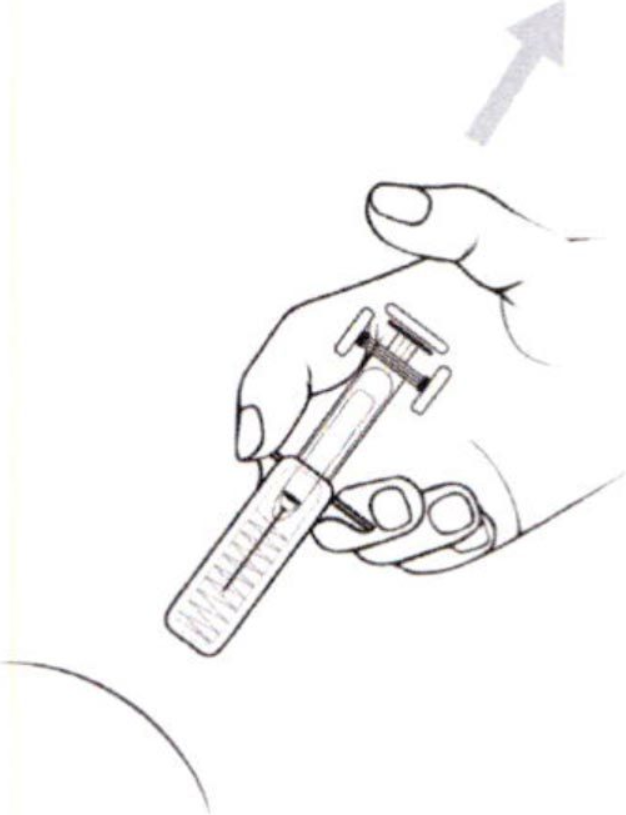
- Внимание: Если защитная система не активировалась или активировалась частично — выбросите шприц с незащищённой иглой. Так как игла не защищена, обратите особое внимание на то, чтобы избежать травм. Выбросите шприц с защищённой иглой в мусорный контейнер.
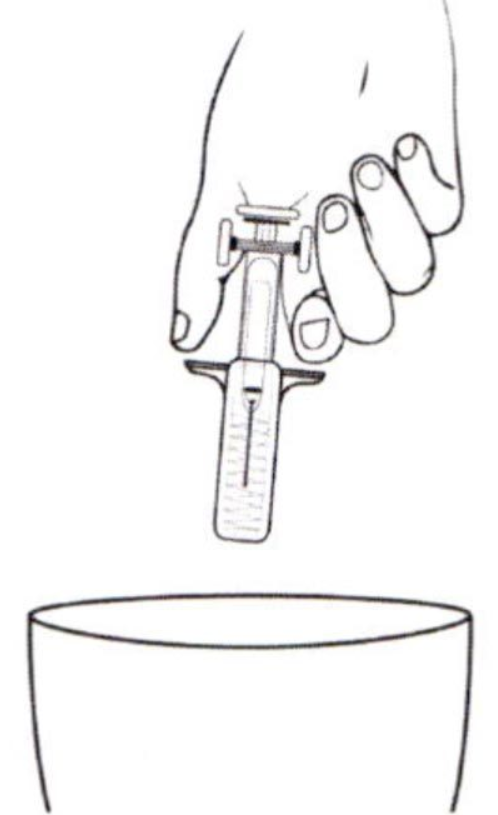
Побочное действие
Изучение побочных эффектов эноксапарина натрия проводилось более чем у 15000 пациентов, участвовавших в клинических исследованиях, из них у 1776 пациентов — при профилактике венозных тромбозов и эмболий при общехирургических и ортопедических операциях; у 1169 пациентов — при профилактике венозных тромбозов и эмболий у пациентов, находящихся на постельном режиме вследствие острых терапевтических заболеваний; у 559 пациентов — при лечении тромбоза глубоких вен с тромбоэмболией лёгочной артерии или без тромбоэмболии лёгочной артерии; у 1578 пациентов — при лечении нестабильной стенокардии и инфаркта миокарда без зубца Q; у 10176 пациентов — при лечении инфаркта миокарда с подъёмом сегмента ST. Режим введения эноксапарина натрия отличался в зависимости от показаний. При профилактике венозных тромбозов и эмболий при общехирургических и ортопедических операциях или у пациентов, находящихся на постельном режиме, вводилось 40 мг подкожно 1 раз в сутки. При лечении тромбоза глубоких вен с тромбоэмболией лёгочной артерии или без неё, пациенты получали эноксапарин натрия из расчёта 1 мг/кг массы тела подкожно каждые 12 ч или 1,5 мг/кг массы тела подкожно 1 раз в сутки. При лечении нестабильной стенокардии и инфаркта миокарда без зубца Q доза эноксапарина натрия составляла 1 мг/кг массы тела подкожно каждые 12 ч, а в случае инфаркта миокарда с подъёмом сегмента ST проводилось внутривенное болюсное введение 30 мг с последующим введением 1 мг/кг массы тела подкожно каждые 12 ч.
Частота возникновения нежелательных реакций определялась в соответствии с классификацией ВОЗ: очень часто (≥1/10); часто (≥1/100 и <1/10); нечасто (≥1/1000 и <1/100); редко (≥1/10000 и <1/1000); очень редко (<1/10000), частота неизвестна (не может быть подсчитана на основании имеющихся данных).
Нарушения со стороны сосудов:
Кровотечения
В клинических исследованиях кровотечения были наиболее часто встречающимися нежелательными реакциями. К ним относились большие кровотечения, наблюдавшиеся у 4,2 % пациентов (кровотечение считалось большим, если оно сопровождалось снижением содержания гемоглобина на 2 г/л и более, требовало переливания 2 или более доз компонентов крови, а также, если оно было забрюшинным или внутричерепным). Некоторые из этих случаев были летальными. Как и при применении других антикоагулянтов при применении эноксапарина натрия возможно возникновение кровотечения, особенно при наличии факторов риска, способствующих развитию кровотечения, при проведении инвазивных процедур или применении препаратов, нарушающих гемостаз (см. разделы «Взаимодействие с другими лекарственными средствами» и «Особые указания»). При описании кровотечений ниже знак «*» означает указание на следующие виды кровотечений: гематома, экхимозы (кроме развившихся в месте инъекции), раневые гематомы, гематурия, носовые кровотечения, желудочно-кишечные кровотечения.
Очень часто — кровотечения* при профилактике венозных тромбозов у хирургических пациентов и лечении тромбоза глубоких вен с тромбоэмболией или без неё.
Часто — кровотечения* при профилактике венозных тромбозов у пациентов, находящихся на постельном режиме, и при лечении нестабильной стенокардии, инфаркта миокарда без зубца Q и инфаркта миокарда с подъёмом сегмента ST.
Нечасто — забрюшинные кровотечения и внутричерепные кровоизлияния у пациентов при лечении тромбоза глубоких вен с тромбоэмболией лёгочной артерии или без неё, а также при инфаркте миокарда с подъёмом сегмента ST.
Редко — забрюшинные кровотечения при профилактике венозных тромбозов у хирургических пациентов и при лечении стенокардии, инфаркта миокарда без зубца Q.
Тромбоцитопения и тромбоцитоз
Очень часто — тромбоцитоз (количество тромбоцитов в периферической крови более 400 × 109/л) при профилактике венозных тромбозов у хирургических пациентов и лечении тромбоза глубоких вен с тромбоэмболией лёгочной артерии или без неё.
Часто — тромбоцитоз при лечении пациентов с острым инфарктом миокарда с подъёмом сегмента ST. Тромбоцитопения при профилактике венозных тромбозов у хирургических пациентов и лечении тромбоза глубоких вен с тромбоэмболией лёгочной артерии или без неё, а также при остром инфаркте миокарда с подъёмом сегмента ST.
Нечасто — тромбоцитопения при профилактике венозных тромбозов у пациентов, находящихся на постельном режиме и при лечении нестабильной стенокардии, инфаркта миокарда без зубца Q.
Очень редко — аутоиммунная тромбоцитопения при лечении пациентов с острым инфарктом миокарда с подъёмом сегмента ST.
Другие клинически значимые нежелательные реакции вне зависимости от показаний
Нежелательные реакции, представленные ниже, сгруппированы по системно-органным классам, даны с указанием определённой выше частоты их возникновения и в порядке уменьшения их тяжести.
Нарушения со стороны крови и лимфатической системы
Часто — кровотечение, тромбоцитопения, тромбоцитоз.
Редко — случаи развития аутоиммунной тромбоцитопении с тромбозом; в некоторых случаях тромбоз осложнялся развитием инфаркта органов или ишемии конечностей (см. раздел «Особые указания», подраздел «Контроль количества тромбоцитов в периферической крови»).
Нарушения со стороны иммунной системы
Часто — аллергические реакции.
Нарушения со стороны печени и желчевыводящих путей
Очень часто — повышение активности «печёночных» ферментов, главным образом повышение активности трансаминаз, более чем в три раза превышающее верхнюю границу нормы.
Нарушения со стороны кожи и подкожных тканей
Часто — крапивница, кожный зуд, эритема.
Нечасто — буллёзный дерматит.
Общие расстройства и нарушения в месте введения
Часто — гематома в месте инъекции, боль в месте инъекции, отёк в месте инъекции, кровотечение, реакции повышенной чувствительности, воспаление, образование уплотнений в месте инъекции.
Нечасто — раздражение в месте инъекции, некроз кожи в месте инъекции.
Данные, полученные в пострегистрационный период
Следующие нежелательные реакции отмечались при постмаркетинговом применении препарата. Об этих побочных реакциях имелись спонтанные сообщения.
Нарушения со стороны иммунной системы
Редко — анафилактические/анафилактоидные реакции, включая шок.
Нарушения со стороны нервной системы
Часто — головная боль.
Нарушения со стороны сосудов
Редко — при применении эноксапарина натрия на фоне спинальной/эпидуральной анестезии или спинальной пункции отмечались случаи развития спинальной гематомы (или нейроаксиальной гематомы). Эти реакции приводили к развитию неврологических нарушений различной степени тяжести, включая стойкий или необратимый паралич (см. раздел «Особые указания»).
Нарушения со стороны крови или лимфатической системы
Часто — геморрагическая анемия.
Редко — эозинофилия.
Нарушения со стороны кожи и подкожных тканей
Редко — алопеция; в месте инъекции может развиться кожный васкулит, некроз кожи, которым обычно предшествует появление пурпуры или эритематозных папул (инфильтрированных и болезненных). В этих случаях терапию препаратом следует прекратить. Возможно образование твёрдых воспалительных узелков-инфильтратов в месте инъекции препарата, которые исчезают через несколько дней и не являются основанием для отмены препарата.
Нарушения со стороны печени и желчевыводящих путей
Нечасто — гепатоцеллюлярное поражение печени.
Редко — холестатическое поражение печени.
Нарушения со стороны скелетно-мышечной и соединительной ткани
Редко — остеопороз при длительной терапии (более трёх месяцев).
Лабораторные и инструментальные данные
Редко — гиперкалиемия.
Передозировка
Случайная передозировка препаратом при внутривенном, экстракорпоральном или подкожном применении может привести к геморрагическим осложнениям. При приёме внутрь даже в больших дозах всасывание препарата маловероятно. Антикоагулянтные эффекты можно в основном нейтрализовать путём медленного внутривенного введения протамина сульфата, доза которого зависит от дозы введённого препарата. Один мг (1 мг) протамина сульфата нейтрализует антикоагулянтный эффект одного мг (1 мг) препарата, если эноксапарина натрия вводился не более чем за 8 ч до введения протамина. 0,5 мг протамина нейтрализует антикоагулянтный эффект 1 мг препарата, если с момента введения последнего прошло более 8 ч или при необходимости введения второй дозы протамина. Если же после введения эноксапарина натрия прошло 12 ч и более, введения протамина не требуется. Однако даже при введении больших доз протамина сульфата, анти-Ха активность препарата полностью не нейтрализуется (максимально на 60 %).
Взаимодействие с другими лекарственными средствами
Эноксапарин натрия нельзя смешивать с другими препаратами!
Нерекомендуемые комбинации
Препараты, влияющие на гемостаз (салицилаты системного действия, ацетилсалициловая кислота в дозах, оказывающих противовоспалительное действие, нестероидные противовоспалительные препараты, включая кеторолак, другие тромболитики (альтеплаза, ретеплаза, стрептокиназа, тенектеплаза, урокиназа)), рекомендуется отменить до начала терапии эноксапарином натрия. При необходимости одновременного применения с эноксапарином натрия следует соблюдать осторожность и проводить тщательное клиническое наблюдение и мониторинг соответствующих лабораторных показателей.
Комбинации, требующие соблюдения осторожности
-
Прочие лекарственные препараты, влияющие на гемостаз, такие как:
◦ ингибиторы агрегации тромбоцитов, включая ацетилсалициловую кислоту в дозах, оказывающих антиагрегантное действие (кардиопротекция), клопидогрел, тиклопидин и антагонисты гликопротеина IIb/IIIа рецепторов, показанные при остром коронарном синдроме, вследствие повышенного риска кровотечения;
◦ декстран с молекулярной массой 40 кДа;
◦ системные глюкокортикостероиды.
- Лекарственные препараты, повышающие содержание калия
При одновременном применении с лекарственными препаратами, повышающими содержание калия в сыворотке крови, следует проводить клинический и лабораторный контроль.
Особые указания
Общие
Низкомолекулярные гепарины не являются взаимозаменяемыми, так как они различаются по процессу производства, молекулярной массе, специфической анти-Ха активности, единицам дозирования и режиму дозирования, с чем связаны различия в их фармакокинетике и биологической активности (антитромбиновая активность и взаимодействие с тромбоцитами). Поэтому требуется строго выполнять рекомендации по применению для каждого препарата, относящегося к классу низкомолекулярных гепаринов.
Кровотечение
Как и при применении других антикоагулянтов, при введении препарата возможно развитие кровотечений любой локализации (см. раздел «Побочное действие»). При развитии кровотечения необходимо найти его источник и назначить соответствующее лечение. Эноксапарин натрия, как и другие антикоагулянты, следует применять с осторожностью при состояниях с повышенным риском кровотечения, таких как:
- нарушения гемостаза;
- язвенная болезнь в анамнезе;
- недавно перенесённый ишемический инсульт;
- тяжёлая артериальная гипертензия;
- диабетическая ретинопатия;
- нейрохирургическое или офтальмологическое оперативное вмешательство;
- одновременное применение препаратов, влияющих на гемостаз (см. раздел «Взаимодействие с другими лекарственными средствами»).
Кровотечения у пациентов пожилого возраста
При применении препарата в профилактических дозах у пациентов пожилого возраста не отмечено увеличение риска развития кровотечений. При применении препарата в терапевтических дозах у пациентов пожилого возраста (особенно в возрасте 80 лет и старше) существует повышенный риск развития кровотечений. Рекомендуется проведение тщательного наблюдения за состоянием таких пациентов (см. раздел «Фармакокинетика» и раздел «Способ применения и дозы», подраздел «Пациенты пожилого возраста»).
Одновременное применение других препаратов, влияющих на гемостаз
Применение препаратов, влияющих на гемостаз (салицилаты системного действия, в том числе ацетилсалициловая кислота в дозах, оказывающих противовоспалительное действие, нестероидные противовоспалительные препараты, включая кеторолак, другие тромболитики (альтеплаза, ретеплаза, стрептокиназа, тенектеплаза, урокиназа)), рекомендуется отменить до начала лечения эноксапарином натрия за исключением случаев, когда их применение является необходимым. Если показаны комбинации эноксапарина натрия с этими препаратами, то следует проводить тщательное клиническое наблюдение и мониторинг соответствующих лабораторных показателей.
Почечная недостаточность
У пациентов с нарушением функции почек существует риск развития кровотечения в результате увеличения системной экспозиции эноксапарина натрия. У пациентов с тяжёлыми нарушениями функции почек (клиренс креатинина ≥15 и <30 мл/мин) отмечается значительное увеличение экспозиции эноксапарина натрия, поэтому рекомендуется проводить коррекцию дозы как при профилактическом, так и терапевтическом применении препарата. Хотя не требуется проводить коррекцию дозы у пациентов с лёгкими и умеренными нарушениями функции почек (клиренс креатинина 30–50 мл/мин или 50–80 мл/мин), рекомендуется проведение тщательного контроля состояния таких пациентов, и может рассматриваться проведение биологического мониторинга с измерением анти-Ха активности (см. разделы «Фармакокинетика» и «Способ применения и дозы», подраздел «Пациенты с нарушениями функции почек»). Применение эноксапарина натрия не рекомендуется пациентам с терминальной стадией хронической болезни почек (клиренс креатинина <15 мл/мин) ввиду отсутствия данных, кроме случаев профилактики тромбообразования в системе экстракорпорального кровообращения во время гемодиализа.
Низкая масса тела
Отмечалось увеличение экспозиции эноксапарина натрия при его профилактическом применении у женщин с массой тела менее 45 кг и у мужчин с массой тела менее 57 кг, что может приводить к повышенному риску развития кровотечений. Рекомендуется проведение тщательного контроля состояния таких пациентов.
Пациенты с ожирением
Пациенты с ожирением имеют повышенный риск развития тромбозов и эмболий. Безопасность и эффективность применения эноксапарина натрия в профилактических дозах у пациентов с ожирением (ИМТ более 30 кг/м2) до конца не определена и нет общего мнения по коррекции дозы. Этих пациентов следует внимательно наблюдать на предмет развития симптомов и признаков тромбозов и эмболий.
Контроль количества тромбоцитов в периферической крови
Риск развития антитело-опосредованной гепарин-индуцированной тромбоцитопении существует и при применении низкомолекулярных гепаринов, при этом этот риск выше у пациентов, перенёсших операции на сердце, и пациентов с онкологическими заболеваниями. Если развивается тромбоцитопения, то её обычно выявляют между 5-м и 21-м днями после начала терапии эноксапарином натрия. В связи с этим рекомендуется регулярно контролировать количество тромбоцитов в периферической крови до начала лечения препаратом и во время его применения. Следует определять количество тромбоцитов в крови при наличии симптомов, указывающих на ГИТ (новый эпизод артериальных и/или венозных тромбоэмболических осложнений, болезненное поражение кожи в месте инъекции, аллергическая или анафилактическая реакция при лечении). При возникновении указанных симптомов следует проинформировать лечащего врача. При наличии подтверждённого значительного снижения количества тромбоцитов (на 30–50 % по сравнению с исходным показателем) необходимо немедленно отменить эноксапарин натрия и перевести пациента на другую антикоагулянтную терапию без применения гепаринов.
Спинальная/эпидуральная анестезия
Описаны случаи возникновения нейроаксиальных гематом при применении препарата при одновременном проведении спинальной/эпидуральной анестезии с развитием длительно существующего или необратимого паралича. Риск возникновения этих явлений снижается при применении препарата в дозе 40 мг или ниже. Риск повышается при применении более высоких доз препарата, а также при использовании постоянных катетеров после операции, или при одновременном применении дополнительных препаратов, влияющих на гемостаз, таких как нестероидные противовоспалительные препараты (см. раздел «Взаимодействие с другими лекарственными средствами»). Риск также повышается при травматически проведённой или повторной спинномозговой пункции или у пациентов, имеющих в анамнезе указания на перенесённые операции в области позвоночника или деформацию позвоночника. Для снижения возможного риска кровотечения, связанного с применением эноксапарина натрия и проведением эпидуральной или спинальной анестезии/анальгезии необходимо учитывать фармакокинетический профиль препарата (см. раздел «Фармакокинетика»). Установку или удаление катетера лучше проводить при низком антикоагулянтном эффекте эноксапарина натрия, однако точное время для достижения достаточного снижения антикоагулянтного эффекта у разных пациентов неизвестно. Следует дополнительно учитывать, что у пациентов с клиренсом креатинина 15–30 мл/мин выведение эноксапарина натрия замедляется. Если по назначению врача применяется антикоагулянтная терапия во время проведения эпидуральной/спинальной анестезии или люмбальной пункции, необходимо постоянное наблюдение за пациентом для выявления любых неврологических симптомов, таких как боли в спине, нарушение сенсорных и моторных функций (онемение или слабость в нижних конечностях), нарушение функции кишечника и/или мочевого пузыря. Пациента необходимо проинструктировать о необходимости немедленного информирования врача при возникновении вышеописанных симптомов. При подозрении на симптомы, характерные для гематомы спинного мозга, необходимы срочная диагностика и лечение, включая, при необходимости, декомпрессию спинного мозга.
Гепарин-индуцированная тромбоцитопения
Применение эноксапарина натрия у пациентов, имеющих в анамнезе указания на наличие гепарин-индуцированной тромбоцитопении в течение последних 100 дней или при наличии циркулирующих антител, противопоказано (см. раздел «Противопоказания»). Циркулирующие антитела могут персистировать несколько лет. Эноксапарин натрия следует применять с особой осторожностью у пациентов, имеющих в анамнезе (более чем 100 дней) гепарин-индуцированную тромбоцитопению без циркулирующих антител. Решение о применении эноксапарина натрия в данной ситуации должно быть принято только после оценки соотношения польза/риск и при отсутствии безгепариновой (не содержащей гепарин) альтернативной терапии.
Чрескожная коронарная ангиопластика
С целью минимизации риска кровотечения, связанного с инвазивной сосудистой инструментальной манипуляцией при лечении нестабильной стенокардии и инфаркта миокарда без зубца Q и острого инфаркта миокарда с подъёмом сегмента ST, эти процедуры следует проводить в интервалах между введением препарата. Это необходимо для того, чтобы достигнуть гемостаза в месте введения катетера после проведения чрескожного коронарного вмешательства. При использовании закрывающего устройства интродьюсер бедренной артерии может быть удалён немедленно. При применении мануальной (ручной) компрессии интродьюсер бедренной артерии следует удалить через 6 ч после последней внутривенной или подкожной инъекции эноксапарина натрия. Если лечение эноксапарином натрия продолжается, то следующую дозу следует вводить не ранее, чем через 6–8 ч после удаления интродьюсера бедренной артерии. Необходимо следить за местом введения интродьюсера, чтобы своевременно выявить признаки кровотечения и образования гематомы.
Пациенты с механическими искусственными клапанами сердца
Применение препарата для профилактики тромбообразования у пациентов с механическими искусственными клапанами сердца изучено недостаточно. Имеются отдельные сообщения о развитии тромбоза клапанов сердца у пациентов с механическими искусственными клапанами сердца на фоне терапии эноксапарином натрия для профилактики тромбообразования. Ввиду недостаточности клинических данных и наличия неоднозначных факторов, включая основное заболевание, оценка таких сообщений затруднена.
Беременные женщины с механическими искусственными клапанами сердца
Применение препарата для профилактики тромбообразования у беременных женщин с механическими искусственными клапанами сердца изучено недостаточно. В клиническом исследовании беременных женщин с механическими искусственными клапанами сердца при применении эноксапарина натрия в дозе 1 мг/кг массы тела 2 раза в сутки для уменьшения риска тромбозов и эмболий, у 2-х из 8-ми женщин образовались тромбы, приведшие к блокированию клапанов сердца и к смерти матери и плода. Имеются отдельные постмаркетинговые сообщения о тромбозе клапанов сердца у беременных женщин с механическими искусственными клапанами сердца, получавших лечение эноксапарином для профилактики тромбообразования. Беременные женщины с механическими искусственными клапанами сердца имеют высокий риск развития тромбоза и эмболий.
Некроз кожи/кожный васкулит
Сообщалось о развитии некроза кожи и кожного васкулита при применении низкомолекулярных гепаринов. В случае развития некроза кожи/кожного васкулита применение препарата следует прекратить.
Острый инфекционный эндокардит
Применение гепарина не рекомендуется у пациентов с острым инфекционным эндокардитом вследствие риска развития геморрагического инсульта. В случае, если применение препарата считается абсолютно необходимым, решение следует принимать только после тщательной индивидуальной оценки соотношения пользы и риска.
Лабораторные тесты
В дозах, применяемых для профилактики тромбоэмболических осложнений, препарат существенно не влияет на время кровотечения и показатели свёртывания крови, а также на агрегацию тромбоцитов или на связывание их с фибриногеном. При повышении дозы может удлиняться АЧТВ и активированное время свёртывания крови. Увеличение АЧТВ и активированного времени свёртывания не находятся в прямой линейной зависимости от увеличения антикоагулянтной активности препарата, поэтому нет необходимости в их мониторинге.
Гиперкалиемия
Гепарины могут подавлять секрецию альдостерона надпочечниками, что приводит к развитию гиперкалиемии, особенно у пациентов с сахарным диабетом, хронической почечной недостаточностью, предшествующим метаболическим ацидозом, принимающих лекарственные препараты, повышающие содержание калия (см. раздел «Взаимодействие с другими лекарственными препаратами»). Следует регулярно контролировать содержание калия в плазме крови, особенно у пациентов группы риска.
Профилактика венозных тромбозов и эмболий у пациентов с острыми терапевтическими заболеваниями, находящихся на постельном режиме
В случае развития острой инфекции, острых ревматических состояний профилактическое применение эноксапарина натрия оправдано только, если вышеперечисленные состояния сочетаются с одним из нижеперечисленных факторов риска венозного тромбообразования:
- возраст более 75 лет;
- злокачественные новообразования;
- тромбозы и эмболии в анамнезе;
- ожирение;
- гормональная терапия;
- сердечная недостаточность;
- хроническая дыхательная недостаточность.
Нарушение функции печени
Эноксапарин натрия следует с осторожностью применять у пациентов с нарушениями функции печени вследствие увеличения риска кровотечений. Коррекция дозы на основании мониторирования анти-Ха активности у пациентов с циррозом печени является ненадёжной и не рекомендуется.
Влияние на способность управлять транспортными средствами, механизмами
Эноксапарин натрия не оказывает влияния на способность управлять транспортными средствами и механизмами.
Форма выпуска
Раствор для инъекций, 10000 анти-Ха МЕ/мл.
По 0,2 мл (2000 анти-Ха ME), 0,3 мл (3000 анти-Ха ME), 0,4 мл (4000 анти-Ха ME), 0,5 мл (5000 анти-Ха ME), 0,6 мл (6000 анти-Ха ME), 0,7 мл (7000 анти-Ха ME), 0,8 мл (8000 анти-Ха ME) или 1,0 мл (10000 анти-Ха ME) в шприцы стеклянные стерильные, укомплектованные устройствами предохранительными и защитными этикетками для игл, или без устройств предохранительных и защитных этикеток для игл. По 2 шприца в контурную ячейковую упаковку из плёнки поливинилхлоридной или полиэтилентерефталатной с плёнкой полимерной или фольгой алюминиевой лакированной, или без плёнки полимерной и фольги алюминиевой лакированной. По 1, 2, 3, 5 или 10 контурных ячейковых упаковок вместе с инструкцией по применению в пачке из картона. По 0,2 мл (2000 анти-Ха ME), 0,3 мл (3000 анти-Ха ME), 0,4 мл (4000 анти-Ха ME), 0,5 мл (5000 анти-Ха ME), 0,6 мл (6000 анти-Ха ME), 0,7 мл (7000 анти-Ха ME), 0,8 мл (8000 анти-Ха ME) или 1,0 мл (10000 анти-Ха ME) в ампулы из бесцветного или тёмного стекла. По 5 или 10 ампул из стекла в контурную ячейковую упаковку из плёнки поливинилхлоридной или полиэтилентерефталатной с плёнкой полимерной или фольгой алюминиевой лакированной, или без плёнки полимерной и фольги алюминиевой лакированной, или в форму из картона. По 1, 2, 3 или 4 контурные ячейковые упаковки или формы из картона с 5 ампулами или по 1 или 2 контурные ячейковые упаковки или формы из картона с 10 ампулами вместе с инструкцией по применению и скарификатором ампульным или без него в пачке из картона.
Хранение
При температуре не выше 25 °С. Хранить в недоступном для детей месте.
Срок годности
3 года. Не применять после окончания срока годности!
Условия отпуска из аптек
Отпускают по рецепту
Производитель
Гротекс, ООО, Российская Федерация
Владелец регистрационного удостоверения
ООО «Гротекс», Россия 195279, Санкт-Петербург. Индустриальный пр., д. 71, корп. 2, лит. А
Производитель/Организация, принимающая претензии
ООО «Гротекс», Россия 195279, Санкт-Петербург. Индустриальный пр., д. 71, корп. 2, лит. А
Способ применения и дозировка
Индивидуальный. Вводят п/к в передне- или заднелатеральную область брюшной стенки на уровне пояса.
Фармакотерапевтическая группа
Антикоагулянт прямого действия. Относится к группе низкомолекулярных гепаринов (молекулярной массой около 4500 дальтон). Оказывает антитромботическое действие. Обладает выраженной активностью в отношении фактора Xa и слабой активностью в отношении фактора IIa. В отличие от нефракционированного стандартного гепарина антиагрегантная активность выражена сильнее, чем антикоагулянтная активность. Не оказывает влияния на агрегацию тромбоцитов.
Показания
Профилактика тромбоэмболий, особенно в ортопедической практике и общей хирургии; лечение тромбозов глубоких вен; профилактика гиперкоагуляции в системе экстракорпоральной циркуляции при проведении гемодиализа. Лечение нестабильной стенокардии и инфаркта миокарда без патологического зубца Q на ЭКГ (в сочетании с ацетилсалициловой кислотой).
Противопоказания
Состояния с высоким риском развития неконтролируемых кровотечений (в том числе язвенные поражения ЖКТ, недавно перенесенный геморрагический инсульт); повышенная чувствительность к эноксапарину.
Побочное действие
Со стороны свертывающей системы крови: редко — умеренная асимптоматическая тромбоцитопения. Со стороны печени: редко — обратимое повышение уровня активности печеночных ферментов. Аллергические реакции: редко — кожная сыпь, зуд Местные реакции: редко — воспалительная реакция; в единичных случаях — некроз.

