Локализованная склеродермия

Версия: Клинические рекомендации РФ 2013-2017 (Россия)
Категории МКБ:
Локализованная склеродермия [morphea] (L94.0)
Разделы медицины:
Дерматовенерология
Общая информация
Краткое описание
РОССИЙСКОЕ ОБЩЕСТВО ДЕРМАТОВЕНЕРОЛОГОВ И КОСМЕТОЛОГОВ
ФЕДЕРАЛЬНЫЕ КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ВЕДЕНИЮ БОЛЬНЫХ ЛОКАЛИЗОВАННОЙ СКЛЕРОДЕРМИЕЙ
Шифр по Международной классификации болезней МКБ-10
L94.0
ОПРЕДЕЛЕНИЕ
Локализованная склеродермия – хроническое заболевание соединительной ткани, которое характеризуется появлением на различных участках тела очагов локального воспаления (эритемы, отёка) с последующим формированием в них склероза и / или атрофии кожи и подлежащих тканей.
Облачная МИС «МедЭлемент»
Облачная МИС «МедЭлемент»

Версия: Клинические рекомендации РФ 2013-2017 (Россия)
Категории МКБ:
Локализованная склеродермия [morphea] (L94.0)
Разделы медицины:
Дерматовенерология
Общая информация
Краткое описание
РОССИЙСКОЕ ОБЩЕСТВО ДЕРМАТОВЕНЕРОЛОГОВ И КОСМЕТОЛОГОВ
ФЕДЕРАЛЬНЫЕ КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ВЕДЕНИЮ БОЛЬНЫХ ЛОКАЛИЗОВАННОЙ СКЛЕРОДЕРМИЕЙ
Шифр по Международной классификации болезней МКБ-10
L94.0
ОПРЕДЕЛЕНИЕ
Локализованная склеродермия – хроническое заболевание соединительной ткани, которое характеризуется появлением на различных участках тела очагов локального воспаления (эритемы, отёка) с последующим формированием в них склероза и / или атрофии кожи и подлежащих тканей.
Облачная МИС «МедЭлемент»
Облачная МИС «МедЭлемент»

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место — 800 RUB / 5500 KZT / 27 BYN в месяц
Классификация
Общепринятой классификации не существует.
Этиология и патогенез
Этиология локализованной склеродермии не известна. В патогенезе заболевания основную роль отводят аутоиммунным нарушениям, повышенному синтезу и отложению в коже и подкожной клетчатке коллагена и других компонентов соединительной ткани, микроциркуляторным расстройствам.
Заболеваемость локализованной склеродермией составляет 2,7 случаев на 100000 населения, распространенность – 2 случая на 1000 населения [1]. В Российской Федерации заболеваемость склеродермией в 2014 году составила 3,9 случаев на 100000 населения [2].
Заболевание встречается у представителей любой расы, чаще у женщин, чем у мужчин (2,6:1).
Клиническая картина
Cимптомы, течение
Наиболее часто выделяют следующие формы локализованной склеродермии:
Бляшечная склеродермия
— очаговая (морфеа);
— узловатая (келоидоподобная)
Линейная склеродермия
— полосовидная форма;
— склеродермия по типу «удар саблей»
Генерализованная (многоочаговая) склеродермия
Глубокая склеродермия
Пансклеротическая склеродермия
Буллёзная склеродермия
Идиопатическая атрофодермия Пазини-Пьерини
Прогрессирующая гемиатрофия лица Парри-Ромберга
Склероатрофический лихен
У некоторых больных одновременно могут наблюдаться проявления нескольких форм заболевания.
Больные могут предъявлять жалобы на зуд, болезненность, чувство покалывания и стянутости кожи, ограничение движений в суставах, изменение объема и деформацию пораженных участков.
Принято выделять три стадии развития очагов склеродермии: эритемы/отёка, склероза (уплотнения) и атрофии кожи. Однако такая стадийность наблюдается не у всех больных. В типичных случаях заболевание начинается с появления на коже розовых, розовато-сиреневых, ливидных или гиперпигментированных пятен округлой и/или полосовидной формы, иногда – с явлениями отека. В стадию склероза в пятнах образуются очаги уплотнения кожи цвета слоновой кости с гладкой поверхностью и характерным восковидным блеском. По периферии очагов часто наблюдается воспалительный венчик лилового или розовато-сиреневого цвета, являющийся показателем активности процесса. В местах поражения кожа плохо собирается в складку, потоотделение уменьшено или отсутствует, нарушается функция сальных желёз и рост волос. С течением времени уплотнение кожи может уменьшаться. В стадию атрофии в очагах склеродермии развивается атрофия кожи, появляются телеангиэктазии, стойкая гипер- или гипопигментация.
При формировании глубоких очагов склеродермии кроме кожи в патологический процесс могут вовлекаться подлежащие ткани: подкожная клетчатка, фасции, мышцы и кости.
Бляшечная склеродермия характеризуется появлением на голове, туловище или конечностях очагов эритемы и/или индурации кожи округлой формы с типичной клинической картиной.
Узловатая (келоидоподобная) склеродермия характеризуется образованием на коже единичных или множественных узелков или узлов, внешне напоминающих келоидные рубцы. Очаги поражения развиваются, как правило, у больных, не имеющих склонности к развитию келоидов; их появление не связано с предшествующей травмой. Кожа в очагах склеродермии имеет телесный цвет или пигментирована; наиболее частая локализация — шея, туловище, верхние конечности.
При линейной склеродермии на коже возникают очаги эритемы и/или склероза линейной формы, локализующиеся, как правило, на одной половине тела или по ходу нервно-сосудистого пучка. Очаги поражения чаще всего возникают на голове или конечностях.
Линейная склеродермия на лице и волосистой части головы обычно выглядит в виде плотного тяжа склерозированной кожи, в которой отсутствует рост волос (форма «удар саблей»). Со временем поверхность очага сглаживается, образуя западение, обусловленное атрофией кожи, мышц и костной ткани.
При генерализованной склеродермии наблюдается появление множественных очагов эритемы и/или индурации кожи, занимающих несколько областей тела и нередко сливающихся в обширные очаги поражения.
Для глубокой склеродермии характерно появление глубоких очагов уплотнения кожи и подкожной клетчатки. Кожа над очагами незначительно пигментирована или не изменена.
Пансклеротическая инвалидизирующая склеродермия является наиболее тяжёлой формой заболевания, при которой поражаются все слои кожи и подлежащих тканей вплоть до костей, часто формируются контрактуры суставов с деформацией конечностей и длительно существующие язвы. Эта форма склеродермии обычно наблюдается у детей, быстро прогрессирует, резистентна к терапии и нередко заканчивается фатальным исходом.
Буллёзная склеродермия характеризуется появлением в очагах склеродермии прозрачных пузырей, нередко сопровождающихся геморрагиями.
Идиопатическая атрофодермия Пазини-Пьерини многими экспертами считается поверхностным вариантом локализованной склеродермии. Клинически она проявляется длительно существующими, незначительно западающими пятнистыми очагами коричневого или серо-коричневого цвета с фиолетово-сиреневым оттенком, в которых отсутствует уплотнение кожи. Очаги располагаются чаще всего на туловище и верхних конечностях.
Прогрессирующая гемиатрофия лица Парри-Ромберга считается одной из наиболее тяжёлых и резистентных к терапии форм заболевания, при которой развивается прогрессирующее западение и деформация половины лица с вовлечением в патологический процесс кожи, подкожной клетчатки, мышц и костей лицевого скелета. Указанные симптомы могут сочетаться с другими проявлениями локализованной склеродермии, а также сопровождаться поражением глаз и различными неврологическими нарушениями, включая эпилепсию.
При склероатрофическом лихене Цумбуша (синонимы: болезнь белых пятен, каплевидная склеродермия) участки поражения представлены перламутрово-белыми пятнами, папулами или бляшками с блестящей поверхностью, иногда сливающимися в очаги с фестончатыми очертаниями и четкими границами. Вокруг высыпаний может наблюдаться эритематозный венчик розового или красно-лилового цвета. Кожа в очагах поражения часто атрофирована, легко собирается в складку по типу «смятой папиросной бумаги».
Диагностика
Диагноз основывается на данных анамнеза и клинической картине заболевания.
Для исключения системной склеродермии и других болезней соединительной ткани необходима консультация ревматолога.
Для выявления сопутствующих заболеваний и противопоказаний к лечению необходимы консультации:
— терапевта (при назначении физиотерапии обязательна);
— эндокринолога (при назначении физиотерапии обязательна);
— гинеколога (при назначении физиотерапии обязательна);
— офтальмолога (при назначении физиотерапии обязательна);
— невропатолога;
— гастроэнтеролога;
— оториноларинголога;
— стоматолога.
При наличии сгибательных контрактур, деформаций скелета и косметических дефектов необходима консультация хирурга для решения вопроса о проведении хирургической коррекции.
Для уточнения активности патологического процесса, выявления осложнений заболевания, исключения системной склеродермии и других болезней соединительной ткани, а также противопоказаний к лечению необходимо проведение следующих исследований.
Обязательные лабораторные исследования:
— клинический анализ крови;
— клинический анализ мочи;
— биохимический анализ крови.
Дополнительные лабораторные и инструментальные исследования:
— гистологическое исследование кожи (в сомнительных случаях);
— определение антинуклеарного фактора с помощью метода непрямой иммунофлуоресценции на перевиваемой клеточной линии HEp-2 (для исключения диффузных болезней соединительной ткани);
— исследование содержания в сыворотке крови иммуноглобулинов IgA, IgM, IgG, ревматоидного фактора;
— исследование в сыворотке крови уровня антител к тиреоглобулину и тиреоидной пероксидазе (по возможности исследование содержания других антител: антител к париетальным клеткам желудка и др.);
— анализ крови на антинуклеарные антитела;
— анализ крови на антитела к топоизомеразе I (анти-Scl 70) и антицентромерные антитела (для исключения системной склеродермии);
— обследование на боррелиоз;
— УЗИ органов брюшной полости, почек, щитовидной железы;
— электрокардиография;
— рентгенография грудной клетки, областей деформации скелета, черепа;
— электроэнцефалография;
— компьютерная томография;
— магнитно-резонансная томография.
Дифференциальный диагноз
Локализованную склеродермию следует дифференцировать с такими заболеваниями, как келоидные и гипертрофические рубцы, рубцовая алопеция, системная склеродермия и другие болезни соединительной ткани, диффузный эозинофильный фасциит Шульмана, скередема Бушке, липодерматосклероз, склеромикседема, липоидный некробиоз, панникулит.
Реже локализованную склеродермию дифференцируют от лайм-боррелиоза, склеродермоподобной формы хронической реакции “трансплантат против хозяина”, радиационного фиброза, склеродермоподобной формы базальноклеточного рака кожи, синдрома «жёсткой кожи», нефрогенного системного фиброза, поздней кожной порфирии, саркоидоза, амилоидоза, синдрома Вернера, фенилкетонурии, соединительнотканного невуса, синдрома POEMS, индуцированных склеродермоподобных заболеваний, вызванных применением лекарственных средств и пищевых добавок (блеомицина, витамина К, L-триптофана), использованием силиконовых протезов, контактом с химикатами (хлорвинилом, органическими растворителями) и др.
Лечение
Цели лечения
— остановить прогрессирование заболевания;
— снизить активность патологического процесса;
— уменьшить площадь поражения кожи и выраженность клинических симптомов заболевания;
— предотвратить развитие осложнений;
— улучшить качество жизни больных.
Общие замечания по терапии
Лечение необходимо подбирать индивидуально каждому пациенту в зависимости от формы, стадии и тяжести течения заболевания, а также локализации очагов поражения.
Больным бляшечной, генерализованной и линейной склеродермией, а также атрофодермией Пазини-Пьерини и экстрагенитальным склероатрофическим лихеном при неглубоком поражении кожи и подлежащих тканей рекомендуется проведение курсового медикаментозного лечения (с включением пенициллина, гиалуронидазы, вазоактивных и наружных средств) или фототерапии (УФА-1 терапии или ПУВА-терапии).
Больным с активным, быстро прогрессирующим течением заболевания и выраженными воспалительными явлениями (главным образом, при наличии линейных или множественных очагов склеродермии) показано включение в комплексное лечение глюкокортикостероидных препаратов системного действия.
Больным тяжёлыми формами локализованной склеродермии с формированием глубокого поражения кожи и подлежащих тканей (линейная, генерализованная, пансклеротическая склеродермия, прогрессирующая гемиатрофия лица Парри-Ромберга) назначают лечение метотрексатом в виде монотерапии или в комбинации с глюкокортикостероидными препаратами системного действия.
При наличии эрозивно-язвенных дефектов и поверхностной атрофии кожи показано применение стимуляторов регенерации тканей, при сухости кожи — использование увлажняющих и смягчающих наружных средств.
Иногда может наблюдаться спонтанный регресс склероза кожи или полное разрешение очагов поражения.
Показания к госпитализации
Генерализованные формы склеродермии
Схемы лечения
Медикаментозная терапия
Системная терапия
1. Метотрексат (A)
При тяжёлых формах локализованной склеродермии (линейная, генерализованная, пансклеротическая склеродермия, прогрессирующая гемиатрофия лица Парри-Ромберга) эффективным методом лечения является применение метотрексата в виде монотерапии или в комбинации с глюкокортикостероидными препаратами системного действия [3].
Согласно опубликованным данным, эффективны следующие схемы лечения метотрексатом [3-6]:
— метотрексат: взрослым — 15-25 мг, детям — 0,3-1 мг на кг массы тела (максимальная доза 25 мг) 1 раз в неделю подкожно или перорально в течение 6-12 месяцев и более
или
— метотрексат: взрослым — 15-25 мг, детям — 0,3-1 мг на кг массы тела (максимальная доза 25 мг) 1 раз в неделю подкожно или перорально в течение 6-12 месяцев и более
+
метилпреднизолон: взрослым — 1000 мг в сутки, детям — 30 мг/кг массы тела в сутки (максимальная доза 500-1000 мг) — 3 последовательных ежедневных внутривенных вливания в месяц в течение 3 месяцев (всего 9 вливаний) или 1 внутривенное вливание 1 раз в неделю в течение 12 недель (всего 12 вливаний)
или
— метотрексат: взрослым — 15-25 мг, детям — 0,3-1 мг на кг массы тела (максимальная доза 25 мг) 1 раз в неделю подкожно или перорально в течение 6-12 месяцев и более
+
преднизолон 0,5-1 мг на кг массы тела в сутки (максимальная доза 60 мг) перорально в течение 2-4 недель с последующей постепенной отменой
Примечание. В инструкциях по медицинскому применению метотрексата, метилпреднизолона и преднизолона локализованная склеродермия не включена в показания к применению препаратов.
2. Глюкокортикостероидные препараты (C)
Пероральное применение глюкокортикостероидных препаратов может оказать положительный эффект при активном, быстро прогрессирующем течении локализованной склеродермии, однако после отмены препаратов высока частота рецидивов [7-8].
— преднизолон 0,3-1 мг на кг массы тела перорально 1 раз в сутки в течение 3-12 месяцев
В отдельных случаях рекомендуется введение глюкокортикостероидных препаратов непосредственно в очаг склеродермии (D) [9].
— бетаметазон 0,2 мл/см2 (но не более 1 мл) — введение в очаг поражения 1 раз в месяц в течение 3 месяцев.
3. Гиалуронидаза (С)
Согласно опубликованным данным, применение гиалуронидазы может приводить к уменьшению индурации кожи в очагах склеродермии [10-12]:
— гиалуронидаза 32-64 УЕ 1 раз в сутки внутримышечно ежедневно или через день, на курс 15-20 инъекций или 64 УЕ — введение в очаг склеродермии 1 раз в 3 дня, на курс 7-10 процедур.
Гиалуронидазу можно также вводить в очаги поражения путём ультрафонофореза или электрофореза (D) [13, 14].
— фонофорез гиалуронидазы 64 УЕ гиалуронидазы растворяют в 1 мл 1% раствора новокаина, наносят на очаги поражения пипеткой и втирают, затем покрывают контактной средой (вазелиновым маслом, растительным маслом или гелем) и проводят озвучивание с частотой колебаний 880 кГц, интенсивностью 0,5-1,2 Вт/см2, экспозицией 3-10 минут на поле по лабильной методике в непрерывном режиме.
— электрофорез гиалуронидазы 64 УЕ лидазы растворяют в 30 мл дистиллированной воды, для подкисления среды до pH 5,2 добавляют 4-6 капель 0,1 н. раствора хлористоводородной кислоты, вводят в очаги склеродермии при силе тока не более 0,05 мА/см2, экспозиции 12-20 минут.
Процедуры ультрафонофореза или электрофореза гиалуронидазы проводят ежедневно или через день, на курс назначают 8-12 процедур. Возможно проведение 2-3 повторных курсов с интервалом 3-4 месяца.
4. Пеницилламин (C)
В нескольких исследованиях установлен положительный эффект при лечении больных локализованной склеродермией пеницилламином [15-17]. Однако имеются данные и об отсутствии какого-либо улучшения кожного процесса при использовании данного препарата [18].
— пеницилламин 125-500 мг перорально ежедневно или через день в течение 6-12 месяцев и более.
Учитывая довольно большое количество побочных эффектов и возможность токсического действия даже при лечении низкими дозами, пеницилламин в последние годы назначают реже, в основном, в случаях отсутствия эффекта от других терапевтических средств.
5. Пенициллин (С)
В клинической практике пенициллин применяется для лечения локализованной склеродермии в течение нескольких десятилетий, хотя публикации по эффективности его применения немногочисленны [19, 20].
— бензилпенициллина натриевая соль 300000-500000 ЕД 3-4 раза в сутки или 1 млн ЕД 2 раза в сутки внутримышечно, на курс 15-40 млн ЕД.
Проводят 2-3 курса терапии пенициллином с интервалом 1,5-4 месяца.
Примечание. В инструкции по медицинскому применению пенициллина локализованная склеродермия не включена в показания к медицинскому применению препарата.
6. Вазоактивные препараты (D)
Имеются данные об эффективности применения в комплексном лечении больных локализованной склеродермией вазоактивных препаратов [21, 22]:
— пентоксифиллин 100-200 мг перорально 3 раза в сутки или 400 мг перорально 1-2 раза в сутки в течение 4-6 недель
или
— ксантинола никотинат 75-150 мг перорально 2-3 раза в сутки в течение 4-6 недель
или
— ксантинола никотинат, раствор для инъекций 15% (300 мг) 2 мл внутримышечно 1 раз в сутки ежедневно, на курс 15-20 инъекций.
Терапию вазоактивными препаратами рекомендуется проводить повторными курсами с интервалом 3-4 месяца, всего 2-3 курса в год. Наружная терапия
1. Топические глюкокортикостероидные препараты (D)
При лечении ограниченных форм локализованной склеродермии определенный эффект оказывает наружное применение глюкокортикостероидных средств [9]:
— мометазона фуроат, крем, мазь наружно 1 раз в сутки в виде аппликаций или окклюзионных повязок
или
— алклометазона дипропионат, крем, мазь наружно 1 раз в виде аппликаций или окклюзионных повязок
или
— метилпреднизолона ацепонат, крем, мазь наружно 1 раз в сутки в виде аппликаций или окклюзионных повязок
или
— бетаметазон, крем, мазь наружно 1 раз в сутки в виде аппликаций или окклюзионных повязок
или
— клобетазола пропионат, крем, мазь наружно 1 раз в сутки в виде аппликаций или окклюзионных повязок
При назначении топических глюкокортикостероидных препаратов в виде аппликаций курс лечения составляет 4-12 недель, при использовании их в виде окклюзионных повязок – 2-3 недели.
2. Топические ингибиторы кальциневрина (A).
В рандомизированном, плацебо-контролируемом исследовании показана эффективность применения 0,1% мази такролимуса при локализованной склеродермии [23].
— такролимус, 0,1% мазь наружно 2 раза в сутки в виде аппликаций или окклюзионных повязок в течение 3 месяцев.
Примечание. В инструкции по медицинскому применению мази такролимуса локализованная склеродермия не включена в показания к применению препарата.
3. Диметилсульфоксид (С)
Лечение диметилсульфоксидом в ряде случаев может приводить к уменьшению эритемы и индурации кожи в очагах склеродермии [24].
— диметилсульфоксид: препарат растворяют в воде, применяют в виде аппликаций 25-75% водного раствора 1 раз в сутки в течение 30 минут. Длительность курса лечения составляет 3-4 недели. Терапию диметилсульфоксидом проводят повторными курсами с интервалами 1-2 месяца.
4. Стимуляторы регенерации тканей (D) [25].
— депротеинизированный гемодериват из крови телят, 5% мазь наружно 2-3 раза в сутки в течение 1-2 месяцев
или
— депротеинизированный гемолизат из крови телят, 5% мазь наружно 2-3 раза в сутки в течение 1-2 месяцев.
Немедикаментозная терапия
Физиотерапевтическое лечение
1. Ультрафиолетовая терапия дальнего длинноволнового диапазона (УФА-1 терапия, длина волны 340-400 нм) (А)
УФА-1 терапия — один из эффективных методов лечения бляшечной, генерализованной и линейной склеродермии, а также экстрагенитального склероатрофического лихена при неглубоком поражении кожи и подлежащих тканей [26, 27].
— облучения УФА-1 светом начинают с дозы 5-20 Дж/см2, последующие разовые дозы повышают на 5-15 Дж/см2 до максимальной разовой дозы 20-60 Дж/см2. Процедуры проводят с режимом 3-5 раз в неделю, курс составляет 20-60 процедур.
2. ПУВА-терапия (B)
ПУВА-терапия как с пероральным, так и с наружным применением фотосенсибилизатора, позволяет значительно улучшить состояние кожи в очагах склеродермии у больных бляшечной, линейной и генерализованной формами заболевания, а также экстрагенитальным склероатрофическим лихеном [28-31].
2.1. ПУВА-терапия с пероральным применением фотосенсибилизатора
— Амми большой плодов фурокумарины 0,8 мг на кг массы тела перорально однократно за 2 часа до облучения длинноволновым ультрафиолетовым светом (длина волны 320-400 нм)
или
— метоксален 0,6 мг на кг массы тела перорально однократно за 1,5-2 часа до облучения длинноволновым ультрафиолетовым светом (длина волны 320-400 нм).
Облучения начинают с дозы 0,25-0,5 Дж/см2, последующие разовые дозы увеличивают через каждые 2-3 сеанса на 0,25-0,5 Дж/см2 до максимальной дозы 3-6 Дж/см2. Процедуры проводят 2-4 раза в неделю, курс лечения составляет 20-60 процедур.
Примечание. В инструкциях по медицинскому применению Амми большой плодов фурокумарины и метоксалена локализованная склеродермия не включена в показания к применению препаратов.
2.2. ПУВА-терапия с наружным применением фотосенсибилизатора
— изопимпинеллин/бергаптен/ксантотоксин 0,3% спиртовой раствор наружно однократно на очаги поражения за 15-30 минут до облучения длинноволновым ультрафиолетовым светом (длина волны 320-400 нм).
Облучения начинают с дозы 0,1-0,3 Дж/см2, последующие разовые дозы увеличивают через каждые 2-3 сеанса на 0,1-0,2 Дж/см2 до максимального значения 3,5-5 Дж/см2. Процедуры проводят 2-4 раза в неделю, курс составляет 20-60 процедур.
Примечание. В инструкции по медицинскому применению раствора изопимпинеллина/бергаптена/ксантотоксина локализованная склеродермия не включена в показания к применению препарата.
УФА-1 и ПУВА-терапию проводят как в виде монотерапии, так и в комплексе с медикаментозными средствами.
3. Ультразвуковая терапия (D)
При лечении ограниченных форм локализованной склеродермии применение ультразвуковой терапии может способствовать уменьшению интенсивности клинических симптомов заболевания [13].
Озвучивание очагов поражения проводят с частотой колебаний 880 кГц, интенсивностью 0,05-0,8 Вт/см2, экспозицией 5-10 мин на поле по лабильной методике в непрерывном или импульсном режиме. Курс составляет 10-15 ежедневных процедур.
Возможно проведение повторных курсов ультразвуковой терапии с интервалом 3-4 месяца.
4. Низкоинтенсивная лазерная терапия (C).
Известно, что низкоинтенсивная лазерная терапия способна улучшать микроциркуляцию крови в коже. В отдельных работах показана эффективность применения низкоинтенсивной лазерной терапии в комплексном лечении ограниченных форм локализованной склеродермии [32].
— терапию лазерным излучением красного диапазона (длина волны 0,63-0,65 мкм) проводят по дистанционной стабильной методике, расфокусированным лучом с плотностью мощности 3-5 мВт/см2 и экспозицией 5-8 минут на поле. За процедуру облучают не более 4-5 полей при общей продолжительности воздействий не более 30 минут.
— терапию лазерным излучением инфракрасного диапазона (длина волны 0,89 мкм) проводят по дистанционной или контактной, стабильной или лабильной методике, в непрерывном или импульсном (80-150 Гц) режиме. Воздействия осуществляют по полям: при непрерывном режиме мощность излучения составляет не более 15 мВт, экспозиция на одно поле 2-5 мин, продолжительность процедуры — не более 30 минут. При импульсном режиме мощность излучения составляет 5-7 Вт/имп, экспозиция 1-3 минуты на поле, общее время воздействия — не более 10 минут. За процедуру облучают не более 4-6 полей.
Курс лазерной терапии составляет 10-15 ежедневных процедур. Повторные курсы проводят с интервалом 3-4 месяца.
Лечебная гимнастика и массаж
Лечебную гимнастику и массаж рекомендуют больным линейной формой склеродермии при ограничении движений в суставах и формировании контрактур.
Хирургическое лечение
Хирургическое лечение проводят в отдельных случаях при наличии сгибательных контрактур или косметических дефектов (при локализованной склеродермии по типу «удар саблей», прогрессирующей гемиатрофии Парри-Ромберга). Хирургические вмешательства осуществляют в неактивную стадию заболевания (при отсутствии признаков активности склеродермии в течение нескольких лет).
Особые ситуации
Лечение беременных
Лечение беременных проводится по строго обоснованным показаниям с учётом соотношения пользы и потенциального риска для матери и плода.
Проведение ПУВА-терапии при беременности и лактации противопоказано.
Лечение детей
Локализованная склеродермия, возникшая в детском возрасте, нередко протекает длительно на протяжении нескольких лет: у 30% пациентов активность заболевания сохраняется после достижения совершеннолетия [33]. Более, чем у 20% больных ювенильной локализованной склеродермией могут наблюдаться различные внекожные симптомы (суставные, неврологические, сосудистые, офтальмологические, респираторные и др.) [34].
При ювенильной склеродермии существует риск развития ряда осложнений, приводящих к инвалидизации больных: уменьшение длины и объёма конечностей, формирование контрактур, деформаций лица. В связи с этим лечение локализованной склеродермии у детей необходимо начинать как можно раньше, проводя более активную терапию. Так, больным тяжёлыми формами заболевания в качестве первой линии терапии рекомендуется назначать метотрексат в виде монотерапии или в комбинации с глюкокортикостероидными препаратами системного действия. Такое лечение позволяет достичь длительной ремиссии заболевания (2 года и более) у 74% больных [35].
УФА-1 терапия назначается детям только при тяжёлых формах заболевания (линейной, генерализованной, пансклеротической) в случаях отсутствия эффекта от применения других лечебных средств.
Применение ПУВА-терапии в детском возрасте противопоказано.
Требования к результатам лечения
— уменьшение активности течения склеродермии;
— предотвращение появления новых и увеличения существующих очагов поражения (прекращение прогрессирования заболевания);
— регресс или уменьшение симптомов заболевания;
— уменьшение площади поражения;
— предотвращение развития осложнений;
— повышение качества жизни больных.
Тактика при отсутствии эффекта от лечения
При отсутствии эффекта от применения лекарственных средств рекомендуется назначение препаратов других фармакологических групп.
При отсутствии эффекта от медикаментозного лечения рекомендуется назначение УФА-1 терапии или ПУВА-терапии.
ПРОФИЛАКТИКА
Больным рекомендуется избегать травматизации кожи, переохлаждения и перегревания, стрессовых ситуаций.
Информация
Источники и литература
-
Клинические рекомендации Российского общества дерматовенерологов и косметологов
- 1. Peterson L.S., Nelson A.M., Su W.P. et al. The epidemiology of morphea (localized scleroderma) in Olmsted County 1960-1993. J Rheumatol 1997; 24(1): 73-80.
2. Кубанова А.А., Кубанов А.А., Мелехина Л.Е., Богданова Е.В. Дерматовенерология в Российской Федерации. Итоги 2014 г. Успехи, достижения. Основные пути раз-вития. Вестник дерматол венерол 2015; 4:13-26.
3. Zulian F., Martini G., Vallongo C. et al. Methotrexate treatment in juvenile localized scleroderma: a randomized, double-blind, placebo-controlled trial. Arthritis Rheum 2011; 63(7):1998-2006.
4. Seyger M.M., van den Hoogen F.H., de Boo T., de Jong E.M. Low-dose methotrexate in the treatment of widespread morphea. J Am Acad Dermatol 1998; 39(2 Pt 1):220-225.
5. Kreuter A, Gambichler T, Breuckmann F. et al. Pulsed high-dose corticosteroids com-bined with low-dose methotrexate in severe localized scleroderma. Arch Dermatol 2005;141(7):847-52
6. Torok K.S., Arkachaisri T. Methotrexate and corticosteroids in the treatment of localized scleroderma: a standardized prospective longitudinal single-center study. J Rheumatol 2012; 39(2):286-294.
7. Joly P., Bamberger N., Crickx B. et al. Treatment of severe forms of localized scleroderma with oral corticosteroids: follow-up study on 17 patients. Arch Dermatol 1994; 130:5:663-664.
8. Amy de la Bretèque M., Rybojad M., Cordoliani F. et al. Relapse of severe forms of adult morphea after oral corticosteroid treatment. J Eur Acad Dermatol Venereol 2013; 27(9):1190-1191.
9. Sapadin A.N., Fleischmajer R. Treatment of scleroderma. Arch Dermatol 2002; 138(1):99-105.
10. Хмельницкий Р.Х. Опыт лечения склеродермии лидазой. Вестн дерматол венерол 1958; 4: 66-68.
11. Рахманов В.А., Хмельницкий Р.Х. К механизму действия лидазы при лечении больных склеродермией. Вестн дерматол венерол 1959; 6: 3-7.
12. Данильянц Е.И. О лечении склеродермии лидазой. Мед журн Узбекистана 1965; 5: 22-25.
13. Диденко И.Г. Терапевтическая эффективность ультразвука и фонофореза лидазы при различных формах склеродермии. Вестн дерматол венерол 1978;6:76-79.
14. Ананьева К.А., Вербенко Е.В. Новый метод лечения различных форм склеродер-мии электрофорезом с лидазой. Методики по диагностике, лечению и профилакти-ке заболеваний, разработанные и усовершенствованные в МОНИКИ. М., 1970: 148-149.
15. Curley R.K., Macfarlane A.W., Evans S., Woodrow J.C. The treatment of linear mor-phoea with D-penicillamine. Clin Exp Dermatol 1987; 12(1):56-57.
16. Falanga V., Medsger T.A.Jr. D-penicillamine in the treatment of localized scleroderma. Arch Dermatol 1990; 126:5:661-664.
17. van Bergen B.H., van Dooren-Greebe R.J., Fiselier T.J., Koopman R.J. [D-penicillamine in treatment of scleroderma «en coup de sabre»]. Hautarzt 1997; 48(1):42-44.
18. Kaur S., Dhar S., Kanwar A.J. Treatment of childhood linear morphea with D-penicillamine. Pediatr Dermatol 1993; 10(2):201-202.
19. Nagy E., Ladányi E. [Treatment of circumscribed scleroderma in childhood]. Z Hautkr. 1987; 1:62(7):547-549.
20. Valančienė G., Jasaitienė D., Valiukevičienė S. Pathogenesis and treatment modalities of localized scleroderma. Medicina (Kaunas). 2010; 46(10):649-656.
21. Смирнов А.В., Главинская Т.А. Современные представления о патогенезе и воз-можностях терапии ограниченной склеродермии. Нижегородский медицинский журнал 1997; 3:73-82.
22. Гребенюк В.Н. Ограниченная склеродермия у детей. Русский медицинский журнал 1998; 6(6): 352-356.
23. Kroft E.B., Groeneveld T.J., Seyger M.M., de Jong E.M. Efficacy of topical tacrolimus 0.1% in active plaque morphea: randomized, double-blind, emollient-controlled pilot study. Am J Clin Dermatol 2009; 10(3):181-187.
24. Сергеев В.П., Закиев Р.З. Лечение склеродермии диметилсульфоксидом. Вестн дерматол венерол 1976; 3:70-73.
25. Хамаганова И.В., Чулкова Е.В., Акулова С.Е. Применение актовегина в дерматоло-гической практике. Вестн дерматол венерол 1995; 5:47-49.
26. Kreuter A., Hyun J., Stücker M. et al. A randomized controlled study of low-dose UVA1, medium-dose UVA1, and narrowband UVB phototherapy in the treatment of localized scleroderma. J Am Acad Dermatol 2006; 54(3):440-447.
27. Kroft E.B., Berkhof N.J., van de Kerkhof P.C., Gerritsen R.M, de Jong EM. Ultraviolet A phototherapy for sclerotic skin diseases: a systematic review. J Am Acad Dermatol. 2008; 59(6):1017-1030.
28. Breuckmann F., Gambichler T., Altmeyer P., Kreuter A. UVA/UVA1 phototherapy and PUVA photochemotherapy in connective tissue diseases and related disorders: a research based review. BMC Dermatol. 2004; 20;4(1):11.
29. Brenner M., Herzinger T., Berking C. et al. Phototherapy and photochemotherapy of sclerosing skin diseases. Photodermatol Photoimmunol Photomed 2005; 21:157-165.
30. Волнухин В.А., Мурадян Н.Л., Выборнова О.В., Боровая О.В. Фотохимиотерапия склеродермии и склеродермоподобных заболеваний кожи. Вестн дерматол венерол 2008; 4:39-48.
31. Zwischenberger B.A., Jacobe H.T. A systematic review of morphea treatments and therapeutic algorithm. J Am Acad Dermatol 2011; 65(5):925-941.
32. Волнухин В.А., Харитонова Н.И., Знаменская Л.Ф. Опыт применения сочетанных методов низкоинтенсивной лазеротерапии при лечении заболеваний с проявле-ниями склероза и атрофии кожи. Лазерная медицина 1997; 1(2):12-15.
33. Saxton-Daniels S., Jacobe H.T. An evaluation of long-term outcomes in adults with pedi-atric-onset morphea. Arch Dermatol 2010; 146(9):1044-1045.
34. Zulian F., Vallongo C., Woo P. et al. for the Juvenile Scleroderma Working Group of the Pediatric Rheumatology European Society (PRES). Localized scleroderma in childhood is not just a skin disease. Arthritis Rheum. 2005; 52(9):2873-2881.
35. Zulian F., Vallongo C., Patrizi A. et al. A long-term follow-up study of methotrexate in juvenile localized scleroderma (morphea). J Am Acad Dermatol 2012; 67(6):1151-1156.
- 1. Peterson L.S., Nelson A.M., Su W.P. et al. The epidemiology of morphea (localized scleroderma) in Olmsted County 1960-1993. J Rheumatol 1997; 24(1): 73-80.
Информация
Персональный состав рабочей группы по подготовке федеральных клинических рекомендаций по профилю «Дерматовенерология», раздел «Локализованная склеродермия»:
Волнухин Владимир Анатольевич – ведущий научный сотрудник отделения разработки физиотерапевтических методов лечения ФГБУ «Государственный научный центр дерматовенерологии и косметологии» Минздрава России, доктор медицинских наук, профессор
МЕТОДОЛОГИЯ
Методы, использованные для сбора/селекции доказательств:
поиск в электронных базах данных.
Описание методов, использованных для сбора/селекции доказательств:
доказательной базой для рекомендаций являются публикации, вошедшие в Кокрановскую библиотеку, базы данных EMBASE и MEDLINE.
Методы, использованные для оценки качества и силы доказательств:
· Консенсус экспертов;
· Оценка значимости в соответствии с рейтинговой схемой (схема прилагается).
Рейтинговая схема для оценки силы рекомендаций:
| Уровни доказательств | Описание |
| 1++ | Мета-анализы высокого качества, систематические обзоры рандомизированных контролируемых исследований (РКИ) или РКИ с очень низким риском систематических ошибок |
| 1+ | Качественно проведенные мета-анализы, систематические, или РКИ с низким риском систематических ошибок |
| 1- | Мета-анализы, систематические, или РКИ с высоким риском систематических ошибок |
| 2++ | Высококачественные систематические обзоры исследований случай-контроль или когортных исследований. Высококачественные обзоры исследований случай-контроль или когортных исследований с очень низким риском эффектов смешивания или систематических ошибок и средней вероятностью причинной взаимосвязи |
| 2+ | Хорошо проведенные исследования случай-контроль или когортные исследования со средним риском эффектов смешивания или систематических ошибок и средней вероятностью причинной взаимосвязи |
| 2- | Исследования случай-контроль или когортные исследования с высоким риском эффектов смешивания или систематических ошибок и средней вероятностью причинной взаимосвязи |
| 3 | Неаналитические исследования (например: описания случаев, серий случаев) |
| 4 | Мнение экспертов |
Методы, использованные для анализа доказательств:
· Обзоры опубликованных мета-анализов;
· Систематические обзоры с таблицами доказательств.
Методы, использованные для формулирования рекомендаций:
Консенсус экспертов.
Рейтинговая схема для оценки силы рекомендаций:
| Сила | Описание |
| А |
По меньшей мере один мета-анализ, систематический обзор или РКИ, оцененные как 1++ , напрямую применимые к целевой популяции и демонстрирующие устойчивость результатов или группа доказательств, включающая результаты исследований, оцененные как 1+, напрямую применимые к целевой популяции и демонстрирующие общую устойчивость результатов |
| В |
Группа доказательств, включающая результаты исследований, оцененные как 2++, напрямую применимые к целевой популяции и демонстрирующие общую устойчивость результатов или экстраполированные доказательства из исследований, оцененных как 1++ или 1+ |
| С |
Группа доказательств, включающая результаты исследований, оцененные как 2+, напрямую применимые к целевой популяции и демонстрирующие общую устойчивость результатов; или экстраполированные доказательства из исследований, оцененных как 2++ |
| D |
Доказательства уровня 3 или 4; или экстраполированные доказательства из исследований, оцененных как 2+ |
Индикаторы доброкачественной практики (Good Practice Points – GPPs):
Рекомендуемая доброкачественная практика базируется на клиническом опыте членов рабочей группы по разработке рекомендаций.
Экономический анализ:
Анализ стоимости не проводился и публикации по фармакоэкономике не анализировались.
Метод валидизации рекомендаций:
· Внешняя экспертная оценка;
· Внутренняя экспертная оценка.
Описание метода валидизации рекомендаций:
Настоящие рекомендации в предварительной версии рецензированы независимыми экспертами.
Комментарии, полученные от экспертов, систематизированы и обсуждены членами рабочей группы. Вносимые в результате этого изменения в рекомендации регистрировались. Если же изменения не были внесены, то зарегистрированы причины отказа от внесения изменений.
Консультация и экспертная оценка:
Предварительная версия была выставлена для обсуждения на сайте ФГБУ «Государственный научный центр дерматовенерологии и косметологии» Минздрава России для того, чтобы лица, не участвующие в разработке рекомендаций, имели возможность принять участие в обсуждении и совершенствовании рекомендаций.
Рабочая группа:
Для окончательной редакции и контроля качества рекомендации повторно проанализированы членами рабочей группы.
Основные рекомендации:
Сила рекомендаций (A–D) приводится при изложении текста рекомендаций.
Прикреплённые файлы
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники. Стандарты лечения
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Внимание!
Если вы не являетесь медицинским специалистом:
-
Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
-
Информация, размещенная на сайте MedElement и в мобильных приложениях «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта», не может и не должна заменять очную консультацию врача.
Обязательно
обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
-
Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может
назначить
нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
-
Сайт MedElement и мобильные приложения «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта» являются исключительно информационно-справочными ресурсами.
Информация, размещенная на данном
сайте, не должна использоваться для самовольного изменения предписаний врача.
-
Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший
в
результате использования данного сайта.
Ограниченная склеродермия (ОС) (шифр L94 по МКБ-10) – хроническое заболевание соединительной ткани, принадлежащее к семейству коллагенозов и характеризующееся формированием в коже и подлежащих тканях воспалительно-склеротических изменений ограниченного (очагового) характера, без вовлечения в процесс внутренних органов. Этиология и патогенез ОС не уточнены. Имеются предположения об инфекционном происхождении заболевания, поскольку в ряде случаев оно ассоциируется с острыми и хроническими инфекциями, что не исключает роли наследственных факторов, генетически обусловленных детерминант, эндокринопатий, аутоиммунных патогенетических процессов. Таким образом, склеродермия в целом и ОС в частности могут быть отнесены к мультифакторным заболеваниям, в которых значение отдельных факторов, инициирующих либо промотирующих, не может быть четко определено.
Ключевую роль в патогенезе данного дерматоза играют аутоиммунные реакции к коллагену, возникающие вследствие высокого уровня антигенной коллагеновой стимуляции.

Таблица 1. Последовательность обследования больных

Таблица 2. Распределение больных по группам сравнения
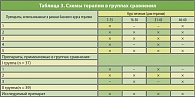
Таблица 3. Схемы терапии в группах сравнения

Таблица 4. Изменения горизонтальных размеров (площади) очагов поражения в группах в зависимости от используемого средства наружной терапии

Таблица 5. Изменения толщины (вертикальных границ) индуративных очагов поражения в группах в зависимости от используемого средства наружной терапии (по данным УЗ-морфометрии, гистомикрометрии)

Таблица 6. Оценка влияния используемого средства наружной терапии на величину показателя плотности очага поражения (по данным соноэластографии)

Таблица 7. Совокупная оценка степени выраженности индурации (глубина инвазии + интенсивность) до и после лечения

Таблица 8. Изменения показателей интенсивности эритемы в очагах ОС в зависимости от используемого средства наружной терапии на основании различия цветовых характеристик зоны поражения до и после лечения (по данным колориметрии)

Таблица 9. Изменения показателей интенсивности кровотока в зоне поражения в зависимости от используемого средства наружной терапии до и после лечения (по данным ЛДФ)

Таблица 10. Глобальная оценка терапевтического эффекта в группах сравнения

Таблица 11. Побочные эффекты терапии в группах наблюдения

Таблица 12. Анализ силы влияния использованного метода терапии (препарата) на качество жизни пациентов в группах сравнения (ДИКЖ до и после лечения)

Таблица 13. Оценка потребительских свойств препаратов наружного применения в группах сравнения
Инспирируемые ими функциональные изменения деятельности фибробластов и других коллагенобразующих клеток приводят к глубоким нарушениям внутриклеточного метаболизма коллагена. Об этом свидетельствуют данные, демонстрирующие высокой уровень цитотоксической активности сывороток больных в отношении фибробластов, величины титров антинуклеарных антител, дисиммуноглобулинемия и пр. (1). Для лечения ОС представляется весьма перспективным применение отечественного препарата Эгаллохит (галадерм), активной субстанцией которого является 10% эпигаллокатехин-3-галлат.
Клинически различают две формы ОС – бляшечную (sclerodermia en plaque, morfea) и линейную (sclerodermia en band, sclerodermia en coup de sabre). Иногда в качестве отдельных форм или разновидностей ОС рассматривают так называемую поверхностную (каплевидную) склеродермию – склероатрофический лихен, белый лишай Цимбуша (lichen albus Zumbusch), идиопатическую атрофодермию Пазини Пьерини, склередерму новорожденных, склередерму взрослых Бушке (scleroederma adultorum Buschke) и пр.
Клиническая картина ОС вполне характерна. В классическом варианте течения болезни очаги поражения в своем развитии проходят 3 стадии: пятна, бляшки, атрофии (4). Процесс начинается с появления одного (реже – нескольких) розовато-красного с фиолетовым оттенком пятна, почти без уплотнения, округлой или овальной формы, с сиреневым ободком по периферии, за более или менее продолжительное время достигающего размеров ладони и более (стадия 1 – пятна, эритематозная). В дальнейшем в центре пятна формируется уплотнение, которое может быть поверхностным либо проникающим глубоко в дерму, иногда до фасций и мышц. Вскоре очаг превращается в плотную (деревянистой консистенции) бляшку характерного желтовато-белого цвета с гладкой поверхностью, напоминающей слоновую кость. В таком состоянии он может сохраняться без видимых изменений месяцами и годами (стадия 2 – бляшки, индуративная). Поздняя эволюция очагов состоит в исчезновении сиреневого кольца, постепенном размягчении и рассасывании уплотнения от центра к периферии, в результате чего центр бляшки начинает западать, а вскоре и весь очаг превращается в участок атрофии (стадия 3 – атрофия). Имеются наблюдения, когда при рано начатом и адекватном лечении очаг бляшечной склеродермии может исчезнуть, не оставляя атрофии.
В нетипичных случаях исходом процесса может явиться формирование в зоне поражений плотной грубой рубцовой ткани по типу гипертрофического или келоидного рубца – «келоидоподобная склеродермия», отложение в коже извести, изъязвление очага, малигнизация.
Несмотря на очевидный прогресс в изучении склеродермии, в целом, вопросы профилактики рецидивов, трудоспособности и качества жизни больных с ОС по-прежнему нуждаются в анализе и разработке (6). Существует мнение о том, что ОС, в особенности бляшечная форма болезни, является достаточно редкой, изолированной патологией с благоприятным течением и прогнозом, мало влияющей на качество жизни пациентов, уровень их социальной и профессиональной адаптации. Вместе с тем, по мнению ряда исследователей, вероятность трансформации ОС в системную склеродермию составляет до 40%, а распространенность данного дерматоза такова, что доля его в структуре дерматологической патологии достигает 1% и имеет неуклонную тенденцию к росту (1, 2).
Даже при наличии потенциальных возможностей раннего выявления, полноценной диагностики и адекватной терапии диагноз «бляшечной склеродермии» нередко устанавливается с большим опозданием. Этому способствует ряд обстоятельств, в частности, сложность, многоэтапность диагностики и терапии, преимущественная ориентированность лечебных мероприятий на воспрепятствование и исключение предпосылок к приобретению процессом системного характера. Они сложны, дорогостоящи, инвазивны (инъекции, местные обкалывания, электро- и фонофорез, УФА и ПУВА-терапия и пр.), имеют ряд серьезных противопоказаний, могут быть выполнены только в условиях стационара, а потому ограничены по времени, подразумевают под собой необходимость госпитализации, отказа от бытовой и профессиональной деятельности. Местные же процедуры в виде мазей и аппликаций, в основном, гормоносодержащих (мометазон, гидрокортизон, метилпреднизолон и пр.), пугают пациентов приобретением зависимости, заставляя уклоняться от выполнений данных рекомендаций врача. Следствием этого становятся рецидивирование и прогрессирование заболевания, повторные, по истечении месяцев и лет обращения к специалистам, когда и диагноз, и прогноз уже однозначно неблагоприятны и свидетельствуют о наличии тяжелого терапевтического недуга из группы коллагенозов (6). В сложившихся условиях очевидна необходимость поиска новых препаратов и лекарственных форм, применение которых в создавшихся условиях являлось бы адекватной альтернативой уже имеющимся средствам и отвечало бы следующим требованиям: патогенетическая направленность терапии, безопасность, удобство и простота применения, возможность длительного использования в амбулаторных условиях.
В этом смысле применение оте-чественного препарата «Эгаллохит» (Галадерм), активной субстанцией которого является 10% эпигаллокатехин-3-галлат, представляется весьма перспективным. Механизмы действия данного препарата, направленные на основные звенья патогенеза патологического рубцевания, а именно: влияние на активность факторов роста, особенно VEGF, синтез и метаболизм коллагена, подавление синтеза цитокинов (ИЛ-1, 6, 8; ФНО-α, циклооксигеназы второго типа и простагландинов), поглощение пероксидных радикалов, снижение уровня чувствительности рецепторов клетки к Ig E и пр., дают основание к предположению о патогенетической обоснованности использования его при лечении склеродермии. Тем более, благодаря своей безопасности и эффективности, подтвержденной клиническими исследованиями, данный препарат давно и широко применяется как средство предотвращения патологического рубцевания после пластических операций, лазерных шлифовок кожи, фотодинамической терапии и пр., а также используется в комплексной терапии уже имеющихся гипертрофических, келоидных и атрофических рубцов совместно с инъекционной, лучевой терапией и другими методами (5).
В связи с этим целью настоящей работы явилось научно–практическое обоснование целесообразности применения крема (геля) «Эгаллохит» в комплексной терапии ОС как патогенетически оправданного неинвазивного средства лечения. В ходе исследования были поставлены и нашли свое решение следующие задачи:
- сравнительная оценка кожного статуса в очагах склеродермии до и после лечения: площадь эритемы и индурации кожи; выраженность индурации (плотность и вертикальные размеры зоны поражения), степень интенсивности эритемы;
- сравнительный анализ клинической эффективности применения изучаемого препарата и традиционных препаратов наружного применения в группах сравнения;
- сравнительная оценка безопасности и переносимости традиционных препаратов местного применения и изучаемого препарата при лечении ограниченных форм склеродермии;
- оценка психосоматического статуса у больных с ОС до и после лечения. Анализ силы влияния различных по своей природе средств наружной терапии на уровень и качество физического, психического, социального и ролевого или функционально-ассоциированного образа жизни индивидуума;
- изучение реакции и отношения пациентов на использование нового для них средства наружной терапии хронического дерматоза.
Построенное в рамках программы клинических испытаний на предмет оценки применимости и безопасности выше обозначенного препарата в сравнении с традиционно используемыми наружным средствами данное исследование осуществлялось в группах пациентов с использованием следующих клинических критериев эффективности терапии:
влияние используемых средств терапии на выраженность основных клинических признаков патологического процесса (критерий 1);
- терапевтический эффект (ГОТЭ) (вариант адаптации применительно к условиям данного исследования) (критерий 2);
- частота возникновения побочных эффектов терапии (критерий 3);
- качество жизни пациентов в группах сравнения (ДИКЖ) (критерий 4);
- потребительские свойства препарата «Эгаллохит» (критерий 5).
Объект, объем, материалы и методы исследования
Работа выполнялась в течение 2008-2009 гг. сотрудниками Северо-Западного центра лазерной хирургии кожи на базе кафедры кожных и венерических болезней СПбГМА им. И.И. Мечникова.
Объектом исследования стали амбулаторные больные в количестве 76 лиц мужского (21 случай наблюдения) и женского (55 случаев наблюдения) пола в возрасте от 18 до 69 лет (средний возраст 39,5 ± 3,4 года), страдающие ОС (бляшечная форма), имевшие очаги поражения 1 (эритематозной) и 2 (индуративной) стадии, не имевшие признаков системности процесса с продолжительностью заболевания от 3 мес. до 20 лет. Ввиду критического сокращения числа участников испытания вследствие использования критериев включения (исключения), в качестве альтернативного рандомизации способа распределения участников по группам наблюдения был использован метод минимизации как единственно способный обеспечить сопоставимость групп по признакам, предположительно влияющим на исход терапии (пол, возраст, продолжительность, клиническая форма заболевания и пр.). Таким образом, при распределении участников по группам наблюдения были сформированы 2 равноценные группы сравнения: группа I (контрольная) и группа II (таблица 2). Значимых различий в степени выраженности оцениваемых клинических проявлений заболевания – эритемы, индурации, площади поражения кожи и пр., а также существенных расхождений в оценке качества жизни на долечебном этапе у представителей обеих групп отмечено не было – исходные показатели в группах сравнения статистически значимо не различаются, p < 0,05; (см. таблицу. 4 – 9, 12).
В целях верификации диагноза в комплекс предварительных диагностических мероприятий, наряду со сбором анамнеза и физикальным обследованием, были включены обязательные исследования, выполненные в соответствии с ныне действующими рекомендациями по диагностике ОС (3, 7).
В качестве используемых методов лечения применялись:
Общая терапия ОС, применя-емая ко всем участникам клинических испытаний (базовый курс).
Препарат 1 – бензилпенициллина натриевая соль в/м по 1 млн ЕД 2 раза в сутки, 15 дней, 2 курса с интервалом в 30 дней.
Препарат 2 – гиалуронидаза в/м по 64 УЕ 1 раз в сутки через день, № 30.
Препарат 3 – пентоксифиллин внутрь по 400 мг 1-2 раза в сутки ежедневно, 60 дней.
Препарат 4 – депротеинизированный гемодериват из крови телят (Актовегин) в/м по 5 мл ежедневно, 15 дней, 2 курса с интервалом в 15 дней.
Препарат 5 – α-токоферола ацетат внутрь по 200 мг 2 раза в сутки ежедневно, 60 дней.
Местная терапия ОС, применяемая в зависимости от принадлежности участников к группе сравнения.
В I группе:
Препарат 1 – гидрокортизона бутират – аппликации или окклюзионные повязки 1 раз в сутки, 15 дней, 2 курса с интервалом в 15 дней.
Препарат 2 – депротеинизированный гемолизат из крови телят (Солкосерил) мазь 5% 2 раза в сутки ежедневно, 60 дней.
Препарат 3 – гепарин натрия + бензокаин + бензилникотинат (мазь) 2 раза в сутки 15 дней, 2 курса с интервалом в 15 дней.
Во II группе:
Изучаемый препарат – крем (гель) «Эгаллохит» (Галадерм) – 10% эпигаллокатехин-3-галлат; 2 раза в сутки ежедневно, 60 дней (таблица 3).
В качестве методов инструментальной (аппаратной) диагностики были использованы:
- бинокулярная дистанционная дермоскопия, дигитальная фотосъемка, фотопротокол с последующим вычислением площадей поражения на основании их графических TIFF-изображений с использованием программы Data Master 2000 (© 1993, 2003 RRR), предназначенной для визуального редактирования и численной обработки данных;
- ультрасонография, УЗ-мор-фометрия, трепанационная биопсия, ультразвуковая денсиметрия, гистомикрометрия (выборочно);
- дигитальная видео- и фотосъемка, фиксация изображений в формате TIFF с последующей обработкой компьютерными методами, включающими в себя анализ цветовых характеристик (колориметрия) объекта;
- лазерная доплеровская флоуметрия (ЛДФ). Анализ изменений степени интенсивности кровотока в сосудах кожи в очаге поражения и за его пределами до и после лечения.
Методы получения информации: данные клинического наблюдения, анкетирование (таблица 1). Методики – самостоятельное заполнение универсальной формы стандартного опросника, представляющего собой русифицированную версию Dermatology Life Quality Index (DLQI) и опросника, содержащего вопросы, оценива-ющие используемый препарат.
При выборе статистических процедур для регистрации достоверности полученных результатов были учтены методологические требования Международного конгресса по гармонизации GCP («Статистические принципы для клинических исследований»; ICH Guidelines. Good Clin Pract J 1998). Обработку полученных данных проводили с использованием общепринятых методов параметрической и непараметрической статистики с использованием пакетов прикладных программ для статистического анализа: «Excel» и «Statistica 6.0».
Результаты и обсуждение
1. Анализ влияния используемого средства наружной терапии на величину площади очагов поражения (таблица 4) продемонстрировал положительную динамику у пациентов в обеих группах. Однако сила влияния метода терапии на оцениваемый клинический признак патологического процесса оказалась различной. Так, у пациентов I группы наблюдения использование заявленных препаратов в совокупности привело к сокращению площадей поражения на 56% и к моменту окончания исследования составило 44% от исходного уровня, что может быть интерпретировано лишь как клинически значимый позитивный результат (p > 0,05). В то же время, у пациентов II группы наблюдения отмечалось более выраженное сокращение величины исследуемого параметра – до 19% от исходного уровня (p < 0,001), что является не только клинически, но и статистически значимым показателем эффективности примененного метода лечения. Кроме того во II группе интенсивность снижения величины изучаемого параметра была более выраженной, нежели в I группе. Так, статистически значимое сокращение показателя площади поражения отмечалось уже к 45 дню исследования (4 контрольный пункт наблюдения).
2. Анализ влияния используемого метода терапии (препарата) на изменение величины вертикальных границ очага поражения (таблица 5) выявил факт отсутствия в группе I статистически значимых различий показателя глубины инвазии в контрольных точках регистрации за весь период наблюдения (p > 0,05), наряду с чем у пациентов группы II наблюдалась выраженное, клинически значимое сокращение величины данного параметра (до 24% от исходного уровня) и статистически значимое уменьшение его абсолютной величины в конечной точке регистрации по сравнению с исходным уровнем (p < 0,001).
3. При оценке влияния метода терапии на величину показателя плотности очага поражения (таблица 6) были установлены вполне отчетливые различия результатов в группах наблюдения.
Так, несмотря на положительную в целом динамику процесса, у пациентов группы I в заключительном пункте регистрации сохранялись статистически значимые (p < 0,05) различия величины изучаемого параметра относительно контрольной группы при отсутствии таковых по сравнению с исходными показателями (p > 0,05).
Во II же группе, напротив, удалось констатировать достоверное, клинически и статистически значимое (p < 0,05) сокращение абсолютной и относительной величины изучаемого параметра в конечной точке регистрации, а так же отсутствие значимых различий данных показателей относительно контрольной группы наблюдения.
4. Интеграционный анализ, суммирующий результаты динамики показателей индурации в процессе лечения, в целом, подтвердил мнение о более высокой эффективности метода (препарата) терапии, использованного пациентами группы наблюдения II (таблица 7). Сила влияния его на выраженность изучаемого клинического признака оказалась достоверно более высокой, нежели препаратов, использованных больными I группы.
Свидетельством этого может служить средняя величина совокупного показателя (балла) интенсивности индурации в конечной точке регистрации (после лечения), равного 0,5, статистически значимо (p < 0,05) отличающегося от такового в группе I (1, 6) и исходных значений (2, 7) до лечения (p < 0,001).
5. Получены данные, свидетельствующие о выраженном влиянии обоих методов лечения на интенсивность эритемы, что подтверждается статистически значимыми различиями величин оцениваемых показателей во всех контрольных точках регистрации относительно исходного уровня (таблица 8). Несмотря на отсутствие достоверных свидетельств большей эффективности метода (препарата), использовавшегося в группе II (отсутствие статистически значимых различий величин сравниваемых показателей после лечения, (p > 0,05)), клинические преимущества его очевидны. Основаниями для данного вывода являются статистически значимые различия величин оцениваемых показателей в промежуточной контрольной точке регистрации, а также отчетливо более выраженное и клинически значимое снижение интенсивности эритемы (до 10% от исходного уровня) по завершении курса терапии.
6. При исследовании базовых показателей ЛДФ у пациентов, страдающих ОС, в зависимости от фазы развития очага поражения (эритематозная/индуративная), изменения носили разнонаправленный характер. Так, в индуративных очагах, до лечения, ПМ оказался достоверно более чем на 2σ ниже, чем в контрольной группе и колебался в диапазоне от 4,55 до 5,75 пф. ед., что соответствовало картине ангиоспастического синдрома. Резкое снижение ПМ, подавление амплитуд всех видов ритмов кровотока по сравнению с контрольной группой позволил интерпретировать данные показатели двумя возможными вариантами: стазический или смешанный, стазический-спастический тип нарушения микрогемодинамики (классиф. В.И. Маколкин и соавт., 1999 г.). В эритематозных очагах поражения ПМ был зарегистрирован на уровне, в 1,5 раза превышающем средние значения в контрольной группе и составлял величины в пределах от 23,8 до 25,1 пф. ед. (в норме – 16,7 ± 1,5), что соответствовало картине периферического ангиодистонического синдрома, с характерным и типичным гиперемическим типом нарушения микроциркуляции. Таким образом, у всех больных до лечения имелись выраженные, клинически и статистически достоверные изменения показателей кровотока в очагах поражения, в основном обусловленные депрессией медленных ритмов кровотока, характеризующих нейрогенный и миогенный тонус, а также признаки микроциркуляторного стаза, являющегося свидетельством наличия внутрисосудистых изменений (нарушения реологических свойств крови, агрегации форменных элементов, сладж-синдрома). В результате проведенного лечения у пациентов обеих групп сравнения удалось констатировать более или менее выраженные позитивные изменения ПМ. Однако в I группе наблюдения они могли быть расценены лишь как клинически значимые (различия показателей с контрольной группой статистически недостоверно (p ≥ 0,05), в то время как во II группе отмечалось достоверное, статистически значимое улучшение базовых показателей М, σ и Кv, в финальных измерениях не отличавшихся от таковых в контрольной группе.
7. Сравнительный анализ эффективности лечения ограниченных форм склеродермии в зависимости от используемого средства наружной терапии выявил явные преимущества метода лечения (препарата), использованного во II группе наблюдения. Свидетельством этого явились результаты глобальной оценки терапевтического эффекта (индекс ГОТЭ).
Согласно полученным данным, величина данного показателя в II группе составила 1,97 балла, тогда как в I группе лишь 1,41 балла (таблица 10). При этом состояние клинического выздоровления (уменьшение выраженности клинического признака от 75% и выше от исходного уровня) было зарегистрировано у 8 (20,5%), значительного улучшения (уменьшение выраженности клинического признака от 50% до 75% от исходного уровня) – у 23 (59,0%) пациентов II группы. В то же время в группе I доля лиц с подобным результатом оказалась почти в 2 раза меньше (5,4% и 37,8% соответственно). Доля пациентов с отличным и хорошим результатом лечения была статистически значимо выше во II группе (p = 0,0012 по критерию x²). Это, в свою очередь, позволяет говорить о наличии прямой положительной корреляционной связи между результатами оценки динамики клинических проявлений заболевания и данными ГОТЭ.
8. Сравнительная оценка безопасности и переносимости препаратов местного применения, использованных при лечении ОС, представленная на основании показателя «частота развития нежелательных побочных эффектов терапии» выявила существенные различия величины данного показателя в группах сравнения (таблица 11).
Полученные результаты свидетельствуют как о большем числе возможных вариантов осложнений, возникших у представителей группы I (10 против 4), так и о большей частоте случаев их регистрации (14 против 5) по сравнению со II группой.
Существенно большее абсолютное количество случаев регистрации нежелательных побочных эффектов терапии и значимо больший удельный вес случаев применения метода лечения (препарата), осложненных развитием побочных эффектов в I группе (37,8% против 12,8%, p = 0,0118 по критерию x²), дает основания к выводу о значительно лучшей переносимости и большей безопасности метода лечения (препарата), использованного во II группе сравнения.
9. Детальный анализ ДИКЖ, проведенный по 6 основным разделам, показал наличие клинически значимых различий в оценке качества жизни до и после проведенного лечения абсолютным большинством пациентов в обеих группах наблюдения (таблица 12). Исключением из этого явились различия в оценке степени влияния на данный показатель метода терапии (раздел 6).
Так, если больные I группы с учетом предшествующего опыта лечения не изменили своего отношения к нему и после настоящих клинических испытаний (средний балл до и после лечения составил 2,1 ± 0,8 и 2,1 ± 1,1 соответственно), то у больных II группы можно констатировать явные позитивные сдвиги в оценке влияния терапии на качество их жизни (2,3 ± 0,7 балла – до лечения и 1,2 ± 0,5 балла – после лечения). Несмотря на отсутствие достоверных различий цифровых значений показателя качества жизни до и после лечения по 4 из 6 разделов, у пациентов в обеих группах наблюдения зарегистрировано статистически значимое снижение совокупного показателя (индекса) качества жизни после проведенной терапии: в I группе с 12,2 ± 1,3 балла до 6,9 ± 0,6 балла (p < 0,05); во II группе – с 12,0 ± 1,0 баллов до 3,7 ± 0,3 балла (p < 0,001), что можно интерпретировать как почти двукратное улучшение качества жизни по критерию ДИКЖ (43,4%) у больных в I группе и почти трехкратное (69,2%) – у больных во II группе.
10. При сравнительном анализе потребительских свойств лекарственных форм крема (геля) «Эгаллохит», реализованном посредством заполнения индивидуальной карты-опросника, выдаваемой каждому участвующему в исследовании респонденту, были получены следующие данные.
Респонденты, принадлежавшие к II группе, значительно реже (в 12,8% случаев), нежели представители I группы (37,8%), акцентировали внимание на наличии нежелательных побочных эффектов лечения. Существенно реже (лишь в 7,7% против 73,0% случаев) предъявляли претензии к удобству применения препарата. Объективно реже (в 17,9% против 43,2% случаев, p = 0,0061 по критерию x²) изъявляли дополнительные пожелания во время лечения. Значимо чаще, нежели их оппоненты (в 87,2% против 59,5% случаев), позитивно оценивали результаты терапии (таблица 13).
Выводы
Препарат Эгаллохит (галадерм), использованный в качестве средства наружной терапии у пациентов с бляшечной формой ОС, продемонстрировал значительно более высокий уровень эффективности, нежели традиционно применяемые в этих целях препараты.
Об этом свидетельствуют результаты клинических наблюдений в группах сравнения, позволяющие констатировать факт значительного сокращения числа и степени выраженности клинических проявлений заболевания на фоне его применения:
- значительное, до 19% от исход-ного уровня, сокращение горизонтальных размеров (площадей) очагов поражения в основной группе против 44% в группе сравнения;
- выраженное, до 24% от исходного уровня, уменьшение вертикальных границ (глубины инвазии) индуративных очагов поражения в основной группе против 67% в группе сравнения;
- достоверное в основной группе наблюдения снижение плотности (интенсивности индурации) тканей в очагах поражения (с 2,7 баллов до 0,5 баллов), что на момент завершения терапии оказалось сопоставимым с таковой у здоровых лиц и статистически значимо отличалось от аналогичных показателей (1,6 балла) в группе сравнения;
- клинически более выраженное (при отсутствии статистически значимых различий), нежели в группе сравнения, снижение показателей интенсивности эритемы у пациентов основной группы (до 20,7% против 39,3% от исходного уровня);
- достоверное, статистически значимое улучшение у пациентов основной группы наблюдения, изменения базовых показателей микроциркуляции крови в очагах поражения (М, σ и Кv), которые в результате лечения перестали отличаться от таковых у здоровых лиц. Эти наблюдения являются так же косвенным свидетельством патогенетической обоснованности применения препарата «Эгаллохит» при данном заболевании;
- существенно большая величина индекса ГОТЭ, составившая в основной группе 1,97 балла против 1,41 балла в группе сравнения;
- существенно меньшее число случаев регистрации нежелательных побочных эффектов терапии в основной группе наблюдения – 4 против 10 – в группе сравнения, а так же значимо меньший показатель частоты возникновения осложнений, который при использовании данного препарата составил 12,8% против 37,8% при применении традиционных средств терапии;
- статистически значимое, на 69,2% (с 12,0 ± 1,0 баллов до 3,7 ± 0,3 балла) снижение совокупного показателя (индекса) качества жизни больных основной группы против 43,4% (с 12,2 ± 1,3 балла до 6,9 ± 0,6 балла) в группе сравнения.
Все выше изложенное, а также признание факта удобства применения изучаемого препарата 36 из 39 (92,3%) респондентами, невысокая частота выявления нежелательных побочных эффектов лечения, зарегистрированная у 5 из 39 (12,8%) пациентов, незначительность претензий и дополнительных пожеланий во время лечения, возникшая у 7 из 39 (17,9%) опрашиваемых, высокая степень позитивности в оценке результатов терапии, отмечаемая в 87,2% случаев наблюдений, является достаточным основанием к положительному заключению об эффективности, безопасности и переносимости препарата Эгаллохит (галадерм) при использовании его в качестве средства наружной терапии у пациентов с бляшечной формой ОС. Отмеченная, по результатам проведенных исследований, высокая степень патогенетической обоснованности и применимости, а также положительная оценка потребительских свойств позволяют рассматривать данную лекарственную форму как перспективное средство в комплексной терапии ограниченных форм склеродермии.
Aim:
The trial of efficacy of 6-month therapy with madecassol (tablets, ointment, powder) of patients with systemic and focal scleroderma (SS and FS).
Materials and methods:
54 patients (49 females and 5 males) aged 15 to 70 years with scleroderma running from 3 months to 15 years entered the study. 30 patients had typical SS, 24 patients had FS. Tablets were given to 18 patients, ointment was applied in 42 patients, powder in 3 and tablets + ointment in 9 patients. Madecassol 10 mg tablets were taken 3 times a day by patients with SS and advanced FS. The ointment was preferred in ulcers and scars on fingers and toes in SS and vascular trophic lesions in FS. In active focal scleroderma the ointment was applied to the skin lesions. The ointment was used 2 times a day (in the morning and evening) for 1-6 months. Madecassol powder was employed rarely, primarily of anal and vulval lesions.
Results:
6-month oral course (30 mg/day) in 12 SS patients brought about a decrease of indurative lesions, hyperpigmentation (8), vascular trophic disorders (6) and improvement of general condition (5). Subjective response was good in 10 patients and corresponded to absence of progression. In progressive disease and diffuse skin lesions the drug was ineffective. The best response was obtained in local application of madecassol ointment on digital ulcers in SS.
Conclusion:
Madecassol is effective and well tolerated and therefore recommended for oral and local use in combined treatment of SS adn FS. Indications for per os utelization are: chronic or subchronic SS with limited skin involvement, advanced and/or prone to progression FS in which combined administration of the tablets and ointment is proposed.
Федеральные клинические рекомендации по ведению больных локализованной склеродермией
РОССИЙСКОЕ ОБЩЕСТВО ДЕРМАТОВЕНЕРОЛОГОВ И КОСМЕТОЛОГОВ
ФЕДЕРАЛЬНЫЕ КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ
ПО ВЕДЕНИЮ БОЛЬНЫХ ЛОКАЛИЗОВАННОЙ СКЛЕРОДЕРМИЕЙ
Москва — 2013
2
Персональный состав рабочей группы по подготовке федеральных кли-нических рекомендаций по профилю «Дерматовенерология», раздел «Локализованная склеродермия»:
Волнухин Владимир Анатольевич – ведущий научный сотрудник отделения разработки физиотерапевтических методов лечения ФГБУ «Государственный научный центр дерматовенерологии и косметологии» Минздрава России, доктор медицинских наук, профессор
3
МЕТОДОЛОГИЯ
Методы, использованные для сбора/селекции доказательств:
поиск в электронных базах данных.
Описание методов, использованных для сбора/селекции доказательств:
доказательной базой для рекомендаций являются публикации, вошедшие в Кокрановскую библиотеку, базы данных EMBASE и MEDLINE.
Методы, использованные для оценки качества и силы доказательств:
Консенсус экспертов;
Оценка значимости в соответствии с рейтинговой схемой (схема прилага-ется).
Рейтинговая схема для оценки силы рекомендаций:
Уровни дока-зательств Описание
1++
Мета-анализы высокого качества, систематические обзоры рандомизированных контролируемых исследований (РКИ) или РКИ с очень низким риском систематических ошибок
1+
Качественно проведенные мета-анализы, систематические, или РКИ с низким риском систематических ошибок
1-
Мета-анализы, систематические, или РКИ с высоким риском систематических ошибок
2++
Высококачественные систематические обзоры исследований случай-контроль или когортных исследований. Высококаче-ственные обзоры исследований случай-контроль или ко-гортных исследований с очень низким риском эффектов смешивания или систематических ошибок и средней веро-ятностью причинной взаимосвязи
2+
Хорошо проведенные исследования случай-контроль или когортные исследования со средним риском эффектов сме-шивания или систематических ошибок и средней вероятно-стью причинной взаимосвязи
2-
Исследования случай-контроль или когортные исследования с высоким риском эффектов смешивания или систематиче-ских ошибок и средней вероятностью причинной взаимосвя-зи
3
Неаналитические исследования (например: описания случа-ев, серий случаев)
4
Мнение экспертов
4
Методы, использованные для анализа доказательств:
Обзоры опубликованных мета-анализов;
Систематические обзоры с таблицами доказательств.
Методы, использованные для формулирования рекомендаций:
Консенсус экспертов.
Рейтинговая схема для оценки силы рекомендаций:
Сила Описание
А
По меньшей мере один мета-анализ, систематический обзор или РКИ, оцененные как 1++ , напрямую применимые к целевой популя-ции и демонстрирующие устойчивость результатов
или
группа доказательств, включающая результаты исследований, оце-ненные как 1+, напрямую применимые к целевой популяции и де-монстрирующие общую устойчивость результатов
В
Группа доказательств, включающая результаты исследований, оце-ненные как 2++, напрямую применимые к целевой популяции и де-монстрирующие общую устойчивость результатов
или
экстраполированные доказательства из исследований, оцененных как 1++ или 1+
С
Группа доказательств, включающая результаты исследований, оце-ненные как 2+, напрямую применимые к целевой популяции и де-монстрирующие общую устойчивость результатов;
или
экстраполированные доказательства из исследований, оцененных как 2++
D
Доказательства уровня 3 или 4;
или
экстраполированные доказательства из исследований, оцененных как 2+
Индикаторы доброкачественной практики (Good Practice Points – GPPs):
Рекомендуемая доброкачественная практика базируется на клиниче-ском опыте членов рабочей группы по разработке рекомендаций.
Экономический анализ:
5
Анализ стоимости не проводился и публикации по фармакоэкономике не анализировались.
Метод валидизации рекомендаций:
Внешняя экспертная оценка;
Внутренняя экспертная оценка.
Описание метода валидизации рекомендаций:
Настоящие рекомендации в предварительной версии рецензированы независимыми экспертами.
Комментарии, полученные от экспертов, систематизированы и обсуж-дены членами рабочей группы. Вносимые в результате этого изменения в ре-комендации регистрировались. Если же изменения не были внесены, то заре-гистрированы причины отказа от внесения изменений.
Консультация и экспертная оценка:
Предварительная версия была выставлена для обсуждения на сайте ФГБУ «Государственный научный центр дерматовенерологии и косметоло-гии» Минздрава России для того, чтобы лица, не участвующие в разработке рекомендаций, имели возможность принять участие в обсуждении и совер-шенствовании рекомендаций.
Рабочая группа:
Для окончательной редакции и контроля качества рекомендации по-вторно проанализированы членами рабочей группы.
Основные рекомендации:
Сила рекомендаций (A–D) приводится при изложении текста рекомендаций.
6
ЛОКАЛИЗОВАННАЯ СКЛЕРОДЕРМИЯ
Шифр по Международной классификации болезней МКБ-10
L94.
ОПРЕДЕЛЕНИЕ
Локализованная склеродермия – хроническое заболевание соединительной ткани, которое характеризуется появлением на различных участках тела оча-гов локального воспаления (эритемы, отёка) с последующим формированием в них склероза и/или атрофии кожи и подлежащих тканей.
ЭТИОЛОГИЯ И ЭПИДЕМИОЛОГИЯ
Этиология локализованной склеродермии не известна. В патогенезе за-болевания основную роль отводят аутоиммунным нарушениям, повышенно-му синтезу и отложению в коже и подкожной клетчатке коллагена и других компонентов соединительной ткани, микроциркуляторным расстройствам.
Заболеваемость локализованной склеродермией составляет 2,7 случаев на 100000 населения, распространенность – 2 на 1000 населения [1]. В Рос-сийской Федерации распространенность локализованной склеродермии в 2009 г. составила 16140 случаев: взрослых больных зарегистрировано 13885, подростков 15-17 лет – 690, детей в возрасте 14 лет и младше – 1565 [2].
Заболевание встречается у представителей любой расы, чаще у женщин, чем у мужчин (2,6:1).
КЛАССИФИКАЦИЯ
Общепринятой классификации не разработано. Наиболее часто выделя-ют следующие формы локализованной склеродермии.
Бляшечная склеродермия
очаговая (морфеа)
узловатая (келоидоподобная)
Линейная склеродермия
полосовидная форма
склеродермия по типу «удар саблей»
Генерализованная (многоочаговая) склеродермия
Глубокая склеродермия
Пансклеротическая склеродермия
Буллёзная склеродермия
Идиопатическая атрофодермия Пазини-Пьерини
Прогрессирующая гемиатрофия лица Парри-Ромберга
Склероатрофический лихен.
7
У некоторых больных одновременно могут наблюдаться проявления не-скольких форм заболевания.
КЛИНИЧЕСКАЯ КАРТИНА
Больные могут предъявлять жалобы на зуд, болезненность, чувство по-калывания и стянутости кожи, ограничение движений в суставах, изменение объема и деформацию пораженных участков тела.
Принято выделять три стадии развития очагов склеродермии: эрите-мы/отёка, склероза (уплотнения) и атрофии кожи. Однако такая стадийность наблюдается не у всех больных. В типичных случаях заболевание начинается с появления на коже розовых, розовато-сиреневых, ливидных или гиперпиг-ментированных пятен округлой и/или полосовидной формы, иногда с явле-ниями отека. В стадию склероза в пятнах образуются очаги уплотнения кожи цвета слоновой кости с гладкой поверхностью и характерным восковидным блеском. По периферии очагов часто наблюдается воспалительный венчик лилового или розовато-сиреневого цвета, являющийся показателем активно-сти процесса. В местах поражения кожа плохо собирается в складку, потоот-деление уменьшено или отсутствует, нарушается функция сальных желёз и рост волос. С течением времени уплотнение кожи может уменьшаться. В стадию атрофии в очагах склеродермии развивается атрофия кожи, появля-ются телеангиэктазии, стойкая гипер- или гипопигментация.
При формировании глубоких очагов склеродермии кроме кожи в пато-логический процесс могут вовлекаться подлежащие ткани: подкожная клет-чатка, фасции, мышцы и кости.
Бляшечная склеродермия характеризуется появлением на голове, туло-вище или конечностях очагов эритемы и/или индурации кожи округлой фор-мы с типичной клинической картиной (см. выше).
Узловатая (келоидоподобная) склеродермия характеризуется образова-нием на коже единичных или множественных узелков или узлов, внешне на-поминающих келоидные рубцы. Очаги поражения развиваются, как правило, у больных, не имеющих склонности к развитию келоидов; их появление не связано с предшествующей травмой. Кожа в очагах склеродермии имеет те-лесный цвет или пигментирована; излюбленная локализация — шея, тулови-ще, верхние конечности.
При линейной склеродермии на коже возникают очаги эритемы и/или склероза линейной формы, локализующиеся, как правило, на одной половине тела или по ходу нервно-сосудистого пучка. Очаги поражения чаще всего возникают на голове или конечностях.
Линейная склеродермия на лице и волосистой части головы обычно вы-глядит в виде плотного тяжа склерозированной кожи, в которой отсутствует рост волос (форма «удар саблей»). Со временем поверхность очага сглажива-ется, образуя западение, обусловленное атрофией кожи, мышц и костной ткани.
8
При генерализованной склеродермии наблюдается появление множест-венных очагов эритемы и/или индурации кожи, занимающих несколько об-ластей тела и нередко сливающихся в обширные очаги поражения.
Для глубокой склеродермии характерно появление глубоких очагов уп-лотнения кожи и подкожной клетчатки. Кожа над очагами незначительно пигментирована или не изменена.
Пансклеротическая инвалидизирующая склеродермия является наиболее тяжёлой формой заболевания, при которой поражаются все слои кожи и под-лежащих тканей вплоть до костей, часто формируются контрактуры суставов с деформацией конечностей и длительно существующие язвы. Эта форма склеродермии обычно наблюдается у детей, быстро прогрессирует, рези-стентна к терапии и нередко заканчивается фатальным исходом.
Буллёзная склеродермия характеризуется появлением в очагах склеро-дермии прозрачных пузырей, нередко сопровождающихся геморрагиями.
Идиопатическая атрофодермия Пазини-Пьерини многими экспертами считается поверхностным вариантом локализованной склеродермии. Клини-чески она проявляется длительно существующими, незначительно западаю-щими пятнистыми очагами коричневого или серо-коричневого цвета с фио-летово-сиреневым оттенком, в которых отсутствует уплотнение кожи. Очаги располагаются чаще всего на туловище и верхних конечностях.
Прогрессирующая гемиатрофия лица Парри-Ромберга считается одной из наиболее тяжёлых и резистентных к терапии форм, при которой развива-ется прогрессирующее западение и деформация половины лица с вовлечени-ем в патологический процесс кожи, подкожной клетчатки, мышц и костей лицевого скелета. Указанные симптомы могут сочетаться с другими прояв-лениями локализованной склеродермии, а также сопровождаться поражением глаз и различными неврологическими нарушениями, включая эпилепсию.
При склероатрофическом лихене Цумбуша (синонимы: болезнь белых пятен, каплевидная склеродермия) участки поражения представлены перла-мутрово-белыми пятнами, папулами или бляшками с блестящей поверхно-стью, иногда сливающимися в очаги с фестончатыми очертаниями и четкими границами. Вокруг высыпаний может наблюдаться эритематозный венчик розового или красно-лилового цвета. Кожа в таких очагах часто атрофирова-на, легко собирается в складку по типу «смятой папиросной бумаги».
ДИАГНОСТИКА
Диагноз основывается на данных анамнеза и клинической картине забо-левания.
Для исключения системной склеродермии и других болезней соедини-тельной ткани необходима консультация ревматолога.
Для выявления сопутствующих заболеваний и противопоказаний к ле-чению необходимы консультации:
терапевта (при назначении физиотерапии обязательна);
9
эндокринолога (при назначении физиотерапии обязательна);
гинеколога (при назначении физиотерапии обязательна);
офтальмолога (при назначении физиотерапии обязательна);
невропатолога;
гастроэнтеролога;
оториноларинголога;
стоматолога.
При наличии сгибательных контрактур, деформаций скелета и косметиче-ских дефектов необходима консультация хирурга для решения вопроса о проведении хирургической коррекции.
Для уточнения активности патологического процесса, выявления ослож-нений заболевания, исключения системной склеродермии и других болезней соединительной ткани, а также противопоказаний к лечению необходимо проведение следующих исследований.
Обязательные лабораторные исследования:
клинический анализ крови;
клинический анализ мочи;
биохимический анализ крови.
Дополнительные исследования:
гистологическое исследование кожи (в сомнительных случаях);
определение антинуклеарного фактора с помощью метода непрямой иммунофлуоресценции на перевиваемой клеточной линии HEp-2 (для исключения диффузных болезней соединительной ткани);
исследование содержания в сыворотке крови иммуноглобулинов IgA, IgM, IgG, ревматоидного фактора;
исследование в сыворотке крови уровня антител к тиреоглобулину и тиреоидной пероксидазе (по возможности исследование содержания других антител: антител к париетальным клеткам желудка и др.);
анализ крови на антинуклеарные антитела;
анализ крови на антитела к топоизомеразе I (анти-Scl 70) и антицен-тромерные антитела (для исключения системной склеродермии);
обследование на боррелиоз;
УЗИ органов брюшной полости, почек, щитовидной железы;
электрокардиография;
рентгенография грудной клетки, областей деформации скелета, черепа;
электроэнцефалография;
компьютерная томография;
магнитно-резонансная томография.
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА
Локализованную склеродермию следует дифференцировать, главным
10
образом, с такими заболеваниями, как келоидные и гипертрофические рубцы, рубцовая алопеция, системная склеродермия и другие болезни соединитель-ной ткани, диффузный эозинофильный фасциит Шульмана, скередема Буш-ке, липодерматосклероз, склеромикседема, липоидный некробиоз, паннику-лит.
Реже локализованную склеродермию дифференцируют от лайм-боррелиоза, склеродермоподобной формы хронической реакции “трансплан-тат против хозяина”, радиационного фиброза, склеродермоподобной формы базальноклеточного рака кожи, синдрома жёсткой кожи, нефрогенного сис-темного фиброза, поздней кожной порфирии, саркоидоза, амилоидоза, син-дрома Вернера, фенилкетонурии, соединительнотканного невуса, синдрома POEMS, индуцированных склеродермоподобных заболеваний, вызванных применением лекарственных средств и пищевых добавок (блеомицина, вита-мина К, L-триптофана), использованием силиконовых протезов, контактом с химикатами (хлорвинилом, органическими растворителями) и др.
ЛЕЧЕНИЕ
Цели лечения:
остановить прогрессирование заболевания;
снизить активность патологического процесса;
уменьшить площадь поражения кожи и выраженность клинических симптомов заболевания;
предотвратить развитие осложнений;
улучшить качество жизни больных.
Общие замечания по терапии
Лечение необходимо подбирать индивидуально каждому пациенту в за-висимости от формы, стадии и тяжести течения заболевания, а также локали-зации очагов поражения.
Больным бляшечной, генерализованной и линейной склеродермией, а также атрофодермией Пазини-Пьерини и экстрагенитальным склероатрофи-ческим лихеном при неглубоком поражении кожи и подлежащих тканей ре-комендуется проведение курсового медикаментозного лечения (с включени-ем пенициллина, гиалуронидазы, вазоактивных и наружных средств) или фо-тотерапии (УФА-1 или ПУВА-терапии).
Больным с активным, быстро прогрессирующим течением заболевания и выраженными воспалительными явлениями (главным образом при наличии линейных или множественных очагов склеродермии) показано включение в комплексное лечение глюкокортикостероидных препаратов системного дей-ствия.
Больным тяжёлыми формами локализованной склеродермии с формиро-ванием глубокого поражения кожи и подлежащих тканей (линейная, генера-
11
лизованная, пансклеротическая склеродермия, прогрессирующая гемиатро-фия лица Парри-Ромберга) назначают лечение метотрексатом в виде моноте-рапии или в комбинации с глюкокортикостероидными препаратами систем-ного действия.
При наличии эрозивно-язвенных дефектов и поверхностной атрофии кожи показано применение стимуляторов регенерации тканей, при сухости кожи — использование увлажняющих и смягчающих наружных средств.
Иногда может наблюдаться спонтанный регресс склероза кожи или пол-ное разрешение очагов поражения.
Схемы лечения
Медикаментозная терапия
Системная терапия
1. Метотрексат (A)
При тяжёлых формах локализованной склеродермии (линейная, генера-лизованная, пансклеротическая склеродермия, прогрессирующая гемиатро-фия лица Парри-Ромберга) эффективным методом лечения является приме-нение метотрексата в виде монотерапии или в комбинации с глюкокортико-стероидными препаратами системного действия [3].
Общепринятые рекомендации по лечению метотрексатом больных лока-лизованной склеродермией не разработаны.
Согласно опубликованным данным, эффективны следующие схемы ле-чения метотрексатом [3-6]:
метотрексат, раствор для инъекций или таблетки: взрослым — 15-25 мг, детям — 0,3-1 мг на кг массы тела (максимальная доза 25 мг) 1 раз в не-делю подкожно или внутрь в течение 6-12 месяцев и более
или
метотрексат, раствор для инъекций или таблетки: взрослым — 15-25 мг, детям — 0,3-1 мг на кг массы тела (максимальная доза 25 мг) 1 раз в не-делю подкожно или внутрь в течение 6-12 месяцев и более
+
метилпреднизолон, лиофилизат для приготовления раствора для внут-ривенного и внутримышечного введения: взрослым — 1000 мг в сутки, детям — 30 мг/кг массы тела в сутки (максимальная доза 500-1000 мг) — 3 последовательных ежедневных внутривенных вливания в месяц в тече-ние 3 месяцев (всего 9 вливаний) или 1 внутривенное вливание 1 раз в неделю в течение 12 недель (всего 12 вливаний)
или
метотрексат, раствор для инъекций или таблетки: взрослым — 15-25 мг, детям — 0,3-1 мг на кг массы тела (максимальная доза 25 мг) 1 раз в не-делю подкожно или внутрь в течение 6-12 месяцев и более
+
12
преднизолон, таблетки 0,5-1 мг на кг массы тела в сутки (максималь-ная доза 60 мг) внутрь в течение 2-4 недель с последующей постепен-ной отменой
Примечание. В инструкциях по медицинскому применению метотрексата, метилпреднизолона и преднизолона локализованная склеродермия не вклю-чена в показания к применению препаратов.
2. Глюкокортикостероидные препараты (C)
Пероральное применение глюкокортикостероидных препаратов может оказать положительный эффект при активном, быстро прогрессирующем те-чении локализованной склеродермии, однако после отмены препаратов вы-сока частота рецидивов [7-8].
преднизолон, таблетки 0,3-1 мг на кг массы тела внутрь 1 раз в сутки в течение 3-12 месяцев
Примечание. В инструкции по медицинскому применению преднизолона локализованная склеродермия не включена в показания к медицинскому применению препарата.
В отдельных случаях рекомендуется введение глюкокортикостероидных препаратов непосредственно в очаг склеродермии (D) [9].
бетаметазон, суспензия для инъекций: 0,2 мл/см2 (но не более 1 мл) — введение в очаг поражения 1 раз в месяц в течение 3 месяцев.
3. Гиалуронидаза (С)
Согласно опубликованным данным, применение гиалуронидазы способст-вует уменьшению индурации кожи в очагах склеродермии [10-12]:
гиалуронидаза, лиофилизат для приготовления раствора для инъекций и местного применения, 32-64 УЕ 1 раз в сутки внутримышечно ежедневно или через день, на курс 15-20 инъекций или 64 УЕ — введение в очаг склеро-дермии 1 раз в 3 дня, на курс 7-10 процедур.
Гиалуронидазу можно также вводить в очаги поражения путём ультра-фонофореза или электрофореза (D) [13, 14].
фонофорез гиалуронидазы: 64 УЕ гиалуронидазы растворяют в 1 мл 1% раствора новокаина, наносят на очаги поражения пипеткой и вти-рают, затем покрывают контактной средой (вазелиновым маслом, рас-тительным маслом или гелем) и проводят озвучивание с частотой ко-лебаний 880 кГц, интенсивностью 0,5-1,2 Вт/см2, экспозицией 3-10 ми-нут на поле по лабильной методике в непрерывном режиме.
13
электрофорез гиалуронидазы: 64 УЕ лидазы растворяют в 30 мл дис-тиллированной воды, для подкисления среды до pH 5,2 добавляют 4-6 капель 0,1 н. раствора хлористоводородной кислоты, вводят в очаги склеродермии при силе тока не более 0,05 мА/см2, экспозиции 12-20 минут.
Процедуры ультрафонофореза или электрофореза гиалуронидазы прово-дят ежедневно или через день, на курс назначают 8-12 процедур. Возможно проведение 2-3 повторных курсов с интервалом 3-4 месяца.
4. Пеницилламин (C)
В нескольких исследованиях установлен положительный эффект при ле-чении больных локализованной склеродермией пеницилламином [15-17]. Однако имеются данные об отсутствии какого-либо улучшения кожного процесса при использовании данного препарата [18].
пеницилламин, таблетки 125-500 мг внутрь ежедневно или через день в течение 6-12 месяцев и более.
Учитывая довольно большое количество побочных эффектов и возмож-ность токсического действия даже при лечении низкими дозами, пеницилла-мин в последние годы назначают реже, в основном, в случаях отсутствия эф-фекта от других терапевтических средств.
5. Пенициллин (С)
В клинической практике пенициллин применяется для лечения локали-зованной склеродермии несколько десятилетий, хотя публикации по эффек-тивности его применения немногочисленны [19, 20].
бензилпенициллина натриевая соль, порошок для приготовления рас-твора для инъекций, 300000-500000 ЕД 3-4 раза в сутки или 1 млн ЕД 2 раза в сутки внутримышечно, на курс 15-40 млн ЕД.
Обычно проводят 2-3 курса терапии пенициллином с интервалом 1,5-4 месяца.
Примечание. В инструкции по медицинскому применению пенициллина ло-кализованная склеродермия не включена в показания к медицинскому при-менению препарата.
6. Вазоактивные препараты (D)
Имеются данные об эффективности применения в комплексном лечении больных локализованной склеродермией вазоактивных препаратов [21, 22]:
пентоксифиллин, таблетки: 100-200 мг внутрь 3 раза в сутки или 400 мг внутрь 1-2 раза в сутки в течение 4-6 недель
или
14
ксантинола никотинат, таблетки: 75-150 мг внутрь 2-3 раза в сутки в течение 4-6 недель
или
ксантинола никотинат, раствор для инъекций 15% (300 мг) 2 мл внут-римышечно 1 раз в сутки ежедневно, на курс 15-20 инъекций.
Терапию вазоактивными препаратами рекомендуется проводить повтор-ными курсами с интервалом 3-4 месяца, всего 2-3 курса в год.
Наружная терапия
1. Топические глюкокортикостероидные препараты (D)
При лечении ограниченных форм локализованной склеродермии опре-деленный эффект оказывает наружное применение глюкокортикостероидных средств [9]:
мометазона фуроат, крем, мазь наружно 1 раз в сутки в виде апплика-ций или окклюзионных повязок
или
алклометазона дипропионат, крем, мазь наружно 1 раз в виде апплика-ций или окклюзионных повязок
или
метилпреднизолона ацепонат, крем, мазь наружно 1 раз в сутки в виде аппликаций или окклюзионных повязок
или
бетаметазон, крем, мазь наружно 1 раз в сутки в виде аппликаций или окклюзионных повязок
или
клобетазола пропионат, крем, мазь наружно 1 раз в сутки в виде аппли-каций или окклюзионных повязок
При назначении топических глюкокортикостероидных препаратов в ви-де аппликаций курс лечения составляет 4-12 недель, при использовании их в виде окклюзионных повязок курс лечения составляет 2-3 недели.
2. Топические ингибиторы кальциневрина (A).
Показано, что применение 0,1% мази такролимуса может способство-вать уменьшению клинических проявлений локализованной склеродермии [23].
такролимус, 0,1% мазь наружно 2 раза в сутки в виде аппликаций или окклюзионных повязок в течение 3 месяцев.
Примечание. В инструкции по медицинскому применению мази такролиму-са локализованная склеродермия не включена в показания к применению препарата.
15
3. Диметилсульфоксид (С)
Лечение диметилсульфоксидом в ряде случаев может приводить к уменьшению эритемы и индурации кожи в очагах склеродермии [24].
диметилсульфоксид, концентрат для приготовления раствора для на-ружного применения: препарат растворяют в воде, применяют в виде аппликаций 25-75% водного раствора 1 раз в сутки в течение 30 минут. Длительность курса лечения составляет 3-4 недели. Терапию диметил-сульфоксидом проводят повторными курсами с интервалами 1-2 меся-ца.
4. Стимуляторы регенерации тканей (D)
При наличии эрозивно-язвенных дефектов или атрофических изменений кожи в очагах склеродермии определенный эффект могут оказать стимулято-ры регенарации тканей [25].
депротеинизированный гемодериват из крови телят, 5% мазь наружно 2-3 раза в сутки в течение 1-2 месяцев
или
депротеинизированный гемолизат из крови телят, 5% мазь наружно 2-3 раза в сутки в течение 1-2 месяцев.
Немедикаментозное лечение
Физиотерапевтическое лечение
1. Ультрафиолетовая терапия дальнего длинноволнового диапазона (УФА-1 терапия, длина волны 340-400 нм) (А)
УФА-1 терапия — один из эффективных методов лечения бляшечной, ге-нерализованной и линейной склеродермии, а также экстрагенитального скле-роатрофического лихена при неглубоком поражении кожи и подлежащих тканей [26, 27].
— облучения УФА-1 светом начинают с дозы 5-20 Дж/см2, последующие разовые дозы повышают на 5-15 Дж/см2 до максимальной разовой дозы 20-60 Дж/см2. Процедуры проводят с режимом 3-5 раз в неделю, курс составляет 20-60 процедур.
2. ПУВА-терапия (B)
ПУВА-терапия как с пероральным, так и с наружным применением фо-тосенсибилизатора, позволяет значительно улучшить состояние кожи в оча-гах склеродермии у больных бляшечной, линейной и генерализованной фор-мами заболевания, а также экстрагенитальным склероатрофическим лихеном [28-31].
2.1. ПУВА-терапия с пероральным применением фотосенсибилиза-тора
16
Амми большой плодов фурокумарины, таблетки 0,8 мг на кг массы те-ла внутрь однократно за 2 часа до облучения длинноволновым ультра-фиолетовым светом (длина волны 320-400 нм)
или
метоксален, капсулы 0,6 мг на кг массы тела внутрь однократно за 1,5-2 часа до облучения длинноволновым ультрафиолетовым светом (дли-на волны 320-400 нм).
Облучения начинают с дозы 0,25-0,5 Дж/см2, последующие разовые до-зы увеличивают через каждые 2-3 сеанса на 0,25-0,5 Дж/см2 до максимальной дозы 3-6 Дж/см2. Процедуры проводят 2-4 раза в неделю, курс лечения со-ставляет 20-60 процедур.
Примечание. В инструкциях по медицинскому применению Амми боль-шой плодов фурокумарины и метоксалена локализованная склеродермия не включена в показания к применению препаратов.
2.2. ПУВА-терапия с наружным применением фотосенсибилизатора
изопимпинеллин/бергаптен/ксантотоксин 0,3% спиртовой раствор на-ружно однократно на очаги поражения за 15-30 минут до облучения длинноволновым ультрафиолетовым светом (длина волны 320-400 нм).
Облучения начинают с дозы 0,1-0,3 Дж/см2, последующие разовые дозы увеличивают через каждые 2-3 сеанса на 0,1-0,2 Дж/см2 до максимального значения 3,5-5 Дж/см2. Процедуры проводят 2-4 раза в неделю, курс состав-ляет 20-60 процедур.
Примечание. В инструкции по медицинскому применению раствора изо-пимпинеллина/бергаптена/ксантотоксина локализованная склеродермия не включена в показания к применению препарата.
УФА-1 и ПУВА-терапию проводят как в виде монотерапии, так и в ком-плексе с медикаментозными средствами.
3. Ультразвуковая терапия (D)
При лечении ограниченных форм локализованной склеродермии приме-нение ультразвуковой терапии может способствовать уменьшению интен-сивности клинических симптомов заболевания [13].
озвучивание очагов поражения проводят с частотой колебаний 880 кГц, интенсивностью 0,05-0,8 Вт/см2, экспозицией 5-10 мин на поле по ла-бильной методике в непрерывном или импульсном режиме. Курс со-ставляет 10-15 ежедневных процедур.
17
Возможно проведение повторных курсов ультразвуковой терапии с ин-тервалом 3-4 месяца.
4. Низкоинтенсивная лазерная терапия (C).
Известно, что низкоинтенсивная лазерная терапия способна улучшать микроциркуляцию крови в коже. В отдельных работах показана эффектив-ность применения низкоинтенсивной лазерной терапии в комплексном лече-нии ограниченных форм локализованной склеродермии [32].
терапию лазерным излучением красного диапазона (длина волны 0,63-0,65 мкм) проводят по дистанционной стабильной методике, расфоку-сированным лучом с плотностью мощности 3-5 мВт/см2 и экспозицией 5-8 минут на поле. За процедуру облучают не более 4-5 полей при об-щей продолжительности воздействий не более 30 минут.
терапию лазерным излучением инфракрасного диапазона (длина волны 0,89 мкм) проводят по дистанционной или контактной, стабильной или лабильной методике, в непрерывном или импульсном (80-150 Гц) ре-жиме. Воздействия осуществляют по полям: при непрерывном режиме мощность излучения составляет не более 15 мВт, экспозиция на одно поле 2-5 мин, продолжительность процедуры — не более 30 минут. При импульсном режиме мощность излучения составляет 5-7 Вт/имп, экс-позиция 1-3 минуты на поле, общее время воздействия — не более 10 минут. За процедуру облучают не более 4-6 полей.
Курс лазерной терапии составляет 10-15 ежедневных процедур. Повтор-ные курсы проводят с интервалом 3-4 месяца.
Лечебная гимнастика и массаж.
Лечебная гимнастика и массаж рекомендуются больным линейной фор-мой склеродермии при ограничении движений в суставах и формировании контрактур.
Хирургическое лечение.
Хирургическое лечение проводят в отдельных случаях при наличии сги-бательных контрактур или косметических дефектов (при локализованной склеродермии по типу «удар саблей», прогрессирующей гемиатрофии Парри-Ромберга). Хирургические вмешательства осуществляют в неактивную ста-дию заболевания (при отсутствии признаков активности склеродермии в те-чение нескольких лет).
Больным генитальным склероатрофическим лихеном при локализации очагов поражения на крайней плоти полового члена и наличии стойкого фи-моза в случаях отсутствия эффекта от консервативной терапии рекомендует-ся циркумцизия.
18
Особые ситуации
Лечение детей
Локализованная склеродермия, возникшая в детском возрасте, нередко протекает длительно на протяжении нескольких лет: у 30% пациентов актив-ность заболевания сохраняется после достижения совершеннолетия [33]. Бо-лее, чем у 20% больных ювенильной локализованной склеродермией могут наблюдаться различные внекожные симптомы (суставные, неврологические, сосудистые, офтальмологические, респираторные и др.) [34].
При ювенильной склеродермии существует риск развития ряда ослож-нений, приводящих к инвалидизации больных: уменьшение длины и объёма конечностей, формирование контрактур, деформаций лица. В связи с этим лечение локализованной склеродермии у детей необходимо начинать как можно раньше, проводя более активную терапию. Так, больным тяжёлыми формами заболевания в качестве первой линии терапии рекомендуется на-значать метотрексат в виде монотерапии или в комбинации с глюкокортико-стероидными препаратами системного действия. Такое лечение позволяет достичь длительной ремиссии заболевания (2 года и более) у 74% больных [35].
УФА-1 терапия назначается детям только при тяжёлых формах заболе-вания (линейной, генерализованной, пансклеротической) в случаях отсутст-вия эффекта от применения других лечебных средств.
Применение ПУВА-терапии в детском возрасте противопоказано.
Лечение беременных
Лечение беременных проводится по строго обоснованным показаниям с учётом соотношения пользы и потенциального риска для матери и плода.
Проведение ПУВА-терапии беременным и кормящим матерям противо-показано.
Требования к результатам лечения
уменьшение активности течения склеродермии;
предотвращение появления новых и увеличения существующих очагов поражения (прекращение прогрессирования заболевания);
регресс или уменьшение симптомов заболевания;
уменьшение площади поражения;
предотвращение развития осложнений;
повышение качества жизни больных.
Тактика при отсутствии эффекта от лечения
При отсутствии эффекта от применения лекарственных средств реко-мендуется назначение препаратов других фармакологических групп.
19
При отсутствии эффекта от медикаментозного лечения рекомендуется назначение УФА-1 терапии или ПУВА-терапии.
ПРОФИЛАКТИКА
Больным рекомендуется избегать травматизации кожи, переохлаждения и перегревания, стрессовых ситуаций.
- SALE
- От рубцов
- От растяжек
- Вопрос-Ответ
Как решить проблемы с кожей при склеродермии?
![]() Загрузка…
Загрузка…

В этой статье речь пойдет про хроническое системное заболевание соединительной ткани, которое характеризуется воспалительным процессом, нарушениями работы опорно-двигательного аппарата, сосудов и внутренних органов. Болезнь может прогрессировать под влиянием разнообразных факторов. Важную роль в этом процессе играет генетическая предрасположенность.
Также усугублять течение болезни могут внешние условия. Воздействие ультрафиолетовых лучей, радиации, прием определенных лекарств, наличие инфекций и резкие температурные колебания не только способствуют прогрессированию недуга, но и ухудшают состояние кожного покрова пациента.
Проблемы с кожей при склеродермии
Болезнь влечет за собой целый спектр визуальных проявлений на всех стадиях развития. При этом у разных пациентов пораженные участки кожи могут отличаться внешним видом (размером, цветом бляшек), а также сопутствующими симптомами (зуд, чувство стянутости, жжение).
Чаще всего на начальном этапе развития патологии появляются пятнистые очаги лилового или фиолетового цвета, которые не вызывают беспокойства и болезненных ощущений. При прогрессировании склеродермии они становятся отечными, а ткани в центре уплотняются. Кожа приобретает неприятный блеск и желтую окраску с голубовато-фиолетовым ободком. Этот период сопровождается чувством стянутости, зудом и слабовыраженными болями.
Также при прогрессировании склеродермии у пациента отмечаются следующие симптомы:
- Уплотнение кожного покрова — он становится твердым, что может ограничивать амплитуду движений и вызывать дискомфорт.
- Первый пункт очень быстро приводит к образованию растяжек, особенно в местах, где сустав больше всего двигается.
- Потеря волос — на пораженных склеродермией участках могут появляться залысины.
- Изменения пигментации — кожа становится темнее или светлее.
На атрофической стадии заболевания потовые и жировые железы перестают полноценно функционировать, что приводит к повышенной сухости кожи. При нарушении кровообращения возможно образование язв и ран. Важно своевременно обратиться к врачу при появлении любых беспокоящих симптомов.
Рекомендации по уходу за кожей при склеродермии
В этом вопросе обязательно требуется своевременный и индивидуальный подход. Надо придерживаться следующих правил:
- Увлажнение — для предотвращения сухости и поддержания эластичности кожи используйте назначенные кремы и лосьоны.
- Защита от солнца — во время недуга повышается чувствительность к ультрафиолету, поэтому нужно применять солнцезащитные средства.
- Выбор правильного гардероба — необходимо носить одежду из натуральных тканей, которая не будет прилегать к телу. Это важно, чтобы исключить дополнительное раздражение кожи.
- Регулярный осмотр на наличие новых уплотнений, растяжек или язв помогает вовремя обнаружить изменения и обсудить их с врачом для выбора дальнейшей тактики лечения.
- Мягкий уход — использование нежных очищающих средств минимизирует раздражения и аллергические реакции.
- Правильное питание — акцент на продуктах, содержащих антиоксиданты, омега–3 кислоты и витамины, способствует синтезу коллагена и, как следствие, поддержанию здоровья кожи.
Определение характера заболевания, будь то системная или локальная склеродермия – ключевой этап при выборе стратегии лечения. В связи с этим ранняя консультация с дерматологом или ревматологом особенно важна для достижения положительной динамики.
Лечение
Терапия склеродермии зависит от формы и тяжести заболевания, а также от степени поражения тканей. При локальных формах склеродермии чаще всего используются глюкокортикостероиды (например, бетаметазон, триамцинолон) и синтетические аналоги витамина D. Если наблюдается уплотнение кожи, применяют аппликации с диметилсульфоксидом.
При поражении внутренних органов — пеницилламин и инъекции гиалуронидазы для снижения фиброза. При поверхностных формах болезни назначают ПУВА-терапию, а также комбинирующее УФ-облучение с применением фотосенсибилизаторов.
При серьезном поражении склеродермией и синдроме Рейно используются следующие группы лекарственных препаратов:
- иммуносупрессоры (метотрексат, такролимус, микофенолат);
- блокаторы кальциевых каналов (нифедипин);
- средства, улучшающие микроциркуляцию (пентоксифиллин, ксантинол никотинат).
При склероатрофическом лихене может быть назначена низкоинтенсивная лазерная терапия. Если наблюдаются контрактуры суставов или деформации скелета, требуется хирургическое вмешательство.
Специалисты рекомендуют дополнительно заниматься восстановлением пораженного покрова для улучшения качества жизни пациентов. Свою эффективность в данном вопросе продемонстрировали средства линейки Ферменкол, основу которых составляют ферменты коллагеназы. Ферменкол заметно влияет на патологические рубцы и уплотнения при склеродермии — снимает зуд и ощущение напряжения, корректирует излишнее нарастание рубцовой ткани. Также Ферменкол успешно применяется для устранения фиброза в сочетании с физиопроцедурами.
Для коррекции стрий (растяжек) назначается Ферменкол Элактин. Он не только устраняет деформированные волокна коллагена, но и стимулирует синтез нативного коллагена. Таким образом, кожа восстанавливается, выглядит более здоровой. Оптимальным методом в этом случае выступает сочетание фонофореза или электрофореза с набором или гелем Ферменкол. Процедуры обеспечивают доставку ферментов коллагеназы глубоко в уплотненную ткань, в дерме формируется лекарственное депо, и с его помощью видимый противорубцовый результат достигается в разы быстрее, чем при обычных накожных аппликациях. Общая продолжительность процедуры не более 20 минут в день. Длительность курса лечения — 10–15 сеансов.
Процедуры с Ферменкол можно легко проводить дома, они безболезненны и безопасны. Главное исключить противопоказания к физическим воздействиям ультразвука и электрического тока, а также аллергию на морепродукты, так как ферменты коллагеназы добываются путем очистки пищеварительной системы краба. Эффективность средств Ферменкол научно обоснована и доказана опытом применения в медицинских учреждениях по всей России, а также тысячами наших пациентов. Результатом станет красивая, гладкая и ровная кожа без дефектов.
Если вы затрудняетесь с выбором средства для коррекции, то обратитесь за бесплатной консультацией в наш специальный раздел «Вопрос–Ответ». Практикующий врач Светлана Огородникова отправит рекомендации в течение трех рабочих дней.
Приобрести все средства Ферменкол вы можете в нашем интернет-магазине с доставкой по России, а также в Казахстан, Беларусь, Грузию и Абхазию.
Начните путь к жизни без ограничений уже сегодня!
Вам может быть интересно
Блог компании «Ферменкол» несет исключительно ознакомительный характер и не может заменить индивидуальную консультацию с практикующим врачом. Все статьи информируют о проблемах кожи, однако не являются руководством к действию. Перед употреблением вышеупомянутых средств и применением лечебных методик обязательно проконсультируйтесь с врачом!
