Описание препарата Мозобаил (раствор для подкожного введения, 20 мг/мл) основано на официальной инструкции, утверждено компанией-производителем в 2016 году
Дата согласования: 23.09.2016
Особые отметки:
Содержание
- Фотографии упаковок
- Действующее вещество
- ATX
- Фармакологическая группа
- Нозологическая классификация (МКБ-10)
- Состав
- Описание лекарственной формы
- Фармакологическое действие
- Фармакодинамика
- Фармакокинетика
- Показания
- Противопоказания
- Применение при беременности и кормлении грудью
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Передозировка
- Особые указания
- Форма выпуска
- Производитель
- Условия отпуска из аптек
- Условия хранения
- Срок годности
- Заказ в аптеках Москвы
Фотографии упаковок
23.09.2016
Действующее вещество
ATX
Фармакологическая группа
Состав
| Раствор для подкожного введения | 1 фл. |
| активное вещество: | |
| плериксафор | 24 мг |
| вспомогательные вещества: натрия хлорид — 5,9 мг; 0,1 М раствор натрия гидроксида или 0,1 М раствора кислоты хлористоводородной — до рН 6,0–7,5; вода для инъекций — до 1,2 мл |
Описание лекарственной формы
Прозрачная бесцветная или светло-желтая жидкость.
Фармакологическое действие
Фармакологическое действие
—
гемопоэтическое, мобилизирующее гемопоэтические стволовые клетки, иммуномодулирующее.
Фармакодинамика
Механизм действия
Плериксафор представляет собой производное бициклама и является селективным обратимым антагонистом CXCR4 хемокинового рецептора, блокируя его за счет связывания с когнатным лигандом, фактором стромальных клеток-l? (SDF-l?), также известным как CXCL12. Считается, что индуцированный плериксафором лейкоцитоз и увеличение количества циркулирующих гемопоэтических прогениторных клеток является результатом нарушения связи между CXCR4 и его когнатным лигандом, которое приводит к появлению в системном кровотоке как зрелых, так и полипотентных клеток. CD34+ клетки, мобилизованные с помощью плериксафора, являются функциональными и способными к приживлению, с долгосрочным потенциалом восстановления популяции.
Фармакодинамика
В двух плацебо-контролируемых клинических исследованиях с участием пациентов с лимфомой и множественной миеломой (AMD3100-3101 и AMD3100-3102 соответственно) оценивалось увеличение содержания CD34+ клеток (клеток/мкл) за 24 ч, в течение дня перед первым аферезом (см. табл. 1). В оцениваемый 24-часовой период первая доза плериксафора (0,24 мг/кг) или плацебо вводилась за 10–11 ч до афереза.
Таблица 1
Увеличение числа CD34+ клеток в периферической крови после введения препарата Мозобаил совместно с Г-КСФ
| Исследование | Препарат Мозобаил + Г-КСФ | Плацебо + Г-КСФ | ||
| Медиана | Среднее (СО) | Медиана | Среднее (СО) | |
| AMD3100-3101 | 5,0 | 6,1 (5,4) | 1,4 | 1,9 (1,5) |
| AMD3100-3102 | 4,8 | 6,4 (6,8) | 1,7 | 2,4 (7,3) |
В исследованиях фармакодинамики у здоровых добровольцев с применением только плериксафора пик мобилизации CD34+ клеток наблюдался в течение 6–9 ч после введения препарата. При исследовании фармакодинамики как у здоровых добровольцев, так и у пациентов с применением схемы мобилизации, включающей гранулоцитарный колониестимулирующий фактор (Г-КСФ) и плериксафор в тех же дозах, наблюдался более длительный подъем CD34+ клеток в периферической крови в течение с 4 до 18 ч после введения препарата, пик был отмечен между 10 и 14 ч.
Дети. Эффективность и безопасность применения препарата Мозобаил у детей и подростков в возрасте до 18 лет в клинических исследованиях не изучались.
Европейское медицинское агентство отказалось от обязательного предоставления компанией результатов исследований по применению препарата Мозобаил у детей и подростков в возрасте до 18 лет при миелосупрессии (вследствие химиотерапии, проводимой для лечения злокачественных новообразований), требующей аутотрансплантации гемопоэтических стволовых клеток (см. «Способ применения и дозы»).
Фармакокинетика
Фармакокинетику плериксафора изучали у пациентов с лимфомой и множественной миеломой с применением клинической дозы (0,24 мг/кг) после предварительного лечения Г-КСФ (10 мкг/кг 1 раз в день в течение от 2 до 4 дней, при необходимости курс продлевали до 7 дней).
Абсорбция
Плериксафор быстро всасывается после п/к введения, Cmax достигается приблизительно через 30–60 мин (Tmax). После п/к введения плериксафора в дозе 0,24 мг/кг, которому предшествовало предварительное лечение Г-КСФ в течение 4 дней подряд, Cmax плериксафора в плазме крови и среднее значение AUC0–24 составили (887±217) нг/мл и (4337±922) нг·ч/мл соответственно.
Распределение
Плериксафор умеренно связывается с белками плазмы человека (до 58%). Кажущийся Vd плериксафора у людей составляет 0,3 л/кг, это говорит о том, что препарат склонен к распределению во внесосудистом пространстве, но не ограничен им.
Метаболизм
В экспериментах in vitro плериксафор не подвергался метаболизму печеночными микросомами человека и эмбриональными гепатоцитами человека. Также in vitro было показано, что препарат не угнетает основные метаболизирующие изоферменты цитохрома Р450 (1A2, 2A6, 2B6, 2C8, 2C9, 2C19, 2D6, 2E1 и 3A4/5). В экспериментах in vitro с человеческими гепатоцитами плериксафор не индуцировал изоферменты CYP1A2, CYP2B6 и CYP3A4. Полученные данные позволяют предположить, что потенциал лекарственных взаимодействий, опосредованных системой Р450, для плериксафора низок.
Элиминация
Основной путь элиминации плериксафора — выведение через почки. После введения плериксафора в дозе 0,24 мг/кг здоровым добровольцам с нормальной функцией почек, примерно 70% препарата выводилось с мочой в неизмененном виде в течение первых 24 ч после введения. T1/2 из плазмы составляет 3–5 ч. По данным исследований in vitro с использованием клеточных моделей MDCKII и MDCKII-MDR1, плериксафор не является субстратом или ингибитором Р-гликопротеина.
Особые группы пациентов
Пациенты с нарушением функции почек. У лиц с различной степенью почечной недостаточности клиренс плериксафора после однократной дозы (0,24 мг/кг) уменьшался; наблюдалась положительная корреляция с Cl креатинина. Средние показатели AUC0–24 плериксафора у пациентов с легкой (Cl креатинина 51–80 мл/мин), умеренной (Cl креатинина 31–50 мл/мин) и тяжелой (Cl креатинина ≤30 мл/мин) степенью почечной недостаточности составили 5410, 6780 и 6990 нг·ч/мл соответственно, что превышает значения экспозиции препарата, наблюдаемые при нормальной функции почек (5070 нг·ч/мл). Почечная недостаточность не оказывала влияние на Cmax.
Пол. Популяционный анализ не выявил различий фармакокинетики плериксафора по полу.
Пожилые. Популяционный анализ не выявил различий фармакокинетики плериксафора по возрасту.
Дети. Данные по фармакокинетике у детей ограничены.
Показания
Для усиления мобилизации гемопоэтических стволовых клеток в периферический кровоток с целью их сбора и последующей аутотрансплантации пациентам с лимфомой и множественной миеломой в сочетании с гранулоцитарным колониестимулирующим фактором (Г-КСФ).
Противопоказания
- повышенная чувствительность к плериксафору или любым вспомогательным веществам препарата;
- беременность (см. «Применение при беременности и кормлении грудью»);
- лактация (см. «Применение при беременности и кормлении грудью»);
- детский и подростковый возраст до 18 лет (в связи с отсутствием опыта применения).
Применение при беременности и кормлении грудью
Данных по применению плериксафора у беременных женщин недостаточно. Исследования на животных показали наличие тератогенного действия препарата. Пациент должен быть проинформирован, что применение плериксафора во время беременности может привести к врожденным порокам развития. Применение препарата Мозобаил во время беременности возможно только в тех случаях, когда польза от применения превышает возможный потенциальный риск для плода.
Женщинам детородного возраста во время лечения необходимо использовать эффективные средства контрацепции.
Данные о возможном проникновении плериксафора в грудное молоко отсутствуют, поэтому риск для грудного ребенка не может быть исключен. Во время терапии препаратом Мозобаил следует прекратить грудное вскармливание.
Способ применения и дозы
Реклама: ООО «РЛС-Патент», ИНН 5044031277, erid=4CQwVszH9pUkpHxmQQo
Реклама: ООО «РЛС-Патент», ИНН 5044031277, erid=4CQwVszH9pUkpHxmQQo
П/к.
Лечение препаратом Мозобаил должен назначать и проводить квалифицированный онколог и/или гематолог. Мобилизация и аферез клеток должны проводиться в сотрудничестве с онкогематологическим центром, имеющим достаточный опыт в данной области, где есть возможность надлежащего контроля уровня гемопоэтических прогениторных клеток.
Дозы. Рекомендованная доза плериксафора — 0,24 мг/кг/сут. Препарат вводится п/к за 6–11 ч до начала афереза после предварительной четырехдневной терапии Г-КСФ. В клинических исследованиях Мозобаил обычно вводился в течение 2–4 дней подряд (до 7 дней непрерывного применения).
Для расчета дозы плериксафора используют среднее значение массы тела, измеряемое в течение 1 нед до введения первой дозы препарата.
В клинических исследованиях дозу плериксафора рассчитывали на основании массы тела пациентов, у которых отклонения массы тела от идеальной составляли не более 175%. Режим дозирования и особенности лечения пациентов, отклонения массы тела у которых составляют более 175% от идеальной, не изучали.
Дозу препарата Мозобаил (в мл) рассчитывают по формуле: 0,012 × фактическая масса тела (кг). Учитывая, что воздействие препарата с увеличением массы тела возрастает, доза плериксафора не должна превышать 40 мг/сут.
Рекомендованные сопутствующие препараты
В базовых клинических испытаниях, поддерживающих лечение препаратом Мозобаил, все пациенты получали Г-КСФ в дозе 10 мкг/кг, утром, в течение 4 дней подряд до первого введения плериксафора, а затем — каждое утро до проведения афереза.
Применение препарата у особых групп пациентов
Нарушение функции почек. При Cl креатинина <50 мл/мин доза плериксафора должна быть уменьшена на треть, до 0,16 мг/кг/сут (см. «Фармакокинетика»). Клинические данные по применению скорректированной дозы препарата ограничены. Имеющийся опыт клинического применения плериксафора не позволяет дать рекомендации по дозированию препарата при Cl креатинина <20 мл/мин, а также у пациентов, находящихся на гемодиализе. Учитывая, что воздействие препарата с увеличением массы тела возрастает, доза плериксафора не должна превышать 27 мг/сут, если Cl креатинина <50 мл/мин.
Клиренс креатинина (в мл/мин) рассчитывают по формуле:
Женщины: Cl креатинина (мл/мин)=0,85 × значение, рассчитанное по формуле для мужчин.
Дети. Опыт использования препарата у детей ограничен. Безопасность и эффективность препарата Мозобаил для лечения детей не оценивались в контролируемых клинических исследованиях.
Пациенты пожилого возраста (более 65 лет). У пожилых пациентов с нормальной функцией почек коррекция дозы не требуется. При Cl креатинина <50 мл/мин рекомендуется изменить дозу препарата (см. выше «Нарушение функции почек»). Следует помнить, что с возрастом вероятность снижения почечной функции увеличивается, поэтому пожилым пациентам дозу препарата следует подбирать с осторожностью.
Способ применения
П/к. 1 фл. препарата Мозобаил предназначен для однократного применения.
Перед введением необходимо осмотреть флакон. Если в препарате присутствуют механические включения или есть изменения цвета раствора, его вводить нельзя. Препарат Мозобаил является стерильным препаратом, не содержащим консерванты, поэтому в процессе набора содержимого флакона в шприц для п/к инъекций необходимо соблюдать правила асептики.
Исследования по совместимости препарата Мозобаил с другими препаратами не проводились, поэтому не следует его смешивать с другими препаратами в одном шприце.
Препарат, оставшийся после введения необходимой дозы, должен быть уничтожен.
Побочные действия
Данные по безопасности применения препарата Мозобаил в сочетании с Г-КСФ у онкологических пациентов с лимфомой и множественной миеломой были получены в 2 плацебо-контролируемых (фаза III) и 10 неконтролируемых исследованиях (фаза II) у 543 пациентов. Пациенты получали лечение плериксафором в дозе 0,24 мг/кг/сут п/к. Длительность лечения в этих исследованиях составила от 1 до 7 дней непрерывно (медиана — 2 дня).
В двух исследованиях (фаза III) с участием пациентов с неходжкинской лимфомой и множественной миеломой (AMD3100-3101 и AMD3100-3102 соответственно) был исследован 301 пациент, получавший лечение препаратом Мозобаил и Г-КСФ, и 292 пациента, получавших плацебо и Г-КСФ. Суточная доза Г-КСФ составляла 10 мкг/кг утром в течение 4 дней подряд до первой инъекции плериксафора или плацебо, а также каждое утро до проведения афереза.
Ниже представлены нежелательные реакции, которые чаще наблюдались в группе, получавшей препарат Мозобаил и Г-КСФ, чем в группе плацебо и Г-КСФ. Частота нежелательных реакций, связанных с лечением, составила >1% среди пациентов, получавших препарат Мозобаил, при мобилизации гемопоэтических стволовых клеток и аферезе, а также перед химиотерапией/миелоаблятивной терапией при подготовке к трансплантации. Нежелательные реакции указаны в соответствии с системно-органным классом и частотой возникновения. Частоту определяли на основании следующих критериев: очень часто (≥1/10); часто (≥1/100 до <1/10); нечасто (≥1/1000 до <1/100); редко (≥1/10000 до <1/1000); очень редко <1/10000), частота неизвестна (нельзя оценить по имеющимся данным).
При использовании химиотерапии/абляции в рамках подготовки к трансплантации не было отмечено значимой разницы в частоте нежелательных реакций между группами лечения через 12 мес после трансплантации.
Ниже приведены нежелательные реакции, наблюдавшиеся в группе препарата Мозобаил чаще, чем в группе плацебо, связанные с применением препарата Мозобаил при проведении мобилизации и афереза в III фазе исследований.
Нарушения со стороны иммунной системы: нечасто — аллергические реакции, анафилактические реакции, включая анафилактический шок (см. Постмаркетинговые наблюдения и «Особые указания»).
Нарушения психики: часто — бессонница.
Нарушения со стороны нервной системы: часто — головная боль, головокружение.
Нарушения со стороны ЖКТ: очень часто — диарея, тошнота; часто — метеоризм, боли в животе, рвота, вздутие живота, сухость во рту, дискомфорт в эпигастральной области, запор, диспепсические явления, гипестезия слизистой оболочки полости рта.
Нарушения со стороны кожи и подкожных тканей: часто — гипергидроз, эритема.
Нарушения со стороны скелетно-мышечной и соединительной ткани: часто — артралгия, скелетно-мышечная боль.
Общие расстройства и нарушения в месте введения: очень часто — реакции в местах инъекции; часто — усталость, недомогание.
Нежелательные реакции у пациентов с лимфомой и множественной миеломой, получавших препарат Мозобаил в контролируемых исследованиях III фазы и неконтролируемых исследованиях, включая исследование II фазы, в котором препарат Мозобаил использовали в режиме монотерапии для мобилизации гемопоэтических стволовых клеток, сходны. У пациентов с онкологическими заболеваниями частота нежелательных реакций не отличалась в зависимости от заболевания, возраста или пола.
Аллергические реакции
Аллергические реакции включали в себя одно или несколько следующих нежелательных явлений: крапивница (n=2), периорбитальный отек (n=2), одышка (n=1) или гипоксия (n=1). Данные явления были легкой или умеренной степени тяжести и возникали в течение приблизительно 30 мин после введения препарата Мозобаил.
Инфаркт миокарда
Согласно клиническим исследованиям, 7 из 679 онкологических пациентов перенесли инфаркт миокарда после мобилизации стволовых клеток с помощью плериксафора и Г-КСФ. Все случаи инфаркта миокарда наблюдались как минимум через 14 дней после последнего введения препарата Мозобаил. Кроме того, две пациентки, участвовавшие в программе по применению исследуемого препарата в индивидуальном порядке, перенесли инфаркт миокарда после мобилизации стволовых клеток с помощью плериксафора и Г-КСФ. Один из случаев инфаркта миокарда произошел через 4 дня после последнего введения препарата Мозобаил.
Отсутствие временной связи у 8 из 9 пациентов и профиль риска участников, перенесших инфаркт миокарда, не позволяют считать препарат Мозобаил независимым фактором риска развития инфаркта миокарда у пациентов, получающих Г-КСФ.
Вазовагальные реакции
Вазовагальные реакции (ортостатическая гипотензия и/или синкопе) отмечались менее чем у 1% участников клинических исследований по применению препарата Мозобаил (онкологических пациентов и здоровых добровольцев), получавших плериксафор в дозе <0,24 мг/кг. В большинстве случаев данные явления наблюдались в течение 1 ч после введения препарата Мозобаил.
Нарушения со стороны ЖКТ
В клинических исследованиях по применению препарата Мозобаил у онкологических пациентов сообщения о тяжелых нарушениях со стороны ЖКТ (включая диарею, тошноту, рвоту, боли в животе) регистрировались редко.
Парестезии
Часто наблюдаются у онкологических пациентов после аутотрансплантации вследствие проводимых многочисленных медицинских процедур. В плацебо-контролируемых клинических исследованиях III фазы частота парестезий составила 20,6 и 21,2% в группах плериксафора и плацебо соответственно.
Гиперлейкоцитоз
В исследованиях III фазы увеличение количества лейкоцитов за день до афереза или в любой день афереза до 100·109/л и выше наблюдалось у 7% пациентов, получавших препарат Мозобаил, и у 1% пациентов, получавших плацебо. При этом осложнения или клинические проявления лейкоцитоза отсутствовали.
Пациенты пожилого возраста
24% участников двух плацебо-контролируемых клинических исследований по применению плериксафора были старше 65 лет. Значимых различий по частоте нежелательных реакций в подгруппе пациентов пожилого возраста (по сравнению с пациентами более молодого возраста) не наблюдалось.
Постмаркетинговые наблюдения
Ниже приведены нежелательные реакции, которые были сообщены в постмаркетинговый период применения препарата Мозобаил в дополнение к тем, которые были зафиксированы во время клинических исследований. Частоту нежелательных реакций определить было невозможно, т.к. сообщения о них были получены из популяции с неопределенным количеством пациентов, также как и возможную взаимосвязь с применением препарата.
Со стороны иммунной системы: анафилактические реакции, включая анафилактический шок.
Нарушения психики: необычные сновидения, ночные кошмары.
Взаимодействие
Реклама: ООО «ВЕДАНТА», ИНН 7714886235, erid 4CQwVszH9pUkKJ7jUDd
Реклама: ООО «РЛС-Библиомед» ИНН 7714758963
Реклама: ООО «ВЕДАНТА», ИНН 7714886235, erid 4CQwVszH9pUkKJ7jUDd
Реклама: ООО «РЛС-Библиомед» ИНН 7714758963
Исследования по изучению взаимодействий данного препарата не проводились. Тесты, проведенные in vitro, показали, что плериксафор не метаболизируется изоферментами цитохрома Р450, а также не подавляет и не усиливает их активность. Согласно исследованиям in vitro, плериксафор не является субстратом или ингибитором Р-гликопротеина.
Добавление ритуксимаба к режиму мобилизации (плериксафор и Г-КСФ) в клинических исследованиях с участием пациентов с неходжкинской лимфомой, не оказывало влияние на безопасность пациента или концентрацию CD34+ клеток.
Передозировка
Случаев передозировки зафиксировано не было. С учетом ограниченных данных о применении препарата в дозе, превышающей рекомендованную (до 0,48 мг/кг/сут), можно предположить, что частота расстройств ЖКТ, вазовагальных реакций, ортостатической гипотензии и/или синкопе может увеличиваться.
Особые указания
Мобилизация опухолевых клеток у пациентов с лейкозами
Препарат Мозобаил и Г-КСФ назначали при остром миелоидном и плазмоцитарном лейкозах в рамках программы по применению исследуемого препарата в индивидуальном порядке. При этом в отдельных случаях наблюдалось увеличение числа циркулирующих лейкемических клеток. Плериксафор, назначаемый для мобилизации гемопоэтических стволовых клеток, может вызвать мобилизацию клеток опухоли с последующим их попаданием в продукт афереза. Поэтому плериксафор не рекомендуется применять при лейкозах для мобилизации гемопоэтических стволовых клеток и их последующего забора.
Гематологические эффекты
Гиперлейкоцитоз. Препарат Мозобаил, назначаемый в сочетании с Г-КСФ, увеличивает не только популяцию гемопоэтических стволовых клеток, но и количество циркулирующих лейкоцитов. Во время применения препарата Мозобаил следует контролировать количество лейкоцитов. Следует тщательно оценивать каждый случай назначения препарата Мозобаил пациентам, у которых количество нейтрофилов в периферической крови превышает 50000 клеток/мкл.
Тромбоцитопения. Является известным осложнением афереза и наблюдается у пациентов, получающих препарат Мозобаил. Число тромбоцитов необходимо контролировать у всех пациентов, которые получают препарат Мозобаил и которым планируется проведение афереза.
Возможность мобилизации опухолевых клеток у пациентов с лимфомой и множественной миеломой. Последствия потенциальной реинфузии опухолевых клеток должным образом не изучены. При использовании препарата Мозобаил в сочетании с Г-КСФ (для мобилизации гемопоэтических стволовых клеток при лимфоме или множественной миеломе) возможно высвобождение клеток опухоли из костного мозга и их последующий забор при лейкоферезе.
Клиническое значение возможного риска мобилизации опухолевых клеток определено не полностью. В клинических исследованиях с участием пациентов с неходжкинской лимфомой и множественной миеломой не наблюдалось мобилизации клеток опухоли при применении плериксафора.
Аллергические реакции
Легкие и средней степени аллергические реакции (см. «Побочные действия») разрешались спонтанно или курировались соответствующей терапией (например антигистаминные препараты, ГКС, гидратация, оксигенотерапия). Серьезные реакции гиперчувствительности, в т.ч. анафилактические реакции, некоторые из которых были угрожающие жизни с клинически значимым снижением АД и шоком, были зарегистрированы у пациентов, получающих Мозобаил. Рекомендуется наблюдение пациентов во время и после введения Мозобаила в течение, по крайней мере, 30 мин после каждого применения препарата. Потенциальный риск аллергических реакций требует соблюдения соответствующих мер предосторожности.
Вазовагальные реакции
После п/к инъекций препарата могут отмечаться вазовагальные реакции, ортостатическая гипотензия и/или синкопе (см. «Побочные действия»). В связи с возможностью развития таких реакций необходимо соблюдать соответствующие меры предосторожности. В основном эти реакции развивались в течение 1 ч после применения препарата Мозобаил.
Спленомегалия
В доклинических исследованиях наблюдалось увеличение абсолютной и относительной массы селезенки, связанное с экстрамедуллярным кроветворением, при длительном (2–4 нед) ежедневном введении плериксафора крысам (п/к инъекции; доза препарата превышала дозу, рекомендованную для человека, в 4 раза).
В клинических исследованиях влияние плериксафора на размер селезенки специально не оценивалось. Таким образом, нельзя полностью исключить возможность увеличения селезенки на фоне приема плериксафора и Г-КСФ. В очень редких случаях назначение Г-КСФ приводит к разрыву селезенки. Об этом следует помнить, когда пациенты, получающие препарат Мозобаил в сочетании с Г-КСФ, предъявляют жалобы на боли в левом подреберье и/или в области лопатки или плеча.
Контроль лабораторных показателей
У пациентов, получающих препарат Мозобаил и проходящих аферез, необходимо контролировать число лейкоцитов и тромбоцитов крови.
Натрий
Каждая доза препарата Мозобаил содержит менее 1 ммоль натрия (23 мг), т.е. практически его не содержит.
Влияние на способность управлять транспортными средствами и заниматься другими потенциально опасными видами деятельности. Поскольку у некоторых пациентов наблюдалось головокружение, утомляемость или вазовагальные реакции, необходимо соблюдать осторожность при управлении транспортными средствами и занятии другими потенциально опасными видами деятельности.
При появлении описанных нежелательных явлений следует воздержаться от выполнения указанных видов деятельности.
Форма выпуска
Раствор для подкожного введения, 20 мг/мл. По 1,2 мл раствора во флаконе из бесцветного стекла I типа, укупоренном резиновой пробкой, обжатой алюминиевым колпачком с пластиковой крышечкой типа flip-off. По 1 фл. в картонную пачку.
Производитель
Патеон ЮК Лимитед, Великобритания.
Выпускающий контроль качества: Джензайм Лтд, Великобритания.
Владелец регистрационного удостоверения: Джензайм Европа Б.В., Нидерланды.
Претензии потребителей направлять по адресу представительства компании в России: 125009, Москва, ул. Тверская, 22.
Тел.: (495) 721-14-00; факс: (495) 721-14-11.
Условия отпуска из аптек
По рецепту.
Условия хранения
При температуре 15–30 °C.
Хранить в недоступном для детей месте.
Срок годности
3 года.
Не применять по истечении срока годности, указанного на упаковке.
Представленная информация о ценах на препараты не является предложением о продаже или покупке товара.
Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в
соответствии со статьей 55 Федерального закона «Об обращении лекарственных средств» от 12.04.2010 № 61-ФЗ.
Мозобаил (Mozobil) инструкция по применению
📜 Инструкция по применению Мозобаил
💊 Состав препарата Мозобаил
✅ Применение препарата Мозобаил
📅 Условия хранения Мозобаил
⏳ Срок годности Мозобаил
Описание лекарственного препарата
Мозобаил
(Mozobil)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для печатного издания справочника Видаль 2019 года.
Дата обновления: 2018.11.28
Владелец регистрационного удостоверения:
Контакты для обращений:
САНОФИ
Код ATX:
L03AX16
(Плериксафор)
Лекарственная форма
| Мозобаил |
Р-р д/п/к введения 20 мг/1 мл: фл. 1.2 мл 1 шт. рег. №: ЛП-002352 |
Форма выпуска, упаковка и состав
препарата Мозобаил
Раствор для п/к введения прозрачный, бесцветный или светло-желтый.
Вспомогательные вещества: натрия хлорид — 5.9 мг, 0.1М раствор натрия гидроксида или 0.1М раствор кислоты хлористоводородной — до pH 6.0-7.5, вода д/и — до 1.2 мл.
1.2 мл — флаконы бесцветного стекла I типа (1) — пачки картонные.
Фармакологическое действие
Механизм действия
Плериксафор представляет собой производное бициклама и является селективным обратимым антагонистом CXCR4 хемокинового рецептора, блокируя его за счет связывания с когнатным лигандом, фактором стромальных клеток-1α (SDF-1α), также известным как CXCL12. Считается, что индуцированный плериксафором лейкоцитоз и увеличение количества циркулирующих гемопоэтических прогениторных клеток является результатом нарушения связи между CXCR4 и его когнатным лигандом, которое приводит к появлению в системном кровотоке как зрелых, так и полипотентных клеток. CD34+ клетки, мобилизованные с помощью плериксафора, являются функциональными и способными к приживлению, с долгосрочным потенциалом восстановления популяции.
Фармакодинамика
В двух плацебо-контролируемых клинических исследованиях с участием пациентов с лимфомой и множественной миеломой (AMD3100-3101 и AMD3100-3102 соответственно) оценивалось увеличение содержания CD34+ клеток (клеток/мкл) за 24 ч, в течение дня перед первым аферезом (Таблица 1). В оцениваемый 24-часовой период первая доза плериксафора (0.24 мг/кг) или плацебо вводилась за 10-11 ч до афереза.
Таблица 1. Увеличение числа CD34+ клеток в периферической крови после введения препарата Мозобаил совместно с гранулоцитарным колониестимулирующим фактором (Г-КСФ)
В исследованиях фармакодинамики у здоровых добровольцев с применением только плериксафора пик мобилизации CD34+ клеток наблюдался в течение 6-9 ч после введения препарата. При исследовании фармакодинамики как у здоровых добровольцев, так и у пациентов с применением схемы мобилизации, включающей Г-КСФ и плериксафор в тех же дозах, наблюдался более длительный подъем CD34+ клеток в периферической крови в течение с 4 ч до 18 ч после введения препарата, пик был отмечен между 10 ч и 14 ч.
Дети
Эффективность и безопасность применения препарата Мозобаил у детей и подростков в возрасте до 18 лет в клинических исследованиях не изучались.
Европейское медицинское агентство отказалось от обязательного предоставления компанией результатов исследований по применению препарата Мозобаил у детей и подростков в возрасте до 18 лет при миелосупрессии (вследствие химиотерапии, проводимой для лечения злокачественных новообразований), требующей аутотрансплантации гемопоэтических стволовых клеток.
Фармакокинетика
Фармакокинетику плериксафора изучали у пациентов с лимфомой и множественной миеломой с применением клинической дозы (0.24 мг/кг) после предварительного лечения Г-КСФ (10 мкг/кг 1 раз/сут в течение от 2 до 4 дней, при необходимости курс продлевали до 7 дней).
Всасывание
Плериксафор быстро всасывается после п/к введения, Cmax достигается приблизительно через 30-60 мин (Тmax). После п/к введения плериксафора в дозе 0.24 мг/кг, которому предшествовало предварительное лечение Г-КСФ в течение 4 дней подряд, Сmax плериксафора в плазме крови и среднее значение AUC0-24 составили 887±217 нг/мл и 4337±922 нг×ч/мл соответственно.
Распределение
Плериксафор умеренно связывается с белками плазмы человека (до 58%). Кажущийся Vd плериксафора составляет 0.3 л/кг, это говорит о том, что препарат склонен к распределению во внесосудистом пространстве, но не ограничен им.
Метаболизм
В экспериментах in vitro плериксафор не подвергался метаболизму печеночными микросомами человека и эмбриональными гепатоцитами человека. Также in vitro было показано, что препарат не угнетает основные метаболизирующие изоферменты цитохрома Р450 (1А2, 2А6, 2В6, 2С8, 2С9, 2С19, 2D6, 2Е1 и 3А4/5). В экспериментах in vitro с человеческими гепатоцитами плериксафор не индуцировал изоферменты CYP1A2, CYP2B6 и CYP3A4. Полученные данные позволяют предположить, что потенциал лекарственного взаимодействия, опосредованного системой Р450, для плериксафора низок.
Выведение
Основной путь элиминации плериксафора — выведение почками. После введения плериксафора в дозе 0.24 мг/кг здоровым добровольцам с нормальной функцией почек, примерно 70% препарата выводилось с мочой в неизмененном виде в течение первых 24 ч после введения. T1/2 составляет 3-5 ч. По данным исследований in vitro с использованием клеточных моделей MDCKII и MDCKII-MDR1, плериксафор не является субстратом или ингибитором Р-гликопротеина.
Фармакокинетика у особых групп пациентов
У лиц с различной степенью почечной недостаточности клиренс плериксафора после однократной дозы (0.24 мг/кг) уменьшался; наблюдалась положительная корреляция с КК. Средние показатели AUC0-24 для плериксафора, вводимого субъектам с почечной недостаточностью легкой (КК 51-80 мл/мин), умеренной (КК 31-50 мл/мин) и тяжелой (КК ≤30 мл/мин) степени, составили 5410, 6780 и 6990 нг×ч/мл соответственно, что превышает значения экспозиции препарата, наблюдаемые при нормальной функции почек (5070 нг×ч/мл). Почечная недостаточность не оказывала влияния на Сmax.
Популяционный анализ не выявил различий фармакокинетики плериксафора в зависимости от пола и возраста.
Данные по фармакокинетике у детей ограничены.
Показания препарата
Мозобаил
- для усиления мобилизации гемопоэтических стволовых клеток в периферический кровоток с целью их сбора и последующей аутотрансплантации пациентам с лимфомой и множественной миеломой в сочетании с Г-КСФ.
Режим дозирования
Лечение препаратом Мозобаил должен назначать и проводить квалифицированный онколог и/или гематолог. Мобилизация и аферез клеток должны проводиться в сотрудничестве с онкогематологическим центром, имеющим достаточный опыт в данной области, где есть возможность надлежащего контроля уровня гемопоэтических прогениторных клеток.
Рекомендованная доза плериксафора составляет 0.24 мг/кг/сут. Препарат вводят п/к за 6-11 ч до начала афереза после предварительной 4-дневной терапии Г-КСФ. В клинических исследованиях препарат Мозобаил обычно использовался в течение 2-4 дней подряд (до 7 дней непрерывного применения).
Для расчета дозы плериксафора используют среднее значение массы тела, измеряемое в течение 1 недели до введения первой дозы препарата.
В клинических исследованиях дозу плериксафора рассчитывали на основании массы тела пациентов, у которых отклонения массы тела от идеальной составляли не более 175%. Режим дозирования и особенности лечения пациентов, отклонения массы тела у которых составляют более 175% от идеальной, не изучали.
Дозу препарата Мозобаил (в мл) рассчитывают по формуле: 0.012 × фактическая масса тела (кг).
Учитывая, что воздействие препарата с увеличением массы тела возрастает, доза плериксафора не должна превышать 40 мг/сут.
Рекомендованные сопутствующие препараты
В базовых клинических исследованиях, поддерживающих лечение препаратом Мозобаил, все пациенты получали Г-КСФ в дозе 10 мкг/кг, утром, в течение 4 дней подряд до первого введения плериксафора, а затем каждое утро до проведения афереза.
У пациентов с нарушением функции почек при КК≤50 мл/мин дозу плериксафора следует уменьшить на 1/3 до 0.16 мг/кг/сут. Клинические данные по применению скорректированной дозы препарата ограничены. Имеющийся опыт клинического применения плериксафора не позволяет дать рекомендаций по дозированию препарата при КК<20 мл/мин, а также у пациентов, находящихся на гемодиализе.
Учитывая, что воздействие препарата с увеличением массы тела возрастает, доза плериксафора не должна превышать 27 мг/сут, если КК≤50 мл/мин. КК (мл/мин) рассчитывают по формуле:
Мужчины
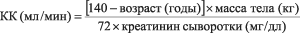
Женщины: КК (мл/мин) = 0.85 × значение, рассчитанное по формуле для мужчин.
Опыт применения препарата у детей ограничен. Безопасность и эффективность препарата Мозобаил для лечения детей не оценивались в контролируемых клинических исследованиях.
У пациентов пожилого возраста (старше 65 лет) с нормальной функцией почек коррекция дозы не требуется. При КК≤50 мл/мин рекомендуется коррекция дозы препарата. Следует помнить, что с возрастом вероятность снижения почечной функции увеличивается, поэтому у пациентов пожилого возраста дозу препарата следует подбирать с осторожностью.
Правила введения препарата
Для п/к введения. Один флакон препарата Мозобаил предназначен для однократного применения.
Перед введением необходимо осмотреть флакон. Если в препарате присутствуют механические включения или есть изменения цвета раствора, его вводить нельзя. Препарат Мозобаил является стерильным препаратом, не содержащим консерванты, поэтому в процессе набора содержимого флакона в шприц для п/к инъекций необходимо соблюдать правила асептики.
Исследования по совместимости препарата Мозобаил с другими препаратами не проводились, поэтому не следует его смешивать с другими препаратами в одном шприце.
Препарат, оставшийся после введения необходимой дозы, должен быть уничтожен.
Побочное действие
Данные по безопасности применения препарата Мозобаил в сочетании с Г-КСФ у онкологических пациентов с лимфомой и множественной миеломой были получены в 2 плацебо-контролируемых (фаза III) и 10 неконтролируемых исследованиях (фаза II) у 543 пациентов. Пациенты получали лечение плериксафором в дозе 0.24 мг/кг/сут п/к. Длительность лечения в этих исследованиях составила от 1 до 7 дней непрерывно (медиана — 2 дня).
В двух исследованиях (фаза III) с участием пациентов с неходжкинской лимфомой и множественной миеломой (AMD3100-3101 и AMD3100-3102 соответственно) был исследован 301 пациент, получавший лечение препаратом Мозобаил и Г-КСФ, и 292 пациента, получавших плацебо и Г-КСФ. Суточная доза Г-КСФ составляла 10 мкг/кг утром в течение 4 дней подряд до первой инъекции плериксафора или плацебо, а также каждое утро до проведения афереза.
Ниже представлены нежелательные реакции, которые чаще наблюдались в группе, получавшей препарат Мозобаил и Г-КСФ, чем в группе плацебо и Г-КСФ. Частота нежелательных реакций, связанных с лечением, составила ≥1% среди пациентов, получавших препарат Мозобаил, при мобилизации гемопоэтических стволовых клеток и аферезе, а также перед химиотерапией/миелоаблятивной терапией при подготовке к трансплантации.
Нежелательные реакции указаны в соответствии с системно-органным классом и частотой возникновения. Частоту определяли на основании следующих критериев: очень часто (≥1/10), часто (≥1/100 до <1/10), нечасто (≥1/1000 до <1/100), редко (≥1/10 000 до <1/1000), очень редко (<1/10 000), частота неизвестна (нельзя оценить по имеющимся данным).
При использовании химиотерапии/абляции в рамках подготовки к трансплантации не было отмечено значимой разницы в частоте нежелательных реакций между группами лечения через 12 мес после трансплантации.
Ниже приведены нежелательные реакции, наблюдавшиеся в группе препарата Мозобаил чаще, чем в группе плацебо, связанные с применением препарата Мозобаил при проведении мобилизации и афереза в III фазе исследований.
Со стороны иммунной системы: нечасто — аллергические реакции, анафилактические реакции, включая анафилактический шок.
Со стороны психики: часто — бессонница.
Со стороны нервной системы: часто — головная боль, головокружение.
Со стороны пищеварительной системы: очень часто — диарея, тошнота; часто — метеоризм, боли в животе, рвота, вздутие живота, сухость во рту, дискомфорт в эпигастральной области, запор, диспептические явления, гипестезия слизистой оболочки полости рта.
Со стороны кожи и подкожно-жировой клетчатки: часто — гипергидроз, эритема.
Со стороны костно-мышечной системы: часто — артралгия, скелетно-мышечная боль.
Прочие: очень часто — реакции в местах инъекции; часто — усталость, недомогание.
Нежелательные реакции у пациентов с лимфомой и множественной миеломой, получавших препарат Мозобаил в контролируемых исследованиях III фазы и неконтролируемых исследованиях, включая исследование II фазы, в котором препарат Мозобаил использовали в режиме монотерапии для мобилизации гемопоэтических стволовых клеток, сходны. У пациентов с онкологическими заболеваниями частота нежелательных реакций не отличалась в зависимости от заболевания, возраста или пола.
Аллергические реакции: аллергические реакции включали в себя одно или несколько следующих нежелательных реакций: крапивница (n=2), периорбитальный отек (n=2), одышка (n=1) или гипоксия (n=1). Данные реакции были легкой или умеренной степени тяжести и возникали в течение приблизительно 30 мин после введения препарата Мозобаил.
Инфаркт миокарда: согласно клиническим исследованиям, 7 из 679 онкологических пациентов перенесли инфаркт миокарда после мобилизации стволовых клеток с помощью плериксафора и Г-КСФ. Все случаи инфаркта миокарда наблюдались как минимум через 14 дней после последнего введения препарата Мозобаил. Кроме того, две пациентки, участвовавшие в программе по применению исследуемого препарата в индивидуальном порядке, перенесли инфаркт миокарда после мобилизации стволовых клеток с помощью плериксафора и Г-КСФ. Один из случаев инфаркта миокарда произошел через 4 дня после последнего введения препарата Мозобаил. Отсутствие временной связи у 8 из 9 пациентов и профиль риска участников, перенесших инфаркт миокарда, не позволяют считать препарат Мозобаил независимым фактором риска инфаркта миокарда у пациентов, получающих Г-КСФ.
Вазовагальные реакции: вазовагальные реакции (ортостатическая гипотензия и/или синкопе) отмечались менее чем у 1% участников клинических исследований по применению препарата Мозобаил (онкологических пациентов и здоровых добровольцев), получавших плериксафор в дозе ≤0.24 мг/кг. В большинстве случаев данные явления наблюдались в течение 1 ч после введения препарата Мозобаил.
Со стороны пищеварительной системы: в клинических исследованиях по применению препарата Мозобаил у онкологических пациентов сообщения о тяжелых нарушениях со стороны ЖКТ (включая диарею, тошноту, рвоту, боли в животе) регистрировались редко.
Парестезии: парестезии часто наблюдаются у онкологических пациентов после аутотрансплантации вследствие проводимых многочисленных медицинских процедур. В плацебо-контролируемых клинических исследованиях III фазы частота парестезии составила 20.6% и 21.2% в группах плериксафора и плацебо соответственно.
Гиперлейкоцитоз: в исследованиях III фазы увеличение количества лейкоцитов за день до афереза или в любой день афереза до 100×109/л и выше наблюдалось у 7% пациентов, получавших препарат Мозобаил, и у 1% пациентов, получавших плацебо. При этом осложнения или клинические проявления лейкоцитоза отсутствовали.
Пациенты пожилого возраста: 24% участников двух плацебо-контролируемых клинических исследований по применению плериксафора были старше 65 лет. Значимых различий по частоте нежелательных реакций в подгруппе пациентов пожилого возраста (по сравнению с пациентами более молодого возраста) не наблюдалось.
Постмаркетинговые наблюдения
Ниже приведены нежелательные реакции, о которых сообщалось в постмаркетинговый период применения препарата Мозобаил в дополнение к тем, которые были зафиксированы во время клинических исследований. Частоту нежелательных реакций определить было невозможно, т.к. сообщения о них были получены из популяции с неопределенным количеством пациентов, также как и возможную взаимосвязь с применением препарата.
Со стороны иммунной системы: анафилактические реакции, включая анафилактический шок.
Нарушения психики: необычные сновидения, кошмарные сновидения.
Противопоказания к применению
- беременность;
- период лактации (грудного вскармливания);
- детский и подростковый возраст до 18 лет (в связи с отсутствием опыта применения);
- повышенная чувствительность к плериксафору или любым вспомогательным веществам препарата.
Применение при беременности и кормлении грудью
Данных по применению плериксафора у беременных женщин недостаточно. Исследования на животных показали наличие тератогенного действия препарата. Пациент должен быть проинформирован, что применение плериксафора при беременности может привести к врожденным порокам развития. Применение препарата Мозобаил при беременности возможно только в тех случаях, когда польза от применения превышает потенциальный риск.
Женщинам детородного возраста во время лечения необходимо использовать эффективные средства контрацепции.
Данные о возможном проникновении плериксафора в грудное молоко отсутствуют, поэтому риск для грудного ребенка не может быть исключен. Во время терапии препаратом Мозобаил следует прекратить грудное вскармливание.
Применение при нарушениях функции почек
У пациентов с нарушением функции почек при КК≤50 мл/мин дозу плериксафора следует уменьшить на 1/3 до 0.16 мг/кг/сут.
Имеющийся опыт клинического применения плериксафора не позволяет дать рекомендаций по дозированию препарата при КК<20 мл/мин, а также у пациентов, находящихся на гемодиализе.
Применение у детей
Применение препарата противопоказано в возрасте до 18 лет (в связи с отсутствием опыта применения).
Применение у пожилых пациентов
У пожилых пациентов с нормальной функцией почек коррекция дозы не требуется. При КК≤50 мл/мин рекомендуется коррекция дозы препарата.
Особые указания
Мобилизация опухолевых клеток у пациентов с лейкозами
Препарат Мозобаил и Г-КСФ назначали при остром миелоидном и плазмоцитарном лейкозах в рамках программы по применению исследуемого препарата в индивидуальном порядке. При этом в отдельных случаях наблюдалось увеличение числа циркулирующих лейкемических клеток. Плериксафор, назначаемый для мобилизации гемопоэтических стволовых клеток, может вызвать мобилизацию клеток опухоли с последующим их попаданием в продукт афереза. Поэтому плериксафор не рекомендуется применять при лейкозах для мобилизации гемопоэтических стволовых клеток и их последующего забора.
Гематологические эффекты
Гиперлейкоцитоз. Препарат Мозобаил, назначаемый в сочетании с Г-КСФ, увеличивает не только популяцию гемопоэтических стволовых клеток, но и количество циркулирующих лейкоцитов. Во время применения препарата Мозобаил следует контролировать количество лейкоцитов. Следует тщательно оценивать каждый случай назначения препарата Мозобаил пациентам, у которых количество нейтрофилов в периферической крови превышает 50 000 клеток/мкл.
Тромбоцитопения. Тромбоцитопения является известным осложнением афереза и наблюдается у пациентов, получающих препарат Мозобаил. Число тромбоцитов необходимо контролировать у всех пациентов, которые получают препарат Мозобаил и которым планируется проведение афереза.
Возможность мобилизации опухолевых клеток у пациентов с лимфомой и множественной миеломой
Последствия потенциальной реинфузии опухолевых клеток должным образом не изучены. При применении препарата Мозобаил в сочетании с Г-КСФ (для мобилизации гемопоэтических стволовых клеток при лимфоме или множественной миеломе) возможно высвобождение клеток опухоли из костного мозга и их последующий забор при лейкоферезе. Клиническое значение возможного риска мобилизации опухолевых клеток определено не полностью. В клинических исследованиях с участием пациентов с неходжкинской лимфомой и множественной миеломой не наблюдалось мобилизации клеток опухоли при применении плериксафора.
Аллергические реакции
Аллергические реакции легкой и средней степени разрешались спонтанно или купировались соответствующей терапией (например, антигистаминные препараты, ГКС, гидратация, оксигенотерапия). Серьезные реакции гиперчувствительности, в т.ч. анафилактические реакции (некоторые из них были жизнеугрожающими с клинически значимым снижением АД и шоком), были зарегистрированы у пациентов, получающих Мозобаил. Рекомендуется наблюдение пациентов во время и после введения Мозобаила в течение, по крайней мере, 30 мин после каждого применения препарата. Потенциальный риск аллергических реакций требует соблюдения соответствующих мер предосторожности.
Вазовагальные реакции
После п/к инъекций препарата могут отмечаться вазовагальные реакции, ортостатическая гипотензия и/или синкопе. В связи с возможностью развития таких реакций необходимо соблюдать соответствующие меры предосторожности. В основном эти реакции развивались в течение 1 ч после применения препарата Мозобаил.
Спленомегалия
В доклинических исследованиях наблюдалось увеличение абсолютной и относительной массы селезенки, связанное с экстрамедуллярным кроветворением, при длительном (2-4 недели) ежедневном введении плериксафора крысам (п/к инъекции; доза препарата превышала дозу, рекомендованную для человека, в 4 раза).
В клинических исследованиях влияние плериксафора на размер селезенки специально не оценивалось. Таким образом, нельзя полностью исключить возможность увеличения селезенки на фоне приема плериксафора и Г-КСФ. В очень редких случаях назначение Г-КСФ приводит к разрыву селезенки. Об этом следует помнить, когда пациенты, получающие препарат Мозобаил в сочетании с Г-КСФ, предъявляют жалобы на боли в левом подреберье и/или в области лопатки или плеча.
Контроль лабораторных показателей
У пациентов, получающих препарат Мозобаил и проходящих аферез, необходимо контролировать число лейкоцитов и тромбоцитов крови.
Натрий
Каждая доза препарата Мозобаил содержит менее 1 ммоль натрия (23 мг), то есть практически его не содержит.
Влияние на способность управлять транспортными средствами, механизмами
Поскольку у некоторых пациентов наблюдалось головокружение, утомляемость или вазовагальные реакции, необходимо соблюдать осторожность при управлении транспортными средствами и занятии другими потенциально опасными видами деятельности. При появлении описанных нежелательных явлений следует воздержаться от выполнения указанных видов деятельности.
Передозировка
Случаев передозировки зафиксировано не было. С учетом ограниченных данных о применении препарата в дозе, превышающей рекомендованную (до 0.48 мг/кг), можно предположить, что частота нарушений со стороны ЖКТ, вазовагальных реакций, ортостатической гипотензии и/или синкопе может увеличиваться.
Лекарственное взаимодействие
Исследований по изучению лекарственного взаимодействия препарата не проводилось. Тесты, проведенные in vitro, показали, что плериксафор не метаболизируется изоферментами цитохрома Р450, а также не подавляет и не усиливает их активность. Согласно исследованиям in vitro, плериксафор не является субстратом или ингибитором Р-гликопротеина.
Добавление ритуксимаба к «режиму мобилизации» (плериксафор и Г-КСФ) в клинических исследованиях с участием пациентов с неходжкинской лимфомой, не оказывало влияния на безопасность пациента или концентрацию CD34+ клеток.
Условия хранения препарата Мозобаил
Препарат следует хранить в недоступном для детей месте при температуре от 15°С до 30°С.
Срок годности препарата Мозобаил
Срок годности — 3 года. Не применять по истечении срока годности.
Условия реализации
Препарат отпускается по рецепту.
Контакты для обращений
САНОФИ

|
|
Представительство |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Мозобаил — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер:
ЛП-002352.
Торговое название:
Мозобаил
Международное непатентованное название:
плериксафор
Лекарственная форма:
раствор для подкожного введения.
Состав
1 флакон содержит:
действующее вещество: плериксафор 24 мг;
вспомогательные вещества: натрия хлорид 5,9 мг, 0,1 М раствор натрия гидроксида или 0,1 М раствора кислоты хлористоводородной до рН 6,0-7,5, вода для инъекций до 1,2 мл.
Описание:
прозрачная бесцветная или светло-желтая жидкость.
Фармакотерапевтическая группа:
иммуностимулирующее средство.
АТХ код:
L03AX16.
Фармакологические свойства
Фармакодинамика
Механизм действия
Плериксафор представляет собой производное бициклама и является селективным обратимым антагонистом CXCR4 хемокинового рецептора, блокируя его за счет связывания с когнатным лигандом, фактором стромальных клеток-1а (SDF-1a), также известным как CXCL12. Считается, что индуцированный плериксафором лейкоцитоз и увеличение количества циркулирующих гемопоэтических прогениторных клеток является результатом нарушения связи между CXCR4 и его когнатным лигандом, которое приводит к появлению в системном кровотоке как зрелых, так и полипотентных клеток. CD34+ клетки, мобилизованные с помощью плериксафора, являются функциональными и способными к приживлению, с долгосрочным потенциалом восстановления популяции.
Фармакодинамика
В двух плацебо-контролируемых клинических исследованиях с участием пациентов с лимфомой и множественной миеломой (AMD3100-3101 и AMD3100-3102, соответственно) оценивалось увеличение содержания CD34+ клеток (клеток/мкл) за 24 ч, в течение дня перед первым аферезом (Таблица 1). В оцениваемый 24-часовой период первая доза плериксафора (0,24 мг/кг) или плацебо вводилась за 10-11 ч до афереза.
Таблица 1.
Увеличение числа CD34+ клеток в периферической крови после введения препарата Мозобаил совместно с гранулоцитарным колониестимулирующим фактором (Г-КСФ)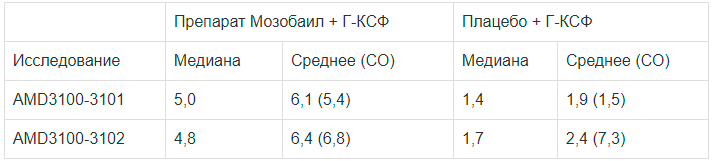
В исследованиях фармакодинамики у здоровых добровольцев с применением только плериксафора пик мобилизации CD34+ клеток наблюдался в течение 6-9 ч после введения препарата. При исследовании фармакодинамики как у здоровых добровольцев, так и у пациентов с применением схемы мобилизации, включающей гранулоцитарный колониестимулирующий фактор (Г-КСФ) и плериксафор в тех же дозах, наблюдался более длительный подъем CD34+ клеток в периферической крови в течение с 4 ч до 18 ч после введения препарата, пик был отмечен между 10 ч и 14 ч.
Дети
Эффективность и безопасность применения препарата Мозобаил у детей и подростков в возрасте до 18 лет в клинических исследованиях не изучались.
Европейское медицинское агентство отказалось от обязательного предоставления компанией результатов исследований по применению препарата Мозобаил у детей и подростков в возрасте до 18 лет при миелосупрессии (вследствие химиотерапии, проводимой для лечения злокачественных новообразований), требующей аутотрансплантации гемопоэтических стволовых клеток (см. раздел «Способ применения и дозы»).
Фармакокинетика
Фармакокинетику плериксафора изучали у пациентов с лимфомой и множественной миеломой с применением клинической дозы (0,24 мг/кг) после предварительного лечения Г-КСФ (10 мкг/кг один раз в день в течение от 2 до 4 дней, при необходимости курс продлевали до 7 дней).
Абсорбция
Плериксафор быстро всасывается после подкожного введения, максимальная концентрация достигает приблизительно через 30-60 мин (Tmax). После подкожного введения плериксафора в дозе 0,24 мг/кг, которому предшествовало предварительное лечение Г-КСФ в течение 4 дней подряд, максимальная концентрация (Cmax) плериксафора в плазме крови и среднее значение площади под фармакокинетической кривой «концентрация-время» (AUC0-24) составили 887 ± 217 нг/мл и 4337 ± 922 нгч/мл соответственно.
Распределение
Плериксафор умеренно связывается с белками плазмы человека (до 58%). Кажущийся объем распределения плериксафора у людей составляет 0,3 л/кг, это говорит о том, что препарат склонен к распределению во внесосудистом пространстве, но не ограничен им.
Метаболизм
В экспериментах in vitro плериксафор не подвергался метаболизму печеночными микросомами человека и эмбриональными гепатоцитами человека. Также in vitro было показано, что препарат не угнетает основные метаболизирующие изоферменты цитохрома Р450 (1A2, 2A6, 2B6, 2C8, 2C9, 2C19, 2D6, 2E1 и 3A4/5). В экспериментах in vitro с человеческими гепатоцитами плериксафор не индуцировал изоферменты CYP1A2, CYP2B6, и CYP3A4. Полученные данные позволяют предположить, что потенциал лекарственных взаимодействий, опосредованных системой P450, для плериксафора низок.
Элиминация
Основной путь элиминации плериксафора — выведение через почки. После введения плериксафора в дозе 0,24 мг/кг здоровым добровольцам с нормальной функцией почек, примерно 70% препарата выводилось с мочой в неизмененном виде в течение первых 24 ч после введения. Период полувыведения из плазмы (T1/2) составляет 3-5 ч. По данным исследований in vitro с использованием клеточных моделей MDCKII и MDCKII-MDR1, плериксафор не является субстратом или ингибитором Р-гликопротеина.
Особые группы пациентов
Пациенты с нарушением функции почек
У лиц с различной степенью почечной недостаточности клиренс плериксафора после однократной дозы (0,24 мг/кг) уменьшался; наблюдалась положительная корреляция с клиренсом креатинина (КК). Средние показатели AUC0-24 для плериксафора, вводимого субъектам с легкой (КК 51-80 мл/мин), умеренной (КК 31-50 мл/мин) и тяжелой (КК ≤ 30 мл/мин) степенью почечной недостаточности, составили 5410, 6780 и 6990 нгч/мл, соответственно, что превышает значения экспозиции препарата, наблюдаемые при нормальной функции почек (5070 нгч/мл). Почечная недостаточность не оказывала влияния на Cmax.
Пол
Популяционный анализ не выявил различий фармакокинетики плериксафора по полу.
Пожилые пациенты
Популяционный анализ не выявил различий фармакокинетики плериксафора по возрасту.
Дети
Данные по фармакокинетике у детей ограничены.
Показания к применению
Для усиления мобилизации гемопоэтических стволовых клеток в периферический кровоток с целью их сбора и последующей аутотрансплантации пациентам с лимфомой и множественной миеломой в сочетании с гранулоцитарным колониестимулирующим фактором (Г-КСФ).
Противопоказания
— Повышенная чувствительность к плериксафору или любым вспомогательным веществам препарата;
— Беременность (см. раздел «Беременность и период грудного вскармливания»);
— Лактация (см. раздел «Беременность и период грудного вскармливания»);
— Детский и подростковый возраст до 18 лет (в связи с отсутствием опыта применения).
Беременность и период грудного вскармливания
Беременность
Данных по применению плериксафора у беременных женщин недостаточно. Исследования на животных показали наличие тератогенного действия препарата. Пациент должен быть проинформирован, что применение плериксафора во время беременности может привести к врожденным порокам развития. Применение препарата Мозобаил во время беременности возможно только в тех случаях, когда польза от применения превышает возможный потенциальный риск.
Женщины детородного возраста
Женщинам детородного возраста во время лечения необходимо использовать эффективные средства контрацепции.
Период грудного вскармливания
Данные о возможном проникновении плериксафора в грудное молоко отсутствуют, поэтому риск для грудного ребенка не может быть исключен. Во время терапии препаратом Мозобаил следует прекратить грудное вскармливание.
Способ применения и дозы
Лечение препаратом Мозобаил должен назначать и проводить квалифицированный онколог и/или гематолог. Мобилизация и аферез клеток должны проводиться в сотрудничестве с онкогематологическим центром, имеющим достаточный опыт в данной области, где есть возможность надлежащего контроля уровня гемопоэтических прогениторных клеток.
Дозы
Рекомендованная доза плериксафора составляет 0,24 мг/кг/сут. Препарат вводят подкожно за 6-11 ч до начала афереза после предварительной четырехдневной терапии Г-КСФ. В клинических исследованиях препарат Мозобаил обычно использовался в течение 2-4 дней подряд (до 7 дней непрерывного применения). Для расчета дозы плериксафора используют среднее значение массы тела, измеряемое в течение 1 недели до введения первой дозы препарата.
В клинических исследованиях дозу плериксафора рассчитывали на основании массы тела пациентов, у которых отклонения массы тела от идеальной составляли не более 175%. Режим дозирования и особенности лечения пациентов, отклонения массы тела у которых составляют более 175% от идеальной, не изучали.
Дозу препарата Мозобаил (в мл) рассчитывают по формуле: 0,012 х фактическая масса тела (кг).
Учитывая, что воздействие препарата с увеличением массы тела возрастает, доза плериксафора не должна превышать 40 мг/сут.
Рекомендованные сопутствующие препараты
В базовых клинических испытаниях, поддерживающих лечение препаратом Мозобаил, все пациенты получали Г-КСФ в дозе 10 мкг/кг, утром, в течение 4 дней подряд до первого введения плериксафора, а затем каждое утро до проведения афереза.
Применение препарата у особых групп пациентов
Пациенты с нарушением функции почек
При клиренсе креатинина ≤ 50 мл/мин доза плериксафора должна быть уменьшена на треть, до 0,16 мг/кг/сут (см. раздел «Фармакокинетика»). Клинические данные по применению скорректированной дозы препарата ограничены. Имеющийся опыт клинического применения плериксафора не позволяет дать рекомендаций по дозированию препарата при клиренсе креатинина < 20 мл/мин, а также у пациентов, находящихся на гемодиализе. Учитывая, что воздействие препарата с увеличением массы тела возрастает, доза плериксафора не должна превышать 27 мг/сут, если клиренс креатинина ≤ 50 мл/мин. Клиренс креатинина (в мл/мин) рассчитывают по формуле:
Дети
Опыт использования препарата у детей ограничен. Безопасность и эффективность препарата Мозобаил для лечения детей не оценивались в контролируемых клинических исследованиях.
Пациенты пожилого возраста (более 65 лет)
У пожилых пациентов с нормальной функцией почек коррекция дозы не требуется. При клиренсе креатинина ≤ 50 мл/мин рекомендуется изменить дозу препарата (см. выше подраздел «Пациенты с нарушением функции почек»). Следует помнить, что с возрастом вероятность снижения почечной функции увеличивается, поэтому у пожилых пациентов дозу препарата следует подбирать с осторожностью.
Способ применения
Для подкожного введения. Один флакон препарата Мозобаил предназначен для однократного применения.
Перед введением необходимо осмотреть флакон. Если в препарате присутствуют механические включения или есть изменения цвета раствора, его вводить нельзя. Препарат Мозобаил является стерильным препаратом, не содержащим консерванты, поэтому в процессе набора содержимого флакона в шприц для подкожных инъекций необходимо соблюдать правила асептики.
Исследования по совместимости препарата Мозобаил с другими препаратами не проводились, поэтому не следует его смешивать с другими препаратами в одном шприце.
Препарат, оставшийся после введения необходимой дозы, должен быть уничтожен.
Побочное действие
Данные по безопасности применения препарата Мозобаил в сочетании с Г-КСФ у онкологических пациентов с лимфомой и множественной миеломой были получены в 2 плацебо-контролируемых (фаза III) и 10 неконтролируемых исследованиях (фаза II) у 543 пациентов. Пациенты получали лечение плериксафором в дозе 0,24 мг/кг/сут подкожно. Длительность лечения в этих исследованиях составила от 1 до 7 дней непрерывно (медиана — 2 дня).
В двух исследованиях (фаза III) с участием пациентов с неходжкинской лимфомой и множественной миеломой (AMD3100-3101 и AMD3100-3102, соответственно) был исследован 301 пациент, получавший лечение препаратом Мозобаил и Г-КСФ, и 292 пациента, получавших плацебо и Г-КСФ. Суточная доза Г-КСФ составляла 10 мкг/кг утром в течение 4 дней подряд до первой инъекции плериксафора или плацебо, а также каждое утро до проведения афереза.
Ниже представлены нежелательные реакции, которые чаще наблюдались в группе, получавшей препарат Мозобаил и Г-КСФ, чем в группе плацебо и Г-КСФ. Частота нежелательных реакций, связанных с лечением, составила ≥ 1 % среди пациентов, получавших препарат Мозобаил, при мобилизации гемопоэтических стволовых клеток и аферезе, а также перед химиотерапией/миелоаблятивной терапией при подготовке к трансплантации. Нежелательные реакции указаны в соответствии с системно-органным классом и частотой возникновения. Частоту определяли на основании следующих критериев: очень часто (≥ 1/10), часто (≥ 1/100 до < 1/10), нечасто (≥ 1/1000 до < 1/100), редко (≥ 1/10000 до < 1/1000), очень редко < 1/10000), частота неизвестна (нельзя оценить по имеющимся данным).
При использовании химиотерапии/абляции в рамках подготовки к трансплантации не было отмечено значимой разницы в частоте нежелательных реакций между группами лечения через 12 мес после трансплантации.
Ниже приведены нежелательные реакции, наблюдавшиеся в группе препарата Мозобаил чаще, чем в группе плацебо, связанные с применением препарата Мозобаил при проведении мобилизации и афереза в III фазе исследований.
Нарушения со стороны иммунной системы
Нечасто: аллергические реакции, анафилактические реакции, включая анафилактический шок (См. подраздел «Постмаркетинговые наблюдения» и раздел «Влияние»).
Нарушения психики
Часто: бессонница.
Нарушения со стороны нервной системы
Часто: головная боль, головокружение.
Нарушения со стороны желудочно-кишечного тракта
Очень часто: диарея, тошнота.
Часто: метеоризм, боли в животе, рвота, вздутие живота, сухость во рту, дискомфорт в эпигастральной области, запор, диспепсические явления, гипестезия слизистой оболочки полости рта.
Нарушения со стороны кожи и подкожных тканей
Часто: гипергидроз, эритема.
Нарушения со стороны скелетно-мышечной и соединительной ткани
Часто: артралгия, скелетно-мышечная боль.
Общие расстройства и нарушения в месте введения
Очень часто: реакции в месте инъекции.
Часто: усталость, недомогание.
Нежелательные реакции у пациентов с лимфомой и множественной миеломой, получавших препарат Мозобаил в контролируемых исследованиях III фазы и неконтролируемых исследованиях, включая исследование II фазы, в котором препарат Мозобаил использовали в режиме монотерапии для мобилизации гемопоэтических стволовых клеток, сходны. У пациентов с онкологическими заболеваниями частота нежелательных реакций не отличалась в зависимости от заболевания, возраста или пола.
Аллергические реакции
Аллергические реакции включали в себя одно или несколько следующих нежелательных реакций: крапивница (n=2), периорбитальный отек (n=2), одышка (n=1) или гипоксия (n=1). Данные реакции были легкой или умеренной степени тяжести и возникали в течение приблизительно 30 мин после введения препарата Мозобаил.
Инфаркт миокарда
Согласно клиническим исследованиям, 7 из 679 онкологических пациентов перенесли инфаркт миокарда после мобилизации стволовых клеток с помощью плериксафора и Г-КСФ. Все случаи инфаркта миокарда наблюдались как минимум через 14 дней после последнего введения препарата Мозобаил. Кроме того, две пациентки, участвовавшие в программе по применению исследуемого препарата в индивидуальном порядке, перенесли инфаркт миокарда после мобилизации стволовых клеток с помощью плериксафора и Г-КСФ. Один из случаев инфаркта миокарда произошел через 4 дня после последнего введения препарата Мозобаил. Отсутствие временной связи у 8 из 9 пациентов и профиль риска участников, перенесших инфаркт миокарда, не позволяют считать препарат Мозобаил независимым фактором риска инфаркта миокарда у пациентов, получающих Г-КСФ.
Вазовагальные реакции
Вазовагальные реакции (ортостатическая гипотензия и/или синкопе) отмечались менее чем у 1 % участников клинических исследований по применению препарата Мозобаил (онкологических пациентов и здоровых добровольцев), получавших плериксафор в дозе ≤ 0,24 мг/кг. В большинстве случаев данные реакции наблюдались в течение 1 ч после введения препарата Мозобаил.
Нарушения со стороны желудочно-кишечного тракта
В клинических исследованиях по применению препарата Мозобаил у онкологических пациентов сообщения о тяжелых нарушениях со стороны желудочно-кишечного тракта (включая диарею, тошноту, рвоту, боли в животе) регистрировались редко.
Парестезии
Парестезии часто наблюдаются у онкологических пациентов после аутотрансплантации вследствие проводимых многочисленных медицинских процедур. В плацебо-контролируемых клинических исследованиях III фазы частота парестезий составила 20,6 % и 21,2 % в группах плериксафора и плацебо, соответственно.
Гиперлейкоцитоз
В исследованиях III фазы увеличение количества лейкоцитов за день до афереза или в любой день афереза до 100 х 109/л и выше наблюдалось у 7 % пациентов, получавших препарат Мозобаил, и у 1 % пациентов, получавших плацебо. При этом осложнения или клинические проявления лейкоцитоза отсутствовали.
Пациенты пожилого возраста
24 % участников двух плацебо-контролируемых клинических исследований по применению плериксафора были старше 65 лет. Значимых различий по частоте нежелательных реакций в подгруппе пациентов пожилого возраста (по сравнению с пациентами более молодого возраста) не наблюдалось.
Постмаркетинговые наблюдения
Ниже приведены нежелательные реакции, о которых сообщалось в постмаркетинговый период применения препарата Мозобаил в дополнение к тем, которые были зафиксированы во время клинических исследований. Частоту нежелательных реакций определить было невозможно, так как сообщения о них были получены из популяции с неопределенным количеством пациентов, также как и возможную взаимосвязь с применением препарата.
Нарушения со стороны иммунной системы
Анафилактические реакции, включая анафилактический шок.
Нарушения психики:
необычные сновидения, ночные кошмары.
Передозировка
Случаев передозировки зафиксировано не было. С учетом ограниченных данных о применении препарата в дозе, превышающей рекомендованную (до 0,48 мг/кг), можно предположить, что частота нарушений со стороны желудочно-кишечного тракта, вазовагальных реакций, ортостатической гипотензии и/или синкопе может увеличиваться.
Взаимодействие с другими лекарственными препаратами
Исследований по изучению взаимодействий данного препарата не проводилось. Тесты, проведенные in vitro, показали, что плериксафор не метаболизируется изоферментами цитохрома P450, а также не подавляет и не усиливает их активность. Согласно исследованиям in vitro, плериксафор не является субстратом или ингибитором Р-гликопротеина.
Добавление ритуксимаба к «режиму мобилизации» (плериксафор и Г-КСФ) в клинических исследованиях с участием пациентов с неходжкинской лимфомой, не оказывало влияния на безопасность пациента или концентрацию CD34+ клеток.
Особые указания
Мобилизация опухолевых клеток у пациентов с лейкозами
Препарат Мозобаил и Г-КСФ назначали при остром миелоидном и плазмоцитарном лейкозах в рамках программы по применению исследуемого препарата в индивидуальном порядке. При этом в отдельных случаях наблюдалось увеличение числа циркулирующих лейкемических клеток. Плериксафор, назначаемый для мобилизации гемопоэтических стволовых клеток, может вызвать мобилизацию клеток опухоли с последующим их попаданием в продукт афереза. Поэтому плериксафор не рекомендуется применять при лейкозах для мобилизации гемопоэтических стволовых клеток и их последующего забора.
Гематологические эффекты
Гиперлейкоцитоз
Препарат Мозобаил, назначаемый в сочетании с Г-КСФ, увеличивает не только популяцию гемопоэтических стволовых клеток, но и количество циркулирующих лейкоцитов. Во время применения препарата Мозобаил следует контролировать количество лейкоцитов. Следует тщательно оценивать каждый случай назначения препарата Мозобаил пациентам, у которых количество нейтрофилов в периферической крови превышает 50000 клеток/мкл.
Тромбоцитопения
Тромбоцитопения является известным осложнением афереза и наблюдается у пациентов, получающих препарат Мозобаил. Число тромбоцитов необходимо контролировать у всех пациентов, которые получают препарат Мозобаил и которым планируется проведение афереза.
Возможность мобилизации опухолевых клеток у пациентов с лимфомой и множественной миеломой
Последствия потенциальной реинфузии опухолевых клеток должным образом не изучены. При использовании препарата Мозобаил в сочетании с Г-КСФ (для мобилизации гемопоэтических стволовых клеток при лимфоме или множественной миеломе) возможно высвобождение клеток опухоли из костного мозга и их последующий забор при лейкоферезе. Клиническое значение возможного риска мобилизации опухолевых клеток определено не полностью. В клинических исследованиях с участием пациентов с неходжкинской лимфомой и множественной миеломой не наблюдалось мобилизации клеток опухоли при применении плериксафора.
Аллергические реакции
Легкие и средней степени аллергические реакции (см. раздел «Побочное действие») разрешались спонтанно или курировались соответствующей терапией (например, антигистаминные препараты, глюкокортикостероиды, гидратация, оксигенотерапия). Серьезные реакции гиперчувствительности, в том числе анафилактические реакции, некоторые из которых были угрожающие жизни с клинически значимым снижением артериального давления и шоком, были зарегистрированы у пациентов, получающих Мозобаил. Рекомендуется наблюдение пациентов во время и после введения Мозобаила в течение, по крайней мере, 30 минут после каждого применения препарата. Потенциальный риск аллергических реакций требует соблюдения соответствующих мер предосторожности.
Вазовагальные реакции
После подкожных инъекций препарата могут отмечаться вазовагальные реакции, ортостатическая гипотензия и/или синкопе (см. раздел «Побочное действие»). В связи с возможностью развития таких реакций необходимо соблюдать соответствующие меры предосторожности. В основном эти реакции развивались в течение 1 ч после применения препарата Мозобаил.
Спленомегалия
В доклинических исследованиях наблюдалось увеличение абсолютной и относительной массы селезенки, связанное с экстрамедуллярным кроветворением, при длительном (2-4 недели) ежедневном введении плериксафора крысам (подкожные инъекции; доза препарата превышала дозу, рекомендованную для человека, в 4 раза).
В клинических исследованиях влияние плериксафора на размер селезенки специально не оценивалось. Таким образом, нельзя полностью исключить возможность увеличения селезенки на фоне приема плериксафора и Г-КСФ. В очень редких случаях назначение Г-КСФ приводит к разрыву селезенки. Об этом следует помнить, когда пациенты, получающие препарат Мозобаил в сочетании с Г-КСФ, предъявляют жалобы на боли в левом подреберье и/или в области лопатки или плеча.
Контроль лабораторных показателей
У пациентов, получающих препарат Мозобаил и проходящих аферез, необходимо контролировать число лейкоцитов и тромбоцитов крови.
Натрий
Каждая доза препарата Мозобаил содержит менее 1 ммоль натрия (23 мг), то есть практически его не содержит.
Влияние на способность управлять транспортными средствами, механизмами
Поскольку у некоторых пациентов наблюдалось головокружение, утомляемость или вазовагальные реакции, необходимо соблюдать осторожность при управлении транспортными средствами и занятии другими потенциально опасными видами деятельности.
При появлении описанных нежелательных явлений следует воздержаться от выполнения указанных видов деятельности.
Форма выпуска
Раствор для подкожного введения 20 мг/мл.
По 1,2 мл раствора во флакон из бесцветного стекла I типа, укупоренный резиновой пробкой и обжатый алюминиевым колпачком с пластиковой крышечкой типа «flip-off». По 1 флакону вместе с инструкцией по применению в картонную пачку.
Условия хранения
Хранить при температуре от 15 °С до 30 °С.
Хранить в недоступном для детей месте.
Срок годности
3 года.
Не использовать по истечении срока годности.
Условия отпуска
Отпускается по рецепту.
Владелец РУ
Джензайм Европа Б.В., Нидерланды.
Производитель
Производитель готовой лекарственной формы и фасовщик (первичная упаковка):
Джензайм Корпорейшн, США.
Genzyme Corporation,
1125 Pleasantview Terrace, Ridgefield, NJ 07657, USA.
Упаковщик (вторичная (потребительская) упаковка и выпускающий контроль качества:
Джензайм Лтд, Великобритания.
Genzyme Ltd.,
37 Hollands Road, Haverhill, Suffolk, CB9 8PU, United Kingdom.
Претензии потребителей направлять по адресу представительства компании в России:
125009, г. Москва, ул. Тверская, 22.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)

Товары из категории — Лекарства от болезней крови
Инструкция по применению
Фармакокинетика
-
Представленная инструкция по применению содержит сведения о показаниях и возможных противопоказаниях к приему Мозобаила — лекарственного средства, относящегося к группе стимуляторов лейкопоэза. Входящее в его состав вещество — Плериксафор, является основой для терапевтического воздействия в отношении лейкопении или агранулоцитоза. При терапии заболеваний крови этот вид патологии при онкологических и опухолевых процессах несет опасность для пациентов. Недостаточная выработка лейкоцитов, подразумевает развитие опасных для здоровья состояний, сопряженных с невозможностью подавления бактериальной флоры и токсинов. Эти вещества входят в цитоплазму, и в научной среде называются гранулоцитами.
Мозобаил при приеме внутрь в терапевтической дозировке представленная производителем инструкция предписывает назначать для коррекции состояний, связанных с понижением содержания лейкоцитов в цитоплазме. Причинами для проведения терапии является проявление заболеваний, вызываемых влиянием инфекционных факторов, микробной среды, яда. В редких случаях агранулоцитоз развивается на фоне приема лекарственных средств, оказывающих негативное воздействие на ткани костного мозга.
Лейкопения в тяжелой форме требует долгого лечения, и представляет серьезную опасность для организма человека. Развитие агранулоцитоза часто оказывается сопряжено с бесконтрольным приемом лекарственных средств для терапии онкологических болезней и опухолевых процессов, бутадиона, фенотиазина, сульфаниламидов. Опасный для жизни порог снижения объемов гранулоцитов в цитоплазме составляет 2000/1 мм3. При выявлении кардинальных изменений в показателях содержания лейкоцитов требуется назначение лечения с использованием Мозобаила и других стимуляторов лейкопоэза.
Действие, которое оказывает препарат основано на его фармакологических свойствах. Плериксафор, входящий в содержимое вещества, относится к разряду лекарств, произведенных на основе бициклама. Средство не назначают детям до 18 лет ввиду отсутствия достоверных данных о безопасности средства. При попадании внутрь препарат в терапевтической дозировке обеспечивает распространение за пределы сосудистой системы, выводится через почки. Лицам с почечными, печеночными болезнями, лекарство назначают с учетом степени тяжести основной патологии. Пожилым людям назначения производят в стандартном объеме.
Состав и форма выпуска
Лекарство назначают в виде инъекционного раствора для п/к введения, бесцветного или со светло-желтым оттенком. Флаконы ампул стеклянные, объемом 1.2 мл, упакованы в картонные пачки. В 1 мл упаковки содержится 20 мг действующего вещества плериксафора. Содержит дополнительные компоненты, при назначении терапии учитывают возможное развитие аллергических реакций.

Показания к применению
Сбор стволовых клеток для последующей аутотрансплантации. Лекарство обеспечивает мобилизацию лейкоцитов в периферическую систему кровотока. При лимфоме, миеломах множественного типа используемые клетки вводятся обратно пациенту, обеспечивая возможности для стимуляции их роста и развития. Обязательно сочетание п/к введения с Г-КСФ.
Международная классификация болезней (МКБ-10)
C90.0 Миелома множественная.
C85 Лимфома (неходжкинская) неуточненной классификации.
Побочные эффекты
Прием лекарства способен вызывать индивидуальные негативные реакции организма. Общее процентное соотношение таких случаев к общей массе назначений составляет не более 1%. Средство совместимо с проведением абляции/химиотерапии. Аллергические реакции непосредственно на активное вещество — плериксафор, выявляются редко. Возможно развитие анафилактического шока в особенно тяжелых случаях.
Средство при введении в периферический кровоток способно вызывать нервное перевозбуждение, нарушать нормальное течение процессов сна. Лекарство способно вызывать головокружение при приеме внутрь. Терапию следует назначать с учетом возможного проявления повышенной потливости, эритемы. Желудочно-кишечные негативные реакции наблюдаются часто, сопровождаются тошнотой, расстройствами стула, вздутиями, рвотным рефлексом, сухостью слизистых оболочек полости рта. Костно-мышечная система способна реагировать на употребление лекарства проявлениями болевых ощущений, развитием артралгии. В отдельных случаях выявляют повышенную усталость, общую слабость. Место укола всегда болезненно, демонстрирует негативные реакции при воздействии. Наличие злокачественных опухолевых процессов не влияет на частоту и интенсивность развития негативных реакций. Около 1% пациентов в качестве негативной реакции организма демонстрировали выявление инфаркта миокарда в период после терапии с использованием плериксафора (по истечению двух недель и более).
Противопоказания
Не назначается лекарство при наличии:
Применение при беременности
Лекарственное средство обладает способностью обеспечивать тератогенное действие на плод в ходе его внутриутробного развития. Беременные женщины в обязательном порядке информируются о повышенном риске развития врожденных пороков. Оценка вероятного риска производится с учетом тяжести состояния пациентки. При назначении терапии женщинам в детородном возрасте следует подобрать надежное средство контрацепции. В период лактации прием отменяют или переводят ребенка на искусственное вскармливание в связи с отсутствием данных исследований о проникновении плериксафора в грудное молоко.
Способ и особенности применения
Употребление лекарственного средства в форме раствора для п/к введения требует назначения Мозобаила исключительно для введения квалифицированным медицинским персоналом (онкологом или гематологом), на базе онкогематологических центров, оборудованных современным оснащением для контроля за уровнем прогениторных клеток (гемопоэтических).
Стандартная (суточная) терапевтическая доза лекарства составляет 0,24 мг/кг. Введение выполняется п/к до начала афереза (выдерживая период в 6-11 часов). Предварительно необходимо проведение терапии Г-КСФ. Продолжительность терапевтического воздействия плериксафора составляет не более 7 суток. Объемы лекарства для введения в кровоток рассчитываются исходя из массы тела пациента. При отклонении весовых показателей более чем на 175% от нормальных требуют индивидуального рассмотрения целесообразности сделанных назначений.
Объемы Мозобаила для терапии у пациентов определяются индивидуально, с учетом 0,012 мл на 1 кг веса, с максимально возможным суточным потреблением в пределах 40 мг. При наличии выявленного нарушения функции почек необходима индивидуальная коррекция схемы терапевтического воздействия. При росте концентрации креатинина в пожилом возрасте объемы лекарства должны быть снижены до необходимых отметок с учетом состояния пациентов.
Введение выполняется только п/к. Один флакон Мозобаила используется исключительно для разового потребления. Перед началом терапии необходимо обеспечить тщательный контроль за прозрачностью, чистотой раствора. Любые изменения цвета требуют отмены использования лекарства. Требуется обеспечить асептический контроль при вскрытии упаковки, не хранить средство после того как флакон будет открыт. Не рекомендуется смешивать лекарство с другими медикаментами в одном шприце.
Взаимодействие с другими лекарствами
Мозобаил при употреблении с другими лекарствами не оказывает выраженного воздействия на их фармакокинетику.
Передозировка
Стимулятор лейкопоэза Мозобаил при соблюдении рекомендованных объемов не приводит к передозировке. Средство вводится в периферический кровоток инъекционно, иных форм выпуска нет. Возможность для самостоятельного увеличения объемов поступающего лекарства у пациента отсутствует. Отсутствие контроля за употреблением средства способно привести к проблемам в работе ЖКТ, усилении гипотензии ортостатического типа, ряда других побочных проявлений.
Аналоги
В продаже отсутствуют лекарства, обладающие идентичным содержанием.
Условия продажи
Отпуск из аптек возможен только по рецепту врача.
Условия хранения
Хранение Мозобаила производят в сухом месте, при комнатной температуре. Не замораживать. Срок хранения лекарства — 36 месяцев.
Цены на Мозобаил в Москве

Заберите заказ в в аптеке
WER (г. Москва)
Выгодные цены
Сертификаты и лицензии
Данные по безопасности применения препарата Мозобаил в сочетании с Г-КСФ у онкологических пациентов с лимфомой и множественной миеломой были получены в 2 плацебо-контролируемых (фаза III) и 10 неконтролируемых исследованиях (фаза II) у 543 пациентов. Пациенты получали лечение плериксафором в дозе 0.24 мг/кг/сут п/к. Длительность лечения в этих исследованиях составила от 1 до 7 дней непрерывно (медиана — 2 дня).
В двух исследованиях (фаза III) с участием пациентов с неходжкинской лимфомой и множественной миеломой (AMD3100-3101 и AMD3100-3102 соответственно) был исследован 301 пациент, получавший лечение препаратом Мозобаил и Г-КСФ, и 292 пациента, получавших плацебо и Г-КСФ. Суточная доза Г-КСФ составляла 10 мкг/кг утром в течение 4 дней подряд до первой инъекции плериксафора или плацебо, а также каждое утро до проведения афереза.
Ниже представлены нежелательные реакции, которые чаще наблюдались в группе, получавшей препарат Мозобаил и Г-КСФ, чем в группе плацебо и Г-КСФ. Частота нежелательных реакций, связанных с лечением, составила ≥1% среди пациентов, получавших препарат Мозобаил, при мобилизации гемопоэтических стволовых клеток и аферезе, а также перед химиотерапией/миелоаблятивной терапией при подготовке к трансплантации.
Нежелательные реакции указаны в соответствии с системно-органным классом и частотой возникновения. Частоту определяли на основании следующих критериев: очень часто (≥1/10), часто (≥1/100 до <1/10), нечасто (≥1/1000 до <1/100), редко (≥1/10 000 до <1/1000), очень редко (<1/10 000), частота неизвестна (нельзя оценить по имеющимся данным).
При использовании химиотерапии/абляции в рамках подготовки к трансплантации не было отмечено значимой разницы в частоте нежелательных реакций между группами лечения через 12 мес после трансплантации.
Ниже приведены нежелательные реакции, наблюдавшиеся в группе препарата Мозобаил чаще, чем в группе плацебо, связанные с применением препарата Мозобаил при проведении мобилизации и афереза в III фазе исследований.
Со стороны иммунной системы: нечасто — аллергические реакции, анафилактические реакции, включая анафилактический шок.
Со стороны психики: часто — бессонница.
Со стороны нервной системы: часто — головная боль, головокружение.
Со стороны пищеварительной системы: очень часто — диарея, тошнота; часто — метеоризм, боли в животе, рвота, вздутие живота, сухость во рту, дискомфорт в эпигастральной области, запор, диспептические явления, гипестезия слизистой оболочки полости рта.
Со стороны кожи и подкожно-жировой клетчатки: часто — гипергидроз, эритема.
Со стороны костно-мышечной системы: часто — артралгия, скелетно-мышечная боль.
Прочие: очень часто — реакции в местах инъекции; часто — усталость, недомогание.
Нежелательные реакции у пациентов с лимфомой и множественной миеломой, получавших препарат Мозобаил в контролируемых исследованиях III фазы и неконтролируемых исследованиях, включая исследование II фазы, в котором препарат Мозобаил использовали в режиме монотерапии для мобилизации гемопоэтических стволовых клеток, сходны. У пациентов с онкологическими заболеваниями частота нежелательных реакций не отличалась в зависимости от заболевания, возраста или пола.
Аллергические реакции: аллергические реакции включали в себя одно или несколько следующих нежелательных реакций: крапивница (n=2), периорбитальный отек (n=2), одышка (n=1) или гипоксия (n=1). Данные реакции были легкой или умеренной степени тяжести и возникали в течение приблизительно 30 мин после введения препарата Мозобаил.
Инфаркт миокарда: согласно клиническим исследованиям, 7 из 679 онкологических пациентов перенесли инфаркт миокарда после мобилизации стволовых клеток с помощью плериксафора и Г-КСФ. Все случаи инфаркта миокарда наблюдались как минимум через 14 дней после последнего введения препарата Мозобаил. Кроме того, две пациентки, участвовавшие в программе по применению исследуемого препарата в индивидуальном порядке, перенесли инфаркт миокарда после мобилизации стволовых клеток с помощью плериксафора и Г-КСФ. Один из случаев инфаркта миокарда произошел через 4 дня после последнего введения препарата Мозобаил. Отсутствие временной связи у 8 из 9 пациентов и профиль риска участников, перенесших инфаркт миокарда, не позволяют считать препарат Мозобаил независимым фактором риска инфаркта миокарда у пациентов, получающих Г-КСФ.
Вазовагальные реакции: вазовагальные реакции (ортостатическая гипотензия и/или синкопе) отмечались менее чем у 1% участников клинических исследований по применению препарата Мозобаил (онкологических пациентов и здоровых добровольцев), получавших плериксафор в дозе ≤0.24 мг/кг. В большинстве случаев данные явления наблюдались в течение 1 ч после введения препарата Мозобаил.
Со стороны пищеварительной системы: в клинических исследованиях по применению препарата Мозобаил у онкологических пациентов сообщения о тяжелых нарушениях со стороны ЖКТ (включая диарею, тошноту, рвоту, боли в животе) регистрировались редко.
Парестезии: парестезии часто наблюдаются у онкологических пациентов после аутотрансплантации вследствие проводимых многочисленных медицинских процедур. В плацебо-контролируемых клинических исследованиях III фазы частота парестезии составила 20.6% и 21.2% в группах плериксафора и плацебо соответственно.
Гиперлейкоцитоз: в исследованиях III фазы увеличение количества лейкоцитов за день до афереза или в любой день афереза до 100×109/л и выше наблюдалось у 7% пациентов, получавших препарат Мозобаил, и у 1% пациентов, получавших плацебо. При этом осложнения или клинические проявления лейкоцитоза отсутствовали.
Пациенты пожилого возраста: 24% участников двух плацебо-контролируемых клинических исследований по применению плериксафора были старше 65 лет. Значимых различий по частоте нежелательных реакций в подгруппе пациентов пожилого возраста (по сравнению с пациентами более молодого возраста) не наблюдалось.
Постмаркетинговые наблюдения
Ниже приведены нежелательные реакции, о которых сообщалось в постмаркетинговый период применения препарата Мозобаил в дополнение к тем, которые были зафиксированы во время клинических исследований. Частоту нежелательных реакций определить было невозможно, т.к. сообщения о них были получены из популяции с неопределенным количеством пациентов, также как и возможную взаимосвязь с применением препарата.
Со стороны иммунной системы: анафилактические реакции, включая анафилактический шок.
Нарушения психики: необычные сновидения, кошмарные сновидения.

