Неуластим (Neulastim) инструкция по применению
📜 Инструкция по применению Неуластим
💊 Состав препарата Неуластим
✅ Применение препарата Неуластим
📅 Условия хранения Неуластим
⏳ Срок годности Неуластим
⚠️ Государственная регистрация данного препарата отменена
Описание лекарственного препарата
Неуластим
(Neulastim)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для электронного издания справочника Видаль 2014
года, дата обновления: 2020.06.19
Владелец регистрационного удостоверения:
Код ATX:
L03AA13
(Пэгфилграстим)
Лекарственная форма
| Неуластим |
Р-р д/п/к введения 6 мг/0.6 мл: шприц 0.6 мл 1 шт. в компл. с иглой д/и рег. №: ЛС-002332 |
Форма выпуска, упаковка и состав
препарата Неуластим
Раствор для п/к введения прозрачный, бесцветный, свободный от механических включений.
Вспомогательные вещества: уксусная кислота — 0.35 мг, натрия гидроксид — q.s., сорбитол — 30 мг, полисорбат 20 — 0.02 мг, вода д/и — до 0.6 мл.
0.6 мл — шприцы стеклянные вместимостью 1 мл (1) со встроенной иглой д/и (1 шт.) — пачки картонные× с фиксатором.
0.6 мл — шприцы стеклянные вместимостью 1 мл (1) со встроенной иглой д/и (1 шт.) — упаковки ячейковые контурные (1) — пачки картонные×.
× на каждую пачку наклеивают прозрачные защитные этикетки для контроля первого вскрытия, имеющие продольную цветную полосу.
Фармакологическое действие
Гемопоэтический фактор роста. Пэгфилграстим — ковалентный конъюгат филграстима (рекомбинантного человеческого гранулоцитарного колониестимулирующего фактора /Г-КСФ/), с одной молекулой полиэтиленгликоля (ПЭГ) 20 кДа, с пролонгированным действием в результате снижения почечного клиренса.
Аналогично филграстиму, пэгфилграстим регулирует образование и высвобождение нейтрофилов из костного мозга, заметно увеличивает количество нейтрофилов с нормальной или повышенной функциональной активностью (хемотаксис и фагоцитоз) в периферической крови в течение 24 ч и вызывает небольшое увеличение количества моноцитов и/или лимфоцитов.
Как и другие гемопоэтические факторы роста, Г-КСФ может стимулировать эндотелиальные клетки in vitro.
Транзиторное увеличение лейкоцитов (лейкоцитоз) является ожидаемым последствием терапии пэгфилграстимом, т.к. соответствует его фармакодинамическим эффектам. Каких-либо побочных явлений, непосредственно связанных с таким лейкоцитозом, не описано.
Клиническая эффективность
Однократное введение пэгфилграстима после каждого цикла миелосупрессивной цитостатической терапии снижает продолжительность нейтропении и частоту возникновения фебрильной нейтропении аналогично ежедневному введению филграстима (в среднем, 11 ежедневных введений). Также показано, что применение пэгфилграстима после химиотерапии значительно снижает частоту в/в введения противомикробных препаратов и госпитализации в связи с фебрильной нейтропенией.
Фармакокинетика
Всасывание
После однократного п/к введения Тmax пэгфилграстима 16-120 ч.
Распределение
Концентрация пэгфилграстима в сыворотке крови поддерживается в течение периода нейтропении после миелосупрессивной химиотерапии.
Распределение пэгфилграстима ограничено плазмой.
Выведение
Выведение пэгфилграстима нелинейное, дозозависимое, насыщаемое. Клиренс, в основном, осуществляется нейтрофилами (>99%) и снижается с увеличением дозы пэгфилграстима. В соответствии с саморегулирующимся механизмом клиренса, концентрация пэгфилграстима в сыворотке быстро снижается с началом восстановления числа нейтрофилов.
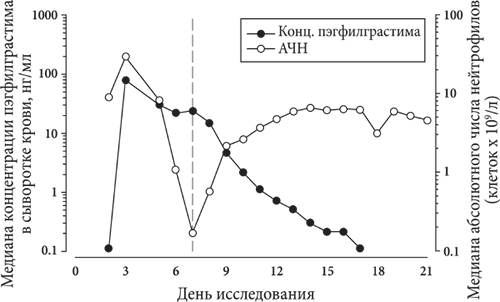
Графики изменения медианы концентрации пэгфилграстима в сыворотке крови и медианы абсолютного числа нейтрофилов (АЧН) во времени после однократной инъекции 6 мг пэгфилграстима пациентам, получающим химиотерапию.
Фармакокинетика у особых групп пациентов
Учитывая клиренс с участием нейтрофилов, вероятно, что фармакокинетика пэгфилграстима не изменяется при почечной или печеночной недостаточности.
Фармакокинетика пэгфилграстима у пациентов старше 65 лет аналогична фармакокинетике у взрослых.
Средняя системная экспозиция AUC0-∞ пэгфилграстима после п/к введения в дозе 100 мкг/кг у детей с саркомой в возрасте 6-11 лет составила 22.0 мкг×ч/мл, у детей 12-21 года — 29.3 мкг×ч/мл, у детей 0-5 лет — 47.9 мкг×ч/мл. Терминальный T1/2 у детей в соответствующих возрастных группах составил 20.2 ч, 21.2 ч и 30.1 ч, соответственно.
Показания препарата
Неуластим
- для снижения продолжительности нейтропении, частоты возникновения фебрильной нейтропении и инфекций, проявляющихся фебрильной нейтропенией, при цитотоксической химиотерапии по поводу злокачественных заболеваний.
Режим дозирования
Взрослым (≥18 лет) препарат назначают п/к в дозе 6 мг (1 шприц-тюбик) через 24 ч после проведения каждого цикла цитотоксической химиотерапии.
Не следует применять Неуластим® менее чем за 14 дней до, во время и менее чем через 24 ч после введения цитотоксических химиотерапевтических средств.
Необходимо отменить введение препарата Неуластим® при повышении общего количества лейкоцитов выше 50 × 109/л.
Рекомендаций по применению препарата Неуластим® у детей и подростков в возрасте до 18 лет нет (недостаточно данных).
Пациентам с массой тела менее 45 кг не должна назначаться фиксированная доза (6 мг) препарата Неуластим® (недостаточно данных).
Инструкции по применению, обращению и уничтожению
Шприц-тюбик с препаратом Неуластим® предназначен только для однократного использования.
Препарат Неуластим® представляет собой стерильный раствор без консервантов.
Перед введением раствор препарата Неуластим® следует осмотреть на наличие посторонних видимых частиц. Допускается введение только прозрачного и бесцветного раствора.
Чрезмерное встряхивание может разрушить пэгфилграстим, сделав его биологически неактивным.
Перед инъекцией раствор в шприц-тюбике следует согреть до комнатной температуры.
Любой неиспользованный препарат или его остатки следует уничтожить в соответствии с санитарными требованиями.
Попадание лекарственных препаратов в окружающую среду должно быть сведено к минимуму. Не следует утилизировать препарат с помощью сточных вод или вместе с бытовыми отходами. По возможности необходимо использовать специальные системы для утилизации лекарственных препаратов.
Побочное действие
Для оценки частоты побочных эффектов используются следующие категории: очень часто (≥10%); часто (≥1%, <10%); нечасто (≥0.1%, <1%); редко (≥0.01%, <0.1%); очень редко (<0.01%, включая отдельные случаи).
Данные клинических исследований
У пациентов, получающих Неуластим® после цитотоксической химиотерапии, большинство нежелательных явлений были обусловлены основным злокачественным заболеванием или цитотоксической химиотерапией.
Очень часто при применении препарата сообщалось о слабых или умеренных болях в костях, которые в большинстве случаев проходили самостоятельно или купировались ненаркотическими анальгезирующими средствами.
Со стороны скелетно-мышечной системы и соединительной ткани: очень часто — боль в костях; часто — артралгия, миалгия, мышечно-скелетная боль, боли в спине, конечностях и шее.
Общие расстройства и нарушения в месте введения: часто — боль и эритема в месте инъекции, боль в груди (некардиальная), боль.
Со стороны нервной системы: часто — головная боль.
Со стороны крови и лимфатической системы: нечасто — лейкоцитоз.
Со стороны ЖКТ: тошнота (частота неизвестна).
Со стороны лабораторных показателей: очень часто — обратимое, слабое или умеренное клинически незначимое повышение активности ЩФ и ЛДГ; часто — обратимое, слабое или умеренное клинически незначимое повышение мочевой кислоты.
Пострегистрационное применение препарата
Со стороны иммунной системы: редко — анафилаксия, сыпь, крапивница, ангионевротический отек, одышка и артериальная гипотензия, эритема и гиперемия в начале терапии или при последующем введении препарата. Иногда возобновление лечения сопровождается рецидивом симптомов. В случае развития серьезных аллергических реакций следует назначить соответствующее лечение с тщательным наблюдением за пациентом в течение нескольких дней. Необходимо прекратить терапию пэгфилграстимом при развитии серьезных аллергических реакций.
Со стороны ЖКТ: боли в верхней левой части живота (частота неизвестна).
Со стороны крови и лимфатической системы: очень редко — разрыв селезенки (в некоторых случаях с фатальным исходом), спленомегалия (частота неизвестна), вазоокклюзионный криз (частота неизвестна).
Со стороны дыхательной системы, органов грудной клетки и средостения: кашель (частота неизвестна), одышка (частота неизвестна), инфильтраты в легких (частота неизвестна), нарушение функции дыхания (частота неизвестна), респираторный дистресс-синдром (частота неизвестна).
Общие расстройства и нарушения в месте введения: лихорадка (частота неизвестна).
Со стороны кожи и подкожно-жировой клетчатки: редко — синдром Свита (острый фебрильный дерматоз); кожный васкулит (расчетная частота сообщений 0.00038%).
Противопоказания к применению
- нейтропения при хроническом миелолейкозе и миелодиспластических синдромах;
- острый лейкоз;
- для увеличения доз цитотоксической химиотерапии выше установленных в режимах дозирования;
- одновременное назначение с цитотоксической химио- и лучевой терапией;
- беременность;
- период кормления грудью;
- возраст до 18 лет;
- гиперчувствительность к белкам, полученным с использованием E. coli, филграстиму, пэгфилграстиму или любому другому компоненту препарата.
С осторожностью следует назначать препарат при злокачественных и предопухолевых заболеваниях миелоидного характера (в т.ч. острый миелолейкоз de novo и вторичный); в комбинации с высокодозной химиотерапией; при серповидно-клеточной анемии, при наследственной непереносимости фруктозы (в составе содержится сорбитол).
Применение при беременности и кормлении грудью
Исследования у беременных женщин не проводились.
При п/к введении пэгфилграстима беременным крысам отрицательного влияния на потомство не выявлено. При п/к введении низких доз пэгфилграстима кроликам наблюдались признаки эмбрио-фетотоксического действия (гибель эмбриона). Пэгфилграстим проникает через плаценту крыс. Потенциальный риск, связанный с влиянием на эмбрион или плод человека, неизвестен.
Исследования у кормящих женщин не проводились, поэтому Неуластим® не следует применять в период грудного вскармливания.
Применение у детей
Противопоказано: возраст до 18 лет.
Особые указания
Лечение препаратом Неуластим® должно проводиться только под контролем онколога или гематолога, имеющих опыт применения Г-КСФ.
Ограниченные данные свидетельствуют о том, что эффективность пэгфилграстима и филграстима одинакова в отношении времени купирования тяжелой нейтропении у пациентов с острым миелолейкозом de novo. Однако следует проявлять осторожность при терапии препаратом Неуластим® у пациентов с острым миелолейкозом de novo, поскольку не установлены отдаленные результаты такой терапии.
Г-КСФ стимулирует эндотелиальные клетки и может ускорять рост миелоидных клеток, включая злокачественные клетки, и некоторые немиелоидные клетки in vitro. Неуластим® не следует использовать при миелодиспластических синдромах, хроническом миелолейкозе, вторичном остром миелолейкозе, поскольку безопасность и эффективность препарата у данных групп пациентов не оценивались. Следует особенно тщательно проводить дифференциальную диагностику между бласттрансформацией при хроническом миелолейкозе и острым миелолейкозом.
Безопасность и эффективность препарата Неуластим® у больных с острым миелолейкозом de novo моложе 55 лет с транслокацией t (15;17) не изучались.
Безопасность и эффективность препарата Неуластим® у больных, получавших высокодозную химиотерапию, не изучались.
Кашель, лихорадка и одышка в сочетании с рентгенологическими инфильтративными изменениями, ухудшением функции легких и увеличением количества нейтрофилов могут служить признаками респираторного дистресс-синдрома у взрослых. В таком случае по усмотрению врача Неуластим® следует отменить и назначить соответствующее лечение.
Зарегистрированы очень редкие случаи разрыва селезенки после применения пэгфилграстима, некоторые — с фатальным исходом. Следует тщательно наблюдать за размерами селезенки с помощью инструментального обследования (ультразвуковое исследование). Следует предусмотреть возможность спленомегалии или разрыва селезенки у больных с жалобами на боль в верхней левой части живота и/или в верхней части левого плеча.
Монотерапия препаратом Неуластим® не исключает развития тромбоцитопении и анемии при продолжении миелосупрессивной химиотерапии в полной дозе. Рекомендуется регулярно определять число тромбоцитов и гематокрит.
Неуластим® не следует использовать для увеличения доз цитотоксической химиотерапии выше установленных в режимах дозирования.
Развитие серповидно-клеточного криза ассоциировалось с терапией пэгфилграстимом у пациентов с серповидно-клеточной анемией. Терапия пэгфилграстимом у пациентов с серповидно-клеточной анемией должна проводиться с осторожностью только после тщательного определения потенциального риска и пользы.
Лейкоцитоз 100 × 109/л или более наблюдается менее чем у 1% больных, получающих Неуластим®, носит временный характер и обычно наблюдается через 24-48 ч после введения препарата в соответствии с его фармакодинамическими эффектами. Каких-либо побочных явлений, непосредственно связанных с таким лейкоцитозом, не описано.
Безопасность и эффективность пэгфилграстима при мобилизации периферических стволовых клеток крови у больных соответствующим образом не оценивались.
Возросшая гемопоэтическая активность костного мозга в ответ на терапию факторами роста приводит к транзиторным положительным изменениям при визуализации костей, что следует принимать во внимание при интерпретации результатов.
В клиническом исследовании у детей среди нежелательных явлений наиболее часто, как и у взрослых, отмечалась боль в костях.
Влияние на способность к управлению транспортными средствами и механизмами
Исследования по влиянию препарата Неуластим® на способность к вождению транспортных средств и занятий потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций, не проводились.
Передозировка
При однократном п/к введении препарата в дозе 300 мкг/кг серьезных нежелательных явлений не возникло ни у здоровых добровольцев, ни у пациентов с немелкоклеточным раком легкого. Побочные явления при передозировке не отличались от побочных явлений при обычном применении препарата в рекомендованных дозах.
Лекарственное взаимодействие
Цитотоксическая химиотерапия: из-за возможной чувствительности быстро делящихся миелоидных клеток к цитотоксической терапии Неуластим® следует вводить через 24 ч после введения цитотоксических химиотерапевтических средств. В клинических исследованиях препарат безопасно применялся за 14 дней до введения цитотоксических химиотерапевтических средств.
Фторурацил или другие антиметаболиты: усиление угнетения кроветворения in vivo (у животных). Взаимодействие с другими гемопоэтическими факторами роста и цитокинами неизвестно.
Возможность взаимодействия с литием, который также способствует высвобождению нейтрофилов, специально не исследовали. Нет подтверждения, что данное взаимодействие может быть опасным.
Исследования, посвященные специфическим взаимодействиям или метаболизму, не проводили.
Безопасность и эффективность препарата Неуластим® у пациентов, получающих химиотерапию, приводящую к отсроченной миелосупрессии (например, препараты из группы производных нитрозомочевины), не изучалась.
Признаков взаимодействия препарата Неуластим® с другими лекарственными препаратами на настоящее время не зафиксировано.
Несовместимость
Неуластим® несовместим с растворами натрия хлорида.
Условия хранения препарата Неуластим
Препарат следует хранить в недоступном для детей, защищенном от света месте при температуре от 2° до 8°С; не замораживать.
Срок годности препарата Неуластим
Срок годности — 3 года. Препарат не следует использовать по истечении срока годности, указанного на упаковке.
Условия реализации
Препарат отпускается по рецепту.
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Инструкция по применению Неуластим
- Состав
- Показания к применению
- Противопоказания к применению
- Рекомендации по применению
- Применение при беременности и кормлении грудью
- Фармакологическое действие
- Побочные действия
- Особые указания
- Передозировка
- Лекарственное взаимодействие
- Условия хранения
- Условия отпуска
Состав
Активные вещества: пэгфилграстим 6 мг.
Вспомогательные вещества: натрия ацетат — q.s. до pH 4,0, сорбитол — 30 мг, полисорбат 20 — 0,02 мг, вода д/и — до 0,6 мл.
Показания к применению Неуластим
Для снижения продолжительности нейтропении, частоты возникновения фебрильной нейтропении и инфекций, проявляющихся фебрильной нейтропенией, при цитотоксической химиотерапии по поводу злокачественных заболеваний.
Противопоказания к применению Неуластим
- Нейтропения при хроническом миелолейкозе и миелодиспластических синдромах;
- острый лейкоз;
- для увеличения доз цитотоксической химиотерапии выше установленных в режимах дозирования;
- одновременное назначение с цитотоксической химио- и лучевой терапией;
- беременность;
- период кормления грудью;
- возраст до 18 лет;
- гиперчувствительность к белкам, полученным с использованием E. coli, филграстиму, пэгфилграстиму или любому другому компоненту препарата.
С осторожностью: следует назначать препарат при злокачественных и предопухолевых заболеваниях миелоидного характера (в т.ч. острый миелолейкоз de novo и вторичный); в комбинации с высокодозной химиотерапией; при серповидноклеточной анемии, при наследственной непереносимости фруктозы (в составе содержится сорбитол).
Рекомендации по применению
Взрослым (≥18 лет) препарат назначают п/к в дозе 6 мг (1 шприц-тюбик) через 24 ч после проведения каждого цикла цитотоксической химиотерапии.
Не следует применять Неуластим® менее чем за 14 дней до, во время и менее чем через 24 ч после введения цитотоксических химиотерапевтических средств.
Необходимо отменить введение препарата Неуластим® при повышении общего количества лейкоцитов выше 50 × 109/л.
Рекомендаций по применению препарата Неуластим® у детей и подростков в возрасте до 18 лет нет (недостаточно данных).
Пациентам с массой тела менее 45 кг не должна назначаться фиксированная доза (6 мг) препарата Неуластим® (недостаточно данных).
Инструкции по применению, обращению и уничтожению
Шприц-тюбик с препаратом Неуластим® предназначен только для однократного использования.
Препарат Неуластим® представляет собой стерильный раствор без консервантов.
Перед введением раствор препарата Неуластим® следует осмотреть на наличие посторонних видимых частиц. Допускается введение только прозрачного и бесцветного раствора.
Чрезмерное встряхивание может разрушить пэгфилграстим, сделав его биологически неактивным.
Перед инъекцией раствор в шприц-тюбике следует согреть до комнатной температуры.
Любой неиспользованный препарат или его остатки следует уничтожить в соответствии с санитарными требованиями.
Попадание лекарственных препаратов в окружающую среду должно быть сведено к минимуму. Не следует утилизировать препарат с помощью сточных вод или вместе с бытовыми отходами. По возможности необходимо использовать специальные системы для утилизации лекарственных препаратов.
Применение Неуластим при беременности и кормлении грудью
Исследования у беременных женщин не проводились.
При п/к введении пэгфилграстима беременным крысам отрицательного влияния на потомство не выявлено. При п/к введении низких доз пэгфилграстима кроликам наблюдались признаки эмбрио-фетотоксического действия (гибель эмбриона). Пэгфилграстим проникает через плаценту крыс. Потенциальный риск, связанный с влиянием на эмбрион или плод человека, неизвестен.
Исследования у кормящих женщин не проводились, поэтому Неуластим® не следует применять в период грудного вскармливания.
Фармакологическое действие
Фармакодинамика
Гемопоэтический фактор роста. Пэгфилграстим — ковалентный конъюгат филграстима (рекомбинантного человеческого гранулоцитарного колониестимулирующего фактора /Г-КСФ/), с одной молекулой полиэтиленгликоля (ПЭГ) 20 кДа, с пролонгированным действием в результате снижения почечного клиренса.
Аналогично филграстиму, пэгфилграстим регулирует образование и высвобождение нейтрофилов из костного мозга, заметно увеличивает количество нейтрофилов с нормальной или повышенной функциональной активностью (хемотаксис и фагоцитоз) в периферической крови в течение 24 ч и вызывает небольшое увеличение количества моноцитов и/или лимфоцитов.
Как и другие гемопоэтические факторы роста, Г-КСФ может стимулировать эндотелиальные клетки in vitro.
Транзиторное увеличение лейкоцитов (лейкоцитоз) является ожидаемым последствием терапии пэгфилграстимом, т.к. соответствует его фармакодинамическим эффектам. Каких-либо побочных явлений, непосредственно связанных с таким лейкоцитозом, не описано.
Клиническая эффективность
Однократное введение пэгфилграстима после каждого цикла миелосупрессивной цитостатической терапии снижает продолжительность нейтропении и частоту возникновения фебрильной нейтропении аналогично ежедневному введению филграстима (в среднем, 11 ежедневных введений). Также показано, что применение пэгфилграстима после химиотерапии значительно снижает частоту в/в введения противомикробных препаратов и госпитализации в связи с фебрильной нейтропенией.
Фармакокинетика
Всасывание
После однократного п/к введения Тmax пэгфилграстима 16-120 ч.
Распределение
Концентрация пэгфилграстима в сыворотке крови поддерживается в течение периода нейтропении после миелосупрессивной химиотерапии.
Распределение пэгфилграстима ограничено плазмой.
Выведение
Выведение пэгфилграстима нелинейное, дозозависимое, насыщаемое. Клиренс, в основном, осуществляется нейтрофилами ( > 99%) и снижается с увеличением дозы пэгфилграстима. В соответствии с саморегулирующимся механизмом клиренса, концентрация пэгфилграстима в сыворотке быстро снижается с началом восстановления числа нейтрофилов.
Графики изменения медианы концентрации пэгфилграстима в сыворотке крови и медианы абсолютного числа нейтрофилов (АЧН) во времени после однократной инъекции 6 мг пэгфилграстима пациентам, получающим химиотерапию.
ГРАФИК
Фармакокинетика у особых групп пациентов
Учитывая клиренс с участием нейтрофилов, вероятно, что фармакокинетика пэгфилграстима не изменяется при почечной или печеночной недостаточности.
Фармакокинетика пэгфилграстима у пациентов старше 65 лет аналогична фармакокинетике у взрослых.
Средняя системная экспозиция AUC0-∞ пэгфилграстима после п/к введения в дозе 100 мкг/кг у детей с саркомой в возрасте 6-11 лет составила 22,0 мкг×ч/мл, у детей 12-21 года — 29,3 мкг×ч/мл, у детей 0-5 лет — 47,9 мкг×ч/мл. Терминальный T1/2 у детей в соответствующих возрастных группах составил 20,2 ч, 21,2 ч и 30,1 ч, соответственно.
Побочные действия Неуластим
Для оценки частоты побочных эффектов используются следующие категории:
- очень часто (≥10%);
- часто (≥1%, < 10%);
- нечасто (≥0,1%, < 1%);
- редко (≥0,01%, < 0,1%);
- очень редко ( < 0,01%, включая отдельные случаи).
Данные клинических исследований
У пациентов, получающих Неуластим® после цитотоксической химиотерапии, большинство нежелательных явлений были обусловлены основным злокачественным заболеванием или цитотоксической химиотерапией.
Очень часто при применении препарата сообщалось о слабых или умеренных болях в костях, которые в большинстве случаев проходили самостоятельно или купировались ненаркотическими анальгезирующими средствами.
Со стороны скелетно-мышечной системы и соединительной ткани: очень часто — боль в костях; часто — артралгия, миалгия, мышечно-скелетная боль, боли в спине, конечностях и шее.
Общие расстройства и нарушения в месте введения: часто — боль и эритема в месте инъекции, боль в груди (некардиальная), боль.
Со стороны нервной системы: часто — головная боль.
Со стороны крови и лимфатической системы: нечасто — лейкоцитоз.
Со стороны ЖКТ: тошнота (частота неизвестна).
Со стороны лабораторных показателей: очень часто — обратимое, слабое или умеренное клинически незначимое повышение активности ЩФ и ЛДГ; часто — обратимое, слабое или умеренное клинически незначимое повышение мочевой кислоты.
Пострегистрационное применение препарата
Со стороны иммунной системы: редко — анафилаксия, сыпь, крапивница, ангионевротический отек, одышка и артериальная гипотензия, эритема и гиперемия в начале терапии или при последующем введении препарата. Иногда возобновление лечения сопровождается рецидивом симптомов. В случае развития серьезных аллергических реакций следует назначить соответствующее лечение с тщательным наблюдением за пациентом в течение нескольких дней. Необходимо прекратить терапию пэгфилграстимом при развитии серьезных аллергических реакций.
Со стороны ЖКТ: боли в верхней левой части живота (частота неизвестна).
Со стороны крови и лимфатической системы: очень редко — разрыв селезенки (в некоторых случаях с фатальным исходом), спленомегалия (частота неизвестна), вазоокклюзионный криз (частота неизвестна).
Со стороны дыхательной системы, органов грудной клетки и средостения: кашель (частота неизвестна), одышка (частота неизвестна), инфильтраты в легких (частота неизвестна), нарушение функции дыхания (частота неизвестна), респираторный дистресс-синдром (частота неизвестна).
Общие расстройства и нарушения в месте введения: лихорадка (частота неизвестна).
Со стороны кожи и подкожно-жировой клетчатки: редко — синдром Свита (острый фебрильный дерматоз); кожный васкулит (расчетная частота сообщений 0,00038%).
Особые указания
Лечение препаратом Неуластим® должно проводиться только под контролем онколога или гематолога, имеющих опыт применения Г-КСФ.
Ограниченные данные свидетельствуют о том, что эффективность пэгфилграстима и филграстима одинакова в отношении времени купирования тяжелой нейтропении у пациентов с острым миелолейкозом de novo. Однако следует проявлять осторожность при терапии препаратом Неуластим® у пациентов с острым миелолейкозом de novo, поскольку не установлены отдаленные результаты такой терапии.
Г-КСФ стимулирует эндотелиальные клетки и может ускорять рост миелоидных клеток, включая злокачественные клетки, и некоторые немиелоидные клетки in vitro. Неуластим® не следует использовать при миелодиспластических синдромах, хроническом миелолейкозе, вторичном остром миелолейкозе, поскольку безопасность и эффективность препарата у данных групп пациентов не оценивались. Следует особенно тщательно проводить дифференциальную диагностику между бласт-трансформацией при хроническом миелолейкозе и острым миелолейкозом.
Безопасность и эффективность препарата Неуластим® у больных с острым миелолейкозом de novo моложе 55 лет с транслокацией t (15;17) не изучались.
Безопасность и эффективность препарата Неуластим® у больных, получавших высокодозную химиотерапию, не изучались.
Кашель, лихорадка и одышка в сочетании с рентгенологическими инфильтративными изменениями, ухудшением функции легких и увеличением количества нейтрофилов могут служить признаками респираторного дистресс-синдрома у взрослых. В таком случае по усмотрению врача Неуластим® следует отменить и назначить соответствующее лечение.
Зарегистрированы очень редкие случаи разрыва селезенки после применения пэгфилграстима, некоторые — с фатальным исходом. Следует тщательно наблюдать за размерами селезенки с помощью инструментального обследования (ультразвуковое исследование). Следует предусмотреть возможность спленомегалии или разрыва селезенки у больных с жалобами на боль в верхней левой части живота и/или в верхней части левого плеча.
Монотерапия препаратом Неуластим® не исключает развития тромбоцитопении и анемии при продолжении миелосупрессивной химиотерапии в полной дозе. Рекомендуется регулярно определять число тромбоцитов и гематокрит.
Неуластим® не следует использовать для увеличения доз цитотоксической химиотерапии выше установленных в режимах дозирования.
Развитие серповидно-клеточного криза ассоциировалось с терапией пэгфилграстимом у пациентов с серповидно-клеточной анемией. Терапия пэгфилграстимом у пациентов с серповидно-клеточной анемией должна проводиться с осторожностью только после тщательного определения потенциального риска и пользы.
Лейкоцитоз 100 × 109/л или более наблюдается менее чем у 1% больных, получающих Неуластим®, носит временный характер и обычно наблюдается через 24-48 ч после введения препарата в соответствии с его фармакодинамическими эффектами. Каких-либо побочных явлений, непосредственно связанных с таким лейкоцитозом, не описано.
Безопасность и эффективность пэгфилграстима при мобилизации периферических стволовых клеток крови у больных соответствующим образом не оценивались.
Возросшая гемопоэтическая активность костного мозга в ответ на терапию факторами роста приводит к транзиторным положительным изменениям при визуализации костей, что следует принимать во внимание при интерпретации результатов.
В клиническом исследовании у детей среди нежелательных явлений наиболее часто, как и у взрослых, отмечалась боль в костях.
Влияние на способность управлять транспортными средствами и другими механизмами, требующими повышенной концентрации внимания
Исследования по влиянию препарата Неуластим® на способность к вождению транспортных средств и занятий потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций, не проводились.
Передозировка
При однократном п/к введении препарата в дозе 300 мкг/кг серьезных нежелательных явлений не возникло ни у здоровых добровольцев, ни у пациентов с немелкоклеточным раком легкого. Побочные явления при передозировке не отличались от побочных явлений при обычном применении препарата в рекомендованных дозах.
Лекарственное взаимодействие
Цитотоксическая химиотерапия: из-за возможной чувствительности быстро делящихся миелоидных клеток к цитотоксической терапии Неуластим® следует вводить через 24 ч после введения цитотоксических химиотерапевтических средств. В клинических исследованиях препарат безопасно применялся за 14 дней до введения цитотоксических химиотерапевтических средств.
Фторурацил или другие антиметаболиты: усиление угнетения кроветворения in vivo (у животных). Взаимодействие с другими гемопоэтическими факторами роста и цитокинами неизвестно.
Возможность взаимодействия с литием, который также способствует высвобождению нейтрофилов, специально не исследовали. Нет подтверждения, что данное взаимодействие может быть опасным.
Исследования, посвященные специфическим взаимодействиям или метаболизму, не проводили.
Безопасность и эффективность препарата Неуластим® у пациентов, получающих химиотерапию, приводящую к отсроченной миелосупрессии (например, препараты из группы производных нитрозомочевины), не изучалась.
Признаков взаимодействия препарата Неуластим® с другими лекарственными препаратами на настоящее время не зафиксировано.
Несовместимость
Неуластим® несовместим с растворами натрия хлорида.
Условия хранения
В защищенном от света месте, при температуре 2–8 °C. Срок годности — 3 года.
Условия отпуска
Без рецепта

Товары из категории — Лекарства от болезней крови
Инструкция по применению
Цена в интернет-аптеке WER.RU: от 46 000
Фармакологические свойства
Неуластим – медикаментозное средство, которое содержит гормоноподобные вещества, стимулирующие костный мозг к производству клеток крови. Основной действующий компонент препарата – пэгфилграстим, действие которого направлено на контроль за производством и освобождением активных клеток белой крови, а также на увеличение числа крупных лейкоцитов и лимфоцитов.
Медикаментозное средство Неуластим используется для эффективной борьбы с агранулоцитозом и нейтропенической лихорадкой. Кроме этого, медикамент используется для снижения риска возникновения воспалительных процессов под воздействием микробов после химиотерапии.
назначать препарат может только лечащий врач после установления клинической картины заболевания, сбора всех анализов, проверку на аллергические реакции и проведения всех необходимых для терапии обследований.
Состав и форма выпуска
Медикаментозное средство Неуластим выпускается в виде раствора, предназначенного для инъекций под кожу. Упакован раствор в тюбик-шприц объемом в 0,6 мл. В комплекте с препаратом идет инструкция, раствор и игла для инъекции.
В состав препарата входят следующие компоненты:
Показания к применению
Медикаментозное средство Неуластим предназначено для терапии агранулоцитоза, нейтропенической лихорадки, инфекционных воспалений, вызывающих угрожающее жизни снижение количества нейтрофильных гранулоцитов в крови, в качестве профилактического средства при химиотерапевтическом лечении онкологических заболеваний.
Международная классификация болезней (МКБ-10)

Побочные эффекты
Использование медикамента Неуластим может стать причиной проявления у части пациентов побочных признаков со стороны разных систем жизнедеятельности организма человека:
Противопоказания
Нельзя использовать медикаментозное средство Неуластим при наличии следующих заболеваний и факторов:
Следует использовать медикамент с большой осторожностью и под наблюдением лечащего врача пожилым людям, пациентам с заболеваниями печени и почек, при остром нелимфобластном лейкозе, наследственной гемоглобинопатии, фруктоземии.
Применение при беременности
Нет достаточных исследований и сведений о воздействии медикамента Неуластим на развивающийся внутри утробы плод. Во избежание нарушений развития плода не рекомендуется принимать медикамент в период вынашивания ребенка, а также отказаться от грудного вскармливания на время терапии.
Способ и особенности применения
Рекомендуемая дозировка препарата для взрослого человека составляет 6 мг. (один шприц-тюбик) по истечении суток после химиотерапии злокачественных новообразований. Не рекомендуется использовать медикамент за две недели до начала химиотерапии, непосредственно во время проведения и раньше чем через сутки после нее.
При увеличении количества лейкоцитов в крови необходимо прекратить использование медикамента.
Нет сведений о воздействии компонентов препарата на растущий и развивающийся детский организм, поэтому не рекомендуется назначать медикамент детям и подросткам или делать это с большой осторожностью с учетом всех рисков.
Если масса тела пациента составляет менее 45 кг., то необходима корректировка дозы в сторону уменьшения.
Инструкция по применению содержит все правила и нормы хранения и использования препарата.
Один флакон с раствором предназначен для единоразового использования, после инъекции остатки медикамента и тюбик необходимо утилизировать. Сам раствор является стерильным, не содержит консервантов.
Перед использованием медикамента необходимо проверить упаковку на целостность, при нарушении целостности использовать медикамент нельзя. Раствор должен быть прозрачным, при появлении любых цветовых нарушений раствора или непонятного осадка и примесей, его необходимо утилизировать, так как он не пригоден для использования.
Не рекомендуется встряхивать медикамент перед использованием, так как это может оказать влияние на фармакологические свойства компонентов и эффективность препарата.
Перед использованием необходимо нагреть раствор до комнатной температуры.
Использовать медикамент можно только по назначению и под контролем лечащего врача.
При использовании медикамента необходимо следить за селезенкой, так как действие медикамента может привести к нарушению целостности селезенки или увеличению ее размеров, что может стать причиной смертельного исхода.
Кроме этого, во время прохождения курса терапии медикаментом необходимо следить за показателями количества тромбоцитов и эритроцитов в крови.
Как у детей, так и у взрослых использование медикамента почти всегда сопровождается ломотой и болезненными проявлениями в костной ткани, суставах и мышцах.
Использование медикамента Неуластим не оказывает воздействия на управление транспортными средствами, а также психомоторные реакции человека.
Взаимодействие с другими лекарствами
При использовании и употреблении каких-либо лекарственных средств во время назначения терапии медикаментом Неуластим необходимо сообщить об этом лечащему врачу, который примет решение о показаниях к применению, корректировке дозы, отмене какого-либо из препаратов во избежание проявления рисков для здоровья и угрозы жизни пациента.
Передозировка
Нет особых признаков передозировки медикаментозным средством. При передозировке у ряда пациентов могут проявиться побочные признаки и неприятные симптомы, которые пройдут после распада компонентов препарата в организме.
Аналоги
Аналогом медикаментозного средства по фармакологическим свойствам и составу является препарат Пэгфилграстим. Других схожих аналогов у медикаментозного средства нет.
Условия продажи
Медикаментозное средство продается в аптечных пунктах только по назначению лечащего врача и при наличии рецептурного листа.
Условия хранения
Хранить медикаментозное средство следует в изолированном от досягаемости детьми и проникновения любых источников света месте при температуре от 2 до 8°С. Нельзя хранить медикамент в холодильнике во избежание его заморозки. Срок хранения медикамента составляет три года с момент изготовления. По истечении срока годности и хранения медикамент использовать нельзя и его необходимо утилизировать в соответствии с санитарными нормами.
Цены на Неуластим в Москве

Заберите заказ в в аптеке
WER (г. Москва)
Цена: от 46 000 руб.
Сертификаты и лицензии
Иммуностимуляторы, колониестимулирующий фактор. Код ATX: L03AA13.
Фармакологические свойства
Фармакодинамика
Человеческий гранулоцитарный колониестимулирующий фактор (G-CSF) представляет собой гликопротеин, который регулирует выработку и высвобождение нейтрофилов из костного мозга. Пэгфилграстим представляет собой ковалентный конъюгат рекомбинантного человеческого гранулоцитарного колониестимулирующего фактора G-CSF (r-metHuG-CSF) с одной молекулой полиэтиленгликоля 20 кДа (ПЭГ). Пэгфилграстим является пролонгированной формой филграстима вследствие снижения почечного клиренса. Пэгфилграстим и филграстим, как было показано, имеют одинаковый механизм действия, вызывая значительное увеличение количества нейтрофилов в периферической крови в течение 24 часов и незначительное увеличение моноцитов и/или лимфоцитов. Аналогично филграстиму, нейтрофилы, образовавшихся в ответ на воздействие пэгфилграстима, демонстрируют нормальную или повышенную функциональную активность, что подтверждается с помощью теста хемотаксиса ми фагоцитарной функции. Как и другие гемопоэтические факторы роста, G-CSF может стимулировать эндотелиальные клетки человека in vitro. G-CSF может способствовать росту миелоидных клеток, в том числе злокачественных клеток in vitro аналогичные эффекты могут наблюдаться in vitro для некоторых немиелономных клеток.
В двух рандомизированных двойных слепых исследованиях у пациентов с раком молочной железы II-IV стадии с высоким риском, получавших миелосупрессивную химиотерапию, состоящую из доксорубицина и доцетаксела, применение пэгфилграстима в виде однократной дозы на цикл снижало продолжительность нейтропении и частоту фебрильной нейтропении, аналогично тому, что наблюдалось при ежедневных инъекциях филграстима (медиана 11 ежедневных инъекций). При отсутствии применения гранулоцитарного колониестимулирующего фактора, в случае применения данного режима средняя продолжительность нейтропении 4-й степени составила от 5 до 7 дней, случаи фебрильной нейтропении наблюдались с частотой 30-40%. В одном исследовании (n = 157), в котором применялась фиксированная доза 6 мг пэгфилграстима, средняя продолжительность нейтропении 4-й степени для группы пэгфилграстима составляла 1,8 дня по сравнению с 1,6 днями в группе филграстима (разница 0,23 дня, 95% ДИ -0,15, 0,63). В течение всего исследования частота фебрильной нейтропении составляла 13% у пациентов, получавших пэгфилграстим, по сравнению с 20% у пациентов, получавших филграстим (разница 7%, 95% ДИ -19%, 5%). Во втором исследовании (n = 310), в котором использовалась доза, рассчитанная на вес (100 мкг/кг), средняя продолжительность нейтропении 4-й степени для группы пэгфилграстима составляла 1,7 дня, по сравнению с 1,8 дня в группе филграстима (разница 0,03 дня, 95% ДИ -0,36, 0,30). Общий уровень фебрильной нейтропении составил 9% у пациентов, получавших пэгфилграстим и 18% у пациентов, получавших филграстим (разница 9%, 95% ДИ -16,8%, -1,1%).
В плацебо-контролируемом двойном слепом исследовании у пациентов с раком молочной железы влияние пэгфилграстима на частоту возникновения фебрильной нейтропении оценивали после применения режима химиотерапии, при котором риск развития фебрильной нейтропении составил 10-20% (доцетаксел 100мг/м2 каждые 3 недели в течение 4 циклов). Девятьсот двадцать восемь пациентов были рандомизированы для применения либо разовой дозы пэгфилграстима, либо плацебо через 24 часа (второй день) после химиотерапии в каждом цикле. Частота фебрильной нейтропении была ниже для пациентов, получающих пэгфилграстим, по сравнению с плацебо (1% по сравнению с 17%, р < 0,001). Частота госпитализаций и внутривенного применения антибактериальной терапии, связанная с клиническим диагнозом фебрильная нейтропения, была ниже в группе пэгфилграстима по сравнению с плацебо (1% по сравнению с 14%, р < 0,001 и 2% по сравнению с 10%, р < 0,001).
В небольшом (n = 83) рандомизированном двойном слепом исследовании II фазы пациентов, получавших химиотерапию для лечения впервые возникшего острого миелоидного лейкоза, сравнивали пэгфилграстим (разовая доза 6 мг) с филграстимом, вводимыми во время индукционной химиотерапии. Среднее время восстановления после тяжелой нейтропении оценивалось как 22 дня в обеих группах лечения. Долгосрочный результат не изучался (см. раздел «Меры предосторожности»).
Во II фазе (n = 37) многоцентрового рандомизированного открытого исследования детей с саркомой, получавших 100 мкг/кг пэгфилграстима после 1 -го цикла терапии с применением винкристина, доксорубицина и циклофосфамида (VAdriaC/IE), наблюдалась более длительная продолжительность тяжелой нейтропении (нейтрофилы < 0,5 × 109) у детей младшего возраста в возрасте 0-5 лет (8,9 дня) по сравнению с детьми в возрасте 6-11 лет, 12-21 год (6 дней и 3,7 дня соответственно) и взрослыми. Кроме того, высокая частота фебрильной нейтропении наблюдалась у детей младшего возраста 0-5 лет (75%) по сравнению с детьми в возрасте 6-11 лет, 12-21 год (70% и 33% соответственно) и взрослыми (см. разделы «Побочное действие» и «Фармакокинетика»).
Фармакокинетика
После однократного подкожного введения дозы пэгфилграстима, пик концентрации пэгфилграстима в сыворотке крови наблюдается в период от 16 до 120 часов после введения, концентрация пэгфилграстима в сыворотке крови поддерживается в течение периода нейтропении после миелосупрессивной химиотерапии. Элиминация пэгфилграстима не является линейной относительно дозы; сывороточный клиренс пэгфилграстима уменьшается с увеличением дозы. Клиренс в основном осуществляется нейтрофилами и снижается с увеличением дозы пэгфилграстима. В соответствие с саморегулирующимся механизмом клиренса концентрация пэгфилграстима в сыворотке крови быстро снижается с началом восстановления нейтрофилов (смотри рисунок 1).
Рисунок 1. График изменения медианы концентрации пэгфилграстима в сыворотке крови и медианы абсолютного числа нейтрофилов (АЧН) у пациентов, получающих химиотерапию, после однократного введения 6 мг пэгфилграстима
Учитывая нейтрофил-опосредованный механизм клиренса, вероятно, что фармакокинетика пэгфилграстима не изменяется при почечной или печеночной недостаточности. В открытом исследовании однократной дозы (n = 31) различные стадии нарушения функции почек, в том числе терминальная стадия почечной недостаточности, не оказывали влияния на фармакокинетику пэгфилграстима.
Пожилые пациенты
Имеющиеся ограниченные данные показывают, что фармакокинетика пэгфилграстима у пожилых пациентов (> 65 лет) аналогична фармакокинетике у взрослых.
Детская популяция
Фармакокинетику пэгфилграстима изучали у 37 детей с саркомой, которые получили 100 мкг/кг пэгфилграстима после завершения химиотерапии VAdriaC/lE. Самая младшая возрастная группа (0-5 лет) имела более высокий средний уровень экспозиции пэгфилграстима (AUC) (± стандартное отклонение) (47,9 ± 22,5 мкгч/мл), чем дети в возрасте 6-11 лет и 12-21 года (22,0 ± 13,1 мкгч/мл и 29,3 ± 23,2 мкгч/мл, соответственно) (см. раздел «Фармакодинамика»). За исключением самой младшей возрастной группы (0-5 лет), среднее AUC у детей было схоже с таковым у взрослых пациентов с раком молочной железы II-IV стадии с высоким риском при применении 100 мкг/кг пэгфилграстима после завершения применения доксорубицина/доцетаксела (см. разделы «Побочное действие» и «Фармакодинамика»).
Доклинические данные по безопасности
Доклинические данные, полученные из традиционных исследований токсичности многократной дозы, выявили ожидаемые фармакологические эффекты, включая увеличение количества лейкоцитов, миелоидную гиперплазию в костном мозге, экстрамедуллярный гематопоэз и увеличение селезенки.
Не было отмечено каких-либо побочных эффектов у потомства беременных крыс, получавших пэгфилграстим подкожно, в то время как у кроликов пэгфилграстим оказал токсическое действие на эмбрион/плод (потеря эмбрионов) при кумулятивных дозах, которые примерно в 4 раза превышали рекомендуемую дозу для человека, токсическое действие не наблюдалось у беременных кроликов, которые были подвергнуты воздействию дозы, рекомендованной для человека. В исследованиях на крысах было показано, что пэгфилграстим может проникать через плаценту. Исследования на крысах показали, что репродуктивные характеристики, фертильность, экстральный цикл, дни между спариванием и коитусом и внутриутробная выживаемость не подвергались влиянию пэгфилграстима, который вводился подкожно. Актуальность этих данных для человека неизвестна.
В настоящее время препарат не числится в Государственном реестре лекарственных средств или указанный регистрационный номер исключен из реестра.
Регистрационный номер
ЛС-002332
Торговое название препарата
Неуластим
Международное непатентованное название
Пэгфилграстим (Pegfilgrastim)
Лекарственная форма
Раствор для подкожного введения
Состав
Один шприц-тюбик (0.6 мл) содержит:
активное вещество: пэгфилграстим 6 мг
вспомогательные вещества: натрия ацетат, сорбитол, полисорбат 20, вода для инъекций.
Описание
Прозрачная бесцветная жидкость.
Фармакотерапевтическая группа
Лейкопоэза стимулятор
Код АТХ [L03АА13]
Фармакологические свойства
Фармакодинамика
Гемопоэтический фактор роста.
Пэгфилграстим — ковалентный конъюгат филграстима (рекомбинантного человеческого гранулоцитарного колониестимулирующего фактора [Г-КСФ]) с одной молекулой полиэтиленгликоля (ПЭГ) 20 кДа, с пролонгированным действием в результате снижения почечного клиренса. Аналогично филграстиму, пэгфилграстим регулирует образование и высвобождение нейтрофилов из костного мозга, заметно увеличивает количество нейтрофилов с нормальной или повышенной функциональной активностью (хемотаксис и фагоцитоз) в периферической крови в течение 24 ч и вызывает небольшое увеличение количества моноцитов и/или лимфоцитов.
Как и другие гемопоэтические факторы роста, Г-КСФ может стимулировать эндотелиальные клетки in vitro.
Транзиторное увеличение лейкоцитов (лейкоцитоз) является ожидаемым последствием терапии пэгфилграстимом, т.к. соответствует его фармакодинамическим эффектам. Каких-либо побочных явлений, непосредственно связанных с таким лейкоцитозом, не описано.
Однократное введение пэгфилграстима после каждого цикла миелосупрессивной цитостатической терапии снижает продолжительность нейтропении и частоту возникновения фебрильной нейтропении аналогично ежедневному введению филграстима (в среднем, 11 ежедневных введений).
Фармакокинетика
После однократного подкожного введения время достижения максимальной концентрации (TCmax) пэгфилграстима 16-120 ч. Концентрация пэгфилграстима в сыворотке крови поддерживается в течение периода нейтропении после миелосупрессивной химиотерапии.
Распределение пэгфилграстима ограничено плазмой.
Выведение пэгфилграстима нелинейное, дозозависимое, насыщаемое. Клиренс, в основном, осуществляется нейтрофилами (>99%) и снижается с увеличением дозы пэгфилграстима. В соответствии с саморегулирующимся механизмом клиренса, концентрация пэгфилграстима в сыворотке быстро снижается с началом восстановления числа нейтрофилов.
Фармакокинетика у особых групп пациентов
Учитывая клиренс с участием нейтрофилов, вероятно, что фармакокинетика пэгфилграстима не изменяется при почечной или печеночной недостаточности.
Пожилой возраст
Фармакокинетика пэгфилграстима у пациентов старше 65 лет аналогична фармакокинетике у взрослых.
Показания
Для снижения продолжительности нейтропении, частоты возникновения фебрильной нейтропении и инфекций, проявляющихся фебрильной нейтропенией, при цитотоксической химиотерапии по поводу злокачественных заболеваний.
Противопоказания
Гиперчувствительность к белкам, получаемым с использованием E.coli, филграстиму, пэгфилграстиму или к любому другому компоненту препарата.
Нейтропения при хроническом миелолейкозе и миелодиспластических синдромах.
Острый лейкоз.
Для увеличения доз цитотоксической химиотерапии выше установленных в режимах дозирования.
Одновременное назначение с цитотоксической химио- и лучевой терапией.
Беременность и период кормления грудью.
Возраст до 18 лет.
С осторожностью
Злокачественные и предопухолевые заболевания миелоидного характера (в т. ч. острый миелолейкоз de novo и вторичный).
В комбинации с высокодозной химиотерапией.
Серповидноклеточная анемия.
Способ применения и дозы
Взрослые (≥18 лет): подкожно, 6 мг (один шприц-тюбик) через 24 ч после проведения каждого цикла цитотоксической химиотерапии.
Особые группы больных
Дети: рекомендаций по применению Неуластима у детей и подростков в возрасте до 18 лет нет (недостаточно данных).
Инструкции по применению, обращению и уничтожению
Шприц-тюбик с препаратом Неуластим предназначен только для однократного использования.
Препарат Неуластим представляет собой стерильный раствор без консервантов.
Перед введением раствор Неуластима следует осмотреть на наличие посторонних видимых частиц. Допускается введение только прозрачного и бесцветного раствора.
Чрезмерное встряхивание может разрушить пэгфилграстим, сделав его биологически неактивным.
Перед инъекцией раствор в шприц-тюбике следует согреть до комнатной температуры.
Любой неиспользованный препарат или его остатки следует уничтожить в соответствии с санитарными требованиями.
Препарат Неуластим можно хранить при комнатной температуре (не выше 30°С) в течение максимального однократного периода не более 72 ч.
Препарат Неуластим, подвергшийся воздействию комнатной температуры в течение более 72 ч, применять не следует.
Случайное воздействие отрицательных температур в течение однократного периода менее 24 ч не оказывает отрицательного влияния на стабильность Неуластима.
Побочное действие
Очень частые (≥10%) и частые (≥1%, Со стороны костно-мышечной системы: очень часто — слабые или умеренные боли в костях, которые, в большинстве случаев, проходят самостоятельно или купируются обычными анальгетиками; часто — артралгия, миалгия, боли в спине, конечностях и шее.
Организм в целом: часто — боль в груди (некардиальная), боль, лихорадка.
Реакции гиперчувствительности: редко — анафилаксия, сыпь, крапивница, ангионевротический отек, одышка и гипотензия, эритема и гиперемия в начале или при последующем введении. Иногда возобновление лечения сопровождается рецидивом симптомов. В случае развития серьезных аллергических реакций следует назначить соответствующее лечение с тщательным наблюдением за пациентом в течение нескольких дней. Необходимо прекратить терапию пэгфилграстимом при развитии серьезных аллергических реакций.
Со стороны нервной системы: часто — головная боль.
Местные реакции: часто — боль в месте инъекции.
Со стороны органов дыхания: кашель, одышка, инфильтраты в легких, нарушение функции дыхания, респираторный дистресс-синдром.
Со стороны органов кроветворения: спленомегалия, боли в верхнем левом квадранте живота; редко — тромбоз сосудов; очень редко — разрыв селезенки (в некоторых случаях с фатальных исходом), лейкоцитоз.
Со стороны желудочно-кишечного тракта: тошнота.
Со стороны кожи и подкожно-жировой клетчатки: редкие случаи острого фебрильного дерматоза (синдром Свита).
Со стороны лабораторных показателей: обратимое, слабое или умеренное клинически незначимое повышение мочевой кислоты; очень часто — повышение щелочной фосфатазы и лактатдегидрогеназы.
Передозировка
При однократном подкожном введении препарата в дозе 300 мкг/кг серьезных нежелательных явлений не возникло ни у здоровых добровольцев, ни у пациентов с немелкоклеточным раком легкого. Побочные явления при передозировке не отличались от побочных явлений при обычном применении препарата.
Взаимодействие с другими лекарственными средствами
Цитотоксическая химиотерапия. Из-за возможной чувствительности быстро делящихся миелоидных клеток к цитотоксической терапии Неуластим следует вводить через 24 ч после введения цитотоксических химиотерапевтических средств. В клинических исследованиях препарат безопасно применялся за 14 дней до введения цитотоксических химиотерапевтических средств.
5-фторурацил (5-FU) или другие антиметаболиты. Усиление угнетения кроветворения in vivo. Взаимодействие с другими гемопоэтическими факторами роста и цитокинами неизвестно.
Возможность взаимодействия с литием, который также способствует высвобождению нейтрофилов, специально не исследовали. Нет подтверждения, что данное взаимодействие может быть опасным.
Исследования, посвященные специфическим взаимодействиям или метаболизму, не проводили.
Признаков взаимодействия Неуластима с другими лекарственными препаратами на настоящее время не зафиксировано.
Несовместимость. Неуластим несовместим с растворами натрия хлорида.
Особые указания
Лечение Неуластимом должно проводиться только под контролем онколога или гематолога, имеющих опыт применения Г-КСФ.
Ограниченные данные свидетельствуют о том, что эффективность пэгфилграстима и филграстима одинакова в отношении времени купирования тяжелой нейтропении у пациентов с острым миелолейкозом de novo. Однако, следует проявлять осторожность при терапии Неуластимом у пациентов с острым миелолейкозом de novo, поскольку не установлены отдаленные результаты такой терапии.
Г-КСФ стимулирует эндотелиальные клетки и может ускорять рост миелоидных клеток, включая злокачественные клетки, и некоторые немиелоидные клетки in vitro.
Неуластим не следует использовать при миелодиспластических синдромах, хроническом миелолейкозе, вторичном остром миелолейкозе, поскольку безопасность и эффективность препарата у данных групп пациентов не оценивались. Следует особенно тщательно проводить дифференциальную диагностику между бласт-трансформацией при хроническом миелолейкозе и острым миелолейкозом.
Безопасность и эффективность Неуластима у больных с острым миелолейкозом de novo моложе 55 лет с транслокацией t (15;17) не изучались.
Безопасность и эффективность Неуластима у больных, получавших высокодозную химиотерапию, не изучались.
Кашель, лихорадка и одышка в сочетании с рентгенологическими инфильтративными изменениями, ухудшением функции легких и увеличением количества нейтрофилов могут служить признаками респираторного дистресс-синдрома у взрослых (РДС). В таком случае, по усмотрению врача, Неуластим следует отменить и назначить соответствующее лечение.
Зарегистрированы очень редкие случаи разрыва селезенки после применения пэгфилграстима, некоторые — с фатальным исходом. Следует тщательно наблюдать за размерами селезенки. Следует предусмотреть возможность спленомегалии или разрыва селезенки у больных с жалобами на боль в верхней левой части живота и/или в верхней части левого плеча.
Монотерапия Неуластимом не исключает развития тромбоцитопении и анемии при продолжении миелосупрессивной химиотерапии в полной дозе. Рекомендуется регулярно определять число тромбоцитов и гематокрит.
Неуластим не следует использовать для увеличения доз цитотоксической химиотерапии выше установленных в режимах дозирования.
Развитие серповидно-клеточного криза ассоциировалось с терапией пэгфилграстимом у пациентов с серповидно-клеточной анемией. Терапия пэгфилграстимом у пациентов с серповидно-клеточной анемией должна проводиться с осторожностью только после тщательного определения потенциального риска и пользы.
Лейкоцитоз 100 х 109/л или более наблюдается менее чем у 1% больных, получающих Неуластим, носит временный характер и обычно наблюдается через 24-48 ч после введения препарата в соответствии с его фармакодинамическими эффектами. Каких-либо побочных явлений, непосредственно связанных с таким лейкоцитозом, не описано. Безопасность и эффективность пэгфилграстима при мобилизации периферических стволовых клеток крови у больных соответствующим образом не оценивались.
Возросшая гемопоэтическая активность костного мозга в ответ на терапию факторами роста приводит к транзиторным положительным изменениям при визуализации костей, что следует принимать во внимание при интерпретации результатов.
Форма выпуска
Раствор для подкожного введения 6 мг/0.6 мл
По 6 мг/0.6 мл в шприц-тюбик, корпус которого изготовлен из стекла (гидролитический класс 1 по ЕФ), поршень — из пластмассы, с пробкой из бутилкаучука, ламинированного фторполимером. С другой стороны шприц-тюбик укупорен наконечником из бутилкаучука, ламинированного фторполимером. 1 стерильная игла для инъекций в тубе из полиэтилена, герметично укупоренной фольгой алюминиевой с ПВХ покрытием.
1 шприц-тюбик вместе с 1 иглой для инъекций и инструкцией по применению помещают в картонную пачку.
Условия хранения
При температуре 2-8°С, в защищенном от света месте.
Не замораживать.
Хранить в недоступном для детей месте.
Срок годности
2 года.
Препарат не следует использовать по истечении срока годности, указанного на упаковке.
Условия отпуска из аптек
По рецепту.
Юридический адрес производителя:
Ф. Хоффманн-Ля Рош Лтд, Грензахерштрассе 124, 4070 Базель, Швейцария
F. Hoffmann-La Roche Ltd, Grenzacherstrasse 124, 4070 Basel, Switzerland
Neulastim® — товарный знак Амген Инк США
Neulastim® продается по лицензии Амген Инк США
Претензии потребителей направлять по адресу Представительства в Москве:
107031, Трубная площадь, д.2
