Нимесулид: мифы и реальность
Статьи
Опубликовано в:
«СПРАВОЧНИК ПОЛИКЛИНИЧЕСКОГО ВРАЧА» »» 2013 № 4
А.Е.Каратеев
ФГБУ НИИ ревматологии РАМН, Москва
В настоящий момент врачи располагают богатым арсеналом средств борьбы с острой и хронической болью. Проблема иногда заключается в том, что и какому пациенту предложить. По мнению многих экспертов, нестероидные противовоспалительные препараты (НПВП) должны рассматриваться как средство 1-й линии, к которому следует обратиться во всех клинических ситуациях, когда боль носит ноцицептивный характер, т.е. связана с воспалением или повреждением живой ткани. Применение анальгетических средств с иным механизмом действия, таких как опиоиды, миорелаксанты, средства для лечения нейропатической боли и другие, оправданно лишь в той ситуации, когда НПВП оказались малоэффективными или имеются серьезные противопоказания для их назначения.
Ключевым механизмом воздействия НПВП на периферическую и центральную составляющую хронической боли является блокада фермента циклооксигеназы (ЦОГ)-2 и подавление гиперпродукции простагландинов (ПГ). НПВП являются основным средством для лечения боли у пациентов с ревматическими заболеваниями (РЗ): остеоартрозом (ОА), болью в нижней части спины, ревматоидным артритом (РА), анкилозирующим спондилитом. Конечно, современная терапия заболеваний суставов и позвоночника не основывается лишь на применении обезболивающих препаратов. Напротив, главное направление современного противоревматического лечения — остановка прогрессирования заболевания, подавление хронического воспаления и прекращение разрушения суставов. И эта задача благодаря революционным достижениям современной науки и внедрению в ревматологическую практику новых чрезвычайно эффективных патогенетических средств (таких как генно-инженерные биологические препараты), сегодня может быть решена. Тем не менее обезболивающие препараты продолжают сохранять свое место в комплексной терапии патологии суставов и позвоночника — в качестве вспомогательного, но незаменимого средства.
Необходимость проведения активной анальгетической терапии при РЗ определяется тем фактом, что хроническая боль независимо от этиологии становится самостоятельной угрозой для жизни пациента. Типичными спутниками хронической боли становятся депрессия, тревожность, нарушения сна и иммунитета, постоянное напряжение сердечно-сосудистой системы (ССС). Поэтому представления о том, что боль надо перетерпеть или научиться жить с ней, сегодня считают вредными и порочными.
Применение НПВП и качество жизни больных с РЗ
С точки зрения пациентов, НПВП являются важнейшим средством, позволяющим контролировать их состояние. В этом плане весьма любопытной представляется работа австралийских ученых, оценивших мнение пожилых людей, страдающих ОА, о разных анальгетиках. Само название статьи It looks after me (они заботятся обо мне) показывает позитивный настрой пациентов в отношении этих лекарств. По мнению больных, НПВП весьма эффективны — они хорошо устраняют симптомы болезни, позволяя сохранять повседневную активность. При этом в отличие от популярного безрецептурного анальгетика парацетамола они гораздо удобнее (нет необходимости принимать ежедневно несколько таблеток). В сравнении с опиоидами (они малодоступны у нас, но широко используются для купирования боли при РЗ на Западе) НПВП гораздо лучше переносятся, что имеет принципиальное значение для пожилых людей.
Очень важно, что активное применение НПВП способно не только улучшить качество жизни, но и повысить выживаемость пациентов с хроническими РЗ. В качестве доказательства данного положения можно привести работу T.Lee и соавт. Эти ученые наблюдали когорту 565 454 ветеранов США, страдающих ОА. Оказалось, что больные, регулярно принимавшие НПВП, достоверно реже (более 20%) погибали от кардиоваскулярных катастроф в сравнении с теми, кто не принимал этих препаратов.
Побочные действия НПВП
Однако применение НПВП — палка о двух концах, ведь эти препараты способны вызывать серьезные, угрожающие жизни осложнения, что может существенно ограничивать их терапевтическую ценность.
Желудочно-кишечный тракт
Традиционно на первое место среди этих осложнений ставят НПВП-гастропатию — специфическую патологию верхних отделов желудочно-кишечного тракта (ЖКТ), характеризующуюся появлением эрозий слизистой оболочки, язв и гастроинтестинальных катастроф — кровотечения и перфорации. Согласно общепризнанной теории этот побочный эффект возникает вследствие неселективности НПВП в отношении ЦОГ: помимо «плохой» (индуцируемой) ЦОГ-2 они блокируют также «хорошую» (структурную, постоянно присутствующую в тканях) ЦОГ-1, снижая тем самым синтез цитопротективных ПГ слизистой оболочки ЖКТ и способствуя ее повреждению под действием кислоты желудочного сока. Риск развития такой патологии у лиц, регулярно принимающих неселективные ингибиторы ЦОГ-2 (н-НПВП), возрастает по сравнению с популяцией более чем в 4 раза и составляет примерно 0,5-1 эпизод на 100 пациентов в год. По представлениям 1990-х годов больные, регулярно получавшие НПВП, погибали от ЖКТ-кровотечений в 2-3 раза чаще в сравнении с людьми, не принимающими каких-либо препаратов этой лекарственной группы.
| РЕЖИМ ДОЗИРОВАНИЯ НАЙЗ® Таблетки принимают с достаточным количеством воды предпочтительно после еды. Взрослым и детям старше 12 лет — внутрь по 1 таблетке 2 раза в сутки. При наличии заболеваний желудочно-кишечного тракта препарат желательно принимать в конце еды или после приема пищи. Максимальная суточная доза для взрослых — 200 мг. Пациентам с хронической почечной недостаточностью требуется снижение суточной дозы до 100 мг Представлена краткая информация производителя по дозированию лекарственного средства. Перед назначением препарата внимательно читайте инструкцию. |
Сердечно-сосудистая система
В последние годы принципиальное значение в оценке безопасности НПВП придается риску развития опасных осложнений со стороны ССС — инфаркта миокарда, внезапной коронарной смерти и ишемического инсульта (кардиоваскулярные катастрофы). Опасность тяжелых осложнений со стороны ССС существенно увеличивается у пациентов, в течение длительного времени и регулярно принимающих высокие дозы НПВП. Эта патология возникает вследствие влияния НПВП на баланс синтеза тромбоксана А2 (ЦОГ-1-зависимый процесс) и простациклина (ЦОГ-2-зависимый процесс) — субстанций, обладающих про- и антитромботическим действием.
Ранее считалось, что развитие этой патологии характерно в большей степени для селективных ингибиторов ЦОГ-2 (с-НПВП). Но теперь уже не вызывает сомнений тот факт, что и применение многих н-НПВП (в частности, диклофенака и индометацина) также способно повышать риск опасных осложнений со стороны ССС.
Кроме прокоагулянтного действия, НПВП способны вызывать дестабилизацию артериальной гипертензии (АГ), и это важный момент в патогенезе кардиоваскулярных катастроф. Данное осложнение в большей степени связано с блокадой ЦОГ-2 (а не ЦОГ-1, как думали ранее), которая образуется клетками почек в условиях повышенного артериального давления (АД). В этой ситуации ПГ, синтезируемые благодаря активности ЦОГ-2, играют роль важного фактора контроля АГ.
Факторы риска НПВП-осложнений
Подавляющее большинство серьезных побочных эффектов, связанных с приемом НПВП (как со стороны ЖКТ, так и ССС), возникают у больных, имеющих так называемые факторы риска (рис. 1).
Рис. 1. Факторы риска НПВП-осложнений.
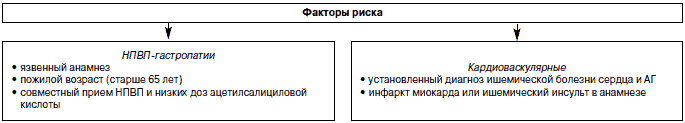
К сожалению, эти факторы очень часто присутствуют у пожилых больных, которые составляют основную часть современной популяции, нуждающейся в активной обезболивающей терапии.
Группа НПВП
Спектр НПВП, представленных сегодня на российском фармакологическом рынке, весьма широк — он насчитывает 18 разных наименований: ацетилсалициловая кислота, ацеклофенак, декскетопрофен, диклофенак, ибупрофен, кетопрофен, кеторолак, лорноксикам, мелоксикам, метамизол, напроксен, нимесулид, пироксикам, теноксикам, фенилбутазон, флубипрофен, целекоксиб и эторикоксиб.
Такое обилие препаратов делает возможным подбор конкретного средства для любой клинической ситуации и каждого конкретного специалиста. Главными факторами, которые учитываются практикующими врачами, является наличие у лекарства быстрого и мощного обезболивающего эффекта, противовоспалительного действия и хорошей переносимости. При этом очень важно, чтобы этот препарат имел достаточно низкий риск развития осложнений -как со стороны ЖКТ, так и ССС. Ведь по меткому замечанию академика Е.Л.Насонова, подбор обезболивающего препарата при РЗ — «путешествие между Сциллой и Харибдой».
Нимесулид
Принципиально важно, чтобы препарат имел невысокую стоимость, делающую его доступным широкому кругу потребителей.
Сочетание этих параметров свойственно нимесулиду -весьма популярному в России представителю группы НПВП. Важным критерием предпочтения практикующих врачей является уровень продаж препарата. Так, с 2006 по 2010 г. продажи нимесулида поднялись с 7 до 18 млн упаковок в год; в этом плане он уступает лишь диклофенаку с его обилием дешевых генериков (около 100 наименований!) и безрецептурному ибупрофену.
Высокий интерес к нимесулиду среди практикующих врачей сохраняется и в ряде стран Восточной и Центральной Европы. По данным A.Inotai и соавт., за период с 2002 по 2007 г., использование двух самых применяемых препаратов из группы с-НПВП — нимесулида и мелоксикама -выросло в этих странах на 325%.
Нимесулид — эффективное и удобное средство для лечения острой боли. У него высокая биодоступность — через 30 мин после перорального приема достигается значимая концентрация препарата в крови (не менее 25% от максимальной). Соответственно, уже через 30 мин препарат начинает работать, а через 1-3 ч развивается полный обезболивающий эффект.
Как было отмечено, фармакологическое действие НПВП связано с подавлением активности ЦОГ-2, а ассоциированные с их приемом осложнения со стороны ЖКТ в основном определяются блокадой ЦОГ-1 в слизистой ЖКТ. Однако ЦОГ-1 также принимает участие в развитии воспаления, поэтому локальное снижение ее активности в области повреждения следует рассматривать как позитивный момент. Нимесулид, обладающий умеренной селективностью в отношении ЦОГ-2, имеет подобное действие: лишь в небольшой степени влияя на «структурную» ЦОГ-1 слизистой желудка, он существенно снижает ее эффекты в области воспаления.
По мнению экспертов, есть основание предполагать для нимесулида ряд фармакологических эффектов, не зависимых от класс-специфического воздействия на ЦОГ-2. Так, он снижает гиперпродукцию основных провоспалительных цитокинов (интерлейкин-6, фактор некроза опухоли a), подавляет активность металлопротеиназ (ответственных, в частности, за разрушение гликопротеинового комплекса хрящевой ткани при ОА), обладает антигистаминным действием. Одним из важнейших «не-ЦОГ2-ассоциированных эффектов» нимесулида является блокада фермента фосфодиэстеразы-4, подавляющая активность макрофагов и нейтрофилов, которые играют важную роль в патогенезе острой воспалительной реакции.
Доказательная база
Терапевтический потенциал нимесулида доказан в ходе многочисленных клинических исследований. Так, имеются данные по его использованию при послеоперационном обезболивании. Например, в исследовании A.Binning и соавт. 94 пациентам, перенесшим артроскопическую операцию, в качестве анальгетика на 3 дня назначались нимесулид 200 мг, напроксен 1000 мг или плацебо. Согласно результатам исследования оба НПВП демонстрировали превосходство над плацебо. Но нимесулид в сравнении с препаратом контроля обеспечивал более высокий обезболивающий эффект в первые 6 ч после операции.
При острой патологии околосуставных мягких тканей — энтезитах, бурситах и тендинитах — нимесулид показал столь же выраженный (или даже несколько более высокий) эффект в отношении купирования боли и восстановления функции опорно-двигательной системы по сравнению с высокими дозами «традиционных» НПВП — диклофенака и напроксена. Например, в исследовании W.Wober 122 пациента с субакромиальным бурситом и тендинитом в течение 14 дней принимали нимесулид 200 мг/сут или диклофенак 150 мг/сут. В конце периода наблюдения хороший или отличный эффект терапии несколько чаще отмечался у получавших нимесулид — 82,3% в сравнении с 78,0% применяющих диклофенак. Субъективная оценка пациентов в отношении переносимости лекарств демонстрировала еще более значимое преимущество нимесулида. При этом 96,8% больных оценили переносимость нимесулида как хорошую или отличную и лишь 72,9% дали аналогичную оценку диклофенаку (p<0,05).
Нимесулид оказался действенным средством для лечения неспецифической боли в нижней части спины. Согласно результатам исследования, проведенного в Финляндии (n=102), нимесулид 100 мг 2 раза в сутки превосходил ибупрофен в дозе 600 мг 3 раза в сутки как по выраженности обезболивающего эффекта, так и по восстановлению функции позвоночника. К 10-му дню от начала лечения на фоне приема нимесулида отмечалось более чем двукратное улучшение функциональной активности. Среди пациентов, принимавших этот препарат, индекс Остверсти в среднем снизился с 38 до 15 баллов (-23), что достоверно отличалось от ибупрофена — с 35 до 20 (-15), р=0,02. При этом в сравнении с препаратом контроля нимесулид существенно реже (примерно в 2 раза — 7 и 13% соответственно) вызывал побочные эффекты со стороны ЖКТ.
Последнее крупное и хорошо организованное исследование, в котором оценивалась эффективность нимесулида, было проведено сербскими учеными L.Konstantinovic и соавт. Вообще эта работа посвящена применению низкоэнергетической лазерной терапии при острой боли в спине, сопровождающейся компрессией седалищного нерва (люмбоишалгия). Однако авторы оценивали эффективность лазеротерапии у больных, которые одновременно принимали НПВП — нимесулид в дозе 200 мг/сут. Всего в исследование были включены 546 больных, которые составили 3 группы: в 1-й пациенты получали нимесулид + настоящую лазеротерапию, 2-й — только нимесулид, 3-й — сочетание этого препарата и ложной лазеротерапии (плацебо). Согласно данным исследования в 1-й группе эффект был максимальным — уровень обезболивания достоверно превосходил результаты, полученные в 2 контрольных группах. Тем не менее весьма интересно отметить тот факт, что нимесулид сам по себе (2-я группа) и в комбинации с плацебо лазера давал весьма существенное облегчение не только механической боли в спине, но и радикулярной (нейропатической). Так, боль в спине уменьшилась в среднем в каждой из групп на 44, 18 и 22 мм, а в ноге — 33, 17 и 20 мм (визуальная аналоговая шкала). При этом переносимость терапии оказалась весьма хорошей — авторы не сообщили ни об одном случае серьезных осложнений, связанных как с использованием лазера, так и нимесулида.
Помимо острой боли нимесулид зарекомендовал себя как эффективное симптоматическое средство при хронических РЗ, прежде всего ОА. Так, P.Locker и соавт. провели сравнение нимесулида 200 мг или этодолака 600 мг у 199 больных ОА в ходе 3-месячного исследования. Лечебное действие нимесулида оказалось более высоким — его оценили как хорошее или превосходное 80% больных и лишь 68% дали аналогичную оценку этодолаку.
В масштабном и более длительном (6 мес) исследовании E.Huskisson и соавт. нимесулид в дозе 200 мг/сут сравнивали с диклофенаком 150 мг/сут у 279 больных ОА. Лечебное действие исследуемых препаратов, которое оценивалось по динамике самочувствия больных и функциональному индексу Лекена, практически не различалось. Однако переносимость нимесулида была достоверно лучше — в частности, осложнения со стороны ЖКТ возникли у 36 и 47% больных соответственно (p<0,05).
Самым крупным из длительных исследований нимесулида стала работа W.Kriegel и соавт., которые оценивали эффективность и безопасность этого препарата в сравнении с напроксеном 750 мг у 370 больных ОА в течение 1 года. Аналогично результатам, полученным E.Huskisson, эффективность обоих препаратов оказалась сопоставимой, правда, с некоторым преимуществом нимесулида. Так, изменение суммарного индекса WOMAC ко времени завершения работы составило 22,5 и 19,9%. Суммарная частота побочных эффектов при использовании нимесулида в сравнении с напроксеном также оказалась ниже — 47,5 и 54,5% соответственно. Следует обратить внимания на тот факт, что во всех трех исследованиях на фоне приема нимесулида не было зафиксировано значимого увеличения кардиоваскулярных осложнений.
Переносимость и безопасность
Однако важнейшим достоинством нимесулида является хорошая переносимость и относительно низкая частота развития осложнений со стороны ЖКТ. Хорошо известно, что именно развитие патологии ЖКТ, относящейся к числу класс-специфических осложнений НПВП, является одним из основных факторов, определяющих соотношение риск/польза для этого класса лекарственных препаратов. Данные, подтверждающие благоприятную переносимость нимесулида в отношении ЖКТ, были получены российскими и зарубежными учеными в ходе серии проспективных и когортных наблюдательных исследований.
Очень показательна работа ирландского ученого F.Bradbury, который провел оценку частоты ЖКТ-осложнений при использовании диклофенака (n=3553), нимесулида (n=3807) и ибупрофена (n=1470) в реальной клинической практике. Суммарная частота этой патологии при использовании нимесулида была существенно меньше в сравнении с диклофенаком — 12,1%, хотя и не отличалась от ибупрофена — 8,1 и 8,6%.
Относительно низкий риск развития ЖКТ-осложнений при использовании нимесулида также был подтвержден работой итальянских эпидемиологов A.Conforti и соавт., которые провели анализ 10 608 спонтанных сообщений о серьезных побочных эффектах (1988-2000 гг.), связанных с приемом разных НПВП. Нимесулид, как оказалось, был причиной развития тех или иных осложнений со стороны ЖКТ в 2 раза реже в сравнении с другими НПВП. Число спонтанных сообщений о проблемах, связанных с этим препаратом, составило лишь 10,4% от их общего числа. При этом диклофенак был причиной проблем в 21,2%, кетопрофен — 21,7%, а пироксикам — 18,6%.
Опасность развития ЖКТ-кровотечения на фоне приема разных НПВП в реальной клинической практике оценивалась в масштабном эпидемиологическом исследовании J.Laporte и соавт. Исследуемый материал был получен при анализе причин 2813 эпизодов этого осложнения (7193 пациента в качестве контроля). Нимесулид оказался более безопасен, чем многие другие популярные в Европе НПВП: относительный риск кровотечения для нимесулида составил 3,2, для диклофенака — 3,7, мелоксикама — 5,7, рофекоксиба — 7,2.
Большое значение имеет оценка влияния нимесулида на состояние ССС. Следует отметить, что вопрос сравнительного риска развития инфаркта миокарда при использовании нимесулида, по всей видимости, был освящен лишь в одной крупной работе, проведенной финскими учеными. В ходе этого масштабного исследования проанализировано 33 309 эпизодов инфаркта миокарда, при этом контроль по полу и возрасту составили 138 949 лиц. Согласно полученным результатам относительный риск инфаркта для нимесулида — 1,69. Это значение приближалось к соответствующему показателю, определенному для мелоксикама, набуметона, этодолака и неселективных НПВП.
Результаты российских исследований
Нимесулид активно изучался в России. Недавно нами был опубликован обзор российских клинических исследований, в которых определяли сравнительную эффективность и безопасность этого препарата. Всего за период с 1995 по 2009 г. было проведено 21 исследование, в которых нимесулид назначался в дозе от 200 до 400 мг/сут на срок от 7 дней до 12 мес (рис. 2). Нимесулид был использован у 1590 больных, причем помимо пациентов, страдающих РЗ, здесь были и пациенты с острыми травмами, урологической патологией, а также люди, перенесшие стоматологические операции.
Рис. 2. Обзор данных 21 российского клинического исследования, в которых проводилось сравнение нимесулида 200–400 мг/сут (n=1590) и активного контроля (n=526): частота основных побочных эффектов.
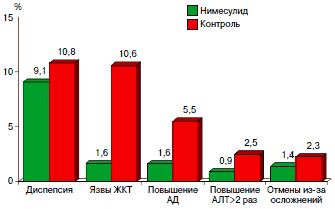
Контроль составили пациенты, которым назначались другие НПВП (в основном диклофенак), парацетамол, трамадол и гомеопатический препарат артрофоон (всего 526 больных). Во всех работах нимесулид не уступал или превосходил препараты сравнения по эффективности: число больных, у которых отмечалось значимое улучшение, составляло от 40 до 90%. В плане безопасности он также показал себя с самой лучшей стороны. Так, число больных с диспепсией при использовании нимесулида составило 9,1%, препаратов сравнения — 10,8%; язвы ЖКТ развились у 1,6 и 10,6% (p<0,001); повышение АД у 1,6 и 5,5% (p<0,001); повышение аланинаминотрансфераз (АЛТ) у 0,9 и 2,5% (p<0,05); потребовались отмены у 1,4 и 2,5% (p<0,05). У единичных больных отмечались отеки и кожные аллергические реакции. В целом, хотя переносимость нимесулида и не была идеальной, она оказалась существенно и достоверно лучше, чем наиболее часто используемого препарата сравнения диклофенака.
В 2009 г. нами была опубликована работа, посвященная изучению развития побочных эффектов при длительном использовании нимесулида. Мы провели ретроспективный анализ частоты осложнений со стороны ЖКТ, кардио-васкулярной системы и печени у 322 больных РЗ, находившихся на стационарном лечении в клинике НИИР РАМН в 2007-2008 гг. и не менее 12 мес до поступления принимавших нимесулид. Всем пациентам была проведены гастроскопия и систематический контроль АД и биохимических показателей крови.
Ни у кого из больных на фоне лечения нимесулидом не развилось опасных осложнений со стороны ЖКТ — таких как кровотечение или перфорации язвы. Язвы желудка и двенадцатиперстной кишки были выявлены у 13,3% обследованных пациентов. Это примерно на 1/3 меньше, чем число язв, возникающих на фоне приема н-НПВП. Так, ранее мы показали, что у 4931 больного, получавшего н-НПВП (преимущественно диклофенак), язвы верхних отделов ЖКТ были выявлены у 18,1% из них.
Несмотря на то что в изучаемой группе был серьезный коморбидный фон по заболеваниям ССС, за 12-месячный предшествующий период инфаркт миокарда был зафиксирован лишь у 1 пациента. Это мужчина 68 лет, страдавший РА, ишемической болезнью сердца в течение многих лет и высокой АГ. Еще у 2 пациенток на фоне приема нимесулида была отмечена отрицательная динамика электрокардиограммы, описанная кардиологом как постинфарктный кардиосклероз.
Стойкое повышение АД в период госпитализации отмечено у 11,5% больных. Среди лиц, исходно имевших эту патологию, частота дестабилизации АГ была существенно выше, чем в целом по группе, и составила 26,8%.
Ни у кого из больных не развилось клинически выраженной патологии печени — желтухи, гепатомегалии, симптомов печеночной недостаточности. Существенное повышение печеночных ферментов (более чем в 2 раза в сравнении с нормой) возникло лишь у 7 (2,2%) больных. Все они страдали РА и помимо нимесулида получали цитотоксические препараты — метотрексат или лефлуномид.
Гепатотоксичность нимесулида
Обсуждая перспективы применения нимесулида, следует обратить особое внимание на проблему осложнений со стороны печени. НПВП-гепатопатия представляет собой проявление метаболической идиосинкразии и возникает редко (в сравнении с другими лекарственными осложнениями). По многолетней статистике серьезные гепатотоксические осложнения, проявляющиеся клинически выраженным внутрипеченочным холестазом или острой печеночной недостаточностью, возникают на фоне регулярного приема НПВП примерно у 1 из 10 тыс. пациентов.
В отношении нимесулида к 2000 г. за 15-летний период (1985-2000 гг.) его применения в 50 разных странах было отмечено лишь 192 случая серьезных осложнений со стороны печени. Учитывая, что на 2000 г. нимесулидом были пролечены 280 млн больных, суммарная частота опасных гепатотоксических реакций составляет менее 1 случая на 1 млн проведенных курсов лечения.
Основной орган Европейского союза, обеспечивающий контроль над оборотом лекарственных препаратов в Европе, — EMEA (European Medicines Agency) после рассмотрения этой проблемы не нашел оснований для прекращения использования нимесулида (пресс-релиз от 21.09.07). Было принято компромиссное решение рекомендовать ограничить применение нимесулида в странах Европы курсом не более 15 дней и в дозе, не превышающей 200 мг/сут. Для исполнения этого решения странам — членам Европейского союза было рекомендовано изъять из аптечной сети упаковки, которые содержат более 30 стандартных доз нимесулида.
Самое важное в этом документе, по мнению C.Mattia и соавт., — признание того факта, что гепатотоксичность нимесулида не превышает гепатотоксичности многих других НПВП, которые успешно используются в клинической практике.
Повторное рассмотрение вопроса о нимесулиде было проведено медицинским руководством Европейского союза 23 июня 2011 г. Новое постановление EMEA подтвердило основные положения, обозначенные в пресс-релизе от 21.09.07: достоинства нимесулида при кратковременном купировании острой боли явно превышают его недостатки, что оправдывает дальнейшее применение препарата.
Действительно, объективный анализ имеющихся литературных данных показывает, что гепатотоксичность нимесулида не выше, чем у многих других представителей класса НПВП. По данным клинических исследований, негативная динамика лабораторных биохимических показателей, свидетельствующая о развитии патологии печени, отмечается при использовании нимесулида с такой же частотой, как и на фоне приема других НПВП. При назначении нимесулида коротким курсом (не более 30 дней) повышение АЛТ в 2 раза и более отмечается лишь у 0,4% больных, а при длительном многомесячном приеме частота подобных изменений не превышает 1,5%.
Очень важные данные о реальной гепатотоксичности нимесулида можно почерпнуть из исследования D.Sanchez-Matienzo и соавт. Обычно эта работа используется в качестве доказательства того факта, что осложнения со стороны печени при использовании нимесулида возникают достоверно чаще в сравнении с другими НПВП, однако при тщательном исследовании представленного материала выводы могут стать совсем иными.
Авторы провели сопоставление частоты осложнений, связанных с приемом разных НПВП. При этом материалом для анализа являлись спонтанные сообщения практикующих врачей, собранные со всего мира Управлением по контролю пищевых продуктов и лекарств в США и Всемирной организацией здравоохранения (ВОЗ). Так, на 2003 г. ВОЗ получила 185 253 таких «сигнала», большинство из которых, естественно, касалось типичных для НПВП осложнений со стороны ЖКТ и ССС. При этом количество сообщений об осложнениях со стороны печени составило для всех НПВП лишь 2,7%.
Для диклофенака эта пропорция была иной: доля сообщений о гепатотоксических реакциях среди всех осложнений, связанных с этим препаратом, выросла до 4,7%. Наименее удачной данная пропорция оказалась для нимесулида — 14,4%. На основании этих цифр, казалось бы, можно сделать вывод, что нимесулид более опасен для печени, чем другие НПВП.
Картина представляется иной, если оценить не относительные, а абсолютные данные по осложнениям со стороны печени. Так, общее количество сообщений о гепатотоксических реакциях при использовании диклофенака составило 990, ибупрофена — 590, а нимесулида — лишь 152. Самое главное, что угрожающая жизни патология — печеночная недостаточность была зафиксирована ВОЗ у 21 больного, получавшего диклофенак, 32 — получавших ибупрофен, и только у 4 использующих нимесулид (!).
Отсюда видно, во-первых, что осложнения со стороны печени при использовании нимесулида возникают крайне редко, а во-вторых, их абсолютное число очень невелико в сравнении с другими популярными НПВП.
Имеется фактически лишь одна масштабная эпидемиологическая работа, в которой изучалась сравнительная гепатотоксичность НПВП, — исследование итальянских ученых G.Traversa и соавт. Они провели анализ частоты гепатотоксических реакций у 397 537 больных за период с 1997 по 2001 г. Суммарная частота осложнений со стороны печени на фоне приема НПВП составила 29,8 на 100 тыс. пациенто-лет. Соответственно, показатель относительного риска гепатотоксических реакций для всех НПВП составил 1,4. Индивидуальная частота серьезных осложнений со стороны печени при использовании нимесулида составила 35,3 на 100 тыс. человеко-лет меньше в сравнении с диклофенаком — 39,2, кеторолаком — 66,8 и ибупрофеном — 44,6.
Для нас очень важен российский опыт применения нимесулида, ведь в нашей стране за последние 15 лет этот препарат был назначен миллионам больных. И тем не менее до настоящего времени в российской медицинской литературе нет ни одного описания тяжелых гепатотоксических реакций, возникших на фоне этого препарата и закончившихся развитием печеночной недостаточности.
Заключение
На сегодняшний день нимесулид представляется одним из наиболее удачных представителей группы НПВП по соотношению эффективности, хорошей переносимости и низкой стоимости, являясь одним из наиболее популярных НПВП в России, Восточной и Центральной Европе.
Основным достоинством нимесулида является сочетание быстрого анальгетического эффекта, хорошего противовоспалительного действия, благоприятной переносимости (в сравнении с «традиционными» НПВП) и низкой стоимости. Риск развития гепатотоксических осложнений при использовании нимесулида не превышает аналогичных показателей для других популярных НПВП (в частности, диклофенака).
В России накоплен большой позитивный опыт применения нимесулида, отражением которого стала серия отечественных контролируемых клинических исследований, где нимесулид показал себя как эффективное и относительно безопасное обезболивающее средство.
В нашей стране нимесулид получили миллионы пациентов, многие из них принимали его в течение длительного времени, и при этом не было зафиксировано ни одного эпизода тяжелых гепатотоксических реакций.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Состав
В состав таблеток Нимесулид входит 100 мг действующего вещества нимесулида, а также вспомогательные вещества: крахмал кукурузный, коллоидный кремния диоксид, тальк, крахмалгликолят натрия, микрокристаллическая целлюлоза, стеарат магния, дигидрат кальция гидрофосфат.
Форма выпуска
Выпускается в виде таблеток.
Фармакологическое действие
Нимесулид — что это такое?
Нестероидное, простивовоспалительное средство. Медикамент обладает антиагрегантным, жаропонижающим, обезболивающим и противовоспалительным эффектами.
Фармакодинамика и фармакокинетика
Принцип воздействия направлен на торможение процесса синтезирования простагландинов в воспалительном очаге, на селективное подавление циклооксигеназы-2.
Показания к применению Нимесулида
От чего таблетки? Показаниями к применению Нимесулида являются:
- остеоартроз;
- ревматоидный артрит;
- бурсит;
- тендинит;
- артриты различного генеза.
Препарат назначают для купирования острого болевого синдрома при миалгии, альгодисменорее, зубной боли, артралгии, головной боли, в послеоперационном периоде.
Лекарственное средство не оказывает воздействия на прогрессирование заболевания, эффективно применяется для уменьшения выраженности воспалительного процесса, для уменьшения боли, а также в качестве симптоматической терапии.
Противопоказания
Нимесулид не назначают при эрозивно-язвенных заболеваниях пищеварительного тракта, при бронхиальной астме, непереносимости препаратов группы НПВС, при цереброваскулярных и других кровотечениях, при язвенном колите, воспалительных заболеваниях кишечника, гемофилии, болезни Крона, рецидивирующей форме полипоза околоносовых пазух и носа, при активном кровотечении в желудочно-кишечном тракте, при нарушении свертываемости крови.
Лекарственное средство не применяется при прогрессирующей патологии почечной системы, при выраженной форме почечной недостаточности, при гепатотоксических реакциях на фоне применения нимесулида в анамнезе, при активных заболеваниях печеночной системы, при декомпенсированной форме хронической сердечной недостаточности, при вынашивании беременности, при гиперкалиемии, детям до достижения 12 лет, при одновременном применении других гапатотоксических препаратов, в период после аортокоронарного шунтирования.
Побочные действия
Применение лекарственного средства Нимесулид может вызвать ряд побочных эффектов.
Центральная нервная система: синдром Рейе, головная боль, «кошмарные» сны, страх, тревожность, головокружения, нервозность.
Кожные покровы: повышенное потоотделение, зуд, высыпания, дерматит, эритема, ангионевротический отек, токсический эпидермальный некролиз, многоформная экссудативная эритема, крапивница, синдром Стивенса-Джонсона.
Мочевыделительная система: интерстициальный нефрит, почечная недостаточность, гематурия, дизурия, задержка мочеиспускания, олигурия.
Пищеварительный тракт: холестаз, гастрит, метеоризм, запоры, повышение уровня ферментов печени, кровотечения из желудочно-кишечного тракта, рвота, тошнота, диарейный синдром, желтуха, молниеносный гепатит, боли в эпигастральной области, перфорация и язвенные поражения стенок желудка.
Органы кроветворения: повышение времени кровотечения, геморрагии, пурпура, панцитопения, тромбоцитопения, анемия.
Дыхательная система: бронхоспазм, одышка, возможно обострение уже существующей бронхиальной астмы.
Органы чувств: нарушения зрительного восприятия в виде нечеткости зрения.
Сердечно-сосудистая система: «приливы» тока крови к кожным покровам лица, падение уровня кровяного давления, учащенное сердцебиение. Также отмечается гипотермия, общая слабость, повышение уровня ионов калия.
Инструкция по применению Нимесулида (Способ и дозировка)
Таблетки Нимесулид, инструкция по применению
Лекарство принимают дважды в день по 50-100 мг, желательно после приема пищи. При выраженной патологии почечной системы суточная дозировка составляет 100 мг. Лекарственное средство рекомендуется по возможности применять минимально короткими курсами в минимальных, но эффективных дозах.
Инструкция по применению Нимесулид Максфарма является аналогичной.
Передозировка
Может проявляться тошнотой, рвотой, повышением сонливости. Также возможны признаки апатии, кровотечений в желудке и кишечном тракте, увеличения артериального давления, угнетения дыхания.
Применяется промывание желудка, использование активированного угля, лечение по симптомам.
Взаимодействие
Риск гепатотоксического воздействия значительно возрастает при одновременном применении гепатотоксических медикаментов. Лекарственное средство повышает эффективность антикоагулянтов. При приеме Фуросемида отмечается снижение выраженности его диуретического действия.
Нимесулид вытесняет салициловую кислоту, фенофибрат и фуросемид из связей с белками. Препарат повышает уровень концентрации ионов лития в плазме крови.
Лекарственное средство способно повышать токсичность метотрексата, усиливать нефротоксическое воздействие Циклоспорина. Риск желудочно-кишечных кровотечений возрастает при одновременной терапии селективными ингибиторами обратного захвата серотонина, глюкокортикостероидами.
Условия продажи
Требуется рецепт.
Условия хранения
В темном, недоступном для детей месте при температуре не более 25 °С.
Срок годности
Не больше 3-х лет.
Особые указания
Пациентам в период лечения препаратом Нимесулид рекомендуется дважды в месяц осуществлять контроль над состоянием печеночной системы. При повышении уровня ферментов печени, появлении зуда, высыпаний, боли в эпигастральной области, желтухи, при потемнении мочи лечение прекращают.
Отзывы о препарате Нимесулид свидетельствуют о нарушении зрительного восприятия у пациентов, длительно принимавших лекарственное средство. При регистрации любых изменений со стороны органов зрения терапию прекращают, проводят обязательное полное офтальмологическое обследование.
Описание медикамента указывает на возможную задержку жидкости в организме, что требует осторожности при лечении пациентов с гипертонической болезнью.
Не рекомендуется назначать Нимесулид совместно с другими медикаментами из группы НПВС.
Лекарственное средство не может заменить профилактическое воздействие антиагрегантов, несмотря на выраженное снижение скорости агрегации тромбоцитов.
Препарат не назначают женщинам, планирующим беременность из-за отрицательного влияния на фертильность.
Нимесулид может оказывать воздействие на управление автотранспортом.
Аналоги Нимесулида
Совпадения по коду АТХ 4-го уровня:
Аналогами Нимесулида являются препараты:
- Амеолин
- Апонил
- Месулид
- Найз
- Ниган
- Нимегезик
- Нимесил
- Нимесин
- Нимид
- Нимуджет
- Нимулид
- Нимуспаз
- Ремесулид
- Ремисид
- Сулидин
Отзывы о Нимесулиде
Подавляющее большинство отзывов о Нимесулиде носят положительный окрас. Лекарство очень эффективно для снятия болевых симптомов, температуры, различного рода воспалений. Препарат помогает быстро и его действие носит продолжительный характер.
В редких отрицательных комментариях встречаются упоминания о побочных эффектах медикамента.
Цена Нимесулида, где купить
Цена Нимесулида на упаковку 20 таблеток по 100 мг составляет 50 — 150 рублей.
- Интернет-аптеки РоссииРоссия
ЗдравСити
-
Нимесулид-Тева таблетки 100мг 20штБлюфарма-Индустрия Фармацеутика
-
Нимесулид-Тева таблетки 100мг 30штБлюфарма-Индустрия Фармацеутика
-
Нимесулид-мбф гран. для пригот. сусп. для вн. приёма 100 мг пак. 2г 30штОАО Марбиофарм
-
Нимесулид таблетки 100мг 10штАО «АВВА РУС»
-
Нимесулид таблетки 100мг 20шт Изварино ФармаООО «Изварино Фарма»
Аптека Диалог
-
Нимесулид-МБФ* (гран. д/приг. сусп. 100мг №30)Марбиофарм ОАО
-
Нимесулид-МБФ* гранулы для приготовления суспензии 100мг №1Марбиофарм ОАО
-
Нимесулид Велфарм таблетки 100мг №30Велфарм ООО
-
Нимесулид-ЛекТ таблетки 100мг №20Тюменский хим-фарм завод/Патент-Фарм
-
Нимесулид-МБФ* гранулы для приготовления суспензии 100мг №5Марбиофарм ОАО
Ригла
-
Нимесулид Форте гель д/наруж. прим. 2% 50гРеплек Фарм ООО Скопье/Березовский фарма
-
Нимесулид-Вертекс гель д/наруж.прим. 1% 50г тубаВертекс АО
-
Нимесулид гель д/наруж.прим. 1% 20гОзон ООО
показать еще
Нимесулид инструкция по применению
Дата публикации: 28.10.2021

ИМЕЮТСЯ ПРОТИВОПОКАЗАНИЯ. ВОЗМОЖНЫ ПОБОЧНЫЕ ЭФФЕКТЫ. НЕОБХОДИМА КОНСУЛЬТАЦИЯ СПЕЦИАЛИСТА.Боль в суставахВоспаление суставовГоловная больДля лежачих больныхЖаропонижающее взросломуЖаропонижающие для детейЖаропонижающие свечиЖаропонижающие сиропыЖаропонижающие таблеткиЗубная больМази от воспаленияПротивовоспалительные каплиСвечи от воспаленияСвечи от температурыСиропы от температурыСредства от температурыТаблетки от воспаленияТаблетки от температуры
Содержание статьи
- Показания к применению нимесулида
- Что лучше сбивает температуру – ибупрофен или нимесулид?
- Противопоказания
- Побочные эффекты
- Как принимать нимесулид
- Нимесулид и алкоголь
- Задайте вопрос эксперту по теме статьи
При наличии боли, для снижения температуры тела люди часто принимают нимесулид. Это нестероидное противовоспалительное средство (НПВС). Его можно приобрести в виде таблеток или суспензии. Препарат оказывает выраженное обезболивающее действие, но обладает и жаропонижающим эффектом. Его назначают взрослым и детям после двенадцати лет.
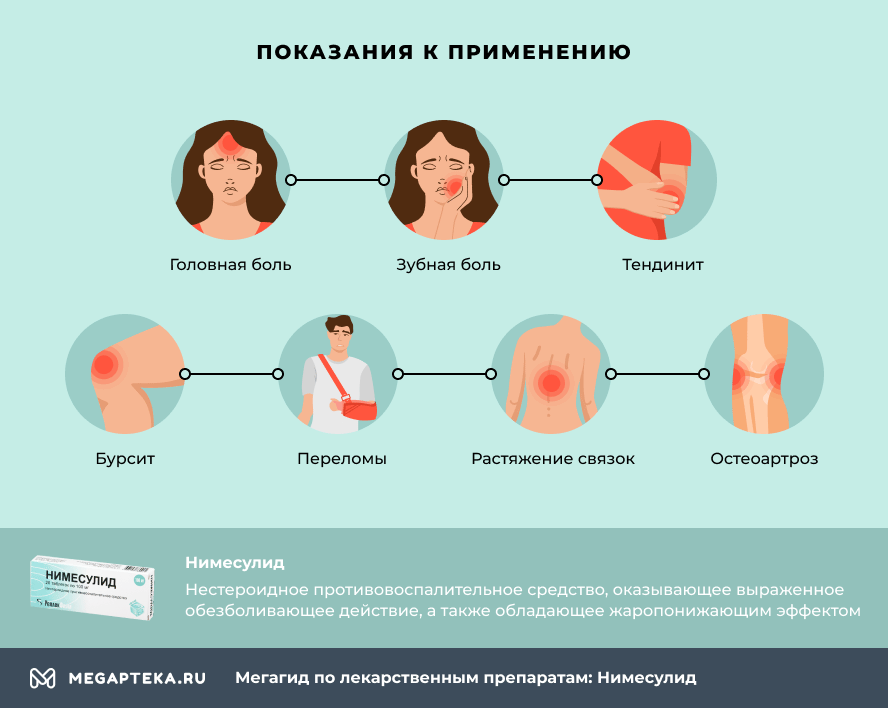
Показания к применению нимесулида
Помогает нимесулид от головной и зубной боли. Препарат используют в качестве обезболивающего и противовоспалительного средства при заболеваниях опорно-двигательной системы:
- Тендините;
- Бурсите;
- Переломах, вывихах костей;
- Растяжении связок;
- Остеоартрозе (остеоартрите).
Лекарственное средство применяют для уменьшения выраженности болевого синдрома у пациентов, страдающих люмбалгией, межреберной невралгией, миалгией.
От чего таблетки применяются? Таблетки нимесулида при месячных гинекологи назначают женщинам, страдающим первичной альгодисменореей.
Через сколько действует нимесулид? Через полчаса после приема препарата в крови находится до 80% основного действующего вещества. Максимальный обезболивающий эффект наблюдается спустя 1-3 часа после приема препарата.
Хотите разбираться в аналогах лекарств, чтобы умело подбирать препараты на свой бюджет? Наша методичка от экспертов-провизоров «Аналоги популярных лекарств» поможет вам в этом! Получить методичку просто: подпишитесь на наши соцсети и напишите в сообщения «аналоги».
Мегаптека в соцсетях: ВКонтакте, Telegram, OK, Viber
Что лучше сбивает температуру – ибупрофен или нимесулид?
Оба препарата относятся к одной и той же фармакологической группе – нестероидным противовоспалительным средствам, обладают аналогичными эффектами и используются для понижения температуры тела. И ибупрофен, и нимесулид оказывают выраженное жаропонижающее действие. Однако нимесулид не используют как жаропонижающее средство — для этой цели лучше подходит ибупрофен. Более того, если во время лечения нимесулидом появились симптомы ОРВИ, препарат следует отменить.
Противопоказания
Нимесулид не применяют при наличии следующих противопоказаний:
- Гиперчувствительность к основному действующему веществу и вспомогательным ингредиентам;
- Бронхоспазм, крапивница, ринит, зарегистрированный ранее после приема других НПВС;
- Сочетания поллиноза или бронхиальной астмы с аллергией на аспирин и НПВС;
- Ранее возникающего токсического действия препарата на печень.
Нимесулид не применяют для лечения пациентов, страдающих болезнью Крона, язвенным колитом, кормящих грудью женщин и детей младше 12 лет. Препарат не назначают пациентам, страдающим алкогольной и наркотической зависимостью, заболеваниями печени в активной фазе, печёночной недостаточностью.
Врачи не рекомендуют принимать нимесулид женщинам во время беременности и на этапе ее планирования.
Побочные эффекты
При приеме нимесулида, как и других нестероидных противовоспалительных средств, иногда у пациентов наблюдаются нежелательные реакции:
- Малокровие, повышение уровня эозинофилов в крови;
- Точечные кровоизлияния на коже;
- Крапивница, кожный зуд, ангионеротический отек;
- Повышенная потливость;
- Многоформная эритема.
Нечасто пациенты жалуются на головную боль, головокружение, сонливость. Редко развивается преходящее нарушение психического здоровья. У пациентов возникает чувство страха, кошмарные ночные сновидения, повышается нервозность.
Осложнения со стороны сердца и сосудов представлены повышением артериального давления, учащением сердечных сокращений. Крайне редко наступает бронхоспазм, обострение бронхиальной астмы. Пациенты, принимающие нимесулид, могут ощущать приливы крови к коже лица, сердцебиение.
При приёме нимесулида повышаетися риск развития острой хирургической патологии органов пищеварительного тракта:
- Желудочного кровотечения;
- Обострения язвенной болезни;
- Прободения язвы.
Может повыситься активность печеночных ферментов, развиться желтуха с застоем желчи, гепатит. У больных может возникнуть нарушение мочеиспускания, в моче появиться кровь.
Как принимать нимесулид
Оптимальную дозу и способ применения препарата определяет врач. Обычно взрослым и детям старше 12 лет рекомендуют принимать внутрь по 100 мг нимесулида дважды в день после еды.
Нимесулид и алкоголь
Совместимость препаратов определяет производитель лекарственного средства. В инструкции нет информации, можно ли одновременно с нимесулидом употреблять спиртные напитки. Но, учитывая, что при приеме препарата может развиться поражение печени, почек, органов пищеварительной системы, от употребления спиртных напитков стоит отказаться. Совместный прием обоих веществ повышает риск развития осложнений.
Задайте вопрос эксперту по теме статьи
Остались вопросы? Задайте их в комментариях ниже – наши эксперты ответят вам. Там же Вы можете поделиться своим опытом с другими читателями Мегасоветов.
Выпускающий редактор
Эксперт-провизор
Поделиться мегасоветом
Понравилась статья? Расскажите маме, папе, бабушке и тете Гале из третьего подъезда
Цены на товар Нимесулид:
Мегаптека,
Цены на Нимесулид в Санкт-Петербурге, Цены на Нимесулид в Новосибирске, Цены на Нимесулид в Екатеринбурге, Цены на Нимесулид в Казани, Цены на Нимесулид в Нижнем Новгороде, Цены на Нимесулид в Челябинске, Цены на Нимесулид в Самаре, Цены на Нимесулид в Уфе, Цены на Нимесулид в Ростове-на-Дону, Цены на Нимесулид в Омске, Цены на Нимесулид в Красноярске, Цены на Нимесулид в Воронеже, Цены на Нимесулид в Перми, Цены на Нимесулид в Волгограде, Цены на Нимесулид в Краснодаре, Цены на Нимесулид в Тюмени, Цены на Нимесулид в Саратове, Цены на Нимесулид в Тольятти, Цены на Нимесулид в Ижевске, Цены на Нимесулид в Барнауле
Гид по аналогам за подписку
подпишитесь на соцсети и напишите в сообщения «аналоги»
Заболевания суставов различной локализации являются одной из самых
частых причин обращения к врачу наряду с артериальной
гипертензией. Заболевания суставов являются социально значимыми
болезнями.
Во-первых, эти заболевания поражают значительную часть населения.
Наиболее распространенным заболеванием суставов является деформирующий
остеоартроз (ОА), особенно у лиц старше 65 лет, когда его
распространенность достигает 97% населения. Среди хронических
воспалительных заболеваний суставов наиболее частым является
ревматоидный артрит (РА) — заболевание, практически облигатно
приводящее к инвалидизации больных уже через 3–5 лет от дебюта
болезни.
Во-вторых, эти заболевания характеризуют развитие стойкого болевого
синдрома, который может быть связан с различными причинами.
Наиболее частая причина боли при патологии суставов — развитие
синовиита. Однако при ОА развитие боли может быть связано
и с другими патогенетическими звеньями болезни. В норме
болевые окончания имеют все структуры сустава, за исключением хряща. Но
при ОА происходит частичная васкуляризация и иннервация хряща.
Истончение и повреждение хряща снижает его амортизационные
свойства, увеличивается нагрузка на субхондральную кость
с развитием ее отека и боли. Кроме того, фибрилляция хряща
также индуцирует боль и воспаления.
Данные, полученные при изучении влияния боли на прогноз при ОА, свидетельствуют:
-
Около 20% больных не получают
адекватного лечения хронического болевого синдрома, так что уровень
боли у них по 10-сантиметровой визуальной аналоговой шкале (ВАШ)
составляет 5 см и более [1]. -
Хроническая боль при ОА приводит к уменьшению продолжительности жизни женщин в среднем на 10–12 лет.
-
Продолжительность жизни пожилых больных с ОА в большей
степени зависит от интенсивности боли, чем от наличия сопутствующих
потенциально жизнеугрожающих заболеваний [2]. -
Риск прогрессирования ОА
в равной степени связан с болевым синдромом, как
и с рентгенологическими изменениями.
Нестероидные противовоспалительные препараты (НПВП) обладают
анальгетическим, противовоспалительным и жаропонижающим эффектами.
Поэтому они являются незаменимыми в лечении артрологических
заболеваний. Быстрое развитие обезболивающего эффекта и определяет
облигатность их применения в лечении суставной патологии.
Позитивный лечебный эффект НПВП связан с ингибицией ЦОГ-2. Этот
фермент, участвующий в каскаде распада поврежденных при воспалении
и других поражениях клеточных мембран, отвечает за выделение
провоспалительных простагландинов и других медиаторов воспаления
не только в суставах, но и в других органах
и тканях, в первую очередь в стенках сосудов. Исходя из
вышесказанного, становится ясно, что использование селективных
ингибиторов ЦОГ-2 имеет важное клиническое и социальное значение.
В клинической практике селективные ингибиторы ЦОГ-2 заняли прочное
место, хотя до сих пор не весь потенциал их возможностей используется
практическими врачами. Нередко возникают «мифы» об их потенциальной
токсичности, в первую очередь в отношении сердечно-сосудистой
системы. В западной литературе была опубликована информация
о гепатотоксичности нимесулидов, основанная на единичных
и плохо документированных клинических случаях. Эти аспекты
хотелось особо обсудить в данном сообщении, взяв в качестве
примера препарат «Найз».
Препарат «Найз» относится к селективным ингибиторам ЦОГ-2, что
доказано в исследованиях in vivo [7] и in vitro на
молекулярных моделях [6]. Кроме того, препарат обладает еще несколькими
важными механизмами действия (рис.). Наибольший опыт применения
препарата «Найз» в ревматологической практике в Российской
Федерации накоплен в лечении больных с ОА. Больные ОА, как
правило, имеют высокий риск развития желудочно-кишечных осложнений
в связи с возрастом, частым наличием сопутствующей
сосудистой, кардиальной, ренальной патологии и необходимостью
использовать сопутствующую терапию. Найз обычно используется этой
категорией больных в суточной дозе 200 мг/сутки. Это
обеспечивает достижение клинического эффекта у 87% [8] — 93%
[9] больных при хорошей переносимости Найза в отношении
желудочно-кишечного тракта, как по отечественным данным (табл. 1), так
и по данным зарубежных контролируемых исследований,
постмаркетингового изучения переносимости нимесулида в 17 странах
у 118 831 385 больных [10–13].


В нашем исследовании участвовало 40 больных с ОА
(32 больных) и с РА (8 больных), в возрасте от 49
до 79 лет (58,8 ± 18,3 года), страдающих
артериальной гипертензией более чем 5 лет, получающих стабильную
дозу антигипертензивных препаратов в течение не менее
6 месяцев, без явных проявлений сердечной недостаточности.
Большинство больных получали ингибиторы АПФ (эналаприл
10–30 мг/сутки) — 28 больных, β-адреноблокаторы
(пропранолол 20–40 мг/сутки) — 12 больных. Всем больным
после 3-дневного периода перерыва в приеме НПВП (ибупрофен,
мелоксикам, кетопрофен, диклофенак) назначался рандомизировано либо
диклофенак в дозе 100–150 мг/сутки, либо Найз в дозе
200–400 мг/сутки на 20 дней. АД регистрировалось 6 раз
в сутки: после пробуждения, перед первым приемом
антигипертензивных или нитратных препаратов, через 2 часа после их
приема и далее еще 3 раза с равными промежутками
в течение всего периода «отмывки», первую и последнюю неделю
приема НПВП, в остальное время исследования АД регистрировалось
4 раза в сутки каждые 3 часа с момента пробуждения.
Пациенты в течение периода исследования вели дневник
с указанием АД, приема антигипертензивных препаратов
и нежелательных реакций. Статистическая обработка проводилась
методом сопряженных пар.
Практически у всех больных обеих групп к концу периода
«отмывки» отмечалось увеличение среднесуточного АД (табл. 2). Тем
не менее, в течение 1-й недели лечения (табл. 2), различия
в среднем систолическом давлении были достоверно больше при приеме
диклофенака, а на фоне Найза практически не отличались от
исходного (p < 0,001). В меньшей степени на фоне
диклофенака в течение 1-й недели лечения увеличилось
среднесуточное диастолическое АД (ДАД) — на 3,31 ± 5,42;
увеличение этого параметра к концу 1-й недели лечения Найзом не
зарегистрировано. У 16 из 20 больных, получавших диклофенак,
отмечено негативное влияние препарата на течение артериальной
гипертензии — повышение систолического и/или диастолического
давления, сопровождавшееся неприятными субъективными ощущениями —
головная боль, кардиалгии (16), развитие гипертонического криза
(2 больных — отмена диклофенака через 6–14 дней приема),
увеличение потребности в приеме антигипертензивных препаратов
(6 больных). Среди больных, получавших Найз, не отмечено случаев
увеличения потребности в антигипертензивной терапии
и значимого изменения уровня АД, так что все 20 больных
закончили 3-недельный период лечения. Диклофенак был отменен
8 больным в связи с изменением течения артериальной
гипертензии: развитие гипертонического криза (2 пациента)
и нарастание уровня АД как систолического, так
и диастолического (2 больных), что потребовало увеличения
дозы эналаприла у обеих больных; у 2 больных
в связи с гастралгиями, у 1 больного из-за диареи;
у 1 больной из-за головной боли. Увеличение среднесуточного
систолического давления у больных, закончивших лечение
диклофенаком, было статистически достоверным и составило
15,74 ± 11,0; к концу лечения Найзом —
1,71 ± 5,22 (р > 0,05). Известно, что изменение
систолического АД (САД) является более важным фактором риска
кардиоваскулярной патологии, чем изменение ДАД [19]. Уменьшение уровня
САД на 12 мм рт. ст. снижает риск развития инфаркта миокарда на
27%, усугубления застойной сердечной недостаточности на 55%
и инсульта на 56% [19, 20].

Аналогичные результаты продемонстрированы в исследовании
В. И. Мазурова и соавт. [21], сравнивших гемодинамические
показатели у больных ОА (n = 40), имеющих
(23 пациента) или не имеющих (17 пациентов) сопутствующую
артериальную гипертензию (АГ), при назначении Найза или диклофенака на
1 месяц. Пациенты всех подгрупп были сопоставимы по локализации
ОА, рентгенологической стадии. Пациенты, имевшие ОА в сочетании
с АГ, были примерно на 10 лет старше больных
с нормальным уровнем АД. Доза Найза составляла 200 мг/сутки
и диклофенака — 100 мг/сутки. Для лечения АГ всем
больным второй подгруппы был назначен Ренитек (эналаприл) по
5–10 мг 2 раза в сутки. Всем больным до назначения НПВП
и через 1 месяц помимо клинического осмотра и оценки
боли (по шкале ВАШ) проводились ЭКГ, суточное мониторирование АД,
импедансометрическая кардиография (ИМК), определение уровня
десквамированных эндотелиоцитов в периферической крови по методике
Hladovec J. и соавт. (1978), определение состояния
эндотелий-зависимой и эндотелий-независимой (проба
с нитроглицерином) вазодилятации (ЭЗВД, ЭНВД соответственно)
плечевой артерии с помощью ультразвука высокого разрешения.
Через один месяц лечения статистически значимых различий
в уменьшении боли по ВАШ на фоне приема Найза или диклофенака не
отмечено (p > 0,05). Данные средних параметров суточного
мониторирования АД представлены в табл. 3 и 4.
При назначении Найза больным ОА без АГ (группа 1А) среднее суточное САД
и среднее дневное САД и ДАД повышались в пределах
нормальных значений без субъективных ощущений. В группе 1Б,
получавшей диклофенак, отмечено более значимое увеличение
систолического и ДАД, как среднесуточного, так
и среднедневного (p < 0,05), что сопровождалось
ухудшением самочувствия больных, а в одном случае
потребовалось назначение гипотензивной терапии.
В группе больных с ОА и АГ, получавших Найз (2А),
статистически значимого увеличения уровня АД не было зарегистрировано,
а при лечении диклофенаком (группа 2Б) достоверно увеличились
уровень среднесуточного САД (p < 0,01), среднедневного САД
(p < 0,05), при этом индекс площади САД за сутки
увеличился более чем в 2 раза (p < 0,05),
а ДАД — почти в 3 раза (p < 0,05), что
свидетельствует о стабильности повышения АД в течение суток.
Эти изменения АД сопровождались ухудшением самочувствия больных,
появлением одышки, отеков нижних конечностей, потребовалась коррекция
гипотензивной терапии (увеличение дозы Ренитека или применение
комбинированной терапии).
При изучении параметров системной гемодинамики в подгруппах
больных, получавших Найз, их существенных изменений выявлено не было.
В подгруппе пациентов с исходно нормальным уровнем АД,
получавших диклофенак, отмечалось достоверное (p < 0,05)
увеличение общего периферического сопротивления (ОПСС), снижение
параметров, отражающих общую производительность сердца: сердечный
индекс (СИ) и ударный индекс (УИ), а также существенное
увеличение объемов внеклеточной жидкости. Еще более значимая
отрицательная динамика показателей системной гемодинамики выявлена
у больных с АГ, получавших диклофенак. При сравнительном
исследовании влияния Найза и диклофенака на функцию эндотелия
у больных ОА с АГ было установлено, что прием Найза не влиял
на показатели ЭЗВД и ЭНВД, тогда как при лечении диклофенаком были
получены статистически значимые (p < 0,05) изменения ЭЗВД,
ЭНВД и количества десквамированных эндотелиоцитов. Эти данные
свидетельствуют, что неселективный ингибитор ЦОГ диклофенак достоверно
ухудшал функцию эндотелия, хотя механизмы такого влияния остаются
неясными и требуют дальнейшего изучения.
Эти данные еще раз подтверждают, что применение селективных ингибиторов
ЦОГ-2, к которым относится препарат «Найз», положительно влияют на
состояние эндотелия сосудов. У больных с риском развития
тромбозов эти препараты должны назначаться совместно с низкими
дозами Аспирина. Такое сочетание может привести к увеличению
частоты осложнений со стороны ЖКТ, поэтому эти больные должны тщательно
наблюдаться с эндоскопическим исследованием состояния ЖКТ
и мониторингом параметров гемодинамики, проведением
профилактических мероприятий (табл. 5).

Препарат «Найз» является эффективным противовоспалительным препаратом.
Как и для всех НПВП, его эффективность является дозозависимой. При
лечении больных ОА, как правило, бывает достаточным назначение его
в дозе 200 мг/сутки, что обеспечивает и анальгетический,
и противовоспалительный эффект. Как уже упоминалось выше, ЦОГ-2
ингибиторы в отличие от классических НПВП не оказывают
отрицательного влияния на суставной хрящ. Кроме того, нимесулид
в спектре своего механизма действия имеет ингибицию IL-1b [22],
ингибицию апоптоза хондроцитов [23], подавление активности
металлопротеаз [24], что подтверждает отсутствие у него
отрицательного влияния на суставной хрящ. При хронических
воспалительных заболеваниях суставов, таких как РА или псориатический
артрит (ПсА), выраженность синовита может во много раз превышать
таковую при ОА, что требует индивидуального подбора суточной дозы Найза
от 200 до 400 мг/сутки. Увеличение его эффективности при
увеличении суточной дозы при РА была показана отечественными авторами,
а при ПсА зарубежными авторами [25].
Таким образом, препарат «Найз» зарекомендовал себя активным НПВП, при
индивидуальном подборе его дозы количество больных «ответчиков»
достигает 93% в сочетании с хорошей переносимостью.
По вопросам литературы обращайтесь в редакцию.
Н. В. Чичасова, доктор медицинских наук, профессор
Г. Р. Имаметдинова
Е. Л. Насонов, доктор медицинских наук, профессор, академик РАМН
ММА им. И. М. Сеченова, Москва
Начну с реального положения вещей. Мой опыт работы с нимесулидом составляет более 10 лет – ровно столько, сколько я занимаюсь подагрой. Ежегодно в лаборатории микрокристаллических артритов проходят стационарное лечение не менее 80–100 больных с тяжелой хронической подагрой. Около 15–20 больных, в том числе повторных, каждую неделю консультируют сотрудники нашего отделения. Количество назначений нимесулида не поддается исчислению – оно огромно. Более того, примерно 300 больных мы включали в протоколы по исследованию различных аспектов эффективности и безопасности нимесулидов, результаты которых потом неоднократно публиковали. К сожалению, еще не напечатана одна крайне кропотливая работа А.Е. Каратеева, который провел своеобразный внутренний аудит, проанализировав около 80 историй болезней больных подагрой подряд по дате поступления, и показал отсутствие значимого подъема уровня печеночных ферментов даже у тех из них, у кого он вначале имелся.
За эти годы мы столкнулись с двумя серьезными реакциями. У одного больного произошел 30–кратный подъем уровня печеночных ферментов на 2–е сутки приема препарата (суммарная доза – 200 мг нимесулида), что, по нашему мнению, является классической идиосинкразией и не поддается прогнозированию и профилактике. От побочных реакций спасает только тщательный контроль в первые дни приема препарата, что является стандартом при назначении любого лекарственного средства. Второй больной самостоятельно бесконтрольно в течение 3–4 мес. принимал по 600 мг нимесулида вечером. Уровень печеночных ферментов поднялся в 10 раз, что мы расценили как последствие приема недопустимых в клинической практике, супервысоких доз нимесулида. Это исключительно произвол пациента, и нет никакой связи ни с лекарством, ни с врачами, так как ни один доктор не порекомендовал бы подобную схему лечения. «Не слишком ли мало нежелательных явлений для такого опыта?» – спросит скептик. Мы ответим ему следующим образом: при назначении любого препарата необходимо отчетливо представлять его фармакокинетику, фармакодинамику, взаимодействие с другими лекарствами и, главное, тщательно контролировать основные параметры безопасности лечения. Мы глубоко уверены, что все катастрофы случаются из–за недостаточно серьезного отношения к этим вопросам как врачей, так и больных.
Для себя мы выработали следующие правила назначения нимесулидов при подагре:
1) обязательно возьми биохимию до приема препарата!
Конечно, мы не можем ждать ее результата, так как боль при подагре крайне интенсивная, и, если ее быстро не снять, побочным эффектом может стать гипертонический криз и т.д.;
2) назначь повторный прием на 3–й день для оценки эффективности лечения и контроля биохимии. Кстати, такая тактика полезна при назначении любой терапии (будь то колхицин, глюкокортикоиды, аллопуринол, бензбромарон и т.д.) любому больному подагрой;
3) не сочетай нимесулид (и другие НПВП) с антикоагулянтами, мочегонными, антибиотиками, парацетамолом, НПВП и другими препаратами, метаболизирующимися печенью;
4) не назначай нимесулиды более 14 дней, придерживайся национальных рекомендаций по лечению. При эффективности препарата лечение может быть продолжено под жестким контролем печеночных ферментов и АД;
5) объясни больному, чего нужно ждать от препарата, и рекомендуй при малейшем подозрении на нежелательные явления обратиться к доктору и отменить препарат.
Кажется, просто, однако в реальной жизни применяется редко. Из–за несоблюдения этих простых правил появляются мифы об «ужасной гепатотоксичности» нимесулида в обсуждение этого вопроса 2 года назад была втянута медицинская общественность. Аналогичные истории случались и с другими препаратами: метформином и бензбромароном – прекрасными лекарствами, неумелое обращение с которыми приводило в лучшем случае к их компрометации, а в худшем – к запрету применения в ряде стран. Это неумелое обращение с препаратом чаще всего исходило от докторов, так как тщательное расследование конкретных клинических ситуаций обычно выявляло пренебрежение к противопоказаниям. В результате страдают больные. Так, в случае с бензбромароном новый препарат еще не пришел на рынок, а старый уже изгнали с позором, лишив медикаментозной поддержки тех, у кого аллопуринол не действует. В Испании, например, бензбромарон продается в аптеках только по рецептам врачей. Вероятнее всего, это сохранение эфемерной возможности для своих больных иметь препарат важнейшей группы при отсутствии альтернативы.
Вернемся к нимесулиду. В таблице 1 приведена краткая характеристика 11 случаев «гепатотоксичности» нимесулида, зарегистрированных в Ирландии, что послужило причиной рассмотрения этого вопроса Европейским медицинским агентством – EMEA (тогда было приведено 8 случаев). Именно этим количеством «смертельных случаев» оперировали оппоненты. Читатели могут убедиться в «реальности» этой ситуации самостоятельно на сайте http://patientsville.com/medication/nimesulide_side_effects.htm (рис. 1). Хотелось бы подчеркнуть, что данные сообщения дают медицинские организации.
При работе с этим сайтом я почувствовала себя Эркюлем Пуаро. При первом же посещении сайта вызвало удивление несколько фактов.
1. Доза и длительность приема нимесулида неизвестны. Больные принимали его самостоятельно? Вряд ли. Должен быть рецепт, запись в амбулаторной карте.
2. Огромное количество сопутствующих препаратов (от 3 до 7), причем ряд из них настойчиво не рекомендуется для сочетанного приема с нимесулидом. Неужели так низка осведомленность ирландских врачей, а ведь эта информация общедоступна.
3. Почему так много 56– и 61–летних женщин? Неужели мы свидетели нового открытия – полового и возрастного диморфизма нимесулида?
При подготовке таблицы я вдруг заметила то, чего не замечала 2 года:
1) у 4 женщин 61 года, в итоге погибших, разные номера подачи сведений, но дата практически одна, и принимали они одно и то же. Можно ли представить такую организованную диверсию в одной стране? Конечно нет! Это одна и та же женщина, она в моей таблице печальных событий выделена желтым цветом. Так что же получается? Умерло не 4 пациентки, а 1, что, при всем сочувствии к ее судьбе, практически реабилитирует препарат;
2) четыре 56–летние женщины (выделены голубым цветом), без сомнения, – вновь одна и та же женщина. Даты близки. Почему исход разный: выздоровление или пересадка печени? Думаю, что данные на сайт подавались разными инстанциями.
Итак, по моим скромным подсчетам, количество больных уменьшилось до 5. Зародилось сомнение в непредвзятом отношении к нимесулиду в Ирландии в октябре–ноябре 2008 г., так как именно ему приписывают возникшие осложнения, хотя больные одновременно принимали целый букет метаболизирующихся в печени лекарств.
Давайте обратимся к другим серьезным источникам. Их много, я процитирую три. На рисунке 2 – отчет разработчика нимесулида Helsinn Healthcare. В конце текста приведена частота гепатотоксичности: 0,1 на 100 тыс. пролеченных больных. Может быть, предвзято?
На рисунке 3 видим другой источник – испанский регистр. В нем нимесулид не на 1–м месте по гепатотоксичности. Аналогичных данных громадное количество, все–таки более 10 лет прошло после внедрения нимесулида в практику – именно столько времени надо, по мнению специалистов–фармакологов, чтобы окончательно стали понятны все нежелательные явления препарата. Ведь клинические испытания несколько рафинированы и не всегда выявляют весь спектр побочных эффектов.
В реальной жизни, как свидетельствует представленная на сайте информация, нарушаются показания, длительность приема, не учитывается возможность сочетания с другими препаратами. Кстати, если серьезно анализировать приведенные случаи гепатотоксичности, что, кстати, делают ведущие специалисты в этой области, публикуя в последующем свои комментарии, то практически всегда выявляются нарушения при назначении препарата, чаще всего это касается длительности приема и сочетания с другими препаратами. Но тогда возникает вопрос: а при чем тут нимесулид? Речь–то идет о «токсичности» невнимательных докторов для больных.
Заслуживает внимания самое большое эпидемиологическое исследование, выполненное G. Traversa и соавт., данные которого опубликованы в 2003 г.: более 2 млн назначений нимесулида по сравнению с другими НПВП в реальной клинической практике. Исследование показало, что у принимавших нимесулид был низкий риск госпитализации из–за острой печеночной недостаточности, а уж случаев смерти или трансплантации не наблюдалось вовсе, в отличие от ирландского опыта.
Совершенно предсказуемо, что EMEA после рассмотрения поднятых вопросов признало соотношение «преимущество/риск» у нимесулида благоприятным.
Наконец, хотелось бы высказать мнение о гепатотоксичности в принципе и нимесулида в частности. Мое мнение не оригинально, и в конце статьи приведены авторы, с которыми я солидарна.
Что такое вообще
гепатотоксичность лекарств?
Доктора видят широкий диапазон проявлений гепатотоксичности: от умеренной дисфункции (транзиторный подъем уровня аминотрансфераз при отсутствии признаков повреждения паренхимы печени является адаптивным ответом на лекарство) до серьезных побочных эффектов (холестаз, печеночный некроз, фульминантый гепатит).
Как и у кого можно предсказать тяжесть этих реакций? Нельзя предсказать. И это отражает наше неполное понимание сути лекарственной гепатотоксичности. Хорошо известны такие факторы, как нарушение гепатобилиарных, почечных механизмов экскреции в связи с длительным применением препарата или высокими его дозами. Очевидно также, что биотрансформация препарата – это ворота для продукции реактивных метаболитов, реагирующих с печеночными клетками. В результате развиваются ковалентное связывание, оксидативный стресс, повреждение митохондрий, апоптоз. Можно рассчитать риск развития нежелательного явления, основываясь на фармакокинетике, но нельзя рассчитать (пока?) вклад «человеческого фактора – Х». Что он может в себя включать? Наследственный порок генов, кодирующих биоактивирующие ферменты, или усиление экспрессии генов, а также эпигенетические факторы, влияющие на метаболизм лекарства: собственно болезнь, инфекции, полипрагмазия, защитные и восстановительные системы, иммунная толерантность. Именно эти факторы и ответственны за развитие идиосинкразии (патологическая реакция на лекарство, детерминированная генетическими или приобретенными факторами, редкая, манифестная лишь у небольшого количества больных с врожденной биореактивностью на компоненты препарата, которую нельзя воспроизвести в эксперименте).
Гепатотоксичность НПВП
vs нимесулид
Я не планировала касаться механизмов гепатотоксичности НПВП в целом, укажу лишь несколько факторов гепатотоксичности, которых нимесулид лишен в отличие от других НПВП:
1) не содержит карбоксильную группу;
2) не метаболизируется до карбоксильной кислоты;
3) не подвергается конъюгированию до реактивного ацилглюкуронида.
Чтобы читатели не обвинили меня в пристрастности (хотя я и предпочитаю назначать нимесулиды больным подагрой), приведу потенциальные механизмы гепатотоксичности нимесулида, которые, однако, показаны только in vitro и не воспроизведены in vivo:
1) нитроредукция (показана у других НПВП, у нимесулида – только in vitro, что означает на практике одно – большие дозы);
2) нитроароматические компоненты метаболизма нимесулида приводят к оксидативному стрессу. Нитроредуктазы локализуются в цитозоле, эндоплазматическом ретикулуме и митохондриях и в анаэробных условиях образуют супероксидные анионные радикалы (показано только in vitro);
3) ковалентная связь с белком: метаболиты нимесулида (общее с сульфонамидными препаратами) подвергаются многоступенчатой редукции. Реактивные нитрозо– и гидроксиламины электрофильны истощают глутатион и формируют ковалентные связи с белком. Но они короткоживущие, и это не было продемонстрировано in vivo.
Что такое «серьезная
гепатотоксичность» нимесулида?
Идиосинкразия с генетической подоплекой: гомо– или гетерозиготность по аллелям гена Р450 (?), NAT–фенотип медленной ацетилизации (?).
Мне ни разу не задавали вопрос: если не с гепатотоксичностью, то с какими проблемами при назначении нимесулидов я столкнулась? Поэтому я задала его себе сама и ответила: биоэквивалентность генерических форм, количество которых растет. Почему? Может происходить снижение эффективности. Об этой проблеме мы говорим открыто, но неохотно пишем; в отношении нимесулидов такое опасение открыто высказал K. Rainsford. Об этом мало пишут и редко сравнивают «лоб в лоб» различные препараты.
Мое опасение основано на результатах тех исследований, которые мы проводили в разные годы у больных подагрой, все они опубликованы. После исследования скорости анальгезии двух форм нимесулида – гранулированной и таблетированной, – показавшего, что она различается, я никак не могла найти объяснение такой разнице. Фармакокинетика эту разницу не объясняла. Один мой коллега, после того как я сделала доклад на эту тему, объяснил результат отсутствием биоэквивалентности. Это последнее, на что мне хотелось бы ссылаться в тот момент. В дальнейшем мы провели еще один эксперимент. Взяли уже две таблетированные формы – и тот же результат. Если провести метаанализ приведенных наших работ, то можно увидеть, что одинаково зарекомендовали себя гранулированный нимесулид и одна из таблетированных форм (Найз). К сожалению, два других таблетированных нимесулида им проигрывали. Учитывая большую разницу в стоимости гранулированной и таблетированной форм, не могу не согласится с А.Е. Каратеевым, метко назвавшим Найз «антикризисным анальгетиком».
В конце статьи хочу еще раз отметить, что нимесулид мы используем более 10 лет и за это время он доказал свою эффективность и безопасность при соблюдении рекомендаций по его назначению. Контролировать прием нимесулида нужно так же, как и других препаратов в начале лечения.
В заключение я хочу выразить надежду, что нимесулиды больше не принесут нам никаких потрясений и будут и дальше солидным подспорьем в нашей практике.
Статья опубликована в журнале
«Современная ревматология», 2010, №3: 80–84
