Блок ротации кондиционеров SB015 предназначен для управления работой сплит-систем, установленных в серверной комнате или в аналогичных помещениях. SB015 предназначен для коммутации 2-х сплит-систем. Управляемые сплит-системы должны иметь функцию “АВТОРЕСТАРТ”.
Блок ротации легок в настройке. Инструкция на SB015 прилагается в комплекте с блоком. Гарантийный срок на блок ротации SB015 составляет 12 месяцев.
Наш сервисный центр производит установку блоков ротации. Стоимость стандартного монтажа и настройки – 5.000 руб.
ВНИМАНИЕ! АКЦИЯ!
Цена SB015 – 10.900 руб.
(количество товара ограничено)
Доставка блока ротации по Москве (390 руб.) и в регионы.
В качестве альтернативы можно использовать блок ротации кондиционеров УРК-2Т (имеет дополнительные функции, ЖК дисплей и многое другое).

Блок ротации кондиционеров SB015
Вы можете скачать Руководство по эксплуатации SB015.pdf

Вы можете купить устройство ротации SB015 в Москве,
Краснодаре, Санкт-Петербурге, Якутске, Сочи, Майкопе и д.р. городах.
Зайдите на страницу Ваш город.
Описание препарата Саксенда® (раствор для подкожного введения, 6 мг/мл) основано на официальной инструкции, утверждено компанией-производителем в 2021 году
Дата согласования: 20.08.2021
Особые отметки:
Содержание
- Фотографии упаковок
- Действующее вещество
- ATX
- Фармакологическая группа
- Нозологическая классификация (МКБ-10)
- Состав
- Описание лекарственной формы
- Фармакологическое действие
- Фармакодинамика
- Фармакокинетика
- Показания
- Противопоказания
- Применение при беременности и кормлении грудью
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Передозировка
- Особые указания
- Форма выпуска
- Производитель
- Условия отпуска из аптек
- Условия хранения
- Срок годности
- Аналоги (синонимы) препарата Саксенда®
- Заказ в аптеках Москвы
Фотографии упаковок

20.08.2021
20.08.2021
Действующее вещество
ATX
Фармакологическая группа
Состав
| Раствор для подкожного введения | 1 мл |
| действующее вещество: | |
| лираглутид | 6 мг |
| (в одной предварительно заполненной шприц-ручке объемом 3 мл содержится 18 мг лираглутида) | |
| вспомогательные вещества: натрия гидрофосфата дигидрат; фенол; пропиленгликоль; натрия гидроксид/кислота хлористоводородная (для коррекции рН); вода для инъекций |
Описание лекарственной формы
Прозрачный, бесцветный или почти бесцветный раствор.
Фармакологическое действие
Фармакологическое действие
—
гипогликемическое.
Фармакодинамика
Действующее вещество препарата Саксенда® — лираглутид — представляет собой ацилированный аналог человеческого ГПП-1, произведенный методом биотехнологии рекомбинантной ДНК с использованием штамма Saccharomyces cerevisiae, имеющий 97% гомологичности аминокислотной последовательности эндогенному человеческому ГПП-1. Лираглутид связывается и активирует рецептор ГПП-1 (ГПП-1Р). Лираглутид устойчив к метаболическому распаду, его T1/2 из плазмы после п/к введения составляет 13 ч. Фармакокинетический профиль лираглутида, позволяющий вводить его пациентам 1 раз в сутки, является результатом самоассоциации, в результате которой происходит замедленное всасывание препарата, связывания с белками плазмы, а также устойчивости к ДПП-4 и нейтральной эндопептидазе (НЭП).
ГПП-1 является физиологическим регулятором аппетита и потребления пищи, а ГПП-1Р расположены в нескольких областях головного мозга, участвующих в процессах регуляции аппетита. В исследованиях на животных периферическое введение лираглутида приводило к захвату препарата в специфических областях головного мозга, включая гипоталамус, где лираглутид посредством специфической активации ГПП-1Р усиливал сигналы насыщения и ослаблял сигналы голода, тем самым приводя к уменьшению массы тела.
ГПП-1Р представлены также в специфических областях сердца, сосудов, иммунной системы и почек. В экспериментах на мышах с атеросклерозом лираглутид предупреждал дальнейшее развитие аортальных бляшек и снижал в них воспаление. В дополнение лираглутид оказывал благоприятный эффект на липиды в плазме. Лираглутид не уменьшал размер уже существующих бляшек.
Лираглутид уменьшает массу тела у человека преимущественно посредством уменьшения массы жировой ткани. Уменьшение массы тела происходит за счет уменьшения потребления пищи. Лираглутид не увеличивает 24-часовой расход энергии. Лираглутид регулирует аппетит с помощью усиления чувства наполнения желудка и насыщения, одновременно ослабляя чувство голода и уменьшая предполагаемое потребление пищи. Лираглутид стимулирует секрецию инсулина и уменьшает неоправданно высокую секрецию глюкагона глюкозозависимым образом, а также улучшает функцию бета-клеток поджелудочной железы, что приводит к снижению концентрации глюкозы натощак и после приема пищи. Механизм снижения концентрации глюкозы также включает небольшую задержку опорожнения желудка.
В долгосрочных клинических исследованиях (КИ) с участием пациентов с избыточной массой тела или ожирением применение препарата Саксенда® в сочетании с низкокалорийной диетой и усиленной физической активностью приводило к значительному снижению массы тела.
Влияние на аппетит, потребление калорий, расход энергии, опорожнение желудка и концентрацию глюкозы натощак и после приема пищи
Фармакодинамические эффекты лираглутида изучались в 5-недельном фармакологическом КИ с участием 49 пациентов с ожирением (ИМТ — 30–40 кг/м2) без сахарного диабета (СД).
Аппетит, потребление калорий и расход энергии
Считается, что снижение массы тела при применении препарата Саксенда® связано с регулированием аппетита и количества потребляемой пищи. Аппетит оценивали перед и в течение 5 ч после стандартизированного завтрака; неограниченное потребление пищи оценивали во время последующего обеда. Препарат Саксенда® увеличивал чувство насыщения и наполнения желудка после приема пищи и уменьшал чувство голода и оценочное количество предполагаемого потребления пищи, а также уменьшал неограниченное потребление пищи по сравнению с плацебо. При оценке с помощью респираторной камеры не было отмечено связанного с терапией увеличения 24-часового расхода энергии.
Опорожнение желудка
Применение препарата Саксенда® приводило к небольшой задержке опорожнения желудка в течение первого часа после приема пищи, в результате чего уменьшалась скорость повышения концентрации, а также общая концентрация глюкозы крови после приема пищи.
Концентрация глюкозы, инсулина и глюкагона натощак и после приема пищи
Концентрацию глюкозы, инсулина и глюкагона натощак и после приема пищи оценивали перед и в течение 5 ч после стандартизированного приема пищи. По сравнению с плацебо препарат Саксенда® уменьшал концентрацию глюкозы крови натощак и после приема пищи (AUC0–60 мин) в течение первого часа после приема пищи, а также уменьшал 5-часовую AUC глюкозы и нарастающую концентрацию глюкозы (AUC0–300 мин). Кроме того, препарат Саксенда® уменьшал постпрандиальную концентрацию глюкагона (AUC0–300 мин) и инсулина (AUC0–60 мин) и нарастающую концентрацию инсулина (iAUC0–60 мин) после приема пищи по сравнению с плацебо.
Концентрации глюкозы и инсулина натощак и нарастающие концентрации глюкозы и инсулина также оценивали во время перорального теста толерантности к глюкозе (ПТТГ) с 75 г глюкозы перед и через 1 год терапии у 3731 пациента с избыточной массой тела и ожирением, а также наличием или отсутствием предиабета. По сравнению с плацебо препарат Саксенда® уменьшал концентрацию глюкозы натощак и нарастающую концентрацию глюкозы. Эффект был более выраженным у пациентов с предиабетом. Кроме того, препарат Саксенда® уменьшал концентрацию инсулина натощак и увеличивал нарастающую концентрацию инсулина по сравнению с плацебо.
После 160 нед продолжающейся терапии лираглутидом в дозе 3,0 мг AUC глюкозы плазмы снизилась, в то время как при применении плацебо оставалась неизменной. Дополнительно AUC инсулина оставалась относительно стабильной в течение 160-недельного периода лечения лираглутидом в дозе 3,0 мг, в то время как при применении плацебо наблюдалось ее снижение. Все изученные эффекты от проводимой терапии были статистически значимыми в пользу лираглутида, 3,0 мг.
Влияние на концентрацию глюкозы натощак и нарастающую концентрацию глюкозы у пациентов с сахарным диабетом типа 2 (СД2) с избыточной массой тела и ожирением
Препарат Саксенда® снижал концентрацию глюкозы натощак и среднюю нарастающую постпрандиальную концентрацию глюкозы (через 90 мин после приема пищи, среднее значение для 3 приемов пищи в сутки) по сравнению с плацебо.
Функция бета-клеток поджелудочной железы
КИ продолжительностью до одного года с применением препарата Саксенда® у пациентов с избыточной массой тела и СД или без такового продемонстрировали улучшение и сохранение функции бета-клеток поджелудочной железы при использовании таких методов измерения, как гомеостатическая модель оценки функции бета-клеток (НОМА-В) и соотношение концентраций проинсулина и инсулина.
Клиническая эффективность и безопасность
Эффективность и безопасность применения препарата Саксенда® для длительной коррекции массы тела в сочетании с низкокалорийной диетой и усилением физической активности была изучена в 4 рандомизированных двойных слепых плацебо-контролируемых исследованиях 3-й фазы SCALE, включавших в общей сложности 5358 взрослых пациентов.
Масса тела
По сравнению с плацебо при применении препарата Саксенда® было достигнуто более выраженное снижение массы тела у пациентов с ожирением/избыточной массой тела во всех исследованных группах, в т.ч. с наличием или отсутствием предиабета, СД2 и обструктивным апноэ во сне средней или тяжелой степени. Кроме того, среди популяции исследования бóльшая часть пациентов достигла снижения массы тела ≥5% и >10% при применении препарата Саксенда® по сравнению с плацебо.
Значительное снижение массы тела наблюдалось также в КИ, в котором пациенты достигли среднего показателя снижения массы тела 6,0% с помощью низкокалорийной диеты в течение 12 нед до начала лечения препаратом Саксенда®. В этом исследовании бóльшее количество пациентов сохранили потерю массы тела, которая была достигнута до начала лечения препаратом Саксенда®, по сравнению с группой плацебо (81,4% и 48,9% соответственно).
Рисунок 1. Изменение массы тела (%) у пациентов в динамике по сравнению с исходным значением в исследовании №1 (0–56 нед).
В КИ длительностью 160 нед пациенты, получавшие препарат Саксенда®, достигли более значительной потери массы тела по сравнению с пациентами, получавшими плацебо. В основном потеря массы тела произошла в первый год и удерживалась на протяжении 160 нед.
В КИ длительностью 160 нед средний процент изменения массы тела и доля пациентов, достигших потери массы тела от исходного значения до 160-й нед не менее чем на 5% и не более 10%, были также значительными по сравнению с плацебо.
Снижение массы тела после 12 нед терапии препаратом Саксенда® (лираглутид 3,0 мг). В двух исследованиях продолжительностью 56 недель после 12 нед терапии препаратом Саксенда® в дозе 3,0 мг 67,5% и 50,4% пациентов достигли снижения массы тела не менее чем на 5%. Среднее снижение массы тела у этих пациентов, завершивших исследование, составило 11,2% по сравнению с исходным значением. У пациентов, достигших снижения массы тела менее чем на 5% после 12 нед терапии в дозе 3,0 мг и завершивших исследование (1 год), среднее снижение массы тела составило 3,8%.
Контроль гликемии
Терапия лираглутидом существенно улучшала гликемические показатели в субпопуляциях с нормогликемией, предиабетом и СД2.
СД2 развился у 0,2% пациентов, получавших препарат Саксенда®, по сравнению с 1,1% в группе плацебо. У 69,2% пациентов с предиабетом наблюдалось обратное развитие этого состояния при применении препарата Саксенда® по сравнению с 32,7% в группе плацебо. На 160-й нед при продолжении лечения диагноз СД2 был поставлен 3% пациентов, получавшим препарат Саксенда®, и 11% пациентов, получавшим плацебо. По сравнению с плацебо время до развития СД2 при применении лираглутида в дозе 3,0 мг было в 2,7 раза больше, а ОР развития СД2 при применении лираглутида равен 0,2. На 160-й нед в группе лираглутида 3,0 мг у 65,9% пациентов с предиабетом наблюдалось обратное развитие этого состояния до нормогликемии по сравнению с 36,3% в группе плацебо.
В одном из исследований 69,2% и 56,5% пациентов с ожирением и СД2, получавших препарат Саксенда®, достигли целевого значения HbA1c <7% и ≤6,5% соответственно по сравнению с 27,2% и 15,0% у пациентов, получавших плацебо.
Кардиометаболические параметры
По сравнению с плацебо препарат Саксенда® значительно улучшал показатели сАД, окружности талии и концентрации липидов натощак.
В КИ длительностью 160 нед среднее уменьшение окружности талии составило 8,2 см при применении препарата Саксенда® и 4,0 см при применении плацебо; уменьшение показателей сАД и дАД составило 4,3 мм рт.ст. и 1,5 мм рт.ст. при применении препарата Саксенда® и 2,7 мм рт.ст. и 1,8 мм рт.ст. при применении плацебо соответственно; уменьшение концентрации Хс-ЛПНП составило 3,1 ммоль/л при применении препарата Саксенда® и 0,7 ммоль/л при применении плацебо; увеличение концентрации Хс-ЛПВП составило 2,3 ммоль/л при применении препарата Саксенда® и 0,5 ммоль/л при применении плацебо.
Индекс апноэ-гипноэ (ИАГ)
По сравнению с плацебо при применении препарата Саксенда® наблюдалось существенное снижение тяжести обструктивного апноэ во сне, которая оценивалась по изменению ИАГ относительно исходного значения.
Иммуногенность
Вследствие потенциальных иммуногенных свойств белковых и пептидных лекарственных препаратов у пациентов могут появиться антитела к лираглутиду после терапии препаратом Саксенда®. В КИ у 2,5% пациентов, получавших препарат Саксенда®, появились антитела к лираглутиду. Образование антител не привело к снижению эффективности препарата Саксенда®.
Оценка сердечно-сосудистых событий
Большие сердечно-сосудистые события (БССС) были оценены группой внешних независимых экспертов и определены как инфаркт миокарда без смертельного исхода, инсульт без смертельного исхода и смерть по причине сердечно-сосудистой патологии. В 5 двойных слепых контролируемых КИ 2-й и 3-й фазы с применением препарата Саксенда® было отмечено 6 БССС у пациентов, получавших препарат Саксенда®, и 10 БССС — у получавших плацебо пациентов. ОР с 95% ДИ составил 0,33 при применении препарата Саксенда® по сравнению с плацебо. В КИ 3-й фазы среднее увеличение ЧСС составило 2,5 уд./мин у пациентов, получавших препарат Саксенда®. Наибольшее увеличение ЧСС наблюдалось после 6 нед терапии. Это увеличение было обратимым и исчезало после прекращения терапии лираглутидом.
Было проведено многоцентровое плацебо-контролируемое двойное слепое КИ «Эффект и воздействие лираглутида при сахарном диабете: оценка сердечно-сосудистых рисков» (LEADER®).
По сравнению с плацебо лираглутид 1,8 мг существенно снижал риск развития БССС (рис. 2). ОР развития БССС был стабильно ниже 1 для всех 3 сердечно-сосудистых событий.
Рисунок 2. График Каплана-Мейера — время до возникновения первого БССС — популяция полного анализа (ППА).
Лираглутид 1,8 мг также существенно снижал риск развития расширенных БССС (первичные БССС, нестабильная стенокардия, приводящая к госпитализации, реваскуляризация миокарда или госпитализация по причине сердечной недостаточности) и прочих вторичных конечных точек.
Дети и подростки. В двойном слепом КИ, сравнивающем эффективность и безопасность препарата Саксенда® в сравнении с плацебо в отношении снижения массы тела у подростков в возрасте 12 лет и старше с ожирением, препарат Саксенда® превосходил плацебо в снижении стандартного отклонения ИМТ (измеренного для оценки снижения массы тела) после 56 недель лечения. Большее количество пациентов достигло ≥5% и ≥10% снижения ИМТ на терапии лираглутидом, чем пациенты, получавшие плацебо, при более значительном снижении среднего ИМТ и массы тела. В течение 26 недель последующего наблюдения без применения препарата наблюдалось восстановление массы тела при применении препарата Саксенда® по сравнению с плацебо (оценивалось как изменение стандартного отклонения ИМТ).
Исходя из переносимости, для большинства пациентов (82,4%) доза препарата была увеличена, и они продолжили получать дозу 3,0 мг, для остальных пациентов доза была увеличена, и они продолжили получать препарат в диапазоне доз от 2,4 мг до 0,6 мг.
Результаты определяемых пациентами показателей
Препарат Саксенда® по сравнению с плацебо улучшал определяемые пациентами оценки по нескольким показателям. Было отмечено значительное улучшение общей оценки по упрощенному опроснику влияния массы тела на качество жизни (IWQoL-Lite) и по всем шкалам опросника для оценки качества жизни SF-36, что указывает на положительное влияние на физический и психологический компоненты качества жизни.
Фармакокинетика
Всасывание. Всасывание лираглутида после п/к введения происходит медленно, Tmax — около 11 ч после введения. У пациентов с ожирением (ИМТ 30–40 кг/м2) после введения лираглутида в дозе 3,0 мг средняя равновесная концентрация лираглутида (AUCτ/24 ч) достигает приблизительно 31 нмоль/л. В диапазоне доз от 0,6 мг до 3,0 мг экспозиция лираглутида увеличивается пропорционально дозе. Абсолютная биодоступность лираглутида после п/к введения составляет приблизительно 55%.
Распределение. Средний кажущийся Vd после п/к введения лираглутида в дозе 3,0 мг составляет 20–25 л (у лиц с массой тела около 100 кг). Лираглутид в значительной степени связывается с белками плазмы крови (>98%).
Метаболизм. На протяжении 24 ч после введения здоровым добровольцам однократной дозы [3Н]-лираглутида главным компонентом в плазме оставался неизмененный лираглутид. Были обнаружены 2 метаболита (≤9% и ≤5% от уровня общей радиоактивности в плазме крови).
Выведение. Лираглутид метаболизируется эндогенно, подобно крупным белкам, без участия какого-либо специфического органа в качестве основного пути выведения. После введения дозы [3Н]-лираглутида неизмененный лираглутид не определялся в моче или кале. Лишь незначительная часть введенной радиоактивности в виде метаболитов лираглутида выводилась почками или через кишечник (6% и 5% соответственно). Радиоактивные вещества выделяются почками или через кишечник, в основном в течение первых 6–8 дней, и представляют собой 3 метаболита.
Средний клиренс после п/к введения лираглутида составляет приблизительно 0,9–1,4 л/ч, T1/2 составляет примерно 13 ч.
Особые группы пациентов
Пожилой возраст. Коррекция дозы с учетом возраста не требуется. Согласно результатам популяционного фармакокинетического анализа у пациентов с ожирением и избыточной массой тела в возрасте 18–82 лет, возраст не оказывал клинически значимое влияние на фармакокинетику лираглутида при п/к введении в дозе 3,0 мг.
Пол. Основываясь на данных популяционного фармакокинетического анализа, у женщин скорректированный по массе тела клиренс лираглутида после п/к введения в дозе 3,0 мг на 24% меньше, чем у мужчин. На основании данных по ответной реакции на воздействие препарата, коррекция дозы с учетом пола не требуется.
Этническая принадлежность. Согласно результатам популяционного фармакокинетического анализа, в который были включены данные исследований у пациентов с ожирением и избыточной массой тела европеоидной, негроидной, азиатской и латиноамериканской расовых групп, этническая принадлежность не оказывала клинически значимое влияние на фармакокинетику лираглутида при п/к введении в дозе 3,0 мг.
Масса тела. Экспозиция лираглутида уменьшается при увеличении исходной массы тела. Применение лираглутида в дозе 3,0 мг ежедневно обеспечивает адекватную экспозицию в диапазоне массы тела 60–234 кг, согласно оценке ответной реакции на системную экспозицию препарата в КИ. Экспозицию лираглутида у пациентов с массой тела больше 234 кг не изучали.
Печеночная недостаточность. Фармакокинетику лираглутида оценивали у пациентов с различной степенью нарушения функции печени в исследовании однократной дозы (0,75 мг). Наблюдалось снижение экспозиции лираглутида на 13–23% у пациентов с печеночной недостаточностью легкой и средней степени тяжести и значительное снижение экспозиции лираглутида (на 44%) у пациентов с печеночной недостаточностью тяжелой степени (>9 баллов по классификации Чайлд-Пью) в сравнении со здоровыми добровольцами.
Почечная недостаточность. В исследовании однократной дозы (0,75 мг) экспозиция лираглутида была меньше у пациентов с почечной недостаточностью по сравнению с лицами с нормальной функцией почек. Экспозиция лираглутида была меньше на 33%, 14%, 27% и 26% соответственно у пациентов с почечной недостаточностью легкой (Cl креатинина 50–80 мл/мин), средней (30–50 мл/мин), тяжелой степени (<30 мл/мин) и с терминальной стадией почечной недостаточности, нуждающихся в гемодиализе.
Дети и подростки. Фармакокинетические свойства лираглутида 3,0 мг оценивались в КИ у подростков от 12 до 18 лет с ожирением (134 пациента, масса тела 62–178 кг). Экспозиция лираглутида у подростков в возрасте от 12 до 18 лет была сопоставима с наблюдаемой у взрослых пациентов с ожирением. Фармакокинетические свойства были также оценены в клиническом фармакологическом исследовании с участием детей от 7 до 11 лет с ожирением (13 пациентов, масса тела 54–87 кг). Экспозиция лираглутида 3,0 мг у детей от 7 лет до 11 лет была сопоставима с наблюдаемой у взрослых пациентов после поправки на массу тела.
Показания
В качестве дополнения к низкокалорийной диете и усиленной физической нагрузке для длительного применения с целью коррекции массы тела у взрослых пациентов с ИМТ:
— ≥30 кг/м2 (ожирение);
— от ≥27 кг/м2 до <30 кг/м2 (избыточная масса тела) при наличии хотя бы одного связанного с избыточной массой тела сопутствующего заболевания/состояния (такого как предиабет, сахарный диабет типа 2, артериальная гипертензия, дислипидемия или синдром обструктивного апноэ во сне.
В качестве дополнения к здоровому питанию и усиленной физической нагрузке с целью коррекции массы тела у подростков в возрасте от 12 лет и старше с:
— массой тела свыше 60 кг и ожирением (ИМТ, соответствующий ≥30 кг/м2 для взрослых согласно международным пороговым значениям — пороговое значение ИМТ IOTF для ожирения в зависимости от пола в возрасте от 12 лет до 18 лет (см. таблицу 1).
Таблица 1
Пороговое значение ИМТ IOTF для ожирения в зависимости от пола и возраста от 12 до 18 лет
| Возраст (количество лет) | ИМТ, 30 кг/м2 | |
| Мужкой пол | Женский пол | |
| 12 | 26,02 | 26,67 |
| 12,5 | 26,43 | 27,24 |
| 13 | 26,84 | 27,76 |
| 13,5 | 27,25 | 28,20 |
| 14 | 27,63 | 28,57 |
| 14,5 | 27,98 | 28,87 |
| 15 | 28,30 | 29,11 |
| 15,5 | 28,60 | 29,29 |
| 16 | 28,88 | 29,43 |
| 16,5 | 29,14 | 29,56 |
| 17 | 29,41 | 29,69 |
| 17,5 | 29,70 | 29,84 |
| 18 | 30,00 | 30,00 |
Противопоказания
- гиперчувствительность к лираглутиду или любому из вспомогательных компонентов препарата;
- медуллярный рак щитовидной железы в анамнезе, в т.ч. семейном;
- множественная эндокринная неоплазия II типа;
- тяжелая депрессия, суицидальные мысли или поведение, в т.ч. в анамнезе.
Противопоказано применение у следующих групп пациентов и при следующих состояниях/заболеваниях в связи с отсутствием данных по эффективности и безопасности:
- почечная недостаточность тяжелой степени (Cl креатинина <30 мл/мин);
- печеночная недостаточность тяжелой степени;
- пациенты в возрасте ≥75 лет;
- хроническая сердечная недостаточность (ХСН) IV функционального класса (в соответствии с классификацией NYHA);
- одновременное применение других препаратов для коррекции массы тела;
- применение в комбинации с другими агонистами рецепторов ГПП-1;
- вторичное ожирение на фоне эндокринологических заболеваний или расстройств пищевого поведения, или на фоне применения лекарственных препаратов, которые могут привести к увеличению массы тела;
- период беременности;
- период грудного вскармливания;
- подростки в возрасте от 12 до 18 лет с массой тела меньше или равной 60 кг
- детский возраст до 12 лет.
У пациентов с сахарным диабетом препарат Саксенда® не должен применяться в качестве заменителя инсулина.
Опыт применения препарата Саксенда® у пациентов с воспалительными заболеваниями кишечника и диабетическим парезом желудка ограничен. Применение лираглутида у таких пациентов не рекомендуется, поскольку оно связано с транзиторными нежелательными реакциями со стороны ЖКТ, включая тошноту, рвоту и диарею.
С осторожностью: пациенты с печеночной недостаточностью легкой и средней степени тяжести, заболеваниями щитовидной железы и наличием острого панкреатита в анамнезе.
Применение при беременности и кормлении грудью
Беременность. Данные по применению препарата Саксенда® у беременных женщин ограничены. В исследованиях на животных была продемонстрирована репродуктивная токсичность (см. Доклинические данные по безопасности). Потенциальный риск для человека неизвестен.
Применение препарата Саксенда® в период беременности противопоказано. При планировании или наступлении беременности терапию препаратом Саксенда® необходимо прекратить.
Период грудного вскармливания. Неизвестно, проникает ли лираглутид в грудное молоко у женщин. В исследованиях на животных было продемонстрировано, что проникновение лираглутида и структурно близких метаболитов в грудное молоко является низким. В доклинических исследованиях было продемонстрировано связанное с терапией замедление роста новорожденных крысят, находящихся на грудном вскармливании. В связи с отсутствием опыта применения, препарат Саксенда® противопоказан во время грудного вскармливания.
Способ применения и дозы
Реклама: ООО «РЛС-Патент», ИНН 5044031277, erid=4CQwVszH9pUkpHxmQQo
П/к. Препарат нельзя вводить в/в или в/м.
Препарат Саксенда® вводят один раз в сутки в любое время, независимо от приема пищи. Его следует вводить в область живота, бедра или плеча. Место и время инъекции могут быть изменены без коррекции дозы. Тем не менее желательно делать инъекции примерно в одно и то же время суток после выбора наиболее удобного времени.
Дозы. Начальная доза составляет 0,6 мг/сут. Дозу увеличивают до 3,0 мг/сут, прибавляя по 0,6 мг с интервалами не менее 1 нед для улучшения желудочно-кишечной переносимости (см. таблицу 2).
Если при увеличении дозы новая плохо переносится пациентом в течение 2 нед подряд, следует рассмотреть вопрос о прекращении терапии. Применение препарата в суточной дозе больше 3,0 мг не рекомендуется.
Таблица 2
Схема увеличения дозы
| Показатели | Доза, мг | Недели |
| Увеличение дозы в течение 4 нед | 0,6 | 1-я |
| 1,2 | 2-я | |
| 1,8 | 3-я | |
| 2,4 | 4-я | |
| Терапевтическая доза | 3,0 |
Взрослые. Терапию препаратом Саксенда® следует прекратить, если после 12 недель применения препарата в дозе 3,0 мг/сут потеря в массе тела составила менее 5% от исходного значения.
Подростки. Терапию препаратом Саксенда® следует прекратить и пересмотреть, если после 12 недель применения препарата в дозе 3,0 мг/сут или максимальной переносимой дозе пациенты потеряли менее 4% от своего ИМТ или z-показателя ИМТ.
Пациенты с СД2. Препарат Саксенда® не следует применять в комбинации с другими агонистами рецепторов ГПП-1.
В начале терапии препаратом Саксенда® рекомендуется уменьшить дозы одновременно применяемого препарата инсулина или секретагогов инсулина (таких как препараты сульфонилмочевины) для уменьшения риска развития гипогликемии. Самоконтроль концентрации глюкозы крови может быть необходим для корректировки дозы инсулина или секретагогов инсулина.
Особые группы пациентов
Пациенты пожилого возраста (≥65 лет). Коррекция дозы с учетом возраста не требуется. Опыт применения препарата у пациентов в возрасте ≥75 лет ограничен, применять препарат у таких пациентов не рекомендуется.
Почечная недостаточность. У пациентов с почечной недостаточностью легкой или средней степени (Cl креатинина ≥30 мл/мин) коррекция дозы не требуется. Имеется ограниченный опыт применения препарата Саксенда® у пациентов с почечной недостаточностью тяжелой степени (Cl креатинина <30 мл/мин). Применение препарата Саксенда® у таких пациентов, включая больных с терминальной стадией почечной недостаточности, противопоказано (см. «Фармакокинетика» и «Противопоказания»).
Печеночная недостаточность. У пациентов с печеночной недостаточностью легкой или средней степени тяжести коррекции дозы не требуется. У пациентов с печеночной недостаточностью легкой или средней степени тяжести препарат следует принимать с осторожностью (см. «Фармакокинетика» и С осторожностью). Применение препарата Саксенда® у пациентов с печеночной недостаточностью тяжелой степени противопоказано (см. «Фармакокинетика» и «Противопоказания»).
Дети и подростки. Применение препарата Саксенда® у детей и подростков в возрасте до 12 лет или у подростков с массой тела, меньшей или равной 60 кг, противопоказано вследствие отсутствия данных (см. Клиническая эффективность и безопасность.)
Для подростков в возрасте от 12 до 18 лет следует применять такой же режим увеличения дозы, как и для взрослых (см. таблицу 2). Дозу препарата следует увеличивать до тех пор, пока не будет достигнуто значение 3,0 мг (терапевтическая доза) или максимально переносимая доза. Применение препарата в суточной дозе >3,0 мг не рекомендуется.
Пропущенная доза
Если после обычного времени введения дозы прошло менее 12 ч, пациент должен ввести дозу как можно быстрее. Если до обычного времени введения следующей дозы осталось менее 12 ч, пациент не должен вводить пропущенную дозу, а должен возобновить введение препарата со следующей запланированной дозы. Не следует вводить дополнительную или повышенную дозу для компенсации пропущенной.
Инструкция для пациентов по применению препарата Саксенда® раствор для п/к введения 6 мг/мл в предварительно заполненной шприц-ручке
Перед использованием предварительно заполненной шприц-ручки с препаратом Саксенда® следует внимательно прочитать эту инструкцию.
Использовать шприц-ручку только после того, как пациент научился ею пользоваться под руководством врача или медсестры.
Проверить маркировку на этикетке шприц-ручки, чтобы убедиться, что она содержит препарат Саксенда® 6 мг/мл, а затем внимательно изучить представленные ниже иллюстрации, на которых показаны детали шприц-ручки и иглы.
Если пациент слабовидящий или у него имеются серьезные проблемы со зрением и он не может различить цифры на счетчике дозы, не использовать шприц-ручку без посторонней помощи. Помочь может человек с хорошим зрением, обученный использованию предварительно заполненной шприц-ручки с препаратом Саксенда®.
Предварительно заполненная шприц-ручка содержит 18 мг лираглутида и позволяет выбрать дозу 0,6 мг, 1,2 мг, 1,8 мг, 2,4 мг и 3,0 мг. Шприц-ручка Саксенда® разработана для использования с одноразовыми иглами НовоФайн® длиной до 8 мм. Иглы не входят в упаковку.
Важная информация
Обратить внимание на информацию, отмеченную как важная, это необходимо для безопасного использования шприц-ручки.
Рисунок 3. Предварительно заполненная шприц-ручка с препаратом Саксенда® и игла (пример).
I. Подготовка шприц-ручки с иглой к использованию
Проверить название и цветовой код на этикетке шприц-ручки, чтобы убедиться, что в ней содержится препарат Саксенда®.
Это особенно важно в том случае, если пациент применяет разные инъекционные препараты. Применение неправильного препарата может быть вредным для его здоровья.
Снять колпачок со шприц-ручки (рис. А).
Рисунок А.
Убедиться, что раствор в шприц-ручке прозрачный и бесцветный (рис. В).
Посмотреть в окошко шкалы остатка. Если препарат мутный, шприц-ручку использовать нельзя.
Рисунок B.
Взять новую одноразовую иглу и удалить защитную наклейку (рис. С).
Рисунок С.
Надеть иглу на шприц-ручку и повернуть ее, чтобы игла плотно держалась на шприц-ручке (рис. D).
Рисунок D.
Снять наружный колпачок иглы, но не выбрасывать его (рис. Е). Он понадобится после завершения инъекции, чтобы безопасно снять иглу со шприц-ручки.
Рисунок Е.
Снять и выбросить внутренний колпачок иглы (рис. F). Если пациент попытается надеть внутренний колпачок обратно на иглу, он может уколоться. На конце иглы может появиться капля раствора. Это нормальное явление, однако пациент все равно должен проверить поступление препарата, если используется новая шприц-ручка в первый раз. Не следует присоединять новую иглу до тех пор, пока пациент не будет готов сделать инъекцию.
Рисунок F.
Важная информация
Всегда использовать новую иглу для каждой инъекции, чтобы избежать закупорки иглы, заражения, инфицирования и введения неправильной дозы препарата. Никогда не использовать иглу, если она погнута или повреждена.
II. Проверка поступления препарата
Перед первой инъекцией с помощью новой шприц-ручки проверить поступление препарата. Если шприц-ручка уже находится в использовании, то перейти к операции III «Установка дозы».
Поворачивать селектор дозы до тех пор, пока в индикаторном окошке символ проверки поступления препарата (vvw ) не поравняется с указателем дозы (рис. G).
Рисунок G.
Держать шприц-ручку иглой вверх.
Нажать пусковую кнопку и удерживать ее в этом положении, пока счетчик дозы не возвратится к нулю (рис. H).
Рисунок H.
«0» должен стоять напротив указателя дозы. На конце иглы должна появиться капля раствора. На конце иглы может оставаться маленькая капля, но она не будет введена при инъекции.
Если капля раствора на конце иглы не появилась, необходимо повторить операцию II «Проверка поступления препарата», но не более 6 раз. Если капля раствора не появилась, следует поменять иглу и повторить эту операцию. Если капля раствора препарата Саксенда® так и не появилась, следует утилизировать шприц-ручку и использовать новую.
Важная информация
Всегда перед использованием новой шприц-ручки в первый раз необходимо убедиться в том, что на конце иглы появилась капля раствора. Это гарантирует поступление препарата.
Если капля раствора не появилась, препарат не будет введен, даже если счетчик дозировки будет двигаться. Это может указывать на то, что игла закупорена или повреждена. Если пациент не проверит поступление препарата перед первой инъекцией с помощью новой шприц-ручки, он может не ввести необходимую дозу, и ожидаемый эффект препарата Саксенда® не будет достигнут.
III. Установка дозы
Поворачивать селектор дозы, чтобы набрать необходимую пациенту дозу (0,6 мг, 1,2 мг, 1,8 мг, 2,4 мг или 3 мг) (рис. I).
Если доза была установлена неправильно, необходимо поворачивать селектор дозы вперед или назад, пока не будет установлена правильная доза. Максимальная доза, которую можно установить, составляет 3,0 мг. Селектор дозы позволяет изменить дозу. Только счетчик дозы и указатель дозы покажут количество мг препарата в выбранной пациентом дозе.
Пациент может набрать до 3,0 мг препарата на дозу. Если в используемой шприц-ручке содержится менее 3,0 мг, счетчик дозы остановится прежде, чем в окошке появится «3,0».
Рисунок I.
При каждом повороте селектора дозы раздаются щелчки, звук щелчков зависит от того, в какую сторону вращается селектор дозы (вперед, назад или, если набранная доза превышает количество мг препарата, оставшееся в шприц-ручке). Не следует считать эти щелчки.
Важная информация
Всегда перед каждой инъекцией проверять, какое количество препарата пациент набрал по счетчику и указателю дозы. Не следует считать щелчки шприц-ручки.
Шкала остатка показывает приблизительное количество оставшегося в шприц-ручке раствора, поэтому ее нельзя использовать для отмеривания дозы препарата.
С помощью селектора дозы нужно выбирать только дозы 0,6 мг, 1,2 мг, 1,8 мг, 2,4 мг или 3,0 мг. Выбранная доза должна находиться точно напротив указателя дозы — такое положение гарантирует, что пациент получит правильную дозу препарата.
Сколько препарата осталось?
Шкала остатка показывает примерное количество оставшегося в шприц-ручке препарата (рис. K).
Рисунок K.
Чтобы точно определить, сколько препарата осталось, использовать счетчик дозы (рис. L).
Поворачивать селектор дозы до остановки счетчика дозы. Если он показывает «3,0», в шприц-ручке осталось как минимум 3,0 мг препарата. Если счетчик дозы показывает менее «3,0», то это означает, что в шприц-ручке осталось недостаточное количество препарата, чтобы ввести полную дозу 3,0 мг.
Рисунок L.
Если необходимо ввести большее количество препарата, чем осталось в шприц-ручке.
Только если пациента обучили врач или медсестра, он может разделить дозу препарата между двумя шприц-ручками (той, которая сейчас находится в использовании, и новой). Использовать калькулятор, чтобы спланировать дозы, как рекомендовано врачом или медсестрой.
Важная информация
Необходимо быть очень внимательным, чтобы правильно рассчитать дозу. Если нет уверенности, как правильно разделить дозу при использовании двух шприц-ручек, следует установить и ввести полную дозу с помощью новой шприц-ручки.
IV. Введение препарата
Ввести иглу под кожу, используя технику инъекций, рекомендованную врачом или медсестрой (рис. М).
Рисунок М.
Убедиться, что счетчик дозы находится в поле зрения пациента. Не дотрагиваться до счетчика дозы пальцами — это может прервать инъекцию.
Нажать пусковую кнопку до упора и удерживать ее в этом положении, пока счетчик дозы не покажет «0» (рис. N).
Рисунок N.
«0» должен находиться точно напротив указателя дозы. При этом пациент может услышать или ощутить щелчок.
Удерживать иглу под кожей после того, как счетчик дозы возвратился к нулевой отметке, и медленно считать до 6 (рис. O).
Рисунок O.
Если пациент извлечет иглу из-под кожи раньше, он увидит, как препарат вытекает из иглы. В этом случае будет введена неполная доза препарата.
Извлечь иглу из-под кожи (рис. Р).
Рисунок Р.
Если в месте инъекции появилась кровь, слегка прижать к месту укола ватный тампон. Не массировать место укола.
После завершения инъекции можно увидеть каплю раствора на конце иглы. Это нормально и не влияет на дозу препарата, которая была введена.
Важная информация
Всегда сверяться с показаниями счетчика дозы, чтобы знать, какое количество препарата Саксенда® введено.
Удерживать пусковую кнопку до тех пор, пока счетчик дозы не покажет «0».
Как выявить закупорку или повреждение иглы?
Если после долгого нажатия на пусковую кнопку на счетчике дозы не появляется «0», это может означать закупорку или повреждение иглы.
Это означает, что пациент не получил препарат, даже если счетчик доз изменил положение с исходной дозы, которую пациент установил.
Что делать с закупоренной иглой?
Снять иглу, как описано в операции V «После завершения инъекции» и повторить все шаги, начиная с операции I «Подготовка шприц-ручки с иглой к использованию».
Следует убедиться, что установлена необходимая пациенту доза.
Никогда не прикасаться к счетчику дозы во время введения препарата. Это может прервать инъекцию.
V. После завершения инъекции
Положив наружный колпачок иглы на плоскую поверхность, ввести конец иглы внутрь колпачка, не касаясь его или иглы (рис. R).
Рисунок R.
Когда игла войдет в колпачок, осторожно надеть наружный колпачок на иглу (рис. S). Отвинтить иглу и выбросить ее, соблюдая меры предосторожности.
Рисунок S.
После каждой инъекции надевать на шприц-ручку колпачок, чтобы защитить содержащийся в ней раствор от воздействия света (рис. Т).
Рисунок Т.
Всегда необходимо выбрасывать иглу после каждой инъекции, чтобы обеспечить комфортную инъекцию и избежать закупорки игл. Если игла будет закупорена, пациент не сможет ввести себе препарат.
Выбрасывать пустую шприц-ручку с отсоединенной иглой, в соответствии с рекомендациями, данными врачом, медсестрой, фармацевтом или в соответствии с местными требованиями.
Важная информация
Чтобы избежать случайных уколов иглой, никогда не пытаться надеть внутренний колпачок обратно на иглу. Всегда удалять иглу со шприц-ручки после каждой инъекции. Это позволит избежать закупорки иглы, заражения, инфицирования, вытекания раствора и введения неправильной дозы препарата.
Хранить шприц-ручку и иглы в недоступном для всех, и в особенности для детей, месте.
Никогда не передавать свою шприц-ручку с препаратом и иглы к ней другим лицам.
Лица, осуществляющие уход за больным, должны обращаться с использованными иглами с особой осторожностью, чтобы избежать случайных уколов и перекрестного инфицирования.
Уход за шприц-ручкой
Не оставлять шприц-ручку в автомобиле или любом другом месте, где она может подвергаться воздействию слишком высоких или слишком низких температур.
Не применять препарат Саксенда®, если он был заморожен. В этом случае ожидаемый эффект от применения препарата не будет достигнут.
Предохранять шприц-ручку от попадания на нее пыли, загрязнений и всех видов жидкостей.
Не мыть шприц-ручку, не погружать ее в жидкость и не смазывать ее. При необходимости, шприц-ручку можно очищать влажной тканью, смоченной мягким моющим средством.
Нельзя ронять или ударять шприц-ручку о твердую поверхность.
Если пациент уронил шприц-ручку или сомневается в ее исправности, следует присоединить новую иглу и проверить поступление препарата перед тем, как сделать инъекцию.
Не допускается повторное заполнение шприц-ручки. Пустую шприц-ручку следует сразу выбросить.
Не пытаться самостоятельно починить шприц-ручку или разобрать ее на части.
Побочные действия
Безопасность препарата Саксенда® была оценена в 5 двойных слепых плацебо-контролируемых исследованиях, в которых приняли участие 5813 пациентов с ожирением или избыточной массой тела и как минимум с одним связанным с избыточной массой тела сопутствующим заболеванием. В целом нарушения со стороны ЖКТ являлись наиболее часто отмечаемыми побочными эффектами во время терапии препаратом Саксенда® (см. Описание отдельных нежелательных реакций).
Ниже представлен перечень нежелательных реакций, зарегистрированных в ходе долгосрочных контролируемых исследований 2-й и 3-й фазы для взрослых пациентов. Нежелательные реакции распределены по группам в соответствии с системами органов MedDRA и частотой. Частота определена следующим образом: очень часто (от ≥1/10); часто (от ≥1/100 до <1/10); нечасто (от ≥1/1000 до <1/100); редко (от ≥1/10000 до <1/1000); очень редко (<1/10000).
Со стороны иммунной системы: редко — анафилактические реакции.
Со стороны обмена веществ и питания: часто — гипогликемия*; нечасто — дегидратация.
Нарушения психики: часто — бессонница**.
Со стороны нервной системы: часто — головокружение**, дисгевзия**.
Со стороны сердца: нечасто — тахикардия.
Со стороны ЖКТ: очень часто — тошнота, рвота, диарея, запор; часто — сухость во рту, диспепсия, гастрит, гастроэзофагеальный рефлюкс, боль в верхних отделах живота, метеоризм, отрыжка, вздутие живота; нечасто — панкреатит ***, задержка опорожнения желудка****.
Cо стороны печени и желчевыводящих путей: часто — холелитиаз***; нечасто — холецистит***.
Со стороны кожи и подкожных тканей: нечасто — крапивница.
Со стороны почек и мочевыводящих путей: редко — острая почечная недостаточность, нарушение функции почек.
Общие расстройства и нарушения в месте введения: часто — реакции в месте введения, астения**, утомляемость**; нечасто — недомогание**.
Лабораторные методы исследования: часто — повышение активности липазы, повышение активности амилазы.
* Гипогликемия (на основании отмеченных пациентами симптомов, не подтвержденная измерениями концентрации глюкозы в крови), отмеченная у пациентов без СД2, получавших препарат Саксенда® в сочетании с диетой и физическими нагрузками. Подробную информацию см. в подразделе Описание отдельных нежелательных реакций.
** Преимущественно отмечали во время первых 3 мес терапии.
*** См. «Особые указания».
**** В соответствии с фазами 2, За и ЗЬ контролируемого клинического исследования.
Описание отдельных нежелательных реакций
Гипогликемия у пациентов без СД2. В КИ с участием пациентов с избыточной массой тела или ожирением без СД2, получавших терапию препаратом Саксенда® в сочетании с диетой и физическими нагрузками, тяжелых гипогликемий (требующих оказания помощи третьим лицом) отмечено не было. О симптомах гипогликемии сообщали 1,6% пациентов, получавших препарат Саксенда®, и 1,1% пациентов, получавших плацебо; однако эти случаи не были подтверждены измерениями концентрации глюкозы в крови. В большинстве случаев отмечалась легкая гипогликемия.
Гипогликемия у пациентов с СД2. В клиническом исследовании с участием пациентов с избыточной массой тела или ожирением и СД2, получавших терапию препаратом Саксенда® в сочетании с диетой и физическими нагрузками, случаи тяжелой гипогликемии (требующие оказания помощи третьим лицом) были отмечены у 0,7% пациентов, получавших препарат Саксенда®, и только у пациентов, одновременно получавших терапию производными сульфонилмочевины. Также в этой группе пациентов подтвержденная гипогликемия (концентрация глюкозы ≤3,9 ммоль/л в сочетании с симптомами) была отмечена у 43,6% пациентов, получавших препарат Саксенда®, и 27,3% пациентов, получавших плацебо. Среди пациентов, не получавших одновременно препарат сульфонилмочевины, подтвержденная гипогликемия была отмечена у 15,7% пациентов, получавших препарат Саксенда®, и у 7,6% пациентов, получавших плацебо.
Гипогликемия у пациентов с СД2, получающих инсулин. В КИ с участием пациентов с избыточной массой тела или ожирением с СД2, получавших терапию инсулином и препаратом Саксенда® в сочетании с диетой и физическими нагрузками и до двух пероральных гипогликемических препаратов, тяжелая гипогликемия (требующая оказания помощи третьим лицом) была отмечена у 1,5% пациентов, получавших терапию препаратом Саксенда®. В данном исследовании подтвержденная гипогликемия (определяемая как уровень глюкозы в плазме ≤3,9 ммоль/л, сопровождаемый симптомами) была зарегистрирована у 47,2% пациентов, получавших терапию препаратом Саксенда®, и у 51,8% пациентов, получавших плацебо. Сообщалось о подтвержденных гипогликемических эпизодах среди пациентов, одновременно получавших производные сульфонилмочевины, у 60,9% пациентов, получавших терапию препаратом Саксенда®, и у 60,0% пациентов, получавших плацебо.
Нежелательные реакции со стороны ЖКТ. Большинство реакций со стороны ЖКТ были легкой или средней степени тяжести, преходящими и в большинстве случаев не приводили к прекращению терапии. Реакции обычно возникали в первые недели терапии, и их проявления постепенно уменьшались в течение нескольких дней или недель при продолжении терапии. У пациентов в возрасте ≥65 лет могут наблюдаться более выраженные проявления нежелательных реакций со стороны ЖКТ во время терапии препаратом Саксенда®. У пациентов с почечной недостаточностью легкой или средней степени тяжести (Cl креатинина ≥30 мл/мин) могут наблюдаться более выраженные проявления нежелательных реакций со стороны ЖКТ во время терапии препаратом Саксенда®.
Аллергические реакции. В пострегистрационном периоде сообщалось о возникновении нескольких случаев анафилактических реакций с такими симптомами, как артериальная гипотензия, ощущение сердцебиения, одышка или периферические отеки. Анафилактические реакции потенциально могут быть угрожающими жизни.
Реакции в месте введения. Сообщалось о развитии реакций в месте введения у пациентов, получавших препарат Саксенда®. Эти реакции, как правило, были легкой степени, носили транзиторный характер и в большинстве случаев исчезали при продолжении терапии.
Тахикардия. В КИ тахикардия была отмечена у 0,6% пациентов, получавших препарат Саксенда®, и у 0,1% пациентов, получавших плацебо. Большинство явлений были легкой или средней степени тяжести. Явления были единичными и в большинстве случаев проходили при продолжении терапии препаратом Саксенда®.
Дети и подростки. В КИ, проведенном с участием подростков от 12 до 18 лет с ожирением, 125 пациентов получали терапию препаратом Саксенда® в течение 56 недель. В целом частота развития, тип и степень тяжести нежелательных реакций у подростков с ожирением были сопоставимы с таковыми у взрослых пациентов. Рвота у подростков возникала в два раза чаще по сравнению со взрослыми пациентами. Никакого влияния на рост или пубертатное развитие обнаружено не было.
Взаимодействие
Реклама: ООО «ВЕДАНТА», ИНН 7714886235, erid 4CQwVszH9pUkKJ7jUDd
Реклама: ООО «РЛС-Библиомед» ИНН 7714758963
Реклама: ООО «ВЕДАНТА», ИНН 7714886235, erid 4CQwVszH9pUkKJ7jUDd
Реклама: ООО «РЛС-Библиомед» ИНН 7714758963
Оценка взаимодействия лекарственных средств in vitro. Лираглутид показал очень низкую способность к лекарственному фармакокинетическому взаимодействию, обусловленному метаболизмом в системе цитохрома Р450 (CYP), а также связыванием с белками плазмы крови.
Оценка взаимодействия лекарственных средств in vivo. Небольшая задержка опорожнения желудка при применении лираглутида может влиять на всасывание одновременно применяемых препаратов для приема внутрь. Исследования лекарственного взаимодействия не показали какого-либо клинически значимого замедления всасывания этих препаратов, поэтому коррекция дозы не требуется.
Исследования взаимодействия проводили с применением лираглутида в дозе 1,8 мг. Влияние на скорость опорожнения желудка было одинаковым при применении лираглутида в дозе 1,8 мг и 3,0 мг (AUC0–300 мин парацетамола). У нескольких пациентов, получавших лираглутид, был отмечен как минимум один эпизод тяжелой диареи. Диарея может влиять на всасывание пероральных лекарственных препаратов, которые применяются одновременно с лираглутидом.
Варфарин и другие производные кумарина. Исследований взаимодействия не проводили. Клинически значимое взаимодействие с действующими веществами с низкой растворимостью или узким терапевтическим индексом, такими как варфарин, не может быть исключено. В начале лечения препаратом Саксенда® у пациентов, получающих варфарин или другие производные кумарина, рекомендуется чаще проводить мониторинг MHO.
Парацетамол (ацетаминофен). Лираглутид не изменял общую экспозицию парацетамола после введения однократной дозы парацетамола 1000 мг. Cmax парацетамола была снижена на 31%, а медиана Tmax увеличена на 15 мин. Коррекция дозы при сопутствующем применении парацетамола не требуется.
Аторвастатин. Лираглутид не изменял общую экспозицию аторвастатина после применения однократной дозы аторвастатина 40 мг. Поэтому коррекция дозы аторвастатина при применении в сочетании с лираглутидом не требуется. Cmax аторвастатина была снижена на 38%, а медиана Tmax увеличена с 1 до 3 ч при применении лираглутида.
Гризеофульвин. Лираглутид не изменял общую экспозицию гризеофульвина после применения однократной дозы гризеофульвина 500 мг. Cmax гризеофульвина была увеличена на 37%, а медиана Tmax не изменилась. Коррекция дозы гризеофульвина и других соединений с низкой растворимостью и высокой проникающей способностью не требуется.
Дигоксин. Применение однократной дозы дигоксина 1 мг в сочетании с лираглутидом привело к уменьшению AUC дигоксина на 16%, уменьшению Cmax на 31%. Медиана Tmax увеличилась с 1 до 1,5 ч. С учетом данных результатов, коррекция дозы дигоксина не требуется.
Лизиноприл. Применение однократной дозы лизиноприла 20 мг в сочетании с лираглутидом привело к уменьшению AUC лизиноприла на 15%, уменьшению Cmax на 27%. Медиана Tmax лизиноприла увеличилась с 6 до 8 ч. С учетом данных результатов, коррекция дозы лизиноприла не требуется.
Пероральные контрацептивы. Лираглутид приводил к уменьшению Cmax этинилэстрадиола и левоноргестрела на 12 и 13% соответственно после применения однократной дозы перорального гормонального контрацептивного препарата. Tmax обоих лекарственных веществ на фоне применения лираглутида увеличивалось на 1,5 ч. Не было отмечено клинически значимое влияние на системную экспозицию этинилэстрадиола или левоноргестрела. Таким образом, не ожидается влияние на контрацептивный эффект при совместном применении с лираглутидом.
Несовместимость. Лекарственные вещества, добавленные к препарату Саксенда®, могут вызвать разрушение лираглутида. В связи с отсутствием исследований совместимости данный лекарственный препарат нельзя смешивать с другими лекарственными препаратами.
Передозировка
По данным КИ и пострегистрационного применения лираглутида, были зарегистрированы случаи передозировки при применении препарата в дозе 72 мг (в 24 раза больше рекомендуемой для коррекции массы тела).
Симптомы: пациенты отмечали сильную тошноту, сильную рвоту и тяжелую гипогликемию.
Лечение: необходимо начать соответствующую поддерживающую терапию в соответствии с клиническими признаками и симптомами. Пациента следует наблюдать на предмет клинических признаков обезвоживания и контролировать концентрацию глюкозы крови.
Особые указания
У пациентов с СД нельзя применять препарат Саксенда® в качестве замены инсулина. Диабетический кетоацидоз отмечался у пациентов, получавших терапию инсулином, после быстрого прекращения или снижения дозы инсулина (см. «Способ применения и дозы»).
Панкреатит. Применение агонистов рецепторов ГПП-1 ассоциировалось с развитием острого панкреатита. Пациенты должны быть проинформированы о характерных симптомах острого панкреатита. В случае подозрения на развитие панкреатита применение препарата Саксенда® следует прекратить; в случае подтверждения острого панкреатита терапию препаратом Саксенда® возобновлять не следует.
Холелитиаз и холецистит. В КИ была отмечена более высокая частота развития холелитиаза и холецистита у пациентов, получавших препарат Саксенда®, по сравнению с получавшими плацебо пациентами. Это может быть частично объяснено тем, что снижение массы тела может увеличить риск развития холелитиаза и, следовательно, холецистита. Холелитиаз и холецистит могут привести к госпитализации и холецистэктомии. Пациенты должны быть проинформированы о характерных симптомах холелитиаза и холецистита.
Заболевания щитовидной железы. В ходе КИ с участием пациентов с СД2 были отмечены нежелательные явления со стороны щитовидной железы, включая увеличение концентрации кальцитонина в сыворотке крови, зоб и новообразование щитовидной железы, в особенности у пациентов, уже имеющих заболевания щитовидной железы. У пациентов с заболеваниями щитовидной железы препарат Саксенда® следует применять с осторожностью.
В постмаркетинговом периоде у пациентов, получавших лираглутид, были отмечены случаи медуллярного рака щитовидной железы. Имеющихся данных недостаточно для установления или исключения причинно-следственной связи возникновения медуллярного рака щитовидной железы с применением лираглутида у человека. Препарат Саксенда® противопоказан к применению у пациентов с медуллярным раком щитовидной железы в анамнезе, в т.ч. семейном, и множественной эндокринной неоплазией II типа.
Необходимо проинформировать пациента о риске развития медуллярного рака щитовидной железы и симптомах опухоли щитовидной железы (уплотнения в области шеи, дисфагия, одышка, непроходящая охриплость голоса).
Текущий контроль концентрации кальцитонина в сыворотке крови или УЗИ щитовидной железы не имеют существенного значения для раннего выявления медуллярного рака щитовидной железы у пациентов, применяющих препарат Саксенда®. Значительное повышение концентрации кальцитонина в сыворотке крови может свидетельствовать о наличии медуллярного рака щитовидной железы, пациенты с медуллярным раком щитовидной железы обычно имеют концентрацию кальцитонина более 50 нг/л. При выявлении повышения концентрации кальцитонина в сыворотке крови необходимо провести дальнейшее обследование пациента. Пациенты с узлами щитовидной железы, выявленными при медосмотре или УЗИ щитовидной железы, также должны быть дополнительно обследованы.
ЧСС. В КИ было отмечено увеличение ЧСС (см. Клиническая эффективность и безопасность). Следует проводить контроль ЧСС с интервалами, соответствующими обычной клинической практике. Пациентов следует проинформировать о симптомах тахикардии (ощущение сердцебиения или ощущение учащенного сердцебиения в покое). У пациентов с клинически значимой постоянной тахикардией в состоянии покоя следует прекратить терапию препаратом Саксенда®.
Обезвоживание. Признаки и симптомы обезвоживания, включая нарушение функции почек и острую почечную недостаточность, были отмечены у пациентов, получавших агонисты рецепторов ГПП-1. Пациенты, получающие препарат Саксенда®, должны быть проинформированы о потенциальном риске обезвоживания, связанного с побочными эффектами со стороны ЖКТ, и необходимости профилактики гиповолемии.
Гипогликемия у пациентов с избыточной массой тела или ожирением и СД2. Риск развития гипогликемии может быть выше у пациентов с СД2, получающих препарат Саксенда® в комбинации с инсулином и/или производными сульфонилмочевины. Этот риск может быть уменьшен путем снижения дозы инсулина и/или производного сульфонилмочевины.
Суицидальные мысли и поведение. В ходе КИ 6 (0,2%) из 3384 пациентов, получавших препарат Саксенда®, сообщили о появлении суицидальных мыслей, один из пациентов предпринял попытку суицида. У пациентов (1941 человек), получавших плацебо, это отмечено не было. Пациентов необходимо контролировать в отношении появления или ухудшения депрессии, суицидальных мыслей или поведения и/или любых неожиданных изменений в настроении или поведении. У пациентов с суицидальными мыслями или поведением применение препарата Саксенда® следует прекратить.
Противопоказано применять препарат Саксенда® у пациентов с суицидальными попытками или активными суицидальными мыслями в анамнезе.
Рак молочной железы (РМЖ). В ходе КИ сообщалось о подтвержденном РМЖ у 14 (0,6%) из 2379 женщин, получавших препарат Саксенда®, по сравнению с 3 (0,2%) из 1300 женщин, получавших плацебо, включая инвазивный рак (11 случаев у женщин, получавших препарат Саксенда®, и 3 случая у женщин, получавших плацебо) и внутрипротоковую карциному in situ (3 случая у женщин, получавших препарат Саксенда®, и 1 случай у женщины, получавшей плацебо). Большинство случаев рака были эстроген- и прогестеронзависимыми. Невозможно определить, были ли эти случаи связаны с применением препарата Саксенда® из-за их слишком небольшого количества. Кроме того, нет достаточных данных, чтобы определить, оказывает ли препарат Саксенда® влияние на уже существующие новообразования молочной железы.
Папиллярный рак щитовидной железы. В ходе КИ сообщалось о подтвержденной папиллярной карциноме щитовидной железы у 7 (0,2%) из 3291 пациента, получавших препарат Саксенда®, по сравнению с отсутствием ее в группе пациентов, получавших плацебо (1843 пациента). Из всех случаев 4 карциномы были менее 1 см в наибольшем диаметре и 4 были диагностированы по результатам гистологии после проведенной по медицинским показаниям тиреоидэктомии.
Неоплазии ободочной и прямой кишки. В ходе КИ сообщалось о подтвержденных доброкачественных неоплазиях ободочной и прямой кишки (преимущественно аденомах ободочной кишки) у 17 (0,5%) из 3291 пациента, получавших препарат Саксенда®, по сравнению с 4 (0,2%) из 1843 пациентов, получавших плацебо. Было зарегистрировано два подтвержденных случая злокачественной карциномы ободочной и прямой кишки (0,1%) у пациентов, получавших препарат Саксенда®, и ни у одного из пациентов, получавших плацебо.
Нарушения сердечной проводимости. В ходе КИ у 11 (0,3%) из 3384 пациентов, получавших препарат Саксенда®, сообщалось о развитии нарушений сердечной проводимости, таких как AV-блокада 1-й степени, блокада правой или блокада левой ножки пучка Гиса. У пациентов (1941 человек), получавших плацебо, о развитии нарушений сердечной проводимости не сообщалось.
Фертильность. За исключением незначительного уменьшения числа живых зародышей, результаты исследований на животных не указывают на наличие неблагоприятного влияния на фертильность.
Доклинические данные по безопасности
Доклинические данные, основанные на исследованиях фармакологической безопасности, токсичности повторных доз и генотоксичности, не выявили какой-либо опасности для человека.
В двухлетних исследованиях канцерогенности у крыс и мышей были выявлены опухоли С-клеток щитовидной железы, не приводившие к летальному исходу. Результаты, полученные в ходе исследований на грызунах, обусловлены тем, что грызуны проявляют особую чувствительность в отношении опосредуемого рецептором ГПП-1 негенотоксичного специфического механизма. Появления других новообразований, связанных с проводимой терапией, отмечено не было.
В исследованиях на животных не выявлено прямого неблагоприятного эффекта препарата на фертильность, но было отмечено незначительное увеличение частоты ранней эмбриональной смерти при применении самых высоких доз препарата.
Руководство по применению. Препарат Саксенда® нельзя применять, если он выглядит иначе, чем прозрачная и бесцветная или почти бесцветная жидкость.
Препарат Саксенда® нельзя применять, если он был заморожен.
Препарат Саксенда® можно вводить при помощи игл длиной до 8 мм. Шприц-ручка предназначена для использования с одноразовыми иглами НовоФайн®. Инъекционные иглы не включены в упаковку.
Пациент должен быть проинформирован о том, что использованную иглу следует выбрасывать после каждой инъекции в соответствии с местными требованиями, а также о том, что необходимо хранить шприц-ручку Саксенда® с отсоединенной иглой. Такая мера позволит предотвратить закупорку игл, загрязнение, инфицирование и вытекание препарата из шприц-ручки и гарантирует точность дозирования.
Влияние на способность управлять транспортными средствами и механизмами. Препарат Саксенда® не влияет или незначительно влияет на способность управлять транспортными средствами и механизмами. В связи с риском развития гипогликемии при применении препарата, особенно при комбинированном применении с препаратами сульфонилмочевины у пациентов с СД2, следует соблюдать осторожность при управлении транспортными средствами и механизмами.
Форма выпуска
Раствор для подкожного введения, 6 мг/мл. По 3 мл в картриджах из стекла I гидролитического класса, укупоренных дисками из бромбутиловой резины/полиизопрена с одной стороны и поршнями из бромбутиловой резины с другой. Картридж запаян в пластиковую мультидозовую одноразовую шприц-ручку для многократных инъекций. По 3 или 5 мультидозовых одноразовых шприц-ручек вместе с инструкцией по применению в картонной пачке.
Производитель
Производитель и владелец регистрационного удостоверения: Ново Нордиск А/С: Ново Алле, DK-2880 Багсваерд, Дания.
www.novonordisk.com
Претензии потребителей направлять по адресу ООО «Ново Нордиск»: 121614, Москва, ул. Крылатская, 15, оф. 41.
Тел.: (495) 956-11-32; факс: (495) 956-50-13.
www.novonordisk.ru
Условия отпуска из аптек
По рецепту.
Условия хранения
При температуре 2–8 °C (в холодильнике), но не рядом с морозильной камерой. Не замораживать..
Используемую шприц-ручку с препаратом хранить при температуре не выше 30 °C или в холодильнике (при температуре от 2 °C до 8 °C). Не замораживать. Использовать в течение 1 мес. Закрывать шприц-ручку колпачком для защиты от света.
Хранить в недоступном для детей месте.
Срок годности
2,5 года.
Не применять по истечении срока годности, указанного на упаковке.
Представленная информация о ценах на препараты не является предложением о продаже или покупке товара.
Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в
соответствии со статьей 55 Федерального закона «Об обращении лекарственных средств» от 12.04.2010 № 61-ФЗ.
Саксенда® (Saxenda®) инструкция по применению
📜 Инструкция по применению Саксенда®
💊 Состав препарата Саксенда®
✅ Применение препарата Саксенда®
📅 Условия хранения Саксенда®
⏳ Срок годности Саксенда®
Описание лекарственного препарата
Саксенда®
(Saxenda®)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для печатного издания справочника Видаль 2023 года.
Дата обновления: 2022.11.10
Владелец регистрационного удостоверения:
Контакты для обращений:
НОВО НОРДИСК ООО
(Россия)
Код ATX:
A10BJ02
(Лираглутид)
Лекарственная форма
| Саксенда® |
Р-р д/п/к введения 6 мг/мл: картридж в шприц-ручке 3 мл 3 или 5 шт. рег. №: ЛП-003491 |
Форма выпуска, упаковка и состав
препарата Саксенда®
Раствор для п/к введения прозрачный, бесцветный или почти бесцветный.
Вспомогательные вещества: натрия гидрофосфата дигидрат, пропиленгликоль, фенол, натрия гидроксид/кислота хлористоводородная (для коррекции pH), вода для инъекций.
3 мл — картриджи стеклянные (1) — шприц-ручки пластиковые мультидозовые одноразовые для многократных инъекций (3) — пачки картонные.
Фармакологическое действие
Фармакодинамика
Действующее вещество препарата Саксенда® — лираглутид — представляет собой ацилированный аналог человеческого ГПП-1, произведенный методом биотехнологии рекомбинантной ДНК с использованием штамма Saccharomyces cerevisiae, имеющий 97% гомологичности аминокислотной последовательности эндогенному человеческому ГПП-1. Лираглутид связывается и активирует рецептор ГПП-1 (ГПП-1Р). Лираглутид устойчив к метаболическому распаду, его период полувыведения из плазмы после подкожного введения составляет 13 ч. Фармакокинетический профиль лираглутида, позволяющий вводить его пациентам 1 раз/сут, является результатом самоассоциации, в результате которой происходит замедленное всасывание препарата; связывания с белками плазмы; а также устойчивости к дипептидилпептидазе-4 (ДПП-4) и нейтральной эндопептидазе (НЭП).
ГПП-1 является физиологическим регулятором аппетита и потребления пищи, а ГПП-1Р расположены в нескольких областях головного мозга, участвующих в процессах регуляции аппетита. В исследованиях на животных периферическое введение лираглутида приводило к захвату препарата в специфических областях головного мозга, включая гипоталамус, где лираглутид посредством специфической активации ГПП-1Р усиливал сигналы насыщения и ослаблял сигналы голода, тем самым приводя к уменьшению массы тела.
ГПП-1Р представлены также в специфических областях сердца, сосудов, иммунной системы и почек. В экспериментах на мышах с атеросклерозом лираглутид предупреждал дальнейшее развитие аортальных бляшек и снижал в них воспаление. В дополнение, лираглутид оказывал благоприятный эффект на липиды в плазме. Лираглутид не уменьшал размер уже существующих бляшек.
Лираглутид уменьшает массу тела у человека преимущественно посредством уменьшения массы жировой ткани. Уменьшение массы тела происходит за счет уменьшения потребления пищи. Лираглутид не увеличивает 24-часовой расход энергии. Лираглутид регулирует аппетит при помощи усиления чувства наполнения желудка и насыщения, одновременно ослабляя чувство голода и уменьшая предполагаемое потребление пищи.
Лираглутид стимулирует секрецию инсулина и уменьшает неоправданно высокую секрецию глюкагона глюкозозависимым образом, а также улучшает функцию β-клеток поджелудочной железы, что приводит к снижению концентрации глюкозы натощак и после приема пищи. Механизм снижения концентрации глюкозы также включает небольшую задержку опорожнения желудка.
В долгосрочных клинических исследованиях с участием пациентов с избыточной массой тела и ожирением применение препарата Саксенда® в сочетании с низкокалорийной диетой и усиленной физической активностью приводило к значительному снижению массы тела.
Влияние на аппетит, потребление калорий и расход энергии, опорожнение желудка и концентрацию глюкозы натощак и после приема пищи
Фармакодинамические эффекты лираглутида изучались в пятинедельном фармакологическом клиническом исследовании с участием 49 пациентов с ожирением (ИМТ 30-40 кг/м2) без сахарного диабета (СД).
Аппетит, потребление калорий и расход энергии
Считается, что снижение массы тела при применении препарата Саксенда® связано с регулированием аппетита и количества потребляемой пищи. Аппетит оценивали перед и в течение 5 ч после стандартизированного завтрака; неограниченное потребление пищи оценивали во время последующего обеда. По сравнению с плацебо препарат Саксенда® увеличивал чувство насыщения и наполнения желудка после приема пищи и уменьшал чувство голода и оценочное количество предполагаемого потребления пищи, а также уменьшал неограниченное потребление пищи. При оценке с помощью респираторной камеры не было отмечено связанного с терапией увеличения 24-часового расхода энергии.
Опорожнение желудка
Применение препарата Саксенда® приводило к небольшой задержке опорожнения желудка в течение первого часа после приема пищи, в результате чего уменьшалась скорость повышения концентрации глюкозы, а также общая концентрация глюкозы крови после приема пищи.
Концентрации глюкозы, инсулина и глюкагона натощак и после приема пищи
Концентрации глюкозы, инсулина и глюкагона натощак и после приема пищи оценивали перед и в течение 5 ч после стандартизированного приема пищи. По сравнению с плацебо препарат Саксенда® уменьшал концентрацию глюкозы натощак и после приема пищи (AUC0-60 мин) в течение первого часа после приема пищи, а также уменьшал 5-часовую AUC глюкозы и нарастающую концентрацию глюкозы (AUC0-300 мин). Кроме того, по сравнению с плацебо препарат Саксенда® уменьшал постпрандиальные концентрации глюкагона (AUC0-300 мин) и инсулина (AUC0-60 мин) и нарастающую концентрацию инсулина (iAUC0-60 мин) после приема пищи.
Концентрации глюкозы и инсулина натощак и нарастающие концентрации глюкозы и инсулина также оценивали во время перорального теста толерантности к глюкозе (ПТТГ) с 75 г глюкозы до начала терапии и через 1 год терапии у 3731 пациента с избыточной массой тела и с ожирением, а также с наличием или отсутствием предиабета. По сравнению с плацебо препарат Саксенда® уменьшал концентрацию натощак и нарастающую концентрацию глюкозы. Эффект был более выраженным у пациентов с предиабетом. Кроме того, по сравнению с плацебо препарат Саксенда® уменьшал концентрацию инсулина натощак и увеличивал нарастающую концентрацию инсулина.
После 160 недель продолжающейся терапии лираглутидом 3.0 мг AUC глюкозы плазмы уменьшилась, в то время как при применении плацебо оставалась неизменной. Дополнительно AUC инсулина оставалась относительно стабильной в течение 160-недельного периода лечения лираглутидом 3.0 мг, в то время как при применении плацебо наблюдалось ее снижение. Все изученные эффекты от проводимой терапии были статистически значимыми в пользу лираглутида 3.0 мг.
Влияние на концентрацию глюкозы натощак и нарастающую концентрацию глюкозы у пациентов с сахарным диабетом 2 (СД2) типа с избыточной массой тела и ожирением
По сравнению с плацебо препарат Саксенда® снижал концентрацию глюкозы натощак и среднюю нарастающую постпрандиальную концентрацию глюкозы (через 90 мин после приема пищи, среднее значение для 3 приемов пищи в сутки).
Функция β-клеток поджелудочной железы
Клинические исследования продолжительностью до одного года с применением препарата Саксенда® у пациентов с избыточной массой тела, а также с наличием или отсутствием СД продемонстрировали улучшение и сохранение функции β-клеток поджелудочной железы. Это было показано с использованием таких методов измерения, как гомеостатическая модель оценки функции β-клеток (НОМА-В) и соотношение концентраций проинсулина и инсулина.
Клиническая эффективность и безопасность
Эффективность и безопасность применения препарата Саксенда® для длительной коррекции массы тела в сочетании с низкокалорийной диетой и усилением физической активности была изучена в 4 рандомизированных двойных слепых плацебо-контролируемых исследованиях 3 фазы SCALE, включавших в общей сложности 5358 пациентов.
Масса тела
По сравнению с плацебо при применении препарата Саксенда® было достигнуто более выраженное снижение массы тела у пациентов с ожирением/избыточной массой тела во всех исследованных группах, в т.ч. с наличием или отсутствием предиабета, СД2 и обструктивным апноэ во сне средней или тяжелой степени. Кроме того, среди популяции исследования большая часть пациентов достигла снижения массы тела ≥5% и >10% при применении препарата Саксенда® по сравнению с плацебо. Значительное снижение массы тела наблюдалось также в клиническом исследовании, в котором пациенты достигли среднего показателя снижения массы тела 6% с помощью низкокалорийной диеты в течение 12 недель до начала лечения препаратом Саксенда®. В этом исследовании большее количество пациентов сохранили потерю массы тела, которая была достигнута до начала лечения препаратом Саксенда® по сравнению с плацебо (81.4% и 48.9% соответственно).
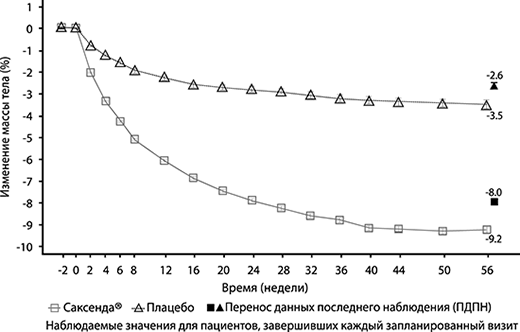
Рис. 1. Изменение массы тела (%) в динамике по сравнению с исходным значением у пациентов в исследовании №1 (0-56 недели).
В клиническом исследовании длительностью 160 недель пациенты, получавшие препарат Саксенда®, достигли более значительной потери массы тела по сравнению с пациентами, получавшими плацебо. В основном потеря массы тела произошла в первый год и удерживалась на протяжении 160 недель.
В клиническом исследовании длительностью 160 недель средний процент изменения массы тела и доля пациентов, достигших потери массы тела от исходного значения до 160 недели не менее чем на 5% и более 10%, были также значительными по сравнению с плацебо.
Снижение массы тела после 12 недель терапии препаратом Саксенда®(лираглутид 3.0 мг)
В двух исследованиях продолжительностью 56 недель после 12 недель терапии препаратом Саксенда® в дозе 3.0 мг 67.5% и 50.4% пациентов достигли снижения массы тела не менее чем на 5%. Среднее снижение массы тела у этих пациентов, завершивших исследование, составило 11.2% по сравнению с исходным значением. У пациентов, достигших снижения массы тела менее чем на 5% после 12 недель терапии в дозе 3.0 мг и завершивших исследование (1 год), среднее снижение массы тела составило 3.8%.
Контроль гликемии
Терапия лираглутидом существенно улучшала гликемические показатели в субпопуляциях с нормогликемией, предиабетом и СД2.
СД2 развился у 0.2% пациентов, получавших препарат Саксенда®, по сравнению с 1.1% в группе плацебо. У 69.2% пациентов с предиабетом наблюдалось обратное развитие этого состояния при применении препарата Саксенда® по сравнению с 32.7% в группе плацебо. На 160-й неделе при продолжении лечения диагноз СД2 был поставлен 3% пациентов, получавшим препарат Саксенда®, и 11% пациентов, получавшим плацебо. По сравнению с плацебо время до развития СД2 при применении лираглутида 3.0 мг было в 2.7 раза больше, а относительный риск (ОР) развития СД2 при применении лираглутида равен 0.2. На 160-й неделе в группе лираглутида 3.0 мг у 65.9% пациентов с предиабетом наблюдалось обратное развитие этого состояния до нормогликемии по сравнению с 36.3% в группе плацебо.
В одном из исследований 69.2% и 56.5% пациентов с ожирением и СД2, получавших препарат Саксенда®, достигли целевого значения HbA1c<7% и ≤6.5% соответственно, по сравнению с 27.2% и 15% у пациентов, получавших плацебо.
Кардиометаболические параметры
По сравнению с плацебо препарат Саксенда® значительно улучшал показатели систолического АД, окружности талии и концентрации липидов натощак.
В клиническом исследовании длительностью 160 недель среднее уменьшение окружности талии составило 8.2 см при применении препарата Саксенда® и 4 см при применении плацебо; уменьшение показателей систолического и диастолического АД составило 4.3 мм рт.ст. и 1.5 мм рт.ст. при применении препарата Саксенда® и 2.7 мм рт.ст. и 1.8 мм рт.ст. при применении плацебо соответственно; уменьшение концентрации холестерина ЛПНП составило 3.1 ммоль/л при применении препарата Саксенда® и 0.7 ммоль/л при применении плацебо; увеличение концентрации холестерина ЛПВП составило 2.3 ммоль/л при применении препарата Саксенда® и 0.5 ммоль/л при применении плацебо.
Индекс апноэ-гипноэ (ИАГ)
По сравнению с плацебо при применении препарата Саксенда® наблюдалось существенное снижение тяжести обструктивного апноэ во сне, которая оценивалась по изменению ИАГ относительно исходного значения.
Иммуногенность
Вследствие потенциальных иммуногенных свойств белковых и пептидных лекарственных препаратов, у пациентов могут появиться антитела к лираглутиду после терапии препаратом Саксенда®. В клиническом исследовании у 2.5% пациентов, получавших препарат Саксенда®, появились антитела к лираглутиду. Образование антител не привело к снижению эффективности препарата Саксенда®.
Оценка сердечно-сосудистых событий
Большие сердечно-сосудистые события (БССС) были оценены группой внешних независимых экспертов и определены как инфаркт миокарда без смертельного исхода, инсульт без смертельного исхода и смерть по причине сердечно-сосудистой патологии. В 5 двойных слепых контролируемых клинических исследованиях 2 и 3 фазы с применением препарата Саксенда® было отмечено 6 БССС у пациентов, получавших препарат Саксенда®, и 10 БССС — у получавших плацебо пациентов. ОР с 95% ДИ составил 0.33 при применении препарата Саксенда® по сравнению с плацебо. В клиническом исследовании 3 фазы среднее увеличение ЧСС составило 2.5 уд./мин у пациентов, получавших препарат Саксенда®. Наибольшее увеличение ЧСС наблюдалось после 6 недель терапии. Это увеличение было обратимым и исчезало после прекращения терапии лираглутидом.
Было проведено многоцентровое, плацебо-контролируемое, двойное слепое клиническое исследование «Эффект и воздействие лираглутида при сахарном диабете: оценка сердечно-сосудистых рисков» (LEADER®).
По сравнению с плацебо лираглутид 1.8 мг существенно снижал риск развития БССС (рисунок 2). ОР развития БССС был стабильно ниже 1 для всех трех сердечно-сосудистых событий.
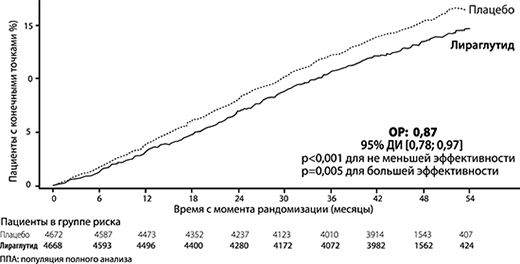
Рис. 2. График Каплан-Мейера — время до возникновения первого БССС — Популяция полного анализа (ППА).
Лираглутид 1.8 мг также существенно снижал риск развития расширенных БССС (первичные БССС, нестабильная стенокардия, приводящая к госпитализации, реваскуляризация миокарда или госпитализация по причине сердечной недостаточности) и прочих вторичных конечных точек.
Дети и подростки
В двойном слепом клиническом исследовании, сравнивающем эффективность и безопасность препарата Саксенда® относительно плацебо в отношении снижения массы тела у подростков в возрасте 12 лет и старше с ожирением, препарат Саксенда® превосходил плацебо в снижении стандартного отклонения ИМТ (измеренного для оценки снижения массы тела) после 56 недель лечения. Большее количество пациентов достигло ≥5% и ≥10% снижения ИМТ на терапии лираглутидом, чем пациенты, получавшие плацебо, при более значительном снижении среднего ИМТ и массы тела. В течение 26 недель последующего наблюдения без применения препарата наблюдалось восстановление массы тела при применении препарата Саксенда® по сравнению с плацебо (оценивалось как изменение стандартного отклонения ИМТ).
Исходя из переносимости, для большинства пациентов (82.4%) доза препарата была увеличена, и они продолжили получать дозу 3.0 мг, для остальных пациентов доза была увеличена, и они продолжили получать препарат в диапазоне доз от 2.4 мг до 0.6 мг.
Результаты определяемых пациентами показателей
Препарат Саксенда® по сравнению с плацебо улучшал определяемые пациентами оценки по нескольким показателям. Было отмечено значительное улучшение общей оценки по Упрощенному опроснику влияния массы тела на качество жизни (IWQoL-Lite) и по всем шкалам опросника для оценки качества жизни SF-36, что указывает на положительное влияние на физический и психологический компоненты качества жизни.
Фармакокинетика
Всасывание
Всасывание лираглутида после п/к введения происходит медленно, время достижения Cmax — около 11 ч после введения. У пациентов с ожирением (ИМТ 30-40 кг/м2) после введения лираглутида в дозе 3.0 мг средняя равновесная концентрация лираглутида (AUCt/24) достигает приблизительно 31 нмоль/л. В диапазоне доз от 0.6 мг до 3.0 мг экспозиция лираглутида увеличивается пропорционально дозе. Абсолютная биодоступность лираглутида после п/к введения составляет приблизительно 55%.
Распределение
Средний кажущийся Vd после п/к введения лираглутида в дозе 3.0 мг составляет 20-25 л (у лиц с массой тела около 100 кг). Лираглутид в значительной степени связывается с белками плазмы крови (>98%).
Метаболизм
На протяжении 24 ч после введения здоровым добровольцам однократной дозы [3Н]-лираглутида главным компонентом в плазме оставался неизмененный лираглутид. Были обнаружены 2 метаболита (≤9% и ≤5% от уровня общей радиоактивности в плазме крови).
Выведение
Лираглутид метаболизируется эндогенно подобно крупным белкам без участия какого-либо специфического органа в качестве основного пути выведения. После введения дозы [3Н]-лираглутида неизмененный лираглутид не определялся в моче или кале. Лишь незначительная часть введенной радиоактивности в виде метаболитов лираглутида выводилась почками или через кишечник (6% и 5% соответственно). Радиоактивные вещества выделяются почками или через кишечник, в основном, в течение первых 6-8 дней и представляют собой 3 метаболита.
Средний клиренс после п/к введения 3.0 мг лираглутида составляет приблизительно 0.9-1.4 л/ч, T1/2 составляет примерно 13 ч.
Фармакокинетика у особых групп пациентов
Пациенты пожилого возраста. Коррекция дозы с учетом возраста не требуется. Согласно результатам популяционного фармакокинетического анализа у пациентов с избыточной массой тела и ожирением в возрасте 18-82 лет возраст не оказывал клинически значимого влияния на фармакокинетику лираглутида при п/к введении в дозе 3.0 мг.
Пол. Основываясь на данных популяционного фармакокинетического анализа, у женщин скорректированный по массе тела клиренс лираглутида после п/к введения в дозе 3.0 мг на 24% меньше, чем у мужчин. На основании данных по ответной реакции на воздействие препарата, коррекции дозы с учетом пола не требуется.
Этническая принадлежность. Согласно результатам популяционного фармакокинетического анализа, в который были включены данные исследований у пациентов с избыточной массой тела и ожирением европеоидной, негроидной, азиатской и латиноамериканской расовых групп, этническая принадлежность не оказывала клинически значимого влияния на фармакокинетику лираглутида при п/к введении в дозе 3.0 мг.
Масса тела. Экспозиция лираглутида уменьшается при увеличении исходной массы тела. Применение лираглутида в дозе 3.0 мг ежедневно обеспечивает адекватную экспозицию в диапазоне массы тела 60-234 кг, согласно оценке ответной реакции на системную экспозицию препарата в клинических исследованиях. Экспозицию лираглутида у пациентов с массой тела больше 234 кг не изучали.
Пациенты с печеночной недостаточностью. Фармакокинетику лираглутида оценивали у пациентов с различной степенью нарушения функции печени в исследовании однократной дозы (0.75 мг). Наблюдалось снижение экспозиции лираглутида на 13-23% у пациентов с печеночной недостаточностью легкой и средней степени тяжести и значительное снижение экспозиции лираглутида (на 44%) у пациентов с печеночной недостаточностью тяжелой степени (>9 баллов по классификации Чайлд-Пью) в сравнении со здоровыми добровольцами.
Пациенты с почечной недостаточностью. В исследовании однократной дозы (0.75 мг) экспозиция лираглутида была меньше у пациентов с почечной недостаточностью по сравнению с лицами с нормальной функцией почек. Экспозиция лираглутида была меньше на 33%, 14%, 27% и 26%, соответственно, у пациентов с почечной недостаточностью легкой (КК 50-80 мл/мин), средней (КК 30-50 мл/мин), тяжелой степени (КК <30 мл/мин) и у пациентов с терминальной стадией почечной недостаточности, нуждающихся в гемодиализе.
Дети и подростки. Фармакокинетические свойства лираглутида 3.0 мг оценивались в клинических исследованиях у подростков с ожирением в возрасте от 12 лет до 18 лет (134 пациента, масса тела 62-178 кг). Экспозиция лираглутида у подростков в возрасте от 12 до 18 лет была сопоставима с наблюдаемой у взрослых пациентов с ожирением.
Фармакокинетические свойства были также оценены в клиническом фармакологическом исследовании с участием детей с ожирением в возрасте от 7 лет до 11 лет (13 пациентов, масса тела 54-87 кг). Экспозиция лираглутида 3.0 мг у детей в возрасте от 7 лет до 11 лет была сопоставима с наблюдаемой у взрослых пациентов после поправки на массу тела.
Показания препарата
Саксенда®
Взрослые
Препарат Саксенда® показан в качестве дополнения к низкокалорийной диете и усиленной физической нагрузке для длительного применения с целью коррекции массы тела у взрослых пациентов с ИМТ:
- ≥30 кг/м2 (ожирение) или
- ≥27 кг/м2 до <30 кг/м2 (избыточная масса тела) при наличии хотя бы одного связанного с избыточной массой тела сопутствующего заболевания, такого как предиабет, сахарный диабет 2 типа, артериальная гипертензия, дислипидемия или синдром обструктивного апноэ во сне.
Подростки
Препарат Саксенда® может быть использован в качестве дополнения к здоровому питанию и усиленной физической нагрузке с целью коррекции массы тела у подростков в возрасте от 12 лет и старше с:
- массой тела свыше 60 кг и
- ожирением (ИМТ, соответствующий ≥30 кг/м2 для взрослых согласно международным пороговым значениям).*
*Пороговое значение ИМТ IOTF для ожирения в зависимости от пола в возрасте от 12 до 18 лет.
Таблица 1. Пороговое значение ИМТ IOTF для ожирения в зависимости от пола в возрасте от 12 до 18 лет
Режим дозирования
Препарат Саксенда® предназначен только для п/к введения. Его нельзя вводить в/в или в/м.
Препарат Саксенда® вводят 1 раз/сут в любое время, независимо от приема пищи. Его следует вводить в область живота, бедра или плеча. Место и время инъекции могут быть изменены без коррекции дозы. Тем не менее, желательно делать инъекции примерно в одно и то же время суток после выбора наиболее удобного времени.
Дозы
Начальная доза составляет 0.6 мг/сут. Дозу увеличивают до 3.0 мг/сут, прибавляя по 0.6 мг с интервалами не менее одной недели для улучшения желудочно-кишечной переносимости (см. таблицу 2). Если при увеличении дозы новая доза плохо переносится пациентом в течение 2 недель подряд, следует рассмотреть вопрос о прекращении терапии. Применение препарата в суточной дозе больше 3.0 мг не рекомендуется.
Таблица 2. Схема увеличения дозы
Взрослые. Терапию препаратом Саксенда® следует прекратить, если после 12 недель применения препарата в дозе 3.0 мг/сут потеря массы тела составила менее 5% от исходного значения.
Подростки. Терапию препаратом Саксенда® следует прекратить и пересмотреть, если после 12 недель применения препарата в дозе 3.0 мг/сут или максимальной переносимой дозе пациенты потеряли менее 4% от своего ИМТ или z-показателя ИМТ.
Пациенты с сахарным диабетом 2 типа
Препарат Саксенда® не следует применять в комбинации с другими агонистами рецепторов ГПП-1.
В начале терапии препаратом Саксенда® рекомендуется уменьшить дозу одновременно применяемого препарата инсулина или секретагогов инсулина (таких как препараты сульфонилмочевины) для уменьшения риска развития гипогликемии. Самоконтроль концентрации глюкозы крови может быть необходим для корректировки дозы инсулина или секретагогов инсулина.
Особые группы пациентов
Коррекция дозы у пациентов пожилого возраста (≥65 лет) не требуется. Опыт применения препарата у пациентов в возрасте ≥75 лет ограничен, применение препарата у этих пациентов не рекомендуется.
У пациентов с почечной недостаточностью легкой или средней степени (КК ≥30 мл/мин) коррекция дозы не требуется. Имеется ограниченный опыт применения препарата Саксенда® у пациентов с почечной недостаточностью тяжелой степени (КК <30 мл/мин). Применение препарата Саксенда® у таких пациентов, включая пациентов с терминальной стадией почечной недостаточности, противопоказано (см. разделы «Фармакокинетика» и «Противопоказания»).
У пациентов с печеночной недостаточностью легкой и средней степени тяжести коррекция дозы не требуется. Применение препарата Саксенда® у пациентов с печеночной недостаточностью тяжелой степени противопоказано. У пациентов с печеночной недостаточностью легкой или средней степени тяжести препарат следует применять с осторожностью (см. раздел «Фармакокинетика» и «Противопоказания»).
Применение препарата Саксенда® у детей и подростков в возрасте до 12 лет или у подростков с массой тела ≤60 кг противопоказано в связи с отсутствием данных (см. раздел «Фармакологическое действие», Клиническая эффективность и безопасность).
Для подростков в возрасте от 12 до 18 лет следует применять такой же режим увеличения дозы, как и для взрослых (см. таблицу 2). Дозу препарата следует увеличивать до тех пор, пока не будет достигнуто значение 3.0 мг (терапевтическая доза) или максимально переносимая доза. Применение препарата в суточной дозе больше 3.0 мг не рекомендуется.
Пропущенная доза
Если после обычного времени введения дозы прошло менее 12 ч, пациент должен ввести дозу как можно быстрее. Если до обычного времени введения следующей дозы осталось менее 12 ч, пациент не должен вводить пропущенную дозу, а должен возобновить введение препарата со следующей запланированной дозы. Не следует вводить дополнительную или повышенную дозу для компенсации пропущенной дозы.
Руководство по применению
Препарат Саксенда® нельзя применять, если он выглядит иначе, чем прозрачная и бесцветная или почти бесцветная жидкость.
Препарат Саксенда® нельзя применять, если он был заморожен.
Препарат Саксенда® можно вводить при помощи игл длиной до 8 мм. Шприц-ручка разработана для использования с одноразовыми иглами НовоФайн® или НовоТвист®. Инъекционные иглы не включены в упаковку.
Пациент должен быть проинформирован о том, что использованную иглу следует выбрасывать после каждой инъекции в соответствии с местными требованиями, а также о том, что шприц-ручку Саксенда® необходимо хранить с отсоединенной иглой. Такая мера позволит предотвратить закупорку игл, загрязнение, инфицирование и вытекание препарата из шприц-ручки и гарантирует точность дозирования.
Инструкция для пациентов по применению препарата Саксенда® раствор для п/к введения 6 мг/мл в предварительно заполненной шприц-ручке
Внимательно прочитайте данную инструкцию перед использованием предварительно заполненной шприц-ручки с препаратом Саксенда®.
Используйте шприц-ручку только после того, как Вы научитесь ею пользоваться под руководством врача или медсестры.
Начните с проверки маркировки на этикетке шприц-ручки, чтобы убедиться, что она содержит препарат Саксенда® 6 мг/мл, а затем внимательно изучите представленные ниже иллюстрации, на которых показаны различные детали шприц-ручки и иглы.
Если Вы слабовидящий или у Вас имеются серьезные проблемы со зрением, и Вы не можете различить цифры на счетчике дозы, не используйте шприц-ручку без посторонней помощи. Помочь Вам может человек с хорошим зрением, обученный использованию предварительно заполненной шприц-ручки с препаратом Саксенда®.
Предварительно заполненная шприц-ручка содержит 18 мг лираглутида и позволяет выбрать дозы 0.6 мг, 1.2 мг, 1.8 мг, 2.4 мг и 3.0 мг. Шприц-ручка разработана для использования с одноразовыми иглами НовоФайн® или НовоТвист® длиной до 8 мм. Иглы не входят в упаковку.
Важная информация: обратите особое внимание на информацию со знаком (!) — это очень важно для безопасного использования шприц-ручки.
Предварительно заполненная шприц-ручка с препаратом Саксенда® и игла (пример)
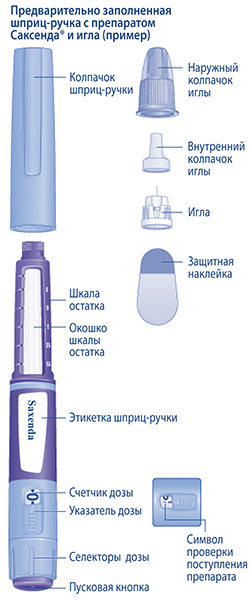
1. Подготовка шприц-ручки с иглой к использованию
- Проверьте название и цветовой код на этикетке шприц-ручки, чтобы убедиться, что в ней содержится препарат Саксенда®. Это особенно важно в том случае, если Вы применяете разные инъекционные препараты. Применение неправильного препарата может быть вредным для Вашего здоровья.
- Снимите колпачок со шприц-ручки (рис. А).

- Убедитесь, что раствор в шприц-ручке прозрачный и бесцветный (рис. В). Посмотрите в окошко шкалы остатка. Если препарат мутный, шприц-ручку использовать нельзя.
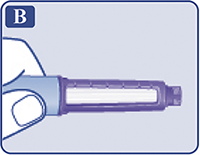
- Возьмите новую иглу и удалите защитную наклейку (рис. С).
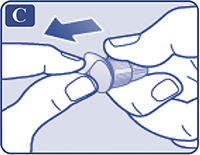
- Наденьте иглу на шприц-ручку и поверните ее, чтобы игла плотно держалась на шприц-ручке (рис. D).
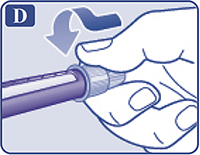
- Снимите наружный колпачок иглы, но не выбрасывайте его (рис. Е). Он понадобится после завершения инъекции, чтобы безопасно снять иглу со шприц-ручки.
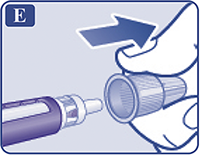
- Снимите и выбросьте внутренний колпачок иглы (рис. F). Если Вы попытаетесь надеть внутренний колпачок обратно на иглу, Вы можете уколоться. На конце иглы может появиться капля раствора. Это нормальное явление, однако Вы все равно должны проверить поступление препарата, если Вы используете новую шприц-ручку в первый раз. Не присоединяйте новую иглу до тех пор, пока Вы не будете готовы сделать инъекцию.
(!) Всегда используйте новую иглу для каждой инъекции. Это может предотвратить закупорку игл, загрязнение, инфицирование и введение неправильной дозы препарата.
(!) Никогда не используйте иглу, если она погнута или повреждена.
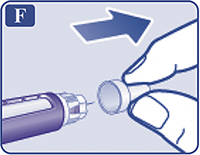
2. Проверка поступления препарата
- Перед первой инъекцией с помощью каждой новой шприц-ручки проверьте поступление препарата. Если шприц-ручка уже находится в использовании, то перейдите к операции 3 «Установка дозы».
- Поворачивайте селектор дозы до тех пор, пока счетчик дозы не поравняется с символом проверки поступления препарата (••—) (рис. А).
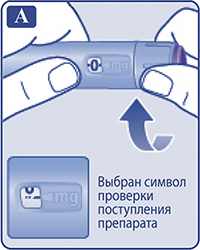
- Держите шприц-ручку иглой вверх. Нажмите пусковую кнопку и удерживайте ее в этом положении, пока счетчик дозы не возвратится к «0» (рис. В). «0» должен стоять напротив указателя дозы.
На конце иглы должна появиться капля раствора. На конце иглы может оставаться маленькая капля, но она не будет введена при инъекции.
Если капля раствора на конце иглы не появилась, необходимо повторить операцию 2 «Проверка поступления препарата», но не более 6 раз. Если капля раствора так и не появилась, следует поменять иглу и повторить операцию 2 «Проверка поступления препарата» еще раз.
Если капля раствора так и не появилась, утилизируйте шприц-ручку и используйте новую.
(!) Всегда перед использованием новой шприц-ручки в первый раз убедитесь в том, что на конце иглы появилась капля раствора. Это гарантирует поступление препарата. Если капля раствора не появилась, препарат не будет введен, даже если счетчик дозы будет двигаться. Это может указывать на то, что игла закупорена или повреждена. Если Вы не проверите поступление препарата перед первой инъекцией с помощью новой шприц-ручки, Вы можете не ввести необходимую дозу и ожидаемый эффект препарата Саксенда® не будет достигнут.
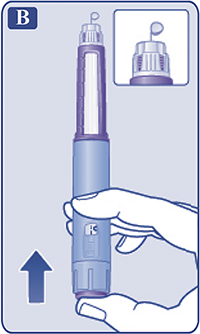
3. Установка дозы
- Поворачивайте селектор дозы до тех пор, пока он не покажет необходимую дозу (0.6 мг, 1.2 мг, 1.8 мг, 2.4 мг или 3.0 мг) (рис. А).
Если доза была выбрана неправильно, Вы можете поворачивать селектор дозы вперед или назад, пока не будет установлена правильная доза.
Максимальная доза, которую можно установить, составляет 3.0 мг.
Селектор дозы позволяет изменить дозу. Только счетчик дозы и указатель дозы покажут количество мг препарата в выбранной Вами дозе.
Вы можете набрать до 3.0 мг препарата на дозу. Если в шприц-ручке содержится менее 3.0 мг, счетчик дозы остановится прежде, чем в окошке появится 3.0.
При каждом повороте селектора дозы раздаются щелчки, звук щелчков зависит от того, в какую сторону вращается селектор дозы (вперед, назад или, если набранная доза превышает количество мг препарата, оставшихся в шприц-ручке). Не считайте эти щелчки.
(!) Всегда перед каждой инъекцией проверяйте, какое количество мг препарата Вы набрали по счетчику дозы и указателю дозы.
Не считайте щелчки шприц-ручки.
Шкала остатка показывает приблизительное количество оставшегося в шприц-ручке раствора, поэтому ее нельзя использовать для отмеривания дозы препарата.
С помощью селектора дозы нужно выбирать только дозы 0.6 мг, 1.2 мг, 1.8 мг, 2.4 мг или 3.0 мг. Выбранная доза должна находиться точно напротив указателя дозы — такое положение гарантирует, что Вы получите правильную дозу препарата.

Сколько препарата осталось?
- Шкала остатка показывает примерное количество оставшегося в шприц-ручке препарата (рис. А).

- Чтобы точно определить, сколько препарата осталось, используйте счетчик дозы (рис. В). Поворачивайте селектор дозы до остановки счетчика дозы. Если он показывает «3.0», в Вашей шприц-ручке осталось, как минимум, 3.0 мг препарата. Если счетчик дозы остановился до того, как в окошке появилось «3.0», то это означает, что в шприц-ручке осталось недостаточное количество препарата, чтобы ввести полную дозу 3.0 мг.
Если Вам необходимо ввести большее количество препарата, чем осталось в шприц-ручке
Только если Вас обучили врач или медсестра, Вы можете разделить дозу препарата между двумя шприц-ручками (той, которая сейчас находится в использовании, и новой). Используйте калькулятор, чтобы спланировать дозы, как рекомендовано врачом или медсестрой.
(!) Будьте очень внимательны, чтобы правильно рассчитать дозу.
Если Вы не уверены в том, как правильно разделить дозу, используя две шприц-ручки, установите и введите полную дозу с помощью новой шприц-ручки.
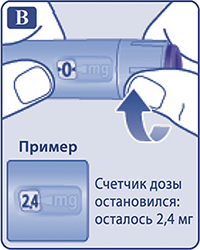
4. Введение препарата
- Введите иглу под кожу, используя технику инъекций, рекомендованную врачом или медсестрой (рис. А).
- Убедитесь, что счетчик дозы находится в поле Вашего зрения. Не дотрагивайтесь до счетчика дозы пальцами — это может прервать инъекцию.
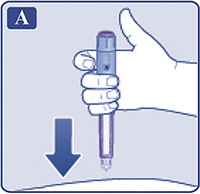
- Нажмите пусковую кнопку до упора и удерживайте ее в этом положении, пока счетчик дозы не покажет «0» (рис. В). «0» должен находиться точно напротив указателя дозы. При этом Вы можете услышать или ощутить щелчок.
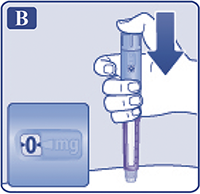
- Удерживайте иглу под кожей, после того, как счетчик дозы возвратился к «0», и медленно считайте до 6 (рис. С).
Если Вы извлечете иглу из-под кожи раньше, Вы можете увидеть, как препарат вытекает из иглы. В этом случае будет введена неполная доза препарата.
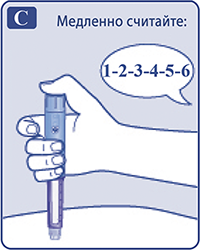
- Извлеките иглу из-под кожи (рис. D). Если в месте инъекции появилась кровь, слегка прижмите к месту укола ватный тампон. Не массируйте место укола.
После завершения инъекции Вы можете увидеть каплю раствора на конце иглы. Это нормально и не влияет на дозу препарата, которую Вы ввели.
(!) Всегда сверяйтесь с показаниями счетчика дозы, чтобы знать, какое количество мг препарата Вы ввели. Удерживайте пусковую кнопку до тех пор, пока счетчик дозы не покажет «0».
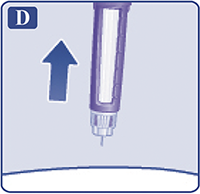
Как выявить закупорку или повреждение иглы?
- Если после долгого нажатия на пусковую кнопку на счетчике дозы не появляется «0», это может означать закупорку или повреждение иглы.
- В этом случае Вы не получили препарат, даже если счетчик дозы изменил положение с исходной дозы, которую Вы установили.
Что делать с закупоренной иглой?
Снимите иглу как описано в операции 5 «После завершения инъекции» и повторите все шаги, начиная с операции 1 «Подготовка шприц-ручки с иглой к использованию». Убедитесь, что установили необходимую Вам дозу.
Никогда не прикасайтесь к счетчику дозы во время введения препарата. Это может прервать инъекцию.
5. После завершения инъекции
- Положив наружный колпачок иглы на плоскую поверхность, введите конец иглы внутрь колпачка, не касаясь его или иглы (рис. А).
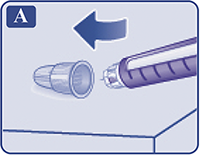
- Когда игла войдет в колпачок, осторожно наденьте наружный колпачок на иглу (рис. В).
- Отвинтите иглу и выбросьте ее, соблюдая меры предосторожности.
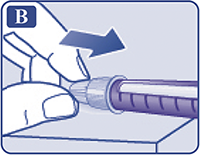
- После каждой инъекции надевайте на шприц-ручку колпачок, чтобы защитить содержащийся в ней раствор от воздействия света (рис. С).
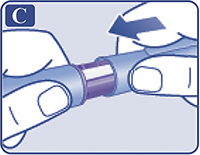
Всегда после каждой инъекции выбрасывайте иглу, чтобы обеспечить комфортную инъекцию и избежать закупорки игл. Если игла закупорена, Вы не введете себе препарат.
Выбрасывайте пустую шприц-ручку с отсоединенной иглой, в соответствии с рекомендациями, данными Вашим врачом, медсестрой, фармацевтом или в соответствии с местными требованиями.
(!) Никогда не пытайтесь надеть внутренний колпачок обратно на иглу. Вы можете уколоться.
(!) Всегда удаляйте иглу со шприц-ручки после каждой инъекции. Это может предотвратить закупорку игл, загрязнение, инфицирование, вытекание раствора и введение неправильной дозы препарата.
(!) Дополнительная важная информация
- Всегда храните шприц-ручку и иглы в недоступном для всех, и в особенности для детей, месте.
- Никогда не передавайте свою шприц-ручку и иглы к ней другим лицам.
- Лица, осуществляющие уход за больным, должны обращаться с использованными иглами с особой осторожностью, чтобы предотвратить уколы иглой и перекрестное инфицирование.
Уход за шприц-ручкой
- Не оставляйте шприц-ручку в автомобиле или любом другом месте, где она может подвергаться воздействию слишком высоких или слишком низких температур.
- Не применяйте препарат Саксенда®, если он был заморожен. В этом случае ожидаемый эффект от применения препарата не будет достигнут.
- Предохраняйте шприц-ручку от попадания на нее пыли, загрязнений и всех видов жидкостей.
- Не мойте шприц-ручку, не погружайте ее в жидкость и не смазывайте ее. При необходимости, шприц-ручку можно очищать влажной тканью, смоченной мягким моющим средством.
- Нельзя ронять или ударять шприц-ручку о твердую поверхность. Если Вы уронили шприц-ручку или сомневаетесь в ее исправности, присоедините новую иглу и проверьте поступление препарата перед тем, как сделать инъекцию.
- Не допускается повторное заполнение шприц-ручки. Пустую шприц-ручку необходимо сразу выбросить.
- Не пытайтесь самостоятельно починить шприц-ручку или разобрать ее на части.
Побочное действие
Безопасность препарата Саксенда® была оценена в 5 двойных слепых плацебо-контролируемых исследованиях, в которых приняли участие 5813 пациентов с ожирением или с избыточной массой тела и, как минимум, с одним связанным с избыточной массой тела сопутствующим заболеванием. В целом, нарушения со стороны ЖКТ являлись наиболее часто отмечаемыми побочными эффектами во время терапии препаратом Саксенда® (см. «Описание отдельных нежелательных реакций»).
В таблице 3 представлен перечень нежелательных реакций, зарегистрированных в ходе долгосрочных контролируемых исследований 2 и 3 фазы. Нежелательные реакции распределены по группам в соответствии с системами органов MedDRA и частотой. Определение частоты нежелательных реакций: очень часто (≥1/10); часто (≥1/100 до <1/10); нечасто (≥1/1000 до <1/100); редко (>1/10000 до <1/1000); очень редко (<1/10000).
Таблица 3. Нежелательные реакции, зарегистрированные в ходе контролируемых исследований 2 и 3 фазы
* Гипогликемия (на основании отмеченных пациентами симптомов и не подтвержденная измерениями концентрации глюкозы крови), отмеченная у пациентов без СД2, получавших препарат Саксенда® в сочетании с диетой и физическими нагрузками. Подробную информацию см. в «Описание отдельных нежелательных реакций».
** Преимущественно отмечали во время первых 3 месяцев терапии.
*** См. раздел «Особые указания».
**** В соответствии с фазами 2, 3a и 3b контролируемого клинического исследования.
Описание отдельных нежелательных реакций
Гипогликемия у пациентов без сахарного диабета 2 типа
В клинических исследованиях с участием пациентов с избыточной массой тела или ожирением без СД2, получавших терапию препаратом Саксенда® в сочетании с диетой и физическими нагрузками, тяжелых гипогликемий (требующих оказания помощи третьим лицом) отмечено не было. О симптомах гипогликемии сообщали 1.6% пациентов, получавших препарат Саксенда®, и 1.1% пациентов, получавших плацебо; однако эти случаи не были подтверждены измерениями концентрации глюкозы крови. В большинстве случаев отмечалась легкая гипогликемия.
Гипогликемия у пациентов с сахарным диабетом 2 типа
В клинических исследованиях с участием пациентов с избыточной массой тела или ожирением и СД2, получавших терапию препаратом Саксенда® в сочетании с диетой и физическими нагрузками, случаи тяжелой гипогликемии (требующие оказания помощи третьим лицом) были отмечены у 0.7% пациентов, получавших препарат Саксенда®, и только у пациентов, одновременно получавших терапию производными сульфонилмочевины. Также в этой группе пациентов подтвержденная гипогликемия (концентрация глюкозы ≤3.9 ммоль/л в сочетании с симптомами) была отмечена у 43.6% пациентов, получавших препарат Саксенда®, и 27.3% пациентов, получавших плацебо. Среди пациентов, не получавших одновременно препарат сульфонилмочевины, подтвержденная гипогликемия была отмечена у 15.7% пациентов, получавших препарат Саксенда®, и у 7.6% пациентов, получавших плацебо.
Гипогликемия у пациентов с сахарным диабетом 2 типа, получающих инсулин
В клинических исследованиях с участием пациентов с избыточной массой тела или ожирением с СД2 типа, получавших терапию инсулином и препаратом Саксенда® в сочетании с диетой и физическими нагрузками и до двух пероральных гипогликемических препаратов, тяжелая гипогликемия (требующая оказания помощи третьим лицом) была отмечена у 1.5% пациентов, получавших терапию препаратом Саксенда®. В данном исследовании подтвержденная гипогликемия (определяемая как уровень глюкозы в плазме ≤3.9 ммоль/л, сопровождаемая симптомами) была зарегистрирована у 47.2% пациентов, получавших терапию препаратом Саксенда®, и у 51.8% пациентов, получавших плацебо. Сообщалось о подтвержденных гипогликемических эпизодах среди пациентов, одновременно получавших производные сульфонилмочевины, у 60.9% пациентов, получавших терапию препаратом Саксенда®, и у 60.0% пациентов, получавших плацебо.
Нежелательные реакции со стороны ЖКТ
Большинство реакций со стороны ЖКТ были легкой или средней степени тяжести, преходящими и, в большинстве случаев, не приводили к прекращению терапии. Реакции обычно возникали в первые недели терапии, и их проявления постепенно уменьшались в течение нескольких дней или недель при продолжении терапии.
У пациентов в возрасте ≥65 лет могут наблюдаться более выраженные проявления нежелательных реакций со стороны ЖКТ во время терапии препаратом Саксенда®.
У пациентов с почечной недостаточностью легкой или средней степени тяжести (КК ≥30 мл/мин) могут наблюдаться более выраженные проявления нежелательных реакций со стороны ЖКТ во время терапии препаратом Саксенда®.
Аллергические реакции
В пострегистрационном периоде сообщалось о возникновении нескольких случаев анафилактических реакций с такими симптомами, как артериальная гипотензия, ощущение сердцебиения, одышка или периферические отеки. Анафилактические реакции потенциально могут быть угрожающими жизни.
Реакции в месте введения
Сообщалось о реакциях в месте введения у пациентов, получавших препарат Саксенда®. Эти реакции, как правило, были легкой степени, носили транзиторный характер и в большинстве случаев исчезали при продолжении терапии.
Тахикардия
В клинических исследованиях тахикардия была отмечена у 0.6% пациентов, получавших препарат Саксенда®, и у 0.1% пациентов, получавших плацебо. Большинство явлений были легкой или средней степени тяжести. Явления были единичными и в большинстве случаев проходили при продолжении терапии препаратом Саксенда®.
Дети и подростки
В клиническом исследовании, проведенном с участием подростков с ожирением в возрасте от 12 до 18 лет, 125 пациентов получали терапию препаратом Саксенда® в течение 56 недель.
В целом, частота развития, тип и степень тяжести нежелательных реакций у подростков с ожирением были сопоставимы с таковыми у взрослых пациентов. Рвота у подростков возникала в два раза чаще по сравнению со взрослыми пациентами.
Никакого влияния на рост или пубертатное развитие обнаружено не было.
Противопоказания к применению
- гиперчувствительность к лираглутиду или любому из вспомогательных веществ препарата;
- медуллярный рак щитовидной железы в анамнезе, в т.ч. в семейном;
- множественная эндокринная неоплазия 2 типа;
- тяжелая депрессия, суицидальные мысли или поведение, в т.ч. в анамнезе.
Противопоказано применение у следующих групп пациентов и при следующих состояниях/заболеваниях в связи с отсутствием данных по эффективности и безопасности:
- почечная недостаточность тяжелой степени (КК менее 30 мл/мин);
- печеночная недостаточность тяжелой степени;
- детский возраст до 12 лет;
- подростки в возрасте от 12 до 18 лет с массой тела ≤60 кг;
- у пациентов в возрасте ≥75 лет;
- беременность;
- период грудного вскармливания;
- хроническая сердечная недостаточность (ХСН) IV функционального класса (в соответствии с классификацией NYHA);
- одновременное применение других препаратов для коррекции массы тела;
- применение в комбинации с другими агонистами рецепторов ГПП-1;
- вторичное ожирение на фоне эндокринологических заболеваний или расстройств пищевого поведения, или на фоне применения лекарственных препаратов, которые могут привести к увеличению массы тела.
У пациентов с сахарным диабетом препарат Саксенда® не должен применяться в качестве заменителя инсулина.
Опыт применения препарата Саксенда® у пациентов с воспалительными заболеваниями кишечника и диабетическим парезом желудка ограничен. Применение лираглутида у таких пациентов не рекомендуется, поскольку оно связано с транзиторными нежелательными реакциями со стороны ЖКТ, включая тошноту, рвоту и диарею.
С осторожностью
Препарат Саксенда® рекомендуется применять с осторожностью у пациентов с печеночной недостаточностью легкой и средней степени тяжести, заболеваниями щитовидной железы и наличием острого панкреатита в анамнезе.
Применение при беременности и кормлении грудью
Беременность
Данные по применению препарата Саксенда® у беременных женщин ограничены. В исследованиях на животных была продемонстрирована репродуктивная токсичность. Потенциальный риск для человека неизвестен.
Применение препарата Саксенда® в период беременности противопоказано. При планировании или наступлении беременности терапию препаратом Саксенда® необходимо прекратить.
Период грудного вскармливания
Неизвестно, проникает ли лираглутид в грудное молоко человека. В исследованиях на животных было продемонстрировано, что проникновение лираглутида и структурно близких метаболитов в грудное молоко является низким. В доклинических исследованиях было продемонстрировано связанное с терапией замедление роста новорожденных крысят, находящихся на грудном вскармливании. В связи с отсутствием опыта применения, препарат Саксенда® противопоказан во время грудного вскармливания.
Фертильность
За исключением незначительного уменьшения числа живых зародышей, результаты исследований на животных не указывают на наличие неблагоприятного влияния на фертильность.
Особые указания
У пациентов с СД нельзя применять препарат Саксенда® в качестве замены инсулина.
Диабетический кетоацидоз отмечался у пациентов, получавших терапию инсулином, после быстрого прекращения или снижения дозы инсулина (см. раздел «Режим дозирования»).
Панкреатит
Применение агонистов рецепторов ГПП-1 ассоциировалось с развитием острого панкреатита. Пациенты должны быть проинформированы о характерных симптомах острого панкреатита.
В случае подозрения на развитие панкреатита применение препарата Саксенда® следует прекратить; в случае подтверждения острого панкреатита терапию препаратом Саксенда® возобновлять не следует.
Холелитиаз и холецистит
В клинических исследованиях была отмечена более высокая частота развития холелитиаза и холецистита у пациентов, получавших препарат Саксенда®, по сравнению с получавшими плацебо пациентами. Это может быть частично объяснено тем, что значительное снижение массы тела при применении препарата Саксенда® может увеличить риск развития холелитиаза и, следовательно, холецистита. Холелитиаз и холецистит могут привести к госпитализации и холецистэктомии. Пациенты должны быть проинформированы о характерных симптомах холелитиаза и холецистита.
Заболевания щитовидной железы
В ходе клинических исследований с участием пациентов с СД2 были отмечены нежелательные реакции со стороны щитовидной железы, включая увеличение концентрации кальцитонина в сыворотке крови, зоб и новообразование щитовидной железы, в особенности у пациентов, уже имеющих заболевания щитовидной железы. У пациентов с заболеваниями щитовидной железы препарат Саксенда® следует применять с осторожностью.
В постмаркетинговом периоде у пациентов, получавших лираглутид, были отмечены случаи медуллярного рака щитовидной железы. Имеющихся данных недостаточно для установления или исключения причинно-следственной связи возникновения медуллярного рака щитовидной железы с применением лираглутида у человека. Препарат Саксенда® противопоказан к применению у пациентов с медуллярным раком щитовидной железы в анамнезе, в т.ч. в семейном, и множественной эндокринной неоплазией 2 типа. Необходимо проинформировать пациента о риске медуллярного рака щитовидной железы и о симптомах опухоли щитовидной железы (уплотнения в области шеи, дисфагия, одышка, непроходящая охриплость голоса).
Текущий контроль концентрации кальцитонина в сыворотке крови или УЗИ щитовидной железы не имеют существенного значения для раннего выявления медуллярного рака щитовидной железы у пациентов, применяющих препарат Саксенда®. Значительное повышение концентрации кальцитонина в сыворотке крови может свидетельствовать о наличии медуллярного рака щитовидной железы, пациенты с медуллярным раком щитовидной железы обычно имеют концентрацию кальцитонина более 50 нг/л. При выявлении повышения концентрации кальцитонина в сыворотке крови необходимо провести дальнейшее обследование пациента. Пациенты с узлами щитовидной железы, выявленными при медосмотре или при УЗИ щитовидной железы, также должны быть дополнительно обследованы.
Частота сердечных сокращений
В клинических исследованиях было отмечено увеличение ЧСС (см. раздел «Фармакологическое действие» — Клиническая эффективность и безопасность). Следует проводить контроль ЧСС с интервалами, соответствующими обычной клинической практике. Пациентов следует проинформировать о симптомах тахикардии (ощущение сердцебиения или ощущение учащенного сердцебиения в покое). У пациентов с клинически значимой постоянной тахикардией в состоянии покоя следует прекратить терапию препаратом Саксенда®.
Обезвоживание
Признаки и симптомы обезвоживания, включая нарушение функции почек и острую почечную недостаточность, были отмечены у пациентов, получавших агонисты рецепторов ГПП-1. Пациенты, получающие препарат Саксенда®, должны быть проинформированы о потенциальном риске обезвоживания, связанного с побочными эффектами со стороны ЖКТ, и о необходимости профилактики гиповолемии.
Гипогликемия у пациентов с избыточной массой тела или ожирением и сахарным диабетом 2 типа
Риск развития гипогликемии может быть выше у пациентов с СД2, получающих препарат Саксенда® в комбинации с производными сульфонилмочевины. Этот риск может быть уменьшен путем снижения дозы производного сульфонилмочевины. Добавление препарата Саксенда® к терапии у пациентов, получающих инсулин, не оценивали.
Суицидальные мысли и поведение
В ходе клинических исследований 6 (0.2%) из 3384 пациентов, получавших препарат Саксенда®, сообщили о появлении суицидальных мыслей, один из пациентов предпринял попытку суицида. У пациентов (1941 человек), получавших плацебо, это отмечено не было. Пациентов необходимо контролировать в отношении появления или ухудшения депрессии, суицидальных мыслей или поведения, и/или любых неожиданных изменений в настроении или поведении. У пациентов с суицидальными мыслями или поведением применение препарата Саксенда® следует прекратить.
Противопоказано применять препарат Саксенда® у пациентов с суицидальными попытками или активными суицидальными мыслями в анамнезе.
Рак молочной железы (РМЖ)
В ходе клинических исследований сообщалось о подтвержденном РМЖ у 14 (0.6%) из 2379 женщин, получавших препарат Саксенда®, по сравнению с 3 (0.2%) из 1300 женщин, получавших плацебо, включая инвазивный рак (11 случаев у женщин, получавших препарат Саксенда®, и 3 случая у женщин, получавших плацебо) и внутрипротоковая карцинома in situ (3 случая у женщин, получавших препарат Саксенда®, и 1 случай у женщины, получавшей плацебо). Большинство случаев рака были эстроген- и прогестерон-зависимыми. Невозможно определить, были ли эти случаи связаны с применением препарата Саксенда® из-за их слишком небольшого количества. Кроме того, нет достаточных данных, чтобы определить, оказывает ли препарат Саксенда® влияние на уже существующие новообразования молочной железы.
Папиллярный рак щитовидной железы
В ходе клинических исследований сообщалось о подтвержденной папиллярной карциноме щитовидной железы у 7 (0.2%) из 3291 пациентов, получавших препарат Саксенда®, по сравнению с отсутствием ее в группе пациентов, получавших плацебо (1843 пациента). Из всех случаев 4 карциномы были менее 1 см в наибольшем диаметре и 4 были диагностированы по результатам гистологии после проведенной по медицинским показаниям тиреоидэктомии.
Неоплазии ободочной и прямой кишки
В ходе клинических исследований сообщалось о подтвержденных доброкачественных неоплазиях ободочной и прямой кишки (преимущественно аденомах ободочной кишки) у 17 (0.5%) из 3291 пациентов, получавших препарат Саксенда®, по сравнению с 4 (0.2%) из 1843 пациентов, получавших плацебо. Было зарегистрировано два подтвержденных случая злокачественной карциномы ободочной и прямой кишки (0.1%) у пациентов, получавших препарат Саксенда®, и ни одного у пациентов, получавших плацебо.
Нарушения сердечной проводимости
В ходе клинических исследований у 11 (0.3%) из 3384 пациентов, получавших препарат Саксенда®, сообщалось о развитии нарушений сердечной проводимости, таких как AV-блокада I степени, блокада правой ножки пучка Гиса или блокада левой ножки пучка Гиса. У пациентов (1941 человек), получавших плацебо, о развитии нарушений сердечной проводимости не сообщалось.
Доклинические данные по безопасности
Доклинические данные, основанные на исследованиях фармакологической безопасности, токсичности повторных доз и генотоксичности, не выявили какой-либо опасности для человека.
В двухлетних исследованиях канцерогенности у крыс и мышей были выявлены опухоли С-клеток щитовидной железы, не приводившие к летальному исходу. Результаты, полученные в ходе исследований на грызунах, обусловлены тем, что грызуны проявляют особую чувствительность в отношении опосредуемого рецептором ГПП-1 не генотоксичного специфического механизма. Появления других новообразований, связанных с проводимой терапией, отмечено не было.
В исследованиях на животных не выявлено прямого неблагоприятного эффекта препарата на фертильность, но было отмечено незначительное увеличение частоты ранней эмбриональной смерти при применении самых высоких доз препарата.
Влияние на способность к управлению транспортными средствами и механизмами
Препарат Саксенда® не влияет или незначительно влияет на способность к управлению транспортными средствами и механизмами. В связи с риском развития гипогликемии при применении препарата, особенно при комбинированном применении с препаратами сульфонилмочевины у пациентов с СД2, следует соблюдать осторожность при управлении транспортными средствами и механизмами.
Передозировка
Симптомы: по данным клинических исследований и пострегистрационного применения лираглутида были зарегистрированы случаи передозировки при применении препарата в дозе от 72 мг (в 24 раза больше рекомендуемой для коррекции массы тела). Пациенты отмечали сильную тошноту, сильную рвоту и тяжелую гипогликемию.
Лечение: в случае передозировки необходимо начать поддерживающую терапию в соответствии с клиническими признаками и симптомами. Пациента следует наблюдать на предмет клинических признаков обезвоживания и контролировать концентрацию глюкозы в крови.
Лекарственное взаимодействие
Оценка взаимодействия лекарственных средств in vitro
Лираглутид показал очень низкую способность к лекарственному фармакокинетическому взаимодействию, обусловленному метаболизмом в системе цитохрома Р450 (CYP), а также связыванием с белками плазмы.
Оценка взаимодействия лекарственных средств in vivo
Небольшая задержка опорожнения желудка при применении лираглутида может влиять на всасывание одновременно применяемых препаратов для приема внутрь. Исследования лекарственного взаимодействия не показали какого-либо клинически значимого замедления всасывания этих препаратов, поэтому коррекции дозы не требуется.
Исследования взаимодействия проводили с применением лираглутида в дозе 1.8 мг. Влияние на скорость опорожнения желудка было одинаковым при применении лираглутида в дозе 1.8 мг и 3.0 мг (AUC0-300 мин парацетамола). У нескольких пациентов, получавших лечение лираглутидом, отмечалось как минимум по одному эпизоду тяжелой диареи. Диарея может оказывать влияние на всасывание пероральных лекарственных препаратов, которые применяются одновременно с лираглутидом.
Варфарин и другие производные кумарина
Исследования по взаимодействию не проводились. Не может быть исключено клинически значимое взаимодействие с действующими веществами с низкой растворимостью или узким терапевтическим индексом, такими как варфарин. В начале лечения препаратом Саксенда® у пациентов, получающих варфарин или другие производные кумарина, рекомендуется чаще проводить мониторинг МНО.
Парацетамол (ацетаминофен)
Лираглутид не изменял общую экспозицию парацетамола после введения однократной дозы парацетамола 1000 мг. Cmax парацетамола была снижена на 31%, а медиана Tmax увеличена на 15 мин. Коррекция дозы при сопутствующем применении парацетамола не требуется.
Аторвастатин
Лираглутид не изменял общую экспозицию аторвастатина после применения однократной дозы аторвастатина 40 мг. Поэтому коррекция дозы аторвастатина при применении в сочетании с лираглутидом не требуется. Cmax аторвастатина была снижена на 38%, а медиана Tmax увеличена с 1 ч до 3 ч при применении лираглутида.
Гризеофульвин
Лираглутид не изменял общую экспозицию гризеофульвина после применения однократной дозы гризеофульвина 500 мг. Сmax гризеофульвина была увеличена на 37%, а медиана Tmax не изменилась. Коррекция дозы гризеофульвина и других соединений с низкой растворимостью и высокой проникающей способностью не требуется.
Дигоксин
Применение однократной дозы дигоксина 1 мг в сочетании с лираглутидом привело к уменьшению AUC дигоксина на 16%, уменьшению Сmax на 31%. Медиана Tmax дигоксина увеличилась с 1 ч до 1.5 ч. С учетом данных результатов, коррекции дозы дигоксина не требуется.
Лизиноприл
Применение однократной дозы лизиноприла 20 мг в сочетании с лираглутидом привело к уменьшению AUC лизиноприла на 15%, уменьшению Сmax на 27%. При применении лираглутида медиана Tmax лизиноприла увеличилась с 6 ч до 8 ч. С учетом данных результатов, коррекции дозы лизиноприла не требуется.
Пероральные контрацептивы
Лираглутид приводил к уменьшению Сmax этинилэстрадиола и левоноргестрела на 12% и 13%, соответственно, после применения однократной дозы перорального гормонального контрацептивного препарата. Tmax обоих лекарственных веществ на фоне применения лираглутида увеличивалась на 1.5 ч. Не было отмечено клинически значимого влияния на системную экспозицию этинилэстрадиола или левоноргестрела. Таким образом, не ожидается влияния на контрацептивный эффект при совместном применении с лираглутидом.
Несовместимость
Лекарственные вещества, добавленные к препарату Саксенда®, могут вызвать разрушение лираглутида. В связи с отсутствием исследований совместимости данный лекарственный препарат нельзя смешивать с другими лекарственными препаратами.
Условия хранения препарата Саксенда®
Препарат следует хранить в недоступном для детей месте при температуре от 2° до 8°С (в холодильнике), но не рядом с морозильной камерой. Не замораживать.
Используемую шприц-ручку с препаратом хранить при температуре не выше 30°С или в холодильнике (при температуре от 2°С до 8°С). Не замораживать. Использовать в течение 1 месяца. Закрывать шприц-ручку колпачком для защиты от света.
Срок годности препарата Саксенда®
Срок годности — 30 месяцев. Не применять по истечении срока, указанного на этикетке шприц-ручки и упаковке.
Условия реализации
Препарат отпускается по рецепту.
Контакты для обращений
НОВО НОРДИСК ООО
(Россия)

|
|
121614 Москва, |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код

БЛОК РОТАЦИИ ДЛЯ
КОНДИЦИОНЕРОВ
SB015

2
Содержание
Назначение ……………………………………………………………………..3
Меры безопасности……………………………………………………………..3
Описание прибора………………………………………………………………3
Технические характеристики…………………………………………………..4
Описание работы………………………………………………………………..4
Монтаж и настройка ………………………………………………………….4
Варианты подключения …………………………………………………….…5
Индикация работы ……………………………………………………………10
Комплектность поставки…………………………………………………….…10
Гарантийные обязательства………………………………………………….…10

3
Назначение
Блок ротации SB015 предназначен для выполнения следующих задач:
1) Обеспечить равномерное использование 2-х кондиционеров путем
попеременного их подключения.
2) При нехватке мощности охлаждения помещения одним
кондиционером, автоматически подключить второй, для поддержания
заданного температурного режима.
3) В случае выхода из строя одного из кондиционеров, блок ротации обеспечит автоматическое включение второго кондиционера, с целью обеспечить заданный температурный режим. Меры безопасности:
При эксплуатации и техническом обслуживании необходимо соблюдать требования ГОСТ 12.3.019 «Правила технической эксплуатации электроустановок потребителей» и «Правила техники безопасности при эксплуатации электроустановок потребителей».
Внимание! На открытых контактах при эксплуатации присутствует напряжение 220В 50Гц. Опасно для жизни.
Любые подключения к блоку ротации производить только при отключенном напряжении питания. Описание блока ротации SB015
Блок ротации SB015 выполнен в пластиковом корпусе с креплением на дин-рельс. На лицевой панели блока расположены:
две ручки настройки уставки температуры; два светодиодных индикатора статуса работы кондиционеров; светодиодный индикатор сигнала «Аварийный режим»; светодиодный индикатор температуры в помещении.

4
Технические характеристики блока ротации SB015 Максимальный ток коммутации кондиционеров 23А Максимальный ток аварийного реле 3А Напряжение питания 220АС Мощность потребления 3Вт Количество подключаемых кондиционеров, шт. 2 Габариты, мм 90×71.5×57.2 Тип датчиков температуры NTC10K Установка и настройка блока ротации
Блок ротации SB015 размещается в электрощите, и крепиться на дин-рельс.
Настройка прибора осуществляется с помощью 2 ручек: температура уставки;
Задаем нужное значение температуры (уставку) в помещении, поддержание которой должна обеспечивать система кондиционирования. Уставку задаем при помощи вращающейся ручки, название которой соответствует настраиваемому параметру.
аварийная температура. Выбирается значение температуры, при которой блок ротации SB015
включит аварийное реле и включит оба кондиционера для быстрого
возвращения к температуре уставки. При достижении аварийной
температуры в помещении, на соответствующем индикаторе загорится
красный светодиод, что говорит о превышении заданного значения.
Аварийная температура задается вращающейся ручкой, название которой
соответствует настраиваемому параметру.
Кнопка ТЕСТ.
Кнопка тест предназначена для проверки блока ротации. Необходимо
нажать и удерживать кнопку в нажатом состоянии не менее 5сек. В данном
режиме запускаются оба кондиционера на 10 минут с последующим
автоматическим отключением режима тест.
При повторном нажатии кнопки во время работы двух кондиционеров,
тестовый режим выключается.

5
Описание работы с вариантами подключения. 1) Эксплуатация блока ротации SB 015 без температурных
датчиков.
Рис.1. Подключение блока ротации SB015 без температурных датчиков
При использовании схемы включения представленной на рис.1, блок ротации
работает в режиме таймера, то есть каждые 8 часов происходит
автоматическое переключение кондиционеров. Тем самым обеспечивается
равномерный износ каждого кондиционера. Общая схема подключения
кондиционеров представлена на рис.5. и рис.5.1. Настройка системы
сводиться к установке температуры на кондиционерах.
Важно: В этом случае кондиционеры должны иметь одинаковую
температуру уставки. Реле аварии¹ не используется.
Реле аварии предназначено для удаленного оповещения оператора о неисправности
системы, а так же использование сухих контактов реле позволяет использовать его для
интеграции в систему диспетчеризации.

6
2) Эксплуатация блока SB015 ротации с одним датчиком
температуры в помещении, комнатный датчик температуры
подключен к контактам 13, 14 блока ротации.
Рис.2. Подключение блока ротации SB015 с использованием одного комнатного
датчика температуры для контроля превышения аварийной температуры
При использовании схемы включения представленной на рис.2, блок
ротации работает в режиме таймера, то есть каждые 8 часов происходит
автоматическое переключение кондиционеров. Дополнительно ведется
контроль температуры в помещении на превышении аварийного значения
уставки. При превышении температуры аварийного значения уставки, блок
ротации обеспечивает включение второго кондиционера, и одновременно
включается выход аварийного реле, что обеспечивает удаленный контроль.
При возвращении температуры в заданное значение, второй кондиционер
отключается, работа системы кондиционирования продолжается в штатном
режиме.
Комнатный датчик температуры в данном случае подключается к контактам
13, 14 блока ротации. Для настройки системы необходимо выставить
желаемую температуру поддержания на кондиционерах и ручкой на блоке
SB015 установить аварийное значение температуры.
Важно: В этом случае, кондиционеры должны иметь одинаковую
температуру уставки.

7
3) Эксплуатация блока ротации SB015 с одним датчиком
температуры в помещении, комнатный датчик температуры подключен
к контактам 9, 10 блока ротации.
Рис.3. Подключение блока ротации SB015 с использованием одного комнатного
датчика температуры для поддержания заданной температуры
При использовании схемы включения представленной на рис.3, блок
ротации поддерживает температуру в помещении путем включения и
выключения кондиционеров поочередно или одновременно в зависимости от
температуры. Дополнительно осуществляется контроль превышения
аварийной температуры.
Комнатный датчик температуры в данном случае подключается к
контактам 9, 10 блока ротации. Для настройки системы необходимо
установить минимальную температуру поддержания на кондиционерах и
ручками на блоке SB015 установить температуру поддержания в помещении
и аварийное значение температуры.
Важно: В этом случае кондиционеры должны иметь минимальную
температуру уставки.
4) Эксплуатация блока SB015 ротации с одним комнатным
датчиками температуры, и двумя датчиками контроля работы
кондиционеров.

8
Рис.4. Подключение блока ротации SB015 с использованием одного комнатного
датчика температуры и двух датчиков контроля температуры кондиционеров
Блок ротации поддерживает температуру в помещении путем
включения и выключения кондиционеров поочередно или одновременно в
зависимости от температуры. Так же осуществляется контроль
работоспособности кондиционеров и контроль аварийной температуры.
Комнатный датчик температуры подключаем к контактам 9, 10 блока
ротации, температурные датчики контроля температуры кондиционеров
подключаем к контактам 11, 12 и 15, 16 для каждого кондиционера
соответственно. Датчики контроля температуры должны быть закреплены на
внутренних блоках кондиционеров и попадать в поток холодного воздуха.
Датчики температуры не имеют полярности.
Кондиционер, подключенный к контактам 1 и 2, соответствует
значение температуры от датчика, подключенного к контактам 11 и 12.
Кондиционер, подключенный к контактам 3 и 4, соответствует значение
температуры от датчика, подключенного к контактам 15 и 16. Для настройки
системы необходимо установить минимальную температуру поддержания на
кондиционерах и ручками на блоке SB015 установить температуру
поддержания в помещении, и аварийное значение температуры.
Важно: В этом случае, кондиционеры должны иметь минимальную
температуру уставки.
Обобщенная схема подключение кондиционеров к блоку ротации SB015.
Для работы блока ротации, на контакты 7 и 8 подаем питание 220В.

9
В зависимости от варианта подачи питания к кондиционерам, необходимо
выбрать нужную схему включения.
Ввод питания во внутренний блок кондиционера.
Рис.5. схема подключения кондиционера при питании от внутреннего блока
Для подключения блока ротации SB015 к кондиционерам необходимо
питающий провод от автомата защиты подключить к контактам 1(3)
соответственно. Затем соединить контакты 2(4) блока ротации с вводной
колодкой кондиционеров, согласно схеме прилагаемой в комплекте с
кондиционером.
Ввод питания от наружного блока кондиционера.
Рис.5.1. Схема подключения кондиционера при питании от наружного блока
Подключения блока ротации SB015 к кондиционерам необходимо
осуществить следующим образом: питающий провод идущий от наружного
блока к внутреннему, подключить к контакту 1 для первого кондиционера (3
для второго кондиционера) блока ротации. Затем соединить контакт 2 для
первого кондиционера (4 для второго кондиционера) блока ротации с
вводной колодкой кондиционеров, согласно схеме прилагаемой в комплекте
с кондиционером.

10
Индикация работы Индикация работы осуществляется с помощью четырех светодиодов. 1) Индикатор температуры в помещении:
ниже уставки – горит зеленый; выше уставки – горит красный; в норме – горит желтый.
2) Индикатор кондиционера (для каждого кондиционера свой). команда на включение – моргает зеленый; кондиционер работает – горит зеленый; кондиционер неисправен – моргает красный.
3)Индикатор работы системы в целом. нет неисправностей – горит зеленый;
есть неисправности – горит красный
Комплектность поставки.
Блок ротации кондиционеров SB015 1шт.
Комнатный датчик температуры 1шт.
Датчик контроля температуры кондиционера 2шт.
Гарантийные обязательства
Производитель гарантирует соответствие прибора техническим
условиям при соблюдении потребителем условий монтажа и эксплуатации.
Гарантийный срок непрерывной работы 2 года со дня продажи.
В случае выхода из строя блока ротации SB015 в период гарантийного
срока, необходимо обратиться в фирму «Спинбрэйн Про» по адресу:
г.Санкт-Петербург, улица Якорная, дом 9«А» офис 47.
Дата продажи «__ »_________20 г

В данной статье подробно расскажем об особенностях работы блока ротации SB015. Данный блок можно использовать максимум с двумя кондиционерами.
УСТРОЙСТВО, НАЗНАЧЕНИЕ, ОСОБЕННОСТИ РАБОТЫ БЛОКА РОТАЦИИ
Для начала перечислим все возможные варианты, под которыми можно встретить устройство, управляющее двумя и более кондиционерами:
1) Блок ротации кондиционеров;
2) Согласователь работы кондиционеров;
3) Система ротации кондиционеров;
Первые три варианта используют проводное подключение кондиционеров и обязательное наличие функции «Рестарт» в подключаемых кондиционерах.
4) Контроллер для мониторинга работы кондиционеров в серверной.
Контроллер — это более сложное устройство, предоставляющее пользователю практически безграничные возможности в мониторинге за работой кондиционеров в серверных помещениях в любой точке нашей планеты, при наличии работающей сети интернет.
Во всех перечисленных случаях, речь идет о приборе, который включает и выключает кондиционеры через установленные интервалы времени, контролирует заданное значение температуры в помещении серверной, уведомляет обслуживающий персонал о любых изменениях температурного режима в серверной.
На примере блока ротации, модель SB015 , ниже будут раскрыты его алгоритмы работы в различных ситуациях и вариантах настройки.
В комплект входит:
Собственно сам блок ротации SB015;
Два датчика температуры для контроля работоспособности каждого подключенного кондиционера;
Комнатный датчик температуры, для постоянного мониторинга температуры в помещении
Далее детально рассмотрим, что есть на лицевой панели блока ротации

Для правильного подключения кондиционеров и датчиков температуры к блоку ротации SB015, предусмотрена подсказка. Она выполнена в виде наклейки и размещена сбоку на пластиковом корпусе согласователя кондиционеров.

После подключения кондиционеров и датчиков, блок ротации будет работать по одному из следующих сценариев:
Сценарий №1
Подключены все датчики температуры из комплекта поставки, в том числе подключен и комнатный датчик температуры. В данном случае блок ротации SB015 выполняет полный контроль за работой каждого из кондиционеров. Светодиодная индикация покажет красным цветом, если кондиционер перестал холодить (то есть нет перепада температур). Если светодиод моргает зеленым цветом, значит система кондиционирования серверной работает в штатном режиме.
Переключение кондиционеров произойдет через 8 часов непрерывной работы одного из них.
Также второй кондиционер включится в следующих ситуациях:
первый кондиционер перестал холодить;
температура в помещении превысила заданное значение;
Сценарий №2
Подключены только два датчика контроля работы кондиционеров, комнатный датчик не подключен. В данном случае, блок ротации SB015 будет осуществлять только переключение кондиционеров каждые 8 часов (другими словами работа по таймеру). Второй кондиционер не будет подключен в этом случае.
Сценарий №3
Подключен только комнатный датчик температуры, в таком случае алгоритм и логику работы блока ротации нагляднее будет рассмотреть на блок-схеме ниже.
Итак, мы разобрали по полочкам все возможные варианты работы блока ротации SB015.
Осталось разобраться со светодиодной индикацией, которая сопровождает работу нашего блока.
Светодиод «Статус» горит зеленым постоянно, блок ротации работает штатно;
Светодиод «Статус» горит красным постоянно, перегрев одного из датчиков температуры;
Светодиод «Т помещения» горит зеленным, температура в норме;
Светодиод «Т помещения» горит красным, температура в помещении выше установленного значения;
Светодиоды Кондиционер 1 и Кондиционер 2
При подключении всех датчиков температуры
— моргает зеленым цветом, кондиционер работает штатно;
— горит красным цветом, отсутствует минимальный перепад температуры на входе и выходе на внутреннем блоке теплобменника кондиционера. В данном случае нужно проверить кондиционер на работоспособность.
При подключении только комнатного датчика температуры к блоку ротации.
Светодиоды Кондиционер 1 и кондиционер 2 горят постоянно, в зависимости от работающего в данный момент, или горит два светодиода, если два кондиционера работают вместе.
Более подробная техническая информация и инструкция к блоку ротации находится здесь, в карточке товара.
В данной статье, мы разобрались что обычно имеют ввиду люди, употребляя термин блок ротации, какие они бывают.
Детально разобрали особенности модели SB015. Включение и алгоритмы работы, в зависимости от типа подключения.
Источник
Блок ротации двух кондиционеров SB015
Блок ротации двух кондиционеров SB015 предназначен для управления кондиционерами (резервированием) в серверных помещениях с выполнением следующих задач:Обеспечить равномерное использование 2-х кондиционеров путем попеременного их подключения;При нехватке мощности охлаждения помещения одним кондиционером, автоматически подключит второй, для поддержания заданного температурного режима;В случае выхода из строя одного из кондиционеров, блок ротации обеспечит автоматическое включение второго кондиционера, с целью обеспечить заданный температурный режим.Основные технические характеристикиПри отключении питания и повторном его появлении, блок ротации сохраняеет все уставки, сделанные при его настройке.Габаритные размеры90×71.5×57.2Напряжение питания220АСПотребляемая мощность3ВтМаксимальный коммутируемый ток23АМаксимальный ток выхода "аварияŗАТочность поддержания температуры, гр.Ц1Тип термодатчиковNTC10Диапазон уставки температуры18-30Диапазон уставки аварийной температуры23
Блок ротации двух кондиционеров SB015 предназначен для управления кондиционерами (резервированием) в серверных помещениях с выполнением следующих задач:Обеспечить равномерное использование 2-х кондиционеров путем попеременного их подключения;При нехватке мощности охлаждения помещения одним кондиционером, автоматически подключит второй, для поддержания заданного температурного режима;В случае выхода из строя одного из кондиционеров, блок ротации обеспечит автоматическое включение второго кондиционера, с целью обеспечить заданный температурный режим.Основные технические характеристикиПри отключении питания и повторном его появлении, блок ротации сохраняеет все уставки, сделанные при его настройке.Габаритные размеры90×71.5×57.2Напряжение питания220АСПотребляемая мощность3ВтМаксимальный коммутируемый ток23АМаксимальный ток выхода "аварияŗАТочность поддержания температуры, гр.Ц1Тип термодатчиковNTC10Диапазон уставки температуры18-30Диапазон уставки аварийной температуры23
Время доставки согласовывается с менеджером Службы доставки, который свяжется с Вами сразу после того, как Вы разместите заказ.
Доставка выполняется по рабочим дням. Товары, заказанные в субботу и воскресенье, доставляются в понедельник. Время осуществления доставки зависит от времени размещения заказа и наличия товара на складе.
Варианты и стоимость доставки:
Вы можете рассчитать стоимость доставки транспортной компанией:
Источник
Блок ротации кондиционеров: устройство, правила подключения и настройки модуля
Согласователь работы кондиционеров: назначение, необходимость, характеристики
Серверное помещение отводится для установки телекоммуникационного оборудования, предназначенного для хранения и обработки информации. К дата-центру предъявляются требования по влажности и температуре воздуха. Поддержанием оптимального микроклимата занимается кондиционер. Сплит-система не в состоянии выдержать режим работы без отключения круглые сутки. Чтобы обеспечить бесперебойное охлаждение помещения устанавливаются резервные климатические установки. Контролирует их устройство ротации кондиционеров.
Назначение блока ротации кондиционера

Для обеспечения стандартных климатических параметров в серверных устанавливается кондиционер. Одно устройство не может гарантировать бесперебойное охлаждение дата-центра. На случай поломки и сервисного обслуживания необходима резервная мощность. Монтаж двух и больше кондиционеров обеспечивает надежную защиту от перегрева дорогостоящего оборудования. Сплит-системы функционируют поочередно, включаясь через определенный промежуток времени. Последовательность их работы контролирует ротационный блок управления кондиционером.
Автоматическое устройство исключает необходимость вмешательства человека. Согласователь работы кондиционеров включает и выключает их через равные промежутки времени. Процедура осуществляется изменением подачи напряжения. Система управления снабжена тремя датчиками температуры: один устанавливается в комнате, два других распределяются между внутренними модулями кондиционеров. Поочередная работа установок способствует равномерному износу и распределению нагрузки.
Назначение блока согласования:
- Переключение напряжения с неисправного оборудования на резервное с оповещением о поломке.
- Чередование включения климатических установок, обеспечивающих заданный температурный режим в помещении.
- В случае временных проблем с электропитанием производится автоматический перезапуск сплит-систем.
- Предотвращается несанкционированное выключение климатического оборудования с пульта управления и внесение изменений заданных параметров температуры.
- Контроль температуры в серверной, при значительном повышении показателей подключение двух кондиционеров одновременно.
Подключение блока ротации для промышленных климатических систем
Промышленные системы кондиционирования отличаются от бытовых высокой мощностью компрессора, позволяющей увеличить производительность, длину трубопровода и диапазон рабочих температур. На объектах с большим тепловыделением устанавливается дополнительное оборудование в формате 100% резерва. Оно оснащается функцией “Авторестарт”, которая позволяет после отключения электричества автоматически вводить сплит-системы в эксплуатацию с сохранением всех настроек.
Подключение блока ротации для 2-х кондиционеров для серверной осуществляется несколькими способами:
- проводное, по питанию;
- по ИК каналу;
- сухой контакт.
Внутренние блоки климатических систем устанавливаются на одном уровне, расстояние между ними не больше 3 м. Монтаж блока ротации выполняется при отключенном электропитании. Датчик температуры устанавливается в точке, равноудаленной от кондиционеров. Контакты подключаются к соответствующим клеммам.
Ротационные системы, работающие через ИК канал, могут управлять 15 устройствами средней мощности.
Ротация с передачей данных по ИК и радиоканалу
 Система ротации и резервирования, использующая для передачи данных инфракрасный канал состоит из нескольких частей:
Система ротации и резервирования, использующая для передачи данных инфракрасный канал состоит из нескольких частей:
- управляющий блок ротации БУРР;
- исполнительный блок ротации БИС.
Инфракрасный канал для передачи данных не нуждается в проводном соединении. Команды от базового модуля по радиоканалу передаются исполнительным блокам, которые устанавливаются по одному на кондиционер. Комплекс может объединить до 15 сплит-систем, разделенных на 2 или 3 группы. Имеется возможность комбинировать различные варианты ротации. Настройка рабочей группы происходит через базовый модуль.
Отличительные характеристики ротации через ИК:
- Широкий выбор параметров охлаждения благодаря использованию 15 сплит-систем. В комплекс подключаются кондиционеры различных брендов и мощности. Не требуется оснащения техники функцией “Рестарт”.
- Беспроводное устройство позволяет сэкономить время и средство на прокладку коммуникаций.
- Высокая надежность системы, не имеющей в конструкции коммутирующих устройств. Исключается отгорание контактов.
- Простая настройка, возможность размещения базы в соседнем помещении.
Команды принимаются исполнительными блоками по радиоканалу на расстоянии до 50 м. Установки хранятся в энергонезависимой памяти. Систему ротации кондиционеров можно использовать в диапазоне температур от -20° до +70°C.
Технические характеристики модуля согласования для кондиционеров
 (СРК) является составной частью климатической системы. Он ориентирован на обеспечение совместной эксплуатации двух или трех устройств, кондиционирующих воздух. Функции модуля согласования:
(СРК) является составной частью климатической системы. Он ориентирован на обеспечение совместной эксплуатации двух или трех устройств, кондиционирующих воздух. Функции модуля согласования:
- контроль одинаковой выработки основного и резервного устройства;
- автоматический перезапуск сплит-систем после включения питания;
- измерение температуры в комнате;
- индикация состояния климатической техники;
- сообщение о внештатной ситуации;
- информация о системе и история основных событий записывается и хранится в энергонезависимом ОЗУ.
Согласователь для кондиционеров представляет собой устройство на базе микропроцессора, осуществляющее сбор и обработку данных, а также управляющее климатическими блоками. Технические параметры СРК:
- напряжение питания – 220 В ;
- ток потребления – 0,5 А;
- частота тока – 50 Гц;
- тип питания – переменный однофазный ток;
- класс защиты – IP40.
 Модуль комплектуется датчиком температуры воздуха, работающим в диапазоне от -50° до +125°C. Климатические системы подключаются к согласователю через адаптеры, установленные на внутреннем блоке. Режим переключения задается таймером. В зависимости от модели допускается установка периода от 1 часа до 10 дней. При тестовом подключении блока согласования кондиционеров запускаются обе климатические системы, подключенные к нему. Затем резервная установка отключается, а основная охлаждает серверное помещение.
Модуль комплектуется датчиком температуры воздуха, работающим в диапазоне от -50° до +125°C. Климатические системы подключаются к согласователю через адаптеры, установленные на внутреннем блоке. Режим переключения задается таймером. В зависимости от модели допускается установка периода от 1 часа до 10 дней. При тестовом подключении блока согласования кондиционеров запускаются обе климатические системы, подключенные к нему. Затем резервная установка отключается, а основная охлаждает серверное помещение.
Согласователи СРК-М совместимы с кондиционерами различных производителей. Различаются способы подключения: Daikin – через адаптеры, Mitsubishi Heavy – напрямую в разъему Cn-T или плате внутреннего модуля, Mitsubishi Electric – зависит от серии, может осуществляться через сухие контакты, адаптер или напрямую. Для кондиционеров других производителей может возникнуть необходимость купить силовые реле, которые устанавливаются в цепь питания внутреннего модуля.
В промышленных и полупромышленных климатических установках управление обычно выполняется через сухие контакты.
Установка блока ротации обеспечивает экономию средств на ремонт и замену климатической техники. Согласователь увеличивает время эксплуатации сплит-систем, служит гарантией надежной защиты серверов от перегрева и колебаний влажности.
Как работает блок ротации SB015

В данной статье подробно расскажем об особенностях работы блока ротации SB015. Данный блок можно использовать максимум с двумя кондиционерами.
УСТРОЙСТВО, НАЗНАЧЕНИЕ, ОСОБЕННОСТИ РАБОТЫ БЛОКА РОТАЦИИ
Для начала перечислим все возможные варианты, под которыми можно встретить устройство, управляющее двумя и более кондиционерами:
1) Блок ротации кондиционеров;
2) Согласователь работы кондиционеров;
3) Система ротации кондиционеров;
Первые три варианта используют проводное подключение кондиционеров и обязательное наличие функции “Рестарт” в подключаемых кондиционерах.
4) Контроллер для мониторинга работы кондиционеров в серверной.
Контроллер – это более сложное устройство, предоставляющее пользователю практически безграничные возможности в мониторинге за работой кондиционеров в серверных помещениях в любой точке нашей планеты, при наличии работающей сети интернет.
Во всех перечисленных случаях, речь идет о приборе, который включает и выключает кондиционеры через установленные интервалы времени, контролирует заданное значение температуры в помещении серверной, уведомляет обслуживающий персонал о любых изменениях температурного режима в серверной.
На примере блока ротации, модель SB015 , ниже будут раскрыты его алгоритмы работы в различных ситуациях и вариантах настройки.
В комплект входит:
Собственно сам блок ротации SB015;
Два датчика температуры для контроля работоспособности каждого подключенного кондиционера;
Комнатный датчик температуры, для постоянного мониторинга температуры в помещении
Далее детально рассмотрим, что есть на лицевой панели блока ротации

Для правильного подключения кондиционеров и датчиков температуры к блоку ротации SB015, предусмотрена подсказка. Она выполнена в виде наклейки и размещена сбоку на пластиковом корпусе согласователя кондиционеров.

После подключения кондиционеров и датчиков, блок ротации будет работать по одному из следующих сценариев:
Сценарий №1
Подключены все датчики температуры из комплекта поставки, в том числе подключен и комнатный датчик температуры. В данном случае блок ротации SB015 выполняет полный контроль за работой каждого из кондиционеров. Светодиодная индикация покажет красным цветом, если кондиционер перестал холодить (то есть нет перепада температур). Если светодиод моргает зеленым цветом, значит система кондиционирования серверной работает в штатном режиме.
Переключение кондиционеров произойдет через 8 часов непрерывной работы одного из них.
Также второй кондиционер включится в следующих ситуациях:
первый кондиционер перестал холодить;
температура в помещении превысила заданное значение;
Сценарий №2
Подключены только два датчика контроля работы кондиционеров, комнатный датчик не подключен. В данном случае, блок ротации SB015 будет осуществлять только переключение кондиционеров каждые 8 часов (другими словами работа по таймеру). Второй кондиционер не будет подключен в этом случае.
Сценарий №3
Подключен только комнатный датчик температуры, в таком случае алгоритм и логику работы блока ротации нагляднее будет рассмотреть на блок-схеме ниже.
Итак, мы разобрали по полочкам все возможные варианты работы блока ротации SB015.
Осталось разобраться со светодиодной индикацией, которая сопровождает работу нашего блока.
Светодиод “Статус” горит зеленым постоянно, блок ротации работает штатно;
Светодиод “Статус” горит красным постоянно, перегрев одного из датчиков температуры;
Светодиод “Т помещения” горит зеленным, температура в норме;
Светодиод “Т помещения” горит красным, температура в помещении выше установленного значения;
Светодиоды Кондиционер 1 и Кондиционер 2
При подключении всех датчиков температуры
– моргает зеленым цветом, кондиционер работает штатно;
– горит красным цветом, отсутствует минимальный перепад температуры на входе и выходе на внутреннем блоке теплобменника кондиционера. В данном случае нужно проверить кондиционер на работоспособность.
При подключении только комнатного датчика температуры к блоку ротации.
Светодиоды Кондиционер 1 и кондиционер 2 горят постоянно, в зависимости от работающего в данный момент, или горит два светодиода, если два кондиционера работают вместе.
Более подробная техническая информация и инструкция к блоку ротации находится здесь, в карточке товара.
В данной статье, мы разобрались что обычно имеют ввиду люди, употребляя термин блок ротации, какие они бывают.
Детально разобрали особенности модели SB015. Включение и алгоритмы работы, в зависимости от типа подключения.
Для чего используется блок ротации кондиционеров

На сегодняшний день трудно представить себе функционирование современного предприятия без компьютерной техники, с которой вся информация стекается в серверные. Серверные предназначены для хранения данных и управления всей электронной инфраструктурой, именно поэтому в них установлено дорогостоящее оборудование, которое, для нормального функционирования должно содержаться в строго определенном, влажностно-температурном режиме.
Учитывая важность такого оборудования, особые требования предъявляются к безотказной работе системы охлаждения в серверных, для обеспечения которой используется резервирование системы охлаждения. Одним из основных устройств, использующихся при резервировании, является блок ротации кондиционеров.
Назначение и функциональные особенности
Основной функцией модуля ротации является чередование работы кондиционеров в заданном интервале времени, путем регулирования подачи напряжения на все устройства охлаждения. Для этого, модуль чередования использует три температурных датчика, один из которых диагностирует температуру помещения, а остальные устанавливаются возле штатных датчиков внутренних блоков. Модуль ротации дает возможность:
- Попеременного переключения климатической техники, частота которой устанавливается пользователем.
- Переключение с неисправного кондиционера на резервный. При этом в локальную сеть оповещения предприятия передается код неисправности.
- Возможность контроля за температурой в серверной, за счет собственного датчика, а в случае ее повышения, подключение дополнительной климатической техники.
- Отключение всего охлаждающего оборудования в случае непредусмотренной или аварийной ситуации, с выдачей во внешнюю сеть сигнала «Авария».
 Следует учесть, что блоки ротации УРК-2 и УРК-2Т являются наиболее простыми устройствами чередования двух групп бытовой климатической техники, полупромышленных кондиционеров или испарительных блоков мультисистем. Использование таких модулей позволяет систему охлаждения интегрировать с охранной или пожарной сигнализацией, что дает возможность оперативно отреагировать на взлом и возгорание в помещении с дорогостоящим оборудованием.
Следует учесть, что блоки ротации УРК-2 и УРК-2Т являются наиболее простыми устройствами чередования двух групп бытовой климатической техники, полупромышленных кондиционеров или испарительных блоков мультисистем. Использование таких модулей позволяет систему охлаждения интегрировать с охранной или пожарной сигнализацией, что дает возможность оперативно отреагировать на взлом и возгорание в помещении с дорогостоящим оборудованием.
Особенности эксплуатации и подключения модуля ротации УРК-2
На этом приборе реализован вход для подключения дополнительного температурного датчика. При повышении температуры в помещении выше порога установленного для датчика, происходит кратковременный ввод в действие всех работающих устройств кондиционирования. Такое совместное охлаждение воздуха, в течение 5 минут способно понизить температуру в помещении. Если этого не происходит, то в локальную сеть оповещения предприятия посылается сигнал «Авария».
Важно!
Для использования модуля УРК-2, климатические устройства должны быть оснащены функцией автоматического рестарта.
Ротация, с передачей данных по ИК и радиоканалу
Многие руководители предприятий для поддержания необходимой температуры лабораторий и серверных применяют бытовые кондиционеры. Это связано с достаточно высокой стоимостью специализированной техники, предназначенной для охлаждения воздуха в таких помещениях. Для экономии электроэнергии, повышения отказоустойчивости бытовой климатической техники, а также для обеспечения бесперебойного функционирования охлаждения, очень часто применяется схемы резервирования и попеременного переключения кондиционеров, выполненные на основе модулей ротации БУРР и БИС.
База работает в комплекте с исполнительными модулями БИС, установленными по одному на каждое устройство, которых может быть 15. База БУРР оснащена собственным датчиком температуры, на основании данных которого и происходит диагностика работы климатической техники. Принцип его работы заключается в переключении подачи электропитания на определенную группу устройств охлаждения.
 Команды, разрешающие или запрещающие подачу электроэнергии, с базового модуля передаются на исполнительные, по радиоканалу. Дальность между исполнительными модулями может составлять 50 м, а они передают команды на кондиционер, посредством ИК канала. Программирование действий ИК излучателей, на включение или выключение определенных климатических приборов осуществляется на базовом модуле. Перед первым пуском «базы», при помощи панели ввода данных устанавливаются предельные величины температуры в помещении.
Команды, разрешающие или запрещающие подачу электроэнергии, с базового модуля передаются на исполнительные, по радиоканалу. Дальность между исполнительными модулями может составлять 50 м, а они передают команды на кондиционер, посредством ИК канала. Программирование действий ИК излучателей, на включение или выключение определенных климатических приборов осуществляется на базовом модуле. Перед первым пуском «базы», при помощи панели ввода данных устанавливаются предельные величины температуры в помещении.
Совет:
Следует понимать, что для эксплуатации систем ротации БУРР и БИС, все устройства для охлаждения воздуха, должны быть оборудованы ИК приемниками.
Такая система дает возможность реализации различных вариантов попеременного использования климатической техники, которая может состоять как из двух, так и из трех групп. Устройство ротации кондиционеров, выполненное на основе модулей БУРР и БИС, дает возможность:
- Мгновенного ввода в эксплуатацию резервной климатической техники. В случае отказа основной группы или нарушение ее нормальной работы происходит резкое повышение температуры в помещении. Именно на это и реагирует базовый модуль, давая команду подключения резерва.
- Подключение дополнительной группы климатической техники, при недостатке производительности основной.
- Эффективного переключения нескольких групп кондиционеров, для выработки ими одинакового ресурса. Частота переключений между группами определяется пользователем.
 Применение приборов БУРР и БИС позволяет автоматически прекращать подачу напряжения на кондиционеры, и передавать в общую сеть команды «Авария» или «Пожар». Основным достоинством использования БУРР и БИС является:
Применение приборов БУРР и БИС позволяет автоматически прекращать подачу напряжения на кондиционеры, и передавать в общую сеть команды «Авария» или «Пожар». Основным достоинством использования БУРР и БИС является:
- Простота установки, настройки, которая функционирует без прокладки коммуникационных линий к каждому прибору.
- Возможность использования для охлаждения климатическую технику, различной мощности, производительности и торговой марки.
- Возможность монтажа базового модуля БУРР в смежном помещении.
Применение блоков ротации для переключения функционирующих устройств охлаждения воздуха с резервной климатической техникой, дает возможность существенно продлить их ресурс благодаря равномерному вводу в эксплуатацию и контролю над температурными показателями.
Особенности работы блока ротации кондиционеров
В современном мире офисные здания оснащаются так, чтобы работникам было не только удобно, но и легко работать. Многочисленная информация, доступная круглые сутки для ведения быстрых дел, хранится на «серверах» (для подобной габаритной техники нужны специальные помещения). Дорогостоящая техника не только прихотлива, она требует особого ухода. Температура, влажность, стабильные показатели вне зависимости от погоды за окном и времени года. Охлаждением серверов занимаются мощные кондиционеры, сконструированы под определенные характеристики. Во избежание нежелательных проблем, техника, установленная в специальном помещении, тестируется каждых полгода (разборка, чистка, сбор). Что делать, если возможностей для установки специализированного кондиционера нет? Блок ротации кондиционеров – это универсальное устройство, позволяющее вести дистанционное управление охладителями в серверном помещении.

Блок ротации требует периодической чистки
Предназначение блока ротации кондиционера любой мощности
Поддержка температурного режима в помещении с одним и больше серверами, является первоначальной задачей. Беспрерывная работа техники обеспечивается кондиционерами с системой резервирования, роль которой выполняет блок ротации. Принцип роботы несложного дополнительного устройства довольно простой. Модуль задает интервалы времени, когда кондиционер должен охлаждать все помещение. Встроенные датчики, фиксируют минимальные изменения, и при необходимости – корректируют температурный режим. Применение блока ротации исключает вмешательство человека. Система работает на автономном режиме, и лишь проверки (диагностика) модуля производится при помощи мастера.
В остальных случаях, необходимость наблюдения живым человеком отпадает полностью. Техническиоснащенное помещение оборудуется только под технику.
Система ротации кондиционеров регулирует уровень напряжения, поступающий в охладитель. Датчики, принимающие непосредственное участие в работе охлаждающей (специальное помещение) техники, расположены по стратегическому принципу. Одна чувствительная к переменам температуры деталь устанавливается непосредственно в комнате, остальные два датчика монтируются внутрь модуля.
Преимущества блока ротации кондиционера:
- пользователь вправе менять температурные режимы и устанавливать их частоту;
- при поломке основного кондиционера, система автоматически переключается на резервное устройство;
- установка дополнительных датчиков (досконально регулируют температуру, подстраиваются под смену факторов внешней среды);
- аварийное отключение оборудования в экстренных ситуациях.
Для синхронной работы нескольких климатических устройств, использовать модули ротации не обязательно, но простые приборы упрощают уход за вспомогательной техникой и позволяют продлить срок ее службы. Связь всей установки с охранным пунктом или аварийными службами, обеспечивает безопасность не только людям, работающим вблизи серверной, но и дорогостоящей техники.

При поломке основного кондиционера блок переключит систему на резервный
Подключение модуля ротации для промышленных кондиционеров
Устройство ротации кондиционеров заблаговременно оснащается блоками для датчиков. Небольшие по размеру детали, фиксируют температуру в помещении (в разных точках серверной). При повышении заданных показателей (влажности, температуры) все кондиционеры включаются и прекращают работу только после того, как климат в помещении придет в указанную норму. В привычных условиях, для охлаждения небольшой комнаты необходим единый, но мощный кондиционер, а совместная работа основных и резервных устройств снижает температуру в серверной комнате за считанные минуты. Подобные меры носят спонтанный характер, ведь постоянная работа сразу двух кондиционеров пусть и эффективна, но затратная по количеству потребляемой электроэнергии.
Довольно часто владельцы офисов или промышленных помещений экономят на дорогостоящей технике и вместо специальных охладителей, кондиционирование воздуха всецело ложится на простое домашнее устройство. Бытовые агрегаты с трудом справляются с чрезмерной нагрузкой, поэтому опасный нагрев внешнего и внутреннего блока неминуем. Оттянуть неизбежную поломку можно, если владелец помещения будет использовать модули ротации, настроенные на частые включения кондиционеров.
Стандартный заводский модуль ротации способен управлять сразу пятнадцатью устройствами средней мощности. Внутри блока в обязательном порядке устанавливается один датчик смены внешней температуры. Крошечный элемент отвечает за переключение нагрузки на подходящий кондиционер, вне зависимости от установок владельца помещения.

Стандартный модуль управляет 15 устройствами
Технические характеристики модуля ротации для кондиционера
При помощи радиосигнала из базового модуля на устройство (блок ротации) подается сигнал о прекращении работы. Подобные команды действуют вопреки первоначальным настройкам всей системы. Радиус действия сигнала достигает пятидесяти метров, что удобно для дистанционного управления охладительной системой серверной. Основным преимуществом модуля ротации является его многозадачность, ведь к одному простому блоку подключается сразу несколько габаритных, сложных в эксплуатации кондиционеров. Запуск резервных устройств, сели возникла подобная необходимость, происходит мгновенно, без заминок и промедлений (они могут стоять владельцу помещения драгоценного оборудования).
Модуль ротации – универсальное устройство, способное скрыть недостатки климатической техники. В условиях неправильной работы кондиционера, при помощи блока, регулируется переключение режимов.
Настройка модуля производится мастером или, при возможности и наличии достаточных знаний, владельцем помещения (к новому устройству прилагается детальная инструкция по эксплуатации).
Для кондиционеров, установленных в помещениях, где поток поступающих данных нуждается в создании отдельной серверной комнаты, распределение нагрузки является первоначальной задачей. Для чего нужен модуль ротации? Устройство с простыми настройками и определенным принципом работы, гарантирует корректную работу охладителей при любых сменах температуры. В жаркую или холодную пору года модули сбалансируют климат внутри технического помещения – серверной комнаты.
Блок ротации кондиционеров. Согласователь работы кондиционеров
Устройство ротации кондиционеров. Блок согласования кондиционеров
Блок ротации кондиционеров, или как его еще называют – устройство ротации кондиционеров, предназначен для обеспечения режима чередования работы двух кондиционеров с заданным периодом времени и обеспечения нормального температурного режима помещения в различных климатических условиях. Блок управления ротацией и резервированием – незаменимый компонент в кондиционирование серверной. Цена на блок ротации кондиционеров различна в зависимости от производителя.
Обычно в системах с резервированием, не имеющих устройства согласования (блока ротации), основные кондиционеры вырабатывают свой ресурс полностью, а резервный кондиционер, практически постоянно простаивая, свой ресурс не вырабатывает. Ресурс наработки подобной системы равен ресурсу наработки основного кондиционера.

СРК М. Согласователь работы кондиционеров
СРК М – Согласователь Работы Кондиционеров Микропроцессорный. СРК-М предназначен для управления системами кондиционирования, имеющими в своем составе 2 или 3 кондиционера. Обеспечивает одинаковую наработку всех кондиционеров в системе с резервированием и позволяет включать резервный кондиционер при отказе одного из основных кондиционеров или повышенной тепловой нагрузке. Согласователь СРК-М делает резервным по очереди каждый кондиционер системы. В результате общий ресурс наработки всей системы возрастает для систем 1+1 (2 кондиционера в системе-основной и резервный) в 2 раза (на 100%), а для систем 2+1 в 1.5 раза (на 50%) !
Повышение ресурса наработки системы кондиционирования приводит к повышению надёжности всей системы кондиционирования.

- СРК-М осуществляет попеременное включение двух из трех (одного из двух) кондиционеров с целью обеспечить равномерную выработку их ресурса и максимальную надежность системы, а также поддерживает температуру воздуха в заданных пределах;
- Подсчитывает суммарное время работы каждого кондиционера;
- Производит автоматический перезапуск кондиционеров при пропадании и восстановлении электропитания;
- В зависимости от превышения установленных порогов температуры воздуха в помещении включает или выключает все кондиционеры системы;
- При отказе одного из кондиционеров, включает остальные в работу системы постоянно;
- Выдает сообщения при нештатной ситуации (аварии, пожаре, пропадании, появлении напряжения питания, изменении настроек и параметров системы с клавиатуры и т.п.) на удаленный терминал системы мониторинга (только версия СРК-М) и внешний модуль индикации;
- Собирает, сохраняет и анализирует данные о состоянии кондиционеров системы, температуры в помещении, напряжение питания, регистрирует аварийные ситуации и обеспечивает светодиодную и символьную индикацию состояния кондиционеров;
- Осуществляет запись и хранение (не менее 1 года) в энергонезависимом ОЗУ всех установленных параметров системы и истории основных событий с указанием даты и времени;
- Предоставляет возможность считывания «журнала событий» с помощью собственного ЖК дисплея или компьютера;
- Позволяет проводить удаленный мониторинг технологической системы кондиционирования средствами специального программного обеспечения по сети RS-232 или ETHERNET или используя промышленный протокол MODBUS;
- Обеспечивает возможность ввода с клавиатуры и контроля на ЖК дисплее настроек и параметров системы;
- Защищает систему с помощью пароля от несанкционированного доступа с клавиатуры или компьютера;
- Исключает несанкционированные действия по управлению кондиционерами с дистанционного ИК пульта.
Для каких кондиционеров подходит согласователь работы кондиционеров СРК-М и СРК-М-01 ?
Согласователи СРК-М и СРК-М-01 могут работать с кондиционерами любых производителей. Различие только в способе подключения.
1. Daikin – подключение СРК-М ко всем кондиционерам Daikin осуществляется через адаптеры серии KRP. Адаптеры приобретаются отдельно у нас или любого дилера Daikin.
2. Mitsubishi Heavy Industries – подключение СРК-М к кондиционерам Mitsubishi Heavy Industries осуществляется напрямую без адаптеров к разъему Cn-T (или CnT-BL) на плате внутреннего блока. Но, так как, наличие этого разъема в последнее время стало необязательной опцией, настоятельно рекомендуется перед покупкой уточнить его наличие на плате.
3. Mitsubishi Electric – способ подключения СРК-М к кондиционерам Mitsubishi Electric, в зависимости от серии может различаться. Подключение может осуществляться либо напрямую, без адаптеров, через сухие контакты CN32 и CN51, либо через адаптер MAC-397IF, либо, к самым простым моделям, только через реле в цепи питания внутренней платы кондиционера. Реле приобретаются отдельно. Наличие сухих контактов CN32 и CN51 на плате внутреннего блока, а также возможность подключения адаптера MAC-397IF к плате внутреннего блока настоятельно рекомендуется уточнять у Вашего дилера Mitsubishi перед покупкой (закладкой в проект) кондиционеров. Парт-номера ответных колодок для разъемов CN32 и CN51, соответственно, PAC-SE55RA-E и PAC-SA88HA-E.
4. Подключение кондиционеров других фирм производителей . Лучше всего перед покупкой кондиционеров уточните у Вашего поставщика, имеется ли у кондиционеров возможность управления через сухие контакты. Как правило, в дешевых бытовых сериях кондиционеров таких контактов нет, но в полупромышленных и промышленных сериях, а так же в канальных сплит системах, fancoil системах и т.д., эти контакты могут присутствовать, либо есть возможность подключения внешнего адаптера, на котором также есть сухие контакты для управления. При невозможности логического управления кондиционерами, подключение СРК-М к кондиционерам других фирм производителей осуществляется через реле в цепи питания платы внутреннего блока кондиционера. В этом случае необходимо дополнительно приобрести силовые реле на каждый управляемый кондиционер. Для нормального функционирования, при таком подключении, кондиционер должен иметь функцию АВТОРЕСТАРТ.
Управляющий блок ротации БУРР-1. Исполнительный блок ротации БИС-1
Система предназначена для обеспечения ротации и резервирования в комплексе из нескольких кондиционеров (сплит-систем), использующих инфракрасные пульты. Система состоит из управляющего блока ротации БУРР-1 и исполнительных блоков БИС-1 (по одному на каждый кондиционер). Комплекс может включать до 15 кондиционеров, объединенных в 2 или 3 группы.

Исполнительные устройства посредством ИК-излучателей осуществляют включение и выключение кондиционеров по команде базового блока. Команды передаются на расстояние до 50м. Могут быть реализованы различные варианты ротации и резервирования групп кондиционеров. Все настройки выполняются с помощью интерактивного меню управляющего блока БУРР-1.

- Не требуется прокладка сигнальных линий
- Гибкий выбор холодопроизводительности системы за счет использования до 15 кондиционеров без ограничения их мощности
- Возможна реализация различных схем ротации и резервирования
- Высокая надежность, обусловленная отсутствием силовых коммутирующих устройств и необходимости использования функции “рестарт” кондиционеров
- Простая настройка системы и наглядная информация о ее работе
- Возможно масштабирование системы с минимальными затратами
- Возможно вынесение управляющего блока в смежное помещение
Характеристики БУРР-1 и БИС-1
| Параметры | БУРР-1 | БИС-1 |
| Напряжение питания, В | 220 | 220 |
| Максимальная потребляемая мощность, Вт | 1.5 | 0.6 |
| Диапазон рабочих температур, °С | -20. +70 | -20. +70 |
| Диапазон измеряемых температур, °С | -55. +125 | -55. +125 |
| Габаритные размеры, мм | 140х88х62 | 105х65х30 |
| Масса, г | 320 | 170 |
| Режим работы | непрерывный | непрерывный |
Блок ротации кондиционеров УРК 2Т
Устройство ротации кондиционеров УРК 2Т обеспечивает чередование работы двух кондиционеров с заданным периодом времени и обеспечение нормального температурного режима помещения. При использовании устройства ротации УРК-2 производится интеграция системы кондиционирования помещения, включающей в себя два кондиционера, с системой охранной или пожарной сигнализации, а также с системой электропитания.

Блок ротации УРК-2Т – универсальный вариант для работы с любыми типами кондиционеров. Для диагностики работы кондиционеров используются три датчика температуры. УРК-2Т имеет три входа для подключения датчиков температуры. Датчик температуры № 3 устанавливается в помещении на равном удалении от кондиционеров и контролирует температуру в помещении. Два других датчика температуры устанавливаются на испарители внутренних блоков кондиционеров, рядом со штатными датчиками, и контролируют работу кондиционеров. УРК-2Т обеспечивает подачу сигнала “Авария” от каждого кондиционера (по одной сигнальной линии на кондиционер) с сухих нормально разомкнутых контактов реле в следующих случаях:
- При возникновении аварии кондиционера
- При отключении автоматов защиты кондиционеров или пропадании фазы 220 В, от которой запитывается УРК-2Т
УРК-2Т имеет вход «Термостат» для подключения дополнительного датчика температуры. При размыкании контактов «Термостат», что соответствует превышению температуры в помещении над порогом термостата, включаются все работоспособные кондиционеры. Совместная работа всех кондиционеров продолжается в течение 5 минут после возврата контактов «Термостат» в исходное состояние (замкнуты). Если в течении 10 минут совместной работы кондиционеров контакты не восстановятся – выдается сигнал “Авария” по каналам всех работающих кондиционеров. Датчик температуры помещения № 3 и вход «Термостат» имеют равный приоритет. Согласователь работы кондиционеров УРК-2Т может работать в двух режимах – Рабочем и Сервисном.
Согласование работы кондиционеров, резервирование и ротация
При установке кондиционера в небольшую серверную комнату часто в целях экономии финансов и места используют не специально разработанное для этого дорогостоящее прецизионное оборудование, а обычные бытовые сплит-системы. Но и в таких серверных к оборудованию предъявляются довольно жeсткие требования: гарантированное поддержание требуемой температуры, круглогодичный бесперебойный режим работы, высокая степень надёжности.
Обычные кондиционеры не могут работать при отрицательной температуре воздуха на улице. В таких условиях резко падает давление конденсации, в результате жидкий хладагент может попадать в картер компрессора. Кроме того, из картера в систему может выбрасываться масло. Все это ведет к обмерзанию внутреннего блока кондиционера, снижению его производительности и быстрому выходу компрессора из строя. Если дренажная система выходит на улицу, то в сильные морозы возникают проблемы и с отводом влаги из системы кондиционирования.
Для устранения этих недостатков и обеспечения круглогодичного использования оборудование дорабатывается зимним комплектом.
Устанавливая только один кондиционер, ответственный за серверную комнату принимает на себя очень большие риски, т.к. любое оборудование может выйти из строя. Кроме того, оборудование требует периодического сервисного обслуживания, в то время как серверная продолжает работать, выделяя тепло. Для повышения уровня надежности в серверную ставится два и более кондиционера, которые работают по очереди, обеспечивая тем самым резервирование.
Существует два способа резервирования мощности. При 100%-ом резервировании устанавливается два одинаковых кондиционера необходимой холодопроизводительности и через определённый промежуток времени (как правило, посуточно) эти кондиционеры будут меняться ролями. Другой вариант резервирования – 50%-ое резервирование мощности: когда в серверную комнату ставятся три аппарата, каждый мощностью в половину от необходимой холодопроизводительности. Одновременно работают два аппарата, а третий простаивает. Ротация кондиционеров осуществляется последовательно, то есть в долгосрочном периоде все кондиционеры проработают примерно одинаковое количество часов.
И в том, и в другом случае обеспечивается равномерный износ оборудования, аварийное включение при неисправности одного из кондиционеров или одновременное включение всех при повышении температуры выше заданной, а также возможность проведения планового технического обслуживания.
Для этого применяют специальные устройства, так называемые согласователи работы кондиционера, устройства резервирования и ротации кондиционеров.
 Согласователь работы кондиционеров СРК
Согласователь работы кондиционеров СРК
предназначен для управления технологических систем охлаждения, состоящей из двух блоков кондиционеров. Для повышения надежности системы технологического кондиционирования в помещении устанавливаются два кондиционера которые работают поочерёдно с заданным интервалом, каждый кондиционер способен отводить 100% тепловой нагрузки. В произвольный момент времени один кондиционер работает, один является резервным.
СРК предназначен для совместной работы с блоками кондиционеров:
Согласователь работы кондиционеров фирмы Daikin (далее изделие или СРК-2.1, СРК-D/DM) предназначен для управления совместной работой двух кондиционеров фирмы Daikin серии Split, использующие адаптеры KRP413A1S. Функции СРК:
– Выполняет автоматическое управление технологической системой кондиционирования, включающей 2 кондиционера.
– Обеспечивает равномерную выработку ресурса рабочего и резервного кондиционеров.
– Включает в работу резервный кондиционер, если происходит аварийная остановка работающего кондиционера.
– Обеспечивает функцию автоматического перезапуска кондиционеров при случайном пропадании и восстановлении электропитания.
– Включает в работу все кондиционеры, если температура в помещении превышает заданную.
– Исключает несанкционированное (случайное) отключение кондиционеров с индивидуального пульта управления и изменение автоматически поддерживаемой температуры.
– Обеспечивает индикацию нормальной работы кондиционеров.
– Осуществляет индикацию аварийной ситуации.
– Имеет выход для удалённого контроля аварийной ситуации (нормально разомкнутый контакт без потенциала (IH=0.5 A. DC=24 В)).
СРК представляет собой блок, показанный на рисунке.
Основными компонентами СРК являются:
– защитный пластмассовый корпус (1):
– реле управления сигналом «авария»(2):
– переключатель управления (3):
– таймер (4):
– индикатор аварии (5):
– индикатор нормальной работы 1-го кондиционера (6):
– индикатор нормальной работы 2-го кондиционера (7);
– блок питания 12 В (8).
Принцип работы
Для повышения надёжности системы технологического кондиционирования в кондиционируемом помещении устанавливают два кондиционера, каждый из которых способен отводить 100% тепловой нагрузки. В этом случае в произвольный момент времени один кондиционер работает, а другой является резервным.
СРК осуществляет попеременное включение одного из двух кондиционеров через равные промежутки времени с целью равномерной выработки ресурса кондиционеров. Время переключения задается таймером (4). На таймере можно установить время переключения в пределах от 1 часа до 10 дней. При поставке таймер установлен на переключение кондиционеров через 24 часа.
При переключении таймера через контакты 3. 4 (рисунок 2) замыкается цепь 1-го адаптера и включается 1-ый кондиционер, следующее переключение таймера размыкает контакты 3. 4 цепи 1-го адаптера и выключается 1-ый кондиционер, в то же время, через контакты 6. 7 замыкается цепь 2-го адаптера и включается 2-ой кондиционер. Далее циклы переключений повторяются бесконечно, до тех пор. пока есть напряжение питания модуля.
Адаптеры KRP413A1S позволяют включать и отключать кондиционеры через штатные цепи управления кондиционеров без нарушений режима работы. Адаптеры устанавливаются отдельно от каждого внутреннего блока кондиционера.
Индикатор (6) (рис.1) показывает включение 1-го кондиционера, индикатор (7) показывает включение 2-го кондиционера. Сигналы о работе кондиционеров снимаются с адаптеров.
Если на работающем кондиционере возникает аварийная ситуация, то автоматически в работу включается второй кондиционер. Сигнал аварии возникает на контактах 1. 3 разъема S5 адаптеров и управляет каждым кондиционером через СРК при этом включается индикатор аварии и выдается сигнал аварии (клеммы 17-18. замкнутое состояние при возникновении сигнала неисправности работающего кондиционера).
Если температура в помещении повышается и превышает заданное значение на термостате, например. +26 °С, СРК также включает в работу оба кондиционера, при этом включается индикатор аварии и выдается сигнал аварии.
Повышение температуры может быть связано либо с нарушением нормальной работы кондиционера, либо с нерасчётным увеличением тепловой нагрузки в помещении. При понижении температуры восстанавливается нормальный режим работы с одним кондиционером. Термостат (3) (рисунок 2) должен быть установлен в месте, где температура воздуха соответствует средней температуре воздуха в рабочей зоне помещения.
При работе кондиционеров с СРК все режимные параметры работы кондиционеров поддерживаются автоматически и не могут быть изменены с индивидуального пульта управления. Для изменения параметров с помощью индивидуального пульта управления на СРК имеется специальный переключатель управления.

Инструкция по использованию согласователя работы кондиционеров СРК-D/DM
Блок управления резервирования и ротации БУРР-1 
Система предназначена для обеспечения ротации и резервирования в комплексе из нескольких кондиционеров (сплит-систем), использующих ИК пульты управления.
Система состоит из одного базового блока (БУРР-1) и нескольких исполнительных блоков (БИС-1), по одному на каждый кондиционер. Комплекс может включать до 15 кондиционеров разных моделей и разных производителей, объединенных в две или три группы произвольного состава. Исполнительные устройства посредством своих ИК-излучателей осуществляют включение и выключение кондиционеров, на которых они установлены. Операция выполняется по команде базового блока. Команды от базового блока на исполнительные передаются по радиоканалу на расстояние до 50 м.
Настройка ИК-излучателей БИС-1 сигналам включения/выключения конкретных кондиционеров производится на базовом блоке, который оснащен специальным ИК-приемником. Перед пуском системы на кондиционерах и базовом блоке устанавливается заданная температура в помещении. Система позволяет реализовать различные варианты ротации и резервирования из 2-х или 3-х групп кондиционеров. Все настройки выполняются с помощью интерактивного меню базового блока.
Устройство обеспечивает:
Особенностями системы являются:
Контроллер для серверных помещений SBR01
Назначение системы
Система автоматического управления кондиционерами SBR01 выполняет следующие функции:
• поддержание заданного уровня температуры в требуемом помещении путем беспроводного автоматического управления от 1 до 8 кондиционерами;
• обеспечение равномерного использования кондиционеров путем их ротации через заданный пользователем промежуток времени (от 4 до 24 часов);
• сигнализацию о неисправностях (передача информации на звуковой и релейный выход, ЖК дисплей, веб-сервер);
• удаленное наблюдение за состоянием и управление системой через веб-сервер.
Технические характеристики
Система автоматического управления кондиционерами состоит из одного центрального контроллера SBR01 и от 1 до 8
подчиненных беспроводных RF модулей. Каждый из RF модулей осуществляет управление одним кондиционером. Связь между контроллером SBR01 и RF модулями осуществляется в нелицензируемом радио-диапазоне 2400Мгц.
Дальность устойчивой связи между RF модулями и контроллером напрямую зависит от помещения эксплуатации.
Дальность устойчивой связи на открытой местности составляет 100 метров.
Источник






