Описание препарата Таксол® (концентрат для приготовления раствора для инфузий, 6 мг/мл) основано на официальной инструкции, утверждено компанией-производителем в 2012 году
Дата согласования: 17.10.2012
Особые отметки:
Содержание
- Действующее вещество
- ATX
- Фармакологическая группа
- Нозологическая классификация (МКБ-10)
- Состав
- Описание лекарственной формы
- Фармакологическое действие
- Фармакодинамика
- Фармакокинетика
- Показания
- Противопоказания
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Передозировка
- Меры предосторожности
- Особые указания
- Форма выпуска
- Производитель
- Комментарий
- Условия отпуска из аптек
- Условия хранения
- Срок годности
Действующее вещество
ATX
Фармакологическая группа
Состав
| Концентрат для приготовления раствора для инфузий | 1 мл |
| активное вещество: | |
| паклитаксел | 6 мг |
| макрогола глицерилрицинолеат (Кремофор® EL) — 527 мг; этанол — 396 мг; азот |
Описание лекарственной формы
Прозрачный бесцветный или слегка желтоватый неводный вязкий раствор. Перед в/в введением препарат разбавляется соответствующим раствором для парентерального применения.
Фармакологическое действие
Фармакологическое действие
—
противоопухолевое.
Фармакодинамика
Стимулирует сборку микротрубочек из димеров тубулина и стабилизирует микротрубочки за счет подавления деполимеризации, что нарушает нормальный процесс динамической реорганизации сети микротрубочек, который важен для клеточных функций на этапе митоза и интерфазы клеточного цикла. Индуцирует образование аномальных скоплений или «связок» микротрубочек на протяжении клеточного цикла и вызывает образование множественных «звезд» микротрубочек во время митоза.
Фармакокинетика
Концентрация паклитаксела в плазме крови после в/в введения уменьшается в соответствии с двухфазной кинетикой.
Фармакокинетика паклитаксела определялась после инфузии препарата в дозах 135 и 175 мг/м2 на протяжении 3 и 24 ч. При инфузии в течение 3 ч фармакокинетика с повышением дозы приобретала нелинейный характер. При увеличении дозы на 30% (от 135 до 175 мг/м2 ) Сmax и AUC0-∞ повышались на 75 и 81% соответственно.
При множественных курсах лечения не было получено указаний на кумуляцию паклитаксела.
Исследования in vitro показывают, что 89–98% препарата находится в связанном состоянии. Циметидин, ранитидин, дексаметазон или дифенгидрамин не влияют на связывание паклитаксела с белками.
Метаболизм у человека не исследован до конца. От 1,3 до 12,6% введенной дозы препарата выделяется с мочой в неизмененном виде. T1/2 составляет 3–52,7 ч. Основными продуктами метаболизма являются гидроксилированные метаболиты. Возможно, основным механизмом метаболизма является биотрансформация в печени и выделение с желчью. Влияние нарушения функции почек или печени на метаболизм паклитаксела в организме после трехчасовой инфузии формально не исследовалось. Фармакокинетические параметры, полученные у одного больного, свидетельствуют о том, что диализ не оказывает влияния на скорость выведения препарата из организма.
Показания
Рак яичников: терапия 1-й линии (в комбинации с цисплатином) у больных с распространенным метастатическим процессом или остаточной опухолью (более 1 см) после лапаротомии и терапия 2-й линии у больных с распространенным метастатическим раком яичников после стандартной терапии, не давшей положительного результата.
Рак молочной железы: адъювантная терапия у больных с наличием метастазов в лимфатических узлах после проведения стандартного комбинированного лечения;
терапия 1-й линии метастатического рака и при прогрессировании заболевания после адъювантной терапии с применением препаратов антрациклинового ряда; терапия 2-й линии при прогрессировании заболевания после комбинированной химиотерапии с применением противоопухолевых антибиотиков антрациклинового ряда.
Немелкоклеточный рак легкого: терапия 1-й линии в комбинации с цисплатином или в монотерапии для лечения больных, которым не планируется проведение хирургического лечения и/или лучевой терапии с возможностью излечения.
Саркома Капоши у больных СПИДом: терапия 2-й линии.
Противопоказания
Тяжелые реакции гиперчувствительности на паклитаксел или любой другой компонент, входящий в состав препарата, особенно полиоксиэтилированное касторовое масло; при беременности и в период кормления грудью, у больных с солидными опухолями при исходном содержании нейтрофилов менее 1500/мм3, а также у больных саркомой Капоши, развившейся на фоне СПИДа, при исходном (или зарегистрированном в процессе лечения) содержании нейтрофилов менее 1000/мм3.
Способ применения и дозы
Реклама: ООО «РЛС-Патент», ИНН 5044031277, erid=4CQwVszH9pUkpHxmQQo
Реклама: ООО «РЛС-Патент», ИНН 5044031277, erid=4CQwVszH9pUkpHxmQQo
В/в, капельно.
Для предупреждения тяжелых реакций гиперчувствительности всем больным должна проводиться премедикация с использованием ГКС, блокаторов H1— и Н2-гистаминовых рецепторов. Например 20 мг дексаметазона (или его эквивалент) внутрь приблизительно за 12 и 6 ч до введения препарата Таксол® или 20 мг дексаметазона в/в примерно за 30–60 мин до введения препарата Таксол®, 50 мг дифенгидрамина (или его эквивалент) в/в и 300 мг циметидина или 50 мг ранитидина в/в за 30–60 мин до введения препарата Таксол®.
Пациентам с сoлидными опухолями повторные курсы лечения препаратом Таксол® назначаются только после достижения содержания нейтрофилов 1500/мкл (1000/мкл у пациентов с саркомой Капоши, обусловленной СПИДом), а содержание тромбоцитов — 100 000/мкл. Для пациентов, у которых развилась тяжелая нейтропения (количество нейтрофилов составляло менее 500/мкл в течение более чем одной недели) или с тяжелой перифирической нейропатией при последующих курсах лечения препаратом Таксол® следует снизить дозу на 20%. Нейротоксичность и нейтропения являются дозозависимыми.
При выборе режима и доз в каждом индивидуальном случае следует руководствоваться данными специальной литературы.
Рак яичников:
Терапия первой линии: рекомендованная доза Таксола® составляет 175 мг/м2 путем 3-часовой в/в инфузии или 135 мг/м2 путем 24-часовой инфузии с последующим введением препарата платины, интервал между курсами лечения должен составлять 3 нед.
Терапия второй линии: в режиме монотерапии в дозе 175 мг/м2 в виде 3-часовой в/в инфузии каждые 3 нед.
Рак молочной железы:
Адъювантная терапия проводится после стандартного комбинированного лечения. Таксол® вводится в дозе 175 мг/м2 в виде 3-часовой в/в инфузии. Всего рекомендуется проведение 4 курсов терапии с интервалом 3 нед.
Терапия первой линии:
— монотерапия: 175 мг/м2 в виде 3-часовой в/в инфузии каждые 3 нед;
— комбинированная терапия: при использовании препарата в комбинации с трастузумабом, рекомендованная доза Таксола® составляет 175 мг/м2 в виде 3-часовой в/в инфузии каждые 3 нед. Начинать применение Таксола® можно на следующий день, после введения больному первой дозы трастузумаба или, при хорошей переносимости, в день применения трастузумаба; при использовании препарата в комбинации с доксорубицином (50 мг/м2) Таксол® применяют в дозе 220 мг/м2 в виде 3-часовой в/в инфузии каждые 3 нед. Начинать применение Таксола® следует через 24 ч после применения доксорубицина.
Терапия второй линии 175 мг/м2 в виде 3-часовой в/в инфузии каждые 3 нед.
Немелкоклеточный рак легких:
В режиме комбинированной терапии рекомендованная доза препарата составляет 175 мг/м2 путем 3-часовой в/в инфузии или 135 мг/м2 путем 24-часовой инфузии с последующим введением препарата платины, интервал между курсами лечения должен составлять 3 нед.
В режиме монотерапии рекомендованная доза препарата составляет от 175 мг/м2 до 225 мг/м2 в виде 3-часовой в/в инфузии каждые 3 нед.
Саркома Капоши у больных СПИДом:
Терапия второй линии — рекомендованная доза Таксола® составляет 135 мг/м2 в виде 3-часовой в/в инфузии каждые 3 нед или 100 мг/м2 в/в капельно в течение 3 ч каждые 2 нед.
В зависимости от уровня иммуносупрессии, наблюдаемой у больных с далеко зашедшей формой СПИДа, рекомендуется:
1) уменьшить пероральную дозу дексаметазона (одного из трех компонентов премедикации) до 10 мг;
2) вводить Таксол® только при содержании нейтрофилов не менее 1000 клеток/мкл крови;
3) больным с тяжелой нейтропенией (менее 500 клеток/мкл крови в течение недели и более) при последующих курсах уменьшить дозу Таксола® на 20%;
4) по клиническим показаниям одновременно применять гемопоэтический фактор роста (Г-КСФ).
Применение при нарушении функции печени
Пациентам с печеночной недостаточностью и связанным с нею повышенным риском токсичности (в частности, миелосупрессии III–IV) рекомендуется коррекция дозы препарата Таксол®.
Необходимо установить тщательный контроль за состоянием пациентов.
Таблица 1
Рекомендуемые дозы для пациентов с нарушениями функции печени
|
Степень печеночной недостаточности |
||
|
Активность печеночных трансаминаз |
Концентрация билирубина в сыворотке крови, мкмоль/л |
Доза* препарата Таксол, мг/м2 |
|
24-часовая инфузия |
||
| <2 ? ВГН и | ?26 | 135 |
| 2?<10 ? ВГН и | ?26 | 100 |
| <10 ? ВГН и | 28–129 | 50 |
| ?10 ? ВГН или | >129 | не рекомендуется |
| 3-часовая инфузия | ||
| <10 ? ВГН и | ?22 ? ВГН | 175 |
| <10 ? ВГН и | 22–25 ? ВГН | 135 |
| <10 ? ВГН и | 35–86 ? ВГН | 90 |
| ?10 ? ВГН или | >86 ? ВГН | не рекомендуется |
*Рекомендуемые дозы для первого курса терапии; корректировка дозы при последующих курсах должна основываться на индивидуальной переносимости препарата.
Правила приготовления раствора для инфузий
Раствор препарата готовят разведением концентрата до конечной концентрации паклитаксела от 0,3 до 1,2 мг/мл. В качестве разбавляющего раствора могут быть использованы: 0,9% раствор натрия хлорида, 5% раствор декстрозы, 5% раствор декстрозы в 0,9% растворе натрия хлорида, 5% раствор декстрозы в растворе Рингера. Приготовленные растворы могут опалесцировать из-за присутствующей в составе лекарственной формы основы-носителя, причем после фильтрования опалесценция раствора сохраняется.
При приготовлении, хранении и введении препарата Таксол® следует пользоваться оборудованием, которое не содержит деталей из ПВХ.
Таксол® следует вводить через систему со встроенным мембранным фильтром (размер пор — не более 0,22 мк).
Побочные действия
При использовании комбинации Таксола с препаратами платины не было отмечено каких-либо существенных в клиническом отношении изменений профиля безопасности препарата по сравнению с его применением в виде монотерапии.
Со стороны костномозгового кроветворения: подавление функции костного мозга было основным токсическим эффектом, ограничивающим дозу Таксола.
Нейтропения, зависящая в меньшей степени от дозы препарата и в большей — от продолжительности инфузии, наблюдается у 90% больных. Выраженная нейтропения (менее <500 клеток/мм3 крови) — приблизительно у половины пациентов, при этом у трети она сопровождается повышением температуры. Инфекционные осложнения отмечались у 30% больных. Летальный исход зарегистрирован у 1% больных с диагнозами сепсис, пневмония и перитонит.
Тромбоцитопения зафиксирована у 20% больных. У 7% больных минимальное содержание тромбоцитов снижалось до уровня менее 50000/мм3 крови.
Анемия наблюдалась у 78% больных, но имела тяжелый характер (гемоглобин менее 8 г/дл) только у 16% больных. Частота и тяжесть анемии зависели от исходного уровня гемоглобина и не зависели от дозы и режима введения препарата паклитаксела.
У больных саркомой Капоши, развившейся на фоне СПИДа, угнетение костномозгового кроветворения, инфекции и фебрильная нейтропения могут возникать более часто и иметь более тяжелое течение. Поэтому таким больным требуются более низкие дозы и поддерживающая терапия.
Реакции повышенной чувствительности: частота и тяжесть реакций повышенной чувствительности не зависели от дозы или режима введения препарата. Выраженные реакции повышенной чувствительности — артериальная гипотензия, требующая терапевтического вмешательства, ангионевротический отек, нарушение функции дыхания, требующее применения бронходилататоров, или генерализованная крапивница — отмечались менее чем в 1% случаев. У 41% больных наблюдались незначительные реакции повышенной чувствительности, в основном проявлявшиеся в виде приливов крови к лицу, сыпи, артериальной гипотензии, одышки, тахикардии и артериальной гипертензии, которые не требовали терапевтического вмешательства и не мешали продолжению лечения паклитакселом. Сообщалось о единичных случаях озноба и болях в спине, которые также были отнесены к реакциям повышенной чувствительности.
Со стороны сердечно-сосудистой системы: артериальная гипотензия или гипертензия и брадикардия обычно отмечаются во время введения препарата. Выраженность этих симптомов обычно была незначительной, терапевтического вмешательства не требовалось. Во время первого часа инфузии паклитаксела рекомендован частый контроль за жизненно важными функциями организма. В ходе клинических испытаний также наблюдались отклонения на ЭКГ. В большинстве случаев не было какой-либо четкой связи между применением паклитаксела и изменениями на ЭКГ, и указанные изменения или не были клинически значимыми, или имели минимальное клиническое значение. У одного больного (менее 1%) во время лечения паклитакселом была зарегистрирована артериальная гипертензия. Кроме того, у двух больных (менее 1%) наблюдались серьезные тромботические эпизоды (тромбоз сосудов верхней конечности и тромбофлебит). Клинически значимые нарушения деятельности сердечно-сосудистой системы (гипотензия на фоне септического шока, кардиомиопатия и тахикардия на фоне лихорадки) отмечались менее чем у 1% больных. На ранних стадиях клинических испытаний, проводившихся с различными дозировками и схемами вливания препарата, у 2% больных отмечались тяжелые побочные эффекты со стороны сердечно-сосудистой системы, вероятно, связанные с паклитакселом, включавшие асимптоматическую желудочковую тахикардию, тахикардию в сочетании с бигеминией, AV блокаду и обморок.
Со стороны дыхательной системы: в редких случаях сообщалось об интерстициальной пневмонии, легочном фиброзе и эмболии легочной артерии, а также о лучевом пневмоните у больных, одновременно проходящих курс лучевой терапии.
Со стороны нервной системы: периферическая нейропатия, главным образом проявляющаяся в форме парестезии, наблюдалась у 60% больных, в тяжелой форме — у 3% больных, и только в 1% случаев служила причиной отмены препарата. Частота периферической нейропатии увеличивалась при нарастании суммарной дозы паклитаксела. Сенсорная симптоматика обычно улучшалась или разрешалась в пределах нескольких месяцев после прекращения лечения. Предшествующие нейропатии вследствие ранее проводившегося лечения не являются противопоказанием для лечения паклитакселом.
Сообщалось о судорожных припадках типа grand mal, изменениях со стороны зрения, атаксии, энцефалопатии, нейропатии на уровне вегетативной нервной системы, приводившей к паралитической непроходимости кишечника и ортостатической гипотензии.
Со стороны скелетно-мышечной системы: артралгия или миалгия отмечались у 60% больных и носили тяжелый характер у 8% больных. Обычно симптомы носили транзиторный характер, появлялись через 2–3 дня после введения препарата Таксол® и прекращались в течение нескольких дней.
Со стороны желудочно-кишечного тракта: тошнота, рвота/понос и мукозиты отмечались у 52, 38 и 31% больных соответственно и носили легкий или умеренный характер. Кроме того, наблюдались явления непроходимости или перфорации кишечника, нейтропенического энтероколита (тифлита), тромбоз брыжеечной артерии (включая ишемический колит).
Со стороны функции печени: увеличение значений АСТ, щелочной фосфатазы и билирубина в сыворотке крови наблюдалось у 19, 22 и 7% больных соответственно. Описаны случаи некроза печени и энцефалопатии печеночного происхождения.
Со стороны мочеполовой системы: у пяти больных саркомой Капоши при лечении препаратом Таксол® развились явления почечной токсичности III или IV степени тяжести. Одному больному с подозрением на ВИЧ-ассоциированную нефропатию IV степени потребовалось прекращение лечения. У остальных больных отмечалась почечная недостаточность с обратимыми повышениями уровня сывороточного креатинина.
Реакции в месте в/в инъекции: возможны местные отеки, болевые ощущения, эритема, индурация; эпизодически экстравазация может вызывать целлюлиты. Также может отмечаться пигментация кожи. В настоящее время какие-либо специфические формы лечения реакций, связанных с экстравазацией препарата, неизвестны.
Со стороны кожных покровов: алопеция наблюдалась почти у всех больных. Нарушение пигментации или обесцвечивание ногтевого ложа встречались редко (2%). Наблюдались транзиторные кожные изменения в связи с повышенной чувствительностью к паклитакселу, макулопапулезная сыпь и зуд.
Прочие побочные реакции: астения и общее недомогание.
Взаимодействие
Реклама: ООО «ВЕДАНТА», ИНН 7714886235, erid 4CQwVszH9pUkKJ7jUDd
Реклама: ООО «РЛС-Библиомед» ИНН 7714758963
Реклама: ООО «ВЕДАНТА», ИНН 7714886235, erid 4CQwVszH9pUkKJ7jUDd
Реклама: ООО «РЛС-Библиомед» ИНН 7714758963
Премедикация циметидином не влияет на клиренс паклитаксела. По данным клинических исследований, более выраженная миелосупрессия и снижение клиренса паклитаксела примерно на 33% наблюдались при введении препарата Таксол® после введения цисплатина по сравнению с обратной последовательностью введения (Таксол® перед цисплатином).
Метаболизм паклитаксела катализируется изоэнзимами цитохрома Р450 CYP2C8 и CYP3A4. Следует соблюдать осторожность при одновременном применении препарата Таксол® и известных субстратов или ингибиторов этих изоэнзимов. Было показано, что метаболизм паклитаксела in vitro подавляется такими препаратами, как кетоконазол, верапамил, диазепам, хинидин, дексаметазон, циклоспорин, тенипозид, этопозид и винкристин. Однако использованные в экспериментах концентрации превышали обнаруживаемые in vivo после введения нормальных терапевтических доз. Тестостерон, 17альфа-этинилэстрадиол, ретиноевая кислота и кверцетин, специфический ингибитор CYP2C8 — также подавляли образование 6альфа-гидроксипаклитаксела in vitro. В результате взаимодействия с субстратами, индукторами или ингибиторами CYP2C8 и/или CYP3A4 фармакокинетика паклитаксела in vivo также может быть изменена.
При применении паклитаксела в комбинации с доксорубицином отмечались побочные эффекты, связанные с последовательностью введения этих препаратов. При введении первым препарата Таксол® (Таксол® вводился в течение 24 ч, доксорубицин — в течение 48 ч) наблюдались более выраженная нейтропения и случаи стоматита. При применении Таксола® в комбинации с доксорубицином может повышаться содержание доксорубицина (и его активного метаболита доксорубицинола) в сыворотке. Однако при струйном введении доксорубицина и введении препарата Таксол® в течение 3 ч каких-либо изменений характера токсических эффектов, связанных с последовательностью введения препаратов, не отмечалось.
Передозировка
Симптомы: подавление функции костного мозга, периферическая нейротоксичность, мукозит.
Противоядия для применения в случае передозировки Таксола® неизвестны.
Меры предосторожности
Таксол® следует вводить через систему со встроенным мембранным фильтром (размер пор не более 0,22 мкм). Во время моделированного введения раствора через трубку для в/в вливания со встроенным фильтром заметной потери активности не наблюдалось.
Таксол® необходимо применять под руководством врача, имеющего опыт использования противоопухолевых химиотерапевтических препаратов.
При использовании Таксола® в комбинации с цисплатином сначала следует вводить Таксол®, а затем цисплатин.
Выраженные реакции повышенной чувствительности, характеризующиеся одышкой, артериальной гипотензией (требующей принятия терапевтических мер), ангионевротическим отеком и генерализованной крапивницей, наблюдались примерно у 2% больных, получавших Таксол® после адекватной премедикации. Вероятно, эти симптомы представляют собой гистаминопосредованные реакции. В случае тяжелых реакций гиперчувствительности вливание препарата следует немедленно прекратить и начать симптоматическое лечение, причем вводить Таксол® повторно недопустимо.
Подавление функции костного мозга (главным образом нейтропения) является токсическим эффектом, ограничивающим дозу препарата. Во время лечения препаратом необходимо через короткие промежутки времени определять содержание форменных элементов крови. Больным не следует вновь назначать препарат до восстановления содержания нейтрофилов до уровня не менее 1500/мм3 крови (не менее 1000/мм3 крови при саркоме Капоши). При развитии тяжелой нейтропении (менее 500/мм3 крови) дозу препарата Таксол® в последующих курсах рекомендуется снижать на 20%.
Тяжелые нарушения сердечной проводимости отмечались редко. При их появлении в ходе лечения Таксолом® необходимо назначить соответствующее лечение, а при последующем введении препарата следует проводить непрерывный мониторинг функций сердца. Остальным больным рекомендуется проводить наблюдение за жизненно важными функциями организма во время первого часа введения Таксола®.
Периферическая нейропатия развивается часто и обычно носит умеренный характер. В случаях выраженной периферической нейропатии при последующих курсах лечения дозу Таксола® рекомендуется снизить на 20%.
Безопасность и эффективность Таксола® у детей не установлена.
Особые указания
При работе с Таксолом, как и с другими противоопухолевыми препаратами, необходимо соблюдать осторожность. Приготовлением растворов для вливания должен заниматься обученный персонал в специально предназначенной для этого зоне с соблюдением асептических условий. Необходимо пользоваться защитными перчатками. Следует принимать меры предосторожности во избежание контакта с кожей и слизистыми оболочками. При попадании на слизистые оболочки — промыть их водой, при попадании на кожу — водой с мылом.
При приготовлении, хранении и введении Таксола следует пользоваться оборудованием, которое не содержит деталей из ПВХ.
Приготовленные растворы стабильны не более 27 ч (включая время подготовки и вливания) при температуре приблизительно 25 °C в условиях комнатного освещения. Разбавленные растворы не следует помещать в холодильник.
Приготовленные растворы могут опалесцировать из-за присутствующей в составе лекарственной формы основы-носителя, причем после фильтрования опалесценция раствора сохраняется.
Форма выпуска
Концентрат для приготовления раствора для инфузий, 30 мг/5 мл или 100 мг/16,7 мл (6 мг/мл). Во флаконах из бесцветного стекла, укупоренных фторрезинофвой или бутилрезиновой пробкой с тефлоновым покрытием под алюминиевой обкаткой с пластиковой крышкой или защитным колпачком, с контролем первого вскрытия. По 1 флакону в защитном контурном вкладыше помещают в картонную коробку.
Производитель
Бристол-Майерс Сквибб С.р.Л., Италия.
Bristol-Myers Squibb S.r.L., Italy.
Виа дел Мурилло Км 2,800, 04010 — Сермонета (ЛТ), Италия.
Via del Murillo Km 2,800, 04010-Sermoneta (LT), Italy.
Претензии потребителей направлять по адресу
ООО «Бристол-Майерс Сквибб», Россия.
105064, Москва, ул. Земляной Вал, 9.
Тел.:+7(495) 755-92-67, факс:+7(495) 755-92-62.
Комментарий
При хранении невскрытых флаконов в холодильнике, может наблюдаться выпадение осадка, который растворяется при согревании флакона до комнатной температуры при незначительном перемешивании (или без него). Качество препарата при этом не ухудшается. Если препарат во флаконе остается мутным или наблюдается нерастворимый осадок, препарат следует уничтожить.
Замораживание не влияет на качество препарата. Разбавленные растворы стабильны в течение 27 ч при хранении при температуре не выше 25 °C и комнатном освещении (с учетом времени инфузии).
Растворы, полученные разведением препарата 5% раствором декстрозы стабильны в течение 7 дней, растворы, полученные разведением 0,9% раствором натрия хлорида стабильны в течение 14 дней при хранении при температуре от 5 до 25 °C.
Разбавленные растворы не следует хранить в холодильнике.
Условия отпуска из аптек
По рецепту.
Условия хранения
В защищенном от света месте, при температуре 15–30 °C.
Замораживание не влияет на качество препарата. Разбавленные растворы не следует помещать в холодильник.
Хранить в недоступном для детей месте.
Срок годности
2 года.
Не применять по истечении срока годности, указанного на упаковке.
Таксол® (Taxol) инструкция по применению
📜 Инструкция по применению Таксол®
💊 Состав препарата Таксол®
✅ Применение препарата Таксол®
📅 Условия хранения Таксол®
⏳ Срок годности Таксол®
⚠️ Государственная регистрация данного препарата отменена
Описание лекарственного препарата
Таксол®
(Taxol)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для электронного издания справочника Видаль 2010
года, дата обновления: 2009.12.01
Владелец регистрационного удостоверения:
Код ATX:
L01CD01
(Паклитаксел)
Лекарственные формы
| Таксол® |
Конц. д/пригот. р-ра д/инф. 6 мг/1 мл: фл. 100 мг 1 шт. рег. №: П N013329/01 |
|
|
Конц. д/пригот. р-ра д/инф. 6 мг/1 мл: фл. 30 мг 1 шт. рег. №: П N013329/01 |
Форма выпуска, упаковка и состав
препарата Таксол®
Концентрат для приготовления раствора для инфузий прозрачный, бесцветный или слегка желтоватый, вязкий раствор.
Вспомогательные вещества: макрогола глицерилрицинолеат (кремофор®ЕL), этанол, азот.
5 мл — флаконы объемом 5 мл (1) — пачки картонные.
Концентрат для приготовления раствора для инфузий прозрачный, бесцветный или слегка желтоватый, вязкий раствор.
Вспомогательные вещества: макрогола глицерилрицинолеат (кремофор®ЕL), этанол, азот.
16.7 мл — флаконы объемом 20 мл (1) — пачки картонные.
Фармакологическое действие
Противоопухолевый препарат, получаемый биосинтетическим путем. Механизм действия связан со способностью стимулировать «сборку» микротрубочек из димерных молекул тубулина, стабилизировать их структуру за счет подавления деполимеризации и тормозить динамическую реорганизацию в интерфазе, что нарушает митотическую функцию клетки.
Кроме того, паклитаксел индуцирует образование аномальных скоплений или «связок» микротрубочек на протяжении клеточного цикла и вызывает образование множественных звезд микротрубочек во время митоза.
Вызывает дозозависимое подавление костномозгового кроветворения.
В экспериментальных исследованиях показано, что паклитаксел обладает мутагенными и эмбриотоксическими свойствами, вызывает снижение репродуктивной функции.
Фармакокинетика
Фармакокинетику паклитаксела изучали после в/в инфузии препарата в дозах 135 мг/м2 и 175 мг/м2 в течение 3 и 24 ч.
Распределение
После в/в введения концентрация паклитаксела в плазме крови уменьшается в соответствии с двухфазной кинетикой.
Средний Vd составляет от 198 до 688 л/м2.
Фармакокинетика паклитаксела с повышением дозы приобретает нелинейный характер. При увеличении дозы препарата на 30% (от 135 мг/м2 до 175 мг/м2) значения Cmax и AUC0-∞ увеличивались на 75% и 81% соответственно.
При повторных курсах терапии не было получено указаний на кумуляцию паклитаксела.
Связывание с белками составляет в среднем 89%.
Метаболизм
В исследованиях in vitro было показано, что паклитаксел метаболизируется в печени с участием изофермента CYP2C8 с образованием метаболита 6-альфа-гидроксипаклитаксел и с участием изофермента CYP3A4 с образованием метаболитов 3-пара-гидроксипаклитаксел и 6-альфа, 3-пара-дигидроксипаклитаксел.
Выведение
T1/2 и общий клиренс паклитаксела вариабельны, зависят от дозы и длительности введения и составляют 13-52.7 ч и 12.2-23.8 л/ч/м2 соответственно
От 1.3% до 12,6 % введенной дозы (15-275 мг/м2 в виде 1-, 6- или 24-часовой инфузии) препарата выделяется с мочой в неизмененном виде, что указывает на наличие интенсивного внепочечного клиренса.
Фармакокинетика в особых клинических случаях
Влияние нарушения функции почек на метаболизм паклитаксела не исследовалось.
Диализ не оказывает влияния на скорость выведения препарата из организма.
Показания препарата
Таксол®
Рак яичников:
- терапия 1 линии в комбинации с цисплатином у больных с распространенным метастатическим процессом или остаточной опухолью (более 1 см) после проведения исходной лапаротомии;
- терапия 2 линии у больных с распространенным метастатическим раком яичников после стандартной терапии, не приведшей к положительному результату.
Рак молочной железы:
- адъювантная терапия у больных с наличием метастазов в лимфатических узлах после проведения стандартного комбинированного лечения;
- терапия 1 линии метастатического рака и при прогрессировании заболевания после адъювантной терапии с применением препаратов антрациклинового ряда;
- терапия 2 линии при прогрессировании заболевания после комбинированной химиотерапии с применением противоопухолевых антибиотиков антрациклинового ряда при отсутствии противопоказаний для их применения;
- адъювантная терапия для лечения пациентов после терапии препаратами антрациклинового ряда и циклофосфамидом;
- терапия 1 линии метастатического рака молочной железы в комбинации с трастузумабом у пациенток с уровнем 3+ экспрессии HER-2 по данным иммуногистохимического исследования и при наличии противопоказаний к терапии препаратами антрациклинового ряда.
Немелкоклеточный рак легкого:
- в качестве терапии 1 линии в комбинации с цисплатином или для монотерапии немелкоклеточного рака легкого у больных, которым не планируется проведение хирургического лечения и/или лучевой терапии.
Саркома Капоши у больных СПИД:
- в качестве терапии 2 линии.
Режим дозирования
Для предупреждения тяжелых реакций повышенной чувствительности до введения препарата Таксол следует провести премедикацию с применением ГКС, блокаторов гистаминовых H1-рецепторов и блокаторов гистаминовых H2-рецепторов. Например, дексаметазон (или его эквивалент) в дозе 20 мг внутрь приблизительно за 12 ч и 6 ч до введения препарата Таксол или дексаметазон в дозе 20 мг в/в примерно за 30-60 мин до введения препарата Таксол, дифенгидрамин (или эквивалент) в дозе 50 мг в/в и циметидин в дозе 300 мг или ранитидин в дозе 50 мг в/в за 30-60 мин до введения препарата Таксол.
Рак яичников
Терапия 1 линии: рекомендуемая доза препарата Таксол составляет 175 мг/м2 в виде в/в инфузии в течение 3 ч или 135 мг/м2 в виде в/в инфузии в течение 24 ч с последующим введением цисплатина в дозе 75 мг/м2; интервал между курсами лечения должен составлять 3 недели.
Терапия 2 линии: в режиме монотерапии доза препарата Таксол составляет 175 мг/м2 в виде в/в инфузии в течение 3 ч каждые 3 недели.
Рак молочной железы
Адъювантная терапия проводится после стандартной комбинированной терапии. Доза препарата Таксол составляет 175 мг/м2 в виде в/в инфузии в течение 3 ч. Всего рекомендуется проведение 4 курсов терапии с интервалом 3 недели.
Терапия 1 линии
В режиме монотерапии: доза препарата Таксол составляет 175 мг/м2 в виде в/в инфузии в течение 3 ч каждые 3 недели.
В режиме комбинированной терапии:
- В комбинации с трастузумабом, рекомендованная доза Таксола составляет 175 мг/м2 в виде в/в инфузии в течение 3 ч каждые 3 недели. Начинать применение Таксола можно на следующий день, после введения первой дозы трастузумаба или, при хорошей переносимости, в день применения трастузумаба.
- В комбинации с доксорубицином (50 мг/м) Таксол назначают в дозе 220 мг/м2 в виде в/в инфузии в течение 3 ч каждые 3 недели. Начинать применение Таксола следует через 24 часа после применения доксорубицина.
Терапия 2 линии
Для лечения больных с диссеминированным заболеванием после комбинированной химиотерапии, не давшей положительного результата -175 мг/м2 в виде в/в инфузии в течение 3 ч каждые 3 недели.
Немелкоклеточный рак легких
- в режиме комбинированной терапии рекомендуемая доза препарата Таксол составляет 175 мг/м2 в виде в/в инфузии в течение 3 ч или 135 мг/м2 в виде в/в инфузии в течение 24 ч с последующим введением цисплатина, интервал между курсами составляет 3 недели;
- в режиме монотерапии рекомендуемая доза препарата Таксол составляет от 175 мг/м2 до 225 мг/м2 в виде в/в инфузии в течение 3 ч каждые 3 недели.
Саркома Капоши у больных СПИД
При терапии 2 линии рекомендуемая доза препарата Таксол составляет 135 мг/м2 в виде в/в инфузии в течение 3 ч каждые 3 недели или 100 мг/м2 в/в капельно в течение 3 ч каждые 2 недели.
В зависимости от иммуносупрессии, наблюдаемой у больных с развивающейся формой СПИД, рекомендуется:
1. уменьшить дозу дексаметазона для приема внутрь (одного из трех компонентов премедикации) до 10 мг;
2. вводить Таксол только при содержании нейтрофилов не менее 1000/мкл;
3. больным с тяжелой нейтропенией (менее 500/мкл в течение недели или более) при последующих курсах уменьшить дозу препарата Таксол на 20%;
4. по клиническим показаниям одновременно применять Г-КСФ.
Правила приготовления раствора для инфузий
Перед введением концентрат разбавляют до концентрации 0.3-1.2 мг/мл 0.9% раствором натрия хлорида, 5% раствором декстрозы, 5% раствором декстрозы в 0.9% растворе натрия хлорида или 5% раствором декстрозы в растворе Рингера.
Таксол следует вводить через систему со встроенным мембранным фильтром с размером пор не более 0.22 мкм.
Приготовленные растворы могут опалесцировать из-за присутствующей в составе лекарственной формы основы-носителя, причем после фильтрования опалесценция раствора сохраняется.
При приготовлении, хранении и введении препарата Таксол следует пользоваться оборудованием, которое не содержит деталей из поливинилхлорида.
Побочное действие
При применении комбинации препарата Таксол с препаратами платины не было отмечено каких-либо существенных в клиническом отношении изменений профиля безопасности препарата, по сравнению с его использованием в виде монотерапии.
У больных саркомой Капоши, развившейся на фоне СПИД, чаще возникают и тяжелее протекают угнетение кроветворения, инфекции (включая оппортунистические инфекции) и фебрильная нейтропения. У этих пациентов требуется снижение дозы препарата и поддерживающая терапия.
Определение частоты побочных эффектов: очень часто (≥1/10), часто (≥1/100, <1/10), иногда (≥1/1000, <1/100), редко (≥1/10 000, <1/1000), очень редко (<1/10 000).
Со стороны системы кроветворения: очень часто — миелосупрессия, нейтропения, анемия, тромбоцитопения, лейкопения, лихорадка, кровотечения; редко — фебрильная нейтропения; очень редко — острый миелоидный лейкоз, миелодиспластический синдром.
Нейтропения (90%), зависящая в меньшей степени от дозы препарата и в большей — от продолжительности инфузии; выраженная нейтропения (менее 500/мкл) чаще наблюдается при 24-часовых инфузиях, чем при 3-часовых примерно у половины пациентов, при этом у 1/3 она сопровождается повышением температуры; развитие инфекционных осложнений (30%); у 1% больных с диагнозами сепсис, пневмония, перитонит зарегистрирован летальный исход.
Тромбоцитопения (20%) с содержанием тромбоцитов менее 100 000/мкл; выраженная тромбоцитопения с минимальным содержанием тромбоцитов ниже 50 000/мкл (7%); анемия (78%); тяжелая анемия с гемоглобином менее 8 г/дл (16%).
Частота и тяжесть анемии зависели от исходного содержания гемоглобина и не зависели от дозы и режима введения препарата Таксол.
Аллергические реакции: очень часто — незначительные проявления, в основном в виде ощущения жара («приливов»), кожной сыпи; иногда — выраженные реакции повышенной чувствительности (снижение АД, ангионевротический отек, тахикардия, нарушение функции дыхания, генерализованная крапивница), боли в спине, озноб; редко — анафилактические реакции (в т. ч. с летальным исходом); очень редко — анафилактический шок.
Со стороны сердечно-сосудистой системы: очень часто — изменения на ЭКГ, снижение АД; часто — брадикардия; иногда — кардиомиопатия, асимптоматическая желудочковая тахикардия, тахикардия с бигеминией, AV — блокада и обморок, инфаркт миокарда, повышение АД, тромбоз, тромбофлефит; очень редко — мерцание предсердий, суправентрикулярная тахикардия, шок.
Со стороны дыхательной системы: редко — одышка, плевральный выпот, дыхательная недостаточность, интерстициальная пневмония, фиброз легких, эмболия легочной артерии; очень редко — кашель. Отмечено более частое развитие лучевого пневмонита у больных, одновременно проходящих курс лучевой терапии.
Со стороны ЦНС и периферической нервной системы: очень часто — периферическая сенсорная невропатия; редко — двигательная невропатия (слабость конечностей); очень редко — вегетативная невропатия, проявляющаяся паралитической непроходимостью кишечника и ортостатической гипотензией, припадки типа grand mal, судороги, энцефалопатия, головокружение, головная боль, атаксия.
Со стороны костно-мышечной системы: очень часто — артралгия, миалгия.
Со стороны пищеварительной системы: очень часто — тошнота, рвота, диарея, мукозит; часто — значительное повышение уровня АСТ, ЩФ; иногда — значительное повышение уровня билирубина; редко — кишечная непроходимость, перфорация кишечника, ишемический колит, панкреатит; очень редко — тромбоз брыжеечной артерии, псевдомембранозный колит, эзофагит, запор, асцит, гепатонекроз с летальным исходом, печеночная энцефалопатия с летальным исходом.
Со стороны мочевыделительной системы: у больных с саркомой Капоши и СПИД описаны случаи нарушения функции почек с обратимыми повышениями уровня сывороточного креатинина.
Дерматологические реакции: очень часто — алопеция; редко — зуд, сыпь, эритема, фиброз, очень редко — синдром Стивенса-Джонсона, эпидермальный некролиз, экссудативная многоформная эритема, эксфолиативный дерматит, крапивница, онихолизис.
Местные реакции: часто — болевые ощущения, отек, эритема, индурация и пигментация кожи в месте инъекции, редко — флебит, шелушение кожи; экстравазация может вызывать воспаление и некроз подкожной клетчатки.
Прочие: анорексия, спутанность сознания, астения и общее недомогание.
Противопоказания к применению
- исходное содержание нейтрофилов менее 1500/мкл у пациентов с солидными опухолями;
- исходное (или зарегистрированное в процессе лечения) содержание нейтрофилов менее 1000/мкл у пациентов с саркомой Капоши у больных СПИД;
- сопутствующие, серьезные, неконтролируемые инфекции у больных саркомой Капоши;
- беременность;
- лактация (грудное вскармливание);
- повышенная чувствительность к компонентам препарата (в т.ч. к полиоксиэтилированному касторовому маслу).
С осторожностью следует применять препарат при тромбоцитопении (менее 100 000/мкл), печеночной недостаточности, острых инфекционных заболеваниях (в т.ч. опоясывающий лишай, ветряная оспа, герпес), тяжелом течении ИБС, при инфаркте миокарда (в анамнезе), при аритмии.
Применение при беременности и кормлении грудью
Таксол противопоказан к применению при беременности и в период лактации (грудного вскармливания).
Больным детородного возраста во время лечения Таксолом и, по крайней мере, в течение 3 месяцев после окончания терапии следует использовать надежные методы контрацепции.
Применение при нарушениях функции печени
Изменения метаболизма паклитаксела при нарушениях функции печени при трехчасовом вливании формально не исследовалось.
Применение при нарушениях функции почек
Изменения метаболизма паклитаксела при нарушениях функции почек при трехчасовом вливании формально не исследовалось.
Применение у детей
Безопасность и эффективность применения препарата Таксол® у детей не установлены.
Особые указания
Лечение Таксолом должен проводить врач, имеющий опыт работы с противоопухолевыми химиотерапевтическими препаратами.
При применении Таксола в комбинации с цисплатином, сначала следует вводить Таксол, а затем цисплатин.
Во время лечения необходимо регулярно контролировать картину периферической крови, АД, ЧСС и число дыханий (особенно на протяжении первого часа инфузии), ЭКГ-контроль (и до начала лечения).
В случае развития тяжелых реакций гиперчувствительности вливание препарата Таксол следует немедленно прекратить и начать симптоматическое лечение, причем вводить препарат повторно не следует.
В случаях развития нарушений AV-проводимости, при повторных введениях необходимо проводить непрерывный кардиомониторинг.
Таксол является цитотоксическим веществом, при работе с которым необходимо соблюдать осторожность, пользоваться перчатками и избегать его попадания на кожу или слизистые оболочки, которые в таких случаях необходимо тщательно промыть мылом и водой, либо (глаза) большим количеством воды.
Влияние на способность к управлению транспортными средствами и механизмами
В период лечения пациенты должны воздерживаться от занятий потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций.
Использование в педиатрии
Безопасность и эффективность применения препарата Таксол® у детей не установлены.
Передозировка
Симптомы: аплазия костного мозга, периферическая невропатия, мукозиты.
Лечение: проводят симптоматическую терапию. Специфический антидот паклитаксела неизвестен.
Лекарственное взаимодействие
Цисплатин снижает общий клиренс паклитаксела на 33% (при этом более выраженная миелосупрессия наблюдается в случае, когда паклитаксел вводят после цисплатина).
При применении Таксола в комбинации с доксорубицином возможно повышение концентрации доксорубицина (и его активного метаболита доксорубицинола) в плазме крови. При введении препарата Таксол (инфузия в течение 24 ч) перед введением доксорубицина (инфузия в течение 48 ч) наблюдались более выраженная нейтропения и случаи стоматита. Однако при струйном введении доксорубицина и введении препарата Таксол в течение 3 ч каких-либо изменений характера токсических эффектов, связанных с последовательностью введения препаратов не отмечалось.
Одновременное применение с циметидином, ранитидином, дексаметазоном или дифенгидрамином не влияет на связывание паклитаксела с белками плазмы крови.
Метаболизм паклитаксела катализируется изоферментами CYP2C8 и CYP3А4, в связи с чем требуется осторожность при применении Таксола на фоне лечения субстратами, индукторами (например, рифампицин, карбамазепин, фенобарбитал, фенитоин, эфавиренз, невирапин) или ингибиторами (например, эритромицин, флуоксетин, гемфиброзил) изоферментов CYP2C8 и CYP3А4.
In vitro ингибиторы микросомального окисления (в т.ч. кетоконазол, верапамил, диазепам, хинидин, циклоспорин) в концентрациях, превышающих при применении в терапевтических дозах in vivo , а также тестостерон, 17α-этинилэстрадиол, ретиноевая кислота и кверцетин подавляют метаболизм паклитаксела.
Макрогола глицерилрицинолеат, входящий в состав препарата Таксол, может вызывать экстракцию ДЭГП [ди-(2-этилгексил)фталата] из пластифицированных поливинилхлоридных контейнеров, причем степень вымывания ДЭГП увеличивается при увеличении концентрации раствора и со временем.
Условия хранения препарата Таксол®
Список Б. Препарат следует хранить в недоступном для детей, защищенном от света месте при температуре от 15° до 30°С.
Срок годности препарата Таксол®
Срок годности — 2 года.
При хранении невскрытых флаконов в холодильнике препарат может выпасть в осадок, который вновь растворяется при согревании флакона до комнатной температуры при незначительном помешивании (или без него). Качество препарата при этом не ухудшается. Если препарат во флаконе остается мутным или наблюдается нерастворимый осадок, препарат следует выбросить. Замораживание не влияет на качество препарата.
Разбавленные растворы стабильны в течение 27 ч при хранении при температуре не выше 25°С и комнатном освещении (с учетом времени инфузии).
Растворы, полученные при разведении препарата 5% раствором декстрозы, стабильны в течение 7 дней; растворы, полученные разведением 0.9% раствором натрия хлорида, стабильны в течение 14 дней при хранении при температуре от 5° до 25°С.
Разбавленные растворы не следует хранить в холодильнике.
Условия реализации
Препарат отпускается по рецепту.
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Аналоги препарата
Абитаксел
(Laboratorio TUTEUR S.A.C.I.F.I.A., Аргентина)
Канатаксен
(GENFA MEDICA, Швейцария)
Митотакс®
(Dr. Reddy`s Laboratories, Индия)
Пакликал®
(OASMIA PHARMACEUTICAL, Швеция)
Паклитаксел
(ДЖОДАС ЭКСПОИМ, Россия)
Паклитаксел
(БЕЛМЕДПРЕПАРАТЫ, Республика Беларусь)
Паклитаксел
(HETERO LABS, Индия)
Паклитаксел
(ИРВИН 2, Россия)
Паклитаксел Эльфа
(Teva Pharmaceutical Industries, Израиль)
Паклитаксел-ДЕКО
(КОМПАНИЯ ДЕКО, Россия)
Все аналоги
При использовании комбинации Таксола с препаратами платины не было отмечено каких-либо существенных в клиническом отношении изменений профиля безопасности препарата по сравнению с его применением в виде монотерапии.
Со стороны костномозгового кроветворения: подавление функции костного мозга было основным токсическим эффектом, ограничивающим дозу Таксола.
Нейтропения, зависящая в меньшей степени от дозы препарата и в большей — от продолжительности инфузии, наблюдается у 90% больных. Выраженная нейтропения (менее <500 клеток/мм3 крови) — приблизительно у половины пациентов, при этом у трети она сопровождается повышением температуры. Инфекционные осложнения отмечались у 30% больных. Летальный исход зарегистрирован у 1% больных с диагнозами сепсис, пневмония и перитонит.
Тромбоцитопения зафиксирована у 20% больных. У 7% больных минимальное содержание тромбоцитов снижалось до уровня менее 50000/мм3 крови.
Анемия наблюдалась у 78% больных, но имела тяжелый характер (гемоглобин менее 8 г/дл) только у 16% больных. Частота и тяжесть анемии зависели от исходного уровня гемоглобина и не зависели от дозы и режима введения препарата паклитаксела.
У больных саркомой Капоши, развившейся на фоне СПИДа, угнетение костномозгового кроветворения, инфекции и фебрильная нейтропения могут возникать более часто и иметь более тяжелое течение. Поэтому таким больным требуются более низкие дозы и поддерживающая терапия.
Реакции повышенной чувствительности: частота и тяжесть реакций повышенной чувствительности не зависели от дозы или режима введения препарата. Выраженные реакции повышенной чувствительности — артериальная гипотензия, требующая терапевтического вмешательства, ангионевротический отек, нарушение функции дыхания, требующее применения бронходилататоров, или генерализованная крапивница — отмечались менее чем в 1% случаев. У 41% больных наблюдались незначительные реакции повышенной чувствительности, в основном проявлявшиеся в виде приливов крови к лицу, сыпи, артериальной гипотензии, одышки, тахикардии и артериальной гипертензии, которые не требовали терапевтического вмешательства и не мешали продолжению лечения паклитакселом. Сообщалось о единичных случаях озноба и болях в спине, которые также были отнесены к реакциям повышенной чувствительности.
Со стороны сердечно-сосудистой системы: артериальная гипотензия или гипертензия и брадикардия обычно отмечаются во время введения препарата. Выраженность этих симптомов обычно была незначительной, терапевтического вмешательства не требовалось. Во время первого часа инфузии паклитаксела рекомендован частый контроль за жизненно важными функциями организма. В ходе клинических испытаний также наблюдались отклонения на ЭКГ. В большинстве случаев не было какой-либо четкой связи между применением паклитаксела и изменениями на ЭКГ, и указанные изменения или не были клинически значимыми, или имели минимальное клиническое значение. У одного больного (менее 1%) во время лечения паклитакселом была зарегистрирована артериальная гипертензия. Кроме того, у двух больных (менее 1%) наблюдались серьезные тромботические эпизоды (тромбоз сосудов верхней конечности и тромбофлебит). Клинически значимые нарушения деятельности сердечно-сосудистой системы (гипотензия на фоне септического шока, кардиомиопатия и тахикардия на фоне лихорадки) отмечались менее чем у 1% больных. На ранних стадиях клинических испытаний, проводившихся с различными дозировками и схемами вливания препарата, у 2% больных отмечались тяжелые побочные эффекты со стороны сердечно-сосудистой системы, вероятно, связанные с паклитакселом, включавшие асимптоматическую желудочковую тахикардию, тахикардию в сочетании с бигеминией, AV блокаду и обморок.
Со стороны дыхательной системы: в редких случаях сообщалось об интерстициальной пневмонии, легочном фиброзе и эмболии легочной артерии, а также о лучевом пневмоните у больных, одновременно проходящих курс лучевой терапии.
Со стороны нервной системы: периферическая нейропатия, главным образом проявляющаяся в форме парестезии, наблюдалась у 60% больных, в тяжелой форме — у 3% больных, и только в 1% случаев служила причиной отмены препарата. Частота периферической нейропатии увеличивалась при нарастании суммарной дозы паклитаксела. Сенсорная симптоматика обычно улучшалась или разрешалась в пределах нескольких месяцев после прекращения лечения. Предшествующие нейропатии вследствие ранее проводившегося лечения не являются противопоказанием для лечения паклитакселом.
Сообщалось о судорожных припадках типа grand mal, изменениях со стороны зрения, атаксии, энцефалопатии, нейропатии на уровне вегетативной нервной системы, приводившей к паралитической непроходимости кишечника и ортостатической гипотензии.
Со стороны скелетно-мышечной системы: артралгия или миалгия отмечались у 60% больных и носили тяжелый характер у 8% больных. Обычно симптомы носили транзиторный характер, появлялись через 2–3 дня после введения препарата Таксол® и прекращались в течение нескольких дней.
Со стороны желудочно-кишечного тракта: тошнота, рвота/понос и мукозиты отмечались у 52, 38 и 31% больных соответственно и носили легкий или умеренный характер. Кроме того, наблюдались явления непроходимости или перфорации кишечника, нейтропенического энтероколита (тифлита), тромбоз брыжеечной артерии (включая ишемический колит).
Со стороны функции печени: увеличение значений АСТ, щелочной фосфатазы и билирубина в сыворотке крови наблюдалось у 19, 22 и 7% больных соответственно. Описаны случаи некроза печени и энцефалопатии печеночного происхождения.
Со стороны мочеполовой системы: у пяти больных саркомой Капоши при лечении препаратом Таксол® развились явления почечной токсичности III или IV степени тяжести. Одному больному с подозрением на ВИЧ-ассоциированную нефропатию IV степени потребовалось прекращение лечения. У остальных больных отмечалась почечная недостаточность с обратимыми повышениями уровня сывороточного креатинина.
Реакции в месте в/в инъекции: возможны местные отеки, болевые ощущения, эритема, индурация; эпизодически экстравазация может вызывать целлюлиты. Также может отмечаться пигментация кожи. В настоящее время какие-либо специфические формы лечения реакций, связанных с экстравазацией препарата, неизвестны.
Со стороны кожных покровов: алопеция наблюдалась почти у всех больных. Нарушение пигментации или обесцвечивание ногтевого ложа встречались редко (2%). Наблюдались транзиторные кожные изменения в связи с повышенной чувствительностью к паклитакселу, макулопапулезная сыпь и зуд.
Прочие побочные реакции: астения и общее недомогание.
Немного фактов
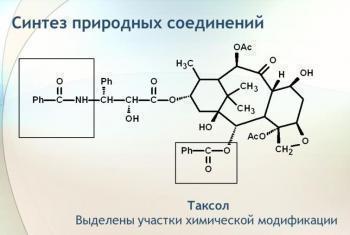
Таксол химиотерапевтический антибластомный медпрепарат, обладающий цитостатическими свойствами. Терапевтический эффект обусловлен включением действующих веществ в структуру ДКН раковых клеток, в связи с чем нарушается митоз и прогрессирование раковых новообразований. Применяется в онкологии для лечения карциномы молочной железы и яичников, а также немелкоклеточного бронхогенного рака.
Нозологическая классификация болезней (МКБ-10)
Таксол относится к цитостатическим антибластомным средствам, которые применяются в химиотерапии заболеваний A00-В99 класс I и C00-D48 класс II.
Форма выпуска и биохимический состав
Цитостатический препарат производится в форме вязкого раствора с желтоватым оттенком. В 1 мл гидрофобной жидкости содержится:
- метилкарбинол 396.2 мг;
- паклитаксел 6.0 мг;
- полиэтоксилированное касторовое масло 527.1 мг.
Таксол выпускается в стеклянных пузырьках объемом по 5 мл. В белой картонной коробке содержится 1 флакон с раствором.
Фармакотерапевтические свойства
Паклитаксел является антинеопластическим средством из группы таксанов, использующихся в химиотерапии злокачественных опухолей. Оказывает выраженное цитотоксическое действие на раковые клетки, что приводит к нарушению процессов их роста, развития и деления.
Противоопухолевое лекарство способствует сборке белковых внутриклеточных структур из тубулиновых димеров в результате подавления деполимеризации. В связи с этим нарушается реорганизация целых структур микротрубочек, необходимых на стадии интерфазы и митоза.
Действующие компоненты индуцируют формирование аномальных структур из цитоскелетов на протяжении всего клеточного цикла. За счет этого нарушается процесс образования дочерних раковых клеток и, как следствие, снижаются темпы разрастания злокачественных новообразований.
Фармакокинетические свойства
Уровень паклитаксела в сыворотке крови понижается после парентерального введения в соответствии с двухфазной кинетикой. Фармакокинетические свойства проявляются в течение 3 и 24 часов после применения антибластомного раствора. В случае многоразового проведения терапии кумуляция действующих веществ не обнаруживается.
В ходе медицинских испытаний in vitro было установлено, что более 95% паклитаксела находится в связанном состоянии. По этой причине параллельное использование Дексаметазона и Циметидина никак не влияет на скорость присоединения молекул цитостатика к белковым компонентам крови.
Процесс метаболизации Таксола в человеческом организме изучен недостаточно. Не более 13% лекарственного раствора выводится в неизменном виде вместе с уриной. Период полураспада колеблется в диапазоне от 3.5 до 52 часов. Основными продуктами распада препарата являются гидроксилированные соединения.
Считается, что паклитаксел подвергается биотрансформации в паренхиматозной ткани под влиянием желчи. Согласно результатам исследований, принудительный диализ не сказывается на скорости выведения метаболитов лекарства из организма.
Показания к применению
Антинеопластический лекарственный раствор используется в химиотерапии злокачественных опухолей, локализующихся преимущественно в органах дыхания и репродуктивной системы. Основными показаниями к назначению противоракового средства являются:
- терапия немелкоклеточной бронхогенной карциномы у больных, прошедших радиационное лечение или при неоперабельной опухоли;
- терапия раковых опухолей в яичниках при использовании Таксола в качестве монопрепарата или в сочетании с другими цитостатическими средствами;
- фармакотерапия метастазирующей карциномы молочной железы после неудачного проведения стандартной схемы лечения.
В случае вторичного развития карциномы яичников антибластомный раствор используют при появлении метастазов. Также Таксол назначается больным, прошедшим лапаротомию и лечение Ципластином.
Методы введения и дозирование
Антибластомный раствор вводится в организм пациента капельно методом инфузии. Дозировка зависит от формы онкологического заболевания и скорости прогрессирования злокачественных опухолей:
- первичная фармакотерапия рака яичников 135 мг/м2 раствора методом капельного вливания в течение суток с последующим использованием Ципластина в дозировке 75 мг/м2 (минимальный интервал между курсами химиотерапии составляет 72 часа);
- вторичная фармакотерапия рака яичников и молочной железы капельное введение 175 мг/ м2 на протяжении 3 часов с перерывом между курсами в 21 день;
- первичная фармакотерапия бронхогенной карциномы капельное вливание 175 мг/ м2 на протяжении 180 минут с интервалом в 21 день.
Цитостатические препараты оказывают выраженные побочные действия на организм. В связи с этим перед началом курса все пациенты проходят премедикацию с применением противоаллергических (антигистаминных) средств и кортикостероидов.
Повторное введение антибластомного раствора совершают только в том случае, если уровень нейтрофилов в крови достигает хотя бы 1.5×109/л. При возникновении агранулоцитоза нужно уменьшить дозировку минимум на 20%.
Приготовление раствора
Перед парентеральным введением Таксол нужно разбавлять с медицинскими растворителями до концентрации не более 1.2 мг/мл. В качестве растворителей обычно используются:
- изотонический раствор хлористого натрия;
- 5% раствор глюкозы для инфузий;
- многокомпонентный физраствор (раствор Рингера) в сочетании с изотоническим раствором глюкозы.
Приготовленный лекарственный препарат необходимо вводить через специальную систему, оснащенную мембранными фильтрами. При этом размер фракций фильтрующей мембраны не должен превышать 0.22 микрон.
Беременность и грудное вскармливание
Испытания на животных указывают на наличие фетотоксического и эмбрионотоксического действия противоопухолевого раствора на плод. Курсовое применение цитостатика сказывается на функционировании репродуктивной системы женщины. В связи с этим Таксол не назначают при гестации и кормлении грудью.
Пациенткам репродуктивного возраста нужно избегать зачатия во время фармакотерапии. Медицинские исследования подтвердили факт развития пороков у эмбриона в случае введения цитостатического средства в терапевтической дозировке.
Совместимость с алкоголем
В противоопухолевом препарате содержится этанол, который может влиять на функционирование ЦНС и других жизненно важных систем. Употребление спиртосодержащих напитков может потенцировать побочное действие противоракового раствора.

Взаимодействие с медикаментами
Премедикация ингибиторами H2-гистаминовых рецепторов никак не влияет на клиренс антибластомного средства. В ходе медицинских исследований было установлено, что миелосупрессия наблюдается в случае введения Таксола сразу после использования Ципластина.
Процесс расщепления действующих веществ ускоряется под воздействием изозимов CYP2C8 и CYP3A4. Нужно с осторожностью использовать медпрепарат в сочетании с ингибиторами упомянутых изоферментов или их субстратами.
Метаболизация паклитаксела замедляется при параллельном использовании таких медикаментов, как:
- Винкристин;
- Хинидин;
- Кетоконазол;
- Тенипозид;
- Диазепам и т.д.
Ингибиторы CYP2C8, андрогены, Третиноин и Кверцетин также препятствует расщеплению активных компонентов до гидроксипаклитаксела. В случае взаимодействия препарата Таксола с субстратами и ингибиторами изофермента CYP3A4 фармакокинетические свойства могут изменяться.
Особые указания
Антибластомный препарат может использоваться только в присутствии лечащего врача, имеющего опыт в терапии злокачественных новообразований. При возникновении нежелательных реакций в виде ангионевротического отека, артериальной гипотензии, одышки и генерализованных высыпаний на коже инфузию нужно прекратить.
На протяжении всего курса химиотерапии следует контролировать частоту сердечных сокращений и артериальное давление. В особенности это касается пациентов только что начавших лечение противоопухолевым средством. В случае нарушения функций жизненно важных органов следует начать паллиативную терапию. При повторном введении раствора рекомендуется вести непрерывный мониторинг функциональной активности сердца.
Вероятность развития лучевого пневмонита повышается при параллельном прохождении лучевой терапии. Поэтому в современных схемах лечения стараются не комбинировать прием цитостатиков с физиотерапевтическими процедурами.
Антибластомный препарат деструктивно влияет не только на раковые, но и на здоровые клетки. В особенности это касается лабильных клеток, из которых состоят иммунокомпетентные и костные ткани. Именно поэтому во время лечения желательно постоянно контролировать уровень форменных элементов крови. Игнорирование этого правила чревато развитием агранулоцитоза и даже летальным исходом.
При дисфункции органов детоксикации химиотерапию проводят под пристальным наблюдением медперсонала. Действующие компоненты антинеопластического средства метаболизируются в паренхиме и почках. Патологии этих органов нередко приводят к развитию осложнений печеночная энцефалопатия, гипербилирубинемия, ишемический колит и т.д.
Передозировка
Превышение терапевтической дозы противоопухолевого раствора проявляется периферической нейротоксичностью, нарушением функций органов кроветворения, а также эритематозно-язвенным воспалением слизистых оболочек ЖКТ, глотки и ротовой полости.
Специфический антидот цитостатика неизвестен. При возникновении осложнений проводят паллиативную терапию. Принудительный диализ не способствует выведению паклитаксела из системного кровотока и мягких тканей.
Побочные эффекты
Таксол вызывает нарушения в работе жизненно важных органов у всех категорий пациентов примерно с одной и той же частотой. При использовании рекомендованных доз противораковое средство переносится хорошо. В процессе исследований четкой взаимосвязи между нежелательными реакциями и возрастом пациентов не было обнаружено.
При длительном использовании паклитаксел может провоцировать следующие побочные действия:
- гипертермия;
- агранулоцитоз;
- тромбоцитопения;
- миелосупрессия;
- брадикардия;
- артериальная гипотензия;
- кардиомиопатия;
- периферическая нейропатия;
- септический шок;
- рецидивы инфекций;
- асимптоматическая тахикардия;
- миалгия и артралгия;
- воспаление кишечника.
При прохождении фармакотерапии не исключено повышение активности щелочной фосфатазы и трансминаз. Примерно у 4% пациентов диагностировали гипербилирубинемию на фоне нарушения функциональной активности паренхимы.
Противопоказания
Таксол не используется при повышенной чувствительности к полиэтоксилированному касторовому маслу или паклитакселу. Противоопухолевый медпрепарат не используется в педиатрии при лечении детей до 18 лет. Ограничения касаются женщин во время гестации и грудного вскармливания.
Категорически не рекомендуется вводить цитостатический раствор при низком содержании в крови тромбоцитов и нейтрофилов. Это может привести к нарушению свертываемости крови и резкому снижению резистентности организма.
Аналоги
Заменить антибластомный препарат можно лекарственными средствами, в которых содержится паклитаксел:
- Пакталек;
- Ютаксан;
- Митотакс;
- Интаксел;
- Паклитера;
- Синдаксел;
- Абитаксел.
Условия продажи и хранения
Таксола отпускается по предписанию онколога. Хранить раствор можно в темном месте при соблюдении температурного режима 15-30 градусов Цельсия. В случае хранения закрытого флакона в холодильнике неактивные компоненты могут выпадать в осадок, который быстро растворяется при комнатной температуре. Срок годности раствора составляет 24 месяца.
Цены на Таксол в Москве

Заберите заказ в в аптеке
WER (г. Москва)
Цена: от 1 726 руб.
Сертификаты и лицензии
Состав
В 1 концентрата паклитаксела 6 мг. Глицерилрицинолеат макрогола, азот, этанол, как вспомогательные вещества.
Форма выпуска
Концентрат 6 мг/мл во флаконах по 5 мл и 16,7 мл.
Фармакологическое действие
Противоопухолевое.
Фармакодинамика и фармакокинетика
Фармакодинамика
Противоопухолевый препарат, получаемый биосинтетическим путем из алкалоидов тисового дерева. Механизм действия обусловлен действием на микротрубочки — внутриклеточные структуры, стенка которых образована белком тубулином. По микротрубочкам происходит синтез органелл, и они поддерживают определенную форму клетки.
Паклитаксел, связываясь с белком тубулином, повышает его полимеризацию, а также стимулирует сборку микротрубочек и препятствуют их распаду. Чрезмерное образование не распадающихся микротрубочек приводит в итоге к нарушению формирования митотического веретена и подавлению клеточного цикла. Паклитаксел нарушает функцию клетки в определенных стадиях митоза и в интерфазе. Также он индуцирует неправильное расположение микротрубочек и вызывает образование из них звезд (астеров) при митозе. Отмечается дозозависимое подавление костного мозга. Обладает мутагенным и эмбриотоксически действием.
Фармакокинетика
При в/в введении концентрация в плазме уменьшается в связи с двухфазной кинетикой. Кумуляции паклитаксела при повторных курсах не отмечается. Связывается с белками на 89%. Метаболизируется в печени изоферментами CYP2C8 и CYP3A4. T1/2 вариабельно, от 13 до 52 часов. До 12,6 % дозы выделяется с мочой. Диализ не влияет на скорость выведения действующего вещества.
Показания к применению
Применение Таксола показано при:
- раке яичников (терапия 1-ой линии с цисплатином при распространенных метастазах или после лапаротомии и остаточной опухоли);
- раке молочной железы (терапия 1-ой линии при метастатическом раке, адъювантная терапия при метастазах в лимфоузлах после проведения лечения, терапия 2 линии, если заболевания прогрессирует после химиотерапии препаратами антрациклинового ряда);
- немелкоклеточном раке легкого (терапии 1 линии с цисплатином или монотерапия, если не планируется хирургическое лечение и лучевая терапия;
- саркоме Капоши (терапия 2 линии у СПИД больных).
Противопоказания
- повышенная чувствительность;
- нейтрофилов меньше 1500/мкл и 1000/мкл у больных СПИД-ом с саркомой Капоши;
- серьезные инфекции;
- беременность;
- грудное вскармливание.
С осторожностью назначают при тромбоцитопении, печеночной недостаточности, аритмии, перенесенном инфаркте миокарда, вирусных заболеваниях.
Побочные действия
Часто встречаемые побочные реакции:
- миелосупрессия, анемия, нейтропения, тромбоцитопения, лейкопения;
- кровотечения;
- тошнота, рвота, понос;
- кожная сыпь, ощущение «приливов»;
- периферическая нейропатия;
- алопеция;
- снижение АД, брадикардия;
- артралгия, миалгия;
- повышение уровня АСТ;
- слабость.
Редко встречаемые побочные реакции:
- фебрильная нейтропения и острый миелоидный лейкоз;
- ангионевротический отек, озноб, анафилактический шок (очень редко);
- двигательная невропатия;
- судороги, атаксия, энцефалопатия;
- кишечная непроходимость, колит, панкреатит, асцит, гепатонекроз;
- одышка, кашель, плевральный выпот;
- мерцание предсердий (очень редко);
- зуд, сыпь, шелушение кожи, синдром Стивенса-Джонсона, флебит.
Таксол, инструкция по применению (Способ и дозировка)
Препарат вводится инфузионно. Перед введением его разбавляют растворами натрия хлорида, декстрозы. Вводят обязательно через систему с фильтром.
Химиотерапия Таксолом при раке яичников
При терапии 1 линии доза препарата 175 мг/м2 (3 часовая инфузия). Через 3 недели введение цисплатина 75 мг/м2.
При терапии 2 линии применяется монотерапия препарата — доза 175 мг/м2 (3 часовая инфузия) раз в 3 недели.
При раке молочной железы
При терапии 1 линии (режим монотерапии) — 175 мг/м2 в виде (3 часовая инфузия) раз в 3 недели.
При комбинации с трастузумабом — 175 мг/м2 (3 часовая инфузия) раз в 3 недели. Лечение начинают на следующий день или в тот же день после первой дозы трастузумаба.
При комбинации с доксорубицином — 220 мг/м2 (3 часовая инфузия) раз в 3 недели, через сутки после введения первого препарата.
При терапии 2 линии, которая назначается при диссеминированном заболевании после безуспешной комбинированной химиотерапии — 175 мг/м2 (3 часовая инфузия) каждые 3 недели.
Перед каждым сеансом химиотерапии проводится премедикация из трех медикаментов.
Передозировка
Передозировка проявляется аплазией костного мозга, невропатиями, мукозитами. Специфический антидот неизвестен. Проводят симптоматическое лечение.
Взаимодействие
Выраженная миелосупрессия отмечается, если данный препарат вводят после цисплатина. Последний снижает клиренс паклитаксела на 33%.
При применении с доксорубицином повышается концентрация последнего в плазме. При длительном введении Таксола (в течение 24 ч), перед длительным введением доксорубицина (в течение 48 ч), отмечаются случаи стоматита и более выраженная нейтропения. При струйном введении сначала доксорубицина и трехчасовой инфузии паклитаксела не отмечалось изменений характера побочных эффектов.
Применение с циметидином, дексаметазоном, ранитидином не влияет на связывание действующего вещества с белками. Требуется осторожность при назначении индукторов изоферментов (рифампицин, фенобарбитал, невирапин, эфавиренз) или ингибиторов (флуоксетин, эритромицин, гемфиброзил).
Входящий в состав макрогола глицерилрицинолеат может вызывать экстракцию ди-2-этилгексил фталата из поливинилхлоридных контейнеров.
Условия продажи
По рецепту.
Условия хранения
Температура до 30°С.
Срок годности
2 года.
Аналоги
Совпадения по коду АТХ 4-го уровня:
Абитаксел, Интаксел, Паклитаксел-Тева, Паксен, Паклитера, Таксакад, Пакликал.
Отзывы о Таксоле
Появление противоопухолевых препаратов нового поколения, среди которых Таксол, Таксотер, Навельбин, Гемцитабин, повысило эффективность лечения. Данный препарат включают в первую линию химиотерапии рака яичников, применяется он в комбинации. Так, комбинация Таксол + Карбоплатин является самым эффективным режимом химиотерапии при диссеминированном раке яичников и ее считают «золотым стандартом» в лечении этого заболевания. Внутривенное введение этих препаратов назначается как режим постоперационной химиотерапии.
Комбинация Таксол + Цисплатин обладает выраженной нейротоксичностью, нефротоксичностью и ототоксичностью обусловленной цисплатином. Комбинация же с Карбоплатином — равная по лечебной эффективности, но отличается меньшей токсичностью. Комбинация Авастина с Таксолом, применяемая при метастатическом раке молочной железы, вдвое увеличивает выживаемость. Таксол + карбоплатин + этопозид являются 1-й линией в лечении рака легкого, а комбинация этой схемы с лучевой терапией может привести к полной ремиссии у 50-70% больных.
Выбор той или иной схемы лечения зависит от многих факторов и определяется спектром токсичности, состоянием больного и переносимости. Пациенты, перенесшие это лечение, делятся своими впечатлениями, советами и почти все отмечают наличие побочных реакций.
- «… Делали раз в неделю, при этом каждую неделю делают дозу меньше и токсический эффект меньше. И так все 12 недель. Переносится она легко».
- «… Очень хороший препарат, многим помогает. У моей подруги был этот препарат в первой линии. У нее уже 7 лет ремиссия».
- «… Таксол добивалась для первой линии, но не дали. Только сейчас капают паклитаксел. Переносимость терпимая».
- «… Маме делали в монорежиме. Волосы только поредели, а лимфоциты сильно снизились. Ну и была тошнота».
- «… Переносила легче, чем доксорубицин, так как тошноты не было».
- «… Онемение пальцев рук и ног во второй половине курса».
- «… К окончанию курса выпадали постепенно все волосы, ресницы и брови».
- «… Были приливы, бессонница и нервозность».
- «… После последнего курса ресницы и брови выпали совсем. Через 1,5 месяца брови полностью восстановились, а ресницы еще короткие».
- «… Прошло все хорошо. Лейкоциты упали через 2 недели, поэтому схему поменяли».
- «… Кровоточила слизистая носа, онемение подошвы ног».
- «… Ноги выворачивало, слабость, лежала пластом. Ногти страшно истончились, но не слезли».
Цена Таксола, где купить
Купить Таксол можно аптеках Москвы и Санкт-Петербурга. Стоимость одного флакона 30 мг, 5 мл составляет 1759-1855 руб., а флакон препарата 100 мг, 16, 7 мл можно приобрести за 3621-3690 руб.
- Интернет-аптеки РоссииРоссия
ЗдравСити
-
Бетаксолол-СОЛОфарм капли глазные 0,5% 5млООО «Гротекс»
-
Бетаксолол кап. глазные 0,5% фл. 5млООО Випс-Мед
-
Бетаксолол-ОПТИК капли глазные 0,5% флакон 5млЗАО «ЛЕККО»
Аптека Диалог
-
Бетаксолол (фл. 0,5% 5мл)ВИПС-Мед
-
Бетаксолол таблетки 20мг №30Московский эндокринный завод
-
Бетаксолол-Солофарм 0,5% глазные капли флакон-капельница 5млГротекс ООО
-
Бетаксолол Велфарм таб.п.пл.об.20мг №30Велфарм ООО
показать еще

