Изменение демографической структуры общества в последние десятилетия привело к увеличению в популяции доли женщин старшей возрастной группы. В настоящее время развитые страны мира стоят перед серьезной социальной и медицинской проблемой — инверсией возрастной «пирамиды», что связано с увеличением продолжительности жизни. Более трети своей жизни современная женщина проводит в состоянии дефицита женских половых гормонов. По данным ВОЗ с каждым годом возрастает число женщин, вступающих в период постменопаузы (к 2030 г. их количество достигнет 1,2 млрд человек). Менопауза, не являясь заболеванием, приводит к нарушению эндокринного равновесия в организме женщины, вызывая приливы, раздражительность, бессонницу, а в последующем — возможные урогенитальные расстройства, повышение риска развития остеопороза и сердечно-сосудистых заболеваний. Все эти данные свидетельствуют о необходимости разработки целого ряда медицинских и социальных мер по защите здоровья, сохранению работоспособности и достойного качества жизни женщин пери- и постменопаузального периода.
Новым этапом в развитии менопаузальной гормональной терапии (МГТ) стали данные о возможности эффективного использования особых групп препаратов как альтернативы традиционной эстрадиолсодержащей заместительной гормональной терапии (ЗГТ) [1]. Одним из таких препаратов является тиболон, относящийся к категории G3H — другие половые гормоны и препараты, применяющиеся для лечения менопаузальных нарушений. Тиболон — синтетический стероид, тканеселективный регулятор эстрогенной активности. В организме человека он метаболизируется в три изомера: 3 альфа-гидрокситиболон, 3 бета-гидрокситиболон и 4 дельта-метаболит, обладающие тканеселективным сродством к эстрогенным рецепторам. Гидроксиметаболиты циркулируют в плазме крови в связанном неактивном состоянии в виде сульфатированных форм. Попадая в ткани-мишени (кости, центральная нервная система, мочеполовые органы, сердечно-сосудистая система), метаболиты тиболона реактивируются под воздействием сульфатазы, что обеспечивает их эстрогеноподобный эффект. В молочной железе и эндометрии 4 дельта-изомер блокирует сульфатазу, препятствуя формированию активных метаболитов, способных взаимодействовать с эстрогенными рецепторами. Этот изомер обладает также гестагенными и слабыми андрогенными свойствами. В результате достигаются благоприятные эстрогенные эффекты в центральной нервной системе, костях и мочеполовом тракте при отсутствии нежелательных влияний в эндометрии и молочных железах.
Тиболон появился на фармацевтическом рынке с 1988 г. Зарегистрирован в 89 странах для лечения климактерического синдрома, в 45 странах — для профилактики остеопороза. В РФ зарегистрирован препарат Ледибон — тиболон 2,5 мг, который применяется один раз в сутки, желательно в одно и то же время. Показания к применению: лечение симптомов эстрогенной недостаточности у женщин спустя 1 год после последней естественной менструации; профилактика остеопороза у женщин в постменопаузе, имеющих высокий риск возникновения переломов, и при непереносимости других препаратов, применяемых для профилактики остеопороза. Начало лечения: естественная менопауза — лечение можно начать через 12 месяцев после последней естественной менструации; хирургическая менопауза — лечение начинают немедленно. Пропуск приема таблетки: менее 12 часов — принять немедленно; более 12 часов — пропустить прием таблетки, следующую таблетку принять в обычное время. Общая переносимость: Ледибон хорошо переносится, нет существенного влияния на массу тела.
В рандомизированных плацебо-контролируемых исследованиях было показано, что тиболон позволяет контролировать приливы жара, потливость и другие типичные симптомы, такие как бессонница, головная боль и утомляемость. В плане облегчения климактерических симптомов он оказался настолько же эффективным, как и многочисленные схемы эстроген-прогестагенной комбинированной и только эстрогенной терапии (ЭПТ/ЭТ) [8–10], хотя, возможно, он и характеризуется несколько более медленным началом действия, но может также использоваться в качестве «терапии прикрытия» для облегчения симптомов дефицита эстрогенов у женщин, получающих лечение агонистами гонадотропин-рилизинг-гормона (аГнРГ) по поводу миомы матки и эндометриоза [11, 12].
Показано, что тиболон способствует обратному развитию атрофии влагалища (увеличивает кариопикнотический индекс и индекс созревания клеток) и улучшает качество цервикальной слизи [13]. Женщины, получающие лечение тиболоном, отмечают значительное уменьшение сухости во влагалище, выраженности диспареунии и мочевых симптомов.
Эффекты тиболона в отношении циркулирующих андрогенов отличаются от действия стандартных пероральных схем МГТ (ЭПТ/ЭТ). При использовании тиболона уровень глобулина, связывающего половые стероиды (ГСПС), снижается, а не увеличивается, в связи с этим концентрация свободного тестостерона повышается, в то время как при стандартной МГТ (ЭПТ/ЭТ) наблюдается ее снижение. Показано, что увеличивается также концентрация дегидроэпиандростеронсульфата (ДЭАС) [14]. Кроме этого, 4 дельта-изомер тиболона также оказывает некоторое андрогенное действие. Эти свойства тиболона способствуют его благоприятному влиянию на сексуальное благополучие, которое заключается в повышении сексуального влечения, возбуждения, стимуляции сексуальных фантазий и повышении увлажненности влагалища [15–17]. В сравнении со стандартными схемами ЭПТ, тиболон в значительно большей степени способствует увеличению частоты коитусов, повышает степень наслаждения и удовлетворенности половым актом [18]. Что касается частоты оргазма и сексуальной чувствительности, то при применении тиболона или комбинации эстрогенов и андрогенов наблюдается более выраженный эффект, нежели при использовании ЭТ или в контрольной группе [19].
Предполагается, что существенное благоприятное воздействие тиболона на уровень настроения обусловлен нормализацией уровня эндорфинов и его андрогенными свойствами [15, 20]. В сравнительном исследовании с использованием ЭПТ тиболон оказался более эффективным в плане уменьшения выраженности расстройств настроения [21]. Кроме того, его эффект может осуществляться синергистически с эффектами психоактивных препаратов, что сопровождается более быстрым достижением улучшения у женщин, страдающих депрессией и психозами. Поскольку применение антидепрессантов часто ассоциируется с сексуальной дисфункцией, влияние тиболона на сексуальность у таких женщин сопровождается дополнительными преимуществами.
В рандомизированных контролируемых исследованиях показано, что тиболон вызывает увеличение минеральной плотности костной ткани (МПК) и предотвращает потерю костного вещества [23, 24]. Благоприятные эффекты тиболона наблюдались как в шейке бедра, так и в позвоночнике. Эти благоприятные эффекты отмечались при длительном (10-летнем) лечении [25] как в ранней, так и в поздней постменопаузе у женщин с установленным диагнозом остеопороза и у женщин, получавших лечение агонистами ГнРГ [11, 12, 26–28].
Терапия тиболоном значительно реже вызывает болезненность молочных желез и масталгию, нежели ЭПТ; эта причина гораздо реже, чем в случае ЭПТ, приводит к прекращению лечения тиболоном [8, 9, 23, 29]. Женщины с болезненностью молочных желез или масталгией на фоне ЭПТ, по-видимому, могут воспользоваться благоприятным эффектом при переходе на тиболон [30].
Тиболон не вызывает увеличения плотности ткани на маммограмме [29, 31]. Самопроизвольно возникшая повышенная рентгенографическая плотность молочных желез рассматривается как независимый фактор риска рака молочной железы. В настоящее время неясно, является ли индуцированная ЭПТ плотность молочных желез суррогатным маркером повышенного риска рака молочной железы, однако повышенная маммографическая плотность может маскировать опухоли молочных желез при скрининговой маммографии, что приводит к поздней диагностике [32]. Кроме того, повышенная маммографическая плотность приводит к увеличению частоты повторных вызовов пациенток, что вызывает страх женщин [33, 34]. Действие тиболона на молочные железы отличается от эффектов ЭПТ. В отличие от ЭПТ, тиболон не повышает риск пролиферации ткани молочной железы, но стимулирует апоптоз [31, 35]. Согласно объединенным данным всех исследований тиболона III/IV фазы, тиболон не вызывал увеличения риска рака молочной железы, в сравнении с плацебо (относительный риск (ОР) 0,50; 95% доверительный интервал 0,11–2,54) [36]. Исследование «Миллион женщин» (MWS) сообщает о повышении ОР рака молочной железы на фоне лечения тиболоном (ОР 1,45; 95% доверительный интервал 1,25–1,67), хотя это увеличение и достоверно (p < 0,0001) меньше, чем на фоне ЭПТ [5]. В другом эпидемиологическом исследовании, где использовалась база данных исследований общей практики Великобритании (GPRD), не обнаружено повышения риска при использовании тиболона (ОР 1,02; 95% доверительный интервал 0,78–1,33) [37]. Однако данные этого исследования были опубликованы только в виде тезисов, а не в виде полнотекстовой статьи.
Хотя лучшие доказательства влияния тиболона на развитие рака молочной железы, имеющиеся в настоящее время, получены от MWS, риски, описанные в этом обсервационном исследовании, вероятно, переоценены [3, 4]. Данные проведенных проспективных исследований [2, 33] свидетельствуют о том, что абсолютное увеличение риска рака молочной железы ниже, чем описано в исследовании MWS, и что риск применения тиболона и ЭТ, вероятно, ниже, чем риск использования ЭПТ.
В итоге: для кого Ледибон?
Пациентки в постменопаузе, имеющие вазомоторные симптомы, у которых Ледибон может иметь особое значение:
- женщины с низким уровнем сексуального влечения или так называемой женской сексуальной дисфункцией;
- женщины с расстройствами настроения и женщины, получающие психоактивные препараты;
- женщины с риском ускоренной потери костной ткани;
- женщины с менопаузальной масталгией;
- женщины с повышенной рентгенологической плотностью молочных желез;
- женщины с миомой матки;
- женщины с урогенитальными жалобами.
Пациентки, у которых может оказаться благоприятным переход с ЭПТ/ЭТ на Ледибон:
- женщины, у которых имеет место усиление боли в молочных железах;
- женщины, у которых наблюдается увеличение плотности молочных желез, что приводит к частым ложным вызовам на осмотр или получению нечитаемых маммограмм;
- женщины с низким сексуальным влечением;
- женщины с колебаниями настроения;
- женщины с кровотечениями (при условии отсутствия гистопатологических причин для кровотечения).
Пациентки без климактерических симптомов, которых следует иметь в виду (некоторые постменопаузальные женщины без климактерических симптомов или со слабо выраженной симптоматикой могут получить преимущество от лечения Ледибоном):
- женщины с низким сексуальным влечением;
- женщины с колебаниями настроения;
- женщины с остеопенией.
Литература
- Smith C. L., O’Malley B. W. Coregulator function: a key to understanding tissue specificity of selective receptor modulators // Endocr Rev. 2004; 25: 45–71.
- Anderson G. L., Limacher M., Assaf A. R. et al. Effects of conjugated equine estrogen in postmenopausalwomen with hysterectomy: the Women’s Health Initiative randomized controlled trial // J Am Med Assoc. 2004; 291: 1701–1712.
- Shapiro S. The Million Women Study: potential biases do not allowuncritical acceptance of the data // Climacteric. 2004; 7: 3–7.1
- Whitehead M., Farmer R. The MillionWomen Study: a critique // Endocrine. 2004; 24: 187–194.
- Million Women Study Collaborators. Breast cancer and hormone replacement therapy in the MillionWomen Study // Lancet. 2003; 362: 419–427.
- EMAS Revised Statement // Maturitas. 2005; 51: 8–14.
- IMS Revised Position Paper // Climacteric. 2004; 7: 333–337.
- Hammar M., Christau S., Nathorst-B¨o¨os J., Rud T., Garre K. A double-blind randomised trial comparing the effects of tibolone and continuous combined hormone replacement therapy in postmenopausal women with menopausal symptoms // Br J Obstet Gynaecol. 1998; 105: 904–911.
- Huber J., Palacios S., Berglund L. et al. The effect of tibolone compared with conjugated equine oestrogens continuously combined with medroxyprogesterone acetate on bleeding rates, quality of life and tolerability in postmenopausal women // Br J Obstet Gynaecol. 2002; 109: 886–893.
- Baracat E. C., Barbosa I. C., Giordano M. G. et al. A randomized, open-label study of conjugated equine estrogens plus medroxyprogesterone acetate versus tibolone: effects on symptom control, bleeding pattern, lipid profile and tolerability // Climacteric. 2002; 5: 60–69.
- Lindsay P. C., Shaw R. W., Coelingh Bennink H. J., Kovic P. The effect of add back treatment with tibolone (Livial®) on patients treated with the gonadotrophin-releasing hormone agonist triptorelin (Decapeptyl) // Fertil Steril. 1996; 65: 342–348.
- Palomba S., Affinito P., Di Carlo C., Bifulco G., Nappi C. Longterm administration of tibolone plus gonadotrophin-releasing hormone agonist for the treatment of uterine leiomyomas: effectiveness and effects on vasomotor symptoms, bone mass and lipid profile // Fertil Steril. 1999; 72: 889–895.
- Morris E. P., Wilson P. O. G., Robinson J., Rymer J. M. Long-term effects of tibolone on the genital tract in postmenopausal women // Br J Obstet Gynaecol. 1999; 106: 954–959.
- Doren M., Rubig A., Coelingh Bennink H. J., Holzgreve W. Differential effects on the androgen status of postmenopausal women treated with tibolone and continuous combined estradiol and norethindrone acetate replacement therapy // Fertil Steril. 2001; 75: 554–559.
- Davis S. R. The effects of tibolone on mood and libido // Menopause. 2002; 9: 162–170.
- Palacios S., Menendez C., Jurado R., Castano J. C., Vargas J. C. Changes in sex behaviour after menopause: effects of tibolone // Maturitas. 1995; 22: 155–161.
- Laan E., van Lunsen R. H. W., Everaerd W. The effects of tibolone on vaginal blood flow, sexual desire and arousability in postmenopausal women // Climacteric. 2001; 4: 28–41.
- Nathorst-Boos J., Hammar M. Effect on sexual life–a comparison between tibolone and a continuous estradiol-norethisterone acetate regimen // Maturitas. 1997; 26: 15–20.
- Castelo-Branco C., Vicente J., Figueras F. et al. Comparative effects of estrogens plus androgens and tibolone on bone, lipid pattern and sexuality in postmenopausal women // Maturitas. 2000; 34: 161–168.
- Genazzani A. R., Petraglia F., Facchinetti F. et al. Effects of Org OD 14 on pituitary and peripheral-endorphin in castrated rats and in postmenopausalwomen // Maturitas. 1987; 1: 35–48.
- Egarter Ch., Huber J., Leikermoser R. et al. Tibolone versus conjugated estrogens and sequential progestogen in the treatment of climacteric complaints // Maturitas. 1996; 23: 55–62.
- Meeuwsen I. B., Samson M. M., Duursma S. A., Verhaar H. J. The influence of tibolone on quality of life in postmenopausal women // Maturitas. 2002; 41: 35–43.
- Roux C., Pelissier C., Fechtenbaum J., Loiseau-Peres S., Benhamou C. L. Randomized, double-blind, 2-year comparison of tibolone with 17-estradiol and norethindrone acetate in preventing postmenopausal bone loss // Osteoporosis Int. 2002; 13: 241–248.
- Lippuner K., Haenggi W., Birkhauser M. H., Casez J.-P., Jaeger P. Prevention of postmenopausal bone loss using tibolone or conventional peroral or transdermal hormone replacement therapy with 17-oestradiol and dydrogesterone // J Bone Min Res. 1997; 12: 806–812.
- Rymer J., Robinson J., Fogelman I. Ten years of treatment with tibolone 2.5 mg daily: effects on bone loss in postmenopausal women // Climacteric. 2002; 5: 390–398.
- Berning B., Kuijk C. V., Kuiper J. W., Coelingh Bennink H. J. T., Kicovic P. M., Fauser B. C. J. M. Effects of two doses of tibolone on trabecular and cortical bone loss in early postmenopausal women: a two-year randomized, placebo-controlled study // Bone. 1996; 19: 395–399.
- Bjarnason N. H., Bjarnason K., Haarbo J., Rosenquist C., Christiansen C. Tibolone: prevention of bone loss in late postmenopausal women // J Clin Endocrinol Metab. 1996; 81: 2419–2422.
- Pavlov P. W., Ginsburg J., Kicovic P. M., van der Schaaf D. B., Prelevic G., Coelingh Bennink H. J. T. Double-blind, placebo controlled study of the effects of tibolone on bone mineral density in postmenopausal osteoporotic women with and without previous fractures // Gynecol Endocrinol. 1999; 13: 230–237.
- Lundstrom E., Christow A., Svane G. et al. Effects of tibolone and a continuous combined HRT regimen on mammographic breast density // Am J Obstet Gynecol. 2002; 186: 717–722.
- Palomba S., Di Carlo C., Morelli M. et al. Effect of tibolone on breast symptoms resulting from postmenopausal hormone replacement therapy // Maturitas. 2003; 45: 267–273.
- Valdivia I., Campodonico I., Tapia A. et al. Effects of tibolone and continuous combined hormone therapy on mammographic breast density and breast histochemical markers in postmenopausal women // Fertil Steril. 2004; 81: 617–623.
- Thurfjell E. Breast density and the risk of breast cancer // N Engl J Med. 2002; 347: 866.
- Chlebowski R. T., Hendrix S. L., Langer R. D. et al. Influence of estrogen plus progestin on breast cancer and mammography in healthy postmenopausal women: theWomen’s Health Initiative Randomized Trial // J Am Med Assoc. 2003; 289: 3243–3253.
- Banks E., Reeves G., Beral V. et al. Impact of use of hormone replacement therapy on false positive recall in the NHS breast screening programme: results from the Million Women Study // Br Med J. 2004; 328: 1291–1292.
- Conner P., ChristowA., Kersemaekerc W. Acomparative study of breast cell proliferation during hormone replacement therapy: effect of tibolone and continuous combined estrogen progestogen therapy // Climacteric. 2004; 7: 50–58.
- Helmond F. A., Kloosterboer H. J. Safety and tolerability profile of Livial. In: Genazzani AR, editor. Hormone replacement therapy and cancer. The current status of research and practice. Boca Raton: The Parthenon Publishing Group; 2002. P. 252–256.
- Allen D. S., de Vries C. S., Farmer R. D. T. Pharmaceutical content and regimen of hormone replacement therapy and risk of breast cancer // Pharmacoepidemiol Drug Saf. 2002; 11 (Suppl 1): 296.
А. Л. Тихомиров1, доктор медицинских наук, профессор
И. Б. Манухин, доктор медицинских наук, профессор
Е. И. Манухина, доктор медицинских наук, профессор
В. В. Казенашев, кандидат медицинских наук
ГБОУ ВПО МГМСУ им. А. И. Евдокимова МЗ РФ, Москва
1 Контактная информация: pacificoff@mail.ru
Тиболон: назад в будущее
Статьи
Опубликовано в журнале:
« Климактерий » №2, 2015г. Сметник В.П.
Список сокращений:
17β-HSD – 17-бета-гидроксистероиддегидрогеназы
AUC – площадь под фармакокинетической кривой
Е2 – эстрадиол
NETA – норэтистерона ацетат
CEE – конъюгированный лошадиный эстроген
MPA – медроксипрогестерона ацетат
АГ – артериальная гипертензия
ИМ – инфаркт миокарда
ЛПВП – липопротеиды высокой плотности
МГТ – менопаузальная гормональная терапия
МЖ – молочные железы
МПК – минеральная плотность костной ткани
ОХС – общий холестерин
РКИ – рандомизированное клиническое исследование
СД – сахарный диабет
ЭПТ – эстроген-прогестагенная терапия
ЭТ – эстрогенная терапия
В истории создания и клинического применения тиболона* можно выделить три важных исторических периода.
I период (1964–1989 гг.).
Синтез и уточнение свойств тиболона
Первое успешное клиническое исследование показало удивительные тканеселективные свойства тиболона: профилактика остеопороза и лечение симптомов климактерического синдрома без стимуляции эндометрия. Первоначально в 1964 г. тиболон был создан как производное 19-нортестостерона. В 1988 г. был выделен кристаллический тиболон [1]. В последующем введение 17-альфа-метильной группы дали этому веществу больше эстрогенных свойств, чем прогестагенных [1].
С помощью классических биологических методов оценки препарата фармакологи показали, что это вещество может демонстрировать активность 3 половых стероидных гормонов. Метаболиты тиболона (рис. 1) представлены двумя 3-гидроксиметаболитами, обладающими эстрогенными свойствами и связывающимися с эстрогенными рецепторами. Третий метаболит – дельта-4-изомер тиболона связывается с прогестагенными и андрогенными рецепторами [2].
* Коммерческое название тиболона — ливиал.
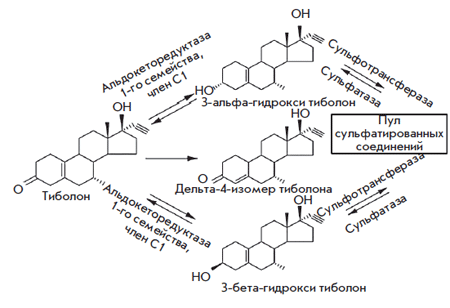
Рис. 1. Структура тиболона и его метаболитов
II период (1990–1999 гг.)
Проведены фундаментальные исследования о влиянии тиболона на молочные железы и эндометрий. Установлен локальный метаболизм тиболона в эндометрии. Показано, что прогестагенная активность тиболона и его дельта-4-изомера была подобна натуральному прогестерону. Однако сродство рецепторов прогестерона с тиболоном в эндометрии было очень низким.
Впервые было показано, что тиболон и его метаболиты локально метаболизируются в ткани эндометрия. При этом доминирует дельта-4-изомер, обладающий прогестагенной и андрогенной активностью. Кроме того, дельта-4-изомер стимулирует сульфотрансферазу и ингибирует сульфатазу (рис. 2).
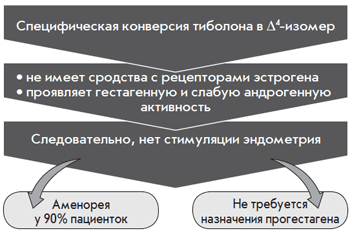
Рис. 2. Тканеселективное действие тиболона в эндометрии
Этим объясняется доминирование атрофических изменений в эндометрии [5]. Что касается молочных желез, то Pasqua-lini J.R. и соавт. убедительно показали, что тиболон и его метаболиты являются очень активными ингибиторами сульфатазы (рис. 3) [6].
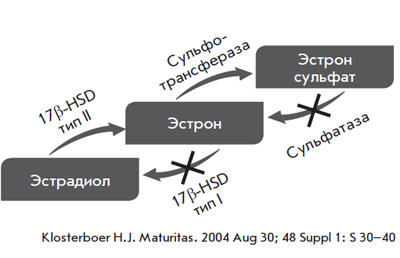
Рис. 3. Метаболизм эстрогенов в молочной железе при приеме тиболона
Установлено, что тиболон и его метаболиты оказывают антипролиферативное влияние на молочные железы и не повышают маммографическую плотность [7] в отличие от E2, Е2/ NETA и CEE/MPA, повышающих маммографическую плотность [8].
Проведено сравнительное клиническое исследование тиболона с эстроген-прогестагенной МГТ. Оба препарата оказывали подобное влияние на вазомоторные симптомы, но тиболон лучше влиял на настроение и кровянистые выделения. В этот же период начаты новые клинические исследования. Были проведены первые двойные-слепые плацебо-контролируемые исследования [3,4], которые позволили прийти к следующим заключениям:
- 2,5 мг тиболона ингибирует овуляцию у фертильных женщин и тормозит выделение гонадотропинов у постменопаузальных женщин;
- у постменопаузальных женщин тиболон не оказывает стимулирующего влияния на эндометрий, через 2 года лечения не было случаев гиперплазии эндометрия;
- тиболон оказывает избирательное воздействие на плотность костной ткани и ослабляет вазомоторные симптомы.
В РКИ сравнительное изучение эффективности тиболона и Е2 2 мг/NETA 1 мг через 1, 3, 6 и 12 мес. у 100 женщин показало, что на фоне тиболона количество кровянистых выделений снизилось значительнее, чем на фоне Е2/NETA, и не было отмечено утолщения эндометрия. На фоне тиболона повышался уровень свободного тестостерона, что не отмечено в группе Е2/NETA. Улучшение настроения и повышение сексуальности объяснялось повышением уровня свободного тестостерона [9].
III период (с 2000 г. по настоящее время)
Результаты многочисленных больших РКИ показали дозозависимое влияние тиболона на симптомы климактерического синдрома, на кости, молочные железы и ЦНС. Тканеспецифический эффект тиболона позволяет представить тиболон как тканеселективный регулятор эстрогенной активности (STEAR) [10–12].
Влияние тиболона и его метаболитов на молочные железы опосредовано уменьшением воздействия на них эстрадиола вследствие блокады ферментов, участвующих в его синтезе при одновременной активации ферментов, способствующих образованию неактивных форм эстрадиола. Тиболон также стимулирует активность сульфотрансферазы, что способствует перерождению активных эстрогенов в неактивные, может блокировать сульфотазу и 17β-HSD-I, участвующих в синтезе активных форм эстрогенов.
В исследовании Nijland E.A. и соавт. была представлена сравнительная частота кровянистых выделений и масталгий при использовании тиболона 2,5 мг и Е2/NETA у постменопаузальных женщин с сексуальной дисфункцией. В исследовании приняли участие 403 женщины (средний возраст 56 лет). Вагинальные кровянистые выделения были отмечены у 11% женщин, принимавших Е2/ NETA, в отличие от тиболона, на фоне которого кровянистых выделений не было. Симптомы нагрубания молочных желез чаще обнаруживались в группе E2/NETA, чем на фоне тиболона (11% vs 4%). Все пациентки, принимавшие тиболон, закончили исследование, в то время как в группе Е2/NETA лечение было отменено у 8% женщин. На фоне тиболона было отмечено также более значительное улучшение сексуальной функции [12].
Данные 7 больших РКИ, посвященных изучению тиболона, были опубликованы после публикации консенсуса, предложившего рекомендации по применению тиболона в качестве постменопаузальной терапии в 2005 г. [13]. Эти исследования подтвердили, что тиболон является значительно более эффективным, чем плацебо [14] и таким же эффективным, как низкие дозы непрерывной терапии E2/NETA в отношении уменьшения выраженности вазомоторных симптомов.
Тиболон более выраженно улучшал сексуальное влечение по сравнению с E2/NETA и показал тенденцию к более значительному улучшению сексуальной функции [15]. Случаи влагалищных кровотечений и чувствительности/болезненности молочных желез встречались значительно реже на фоне приема тиболона, чем на фоне терапии E2/NETA или CEE/ MPA. Данные исследования конечных точек, включавших гистологию эндометрия и молочных желез на фоне терапии тиболоном в течение 2 лет в дозах 1,25 и 2,5 мг/сут без случаев гиперплазии эндометрия или рака в группе любой дозы [16]. Общее количество постменопаузальных пациенток составило 3240 (средний возраст – 54,4 года),в первой группе принимали тиболон (1,25 и 2,5 мг/сут), а во второй группе – CEE/MPA (0,625 и 2,5 мг/сут). После обработки данных авторы пришли к следующим выводам:
- тиболон не стимулирует эндометрий;
- не требует дополнительного приема гестагенов;
- частота аменореи высокая;
- частота кровянистых выделений из половых путей на фоне тиболона ниже, чем на фоне эстроген-прогестагенной терапии;
- стандартный контроль за состоянием эндометрия не требуется.
В исследовании LIFT, посвященном изучению остеопороза, приняли участие 4538 женщин, средний возраст 68 лет (60–80 лет), пост менопауза > 15 лет; участники принимали 2 дозы тиболона (1,25 и 2,5 мг/сут). В обеих дозах тиболон увеличивал минеральную плотность поясничных и тазовых костей в значительно большей степени, чем плацебо у женщин с остеопорозом или без него, как и доза 1,25 мг/сут по сравнению с ралоксифе-ном в исследовании среди пожилых женщин с остео пенией (средний возраст 66 лет). Более низкая доза тиболона также снижала риск вертебральных и невертебральных переломов у пожилых женщин с остеопорозом (средний возраст 68,3 года) [17].
Повышенный риск инсульта, который еще более увеличивается с возрастом, наблюдался на фоне лечения тиболоном по сравнению с плацебо в исследовании LIFT [17]. Однако различия в абсолютном риске между группами лечения не были статистически значимыми, исследуемую популяцию составляли пациенты пожилого возраста (60–85 лет), и не наблюдалось никакого увеличения риска венозной тромбоэмболии. По сравнению с вышеуказанным исследованием риск развития инсульта не наблюдался в исследовании THEBES (средний возраст 54,4 года) и в исследовании Renoux C. и соавт. (средний возраст 70,3 года) [18], хотя число женщин, получавших тиболон, в последнем исследовании было небольшим. Исследователи, проводившие исследование LIFT, пришли к выводу, что тиболон не следует использовать женщинам пожилого возраста (>60 лет) или пациенткам, имеющим серьезные факторы риска развития инсульта, такие как АГ, курение, СД и фибрилляция предсердий [17].
В исследовании LIFT тиболон по сравнению с плацебо уменьшал риск развития РМЖ у женщин пожилого возраста, не имевших РМЖ в анамнезе [17].
Клиническое исследование LIBERATE было проведено с целью определения возможности назначения тиболона женщинам с РМЖ в анамнезе для облегчения симптомов менопаузы без увеличения риска их рецидива. Однако в данном исследовании был показан значительно более высокий риск рецидива РМЖ в группе тиболона по сравнению с группой плацебо, несмотря на тот факт, что большинство пациентов в исследуемой популяции получали адъювантную системную терапию. При включении в исследование пациентов из исследуемых популяций 66% получали тамоксифен, а 6% – ингибиторы ароматазы. Применение ингибиторов ароматазы увеличилось в ходе клинического исследования, и на момент завершения исследования около 80% получали адъювантную эндокринную терапию [14]. Анализы подгрупп позволили предположить, что негативное влияние тиболона у пациентов, получавших ингибиторы ароматазы, было более тяжелым, чем у пациентов, получавших тамоксифен, когда активация эстрогенных рецепторов эстрогенными метаболитами тиболона предотвращается за счет молекул гидрокси-тамоксифена с высоким сродством.
Исследователи пришли к выводу, что расхождения между этими данными и результатами исследования LIFT возникли потому, что обе исследуемые популяции различались во многих отношениях, включая гормональные факторы риска развития РМЖ, и потому что влияние тиболона на здоровые ткани МЖ, весьма вероятно, отличается от влияния на раковые клетки, так как тиболон может оказывать эстрогенное влияние на скрытые, «дремлющие» метастазы РМЖ. Согласно данным клинического исследования LIBERATE, тиболон противопоказан женщинам с установленным и предполагаемым РМЖ или при наличии РМЖ в анамнезе.
Исследование OPAL было посвящено изучению влияния тиболона на профилактику остеопороза и атеросклероза сонных артерий. Участники данного исследования были рандомизированы для получения тиболона, CEE/MPAи плацебо. Тиболон снижал уровень ОХС и ЛПВП в большей степени, чем плацебо, в то время как CEE/MPA увеличивал уровень ЛПВП [19]. Среднее увеличение толщины комплекса интима-медиа сонной артерии (ТКИМС), которое связано с риском развития ССЗ, было аналогичным при лечении тиболоном и CEE/MPA и более выраженным по сравнению с плацебо. Тем не менее, наблюдались несоответствия в данных по ТКИМС между европейской и американской когортами в этом исследовании [20]. Был сделан вывод о том, что ни один из препаратов не показал отрицательного или положительного влияния на развитие атеросклероза [19, 20]. В 5-летнем национальном когортном исследовании в Дании не было выявлено увеличения риска развития ИМ на фоне лечения тиболоном [21].
Согласно данным Я.З. Зайдиевой [25], прием тиболона способствует уменьшению толщины эндометрия. Показатели толщины маточного «эха» на фоне лечения тиболоном в течение 1 года снизились c 0,34 см (0,1–0,5) до 0,2 см (0,1–0,3). По данным гистологического исследования эндометрия установлено, что частота атрофии увеличилась с 72% (фон) до 91%, определение нефункционирующего эндометрия увеличилось с 15 до 3%. Случаев пролиферации и гиперплазии эндометрия выявлено не было.
С учетом клинических исследований азиатских женщин было опубликовано «Согласованное заявление по применению тиболона» в «Обновленных рекомендациях по применению тиболона у жительниц азиатских стран» (табл. 1).
Таблица 1
Согласованное заявление по применению тиболона и уровни подтверждающих доказательств [22]
| Обновленные заявления и/или новые доказательства, опубликованные, начиная с 2005 г. | Уровень доказательств |
|---|---|
| Тиболон является столь же эффективным, как и используемые в настоящее время режимы ЭПТ/ЭТ для лечения климактерических симптомов [23] | IB |
| Тиболон уменьшает местные вагинальные симптомы и лечит атрофию слизистой влагалища [23] | IB |
| Тиболон оказывает положительное влияние на сексуальное благополучие и является более эффективным, чем пероральная ЭПТ/ЭТ в некоторых отношениях, а именно: возбуждение, желание и удовлетворение [15, 23] | IB |
| Тиболон оказывает положительное влияние на настроение и качество жизни [15, 23] | IB |
| Тиболон предотвращает потерю костной массы и является настолько же эффективным, как и стандартные дозы ЭПТ/ЭТ, и более эффективным, чем ралоксифен [24] | IB |
| Тиболон снижает риск вертебральных и невертебральных переломов у пожилых женщин с остеопенией. Абсолютное снижение было более выражено у женщин, у которых в анамнезе уже отмечался вертебральный перелом, по сравнению с теми, у кого анамнез был не отягощен [17] | IB |
| Тиболон не оказывает стимулирующего влияния на эндометрий и не вызывает гиперплазию эндометрия или рак у женщин постменопаузального возраста в рандомизированных контролируемых клинических исследованиях и обладает более низкой частотой встречаемости кровотечений [12, 16, 23] | IB |
| Тиболон реже вызывал чувствительность МЖ или масталгию, чем ЭПТ [23] | IB |
| Тиболон не увеличивает маммографическую плотность | 2B |
| Тиболон, принимаемый женщинами с РМЖ в анамнезе, связан с повышением риска рецидивов РМЖ [14] | 1B |
| Тиболон в дозе 1,25 мг не увеличивал риск развития РМЖ у пожилых женщин с остеопорозом, не имевших РМЖ в анамнезе [16] | 1B |
| До сих пор не получено убедительных данных по конечным точкам относительно влияния тиболона на состояние ССС [17] | 1B |
| Тиболон оказывает влияние на липидный профиль, отличное от ЭПТ/ЭТ [19] | 1B |
| Тиболон увеличивает ТКИМС аналогично ЭПТ [19] | 1B |
| В одном рандомизированном контролируемом исследовании применение тиболона в дозе 1,25 мг у женщин пожилого возраста было связано с повышенным риском инсульта [17]. Следовательно, тиболон следует использовать с осторожностью пожилым женщинам (т. е. старше 60 лет) и не следует использовать пациентам, имеющим серьезные факторы риска инсульта | 1B |
| Тиболон не повышал риск развития инсульта, ВТЭ или ИМ в обсервационных исследованиях [18, 21] | 2B |
| * Определение уровня доказательств: 1B — отдельные рандомизированные клинические исследования; 2B -отдельные когортные исследования; ЭПТ — эстроген-прогестагенная терапия; ЭТ — эстрогенная терапия; ТКИМС — толщина комплекса интима-медиа сонной артерии; ВТЭ — венозная тромбоэмболия |
Болдыревой Н.В. было установлено положительное влияние тиболона на увеличение МПК в поясничном отделе позвоночника (рис. 4) и в шейке бедра (рис. 5) [26]. В проведенном нами исследовании изучалось влияние тиболона на молочные железы, препарат принимался в течение 1 года. По данным исследования отмечалось положительное влияние тиболона на фиброзно-кистозную болезнь (рис. 6) [27].
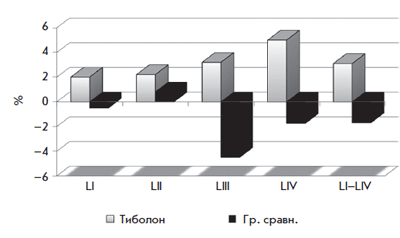
Рис. 4. Динамика МПК в поясничных позвонках на фоне тиболона
в течение 1 года у женщин в постменопаузе
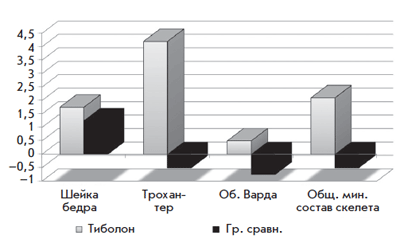
Рис. 5. Динамика МПК в проксимальном отделе бедра на фоне тиболона
в течение 1 года у женщин в постменопаузе
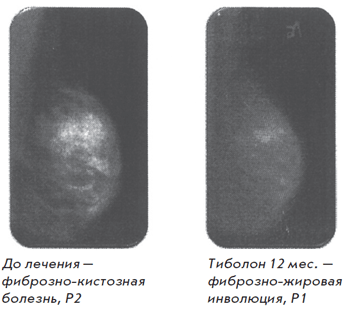
Рис. 6. Пациентка Г. И. П., 41 год
Известно, что на фоне МГТ могут наблюдаться мастодиния/масталгия и повышение маммографической плотности у 20–30% женщин, которые после 3 мес. приема уменьшаются или исчезают. Однако у части женщин на фоне длительной МГТ сохранялась масталгия/мастодиния, что может рассматриваться как своеобразный клинический маркер нарастания доброкачественных диффузных изменений молочных желез.
Наш собственный опыт перехода с эстрогенгестагенной МГТ на тиболон у подобных пациентов позволял добиться существенной положительной динамики в состоянии молочных желез. По данным маммографии отмечено нарастание инволюции, переход фиброзно-кистозной мастопатии в фиброзно-жировую инволюцию и уменьшение объема железистой ткани у 89% пациенток, что клинически сопровождалось значительным уменьшением субъективных ощущений [28].
Особенно выраженный положительный эффект отмечен у женщин после оварэктомии и со сниженным либидо (рис. 7).
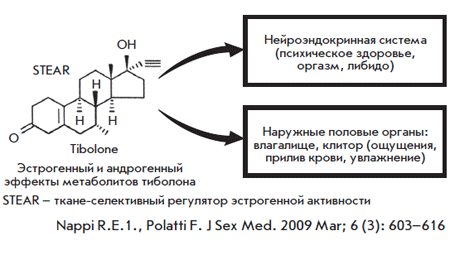
Рис. 7. Влияние Тиболона на сексуальную функцию женщин в постменопаузе
Таким образом, имеющиеся клинические данные указывают на то, что женщины могут получить положительный эффект от перехода с МГТ на тиболон, если на фоне МГТ отмечались следующие симптомы:
1) усиление боли в молочных железах, несмотря на коррекцию дозы МГТ;
2) повышение плотности молочных желез, что привело к нечитабельности маммограмм;
3) низкое половое влечение;
4) расстройство настроения;
5) постоянные кровотечения (без каких-либо существующих гистопатологических причин).
В последние годы в России зарегистрирован дженерик оригинального препарата тиболона – ледибон (2,5 мг, Zentiva, Чехия). Препарат прошел полный цикл доклинических и клинических исследований. Патент и эксклюзивные права находились под защитой в течение 20 лет.
Препарат-дженерик – это лекарственный препарат, срок действия патентной защиты на который уже закончился, и он не является исключительной собственностью фармацевтической компании, которая его разработала или владела первой лицензией на его продажу. Копии – лекарственные препараты, которые представлены на рынках стран со слабой или отсутствующей патентной защитой химических молекул, а отсюда – активных ингредиентов лекарственных средств [29].
Дженерик содержит то же активное лекарственное вещество (активную субстанцию), что и оригинальный (патентованный) препарат, но отличается от него вспомогательными веществами (неактивными ингредиентами, наполнителями, консервантами, красителями и др.). Чтобы доказать, что дженерик такой же, как оригинальный препарат, необходимо доказать его эквивалентность.
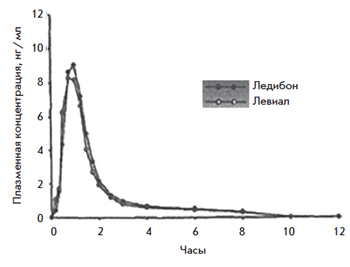
Рис. 8. Сопоставление концентрации 3α-гидрокситиболона
при однократном приеме Ледибона 2,5 мг vs Ливиала 2,5 мг
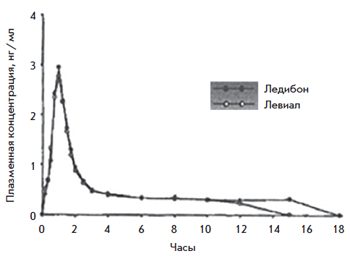
Рис. 9. Сопоставление концентрации 3β-гидрокситиболона при однократном приеме Ледибона 2,5 мг vs Ливиала 2,5 мг
Существует несколько разновидностей эквивалентности: фармацевтическая, биологическая и терапевтическая. Фармацевтическая эквивалентность – эквивалентность, при которой лекарственные препараты содержат одинаковые активные ингридиенты в одинаковой лекарственной форме, предназначены для одного способа введения и являются идентичными по силе действия или концентрации (активных веществ) [30].
Биологическая эквивалентность – эквивалентность, при которой лекарственные препараты имеют сравнимую биодоступность при исследовании в сходных экспериментальных условиях [30]. Терапевтическая эквивалентность – эквивалентность, при которой лекарственные препараты имеют одинаковую эффективность и безопасность [31]. Препарат считается биоэквивалентным оригинальному, если 90% средней AUC вещества входит в диапазон от 80 до 125% от средней AUC оригинального препарата [из правил регистрации дженериков GMP].
Изучение биоэквивалентности препарата Тиболон (Ледибон 2,5 мг vs Ливиал 2,5 мг)
В исследование, проведенное в Чехии в 2005 г., были включены женщины от 18 до 70 лет с естественной или хирургической постменопаузой. Изучалась концентрация 3α- и 3β-гидрокситиболона в плазме крови.
Исследование подтвердило биоэквивалентность ледибона (дженерик) и тиболона (оригинальный препарат) на основе оценки количества основных метаболитов. 90% средней AUC вещества входит в диапазон от 80 до 125% от средней AUC оригинального препарата. Необходимо продолжать накапливать данные о терапевтической эффективности.
Тиболон зарегистрирован в России в 1990 г., и клинический опыт применения его соответствует 25 годам. Применяется в 91 стране по основному показанию – лечение климактерических симптомов и в 55 странах – для профилактики остеопороза. В 2008 г. согласно международной анатомо-терапевтическо-химической классификации лекарственных средств (ВОЗ) тиболон переведен из группы G03D (прогестагенов) в группу G03CX (другие эстрогены). В 2005 г. в журнале Maturitas (51: 21–28) были опубликованы «Клинические рекомендации по применению тиболона». В 2010 г. в журнале Climacteric (4: 317–324) опубликованы «Клинические рекомендации по применению тиболона в странах Азии».
В последних клинических рекомендациях Международной ассоциации по менопаузе (2013) тиболон рекомендуется как средство профилактики и лечения постменопаузального остеопороза.
Заключение
Назначение тиболона (ледибон) предпочтительнее у женщин в постменопаузе, которые отмечают масталгию, нагрубание молочных желез, увеличение маммографической плотности и сексуальные проблемы, особенно после оварэктомии.
Противопоказания для терапии тиболоном такие же, как и для ЭПТ/ЭТ. Кроме того, тиболон следует назначать женщинам, не имеющим РМЖ в анамнезе. Пожилым женщинам (>60 лет) тиболон следует применять с осторожностью и он не должен использоваться пациентками, имеющими серьезные факторы риска развития инсульта.
Список литературы
1. Kloosterboer H.J. Historical milestones in the development of tibolone (Livial®) // Climacteric. 2011 Dec; 14 (6): 609– 621.
2. Markiewicz L., Gurpide E. In vitro evaluation of estrogenic, estrogen antagonistic and progestagenic effects of a stero-idal drug (Org OD-14) and its metabolites on human endo-metrium // J Steroid Biochem. 1990 Apr; 35 (5): 535–541.
3. Tax L., Goorissen E.M., Kicovic P.M. Clinical profile of Org OD 14 // Maturitas. 1987; Suppl 1: 3–13.
4. Punnonen R., Liukko P., Cortes-Prieto J. et al. Multicen-tre study of effects of Org OD 14 on endometrium, vaginal cytology and cervical mucus in post-menopausal and oophorectomized women // Maturitas. 1984 Apr; 5 (4): 281–286.
5. Blom M.J., Wassink M.G., De Gooyer M.E. et al. Metabolism of tibolone and its metabolites in uterine and vaginal tissue of rat and human origin // J Steroid Biochem Mol Biol. 2006 Sep; 101 (1): 42–49.
6. Chetrite G., Kloosterboer H.J., Pasqualini J.R. Effect of tibo-lone (Org OD14) and its metabolites on estronesulphatase activity in MCF-7 and T-47D mammary cancer cells // Anticancer Res. 1997 Jan-Feb; 17 (1A): 135–140.
7. Colacurci N., Mele D., De Franciscis P. et al. Effects of ti-bolone on the breast // Eur J Obstet Gynecol Reprod Biol. 1998 Oct; 80 (2): 235–238.
8. Valdivia I., Ortega D. Mammographic density in postmeno-pausal women treated with tibolone, estriol or conventional hormone replacement therapy // Clin Drug Investig. 2000; 20 (2): 101–107.
9. Nathorst-Böös J., Hammar M. Effect on sexual life–a comparison between tibolone and a continuous estradiol-norethisterone acetate regimen // Maturitas. 1997 Jan; 26 (1): 15–20.
10. Kloosterboer H.J. Tissue-selectivity: the mechanism of action of tibolone // Maturitas. 2004 Aug 30; 48 Suppl 1: S30–40.
11. Reed M.J., Kloosterboer H.J. Tibolone: a selective tissue est-rogenic activity regulator (STEAR) // Maturitas. 2004 Aug 30; 48 Suppl 1: S4–6.
12. Nijland E.A., Nathorst-Böös J., Palacios S. et al. Improved bleeding profile and tolerability of tibolone versus trans-dermal E2/NETA treatment in postmenopausal women with female sexual dysfunction // Climacteric. 2009 Apr; 12 (2): 114–121.
13. Kenemans P., Speroff L. Tibolone: clinical recommendations and practical guidelines. A report of the International Tibolone Consensus Group // Maturitas. 2005 May 16; 51 (1): 21–28.
14. Kenemans P., Bundred N.J., Foidart J.M. et al. Safety and efficacy of tibolone in breast-cancer patients with vasomo- tor symptoms: a double-blind, randomised, non-inferiority trial // Lancet Oncol. 2009 Feb; 10 (2): 135–146.
15. Nijland E.A., Weijmar Schultz W.C., Nathorst-Böös J. et al. Tibolone and transdermal E2/NETA for the treatment of female sexual dysfunction in naturally menopausal women: results of a randomized active-controlled trial // J Sex Med. 2008 Mar; 5 (3): 646–656.
16. Archer D.F., Hendrix S., Gallagher J.C. et al. Endometrial effects of tibolone // J Clin Endocrinol Metab. 2007 Mar; 92 (3): 911–918.
17. Cummings S.R., Ettinger B., Delmas P.D. et al. The effects of tibolone in older postmenopausal women // N Engl J Med. 2008 Aug 14; 359 (7): 697–708.
18. Renoux C., Dell’aniello S., Garbe E. et al. Hormone replacement therapy use and the risk of stroke // Maturitas. 2008 Dec 20; 61 (4): 305–309.
19. Bots M.L., Evans G.W., Riley W. et al. The effect of tibolone and continuous combined conjugated equine oestrogens plus medroxyprogesterone acetate on progression of carotid intima-media thickness: the Osteoporosis Prevention and Arterial effects of tiboLone (OPAL) study // Eur Heart J. 2006 Mar; 27 (6): 746–755.
20. Clarkson T.B. Does tibolone exacerbate atherosclerosis? // Eur Heart J. 2006 Mar; 27 (6): 635–637.
21. Løkkegaard E., Andreasen A.H., Jacobsen R.K. et al. Hormone therapy and risk of myocardial infarction: a national register study // Eur Heart J. 2008 Nov; 29 (21): 2660–2668.
22. Huang K.E., Baber R. Asia Pacific Tibolone Consensus Group. Updated clinical recommendations for the use of tibolone in Asian women // Climacteric. 2010 Aug; 13 (4): 317–327.
23. Hammar M.L., van de Weijer P., Franke H.R. et al. Tibolone and low-dose continuous combined hormone treatment: vaginal bleeding pattern, efficacy and tolerability // BJOG. 2007 Dec; 114 (12): 1522–1529.
24. Delmas P.D., Davis S.R., Hensen J., Adami S. et al. Effects of tibolone and raloxifene on bone mineral density in os-teopenic postmenopausal women // Osteoporos Int. 2008 Aug; 19 (8): 1153–1160.
25. Зайдиева Я.З. Гормонопрофилактика и коррекция системных нарушений у женщин в перименопаузе [Текст]: Дис. … докт. мед. наук: 14.00.01 / Зайдиева Янсият Зайдилаевна. М., 1997: 283: ил. Библиогр.: 244–283.
26. Болдырева Н.В. Гормонопрофилактика и терапия постменопаузального остеопороза [Текст]: Дис. … канд. мед. наук: 14.00.01 / Болдырева Наталья Владимировна. М., 1998: 143: ил. Библиогр.: 129–143.
27. Новикова О.В. Состояние органов репродуктивной системы при длительном использовании заместительной гормонотерапии у женщин в постменопаузе [Текст]: Дис. … канд. мед. наук: 14.00.01 / Новикова Ольга Валерьевна. М., 2002: 213: ил. Библиогр.: 189–213.
28. Медицина климактерия / Под ред. В.П. Сметник. Ярославль: Литера, 2006: 290–348.
29. Policy Relating to Generic Medicines in the OECD. Final report for the European Commission. NERA, S.J. Berwin&Co, YRCR Ltd., December, 1998.
30. FDA, Electronic Orange Book. Approved Drug Products with Therapeutic Equivalence Evaluations, 20th Edition, 2000.
31. Методические рекомендации по проведению качественных клинических исследований биоэквивалентности лекарственных препаратов. МЗ РФ, 2001.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Rec.INN
зарегистрированное ВОЗ
Лекарственное взаимодействие
Входит в состав препаратов:
список
Фармакологическое действие
Анаболический стероид. Обладает эстрогенной, гестагенной и слабой андрогенной активностью, стабилизирует гипоталамо-гипофизарную систему после прекращения функционирования яичников, вызывает снижение секреции гонадотропных гормонов. Тормозит резорбцию костной ткани в постменопаузном периоде, смягчает такие проявления климактерического синдрома, как «приливы» крови к коже лица, повышенное потоотделение, головные боли. Положительно влияет на либидо и настроение (повышает концентрацию центральных и периферических опиоидов). Оказывает стимулирующее действие на слизистую оболочку влагалища, не стимулируя пролиферацию эндометрия. У фертильных женщин подавляет овуляцию.
Предотвращает развитие остеопороза, снижает концентрацию фосфатов и кальция в сыворотке крови.
Фармакокинетика
Абсорбция — высокая. Метаболизируется в печени с образованием гидрофильных продуктов, часть из которых фармакологически активна. Выводится почками (в т.ч. в форме метаболитов), через кишечник.
Показания активного вещества
ТИБОЛОН
Климакс (естественный или вследствие овариэктомии).
Профилактика климактерического остеопороза.
Режим дозирования
Внутрь в дозе 2.5 мг/сут (в одно и то же время); минимальная длительность лечения — 3 мес. Прием препарата начинают через 1 год после последней менструации или сразу же после хирургической менопаузы.
Побочное действие
Со стороны ЦНС: головокружение, головная боль.
Со стороны пищеварительной системы: диарея, повышение активности печеночных трансаминаз, изменение массы тела.
Со стороны эндокринной системы: усиление роста волос на лице, метроррагия, пролиферация эндометрия.
Прочие: отеки голеней, себорейный дерматоз, боли в спине, руках и ногах.
Противопоказания к применению
Беременность, гормонозависимые опухоли (в т.ч. подозрение на них), тромбофлебит, тромбоэмболия (в т.ч. в анамнезе), влагалищное кровотечение неясной этиологии, печеночная недостаточность, сердечно-сосудистая недостаточность, цереброваскулярные расстройства, отосклероз, возникший при беременности или при лечении стероидами, период менее 1 года после последней менструации.
Применение при беременности и кормлении грудью
Противопоказан при беременности.
Применение при нарушениях функции печени
Противопоказан при печеночной недостаточности.
Применение при нарушениях функции почек
C осторожностью применять при почечной недостаточности.
Особые указания
C осторожностью применять при почечной недостаточности, нарушениях углеводного обмена, гиперхолестеринемии, эпилепсии.
Не предназначен для использования в качестве контрацептива. В процессе лечения возможно повышение чувствительности больных к антикоагулянтам вследствие повышения фибринолитической активности крови.
При появлении симптомов тромбоэмболии, желтухи или стойких патологических изменений функциональных печеночных тестов лечение прекращают.
В период лечения необходим регулярный контроль соответствующих лабораторных показателей у больных с гиперхолестеринемией, почечной недостаточностью, сахарным диабетом. На фоне лечения возможно снижение концентраций общего и свободного Т4 и тироксинсвязывающего глобулина.
Лекарственное взаимодействие
Усиливает действие антикоагулянтов.
Препараты с тиболон (tibolone)
Содержимое
- 1 Препараты с тиболон (tibolone)
- 1.1 Препараты с тиболон: инструкция по применению, показания, отзывы
- 1.2 Что такое тиболон?
- 1.3 Препараты с тиболон: виды и названия
- 1.4 Инструкция по применению
- 1.5 Показания для применения
- 1.6 Противопоказания и побочные эффекты
- 1.7 Отзывы о препаратах с тиболон
- 1.8 Вопрос-ответ:
-
- 1.8.0.1 Какие препараты с тиболоном существуют?
- 1.8.0.2 Какие показания для применения препаратов с тиболоном?
- 1.8.0.3 Как принимать препараты с тиболоном?
- 1.8.0.4 Какие побочные эффекты могут возникнуть при применении препаратов с тиболоном?
- 1.8.0.5 Могут ли препараты с тиболоном вызывать аллергические реакции?
- 1.8.0.6 Можно ли применять препараты с тиболоном во время беременности или кормления грудью?
- 1.8.0.7 Какие препараты с тиболоном считаются наиболее эффективными?
- 1.8.0.8 Какие показания для применения препаратов с тиболоном?
- 1.8.0.9 Как применять препараты с тиболоном?
- 1.8.0.10 Какие побочные эффекты могут возникнуть при применении препаратов с тиболоном?
- 1.8.0.11 Какие отзывы есть о препаратах с тиболоном?
-
- 1.9 Где купить препараты с тиболон
- 1.9.1 Аптеки
- 1.9.2 Интернет-аптеки
- 1.9.3 Клиники и медицинские центры
- 1.9.4 Рекомендации
- 1.10 Видео по теме:
Препараты с тиболоном (tibolone) — это гормональные препараты, используемые для лечения симптомов менопаузы у женщин. Они помогают справиться с приливами, нарушениями сна, настроениями, а также уменьшают риск остеопороза. Узнайте больше о преимуществах и побочных эффектах тиболона, а также о том, как правильно использовать эти препараты для достижения наилучших результатов.
Вы ищете эффективный препарат для решения проблем, связанных с климаксом или недостатком эстрогенов? Тогда препараты с тиболоном – ваш выбор! На сайте «Название сайта» вы найдете подробную информацию о препаратах на основе тиболона, их инструкцию по применению, показания к использованию и отзывы реальных пациентов.
Тиболон – это синтетический гормон, который активно применяется для лечения различных женских заболеваний. Его уникальное действие позволяет справиться с такими проблемами, как приливы, нарушение менструального цикла, снижение полового влечения и другие симптомы, связанные с недостатком эстрогенов.
Препараты с тиболоном – это эффективное решение для женщин, страдающих от климакса или других проблем, связанных с гормональным дисбалансом. Они помогут вам вернуться к полноценной жизни и наслаждаться каждым днем!
Инструкция по применению препаратов с тиболоном будет подробно описана на нашем сайте, а также вы сможете ознакомиться с показаниями к использованию и прочитать отзывы пациентов, которые уже испытали на себе положительный эффект от этих препаратов. Не откладывайте свое здоровье на потом – посетите наш сайт и узнайте больше о препаратах с тиболоном уже сегодня!
Препараты с тиболон: инструкция по применению, показания, отзывы
Препараты с тиболон являются эффективным средством для лечения различных заболеваний и симптомов, связанных с недостатком эстрогенов. Тиболон — это синтетическое вещество, которое обладает эстрогенным, прогестагенным и андрогенным действием.
Препараты с тиболоном широко применяются для лечения климактерического синдрома, постменопаузальных нарушений, остеопороза, а также для предотвращения развития сердечно-сосудистых заболеваний. Они помогают справиться с приливами, нервозностью, нарушениями сна, а также улучшают состояние костей и сосудов.
Инструкция по применению препаратов с тиболоном может незначительно различаться в зависимости от конкретного препарата. Однако, обычно рекомендуется принимать 1 таблетку в день, желательно в одно и то же время. Длительность приема определяется врачом и зависит от целей лечения.
Показания для применения препаратов с тиболоном включают следующие состояния:
- Климактерический синдром (приливы, нарушения сна, нервозность и др.)
- Постменопаузальные нарушения (атрофический вагинит, сухость слизистых оболочек и др.)
- Остеопороз (профилактика и лечение)
- Предотвращение сердечно-сосудистых заболеваний у женщин в постменопаузальном периоде
Препараты с тиболоном могут иметь побочные эффекты, такие как тошнота, головная боль, мастодиния, изменение аппетита и т.д. Поэтому перед началом приема препаратов необходимо проконсультироваться с врачом и ознакомиться с инструкцией.
Отзывы о препаратах с тиболоном обычно положительные. Женщины отмечают улучшение самочувствия, снижение симптомов климактерического синдрома, укрепление костной ткани и другие положительные эффекты. Однако, каждый организм индивидуален, поэтому результаты могут различаться.
В целом, препараты с тиболоном являются эффективным средством для лечения различных женских заболеваний и симптомов. Они помогают улучшить качество жизни и предотвратить развитие серьезных осложнений. Однако, перед началом приема препаратов необходимо проконсультироваться с врачом и строго соблюдать инструкцию по применению.
Что такое тиболон?

Тиболон — это препарат, который используется для лечения различных женских заболеваний, связанных с гормональным дисбалансом. Он является синтетическим аналогом женских половых гормонов — эстрогенов, прогестерона и андрогенов.
Тиболон выпускается в виде таблеток, которые принимаются внутрь. Он обладает не только гормональными свойствами, но также имеет противоположное действие на разные органы и ткани, что делает его уникальным средством для лечения различных женских проблем.
Препарат тиболон имеет следующие показания к применению:
- Лечение симптомов менопаузы, таких как приливы, нарушения сна, изменения настроения и др.
- Профилактика остеопороза у женщин после менопаузы.
- Лечение дисменореи (болезненных менструаций).
- Улучшение состояния кожи и волос.
Препарат тиболон имеет некоторые противопоказания и побочные эффекты, поэтому перед его использованием необходимо проконсультироваться с врачом.
Гос. поликлиники и больницы
0%
Частные клиники и мед. центры
0%
Препараты с тиболон: виды и названия

Препараты с тиболоном являются эффективным средством в лечении некоторых женских заболеваний и симптомов менопаузы. Тиболон — это гормональный препарат, который содержит синтетические аналоги женских половых гормонов — эстрогенов и прогестерона.
Существует несколько видов препаратов с тиболоном, каждый из которых имеет свои особенности и назначение:
- Климадион — препарат, который содержит тиболон в дозировке 2,5 мг. Он используется для лечения симптомов менопаузы, таких как приливы жара, нарушения сна, раздражительность и депрессия.
- Ливиал — препарат, который содержит тиболон в дозировке 2,5 мг. Он применяется для лечения симптомов менопаузы и предотвращения остеопороза у женщин после менопаузы.
- Тибофем — препарат, который содержит тиболон в дозировке 2,5 мг. Он применяется для лечения симптомов менопаузы и предотвращения остеопороза.
Препараты с тиболоном эффективны в устранении симптомов менопаузы и улучшении качества жизни женщин. Однако перед началом приема любого препарата необходимо проконсультироваться с врачом и ознакомиться с инструкцией по применению.
Сравнение препаратов с тиболономНазвание препаратаДозировкаПоказания к применению
| Климадион | 2,5 мг | Симптомы менопаузы |
| Ливиал | 2,5 мг | Симптомы менопаузы, остеопороз |
| Тибофем | 2,5 мг | Симптомы менопаузы, остеопороз |
Не забывайте, что самолечение может быть опасным для вашего здоровья. Всегда проконсультируйтесь с врачом, прежде чем начать принимать препараты с тиболоном.
Инструкция по применению
Препарат: Тиболон
Форма выпуска: Таблетки, покрытые оболочкой
Дозировка: 2,5 мг
Показания к применению:
- Хронический вагинит
- Менопаузальный синдром
- Остеопороз
- Гиперэстрогенемия
Способ применения:
- Принимайте таблетки перорально, запивая достаточным количеством воды.
- Выполняйте прием препарата в одно и то же время каждый день.
- Длительность курса лечения определяется врачом в зависимости от показаний и эффективности препарата.
- При необходимости проконсультируйтесь с врачом о возможности продления курса лечения.
Противопоказания:
- Гиперчувствительность к тиболону или любому другому компоненту препарата.
- Рак молочной железы или другие гормонозависимые опухоли.
- Тромбоз или наличие риска его развития.
- Болезни печени или желчного пузыря в активной фазе.
Побочные эффекты:
Система органовПобочные эффекты
| Гинекологическая система | Меноррагия, метроррагия, изменение выделений из влагалища |
| Пищеварительная система | Диспепсия, тошнота, рвота, боли в животе |
| Нервная система | Головная боль, нарушение сна, изменение настроения |
| Кожа и подкожная клетчатка | Сыпь, зуд, аллергические реакции |
Сохранение препарата:
Храните таблетки в недоступном для детей месте при температуре не выше 25°C.
Важно: Данная инструкция предоставлена только для ознакомления. Перед началом приема препарата обязательно проконсультируйтесь с врачом.
Показания для применения

- Климактерический синдром с выраженными симптомами (приливы жара, нарушения сна, изменения настроения, повышенная раздражительность, снижение памяти и концентрации внимания).
- Остеопороз (уменьшение плотности костной ткани, повышенный риск переломов).
- Профилактика остеопороза у женщин в постменопаузе с повышенным риском развития заболевания.
- Повышение уровня холестерина в крови.
- Расстройства менструального цикла.
- Подготовка к гормональной заместительной терапии.
Противопоказания и побочные эффекты
Препараты с тиболоном имеют свои противопоказания, которые нужно учитывать перед началом приема. Не рекомендуется использовать препараты с тиболоном в следующих случаях:
- Индивидуальная непереносимость тиболона или других компонентов препарата;
- Злокачественные опухоли груди или половых органов;
- Тяжелые нарушения функции печени;
- Тромбоз, венозная тромбоэмболия или состояние после их развития;
- Острый или прошедший тромбофлебит;
- Сахарный диабет с сосудистыми осложнениями;
- Заболевания с сердечной недостаточностью, в том числе с артериальной гипертензией.
Прием препаратов с тиболоном может вызвать некоторые побочные эффекты, включая:
- Головные боли и мигрени;
- Нарушение сна и бессонница;
- Раздражительность и изменение настроения;
- Повышение артериального давления;
- Неправильные месячные кровотечения;
- Боли в груди;
- Тошнота и рвота;
- Увеличение молочных желез;
- Отеки и вздутие.
Если у вас возникли какие-либо побочные эффекты или противопоказания, обратитесь к врачу для консультации и рекомендаций.
Отзывы о препаратах с тиболон
Препараты с тиболон являются эффективным средством для лечения различных гинекологических заболеваний и нормализации гормонального фона у женщин. Ниже представлены отзывы пациенток, которые использовали препараты с тиболон и поделились своими впечатлениями:
- Анна: Принимаю препарат с тиболон уже несколько месяцев и заметила значительное улучшение в общем состоянии. Ранее страдала от сильных менструальных болей и нарушений цикла, но после начала приема тиболона все стало намного лучше. Рекомендую!
- Марина: После родов у меня возникли проблемы с гормональным фоном, что приводило к нарушениям цикла и нерегулярным месячным. Мой врач назначил мне препарат с тиболон, и я неожиданно для себя заметила положительные изменения уже через несколько недель. Цикл стал стабильным, а общее самочувствие улучшилось. Очень довольна результатом!
- Екатерина: Препарат с тиболон мне был назначен для лечения симптомов климакса, таких как приливы жара и нарушения сна. Принимаю его уже несколько месяцев и могу сказать, что симптомы стали гораздо слабее. Приливы стали реже и менее интенсивными, а сон улучшился. Рекомендую данный препарат всем женщинам, страдающим от симптомов климакса.
Отзывы пациенток свидетельствуют о высокой эффективности препаратов с тиболон. Однако, перед началом приема данного препарата, необходимо проконсультироваться с врачом и следовать его рекомендациям.
Вопрос-ответ:
Какие препараты с тиболоном существуют?
Существует несколько препаратов с тиболоном, таких как «Ливиал», «Тиболон», «Климадиен», «Ангелик», «Тибофем», «Тибозен».
Какие показания для применения препаратов с тиболоном?
Препараты с тиболоном применяются для лечения симптомов менопаузы, таких как приливы, потливость, нарушение сна, нарушение эмоционального состояния. Также они могут применяться для профилактики остеопороза у женщин в постменопаузальном периоде.
Как принимать препараты с тиболоном?
Дозировка и схема приема препаратов с тиболоном могут различаться в зависимости от конкретного препарата и показаний к применению. Обычно препараты принимаются внутрь, одну таблетку в день, предпочтительно в одно и то же время. Но для точной информации следует обратиться к инструкции по применению конкретного препарата.
Какие побочные эффекты могут возникнуть при применении препаратов с тиболоном?
При применении препаратов с тиболоном возможны побочные эффекты, такие как головная боль, нарушение сна, изменение аппетита, тошнота, желудочно-кишечные расстройства, нарушение менструального цикла, изменение вагинального выделения. Однако не все пациенты испытывают эти эффекты, и они обычно проходят самостоятельно или снижаются со временем.
Могут ли препараты с тиболоном вызывать аллергические реакции?
Да, в редких случаях препараты с тиболоном могут вызывать аллергические реакции, такие как кожная сыпь, зуд, отек лица или горла. Если у вас возникли подобные реакции, следует немедленно прекратить прием препарата и обратиться к врачу.
Можно ли применять препараты с тиболоном во время беременности или кормления грудью?
Препараты с тиболоном противопоказаны во время беременности и кормления грудью. Если вы планируете беременность или уже беременны, следует проконсультироваться с врачом о возможных альтернативных методах лечения.
Какие препараты с тиболоном считаются наиболее эффективными?
Вопрос о наиболее эффективных препаратах сКакие препараты с тиболоном существуют?Существует несколько препаратов с тиболоном, включая Ливиал, Тиболон и Ксеностатин. Каждый из них имеет свои особенности и разные дозировки. Рекомендуется проконсультироваться с врачом, чтобы выбрать подходящий препарат.
Какие показания для применения препаратов с тиболоном?
Препараты с тиболоном обычно применяются для лечения симптомов менопаузы, таких как приливы жара, нарушения сна, раздражительность и депрессия. Они также могут быть назначены для профилактики остеопороза у женщин после менопаузы.
Как применять препараты с тиболоном?
Дозировка и режим применения препаратов с тиболоном зависят от конкретного препарата и индивидуальных особенностей пациента. Обычно препараты принимаются внутрь, одну таблетку в день. Рекомендуется проконсультироваться с врачом или ознакомиться с инструкцией по применению конкретного препарата.
Какие побочные эффекты могут возникнуть при применении препаратов с тиболоном?
При применении препаратов с тиболоном могут возникнуть различные побочные эффекты, такие как головная боль, тошнота, вздутие живота, изменение аппетита и изменение месячных циклов. Если возникают какие-либо неприятные симптомы, следует обратиться к врачу.
Какие отзывы есть о препаратах с тиболоном?
Отзывы о препаратах с тиболоном могут быть разными. Некоторые женщины отмечают положительный эффект от применения препаратов, так как они помогают справиться с симптомами менопаузы и улучшают качество жизни. Однако, у каждого человека организм индивидуален, поэтому эффект может быть разным. Рекомендуется проконсультироваться с врачом и ознакомиться с отзывами других пациентов перед началом приема препарата.
Где купить препараты с тиболон

Препараты с тиболон – это эффективное средство, которое помогает женщинам справиться с проблемами, связанными с нарушением гормонального баланса и менопаузой. Если вы ищете место, где можно приобрести такие препараты, мы предлагаем вам несколько вариантов.
Аптеки
Одним из наиболее доступных и удобных мест для покупки препаратов с тиболон являются аптеки. В них вы можете найти широкий ассортимент препаратов с тиболон различных производителей. Обратитесь к фармацевту, чтобы получить консультацию и выбрать наиболее подходящий препарат для вас.
Интернет-аптеки

Онлайн-аптеки предлагают возможность приобрести препараты с тиболон без выхода из дома. Вы можете легко сравнить цены и ассортимент различных интернет-аптек, прочитать отзывы покупателей и выбрать наиболее надежного поставщика. Обратите внимание на рейтинги интернет-аптек и проверяйте лицензии перед покупкой.
Клиники и медицинские центры
В некоторых клиниках и медицинских центрах вы можете купить препараты с тиболон по рецепту врача. Это может быть удобным вариантом, если вы хотите получить профессиональную консультацию перед покупкой и быть уверенными в качестве препарата.
Рекомендации
Независимо от того, где вы решите приобрести препараты с тиболон, рекомендуется обратиться к врачу перед началом приема. Врач поможет вам определиться с дозировкой и выбрать наиболее подходящий препарат для вашего случая.
Не забывайте, что самолечение может быть опасным для вашего здоровья, поэтому всегда следуйте рекомендациям врача и берегите свое здоровье.
Видео по теме:
-
Архив журнала
/ -
2003
/ - №11
Тиболон как альтернатива заместительной гормональной терапии
Е.А. Ушкалова
Заместительная гормональная терапия (ЗГТ), наряду с положительными эффектами, не лишена и ряда недостатков. Это диктует необходимость поиска эффективных и безопасных альтернатив ЗГТ при постменопаузальных нарушениях, одной из которых является тиболон — синтетический стероид, обладающий андрогенными, гестагенными и эстрогенными свойствами. Рассматривается влияние тиболона на климактерические симптомы и качество жизни женщин в постменопаузе. Обсуждаются эффекты этого препарата на нервно-психическое состояние и когнитивные функции, факторы риска сердечно-сосудистых заболеваний, костную ткань и эндометрий. Отмечается возможное протективное влияние тиболона в отношении рака молочной железы.
Заместительная гормональная терапия (ЗГТ) за последние десятилетия получила широкое распространение, особенно за рубежом. Например, в США в настоящее время ее получают около 6 млн. женщин [1]. Это обусловлено тем, что те или иные климактерические симптомы имеют место более чем у 75% женщин в постменопаузе, причем, примерно, у 25% из них они оцениваются как тяжелые [2]. Наряду с положительными эффектами, ЗГТ не лишена и ряда недостатков, поэтому поиск эффективных и безопасных альтернатив продолжается. В качестве одной из них рассматривается тиболон – синтетический стероид, обладающий андрогенными, гестагенными и эстрогенными свойствами [3]. Препарат находится на мировом фармацевтическом рынке более двух десятилетий и зарегистрирован примерно в 70 странах мира. Он был разработан специально для лечения остеопороза, однако, благодаря уникальным фармакологическим свойствам, вскоре был также зарегистрирован для лечения климактерического синдрома и профилактики остеопороза.
Фармакологические эффекты тиболона преимущественно обусловлены его метаболитами, воздействующими на разные органы и ткани [4]. Тиболон- синтетический стероид, при попадании внутрь метаболизируется с образованием трех метаболитов: 3альфа-OH-тиболон, 3бета-OH-тиболон и 4сигма-изомер, которые обладают различным сродством к стероидным рецепторам. Исследования in vitro показали, что гидроксиметаболиты тиболона имеют высокое сродство к эстрогенным рецепторам (преимущественно к a-рецепторам), а 4сигма-изомер – обладает высоким аффинитетом к рецепторам прогестерона и слабым сродством к андрогенным рецепторам [5]. Концентрация различных метаболитов тиболона варьирует в разных органах и тканях [4], в связи с чем препарат проявляет тканеселективное действие [7]. На костную ткань и влагалище тиболон оказывает эстрогенный эффект. В эндометрии проявляется гестагенное действие 4сигма-изомера, а в головном мозге и печени этот изомер оказывает андрогенные эффекты. В молочной железе тиболон вызывает мощное угнетение сульфатазы и ингибирование 17бета-гидроксистероиддегидрогеназы (тип I), что приводит к блокаде превращения эстрона сульфата в эстрон и затем, в эстрадиол.
Оказывая селективное гормональное действие на разные органы-мишени, тиболон вызывает различные эффекты у женщин в постменопаузе, которые были изучены более чем в 20 рандомизированных контролируемых двойных слепых исследованиях [8].
В связи с уникальным механизмом действия, тиболон выделен в отдельный класс терапии – STEAR (selective tissue estrogenic activity regulator; тканеселективный регулятор эстрогенной активности). Официальное представление тиболона как нового класса терапии состоялось в мае 2003 года на шестом европейском конгрессе по менопаузе.
В настоящее время, с учетом нерандомизированных и открытых исследований, а также клинических испытаний и ретроспективных анализов, изучению тиболона у женщин посвящено более 400 работ [8].
Влияние тиболона на климактерические симптомы и качество жизни женщин в постменопаузе
Влияние тиболона на климактерические симптомы было изучено не менее чем в 8 рандомизированных двойных слепых клинических исследованиях, 4 из которых были плацебо-контролируемыми [9-13]. В одном исследовании проводилось сравнение тиболона с эстрадиола валератом [13], еще в одном – с комбинацией конъюгированных эстрогенов и медрокспрогестерона ацетата [14], в двух – с комбинацией эстрадиола и норэтистерона ацетата [15,16].
Эти исследования показали, что тиболон в дозе 2,5 мг по эффективности ослабления приливов не уступает стандартным режимам ЗГТ. Препарат также эффективен при лечении приливов, развивающихся при терапии агонистами гонадотропин-рилизинг гормона [17].
Во многих исследованиях продемонстрированы благоприятные эффекты тиболона и в отношении других симптомов менопаузы, включая повышенную утомляемость, психологическую нестабильность, головные боли и бессонницу [9,12,14].
В работе Genazzani и соавт. показано, что ослабление приливов жара при лечении тиболоном ассоциируется с улучшением сна и настроения [11]. Исследователи высказали предположение, что последний эффект обусловлен бета-эндорфинами, концентрация которых под влиянием тиболона повышается. В небольшом исследовании, включавшем молодых женщин с удаленной маткой и яичниками, тиболон проявлял одинаковую эффективность в отношении ослабления приливов и улучшения настроения с эстрадиола валератом [13].
Благодаря наличию эстрогенного действия, тиболон нормализует созревание клеток влагалища, уменьшает его сухость и диспареунию у женщин в менопаузе [18,19]. По данным ряда исследований, он не уступает эстрогенам по эффективности устранения этих симптомов. Более того, в проспективных рандомизированных исследованиях показано, что сексуальность женщин при применении тиболона повышается в большей степени, чем при использовании эстрогенов или их комбинаций с прогестинами [15,20-24].
В плацебо-контролируемых исследованиях доказано, что тиболон увеличивает либидо и сексуальную активность [25]. Под влиянием препарата особенно усиливались сексуальные фантазии, половое возбуждение и оргазм. Открытое многоцентровое исследование с участием 184 женщин, впервые получавших тиболон в течение 4 месяцев, продемонстрировало значительное повышение степени их удовлетворенности разными аспектами половой жизни [25]. В основе этих эффектов лежат 2 механизма: прямое андрогенное действие 4сигма-изомера и увеличение циркуляции свободного тестостерона. Под влиянием тиболона количество циркулирующего гормоносвязывающего глобулина снижается примерно на 50% [26,27]. Вследствие этого уменьшается концентрация общего тестостерона, но значительно возрастает уровень его свободной активной фракции. Изменения уровня гормонов, вызываемые тиболоном, благоприятно отличаются от таковых, вызываемых эстрогеном (повышение уровня гормоносвязывающего глобулина и снижение уровней общего и свободного тестостерона). Слабое андрогенноподобное действие при приеме тиболона клинически обусловливает, главным образом, улучшение качества жизни, в виде благоприятного влияния на настроение и улучшение либидо. Некоторые авторы даже рекомендуют применение тиболона для усиления полового влечения у женщин с персистирующим, несмотря на адекватную комбинированную ЗГТ, снижением либидо [30]. При этом важно, что тиболон не вызывает андрогенных побочных эффектов, таких как акне и гирсутизм [3].
В отличие от эстрогенов тиболон не оказывает эстрогенного действия на миометрий, напротив, его 4сигма-изомер вызывает гестагенный эффект. В результате, при применении тиболона не происходит стимуляции эндометрия и, соответственно, нет необходимости в дополнительном назначении гестагена для защиты миометрия [7,28,29].
В сравнительных исследованиях с комбинацией эстрадиола и норэтистерона ацетата количество эпизодов вагинальных кровотечений у женщин, получавших тиболон, было примерно в 2 раза меньшим, чем у женщин, получавших комбинированную терапию [31,32]. По результатам двойного слепого многоцентрового европейского исследования, тиболон вызывал кровотечения существенно реже, чем при использовании комбинированной монофазной терапии (конъюгированные эстрогены с медроксипрогестероном ацетатом) [23]. Еще в одном рандомизированном исследовании пероральное применение тиболона (2,5 мг/сут) было сопряжено с меньшей частотой кровотечений, чем циклическая трансдермальная комбинированная терапия (пластырь 17бета-эстрадиола 50 мкг/сут в течение 14 дней, затем пластырь 17бета-эстрадиола 50 мкг/сут + норэтистерона ацетат 0,25 мг/сут в течение последующих 14 дней) [33]. Кровотечения, вызванные тиболоном, чаще наблюдаются в раннем постменопаузальном периоде, в связи с чем в настоящее время назначение препарата рекомендуют женщинам, которые находятся в менопаузе не менее 1 года [3].
В целом, ослабление климактерических и урогенитальных симптомов под влиянием тиболона ассоциируется с улучшением качества жизни женщин [36].
Влияние тиболона на нервно-психическое состояние и когнитивные функции
Тиболон оказывает умеренный положительный эффект на настроение [27,31]. В небольшом открытом исследовании длительное применение тиболона (10 лет) приводило к уменьшению нервозности в ответ на небольшой стресс [35]. Эти данные были подтверждены в другом рандомизированном исследовании [36].
Эффекты препарата на когнитивные функции изучены недостаточно, что обусловлено сложностью проведения подобных исследований, требующих соответствия основной и контрольной групп по множеству параметров (уровень интеллекта, возраст, образование, занимаемая должность, психический статус и др.), и отсутствием стандартизованных определений ряда понятий и стандартизованных методов их измерения. Результаты небольшого исследования позволяют предположить, что при кратковременном применении (3-6 месяцев) тиболон может способствовать сохранению когнитивной функции у женщин в постменопаузе [37]. Однако все эти данные требуют подтверждения в хорошо спланированных больших исследованиях.
Влияние тиболона на факторы риска сердечно-сосудистых заболеваний
Под влиянием тиболона происходят отличные от традиционной ЗГТ (чистые эстрогены и комбинированные эстроген-гестагенные комбинации) изменения концентраций липидов в крови. Изучению влияния тиболона на липидный профиль и факторы свертывания крови было посвящено 7 плацебо-контролируемых, двойных слепых исследований и 2 сравнительных двойных слепых исследования с комбинацией эстрадиола и норэтистерона ацетата. В краткосрочных исследованиях тиболон в дозе 2,5 мг/сут снижал уровень холестерина липопротеидов высокой плотности (ЛПВП) примерно на 20%, общего холестерина – на 10% и триглицеридов – на 20%. Он также вызывал небольшое снижение концентрации холестерина липопротеидов низкой плотности (ЛПНП) или не влиял на него [25,26,32,38]. В других плацебо-контролируемых исследованиях снижение уровней холестерина ЛПВП и триглицеридов под влиянием препарата было более выраженным, однако концентрации холестерина ЛПНП и липопротеина (альфа) не изменялись [11,28,29]. В некоторых исследованиях снижение уровня ЛПВП под влиянием тиболона имело недостоверный характер [40,41].
Снижение уровня холестерина ЛПВП при применении тиболона ассоциировалось с повышением активности липазы в печени (андрогенный эффект), однако в исследовании показано, что при этом способность плазмы пациенток высвобождать холестерин из артериальных стенок оставалась неизменной [42]. В исследовании на обезьянах значительное снижение уровня холестерина ЛПВП не сопровождалось обострением атеросклероза подвздошной артерии, что связывают с благоприятным влиянием препарата на функцию сосудов или печеночный метаболизм [43].
В рандомизированном клиническом исследовании показано, что существенное снижение уровня ЛПВП (в среднем на 27%) при лечении тиболоном было обусловлено его влиянием лишь на один подкласс ЛПВП, в связи с чем антиатерогенные функции (обратный транспорт холестерина и угнетение окисления ЛПНП) оставались неизмененными [43]. Недостатком данного исследования является его небольшая продолжительность (12 недель), однако полученные результаты полностью совпадают с данными 2-летних экспериментальных исследований на обезьянах. Они были подтверждены еще в одном рандомизированном, плацебо-контролируемом исследовании, продолжавшемся 3 месяца [44].
Потенциально неблагоприятные эффекты, связанные со снижением уровня холестерина ЛПВП, уравновешиваются влиянием тиболона на эндотелин и липопротеин (альфа), антиишемическими эффектами, обнаруженными у женщин со стенокардией, и повышением чувствительности к инсулину [45-49]. В длительных исследованиях уровень холестерина ЛПВП возвращался к исходному через 3 года лечения этим препаратом [46-49]. Недавно была показана способность тиболона снижать концентрации тромбоксана B2, что может приводить к улучшению метаболизма простагландинов и снижать риск сердечно-сосудистых заболеваний [50].
В отличие от эстрогенов тиболон не оказывает выраженного действия на повышение свертываемости крови, но стимулирует фибринолитическую активность. В плацебо-контролируемых исследованиях показано, что длительное применение тиболона приводит к повышению уровней гемоглобина, антитромбина III, плазминогена и числа тромбоцитов [51,52]. В многоцентровом рандомизированном двойном слепом исследовании не удалось выявить существенного влияния препарата на свертываемость крови [32].
По мнению исследователей, клиническое значение эффектов тиболона на метаболизм липидов и гемостаз остается неясным и требует дальнейшего изучения.
При лечении тиболоном наблюдалось 3-4-кратное увеличение уровня С-реактивного белка, что сопоставимо с таковым при применении стандартной ЗГТ [53]. Однако, значение изменений уровня С-реактивного белка для клинических проявлений сердечно-сосудистых заболеваний у женщин в менопаузе остается не до конца ясным [8]. Тиболон не влияет на уровень гомоцистеина – другого вещества, с которым связывают риск коронарной болезни [54].
Тиболон снижает уровень свободных жирных кислот в плазме крови, что приводит к нормализации соотношения симпатических и парасимпатических влияний на сердце и, по мнению исследователей, может способствовать предупреждению инфаркта миокарда и сердечной недостаточности [55]. Еще одним благоприятным эффектом тиболона на сердечно-сосудистую систему является прямое влияние на эндотелиальные клетки, обусловливающее снижение адгезии лейкоцитов к эндотелию [56].
Тромбоэмболических осложнений в клинических исследованиях препарата не наблюдалось [57]. Повышенного риска венозной тромбоэмболии не удалось выявить и по результатам широкого медицинского применения тиболона в течение более 15 лет во многих странах мира [3]. Данные, полученные на 4537 женщинах, участвовавших в III и IV фазах клинических испытаний тиболона, показали, что относительный риск для всех сердечно-сосудистых заболеваний, составил: RR=0,58 (0,31-1,10).
Данные экспериментальных исследований у обезьян дают основание предполагать, что тиболон не оказывает существенного влияния на сердечно-сосудистую систему, по-видимому, вследствие того, что его негативные эффекты уравновешиваются позитивными. Длительное (в среднем 7,5 лет) наблюдение за женщинами, получавшими тиболон, также не позволило выявить повышение толщины интимы сонной артерии и увеличение числа атеросклеротических бляшек [58]. Однако, окончательно вопрос о безопасности тиболона в отношении сердечно-сосудистой системы может быть решен только в хорошо спланированных крупномасштабных клинических исследованиях.
Влияние тиболона на костную ткань
Влияние тиболона на костную ткань является следствием его эстрогенной активности [8]. Оно было изучено в 8 рандомизированных двойных слепых исследованиях, 7 из которых были плацебо-контролируемыми и одно – сравнительным с эстрогенами [59-66]. Во всех исследованиях было продемонстрировано значительное повышение минеральной плотности кости в поясничном отделе позвоночника и шейке бедра под влиянием тиболона по сравнению с плацебо [67]. Наиболее выраженным благоприятное влияние тиболона на костную ткань было у женщин с остеопорозом. Оно проявлялось уже при кратковременном приеме препарата (3 месяца) [65] и сохранялось при длительном применении (10 лет) [68].
По эффективности предотвращения потери костной ткани у женщин в постменопаузе тиболон в клинических исследованиях не уступал эстрогенам и комбинированной ЗГТ [41,59,69,70]. Сходная эффективность тиболона и эстрогенов подтверждена результатами мета-анализа, включавшего 39 рандомизированных контролируемых 2-летних исследований [71]. Преимуществом тиболона перед стандартной ЗГТ является и лучшая переносимость, которая позволяет применять его на протяжении длительного времени (10 лет и более) [68,72]. Препарат также предотвращает потерю костной ткани, вызванную агонистами гонадотропин-рилизинг гормона [73].
Результаты измерения минеральной плотности кости при лечении тиболоном позволяют предположить наличие у него протективного эффекта в отношении переломов, обусловленных остеопорозом, однако это предположение должно быть подтверждено в целенаправленных клинических исследованиях.
Влияние тиболона на эндометрий
Несмотря на отдельные сообщения о пролиферации эндометрия у женщин, получавших тиболон [74,75], в длительных (до 8 лет) исследованиях показано наличие у препарата протективного эффекта в отношении эндометрия [29,76-78]. Он обусловлен тем, что преобладающим (если не единственным) метаболитом тиболона в эндометрии является 4сигма-изомер, связывающийся с рецептором прогестерона и, таким образом, защищающий его от агонистических эффектов двух метаболитов с эстрогенной активностью [79]. Данные, полученные в III и IV фазах клинических испытаний тиболона, показали, что относительный риск рака эндометрия составил RR=0,37 (0,03-0,59).
В открытом проспективном многоцентровом исследовании не было отмечено стимулирующего влияния тиболона на эндометрий через 12 и 24 месяцев лечения соответственно у 98,2% и 91,9% обследованных женщин [81].
Частота прорывных кровотечений при применении тиболона значительно ниже, чем при применении комбинированной ЗГТ [20,26,31,81]. Аменорея при приеме тиболона достигается быстрее: у 90% женщин она наступает в течение 6 месяцев лечения [31,74,75]. Кровотечения реже отмечаются у женщин более старшего возраста [82]. Наблюдение в течение 3 лет за женщинами с фибромами матки, получавшими тиболон, не позволило выявить роста миом [83].
Тиболон и рак молочной железы
Влияние тиболона на клетки молочной железы изучалось особенно тщательно. В ткани молочной железы тиболон и его метаболиты оказывают ингибирующее влияние на ферменты, способствующие локальному синтезу эстрадиола (сульфатаза и 17сигма-гидроксистероид дегидрогеназа (тип I)) и напротив, активирует ферменты (сульфотрансфераза и 17сигма-гидроксистероид дегидрогеназа (тип II)), преобразующие активный эстрадиол в менее активный эстрон и неактивные сульфатированные формы, которые выводятся из организма с мочой. Таким образом, тиболон отличается уникальным механизмом действия, который обусловливает не только отсутствие стимуляции эстрогенных рецепторов в молочной железе эстрогенными метаболитами тиболона, но и благодаря специфической «ферментной регуляции», способствует снижению локальной концентрации активного эстрадиола [84]. Помимо этого в исследованиях in vitro у тиболона была выявлена антипролиферативная активность, способность усиливать клеточную дифференциацию и вызывать апоптоз раковых клеток молочной железы [85].
В клинических исследованиях доказано, что тиболон значительно реже приводит к увеличению плотности молочной железы при маммографии и реже вызывает масталгию, чем эстрогены и комбинированная ЗГТ [31,85-87]. Положительные эффекты тиболона связывают с его влиянием на ферменты, принимающие участие в локальной продукции эстрогенов в тканях молочной железы. В III и IV фазах клинических испытаний препарата с участием 4537 женщин, задокументированная частота рака молочной железы составила 1,59 на 1000 человеко-лет в основной группе против 3,15 в группе плацебо. Относительный риск рака молочной железы при приеме тиболона составил: RR=0,50 (0,11-2,54) [80].
Вышеизложенное позволило высказать предположение о том, что тиболон обладает протективным действием в отношении рака молочной железы [3].
Тиболон и сахарный диабет
У пожилых женщин с сахарным диабетом 2 типа при применении тиболона в дозе 2,5 мг/сут не было выявлено значительных изменений липидного профиля [88]. Препарат повышал чувствительность к инсулину в случае резистентности к гормону [88]. Он не оказывал отрицательного влияния на артериальное давление у женщин с сахарным диабетом и гипертензией [38]. Вышеприведенные эффекты позволяют рекомендовать тиболон для применения больным диабетом в постменопаузе [38,89].
Заключение
На сегодняшний день тиболон может рассматриваться в качестве достойной альтернативы стандартной ЗГТ для большинства женщин в постменопаузе [89]. Тиболон проявляет сходную клиническую эффективность с эстрогенами при симптомах менопаузы, как приливы и различные урогенитальные нарушения, но превосходит последние по влиянию на сексуальность. Его безопасность в отношении эндометрия и способность предотвращать потерю костной ткани сопоставимы с таковыми комбинированной ЗГТ, однако тиболон реже вызывает прорывные кровотечения. Суммарный эффект тиболона и его метаболитов на сердечно-сосудистую систему в настоящее время рассматривают как нейтральное действие. Дальнейшие рандомизированные исследования позволят сделать окончательные выводы. Подтверждения требует и наличие у тиболона протективного эффекта в отношении рака молочной железы.
Такого рода исследования уже начаты. Это крупные многоцентровые рандомизированные слепые плацебо-контролируемые исследования:
- исследование LIFT (Long-term Interventional Fracture study in osteoporotic patients), направленное на выявление частоты переломов;
- исследование OPAL (Osteoporosis Prevention and Antiatherosclerosis effects of TiboLone), оценивающее влияние препарата на костную ткань и сердечно-сосудистую систему;
- исследование LIBERATE (Livial Intervention following Breast Cancer; Efficacy, Recurrence, and Tolerability Endpoints), посвященное безопасности тиболона в отношении молочной железы;
- исследование THEBES (Tibolone Histology of the Endometrium and Breast Endpoints Study), оценивающее ответ эндометрия на лечение [21].
Результаты этих исследований позволят окончательно определить место тиболона в терапии и профилактике постменопаузальных нарушений.
Литература
- Hamdy RC: Hormonal replacement therapy. South Med J 2001; 94:1141-2
- Porter M, Penney GC, Russell D, et al. A population based survey of women’s experience of the menopause. Br J Obstet Gynaecol 2002;103:1025-8.
- Speroff L, Clarkson ThB. Is tibolone a Viable Alternative to HT? Obstet Gynecol 2003;48:54-68.
- Vos RM, Krebbers SF, Verhoeven CH, et al. The in vivo human metabolism of tibolone. Drug Metab Dispos 2002;30:106-12.
- Blok LJ, De Ruiter PE, Kuhne EC, et al. Progestogenic effects of tibolone on human endometrial cancer cells. Clin Endocrinol Metab 2003;88:2327-34.
- Bodine PV, Harris HA, Lyttle CR, Komm BS. Estrogenic effects of 7alpha-methyl-17alpha-ethynylestradiol: a newly discovered tibolone metabolite. Steroids 2002;67:681-6.
- Kloosterboer HJ. Tibolone: a steroid with a tissue-specific mode of action. J Steroid Biochem Mol Biol 2001;76:231-8.
- Modelska K, Cummings S. Tibolone for Postmenopausal Women: Systematic Review of Randomized Trials. J Clin Endocrinol Metab 2002;87:16-23.
- Kicovic PJL, Cort_s-Prieto M, Milojevic S, Franchi F. Placebo-controlled cross-over study of effects of Org OD 14 in menopausal women. Reproduction 1982;6:81-91.
- Cittadini JB, Ben AR, Denari HJ, et al. Use of a new steroid (Org OD 14) in the climacteric syndrome. Reproduccion 1982;6:69-79.
- Genazzani AR, Petraglia F, Genazzani AD, et al. Effects of Org OD 14 on pituitary and peripheral _-endorphin in castrated rats and post-menopausal women. Maturitas 1987;Suppl. 1:35-48.
- Nevinny-Stickel J. Double-blind cross-over study with Org OD 14 and placebo in postmenopausal patients. Arch Gynecol 1983;234:27-31.
- Crona NGL, Samsioe UB, Silfverstolpe G. Treatment of climacteric complaints with Org OD 14: a comparative study with oestradiol valerate and placebo. Maturitas 1988;9:303-8.
- Bedenek-Jaszmann LJ Long-term placebo-controlled efficacy and safety study of ORG OD 14 in climacteric women. Maturitas 1987;Suppl. 1:25-33.
- Nathorst-Boos J, Hammar M. Effect on sexual life-a comparison between tibolone and a continuous estradiol-norethisterone acetate regimen. Maturitas 1997;26:15-20.
- Doren M, Ruebig A, Holzgreve W. Defferential effects on the androgen status of postmenopausal women treated with tibolone and continuous combined estradiol and norethindrone acetate replacement therapy. Fertil Steril 2001;75:554-8.
- Taskin O, Yalcinoglu AI, Kucuk S, et al. Effectiveness of tibolone on hypoestrogenic symptoms induced by goserelin treatment in patients with endometriosis. Fertil Steril 1997;67:40-45.
- Botsis D, Kassanos D, Kalogirou D, et al. Vaginal ultrasound of the endometrium in postmenopausal women with symptoms of urogenital atrophy on low dose oestrogen or tibolone treatment: a comparison. Maturitas 1997;26:57-62.
- Morris E, Wilson P, Robinson J, Rymer J. Long term effects of tibolone on the genital tract in postmenopausal women. Br J Obstet Gynaecol 1999;106: 954-9.
- Kokcu A, Cetinkaya MB, Yanik F, et al. The comparison of effects of tibolone and conjugated estrogen-medroxyprogesterone acetate therapy on sexual performance in postmenopausal women. Maturitas 2000;36:75-80.
- Mendoza N, Suarez AM, Alamo F, et al. Lipid effects, effectiveness and acceptability of tibolone versus transdermic 17 beta-estradiol for hormonal replacement therapy in women with surgical menopause. Maturitas 2000;37:37-43.
- Castelo-Branco C, Vicente JJ, Figueras F, et al. Comparative effects of estrogens plus androgens and tibolone on bone, lipid pattern and sexuality in postmenopausal women. Maturitas 2000;34:161-8.
- Huber J, Palacios S, Berglund L, et al. Effects of tibolone and continuous combined hormone replacement therapy on bleeding rates, quality of life and tolerability in postmenopausal women. BJOG 2002;109:886-93.
- Egarter C, Topcuoglu A, Vogl S, et al. Hormone replacement therapy with tibolone: effects on sexual functioning in postmenopausal women. Acta Obstet Gynecol Scand 2002;81:649-53.
- Davis S, Burger H. Use of androgens in postmenopausal women. Curr Opin Obstet Gynecol 1997; 9:177-80.
- Laan E, van Lunsen RH, Everaerd W. The effects of tibolone on vaginal blood flow, sexual desire and arousability in postmenopausal women. Climacteric 2001;4:28-41.
- Doren M, Rubig A, Coelingh Bennink HJ, et al. Differential effects on the androgen status of postmenopausal women treated with tibolone and continuous combined estradiol and norethindrone acetate replacement therapy. Fertil Steril 2001;75:554-9.
- Tang BLK, Markiewicz HJ, Gurpide E. Human endometrial 3_-hydroxysteroid dehydrogenase/isomerase can locally reduce intrinsic estrogenic/progestagenic activity ratios of a steroidal drug (Org OD 14). J Steroid Biochem Mol Biol 1993;45:345-51.
- Genazzani A, Benedek-Jaszmann DM, Andolsek L, et al. Org OD 14 and the endometrium. Maturitas 1991;13:243-51.
- Davis SR.The effects of tibolone on mood and libido. Menopause 2002;9:162-70.
- Hammar M, Christau J, Rud T, Garre K. A double-blind, randomised trial comparing the effects of tibolone and continuous combined hormone replacement therapy in postmenopausal women with menopausal symptoms. Br J Obstet Gynaecol 1998;105:904-11.
- Winkler U, Altkemper B, Helmond FA, et al. Effects of tibolone and continuous combined hormone replacement therapy on parameters in the clotting cascade: a multicenter, double-blind, randomized study. Fertil Steril 2000;74:10-9.
- Mendoza N, Pison JA, Fernandez M, et al. Prospective, randomised study with three HRT regimens in postmenopausal women with an intact uterus. Maturitas 2002;4:289-98.
- Bukulmez O, Al A, Gurdal H, et al. Short-term effects of three continuous hormone replacement therapy regimens on platelet tritiated imipramine binding and mood scores: a prospective randomized trial. Fertil Steril 2001;75:737-43.
- Fluck E, File SE, Rymer J. Cognitive effects of 10 years of hormone-replacement therapy with tibolone. J Clin Psychopharmacol 2002;22:62-7.
- Yazici K, Pata O, Yazici A, et al. [The effects of hormone replacement therapy in menopause on symptoms of anxiety and depression]. Turk Psikiyatri Derg 2003;14:101-5.
- Pan HA, Wang ST, Pai MC, et al. Cognitive function variations in postmenopausal women treated with continuous, combined HRT or tibolone. A comparison. J Reprod Med.2003;48:375-80.
- Lloyd G, McGing A, Patel N, et al. A randomised placebo controlled trial of the effects of tibolone on blood pressure and lipids in hypertensive women. J Hum Hypertension 2000;14:99-104.
- D_ren M, R_big HJ, Holzgreve W. Resistance of pelvic arteries and plasma lipids in postmenopausal women: comparative study of tibolone and continuous combined estradiol and norethindrone acetate replacement therapy. Am J Obstet Gynecol 2000 183:575-82.
- Bjarnason N, Bjarnason KH, Bennink HJ, Christiansen C. Tibolone: influence on markers of cardiovascular disease. J Clin Endocrinol Metab 1997;82:1752-6.
- Castelo-Branco C, Casals E, Figueras F, et al. Two-year prospective and comparative study on the effects of tibolone on lipid pattern, behavior of apolipoproteins AI and B. Menopause. 1999;6:92-7.
- von Eckardstein A, Crook D, Elbers J, et al. Tibolone lowers high density lipoprotein cholesterol by increasing hepatic lipase activity but does not impair cholesterol efflux. Clin Endocrinol (Oxf) 2003;58:49-58.
- Ginsburg J, Prelevic GM. Antiatherosclerotic effects of tibolone. Menopause 2001;8:79-80.
- Pan HA, Wang ST, Chen CH, et al. Flow resistance in carotid and middle cerebral arteries in postmenopausal women: a comparative study of tibolone and continuous combined hormone replacement therapy. Climacteric 2002;5:259-265.
- Register TC, Wagner JD, Zhang L, et al. Effects of tibolone and conventional hormone replacement therapies on arterial and hepatic cholesterol accumulation and on circulating endothelin-1, vascular cell adhesion molecule-1, and E-selectin in surgically menopausal monkeys. Menopause 2002;9:411-21.
- Cagnacci A, Mallus E, Tuveri F, et al. Effect of tibolone on glucose and lipid metabolism in postmenopausal women. J Clin Endocrinol Metab 1997;82:251-3.
- Haenggi W, Bersinger NA, Mueller MD, et al. Decrease of serum endothelin levels with postmenopausal hormone replacement therapy or tibolone. Gynecol Endocrinol 1999;13:202-5.
- Farish E, Barnes JF, Rolton HA, et al. Effects of tibolone on lipoprotein(a) and HDL subfractions. Maturitas 1994;20:215-9.
- Lloyd GW, Patel NR, McGing EA, et al. Acute effects of hormone replacement with tibolone on myocardial ischaemia in women with angina. Int J Clin Pract 1998;52:155-7.
- Canbaz M, Vural P, Akgul C. Effects of tibolone on thromboxane B(2) levels in postmenopausal women. Gynecol Obstet Invest 2002;53:13-5.
- Parkin D, Smith F, Lindsay R, Hart DM. Effects of long-term Org OD 14 administration on blood coagulation in climacteric women. Maturitas 1989;11:95-101.
- Cortes-Prieto J. Coagulation and fibrinolysis in post-menopausal women treated with Org OD 14. Maturitas 1987;Suppl. 1:67-72.
- Garnero P, Jamin C, Benhamou CL, et al. Effects of tibolone and combined 17bet-estradiol and norethisterone acetate on serum C-reactive protein in healthy post-menopausal women: a randomized trial. Hum Reprod 2002;17:2748-53.
- Celik H, Ayar A, Tug N, et al. Effects of tibolone on plasma homocysteine levels in postmenopausal women. Fertil Steril 2002;78:347-350.
- Manzella D, Fornaro F, Carbonella M, et al. Effect of tibolone administration on heart rate variability and free fatty acid levels in postmenopausal women. Fertil Steri. 2002;78:1005-9.
- de Kleijn MJ, Wilmink HW, Bots ML, et al. Hormone replacement therapy and endothelial function. Results of a randomized controlled trial in healthy postmenopausal women. Atherosclerosis 2001;159:357-65.
- Davis SR Menopause: new therapies. MJA 2003;178:634-7.
- Prelevic GM, Kwong P, Byrne DJ, et al. A cross-sectional study of the effects of hormone replacement therapy on the cardiovascular disease risk profile in healthy postmenopausal women. Fertil Steril 2002;77:945-51.
- Berning B, Kuijk JW, Bennink HJ, et al. Effects of two doses of tibolone on trabecular and cortical bone loss in early postmenopausal women: a two-year randomized, placebo-controlled study. Bone 1996;19:395-9.
- Bjarnason N, Bjarnason J, Rosenquist C, Christiansen C. Tibolone: prevention of bone loss in late postmenopausal women. J Clin Endocrinol Metab 1996;81:2419-22.
- Bjarnason N, Bjarnason C, Christiansen C. The response in spinal bone mass to tibolone treatment is related to bone turnover in elderly women. Bone 1997;20:151-5.
- Studd J, Arnala I, Kicovic PM, et al. A randomized study of tibolone on bone mineral density in osteoporotic postmenopausal women with previous fractures. Obstet Gynecol 1998;92:574-9.
- Milner M, Harrison RF, Gilligan, et al. Bone density changes during two years treatment with tibolone or conjugated estrogens and norgestrel, compared with untreated controls in postmenopausal women. Menopause 2000;7:327-33.
- Rymer J, Robinson J, Fogelman I. Effects of 8 years of treatment with tibolone 2.5 mg daily on postmenopausal bone loss. Osteoporos Int 2001;12:478-83.
- Fenkci V, Yilmazer M, Fenkci S. Effects of short-time (3 months) tibolone treatment on bone turnover in postmenopausal women. Arch Gynecol Obstet 2003;268:85-7.
- Lippuner K, Haenggi W, Birkhaeuser MH, et al. Prevention of postmenopausal bone loss using tibolone or conventional peroral or transdermal hormone replacement therapy with 17beta-estradiol and dydrogesterone. J Bone Miner Res 1997;12:806-12.
- Lamy O, Krieg MA. [Hormone replacement therapy and its derivatives in the prevention and treatment of osteoporosis]. Rev Med Suisse Romande 2002;122:377-81.
- Rymer J, Robinson J, Fogelman I. Ten years of treatment with tibolone 2.5 mg daily: effects on bone loss in postmenopausal women. Climacteric 2002;5:390-8.
- Gambacciani M, Ciaponi M. Postmenopausal osteoporosis management. Curr Opin Obstet Gynecol 2000;12:189-97.
- Lippuner K, Haenggi W, Birkhaeuser MH, et al. Prevention of postmenopausal bone loss using tibolone or conventional peroral or transdermal hormone replacement therapy with 17bet-estradiol and dydrogesterone. J Bone Miner Res 1997;12:806-12.
- Doren M, Nilsson J-A, Johnell O. Effects of specific post-menopausal hormone therapies on bone mineral density in post-menopausal women: a meta-analysis. Human Reproduction 2003;18:1737-46.
- Kloosterboer HJ, Ederveen AG. Pros and cons of existing treatment modalities in osteoporosis: a comparison between tibolone, SERMs and estrogen (+/-progestogen) treatments. J Steroid Biochem Mol Biol 2002;83:157-65.
- Fedele L, Bianchi S, Raffaelli R, et al. A randomized study of the effects of tibolone and transdermal estrogen replacement therapy in postmenopausal women with uterine myomas. Eur J Obstet Gynecol Reprod Biol 2000;88:91-4.
- Ginsburg J, Prelevic G, Butler D, et al. Clinical experience with tibolone (Livial) over 8 years. Maturitas 1995;21:71-76.
- Meuwissen JH, Wiegerinck MA, Haverkorn MJ. Regression of endometrial thickness in combination with reduced withdrawal bleeding as a progestational effect of tibolone in postmenopausal women on oestrogen replacement therapy. Maturitas 1995;21:121-5.
- Siseles NO, Halperin H, Benencia HJ, et al. A comparative study of two hormone replacement therapy regimens on safety and efficacy variables. Maturitas 1995;21:201-10.
- Rymer J, Chapman MG, Fogelman I, et al. A study of the effect of tibolone on the vagina in postmenopausal women. Maturitas 1994;18:127-33.
- Botsis D, Kassanos D, Kalogirou D, et al. Vaginal ultrasound of the endometrium in postmenopausal women with symptoms of urogenital atrophy on low-dose estrogen or tibolone treatment: a comparison. Maturitas 1997;26:57-62.
- Markiewicz L, Gurpide E. In vitro evaluation of estrogenic, estrogen antagonistic and progestagenic effects of a steroidal drug (Org OD-14) and its metabolites on human endometrium. J Steroid Biochem 1990;35:535-41.
- Egarter C, Sator M, Berghammer P, et al. Efficacy, tolerability, and rare side effects of tibolone treatment in postmenopausal women. Int J Gynaecol Obstet 1999;64:281-6.
- Volker W, Coelingh Bennink HJ, Helmond FA. Effects of tibolone on the endometrium. Climacteric 2001;4:203-8.
- Landgren MB, Bennink HJ, Helmond FA, et al. Dose-response analysis of effects of tibolone on climacteric symptoms. BJOG 2002;109:1109-14.
- Berning B, van Kuijk C, Benink HJ, et al. Absent correlation between vaginal bleeding and oestradiol levels or endometrial morphology during tibolone use in early postmenopausal women. Maturitas 2000;35:81-8.
- Chetrite G, Kloosterboer JR. Effect of tibolone (Org OD14) and its metabolites on estrone sulphatase activity in MCF-7 and T-47D mammary cancer cells. Anticancer Res 1997;17:135-40.
- Gompel A, Siromachkova A, Kloosterboer HJ, Rostene W. Tibolone actions on normal and breast cancer cells. Eur J Cancer 2000;36:S76-S77.
- Kloosterboer HJ. Endocrine prevention of breast: any role for tibolone? Eur J Cancer 2002;38(suppl 6):S24-S25.
- Bulbul NH, Ozden S, Dayicioglu V. Effects of hormone replacement therapy on mammographic findings. Arch Gynecol Obstet 2003;268:5-8.
- Prelevic GM, Beljic T, Balint-Peric L, et al. Metabolic effects of tibolone in postmenopausal women with non-insulin dependent diabetes mellitus. Maturitas 1998;28:271-6.
- Szanto F. [Tibolone therapy in postmenopausal women with a history of many risk factors]. Orv Hetil 2003;144:701-4.
