Револейд® (Revolade) инструкция по применению
📜 Инструкция по применению Револейд®
💊 Состав препарата Револейд®
✅ Применение препарата Револейд®
📅 Условия хранения Револейд®
⏳ Срок годности Револейд®
Описание лекарственного препарата
Револейд®
(Revolade)
Основано на листке-вкладыше препарата, утверждено компанией-производителем
и подготовлено для электронного издания справочника Видаль 2014 года.
Дата обновления: 2023.08.28
Владелец регистрационного удостоверения:
Код ATX:
B02BX05
(Элтромбопаг)
Лекарственные формы
| Револейд® |
Таб., покр. пленочной оболочкой, 25 мг: 28 шт. рег. №: ЛП-(001879)-(РГ-RU) |
|
|
Таб., покр. пленочной оболочкой, 50 мг: 28 шт. рег. №: ЛП-(001879)-(РГ-RU) |
Форма выпуска, упаковка и состав
препарата Револейд®
Таблетки, покрытые пленочной оболочкой белого цвета, круглые, двояковыпуклые, на одной стороне выгравировано «GS NX3» и «25».
Вспомогательные вещества: маннитол, целлюлоза микрокристаллическая РН101, повидон К30.
Экстрагрануловые компоненты: целлюлоза микрокристаллическая РН102, карбоксиметилкрахмал натрия (тип А), магния стеарат.
Состав пленочной оболочки: опадрай® белый YS-1-7706-G (гипромеллоза, титана диоксид Е171, макрогол-400, полисорбат 80).
7 шт. — блистеры (4) — пачки картонные.
Таблетки, покрытые пленочной оболочкой коричневого цвета, круглые, двояковыпуклые, на одной стороне выгравировано «GS UFU» и «50».
Вспомогательные вещества: маннитол, целлюлоза микрокристаллическая РН101, повидон К30.
Экстрагрануловые компоненты: целлюлоза микрокристаллическая РН102, карбоксиметилкрахмал натрия (тип А), магния стеарат.
Состав пленочной оболочки: опадрай® коричневый 03B26716 (гипромеллоза, титана диоксид Е171, макрогол-400, краситель железа оксид желтый Е172, краситель железа оксид красный Е172).
7 шт. — блистеры (4) — пачки картонные.
Фармакологическое действие
Стимулятор гемопоэза. Тромбопоэтин — это основной цитокин, который принимает участие в регуляции мегакариопоэза и выработке тромбоцитов. Он является эндогенным лигандом для рецептора тромбопоэтина. Элтромбопаг взаимодействует с трансмембранным доменом человеческого рецептора тромбопоэтина и инициирует каскад передачи сигнала, напоминающий таковой для эндогенного тромбопоэтина, что сопровождается индукцией пролиферации и дифференцировки мегакариоцитов из клеток-предшественников костного мозга.
Элтромбопаг отличается от тромбопоэтина с точки зрения влияния на агрегацию тромбоцитов. В отличие от тромбопоэтина, воздействие элтромбопага на тромбоциты здорового человека не усиливает агрегацию под действием аденозиндифосфата (АДФ) и не стимулирует экспрессию Р-селектина. Элтромбопаг не препятствует агрегации тромбоцитов под действием АДФ или коллагена.
Фармакокинетика
Параметры фармакокинетики элтромбопага после его введения пациентам с идиопатической тромбоцитопенической пурпурой (ИТП) представлены в таблице ниже.
Средние геометрические (доверительный интервал (ДИ) 95%) значения плазменных параметров фармакокинетики элтромбопага в равновесном состоянии у взрослых пациентов с ИТП
Данные зависимости концентрации элтромбопага в плазме крови от времени, полученные у 590 пациентов с вирусным гепатитом С (ВГС), включенных в исследования III фазы TPL103922/ENABLE 1 и TPL108390/ENABLE 2, были объединены с данными у пациентов с ВГС, включенных в исследование II фазы TPL102357, и здоровых взрослых добровольцев в группе для анализа фармакокинетики. Результаты измерений Cmax и AUC(0-t) элтромбопага для пациентов с ВГС, включенных в исследования III фазы, представлены в таблице для каждой исследуемой дозы. Наиболее высокую экспозицию элтромбопага наблюдали у пациентов с ВГС при назначаемых дозах элтромбопага (согласно таблице ниже).
Средние геометрические (ДИ 95%) значения стационарных параметров элтромбопага в плазме крови у пациентов с хроническим ВГС
Данные представлены в виде среднего геометрического (ДИ 95%). AUC (0-t) и Cmax основаны на вторичных оценках данных для каждого пациента из фармакокинетической группы в высокой дозе.
Всасывание
Элтромбопаг всасывается и достигает Cmax через 2-6 ч после приема внутрь. Совместный прием элтромбопага с антацидами и прочими продуктами, содержащими поливалентные катионы (например, молочные продукты и минеральные добавки), значительно снижает экспозицию элтромбопага.
Абсолютная биодоступность элтромбопага при приеме внутрь не была установлена. На основании показателей почечной экскреции препарата и анализа метаболитов, выводимых через кишечник, было показано, что расчетные значения всасывания производных препарата после введения его однократной дозы 75 мг составило, по меньшей мере, 52%.
Распределение
Связывание с белками плазмы человека высокое (>99.9%). Элтромбопаг является субстратом для BCRP (белок резистентного рака молочной железы), но не для Р-гликопротеина или ОАТР1В1.
Метаболизм
Всосавшийся элтромбопаг подвергается активному метаболизму. Метаболизируется преимущественно путем расщепления, окисления и конъюгации, с глюкуроновой кислотой, глутатионом или цистеином. По данным клинического исследования препарата, меченого радиоактивным изотопом, было показано, что на долю элтромбопага приходится около 64% радиоактивного изотопа углерода в плазме. Второстепенные метаболиты, на долю каждого из которых приходится менее 10% радиоактивности плазмы, образуются путем глюкуронидации и окисления.
Основываясь на исследовании меченого радиоактивным изотопом элтромбопага, было установлено, что примерно 20% дозы препарата метаболизируется путем окисления.
Исследования in vitro показали, что CYP1A2 и CYP2C8 являются изоферментами, отвечающими за окислительный метаболизм, тогда как уридиндифосфат-глюкуронилтрансферазы UGT1A1 и UGT1A3 — изоферментами, отвечающими за глюкуронизацию. В процессе расщепления могут принимать участие бактерии из нижних отделов ЖКТ.
Выведение
Преимущественным путем выведения элтромбопага является выделение через кишечник (59%); при этом 31% дозы обнаруживается в моче в виде метаболитов. Исходное вещество в моче отсутствует. В неизменном виде с калом выводится около 20% введенного препарата. T1/2 элтромбопага из плазмы составляет около 21-32 ч.
Фармакокинетика в особых клинических случаях
Фармакокинетика элтромбопага изучалась после назначения препарата взрослым пациентам с нарушением функций почек. После введения элтромбопага в однократной дозе 50 мг пациентам с легкими нарушениями функции почек AUC(0-∞)
элтромбопага уменьшалась на 32% (90% ДИ: 63% снижение и 26% повышение); пациентам с умеренными нарушениями функции почек — на 36% (90% ДИ:- 66% снижение и 19% повышение); пациентам с тяжелыми нарушениями функции почек — на 60% (90% ДИ: 18% снижение, 80% снижение) по сравнению со здоровыми добровольцами. У пациентов с нарушением функции почек отмечалась тенденция к снижению экспозиции элтромбопага в плазме, однако при сравнении таких пациентов и здоровых добровольцев была выявлена существенная вариабельность показателей экспозиции.
После введения внутрь элтромбопага в однократной дозе 50 мг пациентам с циррозом печени (нарушением функции печени) AUC(0-∞) элтромбопага увеличивалась на 41% (90% ДИ: 13% снижение и 128% увеличение); пациентам с умеренными нарушениями функции печени — на 93% (90% ДИ: 19% снижение и 213% увеличение); пациентам с тяжелыми поражениями функции печени — на 80% (90% ДИ: 11% снижение и 192% увеличение) по сравнению со здоровыми добровольцами. При сравнении таких пациентов и здоровых лиц была выявлена существенная вариабельность показателей экспозиции.
Влияние нарушения функции печени на фармакокинетику элтромбопага при повторном назначении препарата оценивалось посредством группового анализа фармакокинетики у 28 здоровых взрослых добровольцев и 79 пациентов с хроническими заболеваниями печени. Согласно результатам группового анализа фармакокинетики, у пациентов с циррозом печени (нарушением функции печени) отмечались более высокие плазменные показатели AUC(0-t) элтромбопага по сравнению с показателями здоровых добровольцев, при этом значения AUC(0-t) возрастали с повышением балловых показателей по шкале Чайлд-Пью. По сравнению со здоровыми добровольцами у пациентов с легкими нарушениями функции печени плазменные показатели AUC(0-t) элтромбопага были выше приблизительно на 87– 110%, а у пациентов с умеренными нарушениями функции печени — приблизительно на 141–240%.
Пациентам с ИТП и циррозом печени (нарушением функции печени) следует назначать элтромбопаг с осторожностью и при наличии постоянного наблюдения. У пациентов с хронической ИТП и легкими, умеренными и тяжелыми нарушениями функции печени терапию элтромбопагом следует начинать со сниженной дозы — 25 мг один раз в сутки.
Аналогичный анализ был проведен с участием 28 здоровых взрослых добровольцев и 635 пациентов с ВГС. У большинства пациентов показатель по шкале Чайлд-Пью составлял 5-6 баллов. По данным фармакокинетического анализа, пациенты с ВГС имели более высокие показатели AUC(0-t) элтромбопага по сравнению с показателями здоровых добровольцев, при этом значения AUC(0-t) возрастали с повышением балловых показателей по шкале Чайлд-Пью. По сравнению со здоровыми добровольцами у пациентов с ВГС плазменные показатели AUC(0-t) элтромбопага были выше приблизительно на 100–144%. У пациентов с ВГС терапию элтромбопагом следует начинать с дозы 25 мг один раз в сутки.
У пациентов восточно-азиатской расы фармакокинетику элтромбопага оценивали при помощи анализа популяционной фармакокинетики у 111 здоровых взрослых (31 — выходцы из Восточной Азии) и 88 пациентов с ИТП (18 — выходцы из Восточной Азии). На основании результатов фармакокинетического анализа у пациентов с ИТП восточноазиатского происхождения (т.е. японцы, китайцы, жители Тайваня и корейцы) показатели AUC(0-t) элтромбопага оказались примерно на 87% выше, чем у пациентов не восточноазиатского происхождения (преимущественно европеоидов); при этом коррекция дозы по массе тела не проводилась.
Изучение влияния этнической принадлежности к выходцам из Восточной Азии на фармакокинетику элтромбопага проводили с помощью популяционного анализа фармакокинетики с участием 635 пациентов с ВГС (145 пациентов восточноазиатского происхождения и 69 пациентов юго-восточноазиатского происхождения). На основании результатов популяционного анализа фармакокинетики установлено, что у пациентов восточноазиатского и юго-восточноазиатского происхождения наблюдалась сходная фармакокинетика элтромбопага. В среднем у пациентов восточноазиатского и южно-азиатского происхождения значения AUC(0-t) элтромбопага в плазме крови были примерно на 55% выше по сравнению с пациентами других рас (преимущественно европеоидной).
Влияние пола на фармакокинетику элтромбопага оценивали при помощи анализа популяционной фармакокинетики у 111 здоровых добровольцев (из них 14 — женского пола) и 88 пациентов с ИТП (из них 57 — женского пола). По данным популяционного фармакокинетического анализа, плазменный показатель AUC(0-t) элтромбопага у пациенток с ИТП оказался примерно на 50% выше по сравнению с пациентами мужского пола; при этом коррекция доз по массе тела не проводилась.
Влияние пола на фармакокинетику элтромбопага оценивали с помощью популяционного анализа фармакокинетики с участием 635 пациентов с ВГС (260 женщин). По результатам оценки с помощью модели у женщин с вирусом гепатита С значения AUC(0-t) элтромбопага в плазме крови были на 41% выше по сравнению с мужчинами.
Возрастные различия по фармакокинетике элтромбопага оценивали с помощью популяционного анализа фармакокинетики с участием 28 здоровых добровольцев и 635 пациентов с ВГС в возрасте от 19 до 74 лет. По результатам оценки с помощью модели у пожилых пациентов (> 60 лет) значения AUC(0-t) элтромбопага в плазме крови были на 36% выше по сравнению с более молодыми пациентами.
Показания препарата
Револейд®
- с целью уменьшения риска кровотечения при лечении тромбоцитопении у пациентов с хронической иммунной (идиопатической) тромбоцитопенической пурпурой (ИТП) при недостаточной эффективности кортикостероидов, иммуноглобулинов или спленэктомии;
- с целью обеспечения возможности проведения или оптимизации проводимой противовирусной терапии, включающей интерферон, при лечении тромбоцитопении у пациентов с хроническим вирусным гепатитом С (ВГС).
Режим дозирования
Режим дозирования устанавливается индивидуально на основании количества тромбоцитов.
У большинства пациентов повышение количества тромбоцитов происходит через 1–2 недели лечения.
Препарат Револейд следует принимать за четыре часа до или через четыре часа после приема антацидов, молочных продуктов или минеральных добавок, содержащих поливалентные катионы (например, алюминий, кальций, железо, магний, селен и цинк).
Препарат можно принимать с пищей, содержащей небольшое количество кальция (50 мг) либо, что предпочтительно, вовсе не содержащей кальций.
Взрослые
Пациенты с хронической иммунной (идиопатической) тромбоцитопенией
Для достижения и поддержания количества тромбоцитов ≥ 50 000/мкл необходимо использовать минимально эффективную дозу препарата Револейд. Подбор доз основан на изменении количества тромбоцитов. В клинических исследованиях повышение количества тромбоцитов наблюдалось в течение 1–2 недель после начала терапии препаратом Револейд и снижение происходило в течение 1–2 недель после прекращения приема препарата.
Первоначальный режим дозирования
Рекомендованная начальная доза препарата Револейд составляет 50 мг 1 раз/сут.
Для пациентов восточноазиатского происхождения (например, китайцев, японцев, жителей Тайваня, корейцев или тайцев) прием препарата Револейд следует начинать со сниженной дозы — 25 мг 1 раз/сут.
Мониторинг и коррекция дозы
После начальной терапии препаратом Револейд необходимо корректировать дозу для поддержания количества тромбоцитов ≥50 000/мкл, что необходимо для уменьшения риска кровотечения. Не следует превышать дозу 75 мг/сут.
Во время терапии препаратом Револейд следует регулярно контролировать гематологические показатели и показатели функции печени. Дозу элтромбопага следует корректировать в соответствии с Таблицей 1 в зависимости от количества тромбоцитов. Во время терапии элтромбопагом еженедельно необходимо проводить полный анализ крови до тех пор, пока не будет достигнуто стабильное содержание тромбоцитов ≥ 50 000/мкл, по крайней мере, в течение 4 недель. После стабилизации содержания тромбоцитов полный анализ крови необходимо проводить ежемесячно.
Следует использовать наименьшую дозу препарата, позволяющую поддерживать содержание тромбоцитов на необходимом с клинической точки зрения уровне.
Таблица 1. Коррекция дозы элтромбопага для пациентов с ИТР
Стандартная коррекция дозы в сторону снижения или повышения должна составлять 25 мг/сут. Однако у некоторых пациентов может потребоваться комбинация различных доз в разные дни.
После любой коррекции дозы препарата Револейд содержание тромбоцитов следует контролировать, по меньшей мере, еженедельно в течение 2-3 недель. Спустя, по меньшей мере, 2 недели следует оценить содержание тромбоцитов у пациентов для рассмотрения необходимости дальнейшей коррекции дозы.
У пациентов с циррозом печени (нарушением функции печени) повышать дозу следует не ранее чем через 3 недели.
Отмена препарата
Лечение препаратом Револейд следует прекратить, если содержание тромбоцитов не увеличивается до значения, достаточного для уменьшения риска кровотечений, после 4 недель терапии элтромбопагом в дозе 75 мг/сут.
Пациенты с хроническим ВГС, сопровождающимся тромбоцитопенией
При приеме препарата Револейд в сочетании с противовирусной терапией необходимо учитывать полную информацию о совместном медицинском применении этих препаратов.
Для поддержания и достижения необходимого количества тромбоцитов используют минимально эффективную дозу препарата необходимого для начала и оптимизации противовирусной терапии. Подбор доз основан на восстановлении количества тромбоцитов.
Препарат Револейд не используют для нормализации количества тромбоцитов. В клинических исследованиях повышение количества тромбоцитов наблюдалось в течение 1 недели после начала терапии препаратом Револейд.
Первоначальный режим дозирования
Начальная доза препарата Револейд составляет 25 мг 1 раз/сут. Не требуется коррекции дозы для пациентов с ВГС восточноазиатского происхождения (например, китайцев, японцев, жителей Тайваня, корейцев или тайцев) или пациентов с легким нарушением функции печени.
Мониторинг и подбор дозы
Дозу элтромбопага увеличивают на 25 мг каждые 2 недели до достижения содержания тромбоцитов в крови, оптимального для начала противовирусной терапии и в соответствии с Таблицей 2. Контролировать количество тромбоцитов необходимо каждую неделю в период начала противовирусной терапии.
Во время противовирусной терапии необходимо корректировать дозу элтромбопага таким образом, чтобы избежать снижения дозы пэгинтерферона. Количество тромбоцитов следует мониторировать еженедельно до достижения их стабильного уровня. В дальнейшем необходимо осуществлять мониторинг общего анализа крови, включая исследования количества тромбоцитов и мазок периферической крови. Не следует превышать дозу 100 мг/сут. Информацию о рекомендуемых дозах пэгинтерферона альфа и рибавирина получают из инструкции по применению этих препаратов.
Таблица 2. Коррекция дозы элтромбопага для пациентов с ВГС во время противовирусной терапии
*Для пациентов, которые принимают элтромбопаг 25 мг 1 раз/сут, следует рассмотреть вопрос о приеме дозы 12,5 мг 1 раз/сут или 25 мг через день.
Отмена препарата
У пациентов с ВГС генотипа 1/4/6, независимо от решения о продолжении терапии интерферонами, следует рассмотреть отмену элтромбопага в случае, если эффект от лечения противовирусными препаратами не достигнут через 12 недель. Следует прекратить лечение препаратом Револейд, если после 24–недельной терапии будет обнаружена РНК ВГС. После отмены противовирусной терапии следует прекратить применение препарата Револейд.
Следует прекратить применение препарата Револейд в случае чрезмерного повышения количества тромбоцитов, как описано в таблице 2, или клинически значимых отклонениях от нормы функциональных проб печени.
Дети
Безопасность и эффективность применения элтромбопага у детей не установлены.
Пациенты пожилого возраста
Имеются ограниченные данные по применению элтромбопага у пациентов в возрасте 65 лет и старше. В ходе клинических исследований элтромбопага не было отмечено клинически значимых различий безопасности препарата у пациентов в возрасте 65 лет и старше, по сравнению с более молодыми пациентами. Однако не исключена повышенная чувствительность к препарату у некоторых пациентов пожилого возраста.
Пациенты с нарушением функции печени
Необходимо соблюдать осторожность при назначении элтромбопага пациентам с ИТП и нарушением функции печени (индекс >5 по шкале Чайлд-Пью). Если использование элтромбопага у пациентов с ИТП, имеющих нарушение функции печени все же необходимо, рекомендуется начинать лечение элтромбопагом в дозе 25 мг 1 раз/сут.
Увеличить дозу препарата Револейд пациентам с печеночной недостаточностью следует не ранее чем через 3 нед после начала терапии.
У пациентов с хроническим ВГС и нарушением функций печени следует назначать препарат Револейд в дозе 25 мг 1 раз/сут.
Выходцы из Восточной Азии
У пациентов с ИТП восточноазиатского происхождения и их потомков (например, китайцев, японцев, жителей Тайваня, корейцев и тайцев) рекомендуется назначать препарат в сниженной начальной дозе 25 мг 1 раз/сут.
Пациентам с тромбоцитопенией и хроническим ВГС восточноазиатского происхождения следует начинать лечение элтромбопагом в дозе 25 мг 1 раз/сут.
Необходимо продолжать осуществлять мониторинг содержания тромбоцитов у пациентов.
У пациентов с ИТП или ВГС восточноазиатского происхождения с нарушением функции печени, следует начинать лечение элтромбопагом с дозы 25 мг 1 раз/сут.
Побочное действие
Безопасность и эффективность элтромбопага была показана в ходе 2 двойных слепых рандомизированных плацебо-контролируемых исследований у взрослых пациентов с хронической ИТП, ранее получавших лечение.
Исследования ENABLE 1 (TPL103922 N=716) и ENABLE 2 (TPL108390 N=805) были рандомизированными, двойными слепыми, плацебо-контролируемыми, многоцентровыми исследованиями для оценки эффективности и безопасности применения элтромбопага у пациентов с тромбоцитопенией и вирусным гепатитом С, которым показана противовирусная терапия.
В исследованиях пациентов с ВГС выборка для оценки безопасности состояла из всех рандомизированных пациентов, которые получали исследуемый препарат согласно двойному слепому методу в части 2 исследований ENABLE 1 (группа лечения элтромбопагом N=449, плацебо N=232) и ENABLE 2 (группа лечения элтромбопагом n=506, плацебо n=252).
Пациентов анализировали в соответствии с получаемой терапией элтромбопагом (общая выборка для оценки безопасности согласно двойному слепому методу, группа лечения элтромбопагом n=955 и плацебо n=484).
Большинство нежелательных реакций, связанных с элтромбопагом, имели легкую или умеренную выраженность, раннее начало, и в редких случаях служили причиной для изменения лечения.
Определение частоты побочных реакций: очень часто (≥1/10), часто (≥1/100 и <1/10), нечасто (≥1/1000 и <1/100), редко (≥1/10 000 и <1/1000), очень редко (<1/10 000, включая отдельные случаи).
Нежелательные явления у пациентов с хронической ИТП
Инфекции и инвазии: часто — фарингит, инфекции мочевыводящих путей.
Со стороны пищеварительной системы: очень часто — тошнота, диарея; часто — сухость во рту, рвота.
Со стороны печени и желчевыводящих путей: часто — повышение активности АСТ, АЛТ.
Дерматологические реакции: часто — алопеция, сыпь.
Со стороны костно-мышечной системы: часто — боль в спине, боль в грудной клетке костно-мышечного характера, костно-мышечная боль, миалгия.
Нежелательные явления у пациентов с хроническим вирусным гепатита С
Со стороны системы кроветворения: очень часто — анемия.
Со стороны обмена веществ: очень часто — понижение аппетита.
Со стороны ЦНС: очень часто — бессонница, головная боль.
Со стороны дыхательной системы: очень часто — кашель.
Со стороны пищеварительной системы: очень часто — тошнота, диарея.
Со стороны печени и желчевыводящих путей: часто — гипербилирубинемия.
Дерматологические реакции: очень часто — зуд, алопеция.
Со стороны костно-мышечной системы: очень часто — миалгии.
Прочие: очень часто — утомляемость, гипертермия, лихорадка, астения, периферический отек, гриппоподобное заболевание.
Противопоказания к применению
Нет известных противопоказаний для применения препарата по показаниям в рекомендуемых дозах.
С осторожностью следует применять препарат у пациентов с нарушением функции почек, печени, при наличии факторов риска тромбоэмболии (например, дефицит V фактора Лейдена, антитромбина III, антифосфолипидный синдром), при беременности, в период лактации.
Препарат Револейд не рекомендуется применять у пациентов с печеночной недостаточностью ≥5 баллов по шкале Чайлд-Пью, если ожидаемая польза не превышает риск тромбоза воротной вены. В случае, если лечение целесообразно, следует проявлять осторожность при применении препарата Револейд у пациентов с печеночной недостаточностью.
Применение при беременности и кормлении грудью
Данных об эффективности и безопасности элтромбопага при беременности не имеется.
Применение препарата при беременности возможно только в том случае, когда предполагаемая польза для матери превосходит потенциальный риск для плода.
Неизвестно, выделяется ли элтромбопаг с грудным молоком. В период грудного вскармливания лечение элтромбопагом не рекомендуется, за исключением случаев, когда ожидаемая польза терапии для матери превышает потенциальный риск для грудного ребенка.
Применение при нарушениях функции печени
С осторожностью следует применять препарат у пациентов с нарушением функции печени.
Применение при нарушениях функции почек
С осторожностью следует применять препарат у пациентов с нарушением функции почек.
Применение у детей
Безопасность и эффективность применения элтромбопага у детей не установлены.
Применение у пожилых пациентов
Имеются ограниченные данные по применению элтромбопага у пациентов в возрасте 65 лет и старше. В ходе клинических исследований элтромбопага не было отмечено клинически значимых различий безопасности препарата у пациентов в возрасте 65 лет и старше, по сравнению с более молодыми пациентами. Однако не исключена повышенная чувствительность к препарату у некоторых пациентов пожилого возраста.
Особые указания
Эффективность и безопасность применения элтромбопага для лечения других заболеваний и состояний, сопровождающихся тромбоцитопенией, включая тромбоцитопению после химиотерапии и миелодиспластические синдромы, в настоящее время не установлены.
Нарушения функции печени
При применении элтромбопага возможны нарушения лабораторных показателей функции печени. В клинических исследованиях отмечено повышение активности АЛТ, ACT и концентрации непрямого билирубина. Эти явления носили по большей части легкий (1-2-й степени) и обратимый характер без клинически значимых симптомов, которые бы свидетельствовали о нарушении функции печени. По данным 2 плацебо-контролируемых исследований нежелательные явления в виде повышения активности АЛТ были отмечены у 5.7% и 4% пациентов, получавших лечение элтромбопагом и плацебо соответственно.
В 2-х контролируемых клинических исследованиях с участием пациентов с тромбоцитопенией и ВГС были зарегистрированы случаи ≥3-кратного увеличения значения верхней границы нормы (ВГН) АЛТ или АСТ в 34% и 38% при приеме в группе элтромбопага и в группе плацебо, соответственно. Назначение элтромбопага в комбинации с пэгинтерфероном/рибавирином было косвенно связанно с гипербилирубинемией. Были зарегистрированы случаи ≥1.5-кратного увеличения общего билирубина выше значения ВГН в 76% и 50% при приеме в группе элтромбопага и в группе плацебо, соответственно.
Активность АЛТ, ACT и концентрацию билирубина в сыворотке необходимо оценить до начала лечения элтромбопагом, затем контролировать каждые 2 недели во время титрования дозы, а также ежемесячно после назначения стабильной дозы. Повторное исследование после выявления нарушений функциональных тестов печени проводят в течение 3-5 дней. Если сывороточная концентрация общего билирубина увеличена, следует определить концентрации его отдельных фракций. В случае подтверждения отклонения мониторинг продолжают до момента стабилизации показателей, либо возвращения показателей к исходному уровню.
Лечение элтромбопагом прекращают в случае увеличения активности АЛТ при ≥3-кратном повышении значения ВГН у пациентов с нормальной функцией печени или ≥3-кратном увеличении относительно исходного уровня у пациентов с повышенной активностью АЛТ до начала лечения и следующих признаков:
- прогрессирование отклонения, либо
- сохранение отклонения ≥4 недель, либо
- его сочетание с повышением концентрации прямого билирубина, либо
- его сочетание с клиническими симптомами поражения печени или признаками декомпенсации функции печени.
У пациентов с ИТП и заболеваниями печени элтромбопаг следует назначать с осторожностью. Необходимо использовать минимальную начальную дозу элтромбопага при назначении пациентам с печеночной недостаточностью.
Декомпенсация функции печени (применение с интерферонами)
У пациентов с хроническим ВГС и циррозом печени при лечении интерферонами альфа может существовать риск декомпенсации функции печени, в некоторых случаях с летальным исходом. В двух контролируемых клинических исследованиях с участием пациентов с тромбоцитопенией и ВГС, в которых элтромбопаг использовали по мере необходимости для достижения целевого количества тромбоцитов, необходимого для проведения противовирусной терапии, о результатах по безопасности, свидетельствующих о декомпенсации функции печени, чаще сообщали в группе элтромбопага (13%), чем в группе плацебо (7%). У пациентов с низким уровнем альбумина (<3.5 г/дл) или баллом ≥10 по шкале MELD (модель конечной стадии заболевания печени) на исходном уровне был более высокий риск декомпенсации функции печени. Пациентов с такими характеристиками следует тщательно наблюдать на наличие признаков и симптомов декомпенсации печеночной недостаточности. Для получения информации о критериях отмены используется инструкция по применению соответствующих препаратов интерферона. Прием препарата Револейд следует прекратить, если противовирусную терапию отменили в связи с декомпенсацией печеночной недостаточности.
Тромботические и/или тромбоэмболические осложнения
Содержание тромбоцитов выше нормы представляет теоретический риск тромботических и/или тромбоэмболических осложнений. В клинических исследованиях элтромбопага у пациентов с ИТП тромбоэмболические осложнения наблюдались при низком и нормальном содержании тромбоцитов.
Пациентам с известными факторами риска тромботических и/или тромбоэмболических осложнений (таких как мутация V фактора Лейдена, дефицит антитромбина III, антифосфолипидный синдром и др.) требуется особый контроль при назначении элтромбопага.
Следует тщательно контролировать содержание тромбоцитов и рассмотреть вопрос о снижении дозы или отмене элтромбопага, если содержание тромбоцитов превышает целевые значения.
При исследованиях ИТП у 17 из 446 пациентов (3.8%) был отмечен 21 тромботический и/или тромбоэмболический эпизод. Тромбоэмболии включали: эмболию, в т.ч. легочную эмболию, тромбоз глубоких вен, транзиторные ишемические атаки, инфаркт миокарда, ишемический инсульт и заподозренный пролонгированный обратимый ишемический неврологический дефицит.
В двух контролируемых исследованиях с участием пациентов с тромбоцитопенией и ВГС, получавших терапию интерфероном, у 31 из 955 пациентов (3%), получавших элтромбопаг, и у 5 из 484 пациентов (1%), получавших плацебо отмечались тромботические и/или тромбоэмболические осложнения. Тромбоз воротной вены был наиболее распространенным из тромботических и/или тромбоэмболических осложнений в обеих группах (у 1% пациентов, получавших элтромбопаг и 1% пациентов, получавших плацебо). Временной связи между началом лечения и развитием тромботических и/или тромбоэмболических осложнений не наблюдалось. Большинство случаев тромботических и/или тромбоэмболических осложнений не привело к прекращению противовирусной терапии.
В контролируемом исследовании с участием пациентов с тромбоцитопенией и хроническими заболеваниями печени (n=288), перенесших элективные инвазивные вмешательства, риск тромбоза в системе воротной вены был повышен у пациентов, получавших элтромбопаг в дозе 75 мг 1 раз/сут в течение 14 дней. Было отмечено 6 эпизодов тромбоэмболии (все — в системе воротной вены) в группе пациентов, получавших элтромбопаг, и 2 — в группе плацебо (первый — в системе воротной вены, второй — инфаркт миокарда).
Препарат Револейд не следует применять для лечения тромбоцитопении у пациентов с хроническим заболеванием печени в рамках подготовки к инвазивным процедурам.
Кровотечение после прекращения лечения элтромбопагом
После прекращения лечения элтромбопагом у большинства пациентов содержание тромбоцитов в течение 2 недель возвращается к исходному значению, что повышает риск развития кровотечения, а в некоторых случаях может вызвать кровотечение. Содержание тромбоцитов следует еженедельно контролировать на протяжении 4 недель после отмены элтромбопага.
Образование ретикулина в костном мозге и риск фиброза костного мозга
Агонисты рецептора тромбопоэтина, включая элтромбопаг, могут повышать риск образования или разрастания ретикулиновых волокон в костном мозге. Перед началом лечения элтромбопагом следует оценить мазки периферической крови для определения исходного уровня морфологических изменений клеток. После достижения стабильной дозы элтромбопага ежемесячно выполняют общий клинический анализ крови с подсчетом лейкоцитарной формулы. При выявлении незрелых или диспластических клеток следует провести исследование мазка периферической крови на предмет появления новых, либо усиления существующих морфологических изменений (например, появления каплевидных и ядерных эритроцитов, незрелых лейкоцитов), либо выявления цитопении. При появлении у пациента новых, либо усилении существующих морфологических отклонений или цитопении следует прекратить лечение элтромбопагом и рассмотреть вопрос о биопсии костного мозга, включая окраску мазка с целью выявления фиброза.
Злокачественные новообразования и прогрессирование злокачественных новообразований
Существует теоретическая возможность того, что агонисты рецептора тромбопоэтина способны стимулировать прогрессирование существующих гематологических новообразований, например, миелодиспластического синдрома. В ходе клинических исследований не было показано различий в частоте злокачественных новообразований или злокачественных новообразований крови между пациентами, получавшими плацебо, и пациентами, получавшими элтромбопаг.
Катаракта
В токсикологических исследованиях элтромбопага у грызунов выявлялась катаракта. Клиническое значение этих данных неизвестно. Рекомендуется плановый контроль пациентов на предмет развития катаракты.
В контролируемых исследованиях с участием пациентов с тромбоцитопенией и ВГС, которые получали лечение на основе интерферонов (n=1439), сообщали о прогрессировании катаракты, существовавшей исходно, или о появлении катаракты у 8% в группе элтромбопага и 5% в группе плацебо.
Влияние на способность к управлению транспортными средствами и механизмами
Исследования по влиянию элтромбопага на способность к управлению автотранспортом или работе с механизмами не проводились. На основании фармакологических свойств элтромбопага отрицательное влияние на такие виды деятельности не ожидается. Однако при оценке способности пациента выполнять действия, которые требуют быстроты мышления, двигательных и познавательных навыков, следует учитывать клиническое состояние пациента и профиль нежелательных эффектов элтромбопага.
Передозировка
В ходе клинических исследований зарегистрирован один случай передозировки, когда пациент принял внутрь 500 мг элтромбопага.
Симптомы: нераспространенная сыпь, преходящая брадикардия, утомляемость, в повышение активности трансаминаз. Данные изменения были обратимыми. Возможно значительное увеличение содержания тромбоцитов, которое может привести к тромботическим и/или тромбоэмболическим осложнениям.
Лечение: следует рассмотреть вопрос о приеме внутрь препаратов, содержащих катионы металлов, например, кальция, алюминия или магния, для уменьшения всасывания элтромбопага. Следует тщательно контролировать содержание тромбоцитов. Лечение элтромбопагом возобновляют в соответствии с рекомендациями по режиму дозирования.
Поскольку почечная экскреция не является основным путем выведения элтромбопага, который активно связывается с белками плазмы крови, вероятнее всего, гемодиализ не является эффективным методом существенного ускорения выведения элтромбопага из организма.
Лекарственное взаимодействие
Розувастатин: исследования in vitro показали, что элтромбопаг не является субстратом для транспортного полипептида органических анионов OATP1B1, но выступает в роли ингибитора этого транспортировщика. Результаты исследований in vitro также позволили установить, что элтромбопаг является субстратом и ингибитором BСRP. При совместном применении элтромбопага и розувастатина в рамках клинического исследования лекарственного взаимодействия наблюдали повышение концентрации розувастатина в плазме крови. При совместном применении с элтромбопагом следует рассмотреть вопрос о снижении дозы розувастатина, a также проводить тщательный мониторинг. В клинических исследованиях элтромбопага при сопутствующей терапии розувастатином было рекомендовано снижение дозы последнего на 50%. Совместное применение элтромбопага и прочих субстратов полипептидных транспортеров органических анионов (OATP1B1) и BCRP требует осторожности.
Поливалентные катионы (образование хелатных комплексов): во избежание значительного снижения всасывания элтромбопага препарат следует принимать, по меньшей мере, за 4 ч до или после приема антацидов, молочных продуктов и прочих веществ, содержащих поливалентные катионы (например, минеральных добавок, содержащих алюминий, кальций, железо, магний, селен и цинк).
Взаимодействие с пищей: введение однократной дозы элтромбопага 50 мг со стандартным высококалорийным завтраком, содержащим большое количество жира и молочные продукты, снижает показатель площади под фармакокинетической кривой AUC(0-∞) на 59% (90% ДИ: 54%, 64%) и Cmax на 65% (90% ДИ: 59%, 70%).Пища с небольшим содержанием кальция (<50 мг кальция), включающая фрукты, постную ветчину, говядину, фруктовый сок, соевое молоко и крупу без добавок кальция, железа и магния, не оказывает существенного влияния на плазменную экспозицию элтромбопага вне зависимости от калорийности и содержания жира в пище.
Комбинация лопинавир/ритонавир (LPV/RTV): одновременное применение элтромбопага и LPV/RTV может привести к снижению концентрации элтромбопага. В исследовании с участием 40 здоровых добровольцев было установлено, что одновременное однократное применение элтромбопага в дозе 100 мг и многократное применение LPV/RTV в дозе 400 мг/100 мг два раза в сутки приводило к снижению значения AUC(0-∞) элтромбопага в плазме крови на 17% (90% ДИ: 6.6 %, 26.6%). Следовательно, при одновременном применении элтромбопага и LPV/RTV необходимо проявлять повышенную осторожность. Следует тщательно контролировать количество тромбоцитов для обеспечения соответствующей дозы элтромбопага при назначении или прекращении терапии LPV/RTV.
Условия хранения препарата Револейд®
Препарат следует хранить в недоступном для детей месте при температуре не выше 30°С.
Срок годности препарата Револейд®
Условия реализации
Препарат отпускается по рецепту.
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Взаимодействие с другими препаратами
Антигриппин Аптекарс…
(ФармФирма Сотекс, Россия)
Антигриппин-максимум
(АнвиЛаб, Россия)
Гастал Ликво
(Teva Pharmaceutical Industries, Израиль)
Изжогофф®
(ЭВАЛАР, Россия)
Кальций Сандоз® Форте
(SANDOZ, Словения)
Компливит® Триместрум 3 триместр
(ОТИСИФАРМ, Россия)
Компливит®-Актив
(ФАРМСТАНДАРТ-УфаВИТА, Россия)
Лавита®
(ВАЛЕНТА ФАРМАЦЕВТИКА, Россия)
Пентанов® Плюс
(ОТИСИФАРМ, Россия)
Флюкомп® Экстратаб
(ФП ОБОЛЕНСКОЕ, Россия)
Все взаимодействия
Описание препарата Револейд® (таблетки, покрытые пленочной оболочкой, 25 мг) основано на официальной инструкции, утверждено компанией-производителем в 2011 году
Дата согласования: 30.08.2011
Особые отметки:
Содержание
- Действующее вещество
- ATX
- Фармакологическая группа
- Нозологическая классификация (МКБ-10)
- Состав и форма выпускa
- Описание лекарственной формы
- Фармакологическое действие
- Фармакодинамика
- Фармакокинетика
- Показания
- Противопоказания
- Применение при беременности и кормлении грудью
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Передозировка
- Особые указания
- Комментарий
- Условия отпуска из аптек
- Условия хранения
- Срок годности
Действующее вещество
ATX
Фармакологическая группа
Состав и форма выпускa
| Таблетки, покрытые пленочной оболочкой | 1 табл. |
| активное вещество: | |
| элтромбопаг оламина измельченный | 31,9 мг (в пересчете на элтромбопаг 25 мг) |
| 63,8 мг (в пересчете на элтромбопаг 50 мг) | |
| вспомогательные вещества: маннитол; МКЦ; повидон К30; карбоксиметилкрахмал натрия (тип А); магния стеарат; Опадрай® белый YS-1-7706-G (таблетки дозировкой 25 мг); Opadry® коричневый 03В26716 (таблетки дозировкой 50 мг) |
в контурной ячейковой упаковке 7 шт.; в пачке картонной 2 или 4 упаковки.
Описание лекарственной формы
Таблетки, покрытые пленочной оболочкой, дозировкой 25 мг: круглые, двояковыпуклые, белого цвета. На одной стороне таблетки выгравировано «GS NX3» и «25».
Таблетки, покрытые пленочной оболочкой, дозировкой 50 мг: круглые, двояковыпуклые, коричневого цвета. На одной стороне таблетки выгравировано «GS UFU» и «50».
Фармакологическое действие
Фармакологическое действие
—
гемопоэтическое, гемостатическое.
Фармакодинамика
Тромбопоэтин (ТРО) — это основной цитокин, который принимает участие в регуляции мегакариопоэза и выработке тромбоцитов; он является эндогенным лигандом для рецептора тромбопоэтина (TPO-R). Элтромбопаг взаимодействует с трансмембранным доменом человеческого рецептора TPO-R и инициирует каскад передачи сигнала, напоминающий таковой для эндогенного ТРО, что сопровождается индукцией пролиферации и дифференцировки мегакариоцитов из клеток-предшественников костного мозга.
Элтромбопаг отличается от ТРО с точки зрения эффектов на агрегацию тромбоцитов. В отличие от ТРО, воздействие элтромбопага на тромбоциты здорового человека не усиливает агрегацию под действием АДФ и не стимулирует экспрессию Р-селектина. Элтромбопаг не препятствует агрегации тромбоцитов под действием АДФ или коллагена.
Фармакокинетика
Параметры фармакокинетики элтромбопага после его введения пациентам с идиопатической тромбоцитопенической пурпурой (ИТП) представлены в таблице ниже.
Средние геометрические (доверительный интервал (ДИ) 95%) значения плазменных параметров фармакокинетики элтромбопага в равновесном состоянии у взрослых пациентов с идиопатической тромбоцитопенической пурпурой
| Схема лечения элтромбопагом | Cmax, мкг/мл | AUCo-t, мкг?ч/мл |
| 50 мг 1 раз в день (n=34) | 8,01 (6,73; 9,53) | 108 (88; 134) |
| 75 мг 1 раз в день (n=26) | 12,7 (11; 14,5) | 168 (143; 198) |
Всасывание и биодоступность. Элтромбопаг всасывается с достижением Cmax через 2–6 ч после приема внутрь. Совместный прием элтромбопага с антацидами и прочими продуктами, содержащими поливалентные катионы (например молочные продукты и минеральные добавки), значительно снижает экспозицию элтромбопага.
Абсолютная биодоступность элтромбопага при приеме внутрь не была установлена. На основании почечной экскреции препарата и анализе метаболитов, выводимых с калом, было показано, что всасывание связанных с препаратом продуктов после введения его однократной дозы 75 мг составило, по меньшей мере, 52%.
Распределение. Элтромбопаг активно связывается с белками плазмы человека (>99,9%). Элтромбопаг является субстратом для белка резистентности рака молочной железы (BCRP), но не для Р-гликопротеина или полипептидных транспортеров органических анионов (ОАТР1В1).
Метаболизм. Элтромбопаг преимущественно метаболизируется посредством расщепления, окисления и конъюгации с глюкуроновой кислотой, глутатионом или цистеином. По данным исследования у человека, с препаратом, меченым радиоактивным изотопом, было показано, что на долю элтромбопага приходится около 64% радиоактивного изотопа углерода в плазме. Второстепенные метаболиты, на долю каждого из которых приходится менее 10% радиоактивности плазмы, образуются путем глюкуронидации и окисления.
Основываясь на исследовании меченого радиоактивным изотопом элтромбопага, было установлено, что примерно 20% дозы препарата метаболизируется путем окисления.
Исследования in vitro показали, что CYP1A2 и CYP2C8 являются изоферментами, отвечающими за окислительный метаболизм, тогда как UGT1A1 и UGT1A3 — изоферментами, отвечающими за глюкуронидацию. В процессе расщепления могут принимать участие бактерии из нижних отделов ЖКТ.
Выведение. Всосавшийся элтромбопаг подвергается активному метаболизму. Преимущественным путем выведения элтромбопага является выделение с каловыми массами (59%); при этом 31% дозы обнаруживается в моче в виде метаболитов. Исходное вещество в моче отсутствует. В неизмененном виде с калом выводится около 20% введенного препарата. T1/2 элтромбопага из плазмы — около 21–32 ч.
Особые группы пациентов
Пациенты с нарушением функции почек. Фармакокинетика элтромбопага изучалась после назначения элтромбопага взрослым пациентам с нарушением функции почек. После введения однократной дозы элтромбопага 50 мг пациентам с легкими нарушениями функции почек AUCo-? элтромбопага снижалась на 32% (ДИ 90%: 63% снижение и 26% повышение); пациентам с умеренными нарушениями функции почек — на 36% (ДИ 90%: 66% снижение и 19% повышение); пациентам с тяжелыми нарушениями функции почек — на 60% (ДИ 90%: 18% снижение, 80% снижение) по сравнению со здоровыми добровольцами. У пациентов с нарушением функции почек отмечалась тенденция к снижению экспозиции элтромбопага в плазме, однако при сравнении таких пациентов и здоровых лиц была выявлена существенная вариабельность показателей экспозиции.
Пациенты с нарушением функции печени. После введения внутрь однократной дозы элтромбопага 50 мг пациентам с легкими нарушениями функции печени AUCo-? элтромбопага увеличивалась на 41% (ДИ 90%: 13% снижение, 128% увеличение); пациентам с умеренными нарушениями функции печени — на 93% (ДИ 90%: 19 и 213%); пациентам с тяжелыми поражениями функции печени — на 80% (ДИ 90%: 11 и 192%) по сравнению со здоровыми добровольцами. При сравнении таких пациентов и здоровых лиц была выявлена существенная вариабельность показателей экспозиции.
Раса. Влияние восточно-азиатской расы на фармакокинетику элтромбопага оценивали при помощи анализа популяционной фармакокинетики у 111 здоровых взрослых (31 — выходцы из Восточной Азии) и 88 пациентов с ИТП (18 — выходцы из Восточной Азии). На основании результатов фармакокинетического анализа у пациентов с ИТП восточно-азиатского происхождения (т.е. японцы, китайцы, жители Тайваня и корейцы) показатели AUCo-t элтромбопага оказались примерно на 87% выше, чем у пациентов невосточно-азиатского происхождения (преимущественно европеоидов); при этом коррекция доз по массе тела не проводилась.
Пол. Влияние пола на фармакокинетику элтромбопага оценивали при помощи анализа популяционной фармакокинетики у 111 здоровых взрослых субъектов (14 женщин) и 88 пациентов с ИТП (57 женщин). На основании показателей популяционного фармакокинетического анализа плазменный показатель AUCo-t элтромбопага у пациенток с ИТП оказался примерно на 50% выше по сравнению с пациентами мужского пола; при этом коррекция по массе тела не проводилась.
Показания
- тромбоцитопения у пациентов с хронической ИТП, у которых отмечался недостаточный ответ на кортикостероиды, иммуноглобулины и/или спленэктомию. Препарат Револейд назначается этим пациентам с целью уменьшения риска кровотечений.
Противопоказания
Неизвестны.
С осторожностью: нарушение функции почек, печени; период беременности; период лактации; факторы риска тромбоэмболии (например дефицит фактора V Лейдена, антитромбина III, антифосфолипидный синдром).
Применение при беременности и кормлении грудью
Эффекты элтромбопага у беременных неизвестны.
Элтромбопаг должен применяться во время беременности лишь в том случае, если ожидаемая польза для матери превышает все потенциальные риски для плода.
Неизвестно, выделяется ли элтромбопаг с грудным молоком.
Лечение элтромбопагом не рекомендовано женщинам в период лактации, за исключением тех случаев, когда ожидаемая польза для матери превышает все потенциальные риски для ребенка.
Способ применения и дозы
Реклама: ООО «РЛС-Патент», ИНН 5044031277, erid=4CQwVszH9pUkpHxmQQo
Реклама: ООО «РЛС-Патент», ИНН 5044031277, erid=4CQwVszH9pUkpHxmQQo
Внутрь, по меньшей мере, за 4 ч до или через 4 ч после приема антацидов, молочных продуктов или минеральных добавок, содержащих поливалентные катионы (например алюминий, кальций, железо, магний, селен и цинк).
Препарат Револейд можно принимать с пищей, содержащей небольшое количество кальция (<50 мг) либо, что предпочтительно, вовсе не содержащей кальций.
Режим дозирования препарата Револейд назначается индивидуально на основании количества тромбоцитов.
Для поддержания необходимого с клинической точки зрения количества тромбоцитов используют минимально эффективную дозу препарата.
У большинства пациентов повышение количества тромбоцитов происходит через 1–2 нед лечения.
Взрослые. Рекомендованная начальная доза — 50 мг 1 раз в сутки. Если по истечении 2–3 нед начальной терапии количество тромбоцитов ниже уровня, необходимого с клинической точки зрения (т.е. 50000/мкл), дозу можно увеличить до максимальной — 75 мг 1 раз в сутки. Стандартная коррекция дозы в сторону снижения или повышения должна составлять 25 мг в день. Однако у некоторых пациентов может потребоваться комбинация различных дозировок в разные дни.
После любой коррекции дозы препарата Револейд количество тромбоцитов следует контролировать, по меньшей мере, еженедельно на протяжении 2–3 нед. Ожидать ответа со стороны уровня тромбоцитов пациента следует, по меньшей мере, 2 нед после коррекции дозы.
При уровне тромбоцитов 200000–400000/мкл рекомендуется снизить дозу препарата Револейд.
Лечение препаратом Револейд следует приостановить, если количество тромбоцитов превысило 400000/мкл. При уменьшении количества тромбоцитов менее 150000/мкл следует возобновить лечение в редуцированной суточной дозе.
Особые группы пациентов
Дети. Безопасность и эффективность применения элтромбопага у детей не установлены.
Пожилые пациенты. Имеются ограниченные данные по применению элтромбопага у пациентов в возрасте 65 лет и старше. В ходе клинических исследований элтромбопага не было отмечено клинически значимых различий безопасности препарата у пациентов в возрасте 65 лет и старше по сравнению с более молодыми пациентами. Однако не исключена повышенная чувствительность к препарату у некоторых пожилых пациентов.
Выходцы из Восточной Азии. У пациентов — жителей и выходцев из Восточной Азии и их потомков (например китайцев, японцев, жителей Тайваня и корейцев) — рекомендуется назначать препарат в сниженной начальной дозе 25 мг 1 раз в сутки. Необходимо осуществлять подсчет количества тромбоцитов пациента. Допускается использовать стандартные критерии и рекомендации для дальнейшей коррекции дозы.
Побочные действия
Клинические исследования
Безопасность и эффективность элтромбопага была показана в ходе двух двойных слепых рандомизированных плацебо-контролируемых исследований у взрослых пациентов с хронической ИТП, ранее подвергавшихся лечению.
Большинство нежелательных реакций, связанных с элтромбопагом, имели легкую или умеренную выраженность, раннее начало и в редких случаях служили причиной для изменения лечения.
Нежелательные реакции перечислены в соответствии с анатомо-физиологической классификацией и частотой встречаемости, которая определялась следующим образом: очень часто — ≥1/10; часто — ≥1/100 и <1/10; иногда — ≥1/1000 и <1/100; редко — ≥1/10000 и <1/1000.
Инфекции и инвазии: часто — фарингит, инфекции мочевыводящих путей.
Со стороны ЖКТ: очень часто — тошнота, диарея; часто — сухость во рту, рвота.
Со стороны печени и желчевыводящих путей: часто — повышение уровня АСТ и АЛТ.
Со стороны кожи и подкожно-жировой клетчатки: часто — алопеция, сыпь.
Со стороны опорно-двигательного аппарата и соединительной ткани: часто — боль в спине, боль в грудной клетке костно-мышечного характера, костно-мышечная боль, миалгия.
Взаимодействие
Реклама: ООО «ВЕДАНТА», ИНН 7714886235, erid 4CQwVszH9pUkKJ7jUDd
Реклама: ООО «РЛС-Библиомед» ИНН 7714758963
Реклама: ООО «ВЕДАНТА», ИНН 7714886235, erid 4CQwVszH9pUkKJ7jUDd
Реклама: ООО «РЛС-Библиомед» ИНН 7714758963
Розувастатин: при совместном применении с элтромбопагом следует рассмотреть вопрос о снижении дозы розувастатина, а также проводить тщательный мониторинг состояния пациента. В клинических исследованиях элтромбопага при сопутствующей терапии розувастатином было рекомендовано снижение дозы последнего на 50%. Сочетанный прием элтромбопага и прочих субстратов ОАТР1В1 и BCRP требует осторожности.
Поливалентные катионы (образование хелатных комплексов): во избежание значительного снижения всасывания элтромбопага препарат следует принимать, по меньшей мере, за 4 ч до или после приема антацидов, молочных продуктов и прочих веществ, содержащих поливалентные катионы (например минеральных добавок, содержащих алюминий, кальций, железо, магний, селен и цинк).
Пища: прием однократной дозы элтромбопага 50 мг со стандартным высококалорийным завтраком, содержащим большое количество жира и молочные продукты, снижает показатель AUCo-∞ на 59% (ДИ 90%: 54 и 64%) и Cmax на 65% (ДИ 90%: 59 и 70%). Пища с небольшим содержанием кальция (<50 мг кальция), включающая фрукты, постную ветчину, говядину, фруктовый сок, соевое молоко и крупу без добавок кальция, железа и магния, не оказывает существенного влияния на плазменную экспозицию элтромбопага вне зависимости от калорийности и содержания жира.
Передозировка
Симптомы: в ходе клинических исследований зарегистрирован один случай передозировки, когда пациент принял внутрь 500 мг элтромбопага, при этом отмечались следующие симптомы: нераспространенная сыпь, преходящая брадикардия, утомляемость и повышение уровня трансаминаз. Данные изменения были обратимыми.
В случае передозировки возможно значительное увеличение количества тромбоцитов, что может приводить к тромботическим/тромбоэмболическим осложнениям.
Лечение: в случае передозировки следует рассмотреть вопрос о приеме внутрь препаратов, содержащих катионы металлов, например кальция, алюминия или магния, для уменьшения всасывания элтромбопага. Следует тщательно контролировать количество тромбоцитов. Лечение элтромбопагом возобновляют в соответствии с рекомендациями по режиму дозирования.
Поскольку почечная экскреция не является основным путем выведения элтромбопага, который активно связывается с белками плазмы крови, вероятнее всего, гемодиализ не является эффективным методом существенного ускорения выведения элтромбопага из организма.
Особые указания
Эффективность и безопасность применения элтромбопага для лечения других заболеваний и состояний, сопровождающихся тромбоцитопенией, включая тромбоцитопению после химиотерапии и миелодиспластические синдромы, в настоящее время не установлены.
Мониторинг функции печени
Применение элтромбопага может вызвать отклонения лабораторных показателей функции печени. В клинических исследованиях отмечено повышение уровня сывороточных АЛТ, ACT и непрямого билирубина. Эти явления носили по большей части легкий (1–2-й степени) и обратимый характер без клинически значимых симптомов, которые бы свидетельствовали о нарушении функции печени. По данным двух плацебо-контролируемых исследований, нежелательные явления в виде повышения уровня АЛТ были отмечены у 5,7 и 4% пациентов, получавших лечение элтромбопагом и плацебо соответственно. Сывороточные уровни АЛТ, ACT и билирубина необходимо оценить до начала лечения элтромбопагом, затем контролировать каждые 2 нед во время титрации дозы, а также ежемесячно после назначения стабильной дозы. Повторное исследование после выявления отклонения тестов функции печени проводят в течение 3–5 дней. В случае подтверждения отклонения мониторинг продолжают до момента разрешения данного явления, его стабилизации либо возвращения показателей к исходному уровню. Лечение элтромбопагом прекращают в случае увеличения уровня АЛТ (≥3-кратное увеличение значения ВГН и наличия следующих признаков:
— прогрессирование отклонения, либо
— сохранение отклонения ≥4 нед, либо
— его сочетание с повышением уровня прямого билирубина, либо
— его сочетание с клиническими симптомами поражения печени или признаками декомпенсации функции печени.
Пациентам с нарушениями функции печени элтромбопаг следует назначать с осторожностью. У пациентов со среднетяжелой или тяжелой печеночной недостаточностью начальная доза должна составлять 25 мг 1 раз в сутки.
Тромботические/тромбоэмболические осложнения
Количество тромбоцитов выше нормы представляет теоретический риск тромботических/тромбоэмболических осложнений. В клинических исследованиях элтромбопага тромбоэмболические осложнения наблюдались при низких и нормальных количествах тромбоцитов. В исследованиях по идиопатической тромбоцитопенической пурпуре у 17 из 446 пациентов (3,8%) был отмечен 21 эпизод тромбоэмболий. Тромбоэмболии включали: эмболию, в т.ч. легочную, тромбоз глубоких вен, транзиторные ишемические атаки, инфаркт миокарда, ишемический инсульт и заподозренный пролонгированный обратимый ишемический неврологический дефицит.
Тромботические/тромбоэмболические осложнения могут быть следствием очень значительного повышения уровня тромбоцитов. Пациентам с известными факторами риска тромботических/тромбоэмболических осложнений (таких как мутация фактора V Лейдена, дефицит АТIII, антифосфолипидный синдром и др.) следует уделять особое внимание при назначении элтромбопага.
Следует тщательно контролировать количество тромбоцитов и рассмотреть вопрос о снижении дозы или отмене элтромбопага, если количество тромбоцитов превышает целевые значения.
В контролируемом исследовании с участием пациентов с тромбоцитопенией и хроническими заболеваниями печени (n = 288), перенесших элективные инвазивные вмешательства, риск тромботических осложнений был повышен у пациентов, получавших элтромбопаг в дозе 75 мг 1 раз в сутки в течение 14 дней. Было отмечено 6 тромботических осложнений в группе пациентов, получавших элтромбопаг, и 1 — в группе плацебо. Все тромботические осложнения, отмеченные у пациентов из группы элтромбопага, были в системе воротной вены.
Кровотечение после прекращения лечения элтромбопагом
После прекращения лечения элтромбопагом у большинства пациентов уровень тромбоцитов в течение 2 нед возвращается к исходному, что повышает риск развития кровотечения, а в некоторых случаях может повлечь кровотечение. Количество тромбоцитов следует еженедельно контролировать на протяжении 4 нед после отмены элтромбопага.
Образование ретикулина в костном мозге и риск фиброза костного мозга
Агонисты рецепторов тромбопоэтина, включая элтромбопаг, могут повышать риск образования или разрастания ретикулиновых волокон в костном мозге. Перед началом лечения элтромбопагом следует оценить мазки периферической крови для определения исходного уровня морфологических изменений клеток. После достижения стабильной дозы элтромбопага ежемесячно выполняют общий клинический анализ крови с подсчетом лейкоцитарной формулы. При выявлении незрелых или диспластических клеток следует провести исследование мазка периферической крови на предмет появления новых либо усиления существующих морфологических изменений (например появления каплевидных и ядерных эритроцитов, незрелых лейкоцитов), либо выявления цитопении. При появлении у пациента новых либо усилении существующих морфологических отклонений или цитопении следует прекратить лечение элтромбопагом и рассмотреть вопрос о биопсии костного мозга, включая окраску мазка с целью выявления фиброза.
Злокачественные новообразования и прогрессирование злокачественных новообразований
Существует теоретическая возможность, что агонисты рецептора тромбопоэтина могут стимулировать прогрессирование существующих гематологических новообразований, например миелодиспластического синдрома. В ходе клинических исследований не было показано различий в частоте злокачественных новообразований или злокачественных новообразований крови между пациентами, получавшими плацебо, и пациентами, получавшими элтромбопаг.
Катаракта
В токсикологических исследованиях элтромбопага у грызунов выявлялась катаракта. Клиническое значение этого признака неизвестно. Рекомендуется плановый мониторинг пациентов на предмет развития катаракты.
Влияние на способность управлять автомобилем и другими движущимися механизмами
Исследования по влиянию элтромбопага на способность к управлению автомобилем или работу с механизмами не проводились. На основании фармакологических свойств элтромбопага отрицательное влияние на такие виды деятельности не ожидается. Однако при оценке способности пациента выполнять действия, которые требуют быстроты мышления, двигательных и познавательных навыков, следует учитывать клиническое состояние пациента и профиль нежелательных явлений элтромбопага.
Комментарий
Организация, принимающая претензии в РФ
ЗАО «ГлаксоСмитКляйн Трейдинг»: 121614, Москва, ул. Крылатская, 17, корп. 3, Бизнес-Парк «Крылатские холмы». Тел: (495) 777-89-00; факс: (495) 777-89-04.
Условия отпуска из аптек
По рецепту.
Условия хранения
При температуре не выше 30 °C.
Хранить в недоступном для детей месте.
Срок годности
3 года.
Не применять по истечении срока годности, указанного на упаковке.
Нежелательные реакции (HP), выявленные в клинических исследованиях, перечислены в соответствии с поражением органов и систем органов и частотой встречаемости (MedDRA).
Частота встречаемости определяется следующим образом: очень часто (>1/10), часто (>1/100 — <1/10), нечасто (> 1/1000 — < 1/100), редко (> 1/10000 — <1/1 000), очень редко (<1/10000, включая отдельные случаи). Категории частоты сформированы на
основании клинических исследований препарата и
пострегистрационного наблюдения.
Нежелательные реакции у пациентов с хронической ИТП
Взрослые
Инфекционные и паразитарные заболевания
Нечасто: грипп, назофарингит, оральный герпес, пневмония, синусит, тонзиллит, инфекция верхних дыхательных путей. Часто: фарингит, инфекции мочевыводящих путей.
Доброкачественные, злокачественные и неуточненные новообразования (включая кисты и полипы)
Нечасто: злокачественные новообразования ректосигмоидного отдела толстой кишки.
Нарушения со стороны крови и лимфатической системы
Нечасто: анемия, анизоцитоз, эозинофилия, гемолитическая анемия, лейкоцитоз, миелоцитоз, тромбоцитопения, увеличение концентрации гемоглобина, увеличение количества палочкоядерных лейкоцитов, уменьшение концентрации гемоглобина, увеличение количества тромбоцитов, уменьшение количества лейкоцитов.
Нарушения со стороны иммунной системы
Нечасто: гиперчувствительность.
Нарушения со стороны обмена веществ и питания
Нечасто: анорексия, гипокалиемия, снижение аппетита, повышение аппетита, подагра, гипокальциемия, повышение концентрации мочевой кислоты в крови.
Нарушения психики Нечасто: нарушение сна (бессонница), тревога, депрессия,
апатия, нарушение настроения, плаксивость.
Нарушения со стороны нервной системы
Часто:парестезия.
Нечасто: дисгевзия, гипестезия, сомноленция, мигрень,
тремор, нарушения равновесия, дизестезия,
гемипарез, мигрень с аурой, периферическая
нейропатия, периферическая сенсорная
нейропатия, нарушение речи, токсическая нейропатия, головная боль (включая сосудистый тип).
Нарушения со стороны органа зрения
Часто: сухость глаза. Нечасто: нечеткость зрения, помутнение хрусталика, астигматизм, кортикальная катаракта, конъюнктивальные кровоизлияния, боль в глазу, повышенное слезоотделение, ретинальное кровоизлияние, ретинальная пигментная эпителиопатия, снижение остроты зрения, нарушение зрения, аномальные результаты исследований остроты зрения, блефарит, сухой кератоконъюнктивит.
Нарушения со стороны органа слуха и лабиринтные нарушения
Нечасто: боль в ухе, головокружение.
Нарушения со стороны сердца
Нечасто: тахикардия, острый инфаркт миокарда, сердечно-сосудистое нарушение, цианоз, ощущение сердцебиения, синусовая тахикардия, удлинение интервала QT на электрокардиограмме.
Нарушения со стороны сосудов
Нечасто: тромбоз глубоких вен, артериальная гипертензия, эмболические осложнения, «приливы» жара,
поверхностный тромбофлебит, ощущение «прилива крови», гематома.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения
Часто: сухость слизистой оболочки полости рта, рвота.
Нечасто: носовое кровотечение, эмболия легочной артерии, инфаркт легкого, кашель, дискомфорт в носу, пузырьковые высыпания на слизистой ротоглотки, боль в ротоглотке, заболевание околоносовых пазух, синдром обструктивного апноэ во сне.
Нарушения со стороны желудочно-кишечного тракта
Часто: тошнота, диарея*, изъязвление слизистой оболочки полости рта.
Нечасто: запор, боли в верхних отделах живота, дискомфорт в животе, ощущение «переполнения» живота, диспепсия, боль в животе, кровотечения из десен, глоссодиния, геморрой, кровотечение из полости рта, болезненность живота, обесцвеченный стул, вздутие живота, пищевое отравление, частая дефекация, рвота с кровью, дискомфорт в полости рта.
* — градация «очень часто» при применении у пациентов с ИТП в возрасте от 1 года до 17 лет.
Нарушения со стороны печени и желчевыводящих путей
Часто: повышение активности аспартатаминотрансферазы (ACT), повышение активности аланинаминотрансферазы (АЛТ), гипербилирубинемия, отклонение показателей функции печени от нормальных значений. Нечасто: холестаз, поражение печени, лекарственное поражение печени, гепатит.
Нарушения со стороны кожи и подкожных тканей
Часто: алопеция, сыпь. Нечасто: зуд, подкожные кровоизлияния, гипергидроз, генерализованный зуд, крапивница, дерматоз, петехии, «холодный» пот, эритема, меланоз, ночная потливость, нарушение пигментации кожи, нарушение окраски кожи, шелушение кожи, отечность лица.
Нарушения со стороны скелетно-мышечной и соединительной ткани
Часто: боль в спине, боль в грудной клетке костно-мышечного характера, костно-мышечная боль, миалгия, артралгия, мышечный спазм, боль в костях, боль в конечностях, ощущение тяжести. Нечасто: мышечная слабость.
Нарушения со стороны почек и мочевыводящих путей
Нечасто: почечная недостаточность, лейкоцитурия, волчаночный нефрит, никтурия, протеинурия, увеличение концентрации мочевины в крови, увеличение концентрации креатинина в крови, повышенное отношение белок/креатинин в моче.
Общие расстройства и нарушения в месте введения
Нечасто: повышенная утомляемость, периферический отек, боль в груди, ощущение жара, боль, кровотечение в месте пункции сосуда, астения, ощущение беспокойства, болезненное состояние, воспаление раны, гриппоподобный синдром, недомогание,воспаление слизистой, некардиальная боль в грудной клетке, лихорадка, ощущение инородного тела.
Лабораторные и инструментальные данные
Нечасто: увеличение концентрации альбумина в крови, повышенная активность щелочной фосфатазы, увеличение концентрации общего белка, увеличение массы тела, уменьшение концентрации альбумина в крови, увеличение рН мочи.
Травмы, интоксикации и осложнения манипуляций
Нечасто: ушиб, солнечный ожог.
Дети и подростки (в возрасте от 1 года до 17 лет)
При применении препарата у детей в возрасте от 1 года до 17 лет дополнительно выявлены нижеуказанные HP.
Инфекционные и паразитарные заболевания
Очень часто: назофарингит, инфекции верхних дыхательныхпутей.
Часто: ринит.
Нарушения со стороны желудочно-кишечного тракта
Часто: боль в животе, зубная боль
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения
Часто: кашель, боль в ротоглотке, риноррея
Общие расстройства и нарушения в месте введения
Часто: лихорадка.
Нежелательные реакции у пациентов с хроническим вирусным гепатитом С
Инфекционные и паразитарные заболевания
Часто:инфекция мочевыводящих путей, инфекция верхних дыхательных путей, бронхит, назофарингит, грипп, оральный герпес, гастроэнтерит, фарингит.
Доброкачественные, злокачественные и неуточненные новообразования (включая кисты и полипы)
Часто:злокачественные новообразования печени.
Нарушения со стороны крови и лимфатической системы
Очень часто: анемия. Часто:лимфопения, гемолитическая анемия.
Нарушения со стороны обмена веществ и питания
Очень часто: снижение аппетита. Часто:гипергликемия, патологическое уменьшение массы тела.
Нарушения психики
Очень часто:бессонница. Часто:депрессия, тревога, нарушение сна, состояние спутанности сознания, возбуждение.
Нарушения со стороны нервной системы
Очень часто: головная боль. Часто:головокружение, нарушение внимания, дисгевзия, печеночная энцефалопатия, летаргия, нарушение памяти, парестезия.
Нарушения со стороны органа зрения
Часто: катаракта, экссудаты сетчатки, сухость глаза, желтушность склер, ретинальное кровоизлияние.
Нарушения со стороны органа слуха и лабиринтные нарушения
Часто:головокружение.
Нарушения со стороны сердца
Часто:ощущение сердцебиения.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения
Очень часто:кашель. Часто:одышка, боль в ротоглотке, одышка при физической нагрузке, продуктивный кашель.
Нарушения со стороны желудочно-кишечного тракта
Очень часто:тошнота, диарея Часто:рвота, асцит, боль в животе, боль в верхних отделах живота, диспепсия, сухость во рту, запор, вздутие живота, зубная боль, стоматит, гастроэзофагеальная рефлюксная болезнь, геморрой, дискомфорт в животе, гастрит, варикозное расширение вен пищевода, афтозный стоматит, кровотечение из варикозно расширенных вен пищевода.
Нарушения со стороны печени и желчевыводящих путей
Часто:гипербилирубинемия, желтуха, тромбоз воротной вены, печеночная недостаточность, лекарственное поражение печени.
Нарушения со стороны кожи и подкожных тканей
Очень часто: зуд, алопеция. Часто:сыпь, сухость кожи, экзема, зудящие кожные высыпания, эритема, гипергидроз, генерализованный зуд, ночная потливость, поражение кожи.
Нарушения со стороны скелетно-мышечной и соединительной ткани
Очень часто: миалгия Часто:артралгия, мышечные спазмы, боль в спине, боль в конечностях, костно-мышечная боль, боль в костях.
Нарушения со стороны почек и мочевыводящих путей
Очень часто: дизурия.
Общие расстройства и нарушения в месте введения
Очень часто: повышенная утомляемость, гипертермия, лихорадка, астения, периферический отек, гриппоподобное заболевание, озноб. Часто:раздражительность, боль, недомогание, реакция в месте инъекции, некардиальная боль в грудной клетке, отек, сыпь в месте инъекции, дискомфорт в грудной клетке, зуд в месте инъекции.
Лабораторные и инструментальные данные
Часто:увеличение концентрации билирубина в крови, уменьшение массы тела, лейкопения, уменьшение концентрации гемоглобина, уменьшение количества нейтрофильных лейкоцитов, увеличение международного нормализованного отношения, увеличение активированного частичного тромбопластинового времени (АЧТВ), гипергликемия, уменьшение концентрации альбумина в крови, удлинение интервала QT на электрокардиограмме.
Нежелательные реакции у пациентов с ТАА
Нарушения со стороны нервной системы
Очень часто:головная боль.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения
Очень часто: кашель, одышка, боль в ротоглотке, ринорея.
Нарушения со стороны желудочно-кишечного тракта
Оченьболь в животе, диарея, тошнота.
часто:
Нарушения со стороны печени и желчевыводящих путей
Очень часто:повышение активности трансаминаз.
Нарушения со стороны колеи и подкожных тканей
Очень часто: кровоподтеки. Часто:кожная сыпь.
Нарушения со стороны скелетно-мышечной и соединительной ткани
Очень часто: артралгия, мышечный спазм, боль в конечностях.
Общие расстройства и нарушения в месте введения
Очень часто: головокружение, утомляемость, фебрильна нейтропения, гипертермия.
В несравнительном открытом исследовании у пациентов с ТАА определяли наличие цитогенетических отклонений в аспирационных биоптатах костного мозга. У 7 пациентов были обнаружены впервые выявленные цитогенетические аномалии, из них у 5 пациентов были изменения в 7-й хромосоме.
Пострегистрационные исследования
При применении элтромбопага в пострегистрационном периодебыли зарегистрированы следующие HP. Сведения о них были получены из спонтанных сообщений, а также были зарегистрированы в качестве серьезных нежелательных явлений в реестрах, исследованиях, спонсированных исследователем, клинико-фармакологических исследованиях и поисковых исследованиях при применении по неутвержденным показаниям.
Нарушения со стороны сосудов
Редко:тромботическая микроангиопатия с острой почечной недостаточностью.
Нарушения со стороны кожи и подкожных тканей
Неизвестно: нарушение окраски кожных покровов*. *- обратимое нарушение окраски кожных покровов, включая гиперпигментацию и «желтушность», отмечалось у пациентов, получавших элтромбопаг в суточной дозе, превышающей 100 мг. В частности, нарушение окраски кожных покровов отмечалось у пациентов, получавших препарат по поводу показаний, требующих применения высоких доз элтромбопага, включая миелодиспластический синдром и ТАА.
Если любые из указанных в инструкции побочных эффектов усугубляются, или Вы заметили любые другие побочные эффекты, не указанные в инструкции, сообщите об этом врачу.
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 10 сентября 2018 года; проверки требуют 8 правок.
| Тромбопоэтин | |||||||
|---|---|---|---|---|---|---|---|
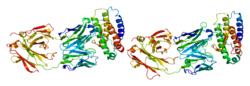 PDB rendering based on 1v7m. PDB rendering based on 1v7m. |
|||||||
| Доступные структуры | |||||||
| PDB | Поиск ортологов: PDBe, RCSB | ||||||
|
Список идентификаторов PDB 1V7M, 1V7N |
|||||||
| Идентификаторы | |||||||
| Символ | THPO ; MGDF; MKCSF; ML; MPLLG; THCYT1; TPO | ||||||
| Внешние ID | OMIM: 600044 MGI: 101875 HomoloGene: 398 ChEMBL: 1293256 GeneCards: Ген THPO | ||||||
|
Генная онтология
|
|||||||
| Профиль экспрессии РНК | |||||||
 |
|||||||
 |
|||||||
 |
|||||||
| Больше информации | |||||||
| Ортологи | |||||||
| Вид | Человек | Мышь | |||||
| Entrez | 7066 | 21832 | |||||
| Ensembl | ENSG00000090534 | ENSMUSG00000022847 | |||||
| UniProt | P40225 | P40226 | |||||
| RefSeq (мРНК) | NM_000460 | NM_001173505 | |||||
| RefSeq (белок) | NP_000451 | NP_001166976 | |||||
| Локус (UCSC) | Chr 3: 184.09 – 184.1 Mb |
Chr 16: 20.73 – 20.73 Mb |
|||||
| Поиск в PubMed | Искать | Искать |
Тромбопоэтин — белок, известный также как фактор роста и развития мегакариоцитов.
Тромбопоэтин — это гликопротеиновый гормон, производимый, главным образом, печенью, в меньшей степени — в почках и поперечно-полосатой мускулатуре, регулирующий выработку тромбоцитов костным мозгом. Стимулирует выработку и дифференцировку мегакариоцитов, клеток костного мозга.
Мегакариоцитопоэз — это процесс клеточного развития, приводящий к выработке тромбоцитов. Белок является лигандом для MLP/C_MPL, продукта миелопролиферативного вирусного онкогена лейкемии.
Открытие[править | править код]
Тромбопоэтин был клонирован пятью независимыми группами в 1994 году. Гипотезы о его функциях были выдвинуты ещё более 30 лет назад, задолго до идентификации. В самых ранних публикациях тромбопоэтин был описан как лиганд мембранного рецептора с-Mpl. Тромбопоэтин входит в состав 1-го класса кроветворных цитокинов. Было доказано, что тромбопоэтин является основным регулятором мегакариоцитопоэза, то есть образования новых тромбоцитов.
Генетика[править | править код]
Ген тромбопоэтина (у человека — THPO) располагается на длинном (q) плече 3-й хромосомы человека, в локусе 3q26.3-27. Мутации этого гена могут приводить к наследственной форме тромбоцитоза и некоторым случаям лейкемии. Первый участок из 155 аминокислот имеет заметную степень гомологии с эритропоэтином.
Функции и регуляция[править | править код]
В печени тромбопоэтин производится паренхимными клетками и синусоидальными эндотелиальными клетками; в почках — проксимальными клетками извитых канальцев. Вместе с этим тромбопоэтин производится клетками поперечно-полосатых мышц и стромальными клетками костного мозга. В печени его производство увеличивается за счёт фактора стимуляции В-клеток 6. Физиологически именно печень и стромальные клетки костного мозга являются важнейшими участками производства тромбопоэтина.
Тромбопоэтин регулирует дифференцировку мегакариоцитов и тромбоцитов, но исследования с помощью удаления рецепторов тромбопоэтина показывают, что его воздействие на гемопоэз более разносторонне.
Регуляция его действия с помощью отрицательной обратной связи отлична от таковой для большинства гормонов: эффектор непосредственно регулирует гормон. Тромбопоэтин связывается с mpl (CD 110) рецептором на поверхности тромбоцитов и уничтожается. Таким образом уменьшается воздействие гормона на мегакариоциты. Следовательно, повышение и понижение концентрации тромбоцитов регулирует уровень тромбопоэтина. Низкий уровень тромбоцитов приводит к увеличению воздействия тромбопоэтина на недифференцированные клетки костного мозга; приводит к дифференцировке и дальнейшему развитию этих клеток. С другой стороны, высокая концентрация тромбоцитов приводит к ингибированию этого воздействия.
Рецептор тромбопоэтина также известен как белок миелопролиферативной лейкемии или CD110 (Cluster of Differentiation 110). У человека кодируется онкогеном MPL (myeloproliferative leukemia virus).
В 1990 году онкоген (v-mpl) был выделен из вируса мышиной миелопролиферативной лейкемии, который был способен иммортализовать стволовые клетки костного мозга разного происхождения (обеспечить их неограниченно долгое деление). Впоследствии был обнаружен гомолог этого онкогена в человеческом геноме.
Терапевтическое применение[править | править код]
Несмотря на многочисленные испытания, тромбопоэтин не используется в терапии. В теории его можно применять для заготовки донорских тромбоцитов[1], а также для восстановления числа тромбоцитов после миелосупрессивной химиотерапии[2].
Исследования модифицированных рекомбинантных форм фактора роста и дифференцировки мегакариоцитов (ФРДМ) были остановлены, когда у здоровых добровольцев были обнаружены аутоиммунные антитела, а позже у добровольцев была выявлена тромбоцитопения[3].
Вместо тромбопоэтина используются препараты, которые воздействуют на его рецепторы, в частности, для лечения иммунной тромбоцитопении[4].
Romiplostim[править | править код]
Ромиплостим[5][6], торговое название Энплейт (Nplate), представляет собой Fc-пептидилированный белок (пептидное антитело), участвующий в проведении сигнала и активации внутриклеточной транскрипции посредством связывания с рецепторами тромбопоэтина и индуцирующий увеличение образования тромбоцитов. Молекула пептидного антитела состоит из Fc-фрагмента человеческого иммуноглобулина IgGl, в которой каждая одноцепочечная субъединица соединена ковалентной связью в С-конце с пептидной цепью, содержащей 2 ТПО-рецептор-связывающих фрагмента[7].
Аминокислотная последовательность ромиплостима не гомологична аминокислотной последовательности эндогенного тромбопоэтина. В доклинических и клинических исследованиях не отмечалось перекрёстной реакции антител к ромиплостиму с эндогенным тромбопоэтином.
Eltrombopag[править | править код]
Элтромбопаг[8][9], торговое название Револейд (Revolade), взаимодействует с трансмембранным доменом человеческого рецептора TPO-R и инициирует каскад передачи сигнала, напоминающий таковой для эндогенного тромбопоээтина, что сопровождается индукцией пролиферации и дифференцировки мегакариоцитов из клеток-предшественников костного мозга[10].
Элтромбопаг отличается от тромбопоэтина с точки зрения эффектов на агрегацию тромбоцитов. В отличие от ТРО, воздействие элтромбопага на тромбоциты здорового человека не усиливает агрегацию под действием АДФ и не стимулирует экспрессию Р-селектина. Элтромбопаг не препятствует агрегации тромбоцитов под действием АДФ или коллагена.
Примечания[править | править код]
- ↑ Kuter D. J., Goodnough L. T., Romo J., DiPersio J., Peterson R., Tomita D., Sheridan W., McCullough J. Thrombopoietin therapy increases platelet yields in healthy platelet donors. (англ.) // Blood. — 2001. — Vol. 98, no. 5. — P. 1339—1345. — doi:10.1182/blood.V98.5.1339. — PMID 11520780.
- ↑ Kaushansky K. Lineage-specific hematopoietic growth factors. (англ.) // The New England journal of medicine. — 2006. — Vol. 354, no. 19. — P. 2034—2045. — doi:10.1056/NEJMra052706. — PMID 16687716.
- ↑ Li J., Yang C., Xia Y., Bertino A., Glaspy J., Roberts M., Kuter D. J. Thrombocytopenia caused by the development of antibodies to thrombopoietin. (англ.) // Blood. — 2001. — Vol. 98, no. 12. — P. 3241—3248. — doi:10.1182/blood.V98.12.3241. — PMID 11719360.
- ↑ Imbach P., Crowther M. Thrombopoietin-receptor agonists for primary immune thrombocytopenia. (англ.) // The New England journal of medicine. — 2011. — Vol. 365, no. 8. — P. 734—741. — doi:10.1056/NEJMct1014202. — PMID 21864167.
- ↑ Энплейт. Энциклопедия лекарств и товаров аптечного ассортимента. РЛС Патент. — Инструкция, применение и формула.
- ↑ Chalmers S., Tarantino M. D. Romiplostim as a treatment for immune thrombocytopenia: a review. (англ.) // Journal of blood medicine. — 2015. — Vol. 6. — P. 37—44. — doi:10.2147/JBM.S47240. — PMID 25632241.
- ↑ FDA Approves Nplate™ for Long-Term Treatment of Adult Chronic ITP // Amgen Inc. Aug. 22, 2008. Дата обращения: 4 апреля 2015. Архивировано 10 октября 2015 года.
- ↑ Револейд. Энциклопедия лекарств и товаров аптечного ассортимента. РЛС Патент. — Инструкция, применение и формула.
- ↑ Park R. Eltrombopag: a new treatment option for chronic refractory adult immune thrombocytopenia. (англ.) // Blood research. — 2015. — Vol. 50, no. 1. — P. 1—2. — doi:10.5045/br.2015.50.1.1. — PMID 25830121.
- ↑ FDA approves Promacta® (eltrombopag), the first oral medication to increase platelet production for people with serious blood disorder Архивная копия от 9 апреля 2015 на Wayback Machine // GlaxoSmithKline group, 20 November 2008
Ссылки[править | править код]
- a b c d e f g h Kaushansky K (2006). «Lineage-specific hematopoietic growth factors». N. Engl. J. Med. 354 (19): 2034-45.[1]
- «Entrez Gene: THPO thrombopoietin (myeloproliferative leukemia virus oncogene ligand, megakaryocyte growth and development factor)»[2]
- Online ‘Mendelian Inheritance in Man'[3]
- Kuter DJ, Goodnough LT, Romo J, et al. (2001). «Thrombopoietin therapy increases platelet yields in healthy platelet donors»[4]
- Li J, Yang C, Xia Y, Bertino A, Glaspy J, Roberts M, Kuter DJ (December 2001). «Thrombocytopenia caused by the development of antibodies to thrombopoietin».[5]
- Imbach P, Crowther M (August 2011). «Thrombopoietin-receptor agonists for primary immune thrombocytopenia». N. Engl. J. Med. 365 (8): 734-41.[6]
- Nakamura T, Miyakawa Y, Miyamura A, et al. (2006). «A novel nonpeptidyl human c-Mpl activator stimulates human megakaryopoiesis and thrombopoiesis»[7]
- Jenkins JM, Williams D, Deng Y, et al. (2007). «Phase 1 clinical study of eltrombopag, an oral, nonpeptide thrombopoietin receptor agonist»[8]
Описание тромбопоэтина человека (рекомбинантный белок), rhTpo
- Источник – клеточная линия CHO, продуцирующая rhTpo;
- молекулярный вес – около 90 кДа в редуцирующих условиях в ПААГ. Окраска Coomassie Brilliant Blu;
- чистота – более 98% в соответствии с электрофорезом в ПААГ с последующим окрашиванием Coomassie Brilliant Blue;
- уровень эндотоксина – менее 0,1 е.а. на 1 мкг белка, LAL-тест.
Форма выпуска тромбопоэтина человека (рекомбинантный белок), rhTpo
Лиофильно высушен из буферного раствора PBS, содержащего 0,05% Tween 20, pH 7,0, профильтрованного через фильтр с диаметром пор 0,22 мкм.
Разведение тромбопоэтина человека (рекомбинантный белок), rhTpo
Центрифугировать флакон при 1000 rpm, 3 мин; добавить стерильный буферный раствор (PBS) до конечной концентрации 0,1-1 мкг/мкл; оставить на 20-30 мин при комнатной температуре, затем центрифугировать при 1000 rpm в течение 1 мин, и мягко ресуспендировать. Для приготовления рабочих растворов можно использовать буфер на водной основе или культуральную среду. Добавление вспомогательных белков (BSA или FBS) не является необходимым.
Условия хранения и транспортировки тромбопоэтина человека (рекомбинантный белок), rhTpo
Стабильность и условия хранения:
- невскрытая упаковка – 12 мес. при температуре от -20 до -70 °C;
- разведенный в стерильных условиях – 1 мес. от 2 до 8 °C; 6 мес. от -20 до -70 °C;
- не рекомендуются повторные циклы замораживания-оттаивания раствора рекомбинантного белка.
Условия транспортировки – при комнатной температуре.
Доставка
Доставка осуществляется по всей России и странам СНГ. Возможен самовывоз со склада по адресу Московская область, г. Мытищи, 7-й Ленинский переулок, д.13. Доставка по Москве и Московской области осуществляется бесплатно.
Цена товара указана со склада в Москве и не включает расходы на доставку в другие города.
Вы можете выбрать способ доставки в личном кабинете, чтобы он автоматически указывался при оформлении всех последующих заказов. При выборе варианта «Транспортная компания по выбору клиента» укажите в комментариях транспортную компанию, с которой вы предпочитаете работать.
Точная стоимость доставки рассчитывается менеджером при подтверждении заказа в зависимости от весообъемных характеристик и дальности. Товары, требующие особого температурного режима, доставляются с соблюдением требуемых условий. Если в заказе есть прекурсоры, необходимо оформить официальное письмо об отпуске прекурсоров. (образец письма об отпуске прекурсоров)
Оплата
Компания Диаэм работает с юридическими и физическими лицами. После оформления заказа продавец-консультант сформирует счет и направит его вам по электронной почте и на страницу заказа в Личном кабинете на сайте. Вы также можете сами сформировать счет из Корзины, авторизовавшись на сайте. Счет оплачивается через банк. Вы можете оплатить товар в кассе Диаэм или любом отделении банка.
Для получения товара необходимо предоставление доверенности организации, а для получения товара при оплате физическим лицом необходим паспорт.

