Варгатеф — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер:
ЛП-002830
Торговое наименование:
ВАРГАТЕФ
Международное непатентованное наименование:
нинтеданиб (nintedanib)
Лекарственная форма:
мягкие капсулы
Состав
Одна капсула 100 мг содержит:
Активное вещество: нинтеданиба этансульфонат — 120,40 мг, что соответствует 100,00 мг нинтеданиба основания;
Вспомогательные вещества: триглицериды средней цепи — 107,40 мг, твердый жир — 51,00 мг, лецитин — 1,20 мг;
Оболочка капсулы: желатин — 111,24 мг, глицерин 85% — 49,09 мг, титана диоксид (Е171) — 1,21 мг, железа оксид красный (суспензия с глицерином 85%) — 0,06 мг, железа оксид желтый (суспензия с глицерином 85 %) — 0,36 мг, чернила Опакод® тип S-1 -17823.
Одна капсула 150 мг содержит:
Активное вещество: нинтеданиба этансульфонат — 180,60 мг, что соответствует 150,00 мг нинтеданиба основания;
Вспомогательные вещества: триглицериды средней цепи — 161,10 мг, твердый жир -76,50 мг, лецитин — 1,80 мг;
Оболочка капсулы: желатин — 141,84 мг, глицерин 85% — 61,43 мг, титана диоксид (Е171) — 0.39 мг, железа оксид красный (суспензия с глицерином 85%) — 1,24 мг, железа оксид желтый (суспензия с глицерином 85 %) — 1,86 мг, чернила Опакод® тип S-1-17823.
Описание
Капсулы 100 мг
Продолговатые непрозрачные мягкие желатиновые капсулы розовато-оранжевого (персикового) цвета, содержащие ярко-желтую вязкую суспензию, на одной стороне которых черным цветом напечатан символ компании Берингер Ингельхайм и «100».
Капсулы 150 мг
Продолговатые непрозрачные мягкие желатиновые капсулы коричневого цвета, содержащие ярко-желтую вязкую суспензию, на одной стороне которых черным цветом напечатан символ компании Берингер Ингельхайм и «150».
Фармакотерапевтическая группа
противоопухолевое средство — протеинтирозинкиназы ингибитор
Код ATX:
L01XE31
Фармакологические свойства
Фармакодинамика
Механизм действия
Нинтеданиб — ингибитор тирозинкиназы, относящийся к классу малых молекул, блокирующий киназную активность рецепторов фактора роста эндотелия сосудов 1-3 (VEGFR 1-3), рецепторов тромбоцитарного фактора роста а и В (PDGFR а и В) и рецепторов фактора роста фибробластов 1-3 (FGFR 1-3). Кроме того, ингибируются Fms-подобная протеинтирозинкиназа (Flt-З), лимфоцит-специфическая протеинтирозинкиназа (Lck), протоонкогенная протеинтирозинкиназа (Src) и киназы рецептора колониестимулирующего фактора 1 (CSF1R). Нинтеданиб конкурентно взаимодействует с аденозинтрифосфат (АТФ) связывающим участком этих киназ и блокирует каскады внутриклеточной передачи сигналов, которые, как было продемонстрировано, участвуют в патогенезе ремоделирования фиброзной ткани.
Фармакодинамические эффекты
Опухолевый ангиогенез является процессом, который вносит существенный вклад в рост, прогрессирование и образование метастазов опухоли. Этот процесс преимущественно запускается проангиогенными факторами такими, как фактором роста эндотелия сосудов и основным фактором роста фибробластов (VEGF и bFGF), секретируемыми опухолевыми клетками, чтобы привлечь эндотелиальные и периваскулярные клетки хозяина и облегчить доставку кислорода и питательных веществ через сосудистую систему.
Нинтеданиб эффективно противодействует образованию и развитию сосудистой системы опухоли, приводит к замедлению и остановке роста опухоли.
В исследованиях in vitro на клетках человека было показано, что нинтеданиб ингибирует процессы, предположительно связанные с инициацией фиброзного патогенеза, с высвобождением профибротических медиаторов из моноцитов периферической крови и с поляризацией макрофагов с образованием макрофагов. активированных по альтернативному пути. Было продемонстрировано, что нинтеданиб ингибирует фундаментальные процессы фиброза органов, пролиферации и миграции фибробластов, трансформацию в активный фенотип миофибробласта и секрецию внеклеточного матрикса. В исследованиях на животных с использованием многочисленных моделей ИЛФ (идиопатический легочный фиброз), ИЗЛ-ССД (интерстициальные заболевания легких при системной склеродермии), ИЗЛ-РА (интерстициальные заболевания легких при ревматоидном артрите) и других видов фиброза органов, было показано противовоспалительное и противофибротическое действие нинтеданиба в легких, коже, сердце, почках и печени. Нинтеданиб также обладает активностью в отношении сосудов. Он уменьшал апоптоз эндотелиальных клеток микрососудов кожи и замедлял ремоделирование легочных сосудов путем уменьшения пролиферации клеток гладкой мускулатуры сосудов, толщины стенки легочных сосудов и уменьшал процентную долю окклюзированных легочных сосудов.
Фармакокинетика
Фармакокинетика нинтеданиба может считаться линейной в отношении времени (т.е. данные, полученные в случае применения однократной дозы, могут экстраполироваться на данные, полученные в результате многократного применения). После многократного применения препарата накопление составляет 1,04 при оценке максимальной концентрации (Cmax) и 1,38 при оценке площади под кривой «концентрация-время» (AUCτ ). Остаточные концентрации нинтеданиба остаются стабильными в течение одного года и более.
Всасывание
Сmах нинтеданиба в плазме крови достигается приблизительно через 2-4 часа после приема препарата во время еды (диапазон 0,5-8 часов). Абсолютная биодоступность дозы 100 мг составляет у здоровых добровольцев 4,69 % (90 % доверительный интервал (ДИ): 3,615-6,078).
Установлено, что экспозиция нинтеданиба увеличивается пропорционально дозе (в диапазонах доз 50-450 мг один раз в день и 150-300 мг два раза в день). Устойчивые концентрации в плазме крови достигаются, как максимум, в течение одной недели после начала приема.
Экспозиция нинтеданиба увеличивается после приема пищи примерно на 20 % по сравнению с приемом препарата натощак (ДИ: 95,3-152,5 %), а всасывание замедляется. Медиана времени достижения максимальной концентрации в плазме крови натощак — 2,00 часа, после еды — 3,98 часа.
Распределение
Распределение нинтеданиба осуществляется путем двухфазной кинетики. После внутривенной инфузии во время терминальной фазы наблюдается большой объем распределения (Vd) 1050 л, геометрический коэффициент вариации (gCV) 45,0 %.
Связывание нинтеданиба с белками плазмы человека in vitro считается значительным, связанная фракция составляет 97,8 %. Основным белком, участвующим в связывании, считается альбумин сыворотки крови. Нинтеданиб преимущественно распределяется в плазме, соотношение кровь/плазма составляет 0,869.
Нинтеданиб является субстратом для гликопротеина-Р (P-gp). Показано, что нинтеданиб in vitro не является субстратом или ингибитором полипептидных переносчиков органических анионов (ОАТР-1В1, ОАТР-1ВЗ, ОАТР-2В1), переносчика органических катионов-2 (ОСТ-2) или белка, ассоциированного с множественной лекарственной устойчивостью-2 (MRP-2). Нинтеданиб также не является субстратом для белка резистентности рака молочной железы (BCRP). In vitro было установлено, что нинтеданиб обладает слабой ингибирующей активностью в отношении ОСТ-1, BCRP и P-gp, что, как считается, имеет небольшую клиническую значимость. Такое же заключение сделано в отношении нинтеданиба как субстрата для ОСТ-1.
Биотрансформация
Основной реакцией, участвующей в метаболизме нинтеданиба, является гидролитическое расщепление с помощью эстераз, что приводит к образованию свободного кислого метаболита нинтеданиба. В доклинических исследованиях in vivo установлено, что данный метаболит не обладает эффективностью, несмотря на влияние на целевые рецепторы препарата. В дальнейшем он глюкуронизируется ферментами уридин-дифосфат-глюкуронозилтрансферазами (UGT 1А1, UGT 1А7, UGT 1А8 и UGT 1А10) с образованием глюкуронида.
Считается, что биотрансформация нинтеданиба с участием изоферментов СУР происходит только в небольшой степени, основное участие принимает изофермент CYP ЗА4. В исследовании ADME у человека основной метаболит, образующийся с участием изоферментов CYP, обнаружить в плазме не удалось. По данным исследования in vitro, CYP-зависимый метаболизм составляет примерно 5 %, тогда как расщепление, осуществляемое эстеразами, составляет 25 %.
Выведение
Общий клиренс из плазмы после внутривенной инфузии составляет 1390 мл/мин (gCV 28,8 %). Экскреция почками неизмененной активной субстанции в течение 48 часов после приема нинтеданиба внутрь составляет примерно 0,05 % от величины дозы (gCV 31,5 %), а после внутривенного введения — примерно 1,4 % (gCV 24,2 %); почечный клиренс составляет 20 мл/мин (gCV 32,6%). После приема внутрь [ 14С]-нинтеданиба радиоактивный материал выводился преимущественно с желчью и обнаруживался в кале (93,4% от величины дозы, gCV 2,61 %). Вклад почечной экскреции в общий клиренс составляет 0.649 % от величины дозы (gCV 26,3 %). Выведение считается полным (более 90 %) через 4 дня после приема. Период полувыведения нинтеданиба составляет от 10 до 15 часов (gCV примерно 50 %).
Зависимость эффекта от экспозиции
Немелкоклеточный рак легкого (НМРЛ)
В ходе исследования зависимости нежелательных явлений от фармакокинетики нинтеданиба была установлена тенденция к более частому повышению активности ферментов печени при большей экспозиции нинтеданиба. Подобной зависимости не отмечается для нарушений со стороны желудочно-кишечного тракта (ЖКТ).
Для клинических конечных точек анализ взаимосвязи фармакокинетики с эффективностью не проводился. С помощью метода логистической регрессии установлена статистически значимая взаимосвязь между экспозицией нинтеданиба и влиянием на изменения, обнаруживаемые методом динамической контрастной магнитно-резонансной томографии.
ИЛФ и ИЗЛ-ССД
Анализ зависимости «экспозиция-ответ» показал наличие взаимосвязи типа Еmах между воздействием в диапазоне, наблюдавшемся в ряде исследований Фазы II и III, и ежегодным уровнем снижения форсированной жизненной емкости легких; ЕС50 составляла около 3-5 нг/мл (относительная стандартная ошибка: приблизительно 55 %). Для сравнения, медиана наблюдаемых минимальных концентраций нинтеданиба при применении препарата ВАРГАТЕФ в дозе 150 мг 2 раза в сутки составляла примерно 10 нг/мл.
В отношении безопасности возможно имеется слабая взаимосвязь между экспозицией нинтеданиба в плазме крови и повышением активности аланинаминотранферазы (АЛТ) и/или аспартатаминотрансферазы (ACT). Фактически применяемая доза может быть более существенным прогностическим фактором риска развития диареи любой интенсивности, даже если экспозицию в плазме крови нельзя исключить в качестве определяющего фактора риска.
Фармакокинетика у особых групп пациентов
Фармакокинетические свойства нинтеданиба были сопоставимы у здоровых добровольцев, пациентов с ИЛФ, ИЗЛ-ССД и НМРЛ. Основываясь на результатах популяционного фармакокинетического анализа и описательных исследований, на воздействие нинтеданиба не влиял пол (с учетом массы тела), нарушения функции почек легкой и средней степени тяжести (рассчитанная по клиренсу креатинина), метастазы в печени, общее состояние больного (оценка по опроснику Восточной Объединенной Онкологической Группы, Eastern Cooperative Oncology Group (ECOG)), употребление алкоголя, или генотип P-gp. Популяционный фармакокинетический анализ выявил умеренное влияние возраста, массы тела и расовой принадлежности на воздействие нинтеданиба. В связи с тем, что наблюдалась высокая межиндивидуальная вариабельность воздействия, эти влияния не считались клинически значимыми. Тем не менее, рекомендуется тщательное мониторирование пациентов, у которых выявляется несколько таких факторов риска, представленных ниже.
Возраст
Экспозиция нинтеданиба линейно увеличивается с возрастом. У 45-летних пациентов (5-й процентиль) значение AUCτ,ss (в равновесном состоянии на период дозирования) было ниже на 16 %, а у 76-летних пациентов (95-й процентиль) выше на 13 % по сравнению с пациентами, медиана возраста которых составляла 62 года. Диапазон возраста, оценивавшийся в ходе анализа, составлял 29-85 лет; возраст более 75 лет отмечался примерно у 5 % популяции пациентов.
Аналогичные исследования у детей не проводились.
Масса тела
Наблюдается обратная корреляция между массой тела и экспозицией нинтеданиба. У пациентов с массой тела 50 кг (5-й процентиль) величина AUCτ,ss увеличивалась на 25 %, а у пациентов с массой тела 100 кг (95-й процентиль) уменьшалась на 19 % по сравнению с пациентами, медиана массы тела которых составляла 71,5 кг.
Раса
Средняя популяционная экспозиция нинтеданиба на 33-50 % выше у пациентов-китайцев, тайваньцев и индийцев, и на 16% выше у пациентов японского происхождения, а у пациентов-корейцев — на 16-22 % ниже, чем у пациентов европеоидной расы (с поправкой на массу тела). Данные в отношении пациентов негроидной расы являются очень ограниченными, диапазон этих данных сходен с пациентами европеоидной расы.
Нарушения функции печени
В исследовании I фазы при изучении однократного введения препарата значения Сmах и AUC были в 2,2 раза выше у добровольцев с легкими нарушениями функции печени (класс А по шкале Чайлд-Пью; 90 % доверительный интервал (ДИ) 1,3-3,7 для Сmax и 1,2-3,8 для AUC, соответственно), чем у здоровых добровольцев.
У добровольцев с умеренными нарушениями функции печени (класс В по шкале Чайлд-Пью) значение Сmах (90 % ДИ 4,4-13,2) было в 7,6 раза выше, и 8,7 раза выше значение AUC (90% ДИ 5,7-13,1) соответственно, в сравнении со здоровыми добровольцами. В исследовании не принимали участия пациенты с тяжелыми нарушениями функции печени (класс С по шкале Чайлд-Пью).
Показания к применению
- Местнораспространенный, метастатический или рецидивирующий немелкоклеточный рак легкого (аденокарцинома) после химиотерапии первой линии в комбинации с доцетакселом.
- Идиопатический легочный фиброз (идиопатический фиброзирующий альвеолит); для лечения и замедления прогрессирования заболевания.
- Интерстициальные заболевания легких при системной склеродермии
Противопоказания
- Гиперчувствительность к нинтеданибу, сое или арахису, или любому вспомогательному компоненту препарата;
- беременность и период грудного вскармливания;
- нарушения функции печени средней и тяжелой степени тяжести (опыт применения отсутствует);
- тяжелые нарушения функции почек (клиренс креатинина < 30 мл/мин) (опыт применения отсутствует)*;
- активные метастазы в головной мозг (опыт применения отсутствует);
- возраст младше 18 лет (опыт применения отсутствует).
* Эффективность и безопасность нинтеданиба у пациентов с тяжелыми нарушениями функции почек (клиренс креатинина < 30 мл/мин) не были изучены. Через почки выводится менее 1 % разовой дозы нинтеданиба.
В отношении противопоказаний для доцетаксела, пожалуйста, обратитесь к соответствующей инструкции по применению этого препарата.
С осторожностью
Нарушения функции печени легкой степени тяжести; наследственная предрасположенность к кровотечениям (болезнь фон Виллебранда); стабильные метастазы в головной мозг; терапия антикоагулянтами; венозные тромбоэмболии; перфорации ЖКТ в анамнезе; пациенты, которые ранее подвергались абдоминальным хирургическим вмешательствам; артериальная тромбоэмболия.
Применение при беременности и в период грудного вскармливания
Беременность
Специальных исследований по применению препарата ВАРГАТЕФ во время беременности у человека не проводилось, однако в доклинических исследованиях у животных установлена репродуктивная токсичность этого препарата. Поскольку нинтеданиб может обладать эмбриотоксическим действием у человека, он не должен применяться во время беременности, поэтому перед началом лечения необходимо проведение теста на беременность, а также во время терапии по мере необходимости. Пациенткам следует немедленно сообщить врачу о развитии беременности во время терапии препаратом ВАРГАТЕФ. Если во время терапии развивается беременность, необходимо прекратить лечение препаратом ВАРГАТЕФ и проинформировать пациентку о потенциальной опасности эмбриотоксического воздействия препарата. Применение нинтеданиба может быть вредно для плода. Женщинам детородного возраста, принимающим препарат ВАРГАТЕФ, следует рекомендовать избегать наступления беременности во время лечения препаратом ВАРГАТЕФ и использовать высокоэффективные методы контрацепции во время применения препарата и на протяжении, по крайней мере, 3 месяцев после приема последней дозы. В данный момент неизвестно, может ли нинтеданиб снижать эффективность гормональных контрацептивов, поэтому женщинам, использующим гормональные контрацептивы, необходимо использовать и барьерные методы контрацепции.
Грудное вскармливание
Специальных исследований у человека о выделении нинтеданиба и его метаболитов в грудное молоко не проводилось. В доклинических исследованиях показано, что у крыс в период лактации в грудное молоко проникает небольшое количество нинтеданиба и его метаболитов (≤ 0,5 % от величины применявшейся дозы). Поэтому нельзя исключить риск для новорожденных и грудных детей. Во время лечения препаратом ВАРГАТЕФ кормление грудью следует прекратить.
Фертильность
В доклинических исследованиях признаков нарушений фертильности у самцов выявлено не было. В субхронических и хронических исследованиях токсичности, во время которых уровень системного воздействия препарата был сравним с уровнем, достигающимся при использовании максимальной рекомендуемой дозы у человека, признаков нарушений фертильности у самок крыс обнаружено не было.
За информацией о влиянии доцетаксела на беременность, грудное вскармливание и фертильность, пожалуйста, обратитесь к соответствующей инструкции по применению этого препарата.
Способ применения и дозы
Капсулы принимают внутрь предпочтительно во время еды. Капсулы следует проглатывать целиком, запивая водой, не разжевывая и не разламывая.
Пропуск дозы
Если какая-либо доза препарата ВАРГАТЕФ была пропущена, то следует продолжить прием препарата в изначально рекомендуемой дозе по расписанию следующего приема препарата. Если доза была пропущена, пациент не должен принимать дополнительную дозу препарата.
НМРЛ
Лечение препаратом ВАРГАТЕФ следует назначать и проводить под контролем врача, имеющего опыт в назначении противоопухолевой терапии.
Рекомендуемая доза препарата ВАРГАТЕФ составляет 200 мг два раза в день с интервалом примерно в 12 часов со 2 по 21 день стандартного 21-дневного цикла лечения доцетакселом.
ВАРГАТЕФ не должен применяться в день начала химиотерапии доцетакселом, т.е. в 1 день лечения.
Максимальная рекомендуемая суточная доза составляет 400 мг.
После окончания применения доцетаксела можно продолжить терапию препаратом ВАРГАТЕФ до тех пор, пока сохраняется клинический эффект, или до развития неприемлемой токсичности.
Изменение дозы в случае развития нежелательных реакций
В качестве первоначальной меры для устранения нежелательных реакций рекомендуется временный перерыв в лечении препаратом ВАРГАТЕФ до тех пор, пока нежелательная реакция не снизится до уровня, который позволит возобновить терапию (см. Таблицы 1 и 2). Лечение может возобновляться в уменьшенной дозе.
Для обеспечения индивидуальной безопасности и переносимости рекомендуется снижение суточной дозы препарата на 100 мг (т.е. уменьшение разовой дозы на 50 мг), как это описывается в Таблицах 1 и 2. Если нежелательная реакция (реакции) сохраняется, т.е. если пациент не переносит препарат в дозе 100 мг два раза в день, лечение препаратом нужно окончательно прекратить.
В случае специфического повышения активности АСТ/АЛТ более чем в 3 раза по сравнению с ВГН в сочетании с повышением концентрации общего билирубина в 2 и более раза по сравнению с ВГН и щелочной фосфатазы (ЩФ) менее чем в 2 раза по сравнению с ВГН (см. Таблицу 2), применение препарата ВАРГАТЕФ следует временно прекратить. Если не будет установлена альтернативная причина нарушений, ВАРГАТЕФ должен быть окончательно отменен.
Таблица 1.
Информация об изменении дозы в случае развития диареи, рвоты и других негематологических или гематологических нежелательных явлений, исключая повышение уровней печеночных ферментов (см. Таблицу 2).
|
Нежелательная реакция* |
Изменение дозы |
|
Диарея 2 степени тяжести в течение более 7 дней подряд, несмотря на антидиарейное лечение. |
После временного прекращения лечения и уменьшения тяжести реакции до 1 степени или восстановления исходного состояния пациента рекомендуется снижение дозы с 200 мг два раза в день до 150 мг два раза в день. |
|
Рвота ≥ 2 степени тяжести Другая негематологическая или |
* Общие терминологические критерии для нежелательных явлений — СТСАЕ (Common Terminology Criteria for Adverse Events)
Таблица 2.
Информация об изменении дозы в случае повышения активности ACT и/или АЛТ и повышения концентрации билирубина.
|
Повышение АСТ/АЛТ и билирубина |
Изменение дозы |
|
Повышение активности ACT и/или АЛТ в > 2,5 раза по сравнению с ВГН в сочетании с повышением общего билирубина в ≥ 1,5 раза по сравнению с ВГН. |
После временного прекращения лечения и снижения активности трансаминаз до ≤ 2,5 раза по сравнению с ВГН в сочетании со снижением билирубина до нормы, доза снижается с 200 мг 2 раза в день до 150 мг 2 раза в день и, если еще одно снижение дозы считается необходимым, то со 150 мг 2 раза в день до 100 мг два раза в день. |
|
Повышение значений ACT и/или АЛТ в > 3 раза по сравнению с ВГН в сочетании с повышением общего билирубина в ≥ 2 раза по сравнению с ВГН и повышением ЩФ в < 2 раза по сравнению с ВГН. |
Если альтернативная причина нарушений не будет установлена, то препарат ВАРГАТЕФ должен быть окончательно отменен. |
ИЛФ и ИЗЛ-ССД
Лечение препаратом ВАРГАТЕФ следует назначать и проводить под контролем врача, имеющего опыт диагностики и лечения заболеваний, при которых показан препарат. Рекомендуемая доза препарата составляет 150 мг два раза в день, приблизительно через каждые 12 часов.
Максимальная суточная доза составляет 300 мг.
Изменение дозы в случае развития нежелательных реакций
При развитии нежелательных реакций таких, как диарея, тошнота и рвота в дополнение к симптоматической терапии, при необходимости, рекомендуется снижение дозы или временное прерывание лечения до тех пор, пока нежелательная реакция не снизится до уровня, который позволит возобновить терапию. Лечение препаратом ВАРГАТЕФ может быть возобновлено в полной дозе (150 мг два раза в день) или в сниженной дозе (100 мг два раза в день). Если пациент не переносит дозу препарата 100 мг два раза в день, лечение препаратом ВАРГАТЕФ следует прекратить.
В случае прерывания лечения вследствие повышения активности трансаминаз (ACT или АЛТ) более чем в 3 раза по сравнению с ВГН после восстановления показателей до нормальных значений рекомендовано возобновить терапию в уменьшенной дозе (100 мг два раза в день). Впоследствии доза может быть увеличена до полной дозы (150 мг два раза в день).
Особые группы пациентов
Детский возраст
Безопасность и эффективность препарата ВАРГАТЕФ у пациентов детского возраста в клинических исследованиях не изучалась.
Пожилой возраст (>65 лет)
Не отмечено никаких общих различий по безопасности и эффективности применения препарата у пожилых пациентов по сравнению с пациентами моложе 65 лет. Исходной коррекции дозы препарата на основании возраста пациента не требуется.
Раса и масса тела
Основываясь на данных популяционного фармакокинетического анализа, исходная коррекция дозы препарата ВАРГАТЕФ в зависимости от расы или массы тела не требуется. Данные по безопасности у пациентов негроидной расы ограничены.
Нарушения функции почек
Через почки выводится менее 1 % однократной дозы нинтеданиба. У пациентов с нарушениями функции почек легкой или средней степени тяжести изменения начальной дозы не требуется. У пациентов с тяжелыми нарушениями функции почек (клиренс креатинина < 30 мл/мин) безопасность, эффективность и фармакокинетика нинтеданиба не изучались.
Нарушения функции печени
Нинтеданиб выводится преимущественно с желчью (через кишечник) (> 90 %). У пациентов с нарушениями функции печени (класс А по шкале Чайлд-Пью, класс В по шкале Чайлд-Пью), концентрация препарата в крови повышалась.
У пациентов с нарушениями функции печени средней и тяжелой степени тяжести (классы В и С по шкале Чайлд-Пью) безопасность, эффективность и фармакокинетика нинтеданиба не изучались. Поэтому лечение пациентов с нарушениями функции печени средней и тяжелой степени тяжести препаратом ВАРГАТЕФ не рекомендуется.
НМРЛ
У пациентов с нарушениями функции печени легкой степени тяжести (класс А по шкале Чайлд-Пью), изменения начальной дозы не требуется.
ИЛФ и ИЗЛ-ССД
Для пациентов с нарушениями функции печени легкой степени тяжести (класс А по шкале Чайлд-Пью) рекомендованная доза препарата ВАРГАТЕФ составляет 100 мг два раза в день с интервалом примерно в 12 часов.
В случае пациентов с нарушениями функции печени легкой степени тяжести (класс А по шкале Чайлд-Пью) для устранения нежелательных реакций следует рассмотреть возможность временного перерыва в лечении препаратом или окончательного прекращения терапии.
За информацией о дозировании, способе применения и модификации дозы доцетаксела, пожалуйста, обратитесь к соответствующей инструкции по применению этого препарата.
Побочное действие
Частота побочных реакций, приведенных ниже, изложена в соответствии со следующей градацией: очень часто (≥ 1/10); часто (≥ 1/100; < 1/10); нечасто (≥ 1/1000; < 1/100); редко (≥ 1/10000; < 1/1000); очень редко (< 1/10000), неизвестно (частота не может быть оценена по доступным данным). Данные о побочных реакциях также учитывают опыт пострегистрационного применения.
НМРЛ
Наиболее часто сообщавшимися нежелательными реакциями, считавшимися связанными с применением препарата ВАРГАТЕФ, были диарея, повышение активности ферментов печени (АЛТ и ACT) и рвота.
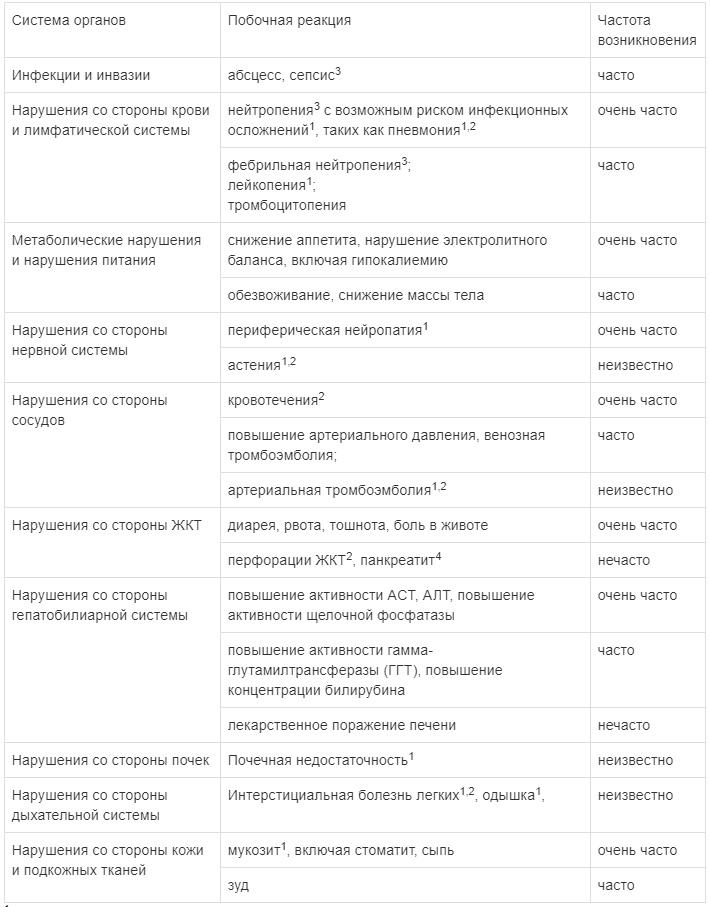 1 — Данные побочные реакции наблюдались при проведении клинических исследований, однако связь с приемом препарата ВАРГАТЕФ не доказана.
1 — Данные побочные реакции наблюдались при проведении клинических исследований, однако связь с приемом препарата ВАРГАТЕФ не доказана.
2 — В клинических исследованиях частота встречаемости данных побочных реакций у пациентов, принимавших нинтеданиб в комбинации с доцетакселом, не превышала частоту встречаемости таковых у пациентов, принимавших плацебо в комбинации с доцетакселом.
3 — Пожалуйста, обратитесь также к инструкции по медицинскому применению доцетаксела.
4 — Случаи панкреатита были зафиксированы у пациентов, принимавших нинтеданиб при лечении ИЛФ и НМРЛ. Большая часть этих случаев была зафиксирована у пациентов с показанием ИЛФ.
Диарея является часто сообщавшимся нежелательным явлением со стороны ЖКТ. Отмечается тесная временная связь между развитием диареи и применением доцетаксела. В клиническом исследовании LUME-Lung 1 диарея легкой и средней степени тяжести отмечалась у большинства пациентов. Диарея ≥ 3 степени тяжести при использовании комбинированного лечения отмечалась у 6,3 % пациентов, тогда как при использовании одного доцетаксела — только у 3,6 % пациентов.
Такие часто сообщающиеся побочные эффекты, как тошнота и рвота, в большинстве случаев были легкой или средней степени тяжести.
По данным клинических исследований, применение препарата ВАРГАТЕФ в комбинации с доцетакселом сопровождалось более частым развитием нейтропении ≥ 3 степени тяжести (по критериям СТСАЕ), чем в случае применения одного доцетаксела.
Повышение активности печеночных ферментов (АЛТ, ACT, ЩФ, гамма-глутамилтрансфераза (ГГТ)) и концентрации билирубина было в большинстве случаев обратимым при уменьшении дозы или прерывании терапии.
Ингибирование VEGFR способно привести к увеличению риска кровотечений. В клинических исследованиях у пациентов с аденокарциномой, принимавших ВАРГАТЕФ. повышение частоты кровотечений было сравнимо в обеих лечебных группах. Самым частым видом кровотечений было носовое кровотечение легкой или средней степени тяжести. Дисбаланса легочных или смертельных кровотечений не наблюдалось, о церебральных кровотечениях не сообщалось. Большинство летальных кровотечений были опухоль — ассоциированными.
В пострегистрационном периоде наблюдались случаи несерьезных и серьезных кровотечений, некоторые из которых приводили к летальному исходу. У пациентов с кровотечениями 3 или 4 степени тяжести следует тщательно оценить пользу и риски продолжения терапии препаратом ВАРГАТЕФ, а также необходимо рассмотреть возможность прекращения данной терапии. При возобновлении терапии препаратом ВАРГАТЕФ рекомендуется использовать сниженную суточную дозу.
Частота артериальных тромбоэмболий в двух лечебных группах исследования LUME-Lung 1 была сравнимой. Пациенты с недавно перенесенным инфарктом миокарда или инсультом из исследования исключались.
Частота перфораций ЖКТ в отдельных лечебных группах в клинических исследованиях была сопоставима.
ИЛФ и ИЗЛ-ССД
Наиболее часто сообщавшимися нежелательными реакциями, связанными с применением нинтеданиба, были диарея, тошнота и рвота, боль в области живота, снижение аппетита, снижение массы тела и повышение активности ферментов печени.
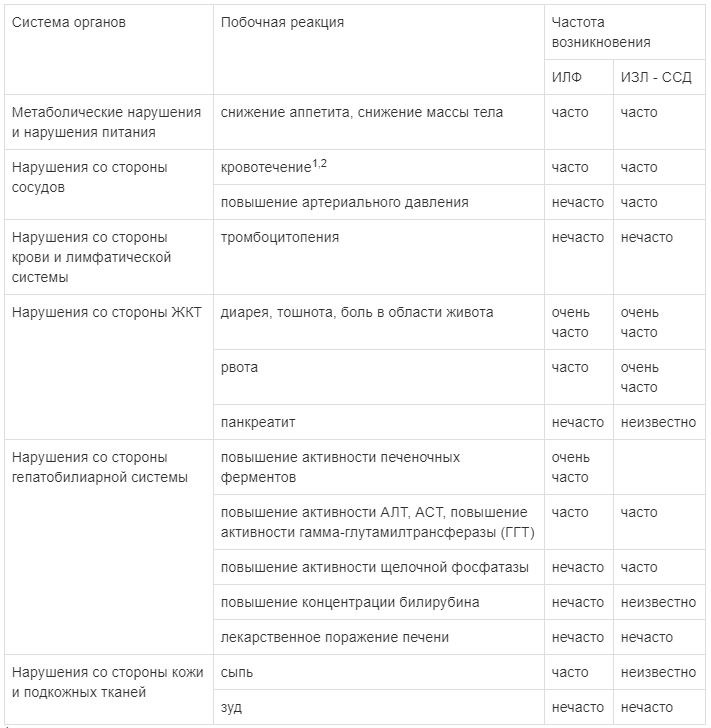 1 — Представленный термин описывает более широкую группу нежелательных явлений, нежели чем отдельное состояние или термин, предусмотренный MedDRA.
1 — Представленный термин описывает более широкую группу нежелательных явлений, нежели чем отдельное состояние или термин, предусмотренный MedDRA.
2 — В пострегистрационном периоде наблюдались случаи несерьезных и серьезных кровотечений, некоторые из которых приводили к летальному исходу.
В клинических исследованиях диарея была наиболее часто репортируемым желудочно-кишечным явлением. У большинства пациентов данные явления были легкой и средней степени тяжести и отмечались на протяжении первых 3 месяцев лечения. В исследованиях INPULSIS у пациентов с ИЛФ диарея отмечалась у 62,4 % по сравнению с 18,4% пациентов, получавших препарат ВАРГАТЕФ или плацебо, соответственно. Диарея стала причиной снижения дозы у 10,7 % пациентов, а прекращения терапии препаратом ВАРГАТЕФ — у 4,4 % пациентов. В исследовании SENSCIS у пациентов с ИЗЛ-ССД диарея отмечалась у 75,7 % в сравнении с 31,6 % пациентов, получавших препарат ВАРГАТЕФ и плацебо, соответственно. Диарея стала причиной снижения дозы препарата ВАРГАТЕФ у 22,2 % пациентов и причиной прекращения терапии препаратом у 6,9 % пациентов.
Тошнота и рвота были часто сообщаемыми нежелательными явлениями. У большинства пациентов отмечалась тошнота и рвота легкой или средней степени тяжести. Тошнота стала причиной прекращения лечения препаратом нинтеданиб у 2 % пациентов. Рвота стала причиной прекращения лечения у 0.8 % пациентов.
Ингибирование VEGFR может быть связано с повышением риска развития кровотечений. В клинических исследованиях частота развития кровотечений у пациентов была немного выше в группе препарата ВАРГАТЕФ (10,3% в исследовании INPULSIS, 11,1 % в исследовании SENSIS), по сравнению с группой плацебо (7.8 % в исследовании INPULSIS, 8,3 % в исследовании SENSIS). Наиболее частыми нежелательными явлениями в виде кровотечений были носовые кровотечения, не относившиеся к категории серьезных. Серьезные кровотечения возникали нечасто и с одинаковой частотой в обеих лечебных группах (плацебо -1,4%; ВАРГАТЕФ — 1,3%). В исследовании SENSCIS серьезные кровотечения возникали нечасто в обеих группах лечения (плацебо — 0,7 %, ВАРГАТЕФ — 1,4 %).
В пострегистрационном периоде наблюдались случаи несерьезных и серьезных кровотечений, некоторые из которых приводили к летальному исходу. Из клинических исследований исключались пациенты с инфарктом миокарда или инсультом в ближайшем анамнезе. В исследовании INPULSIS случаи развития артериальной тромбоэмболии встречались редко: у 0,7 % пациентов, получавших плацебо, и 2,5 % пациентов в группе, получавших препарат ВАРГАТЕФ. В то время как нежелательные реакции в виде ишемической болезни сердца были сравнимы в группах нинтеданиба и плацебо, пациентов, у которых развился инфаркт миокарда, оказалось больше в группе препарата ВАРГАТЕФ (1,6%) по сравнению с группой плацебо (0,5 %). В исследовании SENSCIS случаи развития артериальной тромбоэмболии встречались редко: у 0,7 % пациентов, получавших плацебо, и у 0,7 % пациентов в группе, получавшей препарат ВАРГАТЕФ. Инфаркт миокарда встречался редко в группе плацебо (0,7 %) и не встречался в группе пациентов, получавших препарат ВАРГАТЕФ.
Передозировка
Симптомы
В клинических исследованиях нинтеданиб изучался в наивысшей однократной дозе 450 мг один раз в день. Также зафиксированы случаи передозировки при применении препарата в максимальной дозе 600 мг в течение восьми дней. Наблюдавшиеся нежелательные явления были сопоставимы с известным профилем безопасности нинтеданиба: увеличение активности ферментов печени и нарушения со стороны ЖКТ. Пациенты полностью восстановились после нежелательных явлений. В исследованиях INPULSIS был зафиксирован один случай непреднамеренного повышения дозы до 600 мг 2 раза в день на протяжении 21 дня у пациента с ИЛФ. В период некорректного приема препарата было зафиксировано развитие несерьезного нежелательного явления (назофарингит), которое купировалось в данном периоде без регистрации каких-либо других нежелательных реакций.
Лечение
Специфического антидота на случай передозировки нет. При подозрении на передозировку необходимо отменить ВАРГАТЕФ и проводить симптоматическую терапию.
Взаимодействие с другими лекарственными препаратами
Индукторы/ингибиторы P-gp
Нинтеданиб является субстратом для P-gp. Показано, что совместное применение с активным ингибитором P-gp кетоконазолом увеличивает экспозицию нинтеданиба, судя по величине AUC, в 1,61 раза, а судя по величине Сmах, в 1,83 раза.ли эритромицин) в случае совместного применения с препаратом ВАРГАТЕФ могут увеличивать экспозицию нинтеданиба. У таких пациентов переносимость нинтеданиба должна тщательно мониторироваться.
Активные индукторы P-gp (например, рифампицин, карбамазепин, фенитоин и препараты зверобоя продырявленного) могут уменьшать экспозицию нинтеданиба. Рекомендуется подбор альтернативной сопутствующей терапии с отсутствием или минимальным индуцирующим действием на систему P-gp.
Изоферменты CYP
Изоферменты CYP принимают лишь небольшое участие в биотрансформации нинтеданиба. В доклинических исследованиях нинтеданиб и его метаболиты (свободный кислый метаболит нинтеданиба и его глюкуронид) не ингибировали и не индуцировали изоферменты CYP. Поэтому вероятность лекарственных взаимодействий с нинтеданибом, основанных на влиянии на изоферменты CYP, считается небольшой.
Одновременная терапия с пирфенидоном
Было проведено изучение совместного применения нинтеданиба и пирфенидона у пациентов с ИЛФ в рамках специального фармакокинетического исследования. Пациенты первой группы получали однократную дозу 150 мг нинтеданиба до начала постепенного повышения дозы пирфенидона до максимальной (по 801 мг три раза в сутки), и еще одну дозу нинтеданиба 150 мг по достижении равновесного состояния (в последний день). Пациенты второй группы получали пирфенидон в постоянной дозе 801 мг три раза в сутки. У них была проведена оценка ФК профиля до начала совместной терапии и через 7 дней совместного приема нинтеданиба в дозировке 150 мг два раза в сутки. В первой группе скорректированные соотношения среднегеометрических значений (90 % доверительный интервал (ДИ) составляли 93% (57-151%) и 96% (70-131%) для показателей Сmах и AUCo-tz нинтеданиба соответственно (n=12). Во второй группе скорректированные соотношения среднегеометрических значений (90 % ДИ) составляли 97% (86-110%) и 95% (86-106 %) для показателей Cmax,ss и AUCτ,ss пирфенидона соответственно (n=12).
На основании полученных результатов можно сделать вывод об отсутствии признаков значимого фармакокинетического взаимодействия между нинтеданибом и пирфенидоном при совместном применении.
Одновременное применение с другими препаратами
Одновременное применение нинтеданиба с доцетакселом (75 мг/м2) в существенной степени не изменяет фармакокинетику этих препаратов.
Одновременное применение нинтеданиба с бозентаном не изменяет фармакокинетику нинтеданиба.
Возможность взаимодействий нинтеданиба с гормональными контрацептивными средствами не изучалась.
Одновременный прием с пищей
ВАРГАТЕФ рекомендуется принимать одновременно с пищей (см. раздел «Фармакокинетика»).
Особые указания
Желудочно-кишечные расстройства
— диарея
Лечение диареи (адекватная гидратация и антидиарейные лекарственные средства, например, лоперамид) следует проводить при появлении первых признаков. В случае развития диареи может потребоваться прерывание лечения, снижение дозы или прекращение терапии.
— тошнота и рвота
В случае сохранения симптомов тошноты и рвоты, несмотря на симптоматическое лечение (включая противорвотную терапию), может потребоваться снижение дозы, прерывание лечения или прекращение терапии.
Диарея и рвота могут приводить к обезвоживанию с нарушением или без нарушения водно-электролитного баланса, что может приводить к нарушениям функции почек. В случае обезвоживания рекомендуется восстановление водно-электролитного баланса.
Если возникают существенные желудочно-кишечные нежелательные явления, то необходимо проведение мониторирования концентрации электролитов в крови.
Нейтропения и сепсис
Во время терапии НМРЛ препаратом ВАРГАТЕФ, в частности при комбинации его с доцетакселом, необходимо проводить мониторинг форменных элементов крови на предмет развития нейтропении и возможных последующих осложнений в виде сепсиса или фебрильной нейтропении. Частое мониторирование всех форменных элементов крови следует осуществлять в начале каждого курса лечения у пациентов, получающих лечение нинтеданибом в комбинации с доцетакселом, в период наименьших значений нейтрофилов, а также при наличии клинических показаний после окончания последнего курса терапии данной комбинацией.
Нарушения функции печени
Безопасность и эффективность препарата не изучались у пациентов с нарушениями функции печени средней (класс В по шкале Чайлд-Пью) или тяжелой (класс С по шкале Чайлд-Пью) степени тяжести. Поэтому у таких пациентов применение препарата ВАРГАТЕФ не рекомендуется.
НМРЛ
В связи с повышением концентрации препарата в крови риск развития нежелательных явлений может быть выше у пациентов с легкими нарушениями функции печени (класс А по шкале Чайлд-Пью).
При проведении терапии нинтеданибом наблюдались случаи лекарственного поражения печени. В пострегистрационном периоде были получены сообщения о тяжелых формах лекарственного поражения печени с летальным исходом.
После начала терапии рекомендуется тщательный контроль активности печеночных трансаминаз, щелочной фосфатазы и концентрации билирубина (периодически, во время начала комбинированной терапии с доцетакселом, т.е. в начале каждого лечебного курса). Если отмечается существенное повышение активности печеночных ферментов, может потребоваться прерывание лечения, уменьшение дозы или прекращение терапии препаратом ВАРГАТЕФ.
При начале комбинированного лечения препаратом ВАРГАТЕФ и доцетакселом должны определяться уровни трансаминаз, ЩФ и билирубина. Эти показатели следует мониторировать в зависимости от клинических показаний или периодически во время лечения, например, в фазе комбинации с доцетакселом в начале каждого курса терапии и ежемесячно, если прием препарата ВАРГАТЕФ продолжается в виде монотерапии после прекращения терапии доцетакселом.
Если выявляется соответствующее повышение ферментов печени, может потребоваться перерыв в лечении, снижение дозы или прекращение терапии препаратом ВАРГАТЕФ (см. раздел «Способ применения и дозы»/ Таблица 2). Следует проводить поиск альтернативных причин повышения активности ферментов печени и принятие соответствующих мер при необходимости.
В случае повышения активности ферментов печени (АСТ/АЛТ) более чем в 3 раза по сравнению с ВЕН в сочетании с повышением уровня билирубина в 2 и более раза по сравнению с ВЕН, и повышением ЩФ менее чем в 2 раза по сравнению с ВГН, терапию препаратом ВАРГАТЕФ следует прервать. Если не будет установлена альтернативная причина изменений этих лабораторных показателей, препарат ВАРГАТЕФ следует окончательно отменить.
Для пациентов женского пола и азиатского происхождения характерен более высокий риск повышения активности печеночных ферментов.
Увеличение экспозиции нинтеданиба характеризовалось линейной зависимостью от возраста пациента, а также было обратно пропорционально массе тела, что также может повлечь за собой более высокий риск повышения активности печеночных ферментов. У пациентов с этими факторами риска рекомендуется тщательный контроль показателей функции печени.
ИЛФ и ИЗЛ-ССД
В связи с повышением концентрации препарата в крови риск развития нежелательных явлений может быть выше у пациентов с легкими нарушениями функции печени (класс А по шкале Чайлд-Пью). Пациенты с легкими нарушениями функции печени (класс А по шкале Чайлд-Пью) должны получать сниженную дозу препарата ВАРГАТЕФ.
При проведении терапии нинтеданибом наблюдались случаи лекарственного поражения печени. В пострегистрационном периоде были получены сообщения о несерьезных и серьезных случаях лекарственного поражения печени, включая тяжелые формы лекарственного поражения печени с летальным исходом.
Большая часть нарушений со стороны печени наблюдаются в течение первых 3-х месяцев терапии. Таким образом, рекомендуется оценивать активность печеночных трансаминаз и концентрацию билирубина до начала терапии препаратом ВАРГАТЕФ регулярно в течение первых трех месяцев терапии, а затем периодически во время лечения (например, при каждом визите пациента) или по клиническим показаниям.
Повышение активности печеночных ферментов (АЛТ, ACT, ЩФ. гамма-глутамилтрансфераза (ГГТ)) и билирубина было в большинстве случаев обратимым при уменьшении дозы или прерывании терапии.
В случае повышения уровня трансаминаз (ACT или АЛТ) более чем в 3 раза выше ВГН рекомендовано уменьшить дозу или прервать терапию препаратом ВАРГАТЕФ и проводить мониторирование пациента. Как только показатели трансаминаз вернутся к исходному уровню, доза препарата ВАРГАТЕФ может быть вновь повышена до полной (150 мг два раза в день) или лечение может быть возобновлено в сниженной дозе (100 мг два раза в день), которая впоследствии может быть повышена до полной дозы. Если повышение каких-либо показателей функции печени сопровождается клиническими признаками или симптомами повреждения печени, например, желтухой, лечение препаратом следует окончательно прекратить. Следует провести поиск альтернативных причин повышения активности ферментов печени.
Для пациентов с низкой массой тела (<65 кг), лиц азиатского происхождения и пациентов женского пола характерен более высокий риск повышения активности печеночных ферментов.
Увеличение экспозиции нинтеданиба характеризовалось линейной зависимостью от возраста пациента, что также может повлечь за собой более высокий риск повышения активности печеночных ферментов.
У пациентов с этими факторами риска рекомендуется тщательный контроль показателей функции печени.
Риск развития кровотечений
Данных о применении препарата ВАРГАТЕФ у пациентов с наследственной предрасположенностью к кровотечениям (например, болезнь фон Виллебранда) не имеется.
НМРЛ
Пациенты с недавно отмечавшимся легочным кровотечением (> 2,5 мл крови), а также пациенты с центрально расположенными опухолями и рентгенологическими признаками локальной инвазии крупных сосудов или с рентгенологическими признаками наличия полостей или некротических изменений опухоли исключались из клинических исследований. Поэтому применение препарата ВАРГАТЕФ у таких пациентов не рекомендуется.
— метастазы в головной мозг
Увеличения частоты церебральных кровотечений у пациентов с ранее адекватно лечеными метастазами в головной мозг (стабильными в течение ≥ 4 недель до начала лечения препаратом ВАРГАТЕФ) не наблюдалось. Однако такие пациенты должны тщательно мониторироваться в отношении признаков и симптомов церебральных кровотечений.
Пациенты с активными метастазами в головной мозг исключались из клинических исследований, применение препарата ВАРГАТЕФ у них не рекомендуется.
— терапия антикоагулянтами
В клинические исследования включались пациенты, получавшие длительную терапию низкомолекулярными гепаринами в низких дозах или ацетилсалициловой кислотой в дозах ≤ 325 мг/сут. Увеличения частоты кровотечений у таких пациентов не наблюдалось. Данных о применении препарата ВАРГАТЕФ у пациентов, предварительно получавших лечение антикоагулянтами в более высоких дозах, не имеется. Пациентам, у которых во время лечения препаратом ВАРГАТЕФ развивались тромбоэмболические нарушения, в связи с чем требовалась терапия антикоагулянтами, разрешалось продолжить прием препарата ВАРГАТЕФ, при этом увеличения частоты кровотечений не отмечалось. У пациентов, принимающих такие антикоагулянты, как варфарин или фенпрокумон, необходимо регулярно проверять протромбиновое время, международное нормализованное отношение (МНО) или следить за клиническими признаками кровотечений.
ИЛФ и ИЗЛ-ССД
В клинические исследования не включались пациенты с известным риском развития кровотечений, включая пациентов с наследственной предрасположенностью к кровотечениям или пациентов, получающих антикоагулянтную терапию в высоких дозах. Следовательно, данной категории пациентов лечение препаратом ВАРГАТЕФ должно быть назначено только в том случае, если потенциальная польза проводимой терапии превышает потенциальный риск.
Артериальная тромбоэмболия
Необходимо соблюдать осторожность при лечении пациентов с высоким сердечнососудистым риском, включая ишемическую болезнь сердца. Следует рассмотреть возможность перерыва в лечении пациентов, у которых развились симптомы острой ишемии миокарда.
Венозная тромбоэмболия
НМРЛ
У пациентов, получающих ВАРГАТЕФ, отмечался повышенный риск венозных тромбоэмболий, в том числе тромбоза глубоких вен. Пациенты должны тщательно мониторироваться в отношении тромбоэмболических нарушений. Пациентам с опасными для жизни венозными тромбоэмболиями ВАРГАТЕФ необходимо отменить.
ИЛФ и ИЗЛ-ССД
В клинических исследованиях не наблюдалось повышенного риска развития венозных тромбоэмболических осложнений. Однако в связи с особенностями механизма действия нинтеданиба. у пациентов может отмечаться повышенный риск развития тромбоэмболических явлений.
Перфорации ЖКТ
Частота перфораций ЖКТ в отдельных лечебных группах в клинических исследованиях была сопоставима. Основываясь на механизме действия препарата ВАРГАТЕФ. у пациентов возможен повышенный риск перфораций ЖКТ. В пострегистрационном периоде были получены сообщения о случаях перфорации ЖКТ, некоторые из которых приводили к летальному исходу. Особое внимание должно уделяться лечению пациентов, которые ранее подвергались абдоминальным хирургическим вмешательствам, или перенесших перфорацию полого органа в недавнем анамнезе, а также пациентов с ИЛФ, имеющих в анамнезе пептическую язву, дивертикулез или получающих сопутствующую терапию глюкокортикостероидами или НПВП. В связи с этим ВАРГАТЕФ может применяться только как минимум через 4 недели после больших хирургических, включая абдоминальные, вмешательств. В случае возникновения гастроинтестинальной перфорации терапия препаратом ВАРГАТЕФ должна прекращаться.
Нарушение заживления ран
Нинтеданиб, в связи с особенностями механизма действия, может нарушать заживление ран. В клинических исследованиях увеличения частоты нарушений заживления ран не наблюдалось. Специальных исследований, в которых бы изучалось влияние нинтеданиба на заживление ран, не проводилось. Поэтому лечение должно начинаться или возобновляться (если осуществлялся перерыв в связи с хирургическим вмешательством) с учетом клинического мнения об адекватности заживления раны.
Особые группы пациентов
В исследовании LUME-Lung 1 у пациентов с массой тела менее 50 кг, принимавших нинтеданиб в сочетании с доцетакселом, наблюдалась более высокая частота развития серьезных нежелательных явлений, чем у пациентов с массой тела ≥ 50 кг, хотя число пациентов с массой тела менее 50 кг было небольшим. Поэтому рекомендуется тщательное наблюдение за пациентами с массой тела менее 50 кг.
Влияние препарата на способность управления транспортными средствами, механизмами
Исследований по влиянию препарата на способность управлять транспортными средствами и занятию другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций не проводилось.
Во время применения препарата ВАРГАТЕФ пациентам нужно рекомендовать соблюдать осторожность при управлении транспортными средствами или механизмами.
Форма выпуска
Капсулы 100 мг
По 10 капсул в А1/А1 блистер. 6 блистеров в пачку картонную с инструкцией по медицинскому применению.
или
По 10 капсул в А1/А1 блистер. 6 блистеров в пачку картонную с инструкцией по медицинскому применению. По 2 пачки картонные в пленку из полипропилена.
Капсулы 150 мг
По 10 капсул в А1/А1 блистер. 6 блистеров в пачку картонную с инструкцией по медицинскому применению.
Условия хранения
Хранить в оригинальной упаковке при температуре не выше 25°С.
Хранить в недоступном для детей месте.
Срок годности
3 года.
Не использовать после истечения срока годности.
Условия отпуска
Отпускается по рецепту.
Наименование и адрес юридического лица, на имя которого выдано регистрационное удостоверение
Берингер Ингельхайм Интернешнл ГмбХ
55216, Бингер Штрассе 173, Ингельхайм-на-Рейне, Германия
Наименование и адрес места осуществления производства лекарственного препарата
Производитель готовой лекарственной формы
Каталент Германия Эбербах ГмбХ
69412, Гаммельсбахер Штр. 2, Эбербах, Германия
Первичная, вторичная упаковка и выпускающий контроль качества
Берингер Ингельхайм Фарма ГмбХ и Ко.КГ
55216, Бингер Штрассе 173, Ингельхайм-на-Рейне, Германия
Получить дополнительную информацию о препарате, а также направить свои претензии и информацию о нежелательных явлениях можно по следующему адресу в России
ООО «Берингер Ингельхайм»
125171, Москва, Ленинградское шоссе, 16А, стр.З
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
МНН: Нинтеданиб
Производитель: Каталент Германия Эбербах ГмбХ
Анатомо-терапевтическо-химическая классификация: Нинтеданиб
Номер регистрации в РК:
РК-ЛС-5№022499
Информация о регистрации в РК:
09.11.2021 — 09.11.2031
- Скачать инструкцию медикамента
Торговое название
ВАРГАТЕФ®
Международное непатентованное название
Нинтеданиб
Лекарственная форма
Мягкие
капсулы 100 мг, 150 мг
Состав
Одна
капсула 100 мг содержит
активное
вещество —
нинтеданиба этансульфонат 120,40 мг, что соответствует 100,00 мг
нинтеданиба основания,
вспомогательные
вещества:
триглицериды средней цепи, твердый жир, лецитин,
оболочка
капсулы:
желатин, глицерин 85%, титана диоксид (Е171), железа оксид красный
Е172 в смеси с глицерином 85%, железа оксид желтый Е172 в смеси с
глицерином 85%, чернила Опакод®
тип S-1-17823.
Одна
капсула 150 мг содержит
активное
вещество:
нинтеданиба этансульфонат –180,60 мг, что соответствует 150,00
мг нинтеданиба основания,
вспомогательные
вещества:
триглицериды средней цепи, твердый жир, лецитин,
оболочка
капсулы:
желатин, глицерин 85%, титана диоксид (Е171), железа оксид красный
Е172 в смеси с глицерином 85%, железа оксид желтый Е172 в смеси с
глицерином 85%, чернила Опакод®
тип S-1-17823.
Описание
100
мг: Мягкие
желатиновые капсулы продолговатой формы, непрозрачные, персикового
цвета, с нанесенными черным цветом символом компании и цифрой «100».
Содержимое капсул – вязкая суспензия ярко-желтого цвета;
150
мг:
Мягкие желатиновые капсулы продолговатой формы, непрозрачные,
коричневого цвета, с нанесенными черным цветом символом компании и
цифрой «150». Содержимое капсул – вязкая суспензия
ярко-желтого цвета.
Фармакотерапевтическая группа
Противоопухолевые
препараты. Противоопухолевые препараты другие. Ингибиторы
протеинкиназы. Нинтеданиб
Код
АТХ L01XE31
Фармакологические свойства
Фармакокинетика
Всасывание.
Cmax
нинтеданиба в плазме крови достигается приблизительно через 2-4 часа
после приема препарата во время еды (диапазон 0,5 – 8 часов).
Абсолютная биодоступность дозы 100 мг составляет у здоровых
добровольцев 4,69% (90% доверительный интервал (ДИ): 3,615 –
6,078).
Установлено,
что экспозиция нинтеданиба увеличивается пропорционально дозе (в
диапазонах доз 50 — 450 мг один раз в день и 150 — 300 мг два раза в
день). Устойчивые концентрации в плазме крови достигаются, как
максимум, в течение одной недели после начала приема.
Экспозиция
нинтеданиба увеличивается после приема пищи примерно на 20% по
сравнению с приемом препарата натощак (ДИ: 95,3 – 152,5%), а
всасывание замедляется. Медиана времени достижения максимальной
концентрации в плазме крови натощак – 2,00 часа, после еды –
3,98 часа.
Распределение.
Распределение
нинтеданиба осуществляется путем двухфазной кинетики. После
внутривенной инфузии во время терминальной фазы наблюдается большой
объем распределения (Vd) 1050 л, геометрический коэффициент
вариации (gCV) 45,0 %.
Связывание
нинтеданиба с белками плазмы человека in
vitro
считается значительным, связанная фракция составляет 97,8%. Основным
белком, участвующим в связывании, считается альбумин сыворотки крови.
Нинтеданиб преимущественно распределяется в плазме, соотношение
кровь/плазма составляет 0,869.
Нинтеданиб
является субстратом для гликопротеина-P (P-gp). Показано, что
нинтеданиб in
vitro
не является субстратом или ингибитором полипептидных переносчиков
органических анионов (OATP-1B1, OATP-1B3, OATP-2B1), переносчика
органических катионов-2 (OCT-2) или белка, ассоциированного с
множественной лекарственной устойчивостью-2 (MRP-2). Нинтеданиб также
не является субстратом для белка резистентности рака молочной железы
(BCRP). In
vitro
было установлено, что нинтеданиб обладает слабой ингибирующей
активностью в отношении OCT-1, BCRP и P-gp, что, как считается, имеет
небольшую клиническую значимость. Такое же заключение сделано в
отношении нинтеданиба как субстрата для OCT-1.
Метаболизм.
Основной
реакцией, участвующей в метаболизме нинтеданиба, является
гидролитическое расщепление с помощью эстераз, что приводит к
образованию свободного кислого метаболита нинтеданиба. В
доклинических исследованиях in vivo установлено, что данный метаболит
не обладает эффективностью, несмотря на влияние на целевые рецепторы
препарата. В дальнейшем он глюкуронизируется ферментами
уридин-дифосфат-глюкуронозилтрасферазами (UGT 1A1, UGT 1A7, UGT 1A8 и
UGT 1A10) с образованием глюкуронида.
Считается,
что биотрансформация нинтеданиба с участием изоферментов CYP
происходит только в небольшой степени, основное участие принимает
изофермент CYP 3A4. В исследовании ADME у человека основной
метаболит, образующийся с участием изоферментов CYP, обнаружить в
плазме не удалось. По данным исследования in
vitro
CYP-зависимый метаболизм составляет примерно 5%, тогда как
расщепление, осуществляемое эстеразами, составляет 25%.
Выведение.
Общий
клиренс из плазмы после внутривенной инфузии составляет 1,390 мл/мин
(gCV 28,8%). Экскреция почками неизмененного препарата в течение 48
часов после приема нинтеданиба внутрь составляет примерно 0,05 % от
величины дозы (gCV 31,5%), а после внутривенного введения –
примерно 1,4% (gCV 24,2%); почечный клиренс составляет 20 мл/мин (gCV
32,6%). После приема внутрь [14C]-нинтеданиба радиоактивный материал
выводился преимущественно с желчью и обнаруживался в кале (93,4 % от
величины дозы, gCV 2,61%). Вклад почечной экскреции в общий клиренс
составляет 0,649% от величины дозы (gCV 26,3%). Выведение считается
полным (более 90%) через 4 дня после приема. Период полувыведения
нинтеданиба составляет от 10 до 15 часов (gCV примерно 50%).
Линейность/нелинейность.
Фармакокинетика нинтеданиба может считаться линейной в отношении
времени (т.е. данные, полученные в случае применения однократной
дозы, могут экстраполироваться на данные, полученные в результате
многократного применения). После многократного применения препарата
накопление составляет 1,04 при оценке максимальной концентрации
(Cmax)
и 1,38 при оценке площади под кривой «концентрация-время»
(AUC).
Остаточные концентрации нинтеданиба остаются стабильными в течение
одного года и более.
Транспорт.
Нинтеданиб
является субстратом Р-гликопротеина (P-gP), более подробная
информация по данному взаимодействию приведена в разделе
Лекарственные взаимодействия. Было показано, что нинтеданиб не
является субстратом или ингибитором OATP-1B1, OATP-1B3, OATP-2B1,
ОСТ-2 или MRP-2
in
vitro.
Нинтеданиб также не является субстратом BCRP. Наблюдался лишь слабый
ингибирующий потенциал на OСТ-1, BCRP и P-gP in
vitro,
что имеет низкую клиническую значимость, что также применимо для
нинтеданиба как субстрата ОСТ-1.
Фармакокинетика
у особых групп пациентов
Фармакокинетические
свойства нинтеданиба были сопоставимы у здоровых добровольцев,
пациентов с ИЛФ и НМРЛ. Основываясь на результатах популяционного
фармакокинетического анализа у пациентов с ИЛФ и НМРЛ и описательных
исследований, на воздействие нинтеданиба не влиял пол (с учетом массы
тела), нарушения функции почек легкой и средней степени тяжести
(рассчитанная по клиренсу креатинина), метастазы в печени, общее
состояние больного (оценка по опроснику Восточной Объединенной
Онкологической Группы, Eastern Cooperative Oncology Group (ECOG)),
употребление алкоголя, или генотип Р-гликопротеина. Популяционный
фармакокинетический анализ выявил умеренное влияние пола, массы тела
и расовой принадлежности на воздействие нинтеданиба. В связи с тем,
что наблюдалась высокая межиндивидуальная вариабельность воздействия,
эти влияния не считались клинически значимыми. Тем не менее,
рекомендуется тщательное мониторирование пациентов, у которых
выявляется несколько таких факторов риска, представленных ниже.
Возраст
Экспозиция
нинтеданиба линейно увеличивается с возрастом. У 45-летних пациентов
(5-й процентиль) значение AUCτ,ss
(в равновесном состоянии на период дозирования) было ниже на 16%, а у
76-летних пациентов (95-й процентиль) выше на 13% по сравнению с
пациентами, медиана возраста которых составляла 62 года. Диапазон
возраста, оценивавшийся в ходе анализа, составлял 29-85 лет; возраст
более 75 лет отмечался примерно у 5% популяции пациентов. Основываясь
на результатах популяционного фармакокинетического анализа,
увеличение воздействия нинтеданиба примерно на 20 — 25% наблюдалось у
пациентов ≥ 75 лет по сравнению с пациентами моложе 65 лет.
Аналогичные
исследования у детей не проводились.
Масса
тела
Наблюдается
обратная корреляция между массой тела и экспозицией нинтеданиба. У
пациентов с массой тела 50 кг (5-й процентиль) величина AUCτ,ss
увеличивалась на 25%, а у пациентов с массой тела 100 кг (95-й
процентиль) уменьшалась на 19% по сравнению с пациентами, медиана
массы тела которых составляла 71,5 кг.
Раса
Средняя
геометрическая экспозиция нинтеданиба на 33% выше у пациентов —
китайцев, тайванцев и индийцев, а у пациентов — корейцев — на 22%
ниже, чем у пациентов европеоидной расы (с поправкой на массу тела).
Данные в отношении пациентов негроидной расы являются очень
ограниченными, диапазон этих данных сходен с пациентами европеоидной
расы.
Нарушения
функции печени
Фармакокинетические
показатели нинтеданиба были получены у пациентов с нарушениями
показателей функции печени (повышение активности
аспартатаминотрансферазы (АСТ), аланинаминотранферазы (АЛТ) и
концентрации билирубина). У пациентов с исходным повышением
активности АСТ и АЛТ (до 10 раз по сравнению с верхней границей
нормы) и концентрации билирубина (до 1,5 раз по сравнению с верхней
границей нормы) наблюдается тенденция к увеличению экспозиции
нинтеданиба (по сравнению с пациентами с нормальными значениями
активности АСТ, АЛТ и концентрации билирубина). Ограниченные данные о
пациентах с повышенной активностью АЛТ или АСТ, превышавшим верхнюю
границу нормы более чем в 10 раз, и повышением концентрации
билирубина, превышавшим верхнюю границу нормы более чем в 1,5 раза,
не позволили сделать окончательные выводы.
Одновременно
лечение с пирфенидоном.
В
небольшом исследовании параллельных групп японских пациентов с
идиопатическим
легочным фиброзом (ИЛФ)
(13 пациентов принимали нинтеданиб на пике хронического лечения
стандартными дозами пирфенидона; 11 пациентов принимали нинтеданиб в
монотерапии). Воздействие нинтеданиба снизилось до 68,3% в пересчете
на AUC, и 59,2% в пересчете на Cmax
при одновременном приеме с пирфенидоном по сравнению с приемом
нинтеданиба в монотерапии.
Нинтеданиб
не оказывает никакого эффекта на фармакокинетические показатели
пирфенидона.
Фармакодинамика
Механизм
действия
Нинтеданиб
— это малая молекула, ингибитор рецепторов тирозинкиназы, включая
рецепторы фактора роста эндотелия сосудов 1-3 (VEGFR 1-3), рецепторы
тромбоцитарного фактора роста α и ß (PDGFR α и ß)
и рецепторы фактора роста фибробластов 1-3 (FGFR 1-3), через которые
реализуется активность киназы. Нинтеданиб конкурентно взаимодействует
с АТФ-связывающим участком этих рецепторов и блокирует
внутриклеточную передачу сигналов, которая крайне важна для
пролиферации и выживания эндотелиальных, а также периваскулярных
клеток (перицитов и гладкомышечных клеток сосудов), а также особенно
важна для пролиферации, миграции и трансформации фибробластов,
представляющих основные патологические механизмы идиопатического
легочного фиброза (ИЛФ). Кроме того, нинтеданиб ингибирует Flt-3
(FMS-подобную тирозинпротеинкиназу), Lck (лимфоцит специфическую
тирозинпротеинкиназу), Lyn (тирозинпротеин киназу Lyn) и Src
(прото-онкоген тирозинпротеинкиназу SRC) киназы.
Фармакодинамические
эффекты
Опухолевый
ангиогенез является процессом, который вносит существенный вклад в
рост, прогрессирование и образование метастазов опухоли. Этот процесс
преимущественно запускается проангиогенными факторами, такими, как
фактором роста эндотелия сосудов и основным фактором роста
фибробластов (VEGF и bFGF), секретируемыми опухолевыми клетками,
чтобы привлечь эндотелиальные и периваскулярные клетки хозяина и
облегчить доставку кислорода и питательных веществ через сосудистую
систему. Нинтеданиб эффективно противодействует образованию и
развитию сосудистой системы опухоли, приводит к замедлению и
остановке роста опухоли.
Активация
сигнальных каскадов FGFR и PDGFR также особенно важна для
пролиферации, миграции легочных фибробластов/миофибробластов,
характерных клеток в патогенезе ИЛФ. Потенциальное воздействие на
ингибирование VEGFR в патогенезе ИЛФ в настоящее время полностью не
выяснено. Считается, что на молекулярном уровне нинтеданиб ингибирует
сигнальные каскады FGFR и PDGFR, играющие роль в пролиферации и
миграции легочных фибробластов, путем взаимодействия с АТФ-зоной
связывания внутриклеточного домена рецептора, таким образом,
вмешиваясь в процессы перекрестной активации путем
аутофосфорилирования гомодимеров рецепторов. In
vitro таргетные
рецепторы ингибировались нинтеданибом в малых концентрациях,
измеряемых наномолями. В человеческих легочных фибробластах,
полученных от пациентов с ИЛФ, нинтеданиб ингибировал PDGF-, FGF- и
VEGF стимулированную пролиферацию клеток, значения полумаксимальной
эффективной концентрации (EC50)
составили 11 нмоль/л, 5,5 нмоль/л и менее чем 1 нмоль/л,
соответственно. В концентрации от 100 до 1000 нмоль/л нинтеданиб
также ингибировал PDGF-, FGF- и VEGF стимулированную миграцию
фибробластов и TGF-β2 (трансформирующий фактор роста
β2)-индуцированную трансформацию фибробластов в миофибробласты.
Кроме того, полагают, что противовоспалительная активность
нинтеданиба ограничивает фиброзную стимуляцию путем снижения
фиброзных медиаторов, таких как интерлейкины (ИЛ-1β и ИЛ-6).
Роль антиангиогенной активности нинтеданиба в механизме действия
препарата при фиброзных заболеваниях легких в настоящее время не
ясна. В исследованиях in
vivo
было показано, что нинтеданиб обладает высокой антифиброзной и
противовоспалительной активностью.
Показания к применению
—
идиопатический легочный фиброз (идиопатический фиброзирующий
альвеолит) (ИЛФ); для лечения и замедления прогрессирования
заболевания.
—
местнораспространенный, метастатический или рецидивирующий
немелкоклеточный рак легкого (аденокарцинома) (НМРЛ) после
химиотерапии первой линии в комбинации с доцетакселом;
Способ применения и дозы
Капсулы
принимают внутрь во время еды. Капсулы следует проглатывать целиком,
запивая водой, не разжевывая и не разламывая.
ИЛФ
Лечение
препаратом ВАРГАТЕФ следует назначать и проводить под контролем
врача, имеющего опыт диагностики и лечения ИЛФ.
Рекомендуемая
доза препарата составляет 150 мг два раза в день, приблизительно
через каждые 12 часов.
Максимальная
суточная доза составляет 300 мг.
Пропуск
дозы
Если
какая-либо доза препарата ВАРГАТЕФ была пропущена, то следует
продолжить прием препарата в изначально рекомендуемой дозе по
расписанию следующего приема препарата. Если доза была пропущена,
пациент не должен принимать дополнительную дозу препарата. Пациент не
должен превышать рекомендованную максимальную суточную дозу в 300 мг.
Изменение
дозы в случае развития побочных реакций
При
развитии нежелательных реакций таких, как диарея, тошнота и рвота в
дополнение к симптоматической терапии, при необходимости,
рекомендуется снижение дозы или временное прерывание лечения до тех
пор, пока нежелательная реакция не снизится до уровня, который
позволит возобновить терапию. Лечение препаратом ВАРГАТЕФ может быть
возобновлено в полной дозе (150 мг 2 раза в день) или в сниженной
дозе (100 мг 2 раза в день). Если пациент не переносит дозу препарата
100 мг 2 раза в день, лечение препаратом ВАРГАТЕФ следует прекратить.
В
случае повышения уровня трансаминаз (АСТ или АЛТ) более чем в 3 раза
выше верхней границы нормы рекомендовано прервать терапию препаратом
ВАРГАТЕФ. Как только показатели вернутся к нормальному значению,
лечение препаратом ВАРГАТЕФ можно возобновить в сниженной дозе (100
мг 2 раза в день), которая впоследствии может быть увеличена до
полной дозы (150 мг 2 раза в день).
НМРЛ
Лечение
препаратом ВАРГАТЕФ следует назначать и проводить под контролем
врача, имеющего опыт в назначении противоопухолевой терапии.
Рекомендуемая
доза препарата ВАРГАТЕФ составляет 200 мг два раза в день с
интервалом примерно в 12 часов, со 2 по 21 день стандартного
21-дневного цикла лечения доцетакселом.
ВАРГАТЕФ
не должен применяться в день начала химиотерапии доцетакселом, т.е. в
1 день лечения.
Максимальная
рекомендуемая суточная доза составляет 400 мг.
После
окончания применения доцетаксела можно продолжить терапию препаратом
ВАРГАТЕФ до тех пор, пока сохраняется клинический эффект, или до
развития неприемлемой токсичности.
Пропуск
дозы
Если
какая-либо доза препарата ВАРГАТЕФ была пропущена, то следует
продолжить прием препарата в изначально рекомендуемой дозе по
расписанию следующего приема препарата. Индивидуальная суточная доза
не должна выходить за диапазон рекомендуемой дозы в целях компенсации
пропущенных доз. Если доза пропущена, пациент не должен принимать
дополнительную дозу препарата. Пациент не должен превышать
рекомендованную максимальную суточную дозу в 400 мг.
Изменение
дозы в случае развития нежелательных реакций
В
качестве первоначальной меры для устранения побочных эффектов
рекомендуется временный перерыв в лечении препаратом ВАРГАТЕФ до тех
пор, пока нежелательная реакция не снизится до уровня, который
позволит возобновить терапию (см. Таблицу 1 и 2). Лечение может
возобновляться в уменьшенной дозе.
Для
обеспечения индивидуальной безопасности и переносимости рекомендуется
снижение суточной дозы препарата на 100 мг (то есть, уменьшение
разовой дозы на 50 мг), как это описывается в Таблицах 1 и 2. Если
побочная реакция (реакции) сохраняется, то есть, если пациент не
переносит препарат в дозе 100 мг два раза в день, лечение препаратом
нужно окончательно прекратить.
В
случае специфического повышения активности АСТ и/или АЛТ более чем в
3 раза по сравнению с верхней границей нормы (ВГН) в сочетании с
повышением концентрации общего билирубина в 2 и более раза по
сравнению с ВГН и щелочной фосфатазы (ЩФ) менее чем в 2 раза по
сравнению с ВГН (см. таблицу 2), применение препарата ВАРГАТЕФ
следует прекратить. Если не будет установлена альтернативная причина
нарушений, то препарат ВАРГАТЕФ должен быть окончательно отменен
Таблица
1. Информация об изменении дозы в случае развития побочных реакций.
|
Побочная |
Изменение |
|
Диарея или
диарея |
После
При |
|
Рвота и/или
Тошнота |
|
|
Другая |
*
Общие терминологические критерии для нежелательных явлений — CTCAE
(Common Terminology Criteria for Adverse Events)
Таблица
2. Информация об изменении дозы в случае повышения активности АСТ
и/или АЛТ и повышения концентрации билирубина.
|
Повышение |
Изменение |
|
Повышение или
Повышение |
После |
|
Повышение |
Если |
Особые
группы пациентов
Детский
возраст
Безопасность
и эффективность препарата ВАРГАТЕФ у пациентов детского возраста в
клинических исследованиях не изучалась.
Пожилой
возраст (≥ 65 лет)
Не
отмечено никаких общих различий по безопасности и эффективности
применения препарата у пожилых пациентов по сравнению с пациентами
моложе 65 лет. Снижать дозу препарата на основании возраста пациента
не требуется. Пациентам
≥ 75 лет потребуется снижение дозировки в случае развития
нежелательных реакций.
Раса
и масса тела
Основываясь
на данных популяционного фармакокинетического анализа, исходная
коррекция дозы препарата ВАРГАТЕФ в зависимости от расы и массы тела
не требуется.
Нарушения
функции почек
Через
почки выводится менее 1% однократной дозы нинтеданиба. У пациентов с
нарушениями функции почек легкой или средней степени тяжести
изменения начальной дозы не требуется. У пациентов с тяжелыми
нарушениями функции почек (клиренс креатинина < 30 мл/мин)
безопасность,
эффективность и фармакокинетика нинтеданиба не изучались.
Нарушения
функции печени
Нинтеданиб
выводится преимущественно с желчью (через кишечник)
(> 90%). У пациентов с нарушениями функции печени легкой степени
тяжести (класс А по шкале Чайлд-Пью),
изменения начальной дозы не требуется. У пациентов с нарушениями
функции печени средней и тяжелой степени тяжести
(классы
B и C по шкале Чайлд-Пью) безопасность и эффективность нинтеданиба
не
изучались. Поэтому лечение пациентов с нарушениями функции печени
средней и тяжелой степени тяжести препаратом ВАРГАТЕФ
не
рекомендуется.
За
информацией о дозировании, способе применения и модификации дозы
доцетаксела, пожалуйста, обратитесь к соответствующей инструкции по
применению этого препарата.
Побочные действия
|
Данный мониторинга Просим |
ИЛФ
Наиболее
часто сообщавшимися нежелательными реакциями, связанными с
применением нинтеданиба, были диарея, тошнота и рвота, боль в области
живота, снижение аппетита, снижение массы тела и повышение уровня
ферментов печени. Частота побочных реакций, приведенных в таблице 3,
изложена в соответствии со следующей градацией: очень часто (˃
1/10); часто (˃ 1/100; ≤ 1/10); нечасто (˃ 1/1000; ≤
1/100); редко (˃ 1/10000; ≤ 1/1000); очень редко (≤
1/10000).
Таблица
3. Частота побочных действий, ИЛФ
|
Метаболические |
|
|
— |
Часто |
|
Нарушения |
|
|
— |
Нечасто |
|
Нарушения |
|
|
— |
Очень |
|
— |
часто |
|
Нарушения |
|
|
— |
Очень |
|
— |
часто |
|
повышение |
нечасто |
Диарея.
В исследованиях INPULSIS диарея была наиболее часто репортируемым
желудочно-кишечным явлением у 62,4% по сравнению с 18,4% пациентов,
получавших препарат ВАРГАТЕФ или плацебо, соответственно. У
большинства пациентов данные явления были легкой и средней степени
тяжести и отмечались на протяжении первых 3 месяцев лечения. Диарея
стала причиной прекращения терапии препаратом ВАРГАТЕФ у 4,4%
пациентов.
Повышение
печеночных ферментов.
Повышение ферментов печени было зарегистрировано у 13,6% пациентов,
получавших нинтеданиб. В большинстве случаев повышение активности
трансаминаз было обратимым и не сопровождалось клиническими
симптомами повреждения печени.
Тошнота
и рвота были часто сообщаемыми нежелательными явлениями. У
большинства пациентов отмечалась тошнота и рвота легкой или средней
степени тяжести. Тошнота стала причиной прекращения лечения
препаратом нинтеданиб у 2% пациентов. Рвота стала причиной
прекращения лечения у 0,8 % пациентов.
НМРЛ
Наиболее
часто сообщавшимися нежелательными реакциями, считавшимися связанными
с применением нинтеданиба, были диарея, повышение активности
ферментов печени (АЛТ и АСТ) и рвота. Частота побочных реакций,
приведенных в таблице 4, ниже и изложена в соответствии со следующей
градацией: очень часто (˃ 1/10); часто (˃ 1/100; ≤
1/10); нечасто (˃ 1/1000; ≤ 1/100); редко (˃ 1/10000; ≤
1/1000); очень редко (≤ 1/10000).
Таблица
4. Частота побочных действий, НМРЛ
|
Инфекции |
|
|
— |
Часто |
|
Нарушения |
|
|
— |
Очень |
|
Метаболические |
|
|
— |
Очень |
|
— |
часто |
|
Нарушения |
|
|
— |
Очень |
|
Нарушения |
|
|
— |
Очень |
|
— |
часто |
|
Нарушения |
|
|
— |
Очень |
|
— |
нечасто |
|
Нарушения |
|
|
— |
Очень |
|
— |
часто |
|
Нарушения |
|
|
— |
часто |
*-
данные побочные реакции наблюдались при проведении клинических
исследований, однако связь с приемом препарата ВАРГАТЕФ не доказана.
#—
в клинических исследованиях частота встречаемости данных побочных
реакций у пациентов, принимавших нинтеданиб в комбинации с
доцетакселом, не превышала частоту встречаемости таковых у пациентов,
принимавших плацебо в комбинации с доцетакселом.
Диарея.
Диарея является часто сообщавшимся нежелательным явлением со стороны
ЖКТ. Отмечается тесная временная связь между развитием диареи и
применением доцетаксела. В клиническом исследовании LUME-Lung 1
диарея легкой и средней степени тяжести отмечалась у большинства
пациентов. Диарея отечалась у 43,4 % (≥ 3 степени тяжести : 6,3 %)
при использовании комбинированного лечения пациентов c
доцетакселом. Большинство пациентов оправились от диареи после
прерывания лечения, противодиарейной терапии и снижения дозы
нинтеданиба.
Повышение
печеночных ферментов и гипербилирубинемия.
Нарушение
со стороны печеночных ферментов и гипербилирубинемия отмечались у
42,8% пациентов. Примерно одна треть пациентов относилась ≥ 3
классу степени тяжести. В большинстве случаев повышение печеночных
ферментов было обратимым и не сопровождалось клиническими симптомами
повреждения печени.
Нейтропения,
фебрильная нейтропения и сепсис. Сепсис
и фебрильная нейтропения отмечались как осложнения нейтропении.
Степень развития сепсиса (1,3%) и фебрильной нейтропении (7,5%)
возрастала при лечении нинтеданибом по сравнению с плацебо. Важно
проводить анализ крови пациента во время комбинированного лечения с
доцетакселем.
Кровотечение.
Кровотечение
является часто сообщавшимся нежелательным явлением ввиду механизма
действия нинтеданиба, частота возникновения кровотечений была
сопоставима между 2 группами исследований (плацебо: 11,1%,
нинтеданиб: 10,9%) у больных с аденокарциномой.
Прободения.
В связи с механизмом действия нинтеданиба могут возникать прободения.
Тем не менее, частота больных с желудочно-кишечными прободениями была
низкой.
Периферическая
нейропатия.
Наблюдалось, что при лечении доцетакселем возникает периферическая
нейропатия. Сообщалось о периферической нейропатии 16,5% пациентов в
группе плацебо и 19,1% пациентов в группе нинтеданиба.
Такие
часто сообщающиеся побочные эффекты, как тошнота и рвота, в
большинстве случаев были легкой или средней степени тяжести.
По
данным клинических исследований применение препарата ВАРГАТЕФ в
комбинации с доцетакселом сопровождалось более частым развитием
нейтропении > 3 степени тяжести (по критериям CTCAE), чем в случае
применения одного доцетаксела.
Противопоказания
—
гиперчувствительность к
нинтеданибу,
сое или арахису, или любому вспомогательному компоненту препарата;
—
беременность и период грудного вскармливания;
—
нарушения функции печени средней и тяжелой степени тяжести
(опыт
применения отсутствует);
—
тяжелые нарушения функции почек (клиренс креатинина < 30 мл/мин)
(опыт
применения отсутствует)*;
—
активные
метастазы в головной мозг (опыт применения отсутствует);
—
детский
возраст
до
18 лет (опыт применения отсутствует).
*Эффективность
и безопасность нинтеданиба у пациентов с тяжелыми нарушениями функции
почек (клиренс
креатинина < 30 мл/мин) не
были изучены. Через почки выводится менее 1% разовой дозы
нинтеданиба.
В
отношении противопоказаний для доцетаксела, пожалуйста,
обратитесь к соответствующей инструкции по применению этого
препарата.
Лекарственные взаимодействия
Индукторы/ингибиторы
P-gp
Нинтеданиб
является субстратом для P-gp. Показано, что совместное применение с
активным ингибитором P-gp кетоконазолом увеличивает экспозицию
нинтеданиба, судя по величине AUC, в 1,61 раза, а судя по величине
Cmax,
в 1,83 раза.
Одновременное
применение рифампицина (активного индуктора P-gp) приводит к
уменьшению экспозиции нинтеданиба, судя по величине AUC, на 50,3%, а
судя по величине Cmax,
на 60,3% (по сравнению с применением одного нинтеданиба).
Активные
ингибиторы P-gp (например, кетоконазол или эритромицин) в случае
совместного применения с препаратом ВАРГАТЕФ могут увеличивать
экспозицию нинтеданиба. У таких пациентов переносимость нинтеданиба
должна тщательно мониторироваться.
Активные
индукторы P-gp (например, рифампицин, карбамазепин, фенитоин и
препараты
зверобоя продырявленного)
могут уменьшать экспозицию нинтеданиба. Рекомендуется
подбор альтернативной сопутствующей терапии с отсутствием или
минимальным индуцирующим действием на систему
P-gp.
Изоферменты
CYP
Изоферменты
CYP принимают лишь небольшое участие в биотрансформации нинтеданиба.
В доклинических исследованиях установлено,
что нинтеданиб
и его метаболиты (свободный
кислый метаболит нинтеданиба
и его глюкуронид) не ингибировали и не индуцировали изоферменты CYP.
Поэтому вероятность лекарственных взаимодействий с нинтеданибом,
основанных на влиянии на изоферменты CYP, считается небольшой.
Одновременная
терапия с пирфенидоном
Одновременное
назначение нинтеданиба с пирфенидоном было изучено в исследовании с
параллельными группами японских пациентов с ИЛФ. Воздействие
нинтеданиба имело тенденцию к снижению при одновременном назначении
пирфенидона по сравнению с назначением только нинтеданиба. Нинтеданиб
не оказывал эффекта на фармакокинетику пирфенидона. В связи с
коротким периодом одновременного воздействия и малым количеством
пациентов, никакие выводы о безопасности и эффективности
комбинированного лечения не могут быть сделаны.
Одновременное
применение с другими препаратами
Одновременное
применение нинтеданиба с доцетакселом (75 мг/м2)
не изменяет в существенной степени фармакокинетику этих препаратов.
Возможность
взаимодействий нинтеданиба с гормональными контрацептивными
средствами не изучалась.
Одновременный
прием с пищей
ВАРГАТЕФ
рекомендуется принимать одновременно с пищей (см. раздел
Фармакокинетика).
Особые указания
С
осторожностью
—
нарушения функции печени легкой степени тяжести;
—
наследственная предрасположенность к кровотечениям (болезнь фон
Виллебранда);
—
стабильные метастазы в головной мозг;
—
терапия антикоагулянтами;
—
венозные тромбоэмболии;
—
перфорации ЖКТ в анамнезе;
—
пациенты, которые ранее подвергались абдоминальным хирургическим
вмешательствам;
—
артериальная тромбоэмболия (для ИЛФ).
Желудочно-кишечные
расстройства
—
диарея
Лечение
диареи (адекватная гидратация и антидиарейные лекарственные средства,
например, лоперамид) следует проводить при появлении первых
признаков. В случае развития диареи может потребоваться прерывание
лечения, снижение дозы или прекращение терапии. Лечение
препаратом ВАРГАТЕФ может быть возобновлено в сниженной дозе (100 мг
дважды в сутки) или в полной дозе (по 150 мг два раза в сутки). В
случае персистирования тяжелой диареи, несмотря на симптоматическое
лечение, терапию препаратом ВАРГАТЕФ следует прекратить.
—
тошнота и рвота
В
случае возникновения тошноты и рвоты рекомендовано применение
препаратов с противорвотным действием,
например,
глюкокортикоидов, антигистаминных средств или антагонистов
серотониновых 5-HT3-рецепторов.
Несмотря
на соответствующее поддерживающее лечение, могут потребоваться
прерывание лечения препаратом ВАРГАТЕФ, снижение его дозы или
прекращение терапии.
В
случае
обезвоживания
рекомендуется восстановление водно-электролитного баланса. Если
возникают существенные
желудочно-кишечные нежелательные явления, то необходимо проведение
мониторирования концентрации электролитов в крови. Если
симптомы сохраняются, несмотря на соответствующее поддерживающее
лечение (включая противорвотную терапию), может потребоваться
снижение дозы или прерывание лечения. Лечение может быть возобновлено
со сниженной (100 мг два раза в сутки) или полной дозой (150 мг два
раза в сутки). В случае возникновения серьезных симптомов, терапию
препаратом ВАРГАТЕФ следует прекратить.
Нейтропения
и сепсис
Во
время терапии
препаратом
ВАРГАТЕФ, в частности при комбинации его с доцетакселом, необходимо
проводить мониторинг показателей крови на предмет развития
нейтропении и возможных последующих осложнений в виде сепсиса или
фебрильной нейтропении. Анализы крови должны контролироваться в ходе
терапии, в частности, во время комбинированного лечения с
доцетакселем. Следует часто проводить полный анализ крови в начале
каждого цикла лечения и при максимальном снижении уровня нейтрофилов,
обусловленное проведением химиотерапии, у пациентов, получающих
лечение нинтеданибом в комбинации с доцетакселем, и по клиническим
показаниям после последнего цикла введения комбинации.
Нарушения
функции печени
Безопасность
и эффективность препарата не изучалась у пациентов с нарушениями
функции печени средней (класс B по шкале Чайлд-Пью) или тяжелой
(класс С по шкале Чайлд-Пью) степени тяжести. Поэтому у таких
пациентов применение препарата ВАРГАТЕФ не рекомендуется.
ИЛФ
Рекомендуется
оценивать активность печеночных трансаминаз и концентрацию билирубина
до начала терапии препаратом ВАРГАТЕФ,
а затем периодически во время лечения (например, при каждом визите
пациента) или по клиническим показаниям.
В
случае повышения уровня трансаминаз (АСТ или АЛТ) более чем в 3 раза
выше верхней границы нормы рекомендовано прервать терапию препаратом
ВАРГАТЕФ и проводить мониторирование пациента. Как только показатели
трансаминаз вернутся к исходному уровню, лечение препаратом ВАРГАТЕФ
можно возобновить до полной дозы (150 мг 2 раза в день) или вновь на
сниженной дозе (100 мг 2 раза в день), которая впоследствии может
быть повышена.
Если
повышение каких-либо показателей функции печени связано с
клиническими симптомами поражения печени, например, желтухой, лечение
препаратом ВАРГАТЕФ следует окончательно прекратить. Следует
исследовать альтернативные причины повышения уровней печеночных
ферментов.
НМРЛ
После
начала терапии рекомендуется тщательный контроль активности
печеночных трансаминаз, щелочной фосфатазы и концентрации билирубина
(периодически, во время начала комбинации с доцетакселом, т.е. в
начале каждого лечебного цикла). Если отмечается существенное
повышение активности печеночных ферментов, может потребоваться
прерывание
лечения, уменьшение дозы или прекращение терапии
препаратом
ВАРГАТЕФ.
Уровни
трансаминаз, ЩФ и билирубина следует исследовать до начала
комбинированного лечения препаратами ВАРГАТЕФ плюс доцетаксел.
Следует контролировать показания по клиническим данным или
периодически во время лечения, то есть в фазе комбинирования с
доцетакселем в начале каждого цикла лечения, и ежемесячно если
ВАРГАТЕФ продолжают принимать в виде монотерапии после прекращения
доцетаксела.
В
случае выявления повышения печеночных ферментов, может потребоваться
прерывание лечения, уменьшение дозы или прекращение терапии
препаратом ВАРГАТЕФ. Следует рассмотреть альтернативные причины
повышения ферментов печени и принять соответствующие меры в случае
необходимости. В случае специфических изменений в показателях печени
(АСТ/АЛТ > 3 х ВГН; общий билирубин ≥ 2 х ВГН и ЩФ <2 х
ВГН), лечение препаратом ВАРГАТЕФ следует прерывать. Если не
установлена альтернативная причина, ВАРГАТЕФ следует окончательно
прекратить.
Особые
группы пациентов
НМРЛ
Такие
показатели как возраст, масса тела и отношение к азиатской расе может
привести к более высокому риску повышения активности печеночных
ферментов. У пациентов с несколькими факторами риска рекомендуется
тщательное мониторирование показателей функции печени.
Риск
развития кровотечений
Ингибирование
VEGFR способно привести к увеличению риска
кровотечений. В
клинических исследованиях у пациентов с аденокарциномой, принимавших
ВАРГАТЕФ, повышения
частоты
кровотечений не наблюдалось. Данных
о применении препарата ВАРГАТЕФ
у
пациентов с наследственной предрасположенностью к кровотечениям
(например, болезнь фон Виллебранда) не имеется.
ИЛФ
Во
время проведения клинических исследований не наблюдалось
существенного
риска развития кровотечений
на фоне приема нинтеданиба.
В
клинические исследования не включались пациенты с известным риском
развития кровотечений, включая пациентов с наследственной
предрасположенностью к кровотечениям или пациентов, получающих
антикоагулянтную терапию в высоких дозах. Следовательно, данной
категории пациентов лечение препаратом ВАРГАТЕФ должно быть назначено
только в том случае, если потенциальная польза проводимой терапии
превышает потенциальный риск.
НМРЛ
Пациенты
с недавно отмечавшимся легочным кровотечением (> 2,5 мл крови), а
также пациенты с центрально расположенными
опухолями и рентгенологическими признаками локальной инвазии крупных
сосудов или с рентгенологическими признаками наличия полостей или
некротических изменений опухоли исключались из клинических
исследований.
Поэтому применение препарата ВАРГАТЕФ у таких пациентов не
рекомендуется.
—
метастазы в головной мозг
Увеличения
частоты церебральных кровотечений у пациентов с ранее адекватно
лечеными метастазами в головной мозг (стабильными в течение ≥ 4
недель до начала лечения препаратом ВАРГАТЕФ) не наблюдалось. Однако
такие пациенты должны тщательно мониторироваться в отношении
признаков и симптомов церебральных кровотечений.
Пациенты
с активными метастазами
в головной мозг исключались из клинических исследований, применение
препарата ВАРГАТЕФ у них не рекомендуется.
—
терапия антикоагулянтами
В
клинические исследования включались пациенты, получавшие длительную
терапию низкомолекулярными гепаринами в низких дозах или
ацетилсалициловой кислотой в дозах ≤ 325 мг/сут. Увеличения
частоты кровотечений у таких пациентов не наблюдалось. Данных о
применении препарата ВАРГАТЕФ у пациентов, предварительно получавших
лечение антикоагулянтами в более высоких дозах, не имеется.
Пациентам, у которых во время лечения препаратом
ВАРГАТЕФ
развивались тромбоэмболические нарушения, в связи с чем требовалась
терапия антикоагулянтами, разрешалось продолжить прием препарата
ВАРГАТЕФ,
при этом увеличения
частоты кровотечений не отмечалось. У пациентов, принимающих такие
антикоагулянты, как варфарин или фенпрокумон, необходимо регулярно
проверять протромбиновое время, международное нормализованное
отношение (МНО) или следить за клиническими признаками кровотечений.
Артериальная
тромбоэмболия
ИЛФ
Из
клинических исследований INPULSIS
исключались пациенты с инфарктом миокарда или инсультом в ближайшем
анамнезе. Случаи развития артериальной тромбоэмболии встречались
редко: у 0,7% пациентов, получавших плацебо, и 2,5% пациентов в
группе, получавшей нинтеданиб.
В
то время как нежелательные реакции, отражающие ишемические
заболевания сердца, были сравнимы в группах нинтеданиба и плацебо,
пациентов, у которых развился инфаркт миокарда, оказалось больше в
группе нинтеданиба (1,6%) по сравнению с группой плацебо (0,5%).
Необходимо соблюдать осторожность при лечении пациентов с высоким
сердечно-сосудистым риском, включая известное заболевание коронарных
артерий. Следует рассмотреть возможность перерыва в лечении
пациентов, у которых развились симптомы острой ишемии миокарда.
Венозная
тромбоэмболия
ИЛФ
В
исследованиях INPULSIS не наблюдалось повышенного риска развития
венозных тромбоэмболических осложнений. Однако в связи с
особенностями механизма действия нинтеданиба, у пациентов может
отмечаться повышенный риск развития тромбоэмболических явлений.
НМРЛ
У
пациентов, получающих
ВАРГАТЕФ, отмечался повышенный риск венозных тромбоэмболий, в том
числе тромбоза глубоких вен. Пациенты должны тщательно
мониторироваться в отношении тромбоэмболических нарушений. Пациентам
с опасными для жизни венозными тромбоэмболиями ВАРГАТЕФ
необходимо
отменить.
Перфорации
ЖКТ
Частота
перфораций ЖКТ в отдельных лечебных группах в клинических
исследованиях была сопоставима. Однако механизм действия препарата
ВАРГАТЕФ указывает на возможность повышения риска перфораций ЖКТ.
Особое
внимание должно уделяться
лечению пациентов, которые ранее подвергались абдоминальным
хирургическим вмешательствам. В связи с этим ВАРГАТЕФ
может
применяться только как минимум через 4 недели после больших
хирургических вмешательств. В случае возникновения
гастроинтестинальной перфорации
терапия препаратом
ВАРГАТЕФ
должна
прекращаться.
Нарушение
заживления ран
Нинтеданиб,
в связи с особенностями механизма действия, может нарушать заживление
ран. В исследованиях LUME-Lung 1 и INPULSIS
увеличения частоты нарушений заживления ран не наблюдалось.
Специальных исследований, в которых бы изучалось влияние нинтеданиба
на заживление ран, не проводилось. Поэтому лечение должно начинаться
или возобновляться (если осуществлялся перерыв в связи с
хирургическим вмешательством) с учетом клинического мнения об
адекватности заживления раны.
Соевый
лецитин
Мягкие
капсулы препарата содержат в своем составе соевый лецитин.
В
отношении особых указаний для доцетаксела, пожалуйста, обратитесь к
соответствующей инструкции по применению этого препарата.
Применение
при беременности и в период грудного вскармливания
Беременность
Специальных
исследований по применению препарата
ВАРГАТЕФ
во
время беременности у человека не проводилось, однако в доклинических
исследованиях у животных установлена репродуктивная
токсичность этого препарата.
Поскольку нинтеданиб может обладать эмбриотоксическим действием у
человека, он не должен применяться во время беременности, и, по
меньшей мере, перед началом лечения рекомендуется проведение теста на
беременность.
Пациенткам
следует немедленно сообщить врачу о развитии беременности во время
терапии препаратом
ВАРГАТЕФ. Если
во время терапии
развивается
беременность, пациентку необходимо проинформировать о потенциальной
опасности эмбриотоксического воздействия препарата. Также должен
рассматриваться вопрос о прекращении лечения препаратом ВАРГАТЕФ.
Женщинам
детородного возраста, принимающим препарат ВАРГАТЕФ, следует
рекомендовать использовать надежные методы контрацепции во время
применения препарата и на протяжении, по крайней мере, 3 месяцев
после приема последней дозы.
Грудное
вскармливание
Специальных
исследований о выделении нинтеданиба и его метаболитов в грудное
молоко у человека не проводилось. В доклинических исследованиях
показано, что у крыс в период лактации в грудное молоко проникает
небольшое количество нинтеданиба и его метаболитов (≤ 0,5% от
величины применявшейся дозы). Поэтому нельзя исключить риск для
новорожденных и грудных детей. Во время лечения препаратом ВАРГАТЕФ
кормление
грудью следует прекратить.
Фертильность
В
доклинических исследованиях признаков нарушений фертильности у самцов
выявлено не было. В исследованиях, во время которых уровень
системного воздействия препарата был сравним с уровнем, достигающимся
при использовании максимальной рекомендуемой дозы у человека (250 мг
два раза в день), признаков нарушений фертильности у самок крыс
обнаружено не было.
За
информацией о влиянии доцетаксела на беременность, грудное
вскармливание и фертильность, пожалуйста, обратитесь к
соответствующей инструкции по применению этого препарата.
Особенности
влияния лекарственного средства на способность управлять транспортным
средством и потенциально опасными механизмами
Исследований
по влиянию препарата на способность управлять транспортными
средствами и занятию другими потенциально опасными видами
деятельности, требующими повышенной концентрации внимания и быстроты
психомоторных реакций не проводилось.
Во
время применения препарата ВАРГАТЕФ пациентам нужно рекомендовать
соблюдать осторожность при управлении транспортными средствами или
механизмами.
Передозировка
Симптомы
В
клинических исследованиях нинтеданиб изучался в наивысшей однократной
дозе 450 мг один раз в день. Также зафиксированы случаи передозировки
при применении препарата в максимальной дозе 600 мг в течение восьми
дней. Наблюдавшиеся нежелательные явления были сопоставимы с
известным профилем безопасности нинтеданиба: увеличение активности
ферментов печени и нарушения со стороны ЖКТ. Пациенты полностью
восстановились после нежелательных явлений. В исследованиях INPULSIS
был зафиксирован один случай непреднамеренного повышения дозы до
600 мг 2 раза в день на протяжении 21 дня у пациента с ИЛФ.
В период некорректного приема препарата было зафиксировано развитие
несерьезного нежелательного явления (назофарингит), которое
купировалось в данном периоде без регистрации каких-либо других
нежелательных реакций.
Лечение
Специфического
антидота на случай передозировки нет. При подозрении на передозировку
необходимо отменить ВАРГАТЕФ и проводить симптоматическую терапию.
Форма выпуска и упаковка
100
мг. По
10 капсул помещают в контурную ячейковую упаковку из фольги
алюминиевой. По 6 или 12 контурных упаковок вместе с инструкцией по
медицинскому применению на государственном и русском языках помещают
в картонную пачку.
150
мг. По
10 капсул помещают в контурную ячейковую упаковку из фольги
алюминиевой. По 6 контурных упаковок вместе с инструкцией по
медицинскому применению на государственном и русском языках помещают
в картонную пачку.
Срок хранения
3
года
Не использовать после
истечения срока годности, указанного на упаковке.
Условия хранения
Хранить
в сухом месте, при температуре не выше 25°С.
Хранить
в недоступном для детей месте.
Условия отпуска из аптек
По
рецепту
Производитель
балк-продукта
Каталент
Германия Эбербах ГмбХ
Гаммельсбахер
штрассе 2, 69412 Эбербах, Германия
Контроль
качества, выпуск серии и упаковщик
Берингер
Ингельхайм Фарма ГмбХ и Ко.КГ, Бингер Штрассе 173, 55216 Ингельхайм,
Германия
Держатель
регистрационного удостоверения
Берингер
Ингельхайм Интернешнл ГмбХ, Бингер Штрассе 173, 55216 Ингельхайм,
Германия
Адрес
организации, принимающей на территории Республики Казахстан претензии
от потребителей по качеству продукции и ответственной за
пострегистрационное наблюдение за безопасностью лекарственного
средства
Филиал
«Берингер Ингельхайм Фарма Геселлшафт мбХ» в РК
адрес: г.
Алматы, 050008, пр-т Абая 52
Бизнес-центр
«Innova
Tower»,
7й
этаж
тел:
+7 (727) 250
00
77
факс:
+7 (727)
244
51 77
e-mail:
PV_local_Kazakhstan@boehringer-ingelheim.com
| Варгатеф_инструкция_рус.doc | 0.2 кб |
| Варгатеф_инструкция_каз.doc | 0.27 кб |
Отправить прикрепленные файлы на почту
Национальный центр экспертизы лекарственных средств, изделий медицинского назначения и медицинской техники
Варгатеф® (Vargatef) инструкция по применению
📜 Инструкция по применению Варгатеф®
💊 Состав препарата Варгатеф®
✅ Применение препарата Варгатеф®
📅 Условия хранения Варгатеф®
⏳ Срок годности Варгатеф®
Описание лекарственного препарата
Варгатеф®
(Vargatef)
Основано на листке-вкладыше препарата, утверждено компанией-производителем
и подготовлено для печатного издания справочника Видаль 2021 года.
Дата обновления: 2020.11.17
Код ATX:
L01EX09
(Нинтеданиб)
Лекарственные формы
| Варгатеф® |
Мягкие капс. 100 мг: 60 шт. рег. №: ЛП-(001278)-(РГ-RU) |
|
|
Мягкие капс. 150 мг: 60 шт. рег. №: ЛП-(001278)-(РГ-RU) |
Форма выпуска, упаковка и состав
препарата Варгатеф®
Мягкие капсулы желатиновые, продолговатые, непрозрачные, розовато-оранжевого (персикового) цвета, содержащие ярко-желтую вязкую суспензию, на одной стороне которых черным цветом напечатан символ компании Берингер Ингельхайм и «100».
Вспомогательные вещества: триглицериды средней цепи — 107.40 мг, твердый жир — 51.00 мг, лецитин — 1.20 мг.
Состав оболочки капсулы: желатин — 111.24 мг, глицерин 85% — 49.09 мг, титана диоксид (Е171) — 1.21 мг, железа оксид красный (суспензия с глицерином 85%) — 0.06 мг, железа оксид желтый (суспензия с глицерином 85%) — 0.36 мг, чернила Опакод® тип S-1-17823.
10 шт. — блистеры (6) — пачки картонные.
10 шт. — блистеры (6) — пачки картонные (2) — пленка полипропиленовая.
Мягкие капсулы желатиновые, продолговатые, непрозрачные, коричневого цвета, содержащие ярко-желтую вязкую суспензию, на одной стороне которых черным цветом напечатан символ компании Берингер Ингельхайм и «150».
Вспомогательные вещества: триглицериды средней цепи — 161.10 мг, твердый жир — 76.50 мг, лецитин — 1.80 мг.
Состав оболочки капсулы: желатин — 141.84 мг, глицерин 85% — 61.43 мг, титана диоксид (Е171) — 0.39 мг, железа оксид красный (суспензия с глицерином 85%) — 1.24 мг, железа оксид желтый (суспензия с глицерином 85%) — 1.86 мг, чернила Опакод® тип S-1-17823.
10 шт. — блистеры (6) — пачки картонные.
Фармакологическое действие
Механизм действия
Нинтеданиб — ингибитор тирозинкиназы, относящийся к классу малых молекул, блокирующий киназную активность рецепторов фактора роста эндотелия сосудов 1-3 (VEGFR 1-3), рецепторов тромбоцитарного фактора роста α и β (PDGFR α и β) и рецепторов фактора роста фибробластов 1-3 (FGFR 1-3). Кроме того, ингибируются Fms-подобная протеинтирозинкиназа (Flt-3), лимфоцит-специфическая протеинтирозинкиназа (Lck), протоонкогенная протеинтирозинкиназа (Src) и киназы рецептора колониестимулирующего фактора 1 (CSF1R). Нинтеданиб конкурентно взаимодействует с АТФ-связывающим участком этих киназ и блокирует каскады внутриклеточной передачи сигналов, которые, как было продемонстрировано, участвуют в патогенезе ремоделирования фиброзной ткани при интерстициальных заболеваниях легких.
Фармакодинамические эффекты
Опухолевый ангиогенез является процессом, который вносит существенный вклад в рост, прогрессирование и образование метастазов опухоли. Этот процесс преимущественно запускается проангиогенными факторами, такими как фактор роста эндотелия сосудов и фактор роста фибробластов (VEGF и bFGF), секретируемыми опухолевыми клетками, чтобы привлечь эндотелиальные и периваскулярные клетки хозяина и облегчить доставку кислорода и питательных веществ через сосудистую систему. Нинтеданиб эффективно противодействует образованию и развитию сосудистой системы опухоли, приводит к замедлению и остановке роста опухоли.
В исследованиях in vitro на клетках человека было показано, что нинтеданиб ингибирует процессы, предположительно связанные с инициацией фиброзного патогенеза, с высвобождением профибротических медиаторов из моноцитов периферической крови и с поляризацией макрофагов с образованием макрофагов, активированных по альтернативному пути. Было продемонстрировано, что нинтеданиб ингибирует фундаментальные процессы фиброза органов, пролиферации и миграции фибробластов, трансформацию в активный фенотип миофибробласта и секрецию внеклеточного матрикса. В исследованиях на животных с использованием многочисленных моделей ИЛФ (идиопатический легочный фиброз), ИЗЛ-ССД (интерстициальные заболевания легких при системной склеродермии), ИЗЛ-РА (интерстициальные заболевания легких при ревматоидном артрите) и других видов фиброза органов было показано противовоспалительное и противофибротическое действие нинтеданиба в легких, коже, сердце, почках и печени. Нинтеданиб также обладает активностью в отношении сосудов. Он уменьшал апоптоз эндотелиальных клеток микрососудов кожи и замедлял ремоделирование легочных сосудов путем уменьшения пролиферации клеток гладкой мускулатуры сосудов, толщины стенки легочных сосудов и уменьшал процентную долю окклюзированных легочных сосудов.
Фармакокинетика
Фармакокинетика нинтеданиба может считаться линейной в отношении времени (т.е. данные, полученные при применении однократной дозы, могут экстраполироваться на данные, полученные в результате многократного применения). После многократного применения препарата накопление составляет 1.04 при оценке Сmax и 1.38 при оценке AUCt. Остаточные концентрации нинтеданиба остаются стабильными в течение одного года и более.
Всасывание
Сmax нинтеданиба в плазме крови достигается приблизительно через 2-4 ч после приема препарата во время еды (диапазон 0.5-8 ч). Абсолютная биодоступность при дозе 100 мг составляет у здоровых добровольцев 4.69% (90% доверительный интервал (ДИ): 3.615-6.078).
Установлено, что экспозиция нинтеданиба увеличивается пропорционально дозе (в диапазонах доз 50-450 мг 1 раз/сут и 150-300 мг 2 раза/сут). Css в плазме крови достигаются, как максимум, в течение одной недели после начала приема.
Экспозиция нинтеданиба увеличивается после приема пищи примерно на 20% по сравнению с приемом препарата натощак (ДИ: 95.3-152.5%), а всасывание замедляется. Медиана времени достижения Сmax в плазме крови при приеме натощак — 2 ч, после еды — 3.98 ч.
Распределение
Распределение нинтеданиба осуществляется путем двухфазной кинетики. После в/в инфузии во время терминальной фазы наблюдается большой Vd — 1050 л, геометрический коэффициент вариации (gCV) 45%.
Связывание нинтеданиба с белками плазмы человека in vitro считается значительным, связанная фракция составляет 97.8%. Основным белком, участвующим в связывании, считается альбумин сыворотки крови. Нинтеданиб преимущественно распределяется в плазме, соотношение кровь/плазма составляет 0.869.
Нинтеданиб является субстратом для P-гликопротеина (P-gp). Показано, что нинтеданиб in vitro не является субстратом или ингибитором полипептидных переносчиков органических анионов (ОАТР-1В1, ОАТР-1В3, ОАТР-2В1), переносчика органических катионов-2 (ОСТ-2) или белка, ассоциированного с множественной лекарственной устойчивостью-2 (MRP-2). Нинтеданиб также не является субстратом для белка резистентности рака молочной железы (BCRP). In vitro было установлено, что нинтеданиб обладает слабой ингибирующей активностью в отношении ОСТ-1, BCRP и P-gp, что, как считается, имеет небольшую клиническую значимость. Такое же заключение сделано в отношении нинтеданиба как субстрата для ОСТ-1.
Метаболизм
Основной реакцией, участвующей в метаболизме нинтеданиба, является гидролитическое расщепление с помощью эстераз, что приводит к образованию свободного кислого метаболита нинтеданиба. В доклинических исследованиях in vivo установлено, что данный метаболит не обладает эффективностью, несмотря на влияние на целевые рецепторы препарата. В дальнейшем он глюкуронизируется ферментами уридиндифосфат-глюкуронилтрансферазами (UGT1А1, UGT1А7, UGT1А8 и UGT1А10) с образованием глюкуронида.
Считается, что биотрансформация нинтеданиба с участием изоферментов CYP происходит только в небольшой степени, основное участие принимает изофермент CYP3A4. В исследовании ADME у человека основной метаболит, образующийся с участием изоферментов CYP, обнаружить в плазме не удалось. По данным исследования in vitro CYP-зависимый метаболизм составляет примерно 5%, тогда как расщепление, осуществляемое эстеразами, составляет 25%.
Выведение
Общий клиренс из плазмы после в/в инфузии составляет 1390 мл/мин (gCV 28.8%). Экскреция почками неизмененного нинтеданиба в течение 48 ч после приема препарата внутрь составляет примерно 0.05% дозы (gCV 31.5%), а после в/в введения — примерно 1.4% (gCV 24.2%); почечный клиренс составляет 20 мл/мин (gCV 32.6%). После приема внутрь [14С]-нинтеданиба радиоактивный материал выводился преимущественно с желчью и обнаруживался в кале (93.4% дозы, gCV 2.61%). Вклад почечной экскреции в общий клиренс составляет 0.649% дозы (gCV 26.3%). Выведение считается полным (более 90%) через 4 дня после приема. T1/2 нинтеданиба составляет от 10 до 15 ч (gCV примерно 50%).
Зависимость эффекта от экспозиции
Немелкоклеточный рак легкого (НМРЛ). В ходе исследования зависимости нежелательных явлений от фармакокинетики нинтеданиба была установлена тенденция к более частому повышению активности ферментов печени при большей экспозиции нинтеданиба. Подобной зависимости не отмечается для нарушений со стороны ЖКТ.
Для клинических конечных точек анализ взаимосвязи фармакокинетики с эффективностью не проводился. С помощью метода логистической регрессии установлена статистически значимая взаимосвязь между экспозицией нинтеданиба и влиянием на изменения, обнаруживаемые методом динамической контрастной МРТ.
ИЛФ, другие хронические фиброзирующие ИЗЛ с прогрессирующим фенотипом ИЗЛ-ССД. Анализ зависимости «экспозиция-ответ» показал наличие взаимосвязи типа Еmax между воздействием в диапазоне, наблюдавшемся в ряде исследований фазы II и III, и ежегодным уровнем снижения форсированной жизненной емкости легких; ЕС50 составляла около 3-5 нг/мл (относительная стандартная ошибка: 54-67%). Для сравнения, медиана наблюдаемых минимальных концентраций нинтеданиба при применении препарата Варгатеф® в дозе 150 мг 2 раза/сут составляла примерно 10 нг/мл.
В отношении безопасности возможно имеется слабая взаимосвязь между экспозицией нинтеданиба в плазме крови и повышением активности АЛТ и/или ACT. Фактически применяемая доза может быть более существенным прогностическим фактором риска развития диареи любой интенсивности, даже если экспозицию в плазме крови нельзя исключить в качестве определяющего фактора риска.
Фармакокинетика у особых групп пациентов
Фармакокинетические свойства нинтеданиба были сопоставимы у здоровых добровольцев, пациентов с ИЛФ, другими хроническими фиброзирующими ИЗЛ с прогрессирующим фенотипом, ИЗЛ-ССД и НМРЛ. Согласно результатам популяционного фармакокинетического анализа и описательных исследований, на воздействие нинтеданиба не влиял пол (с учетом массы тела), нарушения функции почек легкой и средней степени тяжести (рассчитанная по КК), метастазы в печени, общее состояние больного (оценка по опроснику Восточной Объединенной Онкологической Группы, Eastern Cooperative Oncology Group (ECOG)), употребление алкоголя или генотип Р-гликопротеина. Популяционный фармакокинетический анализ выявил умеренное влияние возраста, массы тела и расовой принадлежности на воздействие нинтеданиба. В связи с тем, что наблюдалась высокая межиндивидуальная вариабельность воздействия, эти влияния не считались клинически значимыми. Тем не менее, рекомендуется тщательное мониторирование пациентов, у которых выявляется несколько факторов риска, представленных ниже.
Возраст
Экспозиция нинтеданиба линейно увеличивается с возрастом. У 45-летних пациентов (5-й процентиль) значение AUCt,ss (в равновесном состоянии на период дозирования) было ниже на 16%, а у 76-летних пациентов (95-й процентиль) выше на 13% по сравнению с пациентами, медиана возраста которых составляла 62 года. Диапазон возраста, оценивавшийся в ходе анализа, составлял 29-85 лет; возраст более 75 лет отмечался примерно у 5% популяции пациентов.
Аналогичные исследования у детей не проводились.
Масса тела
Наблюдается обратная корреляция между массой тела и экспозицией нинтеданиба. У пациентов с массой тела 50 кг (5-й процентиль) величина AUCt,ss увеличивалась на 25%, а у пациентов с массой тела 100 кг (95-й процентиль) уменьшалась на 19% по сравнению с пациентами, медиана массы тела которых составляла 71.5 кг.
Раса
Средняя популяционная экспозиция нинтеданиба на 33-50% выше у пациентов-китайцев, тайваньцев и индийцев, на 16% выше у пациентов японского происхождения, а у пациентов-корейцев — на 16-22% ниже, чем у пациентов европеоидной расы (с поправкой на массу тела). Данные в отношении пациентов негроидной расы являются очень ограниченными, диапазон этих данных сходен с пациентами европеоидной расы.
Нарушения функции печени
В исследовании I фазы при изучении однократного введения препарата значения Сmax и AUC были в 2.2 раза выше у добровольцев с легкими нарушениями функции печени (класс А по шкале Чайлд-Пью; 90% ДИ 1.3-3.7 для Сmax и 1.2-3.8 для AUC соответственно), чем у здоровых добровольцев.
У добровольцев с умеренными нарушениями функции печени (класс В по шкале Чайлд-Пью) значение Сmax (90% ДИ 4.4-13.2) было в 7.6 раза выше и в 8.7 раза выше значение AUC (90% ДИ 5.7-13.1) соответственно, в сравнении со здоровыми добровольцами. В исследовании не принимали участия пациенты с тяжелыми нарушениями функции печени (класс С по шкале Чайлд-Пью).
Показания препарата
Варгатеф®
- местно-распространенный, метастатический или рецидивирующий немелкоклеточный рак легкого (аденокарцинома) после химиотерапии первой линии в комбинации с доцетакселом;
- идиопатический легочный фиброз (идиопатический фиброзирующий альвеолит); для лечения и замедления прогрессирования заболевания;
- другие хронические фиброзирующие интерстициальные заболевания легких (ИЗЛ) с прогрессирующим фенотипом;
- интерстициальные заболевания легких при системной склеродермии.
Режим дозирования
Препарат принимают внутрь, предпочтительно во время еды. Капсулы следует проглатывать целиком, запивая водой, не разжевывая и не разламывая.
Пропуск дозы
Если очередная доза препарата Варгатеф® пропущена, следует продолжить прием препарата в изначально рекомендуемой дозе по расписанию следующего приема препарата. Если доза была пропущена, пациент не должен принимать дополнительную дозу препарата.
НМРЛ
Лечение препаратом Варгатеф® должен назначать и проводить врач, имеющий опыт в назначении противоопухолевой терапии.
Рекомендуемая доза препарата Варгатеф® составляет 200 мг 2 раза/сут с интервалом примерно в 12 ч, со 2 по 21 день стандартного 21-дневного цикла лечения доцетакселом.
Варгатеф® не должен применяться в день начала химиотерапии доцетакселом, т.е. в 1 день лечения.
Максимальная рекомендуемая суточная доза составляет 400 мг.
После окончания применения доцетаксела можно продолжить терапию препаратом Варгатеф® до тех пор, пока сохраняется клинический эффект, или до развития неприемлемой токсичности.
Изменение дозы в случае развития нежелательных реакций
В качестве первоначальной меры для устранения нежелательных реакций рекомендуется временный перерыв в лечении препаратом Варгатеф® до тех пор, пока нежелательная реакция не снизится до уровня, который позволит возобновить терапию (см. таблицы 1 и 2). Лечение можно возобновлять в уменьшенной дозе.
Для обеспечения индивидуальной безопасности и переносимости рекомендуется снижение суточной дозы препарата на 100 мг (т.е. уменьшение разовой дозы на 50 мг), как это описывается в таблицах 1 и 2. Если нежелательная реакция (реакции) сохраняется, т.е. если пациент не переносит препарат в дозе 100 мг 2 раза/сут, лечение следует прекратить.
В случае специфического повышения активности АСТ/АЛТ более чем в 3 раза по сравнению с ВГН в сочетании с повышением концентрации общего билирубина в 2 и более раза по сравнению с ВГН и ЩФ менее чем в 2 раза по сравнению с ВГН (см. таблицу 2), применение препарата Варгатеф® следует временно прекратить. Если не будет установлена альтернативная причина нарушений, Варгатеф® следует окончательно отменить.
Таблица 1. Информация об изменении дозы в случае развития диареи, рвоты и других негематологических или гематологических нежелательных явлений, исключая повышение активности печеночных ферментов (см. таблицу 2)
* Общие терминологические критерии для нежелательных явлений — СТСАЕ (Common Terminology Criteria for Adverse Events).
Таблица 2. Информация об изменении дозы в случае повышения активности ACT и/или АЛТ и повышения концентрации билирубина
ИЛФ, другие хронические фиброзирующие ИЗЛ с прогрессирующим фенотипом и ИЗЛ-ССД
Лечение препаратом Варгатеф® следует назначать и проводить под контролем врача, имеющего опыт диагностики и лечения заболеваний, при которых показан препарат.
Рекомендуемая доза препарата составляет 150 мг 2 раза/сут, приблизительно через каждые 12 ч.
Максимальная суточная доза составляет 300 мг.
Изменение дозы в случае развития нежелательных реакций
При развитии нежелательных реакций, таких как диарея, тошнота и рвота в дополнение к симптоматической терапии, при необходимости, рекомендуется снижение дозы или временное прерывание лечения до тех пор, пока нежелательная реакция не снизится до уровня, который позволит возобновить терапию. Лечение препаратом Варгатеф® может быть возобновлено в полной дозе (150 мг 2 раза/сут) или в сниженной дозе (100 мг 2 раза/сут). Если пациент не переносит дозу препарата 100 мг 2 раза/сут, лечение препаратом Варгатеф® следует прекратить.
В случае прерывания лечения вследствие повышения активности трансаминаз (ACT или АЛТ) более чем в 3 раза по сравнению с ВГН после восстановления показателей до нормальных значений рекомендовано возобновить терапию в уменьшенной дозе (100 мг 2 раза/сут). Впоследствии доза может быть увеличена до полной дозы (150 мг 2 раза/сут).
Особые группы пациентов
Детский возраст
Безопасность и эффективность препарата у пациентов детского возраста в клинических исследованиях не изучалась.
Пожилой возраст (>65 лет)
Не отмечено никаких различий по безопасности и эффективности применения препарата у пациентов пожилого возраста (>65 лет) по сравнению с пациентами моложе 65 лет. Исходной коррекции дозы препарата в зависимости от возраста пациента не требуется.
Раса и масса тела
Основываясь на данных популяционного фармакокинетического анализа, исходная коррекция дозы препарата Варгатеф® в зависимости от расы и массы тела не требуется. Данные по безопасности у пациентов негроидной расы ограничены.
Нарушения функции почек
Почками выводится менее 1% однократной дозы нинтеданиба. У пациентов с нарушениями функции почек легкой или средней степени изменения начальной дозы не требуется. У пациентов с тяжелыми нарушениями функции почек (КК <30 мл/мин) безопасность, эффективность и фармакокинетика нинтеданиба не изучались.
Нарушения функции печени
Нинтеданиб выводится преимущественно с желчью (через кишечник) (>90%). У пациентов с нарушениями функции печени легкой и средней степени тяжести (класс А по шкале Чайлд-Пью, класс В по шкале Чайлд-Пью) концентрация препарата в крови повышалась. У пациентов с нарушениями функции печени средней и тяжелой степени (классы В и С по шкале Чайлд-Пью) безопасность, эффективность и фармакокинетика нинтеданиба не изучались. Поэтому лечение пациентов с нарушениями функции печени средней и тяжелой степени препаратом Варгатеф® не рекомендуется.
НМРЛ
У пациентов с нарушениями функции печени легкой степени тяжести (класс А по шкале Чайлд-Пью) изменения начальной дозы не требуется.
ИЛФ, другие хронические фиброзирующие ИЗЛ с прогрессирующим фенотипом и ИЗЛ-ССД
Для пациентов с нарушениями функции печени легкой степени тяжести (класс А по шкале Чайлд-Пью) рекомендованная доза препарата Варгатеф® составляет 100 мг 2 раза/сут с интервалом примерно в 12 ч. Для устранения нежелательных реакций у данной категории пациентов следует рассмотреть возможность временного перерыва в лечении препаратом или окончательного прекращения терапии.
За информацией о дозировании, способе применения и модификации дозы доцетаксела следует обратиться к соответствующей инструкции по применению этого препарата.
Побочное действие
Частота побочных реакций, приведенных ниже, изложена в соответствии со следующей градацией: очень часто (≥1/10); часто (≥1/100; <1/10); нечасто (≥1/1000; <1/100); редко (≥1/10000; <1/1000); очень редко (<1/10000); неизвестно (частота не может быть оценена по доступным данным). Данные о побочных реакциях также учитывают опыт пострегистрационного применения.
НМРЛ
Наиболее частыми нежелательными реакциями, считавшимися связанными с применением нинтеданиба, были диарея, повышение активности ферментов печени (АЛТ и ACT) и рвота.
1 Данные побочные реакции наблюдались при проведении клинических исследований, однако связь с приемом препарата Варгатеф® не доказана.
2 В клинических исследованиях частота встречаемости данных побочных реакций у пациентов, принимавших нинтеданиб в комбинации с доцетакселом, не превышала частоту встречаемости таковых у пациентов, принимавших плацебо в комбинации с доцетакселом.
3 Следует обратиться также к инструкции по медицинскому применению доцетаксела.
4 Случаи панкреатита были зафиксированы у пациентов, принимавших нинтеданиб при лечении ИЛФ и НМРЛ. Большая часть этих случаев была зафиксирована у пациентов с показанием ИЛФ.
Диарея является частым нежелательным явлением со стороны ЖКТ. Отмечается тесная временная связь между развитием диареи и применением доцетаксела. В клиническом исследовании LUME-Lung 1 диарея легкой и средней степени тяжести отмечалась у большинства пациентов. Диарея ≥3 степени тяжести при применении комбинированного лечения отмечалась у 6.3% пациентов, тогда как при применении одного доцетаксела — только у 3.6% пациентов.
Такие частые побочные эффекты, как тошнота и рвота, в большинстве случаев были легкой или средней степени тяжести.
По данным клинических исследований применение препарата Варгатеф® в комбинации с доцетакселом сопровождалось более частым развитием нейтропении ≥3 степени тяжести (по критериям СТСАЕ), чем в случае применения одного доцетаксела.
Повышение активности печеночных ферментов (АЛТ, АСТ, ЩФ, ГГТ) или концентрации билирубина было в большинстве случаев обратимым при уменьшении дозы или прерывании терапии.
Ингибирование VEGFR способно привести к увеличению риска кровотечений. В клинических исследованиях у пациентов с аденокарциномой, принимавших Варгатеф®, повышение частоты кровотечений было сравнимо в обеих лечебных группах. Самым частым видом кровотечений было носовое кровотечение легкой или средней степени тяжести. Дисбаланса легочных или смертельных кровотечений не наблюдалось, о церебральных кровотечениях не сообщалось. Большинство летальных кровотечений были опухоль-ассоциированными.
В пострегистрационном периоде наблюдались случаи несерьезных и серьезных кровотечений, некоторые из которых приводили к летальному исходу. У пациентов с кровотечениями 3 или 4 степени тяжести следует тщательно оценить пользу и риск продолжения терапии препаратом Варгатеф®, а также необходимо рассмотреть возможность прекращения данной терапии. При возобновлении терапии препаратом Варгатеф® рекомендуется назначать сниженную суточную дозу.
Частота артериальной тромбоэмболии в двух лечебных группах исследования LUME-Lung 1 была сравнимой. Пациенты с недавно перенесенным инфарктом миокарда или инсультом из исследования исключались.
Частота перфораций ЖКТ в отдельных лечебных группах в клинических исследованиях была сопоставима.
ИЛФ, другие хронические фиброзирующие ИЗЛ с прогрессирующим фенотипом и ИЗЛ-ССД
Наиболее частыми нежелательными реакциями, связанными с применением нинтеданиба, были диарея, тошнота и рвота, боль в области живота, снижение аппетита, снижение массы тела и повышение активности ферментов печени.
1 Представленный термин описывает более широкую группу нежелательных явлений, нежели чем отдельное состояние или термин, предусмотренный MedDRA.
2 В пострегистрационном периоде наблюдались случаи несерьезных и серьезных кровотечений, некоторые из которых приводили к летальному исходу.
В клинических исследованиях диарея была наиболее часто репортируемым желудочно-кишечным явлением. У большинства пациентов данные явления были легкой и средней степени тяжести и отмечались на протяжении первых 3 месяцев лечения. В исследованиях INPULSIS диарея отмечалась у 62.4% по сравнению с 18.4% пациентов, получавших препарат Варгатеф® или плацебо соответственно. Диарея стала причиной снижения дозы у 10.7% пациентов, а прекращения терапии препаратом Варгатеф® — у 4.4% пациентов. В исследовании INBUILD у пациентов с другими хроническими фиброзирующими ИЗЛ с прогрессирующим фенотипом диарея была зарегистрирована у 66.9% пациентов, получавших лечение препаратом Варгатеф® по сравнению с 23.9%, получавших плацебо. Диарея стала причиной снижения дозы препарата Варгатеф® у 16.0% пациентов и причиной прекращения терапии у 5.7% пациентов.
В исследовании SENSCIS у пациентов с ИЗЛ-ССД диарея отмечалась у 75.7% в сравнении с 31.6% пациентов, получавших препарат Варгатеф® и плацебо соответственно. Диарея стала причиной снижения дозы препарата Варгатеф® у 22.2% пациентов и причиной прекращения терапии препаратом у 6.9% пациентов.
Тошнота и рвота были часто сообщаемыми нежелательными явлениями. У большинства пациентов отмечалась тошнота и рвота легкой или средней степени тяжести. Тошнота стала причиной прекращения лечения препаратом нинтеданиб у 2% пациентов, рвота стала причиной прекращения лечения у 0.8% пациентов. В исследовании INBUILD частота возникновения тошноты и рвоты, приводящих к прекращению применения препарата Варгатеф®, составила 0.3% и 0.9% соответственно. В исследовании SENSCIS тошнота и рвота стали причиной прекращения лечения препаратом Варгатеф® у 2.1% и 1.4% пациентов соответственно.
Ингибирование VEGFR может быть связано с повышением риска развития кровотечений.
В клинических исследованиях частота развития кровотечений у пациентов была незначительно выше в группе препарата Варгатеф® или сопоставимой между группами:
10.3% по сравнению с 7.8% в группе плацебо в исследовании INPULSIS;
11.1% по сравнению с 12.7% в группе плацебо в исследовании INBUILD;
11.1% по сравнению с 8.3% в группе плацебо в исследовании SENSCIS.
Наиболее частыми нежелательными явлениями в виде кровотечений были носовые кровотечения, не относившиеся к категории серьезных. Серьезные кровотечения возникали нечасто и с одинаковой частотой в обеих группах терапии:
1.3% по сравнению с 1.4% в группе плацебо в исследовании INPULSIS;
0.9% по сравнению с 1.5% в группе плацебо в исследовании INBUILD;
1.4% по сравнению с 0.7% в группе плацебо в исследовании SENSCIS.
В пострегистрационном периоде наблюдались случаи несерьезных и серьезных кровотечений, некоторые из которых приводили к летальному исходу. Из клинических исследований исключались пациенты с инфарктом миокарда или инсультом в ближайшем анамнезе. В клинических исследованиях случаи развития артериальной тромбоэмболии встречались нечасто:
2.5% по сравнению с 0.7% в группе плацебо в исследовании INPULSIS;
0.9% по сравнению с 0.9% в группе плацебо в исследовании INBUILD;
0.7% по сравнению с 0.7 % в группе плацебо в исследовании SENSCIS.
В исследовании INPULSIS у большего числа пациентов в группе препарата Варгатеф® развивался инфаркт миокарда (1.6%) по сравнению с группой плацебо (0.5%), в то время как нежелательные реакции в виде ИБС были сравнимы в группах нинтеданиба и плацебо. В исследованиях INBUILD и SENSCIS инфаркт миокарда встречался редко в группе пациентов, получавших препарат Варгатеф® — 0.9% по сравнению с 0.9% в группе плацебо в исследовании INBUILD; 0% по сравнению с 0.7% в группе плацебо в исследовании SENSCIS.
Противопоказания к применению
- гиперчувствительность к нинтеданибу, сое или арахису, или любому вспомогательному компоненту препарата;
- нарушения функции печени средней и тяжелой степени (опыт применения отсутствует);
- тяжелые нарушения функции почек (КК <30 мл/мин) (опыт применения отсутствует)*;
- активные метастазы в головной мозг (опыт применения отсутствует);
- беременность;
- период грудного вскармливания;
- возраст до 18 лет (опыт применения отсутствует).
* Эффективность и безопасность нинтеданиба у пациентов с тяжелыми нарушениями функции почек (КК <30 мл/мин) не были изучены. Почками выводится менее 1% разовой дозы нинтеданиба.
В отношении противопоказаний для доцетаксела следует обратиться к соответствующей инструкции по применению этого препарата.
С осторожностью: нарушения функции печени легкой степени тяжести; наследственная предрасположенность к кровотечениям (болезнь фон Виллебранда); стабильные метастазы в головной мозг; терапия антикоагулянтами; венозные тромбоэмболии; перфорации ЖКТ в анамнезе; пациенты, которые ранее подвергались хирургическим вмешательствам на органах брюшной полости; артериальная тромбоэмболия.
Применение при беременности и кормлении грудью
Беременность
Специальных исследований по применению препарата Варгатеф® при беременности у человека не проводилось, однако в доклинических исследованиях у животных установлена репродуктивная токсичность этого препарата. Поскольку нинтеданиб может обладать эмбриотоксическим действием у человека, препарат не следует применять при беременности. Перед началом лечения рекомендуется проведение теста на беременность, а также во время терапии по мере необходимости.
Пациенткам следует немедленно сообщить врачу о развитии беременности во время терапии препаратом Варгатеф®. Если во время терапии развивается беременность, необходимо прекратить лечение препаратом Варгатеф и проинформировать пациентку о потенциальной опасности эмбриотоксического воздействия препарата.
Применение нинтеданиба может быть вредно для плода. Женщинам детородного возраста, принимающим препарат Варгатеф®, следует рекомендовать избегать наступления беременности во время лечения препаратом Варгатеф® и использовать высокоэффективные методы контрацепции во время применения препарата и на протяжении, по крайней мере, 3 месяцев после приема последней дозы. В данный момент неизвестно, может ли нинтеданиб снижать эффективность гормональных контрацептивов, поэтому женщинам, использующим гормональные контрацептивы, необходимо использовать и барьерные методы контрацепции.
Грудное вскармливание
Специальных исследований у человека о выделении нинтеданиба и его метаболитов с грудным молоком не проводилось. В доклинических исследованиях показано, что у крыс в период лактации в грудное молоко проникает небольшое количество нинтеданиба и его метаболитов (≤0.5% от величины применявшейся дозы). Поэтому нельзя исключить риск для новорожденных и грудных детей. Во время лечения препаратом Варгатеф® кормление грудью следует прекратить.
Фертильность
В доклинических исследованиях не было выявлено признаков нарушений фертильности у самцов. В исследованиях субхронической и хронической токсичности, во время которых уровень системного воздействия препарата был сравним с уровнем, достигающимся при применении максимальной рекомендуемой дозы у человека, признаков нарушений фертильности у самок крыс обнаружено не было.
За информацией о влиянии доцетаксела на беременность, грудное вскармливание и фертильность следует обратиться к соответствующей инструкции по применению этого препарата.
Применение при нарушениях функции печени
С осторожностью следует применять препарат у пациентов с нарушениями функции печени легкой степени.
Противопоказано применение препарата пациентам с нарушениями функции печени средней и тяжелой степени (опыт применения отсутствует).
Применение при нарушениях функции почек
С осторожностью следует применять препарат у пациентов с нарушениями функции печени легкой степени.
Противопоказано применение пациентам с тяжелыми нарушениями функции почек (КК <30 мл/мин) (опыт применения отсутствует).
Применение у детей
Применение препарата у детей и подростков в возрасте до 18 лет противопоказано (опыт применения отсутствует).
Применение у пожилых пациентов
Не отмечено никаких общих различий по безопасности и эффективности применения препарата у пациентов пожилого возраста (>65 лет) по сравнению с пациентами в возрасте до 65 лет. Коррекция дозы препарата в зависимости от возраста пациента не требуется.
Особые указания
Желудочно-кишечные расстройства
Диарея. Лечение диареи (адекватная гидратация и антидиарейные лекарственные средства, например, лоперамид) следует проводить при появлении первых признаков. В случае развития диареи может потребоваться прерывание лечения, снижение дозы или прекращение терапии.
Тошнота и рвота. В случае сохранения тошноты и рвоты, несмотря на симптоматическое лечение (включая противорвотную терапию), может потребоваться снижение дозы, прерывание лечения или прекращение терапии.
Диарея и рвота могут приводить к обезвоживанию с нарушением или без нарушения водно-электролитного баланса, что может приводить к нарушениям функции почек. В случае обезвоживания рекомендуется восстановление водно-электролитного баланса.
Если возникают существенные желудочно-кишечные нежелательные явления, необходимо проведение контролировать концентрации электролитов в крови.
Нейтропения и сепсис
Во время терапии НМРЛ препаратом Варгатеф®, в частности при комбинации с доцетакселом, необходимо проводить мониторинг форменных элементов крови на предмет развития нейтропении и возможных последующих осложнений в виде сепсиса или фебрильной нейтропении. Частое мониторирование всех форменных элементов крови следует осуществлять в начале каждого цикла лечения у пациентов, получающих терапию нинтеданибом в комбинации с доцетакселом, в период наименьших значений нейтрофилов, а также при наличии клинических показаний после окончания последнего цикла терапии данной комбинацией.
Нарушения функции печени
Безопасность и эффективность препарата не изучалась у пациентов с нарушениями функции печени средней (класс В по шкале Чайлд-Пью) или тяжелой (класс С по шкале Чайлд-Пью) степени. Поэтому у таких пациентов применение препарата Варгатеф® не рекомендуется.
НМРЛ. В связи с повышением концентрации препарата в крови риск развития нежелательных явлений может быть выше у пациентов с легкими нарушениями функции печени (класс А по шкале Чайлд-Пью).
При проведении терапии нинтеданибом наблюдались случаи лекарственного поражения печени. В пострегистрационном периоде были получены сообщения о тяжелых формах лекарственного поражения печени с летальным исходом.
После начала терапии рекомендуется тщательный контроль активности печеночных трансаминаз, ЩФ и концентрации билирубина (периодически, во время начала комбинации с доцетакселом, т.е. в начале каждого лечебного цикла). Если отмечается существенное повышение активности печеночных ферментов, может потребоваться прерывание лечения, уменьшение дозы или прекращение терапии препаратом Варгатеф®.
Перед началом комбинированного лечения препаратом Варгатеф® и доцетакселом следует определять активность трансаминаз, ЩФ и содержание билирубина. Эти показатели следует контролировать в зависимости от клинических показаний или периодически во время лечения, например, в фазе комбинации с доцетакселом в начале каждого цикла терапии и ежемесячно, если прием препарата Варгатеф® продолжается в виде монотерапии после прекращения терапии доцетакселом.
Если выявляется соответствующее повышение активности ферментов печени, может потребоваться перерыв в лечении, снижение дозы или прекращение терапии препаратом Варгатеф® (см. раздел «Режим дозирования»/таблица 2). Следует проводить поиск альтернативных причин повышения активности ферментов печени и принятие соответствующих мер при необходимости.
В случае повышения активности ферментов печени (ACT/АЛТ) более чем в 3 раза по сравнению с ВГН в сочетании с повышением уровня билирубина в 2 и более раза по сравнению с ВГН и повышением активности ЩФ менее чем в 2 раза по сравнению с ВГН, терапию препаратом Варгатеф® следует прервать. Если не будет установлена альтернативная причина изменений этих лабораторных показателей, Варгатеф® следует окончательно отменить.
Для пациентов женского пола и азиатского происхождения характерен более высокий риск повышения активности печеночных ферментов.
Увеличение экспозиции нинтеданиба характеризовалось линейной зависимостью от возраста пациента, а также было обратно пропорционально массе тела, что также может повлечь за собой более высокий риск повышения активности печеночных ферментов. У пациентов с этими факторами риска рекомендуется тщательный контроль показателей функции печени.
ИЛФ, другие хронические фиброзирующие ИЗЛ с прогрессирующим фенотипом и ИЗЛ-ССД. В связи с повышением концентрации препарата в крови риск развития нежелательных явлений может быть выше у пациентов с легкими нарушениями функции печени (класс А по шкале Чайлд-Пью). Пациенты с легкими нарушениями функции печени (класс А по шкале Чайлд-Пью) должны получать сниженную дозу препарата Варгатеф®.
При проведении терапии нинтеданибом наблюдались случаи лекарственного поражения печени. В пострегистрационном периоде были получены сообщения о несерьезных и серьезных случаях лекарственного поражения печени, включая тяжелые формы лекарственного поражения печени с летальным исходом.
Большая часть нарушений со стороны печени наблюдаются в течение первых 3 месяцев терапии. Таким образом, рекомендуется оценивать активность печеночных трансаминаз и концентрацию билирубина до начала терапии препаратом Варгатеф® регулярно в течение первых 3 месяцев терапии, а затем периодически во время лечения (например, при каждом визите пациента) или по клиническим показаниям.
Повышение активности печеночных ферментов (АЛТ, ACT, ЩФ, ГГТ) и билирубина было в большинстве случаев обратимым при уменьшении дозы или прерывании терапии.
В случае повышения активности трансаминаз (ACT или АЛТ) более чем в 3 раза выше ВГН рекомендовано уменьшить дозу или прервать терапию препаратом Варгатеф® и наблюдать за состоянием пациента. Как только показатели трансаминаз вернутся к исходному уровню, доза препарата Варгатеф® может быть вновь повышена до полной (150 мг 2 раза/сут) или лечение может быть возобновлено в сниженной дозе (100 мг 2 раза/сут), которая впоследствии может быть повышена до полной дозы. Если повышение каких-либо показателей функции печени сопровождается клиническими признаками или симптомами повреждения печени, например, желтухой, лечение препаратом следует окончательно прекратить. Следует провести поиск альтернативных причин повышения активности ферментов печени.
Для пациентов с низкой массой тела (<65 кг), лиц азиатского происхождения и пациентов женского пола характерен более высокий риск повышения активности печеночных ферментов.
Увеличение экспозиции нинтеданиба характеризовалось линейной зависимостью от возраста пациента, что также может повлечь за собой более высокий риск повышения активности печеночных ферментов.
У пациентов с этими факторами риска рекомендуется тщательный контроль показателей функции печени.
Риск развития кровотечений
Данных о применении препарата Варгатеф® у пациентов с наследственной предрасположенностью к кровотечениям (например, болезнь Виллебранда) не имеется.
НМРЛ. Пациенты с недавно отмечавшимся легочным кровотечением (>2.5 мл крови), а также пациенты с центрально расположенными опухолями и рентгенологическими признаками локальной инвазии крупных сосудов или с рентгенологическими признаками наличия полостей или некротических изменений опухоли исключались из клинических исследований. Поэтому применение препарата Варгатеф® у таких пациентов не рекомендуется.
• метастазы в головной мозг
Увеличение частоты церебральных кровотечений у пациентов с ранее адекватно лечеными метастазами в головной мозг (стабильными в течение ≥4 недель до начала лечения препаратом Варгатеф®) не наблюдалось. Однако таких пациентов следует тщательно наблюдать в отношении признаков и симптомов церебральных кровотечений.
Пациенты с активными метастазами в головной мозг исключались из клинических исследований, применение препарата Варгатеф® у них не рекомендуется.
• терапия антикоагулянтами
В клинические исследования включались пациенты, получавшие длительную терапию низкомолекулярными гепаринами в низких дозах или ацетилсалициловой кислотой в дозах ≤325 мг/сут. Увеличение частоты кровотечений у таких пациентов не наблюдалось. Данных о применении препарата Варгатеф® у пациентов, предварительно получавших лечение антикоагулянтами в более высоких дозах, не имеется. Пациентам, у которых во время лечения препаратом Варгатеф® развивались тромбоэмболические нарушения, в связи с чем требовалась терапия антикоагулянтами, разрешалось продолжить прием препарата Варгатеф®, при этом увеличения частоты кровотечений не отмечалось. У пациентов, принимающих такие антикоагулянты, как варфарин или фенпрокумон, необходимо регулярно контролировать протромбиновое время, МНО или следить за клиническими признаками кровотечений.
ИЛФ, другие хронические фиброзирующие ИЗЛ с прогрессирующим фенотипом и ИЗЛ-ССД. В клинические исследования не включались пациенты с известным риском развития кровотечений, включая пациентов с наследственной предрасположенностью к кровотечениям или пациентов, получающих антикоагулянтную терапию в высоких дозах. Следовательно, данной категории пациентов лечение препаратом Варгатеф® следует назначать только в том случае, если потенциальная польза проводимой терапии превышает потенциальный риск.
Артериальная тромбоэмболия
Необходимо соблюдать осторожность при лечении пациентов с высоким сердечно-сосудистым риском, включая ИБС. Следует рассмотреть возможность перерыва в лечении пациентов, у которых развились симптомы острой ишемии миокарда.
Венозная тромбоэмболия
НМРЛ. У пациентов, получающих Варгатеф®, отмечался повышенный риск венозных тромбоэмболий, в т.ч. тромбоза глубоких вен. Пациентов следует тщательно наблюдать в отношении тромбоэмболических нарушений. У пациентов с опасными для жизни венозными тромбоэмболиями Варгатеф® необходимо отменить.
ИЛФ, другие хронические фиброзирующие ИЗЛ с прогрессирующим фенотипом и ИЗЛ-ССД. В клинических исследованиях не наблюдалось повышенного риска развития венозных тромбоэмболических осложнений. Однако в связи с особенностями механизма действия нинтеданиба у пациентов может отмечаться повышенный риск развития тромбоэмболических явлений.
Перфорации ЖКТ
Частота перфораций ЖКТ в отдельных лечебных группах в клинических исследованиях была сопоставима. Однако механизм действия препарата Варгатеф® указывает на возможность повышения риска перфораций ЖКТ. В пострегистрационном периоде были получены сообщения о случаях перфорации ЖКТ, некоторые из которых приводили к летальному исходу. Особое внимание следует уделять лечению пациентов, которые ранее подвергались абдоминальным хирургическим вмешательствам, или перенесших перфорацию полого органа в недавнем анамнезе, а также пациентов с ИЛФ, имеющих в анамнезе пептическую язву, дивертикулез или получающих сопутствующую терапию ГКС или НПВП. В связи с этим Варгатеф® можно применять только, как минимум, через 4 недели после обширных хирургических вмешательств (включая абдоминальные). В случае возникновения гастроинтестинальной перфорации терапию препаратом Варгатеф® следует прекратить.
Нарушение заживления ран
Нинтеданиб, в связи с особенностями механизма действия, может нарушать заживление ран. В клинических исследованиях увеличение частоты нарушений заживления ран не наблюдалось. Специальных исследований, в которых бы изучалось влияние нинтеданиба на заживление ран, не проводилось. Поэтому лечение следует начинать или возобновлять (если осуществлялся перерыв в связи с хирургическим вмешательством) с учетом клинического мнения об адекватности заживления раны.
Особые группы пациентов
В исследовании LUME-Lung 1 у пациентов с массой тела менее 50 кг, принимавших нинтеданиб в сочетании с доцетакселом, наблюдалась более высокая частота развития серьезных нежелательных явлений, чем у пациентов с массой тела ≥50 кг, хотя число пациентов с массой тела менее 50 кг было небольшим. Поэтому рекомендуется тщательное наблюдение за пациентами с массой тела менее 50 кг.
Влияние на способность к управлению транспортными средствами и механизмами
Исследований по влиянию препарата на способность к управлению транспортными средствами и занятию другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций, не проводилось.
Во время применения препарата Варгатеф® пациентам следует соблюдать осторожность при управлении транспортными средствами или механизмами.
Передозировка
Симптомы: в клинических исследованиях нинтеданиб изучался в максимальной однократной дозе 450 мг 1 раз/сут. Также зафиксированы случаи передозировки при применении препарата в максимальной дозе 600 мг в течение 8 дней. Наблюдавшиеся нежелательные явления были сопоставимы с известным профилем безопасности нинтеданиба: увеличение активности ферментов печени и нарушения со стороны ЖКТ. Пациенты полностью восстановились после нежелательных явлений. В исследованиях INPULSIS был зафиксирован один случай непреднамеренного повышения дозы до 600 мг 2 раза/сут на протяжении 21 дня у пациента с ИЛФ. В период некорректного приема препарата было зафиксировано развитие несерьезного нежелательного явления (назофарингит), которое купировалось в данном периоде без регистрации каких-либо других нежелательных реакций.
Лечение: специфического антидота на случай передозировки нет. При подозрении на передозировку необходимо отменить Варгатеф® и проводить симптоматическую терапию.
Лекарственное взаимодействие
Индукторы/ингибиторы P-gp
Нинтеданиб является субстратом для P-gp. Показано, что совместное применение с активным ингибитором P-gp кетоконазолом увеличивает экспозицию нинтеданиба, судя по величине AUC, в 1.61 раза, а судя по величине Сmax, в 1.83 раза.
Одновременное применение рифампицина (активного индуктора P-gp) приводит к уменьшению экспозиции нинтеданиба, судя по величине AUC, на 50.3%, а судя по величине Сmax, на 60.3% (по сравнению с применением только нинтеданиба).
Активные ингибиторы P-gp (например, кетоконазол или эритромицин) в случае совместного применения с препаратом Варгатеф® могут увеличивать экспозицию нинтеданиба. У таких пациентов переносимость нинтеданиба следует тщательно контролировать.
Активные индукторы P-gp (например, рифампицин, карбамазепин, фенитоин и препараты зверобоя продырявленного) могут уменьшать экспозицию нинтеданиба. Рекомендуется подбор альтернативной сопутствующей терапии с отсутствием или минимальным индуцирующим действием на систему P-gp.
Изоферменты CYP
Изоферменты CYP принимают лишь небольшое участие в биотрансформации нинтеданиба. В доклинических исследованиях нинтеданиб и его метаболиты (свободный кислый метаболит нинтеданиба и его глюкуронид) не ингибировали и не индуцировали изоферменты CYP. Поэтому вероятность лекарственного взаимодействия с нинтеданибом, основанного на влиянии на изоферменты CYP, считается небольшой.
Одновременное применение с пирфенидоном
Было проведено изучение совместного применения нинтеданиба и пирфенидона у пациентов с ИЛФ в рамках специального фармакокинетического исследования. Пациенты первой группы получали однократную дозу нинтеданиба 150 мг до начала постепенного повышения дозы пирфенидона до максимальной (по 801 мг 3 раза/сут), и еще одну дозу нинтеданиба 150 мг по достижении равновесного состояния (в последний день). Пациенты второй группы получали пирфенидон в постоянной дозе 801 мг 3 раза/сут. У них была проведена оценка фармакокинетического профиля до начала совместной терапии и через 7 дней совместного приема нинтеданиба в дозе 150 мг 2 раза/сут. В первой группе скорректированные соотношения среднегеометрических значений (90% ДИ) составляли 93% (57-151%) и 96% (70-131%) для показателей Сmax и AUC0-tz нинтеданиба соответственно (n=12). Во второй группе скорректированные соотношения среднегеометрических значений (90% ДИ) составляли 97% (86-110%) и 95% (86-106%) для показателей Cmaxss и AUCt,ss пирфенидона соответственно (n=12). На основании полученных результатов можно сделать вывод об отсутствии признаков значимого фармакокинетического взаимодействия между нинтеданибом и пирфенидоном при совместном применении.
Одновременное применение с другими препаратами
Одновременное применение нинтеданиба с доцетакселом (75 мг/м2) не изменяет в существенной степени фармакокинетику этих препаратов.
Одновременное применение нинтеданиба с бозентаном не изменяет фармакокинетику нинтеданиба.
Возможность взаимодействия нинтеданиба с гормональными контрацептивными средствами не изучалась.
Одновременный прием с пищей
Варгатеф® рекомендуется принимать одновременно с пищей (см. раздел «Фармакокинетика»).
Условия хранения препарата Варгатеф®
Препарат следует хранить в недоступном для детей месте в оригинальной упаковке при температуре не выше 25°С.
Срок годности препарата Варгатеф®
Срок годности — 3 года. Не применять после истечения срока годности.
Условия реализации
Препарат отпускается по рецепту.
Контакты для обращений
БЕРИНГЕР ИНГЕЛЬХАЙМ ИНТЕРНЕШНЛ ГМБХ
(Германия)
|
|
ООО «Берингер Ингельхайм» |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код

Товары из категории — Препараты для лечения онкологических заболеваний
Инструкция по применению
Цена в интернет-аптеке WER.RU: от 74 000
Форма выпуска, состав и упаковка
Варгатеф в Москве выпускается в форме таблеток. Покрытие: пленочная оболочка. Варгатеф имеет следующий состав:
• nintedanib;
• липиды, которые включают в себя три насыщенные жира, привязанные к глицериновой основе;
• сложный эфир трехатомного спирта в твердом виде;
• гидролизованный протеин коллаген;
• смесь фосфолипидов с триглицеридами;
• трехатомный спирт;
• амфотерный оксид четырёхвалентного титана;
• пищевая добавка Е172;
• этанол;
• пропиленгликоль;
• изопропанол;
• шеллак;
• бутанол;
• вода;
• денатурированный спирт.
Варгатеф купить можно в нашей интернет-аптеке. Средняя цена препарата Варгатеф составляет 130 000 рублей. Доставка осуществляет по Московской области и всей территории России. Препарат выпускается в Германии. При заказе обязательно уточните наличие.
Показания
Ингибитор киназы, который блокирует несколько путей. Имеет применение для лечения идиопатического легочного фиброза (ИФЛ), значительно снижает снижение принудительной жизненной емкости.
Не рекомендуется для умеренных и тяжелых заболеваний печени или у женщин, которые могут забеременеть. Использовать контрацепцию во время использования и в течение 3 месяцев после последней дозы. Варгатеф заказать можно у нас на сайте.
Противопоказания
Согласно инструкции, препарат имеет ряд противопоказаний:
• индивидуальная непереносимость любого компонента препарата;
• печеночная недостаточность (легкая форма требует пересмотра дозировки);
• почечная недостаточность (легкая форма требует пересмотра дозировки);
• одновременный прием аналогов варгатефа;
• известная или возможная беременность;
• лактация;
• дети;
• подростки;
• лица, не достигшие 18-ти летнего возраста.
Фармакологическое действие
Патогенез идиопатической болезни легких, при которой стенки воздушных мешочков в легких (альвеолы) зарастают грубой рубцовой тканью и утолщаются (IPF) связан с FGFR, PDGFR и VEGFR; вклад FLT3 в патогенез IPF неизвестен. Nintedanib конкурентно связывается с АТФ-связывающим карманом этих рецепторов, полностью предотвращая передачу сигналов на клеточном уровне и ингибирует разрастание клеток, передвижение и мутацию фибробластов. Вклад ингибирования нерецепторных тирозин-специфичных протеинкиназ в эффективность Активного вещества при IPF неизвестен.
Согласно врачебным отзывам, варгатеф является низкомолекулярным замедляющим веществом многих рецепторов тирозин-специфичних протеинкиназ. Кроме того, Активное вещество ингибирует нерецепторные тирозин-специфичная протеинкиназы (nRTK), Lck, Lyn и Src киназу.
Варгатеф вводят перорально. Фармакокинетические свойства Активного вещества были схожи у здоровых добровольцев, больных с IPF и больных раком, и препарат проявляет линейную фармакокинетику. Активное вещество имеет двухфазное распределение и сильно (97,8%) связан с протеином, причем основным связывающим протеином считается сывороточный альбумин. Препарат имеет объем распределения, который превышает общий объем тела. Препарат преимущественно распределяется в плазму с коэффициентом распределения плазмы к крови 0,87. Стационарные уровня в плазме достигаются в течение 1 недели после введения, а минимальные уровня остаются стабильными в течение более 1 года. Активное вещество обладает умеренной и высокой фармакокинетической вариабельностью между пациентами (уровень изменений стандартного фармакокинетического параметра варьируется от 25 до 65%) и внутрибольничным уровнем от низкого до умеренного (параметр изменений менее 38%).
Более 90% каждой дозы выводится с помощью желчных/фекальных экскреций. Варгатеф подвергается гидролитическому расщеплению эстеразами, что приводит к активному метаболиту BIBF 1202. Однако, будучи активным, BIBF 1202 является значительно менее сильнодействующим, чем исходное соединение, и не вносит основной вклад в общее действие Активного вещества. Затем BIBF 1202 глюкуронидируют до неактивного метаболита парной глюкуроновой кислоты BIBF 1202 с помощью UGT1A1, UGT1A7, UGT1A8 и UGT1A10. CYP3A4 участвует в мутировании активного вещества в незначительной степени, in vitro CYP-зависимый обмен веществ составляет 5% по сравнению с 25% для расщепления сложного эфира. Время 50% выведения варгатефа составляет 9,5 часов, а общий показатель очищения плазмы — 1390 мл/мин внутривенной (в/в) инфузии. Вывод системой мочеиспускания лекарства происходит на протяжении 48 часов и составляет 0,05% от дозировки после перорального принятия и 1,4% после использования внутривенно. При этом очищение плазмы происходило со скоростью 20 мл/мин.
Затрагиваемые изоферменты цитохрома P450 (CYP450) и переносчики лекарств: P-гликопротеин (P-gp), CYP3A4.
Варгатеф является субстратом и слабым замедляющим веществом (P-gp), а также второстепенным субстратом CYP3A4. In vitro варгатеф также является слабым замедляющим веществом OCT-1 и BCRP; эти ингибирующие эффекты имеют низкую клиническую значимость.
Абсолютная пероральная биодоступность составила 4,7% (90% ДИ, от 3,62 до 6,08) для дозы 100 мг у здоровых добровольцев в условиях сытости. Абсорбция и биодоступность снижаются за счет эффектов транспорта и существенного обмена веществ первого прохода. Пища (независимо от типа пищи) увеличивает воздействие варгатефа приблизительно на 20% и задерживает время до максимального уровня (Tmax) с 2 часов до 3,98 часов по сравнению с условиями голодания. При приеме с пищей пиковые уровня варгатефа в плазме (Cmax) достигаются в течение 2–4 часов после перорального приема. Препарат рекомендуется принимать внутрь во время еды.
После внутривенного вливания объем распределения (1050 мл) был больше общего объема тела.
Дозировка
150 мг варгатефа дважды в 24 часа, применяют примерно каждые 12 часов. В 3 рандомизированных двойных слепых плацебо-контролируемых клинических исследованиях (n = 1 231) пациенты с идиопатическим легочным фиброзом (IPF), получавшие нинтеданиб, имели значительно сниженную годовую скорость снижения FVC (от -60 до -115 мл) по сравнению с плацебо (от -191 до -240 мл), после поправки на пол, рост и возраст. В 2 из 3 клинических испытаний нинтеданиб также улучшил процентное изменение принудительной жизненной емкости (FVC) по сравнению с исходным уровнем в течение 52 недель. Клинические испытания фазы II и фазы III продемонстрировали значительно сниженный риск первого острого обострения IPF у больных, получавших нинтеданиб (ЧСС 0,16; 95% ДИ от 0,04 до 0,71) по сравнению с плацебо; третье клиническое исследование (фаза III) не выявило различий между группами лечения. Нинтеданиб не влиял на общую смертность.
Печеночная недостаточность
Исходная печеночная недостаточность
Class A: Уменьшите дозировку варгатефа до 100 мг перорально каждые 12 часов.
Class B или C: лечение nintedanib не рекомендуется. Безопасность и эффективность не были изучены у больных с тяжелой печеночной недостаточностью.
Вызванная лечением гепатотоксичность
Легкая печеночная недостаточность (Child Pugh A): Рассмотрите возможность прерывания или прекращения терапии для лечения побочных реакций.
AST/ALT в 3-5 раз выше верхнего предела нормы (ULN) без признаков серьезного повреждения печени: проводить лечебный курс варгатефом или уменьшить дозировку до 100 мг перорально по дважды в 24 часа. Когда ферменты печени возвращаются к исходному уровню, лечение нинтеданибом может быть возобновлено в уменьшенной дозе (то есть 100 мг перорально по дважды в 24 часа), а затем впоследствии увеличено до полной дозы (150 мг перорально по дважды в 24 часа).
AST/ALT более чем в 3 раза ULN с признаками или симптомами серьезного повреждения печени или AST/ALT более чем в 5 раз ULN: прекратить лечебный курс нинтеданибом.
Почечная недостаточность
CrCl больше или равно 30 мл/мин: корректировка дозировки не требуется.
CrCl менее 30 мл/мин или почечная недостаточность конечной стадии: безопасность и эффективность варгатефа не изучались.
МАКСИМАЛЬНАЯ ДОЗИРОВКА
Взрослые
300 мг/сут.
Гериатрическая группа
300 мг/сут.
Подростки
Не проводились адекватные информативные клинические исследования с данной группой пациентов.
Дети
Не проводились адекватные информативные клинические исследования с данной группой пациентов.
Новорожденные
Не проводились адекватные информативные клинические исследования с данной группой пациентов.
Капсулы Nintedanib должны приниматься с пищей. Администрирование капсулы целиком с жидкостью. Пациент не должен жевать или раздавливать капсулу из-за горького вкуса и неизвестного влияния на эффективность препарата. Если пропущена дозировка, примите следующую дозировку в следующее запланированное время, не принимайте 2 дозы одновременно.
Побочные действия
Описание побочных эффектов:
• тромбоэмболия;
• диарея;
• инфаркт миокарда;
• перфорация GI;
• новое первичное злокачественное новообразование;
• панкреатит;
• кардиомиопатия;
• инсульт;
• тошнота;
• гипертонический криз;
• повышенные печеночные ферменты;
• кровотечение;
• рвота;
• гипертония;
• гипотиреоз;
• обезвоживание;
• желтуха;
• гипербилирубинемия;
• тромбоцитопения;
• боль в животе;
• анорексия;
• потеря веса;
• головная боль;
• инфекция.
Передозировка
При чрезмерном принятии препарата в первую очередь страдает печеночная функциональность, что может привести к тяжелым последствиям.
Лекарственное взаимодействие
Ацетаминофен, Butalbital. Избегайте использования барбитуратов с варгатефом, так как ожидается, что эти препараты уменьшат воздействие nintedanib и поставят под угрозу его эффективность. Барбитураты являются индукторами CYP3A4, и некоторые барбитураты, такие как фенобарбитал, также индуцируют P-гликопротеин (P-gp). В исследованиях взаимодействия лекарств введение двойного P-gp и индуктора CYP3A4 с nintedanib снижало AUC nintedanib на 50%.
Антикоагулянты. Варгатеф является замедляющим веществом VEGFR и может увеличить риск кровотечений. Мониторинг больных, которые принимают антикоагулянты тесно и скорректировать антикоагулянтную лечебный курс по мере необходимости. Используйте Nintedanib у больных с известным риском кровотечения, только если ожидаемая польза превышает потенциальный риск.
Апалутамид. Избегайте совместного назначения варгатеф с апалутамидом из-за снижения уровня nintedanib в плазме. Nintedanib является субстратом P-гликопротеина (P-gp) и, в незначительной степени, CYP3A4. Апалутамид является сильным индуктором CYP3A4, а также слабым индуктором P-gp. Coadministration с пероральными дозировками другого P-GP и CYИндуктор P3A4 снизил воздействие nintedanib на 50%.
Аспирин, Butalbital, кофеин. Избегайте использования барбитуратов с варгатефом, так как ожидается, что эти препараты уменьшат воздействие nintedanib и поставят под угрозу его эффективность. Барбитураты являются индукторами CYP3A4, и некоторые барбитураты, такие как фенобарбитал, также индуцируют P-гликопротеин (P-gp). В исследованиях взаимодействия лекарств введение двойного P-gp и индуктора CYP3A4 с nintedanib снижало AUC nintedanib на 50%.
Карбамазепин. Избегайте использования карбамазепина с nintedanib, так как ожидается, что карбамазепин уменьшит воздействие nintedanib и поставит под угрозу его эффективность. Карбамазепин является мощным P-гликопротеином (P-gp) и индуктором CYP3A4, nintedanib является субстратом P-gp и второстепенным субстратом CYP3A4. В исследованиях взаимодействия лекарств введение двойного P-gp и индуктора CYP3A4 с nintedanib снижало AUC nintedanib на 50%.
Conivaptan. Избегайте одновременного использования, так как производитель conivaptan рекомендует, чтобы взаимодействующие субстраты не использовались одновременно, Лечение Nintedanib может быть начато не ранее, чем через 1 неделю после завершения терапии Кониваптаном. Ожидается, что двойные ингибиторы P-гликопротеина (P-gp) и CYP3A4, такие как кониваптан, увеличат воздействие и клинический эффект nintedanib. Если необходимо совместное использование, внимательно следите за усилением побочных эффектов nintedanib, включая желудочно-кишечную токсичность (тошнотные и рвотные позывы, расстройство желудка, болевые ощущения в брюхе, потеря аппетита), головные боли, повышение уровня печеночных ферментов и гипертонию. Может потребоваться снижение дозы, прерывание терапии или прекращение терапии nintedanib. Кониваптан является двойным замедляющим веществом CYP3A4 и P-gp, nintedanib представляет собой субстрат P-gp и минорный субстрат CYP3A4. В исследованиях лекарственных взаимодействий введение nintedanib с двойным замедляющим веществом P-gp и CYP3A4 увеличило AUC nintedanib на 60%.
Фосфенитоин. Избегайте использования фосфенитоина с nintedanib, если это возможно, так как ожидается, что фосфенитоин уменьшит воздействие nintedanib и поставит под угрозу его эффективность. Фосфенитоин является мощным индуктором CYP3A4 и мягкого P-гликопротеина (P-gp), nintedanib является субстратом P-gp и второстепенным субстратом CYP3A4. В исследованиях взаимодействия лекарств введение двойного P-gp и индуктора CYP3A4 с nintedanib снижало AUC nintedanib на 50%.
Грейпфрутовый сок. Пациентам следует ограничивать или избегать грейпфрутовый сок во время лечения нинтеданибом. Грейпфрутовый сок является мощным ингибитором CYP3A4 и умеренным ингибитором P-гликопротеина (P-gp), nintedanib является субстратом P-gp, а также второстепенным субстратом CYP3A4. Coadministration может увеличить концентрацию и клинический эффект nintedanib. Если пациент продолжает регулярно употреблять грейпфрутовый сок в рационе, внимательно следите за усилением побочных эффектов нинтеданиба, включая тошноту, рвоту, диарею, желудочно-кишечную токсичность или повышенные ферменты печени. Если это произойдет, пациент должен прекратить использование грейпфрутового сока.
Пирфенидон. В исследовании с множественными дозами у японских пациентов с идиопатическим легочным фиброзом совместное введение с пирфенидоном снизило воздействие нинтеданиба до 68,3% на основе AUC и 59,2% на основе Cmax по сравнению с одним нинтеданибом. Клиническая значимость этих изменений, в том числе применимость к другим группам населения, не известна. Влияние комбинированного введения нинтеданиба на AUC и Cmax пирфенидона оценивали в исследовании с множественными дозами. Нинтеданиб не оказывал влияния на воздействие пирфенидона.
Зверобой, зверобой продырявленный. Пациенты избегают использования добавок зверобоя, зверобоя продырявленного, во время лечения нинтеданибом, так как эта трава, вероятно, уменьшает воздействие нинтеданиба и снижает его эффективность. Зверобой является мощным двойным индуктором CYP3A4 и P-гликопротеина (P-gp), nintedanib является субстратом P-gp и второстепенным субстратом CYP3A4. В исследованиях взаимодействия лекарств введение двойного P-gp и индуктора CYP3A4 с нинтеданибом снижало AUC нинтеданиба на 50%.
Thiopental. Избегайте использования барбитуратов с нинтеданибом, так как ожидается, что эти препараты уменьшат воздействие нинтеданиба и поставят под угрозу его эффективность. Барбитураты являются индукторами CYP3A4, и некоторые барбитураты, такие как фенобарбитал, также индуцируют P-гликопротеин (P-gp). В исследованиях взаимодействия лекарств введение двойного P-gp и индуктора CYP3A4 с нинтеданибом снижало AUC нинтеданиба на 50%.
Тикагрелор. Двойные ингибиторыОжидается, что P-гликопротеин (P-gp) и CYP3A4, такие как тикагрелор, увеличат воздействие и клинический эффект нинтеданиба. Если необходимо совместное использование, внимательно следите за усилением побочных эффектов нинтеданиба, включая желудочно-кишечную токсичность (тошнота, рвота, диарея, боль в животе, потеря аппетита), головную боль, повышение уровня печеночных ферментов и гипертонию. Может потребоваться снижение дозы, прерывание терапии или прекращение терапии нинтеданибом. Тикагрелор является слабым ингибитором как P-gp, так и CYP3A4, nintedanib представляет собой субстрат P-gp и минорный субстрат CYP3A4. В исследованиях лекарственных взаимодействий введение нинтеданиба с двойным ингибитором P-gp и CYP3A4 увеличило AUC нинтеданиба на 60%.
Варфарин. Nintedanib является ингибитором VEGFR и может увеличить риск кровотечения. Мониторинг пациентов, которые принимают антикоагулянты тесно и скорректировать антикоагулянтную терапию по мере необходимости. Используйте nintedanib у пациентов с известным риском кровотечения, только если ожидаемая польза превышает потенциальный риск.
Циметидин: (Незначительные) Ингибиторы OCT2 (например, цимедитин) могут увеличивать воздействие препарата, но эти изменения могут не требовать коррекции дозы nintedanib, поскольку увеличение системного воздействия не ожидается клинически значимым. Введение Циметидина (300 мг четыре раза в день) с nintedanib (2 мг однократная доза) 12 курильщикам увеличивало системное воздействие лекарства на 29% из-за уменьшения почечного клиренса. Исследования in vitro показали, что активная почечная секреция вещества опосредуется переносчиком органических катионов человека OCT2. Другой антагонист Н2 может быть предпочтительнее циметидина у пациентов, принимающих nintedanib.
Этанол. Пациентам следует рекомендовать уменьшить количество алкоголя, который они принимают при приеме нинтеданиба, до тех пор, пока они не узнают, влияет ли препарат на их толерантность к этанолу. Некоторые сообщения о психоневрологических расстройствах, включая необычное и иногда агрессивное поведение, направленное на себя или других, могли усугубляться сопутствующим употреблением пациентом алкоголя. Были постмаркетинговые сообщения о пациентах, испытывающих повышенную интоксикацию этанолом при приеме nintedanib. Некоторые случаи описывают необычное и иногда агрессивное поведение и часто сопровождаются амнезией по поводу событий.
Тафенохин. Ингибиторы OCT2 (например, тафенохин) могут увеличивать воздействие nintedanib, но эти изменения могут не требовать коррекции дозы, поскольку увеличение системного воздействия не ожидается клинически значимым. Введение известного ингибитора OCT2 с nintedanib (однократная доза 2 мг) 12 курильщикам увеличивало системное воздействие препарата на 29% из-за уменьшения почечного клиренса. Исследования in vitro показали, что активная почечная секреция нинтеданиба опосредуется переносчиком органических катионов человека OCT2. Влияние совместного назначения тафенохина на фармакокинетику субстратов OCT2 у людей неизвестно. Тем не менее, наблюдения in vitro предполагают возможность увеличения концентрации субстратов OCT2.
Особые указания
Беременность
Не используйте nintedanib во время беременности. Хотя не существует адекватных и контролируемых исследований на беременных женщинах, может возникнуть вред для плода при назначении нинтеданиба во время беременности. Женщинам с репродуктивным потенциалом следует избегать беременности во время терапии нинтеданибом. В исследованиях на репродуктивную токсичность у животных нинтеданиб был тератогенным и эмбриофетоцидным у крыс и кроликов при воздействии в 5 раз или менее, чем максимальная рекомендуемая доза для человека (MRHD) у взрослых. Пороки развития включали аномалии в сосудистой сети (отсутствующие или дополнительные крупные кровеносные сосуды), мочеполовой системы (отсутствующие органы) и скелетной системы. Аномалии скелета включали аномалии в грудных, поясничных и хвостовых позвонках (например, гемивертебра, отсутствующие или асимметрично окостеневшие), ребра (раздвоенные или сросшиеся) и грудные кости (расплавленные, расщепленные или односторонне окостеневшие). У кроликов значительное изменение соотношения полов наблюдалось у плодов (самка: самец примерно 71%: 29%) при AUC, что примерно в 15 раз больше MRHD. Послеродовая жизнеспособность щенков крысы в течение первых 4 постнатальных дней также была снижена, когда плотины подвергались воздействию AUC, эквивалентному меньшему, чем MRHD.
Грудное вскармливание
По словам производителя, неизвестно, если nintedanib из организма в материнском молоке. Из-за возможности серьезных побочных реакций у грудных детей следует рекомендовать женщинам прекратить nintedanib или прекратить грудное вскармливание.
Азиатские пациенты, женщины, гериатрия, заболевание печени, гепатотоксичность, желтуха
Уменьшите дозу нинтеданиба у пациентов с легкими заболеваниями печени (Child Pugh A). Нинтеданиб не рекомендуется пациентам с заболеваниями печени средней или тяжелой степени (ребенок Пью Б или В), это не было изучено в пациентах с серьезной болезнью печени. Терапия Nintedanib может вызвать повышение билирубина и ферментов печени, но увеличение ферментов печени обычно обратимо с изменением дозы или прерыванием терапии. Во время постмаркетингового наблюдения сообщалось о несерьезных и серьезных случаях гепатотоксичности, вызванной лекарственными средствами, включая тяжелые повреждения печени с летальным исходом. Пациенты с низкой массой тела (весом менее 65 кг), азиатские пациенты и женщины могут иметь повышенный риск повышения уровня ферментов печени. Так как воздействие nintedanib увеличивается с возрастом пациента, пожилые пациенты могут также иметь более высокий риск увеличения ферментов печени. Проверяйте функциональные тесты печени (LFTS) и концентрации билирубина перед началом лечения, через регулярные промежутки времени в течение первых 3 месяцев и периодически после этого, а также в соответствии с клиническими показаниями. Модификация дозировки или прерывание терапии nintedanib могут быть необходимы для повышения ферментов печени. Если серьезное повреждение печени с клиническими симптомами и/или гипербилирубинемия или желтуха происходит во время терапии nintedanib, немедленно прервите терапию.
Острый инфаркт миокарда, ишемическая болезнь сердца, инфаркт миокарда, инсульт
Серьезные артериальные события, в том числе инфаркт миокарда (ИМ), были зарегистрированы с использованием nintedanib. Nintedanib следует использовать с осторожностью у пациентов с повышенным сердечно-сосудистым риском, в том числе известных заболеваний коронарной артерии или ишемии. Поощряйте пациентов, получающих nintedanib, немедленно обратиться за медицинской помощью, если они испытывают симптомы, предполагающие сердечный приступ (например, боль в груди или давление, боль в руках, спине, шее или челюсти или одышка) или симптомы инсульта (например, онемение или слабость на одной стороне тела, проблемы с речью или сильная головная боль). Рассмотрим прерывание лечения у пациентов, у которых развиваются признаки или симптомы острого инфаркта миокарда, инсульта или других серьезных артериальных явлений.
Кортикостероидная терапия, диарея, дивертикулит, перфорация желудочно-кишечного тракта, операция, рвота
Желудочно-кишечные (GI) события, такие как диарея и тошнота/рвота, являются общими для терапии nintedanib и могут потребовать поддерживающих мер для контроля. Лечить диарею при первых признаках адекватным увлажнением и антидиарейными препаратами (например, лоперамидом), используйте поддерживающую помощь при тошноте/рвоте, включая противорвотное лечение. Рассмотрим прерывание лечения, если диарея или рвота продолжаются, несмотря на меры поддержки, до разрешения, после которого нинтеданиб может быть возобновлен при полной или уменьшенной дозировке с последующим титрованием. Если тяжелые симптомы сохраняются, рассмотрите возможность постоянного прекращения лечения. Нинтеданиб может увеличивать риск перфорации желудочно-кишечного тракта, основываясь на его механизме действия в качестве ингибитора VEGFR. Используйте Nintedanib у пациентов с известным риском перфорации желудочно-кишечного тракта, только если преимущества терапии перевешивают риски. Соблюдайте осторожность при лечении пациентов, которые недавно перенесли операцию на брюшной полости, ранее имели дивертикулярную болезнь (дивертикулит) в анамнезе или которые получают сопутствующую терапию кортикостероидами или НПВП. В клинических испытаниях перфорация желудочно-кишечного тракта чаще наблюдалась у пациентов, получавших нинтеданиб, по сравнению с плацебо (0,3% против 0%). Во время постмаркетингового наблюдения были зарегистрированы случаи перфорации желудочно-кишечного тракта, некоторые из которых закончились смертельным исходом. Типичная картина может включать боль в животе, связанную с такими симптомами, как запор, лихорадка, тошнота и рвота. Терапия нинтеданибом должна быть окончательно прекращена у пациентов с перфорацией желудочно-кишечного тракта.
Антикоагулянтная терапия, кровотечение
Нинтеданиб может увеличивать риск кровотечения, основываясь на его механизме действия в качестве ингибитора VEGFR. В клинических испытаниях случаи кровотечения чаще возникали у пациентов, получавших нинтеданиб, по сравнению с плацебо (10% против 7%). Внимательно следить за пациентами, получающими антикоагулянтную терапию на предмет кровотечений, и при необходимости корректировать антикоагулянтное лечение. Используйте Nintedanib у пациентов с известным риском кровотечения, только если преимущества терапии перевешивают риски.
Курение табака
Курение табака было связано со снижением воздействия нинтеданиба, что может снизить эффективность лечения. Пациентам следует рекомендовать бросить курить до начала лечения nintedanib и избегать курения во время терапии.
Требования к контрацепции, бесплодие, тестирование на беременность, репродуктивный риск
Консультирование пациентов о репродуктивном риске и требованиях к контрацепции во время лечения нинтеданибом. Nintedanib может быть тератогенным, если принимать его во время беременности. Женщинам следует избегать беременности и использовать эффективную контрацепцию в течение и как минимум 3 месяца после последней дозы нинтеданиба. Женщины репродуктивного потенциала должны пройти тестирование на беременность до начала приема нинтеданиба. Женщины, которые забеременели во время приема нинтеданиба, должны быть проинформированы о потенциальной опасности для плода. Фертильность самок у крыс была снижена, что привело к возможному бесплодию при воздействии нинтеданиба, примерно в 3 раза превышающего MRHD на основе AUC, включая повышенную резорбцию, потерю после имплантации и снижение индекса беременности; увеличение числа женщин только с резорбцией наблюдалось при воздействиях, приблизительно равных MHRD. Количество и размер желтоватого тела в яичниках наблюдали в исследованиях хронической токсичности как на крысах, так и на мышах. Нинтеданиб не влиял на мужскую фертильность у крыс и подвергался воздействию, приблизительно в 3 раза превышающему MRHD на основе AUC.
Сроки и условия хранения
Хранение обуславливается использованием оригинального продукта в собственной упаковке. Температурный режим не более +25 градусов.
Цены на Варгатеф в Москве

Заберите заказ в в аптеке
WER (г. Москва)
Цена: от 74 000 руб.
