Содержание
-
Структурная формула
-
Русское название
-
Английское название
-
Латинское название
-
Химическое название
-
Брутто формула
-
Фармакологическая группа вещества Винорелбин
-
Нозологическая классификация
-
Код CAS
-
Фармакологическое действие
-
Характеристика
-
Фармакология
-
Применение вещества Винорелбин
-
Противопоказания
-
Применение при беременности и кормлении грудью
-
Побочные действия вещества Винорелбин
-
Взаимодействие
-
Передозировка
-
Способ применения и дозы
-
Меры предосторожности
-
Источники информации
-
Торговые названия с действующим веществом Винорелбин
Структурная формула
Русское название
Винорелбин
Английское название
Vinorelbine
Латинское название
Vinorelbinum (род. Vinorelbini)
Химическое название
3′,4′-Дидегидро-4′-дезокси-8′-норвинкалейкобластин (в виде тартрата 1:2)
Брутто формула
C45H54N4O8
Фармакологическая группа вещества Винорелбин
Нозологическая классификация
Код CAS
71486-22-1
Фармакологическое действие
—
противоопухолевое, цитостатическое.
Характеристика
Винорелбина тартрат представляет собой некристаллический (аморфный) порошок от белого до светло-желтого или светло-коричневого цвета, легко растворим в воде (растворимость в дистиллированной воде составляет >1000 мг/мл), хорошо растворим в метаноле и практически не растворим в гексане. Молекулярная масса 1079,12.
Фармакология
Механизм действия
Полусинтетический алкалоид барвинка, который препятствует сборке микротрубочек. Алкалоиды барвинка представляют собой структурно сходные соединения, состоящие из двух полициклических фрагментов, виндолина и катарантина. В отличие от других алкалоидов барвинка, в винорелбине модифицирован катарантиновый фрагмент. Считается, что противоопухолевая активность винорелбина обусловлена главным образом ингибированием митоза в метафазе посредством его взаимодействия с тубулином.
Винорелбин также может влиять на метаболизм аминокислот, цАМФ и глутатиона, активность кальмодулинзависимой Ca2+-транспортной АТФазы, клеточное дыхание и биосинтез нуклеиновых кислот и липидов.
Винорелбин ингибирует образование митотических микротрубочек в тектальных пластинах интактных эмбрионов мыши в концентрации 2 мкмоль, индуцируя блокаду клеток в метафазе, но вызывает деполимеризацию аксональных микротрубочек в концентрации 40 мкМ, что предполагает его умеренную избирательность в отношении митотических микротрубочек.
Фармакокинетика
Парентеральное введение
Фармакокинетические параметры винорелбина в виде раствора для инъекций оценивали у 49 пациентов, получавших его в дозе 30 мг/м2 в виде инфузии продолжительностью 15–20 мин. Концентрация винорелбина в плазме крови снижается трехфазным образом.
Распределение
Значения Vss варьируют от 25,4 до 40,1 л/кг. Винорелбин продемонстрировал высокое связывание с тромбоцитами и лимфоцитами человека. Свободная фракция составляла приблизительно 0,11 в плазме крови человека в диапазоне концентраций от 234 до 1169 нг/мл. Связывание с компонентами плазмы крови у онкологических больных варьировало от 79,6 до 91,2%. Связывание винорелбина не изменялось в присутствии цисплатина, фторурацила или доксорубицина.
Элиминация
T1/2 в терминальной фазе составляет в среднем от 27,7 до 43,6 ч, а средний плазменный клиренс колеблется от 0,97 до 1,26 л/ч/кг.
Метаболизм
Винорелбин подвергается значительной печеночной элиминации у человека, при этом большое количество его выводится с калом. В крови, плазме и моче человека были обнаружены два метаболита винорелбина: N-оксид винорелбина и деацетилвинорелбин. Было показано, что деацетилвинорелбин является основным метаболитом винорелбина в организме человека и обладает противоопухолевой активностью, аналогичной винорелбину. Терапевтические дозы винорелбина (30 мг/м2) дают очень небольшие, поддающиеся количественному определению уровни обоих метаболитов в крови или моче. Метаболизм винорелбина опосредован печеночным CYP3A.
Выведение
После в/в введения радиоактивно меченного винорелбина примерно 18 и 46% введенной радиоактивности выводилось с мочой и калом соответственно. В другом исследовании (10,9±0,7)% в/в дозы 30 мг/м2 выводилось с мочой в виде неизмененного винорелбина.
Особые группы пациентов
Возраст не влияет на фармакокинетику (клиренс, Vss и T1/2) винорелбина.
Пероральное введение
После перорального приема винорелбин быстро всасывается, Tmax составляет 1,5–3 ч, а Cmax в крови, приблизительно равна 130 нг/мл, после приема в дозе 80 мг/м2. Абсолютная биодоступность составляет около 40%, одновременный прием пищи с низким содержанием жира не изменяет AUC. Влияние жирной пищи на абсорбцию не изучалось.
При пероральном приеме винорелбина в дозах 60 и 80 мг/м2 величина AUC сопоставима с таковой при в/в введении в дозах от 25 и 30 мг/м2 соответственно. Межиндивидуальная вариабельность AUC сходна после в/в введения и перорального приема. Наблюдается пропорциональное увеличение AUC от дозы. Средние фармакокинетические параметры оценивали в крови. После в/в введения конечный T1/2 составляет в среднем 38 ч. Клиренс очищения плазмы крови был высоким, приближался к скорости печеночного кровотока и составлял в среднем 0,72 л/ч/кг (диапазон 0,32–1,26 л/ч/кг), а Vss — в среднем 21,2 л/кг (диапазон 7,5–39,7 л/кг) и указывал на обширное распределение в тканях.
Винорелбин интенсивно связывается с клетками крови и особенно тромбоцитами (70–80%), менее интенсивно (около 15%) — с белками плазмы крови. Наблюдается значительное накопление винорелбина в легких, что подтверждается результатами легочной хирургической биопсии, показывающей концентрацию, в 300 раз превышающую таковую в сыворотке крови. Винорелбин не обнаружен в ЦНС.
Винорелбин в основном метаболизируется с участием изофермента CYP3A4. Все метаболиты были идентифицированы, и ни один из них не является активным, за исключением 4-O-деацетилвинорелбина, который является основным метаболитом в крови. Сульфо- или глюкуроновые конъюгаты не определяются. Почечная элиминация низкая (<20% от дозы) и происходит в основном в виде неизмененного винорелбина. Билиарная экскреция является преобладающим путем выведения как метаболитов, так и неизмененного винорелбина. Влияние нарушения функции почек на выведение винорелбина не оценивалось, однако снижение дозы винорелбина при почечной недостаточности не требуется из-за его низкой почечной элиминации.
Винорелбин выводится из кровотока в основном печенью, поэтому у пациентов с печеночной недостаточностью можно ожидать повышения концентрации винорелбина в крови. В фармакокинетическом исследовании I фазы 6 пациентов с тяжелой печеночной недостаточностью получали винорелбин в/в в дозе 20 мг/м2. Плазменная концентрация у них была выше, чем у пациентов с нормальной функцией печени. Винорелбин противопоказан пациентам с тяжелой печеночной недостаточностью. Опыт применения винорелбина у пациентов с легкой или умеренной печеночной недостаточностью ограничен, однако имеющиеся данные свидетельствуют о том, что коррекция дозы не требуется. Следует тщательно контролировать гематологическую токсичность.
Была продемонстрирована сильная связь между AUC и снижением количества лейкоцитов или полиморфонуклеарных нейтрофилов.
Мутагенность, канцерогенность, влияние на фертильность
Винорелбин влияет на количество и, возможно, структуру хромосом in vivo (полиплоидия в клетках костного мозга китайских хомячков и положительный микроядерный тест у мышей). Винорелбин не продемонстрировал признаков мутагенности или цитотоксичности в тесте обратной гистидиновой мутации (тест Эймса), но показал мутагенный потенциал в тесте прямой мутации (локус тимидинкиназы) на мышах.
Исследования канцерогенности на мышах и крысах не выявили онкогенной активности при дозах до 2,4 мг/м2, вводимых в/в каждые 2 нед в течение 18 мес или 2 лет соответственно. Однако положительные результаты анализов на генотоксичность позволяют предположить, что винорелбин может обладать канцерогенным потенциалом при более высоких дозах, применяемых у человека.
Винорелбин не влиял на фертильность в статистически значимой степени при введении самцам и самкам крыс до и во время спаривания, однако дозы, применявшиеся в этом исследовании (9 мг/м2 1 раз в неделю или до 4,2 мг/м2 с 3-дневным интервалом) были ниже, чем применяющиеся у человека.
Неблагоприятное воздействие на мужскую репродуктивную систему наблюдалось в исследованиях токсичности с введением многократных доз у животных, включая снижение сперматогенеза у крыс, получавших дозу 2,1–7,2 мг/м2 2 раза в неделю в течение 13 нед, снижение секреции предстательной железы/семенных пузырьков у крыс, получавших дозу 3 мг/м2 2 раза в неделю в течение 26 нед, снижение массы яичек у мышей, получавших дозу 19 мг/м2/сут в течение 3- и 5-дневных циклов, и снижение массы придатков яичек у собак, получавших дозу 5 мг/м2 в течение 26 нед.
Клинические исследования
Парентеральное введение
Немелкоклеточный рак легкого (НМРЛ)
Монотерапия. Активность винорелбина оценивали в серии исследований II фазы. Общая частота ответов на однократное введение винорелбина у пациентов с НМРЛ варьировала от 8 до 33% у пациентов, ранее не получавших лечение. В двух крупных исследованиях II фазы с участием более 60 пациентов, поддающихся оценке, общая частота ответа составила более 30% у пациентов, не получавших химиотерапию. Высокая активность винорелбина, применяемого в качестве монотерапии при НМРЛ, отмеченная в неконтролируемых исследованиях II фазы, была также подтверждена в трех рандомизированных исследованиях III фазы.
Безопасность и эффективность применения винорелбина оценивали также в одном рандомизированном мультицентровом открытом клиническом исследовании. В этом исследовании сравнивали применение винорелбина и комбинации фторурацил + кальция фолинат у пациентов с IV стадией НМРЛ, ранее не получавших химиотерапию. Всего 211 пациентов были рандомизированы в соотношении 2:1 для получения винорелбина в дозе 30 мг/м2/нед в течение 8-недельного цикла (n=143) или фторурацила в дозе 425 мг/м2 в/в болюсно в комбинации с кальция фолинатом в дозе 20 мг/м2 в/в болюсно ежедневно в течение 5 дней 4-недельного цикла (n=68).
Демографические показатели пациентов и характеристики заболевания в целом были схожи между группами. В общей популяции средний возраст составил 61 год (диапазон 32–83), 74% — составляли мужчины, 88% — представители европеоидной расы, 46% пациентов имели гистологию аденокарциномы. В группе получавших винорелбин 50% пациентов имели значение общего состояния по шкале Карновского ≥90 по сравнению с 38% получавших комбинацию фторурацила и кальция фолината.
Первичным показателем эффективности исследования была общая выживаемость. Медиана выживаемости пациентов, получавших винорелбин, составила 30 нед по сравнению с 22 нед у пациентов, получавших 5-фторурацил и кальция фолинат (p=0,06). Частичный объективный ответ наблюдался у 11,1% (95% ДИ: 6,2; 17,9%) пациентов, получавших винорелбин, и 3,5% (95% ДИ: 0,4; 11,9%) пациентов, получавших фторурацил и кальция фолинат.
Комбинация с цисплатином. Безопасность и эффективность применения винорелбина в комбинации с цисплатином оценивали в двух рандомизированных многоцентровых исследованиях III фазы с участием 782 пациентов. В двух группах лечения сравнивали действие винорелбина в виде монотерапии и комбинации винорелбин + цисплатин. Общая частота ответа на лечение винорелбином в качестве монотерапии составила 16%, а на комбинацию винорелбин + цисплатин — 43%. Медиана выживаемости пациентов, получавших винорелбин в качестве монотерапии, была аналогична таковой при применении винорелбина в комбинации с цисплатином.
Цисплатин в дозе 100 мг/м2. В рандомизированном многоцентровом открытом исследовании 1 оценивали применение винорелбина в комбинации с цисплатином и цисплатина в качестве монотерапии при лечении НМРЛ IV или IIIB стадии у пациентов со злокачественным плевральным выпотом или множественными поражениями более чем одной доли ипсилатерального легкого, не получавших ранее химиотерапию. В общей сложности 432 пациента были рандомизированы в соотношении 1:1 для получения либо винорелбина в дозе 25 мг/м2 в 1-й день, затем каждую неделю каждого 28-дневного цикла в комбинации с введением цисплатина в дозе 100 мг/м2 в 1-й день каждого 28-дневного цикла (n=214), либо монотерапии цисплатином в дозе 100 мг/м2 в 1-й день каждого 28-дневного цикла (n=218).
Демографические данные пациентов и характеристики заболевания были сходными в разных группах. Средний возраст всех участников исследования составил 64 года (диапазон 33–84), 66% составляли мужчины, 80% — представители европеоидной расы, 92% пациентов имели IV стадию заболевания и 8% — IIIB стадию, у 53% пациентов была аденокарцинома, у 21% — плоскоклеточный рак, у 14% — крупноклеточная гистология. Основным показателем эффективности являлась общая выживаемость. Результаты изучения эффективности представлены в таблице 1.
Таблица 1
Показатели эффективности (исследование 1)
| Показатель | Винорелбин + цисплатин (n=214) | Цисплатин (n=218) |
| Общая выживаемость | ||
| Медиана выживаемости (95% ДИ), мес | 7,8 (6,9; 9,6) | 6,2 (5,4; 7,7) |
| Нестратифицированное логранговое значение p | 0,01 | − |
| Частота общего ответа | ||
| Поддающиеся оценке пациенты | n=206 | n=209 |
| Частота общего ответа (95% ДИ), % | 19 (14; 25) | 8 (5; 13%) |
| Значение p согласно хи-квадрат-критерию | <0,001 | − |
Цисплатин в дозе 120 мг/м2. Исследование 2, проведенное в Европе, представляло собой рандомизированное открытое многоцентровое исследование с 3 группами пациентов, получавшими комбинации винорелбин + цисплатин, виндезин + цисплатин и винорелбин в качестве монотерапии для лечения НМРЛ III или IV стадии и ранее не получавшими химиотерапию. В общей сложности 612 пациентов были рандомизированы в соотношении 1:1:1 для получения винорелбина в дозе 30 мг/м2/нед в течение 6-недельного цикла в комбинации с цисплатином в дозе 120 мг/м2 в 1-й и 29-й день, затем каждые 6 нед (n=206), виндезина в дозе 3 мг/м2 в течение 6 нед, затем каждые 2 нед в комбинации с цисплатином в дозе 120 мг/м2 в 1-й и 29-й день, затем каждые 6 нед (n=200) или винорелбина в качестве монотерапии в дозе 30 мг/м2/нед в течение 6-недельного цикл (n=206). Основным показателем эффективности было сравнение общей выживаемости между комбинациями винорелбин + цисплатин и виндезин + цисплатин. Другим показателем эффективности было сравнение общей выживаемости при лучшем из двух комбинированных режимов с таковой при применении винорелбина в качестве монотерапии.
Демографические данные пациентов были в целом сходными между группами: средний возраст всех участников исследования составлял 60 лет (от 30 до 75 лет), 90% — составляли мужчины, 78% имели показатель общего состояния по шкале ВОЗ 0 или 1. Характеристики опухоли были в целом сходными, за исключением гистологического подтипа НМРЛ. Аденокарцинома являлась гистологическим подтипом у 32% пациентов в группе получавших винорелбин + цисплатином, у 40% пациентов в группе получавших виндезин + цисплатином и у 28% пациентов в группе монотерапии винорелбином. Стадию заболевания IIIA имели 10% пациентов, 28% имели стадию IIIB и 50% — стадию IV. 12% пациентов ранее подвергались хирургическому вмешательству или получали лучевую терапию.
Результаты изучения эффективности представлены в таблице 2.
Таблица 2
Показатели эффективности (исследование 2)
| Показатель | Винорелбин (n=206) | Винорелбин + цисплатин (n=206) | Виндезин + цисплатин (n=206) |
| Общая выживаемость | |||
| Медиана выживаемости (99,5% ДИ), мес | 7,2 (5,4; 9,1) | 9,2 (7,4; 11,1) | 7,4 (6,1; 9,1) |
| Нестратифицированное логранговое значение p | 0,05 | 0,087 | − |
| Частота общего ответа | |||
| Поддающиеся оценке пациенты | n=205 | n=203 | n=198 |
| Частота общего ответа, % (95% ДИ) | 14 (10; 20) | 28 (22; 35) | 19 (14; 25) |
| Значение p согласно хи-квадрат-критерию | <0,001 | 0,03 | − |
Распространенный рак молочной железы — терапия второй линии
Проведено 20 исследований II фазы по изучению монотерапии винорелбином для в/в введения в качестве терапии второй линии или дальнейшего лечения у пациентов с распространенным раком молочной железы. Частота и продолжительность ответа на химиотерапию снижалась по мере того, как пациенты проходили первую, вторую и третью линии химиотерапии. 13 из этих исследований II фазы с участием 494 пациентов были проведены в смешанных популяциях, получавших и не получавших антрациклины, частота общего ответа в этих исследованиях составила 14–45% (средневзвешенное значение 29,2%), а медиана выживаемости — 58–69 нед.
Остальные 7 исследований II фазы проводились с участием 339 пациентов, предварительно получавших антрациклин, частота ответа в этих исследованиях составила 16–64% (средневзвешенное значение 30,9%), а медиана выживаемости — 24–82 нед.
В рандомизированном исследовании III фазы, проведенном с целью изучения эффективности при распространенном раке молочной железы, рефрактерном к антрациклину, 115 пациентов получали винорелбин в/в в качестве монотерапии по сравнению с 64 пациентами, получавшими мелфалан в/в. Средняя доза, количество доз и продолжительность лечения винорелбином составили 27,5 мг/м2, 9 доз и 12 нед соответственно, а мелфаланом — 25 мг/м2, 2 дозы и 8 нед соответственно. Целевого ответа достигли 13 из 84 (15,5%) пациентов, получавших винорелбин, с измеримыми проявлениями заболевания по сравнению с 4 из 46 (8,7%) пациентов, получавших мелфалан. Общая выживаемость составила 35 нед для пациентов, получавших винорелбин, по сравнению с 31 нед для пациентов, получавших мелфалан (логранговое значение p=0,023). Ни один из методов лечения не оказывал негативного влияния на качество жизни.
Применение винорелбина для в/в введения также оценивали в комбинации с другими ЛС в качестве терапии второй линии распространенного рака молочной железы. Обобщенные результаты исследований приведены в таблице 3.
Таблица 3
Обобщенные результаты исследований эффективности винорелбина для в/в введения в комбинации с другими ЛС для терапии второй линии у пациентов с распространенным раком молочной железы
| ЛС | Количество исследований | Общее число пациентов | Частота общего ответа, % |
| Митоксантрон | 2 | 60 | 50 |
| 5-фторурацил | 5 | 221 | 26–66 |
| Митомицин C | 11 | 485 | 32–57 |
| Карбоплатин | 1 | 41 | 41 |
| Цисплатин | 1 | 53 | 49 |
| Ифосфамид | 2 | 62 | 28–36 |
| Паклитаксел | 3 | 81 | 32–61 |
| Доцетаксел | 3 | 109 | 37–59 |
| Капецитабин | 1 | 25 | 52 |
| Гемцитабин | 8 | 301 | 22–54 |
| Липосомальный доксорубицин | 1 | 33 | 36 |
Пероральное введение
Винорелбин для перорального применения был разработан для расширения линейки лекарственных форм. Поэтому основной целью клинической программы было продемонстрировать биоэквивалентность лекарственных форм для перорального приема и в/в введения на основе фармакокинетических исследований. Было показано, что пероральная доза винорелбина 80 мг/м2 соответствует в/в дозе 30 мг/м2, а пероральная доза 60 мг/м2 — в/в дозе 25 мг/м2. Последующие исследования II фазы были проведены для изучения эффективности и переносимости винорелбина для перорального приема.
НМРЛ
Было проведено рандомизированное исследование II фазы (97 CA 205) с рекомендованным режимом перорального приема, в котором сравнивалси винорелбин для перорального приема и в/в введения у пациентов с распространенным или метастатическим НМРЛ, ранее не получавших цитотоксическую химиотерапию. Результаты обобщены в таблице 4.
Таблица 4
Обобщенные результаты эффективности, полученные в рандомизированном исследовании II фазы у пациентов с НМРЛ (97 CA 205)
| Показатель | Пероральное применение | В/в введение |
| Количество пациентов | 77 | 38 |
| Частота ответов (все рандомизированные пациенты, получившие не менее одной дозы), % | 11,7 | 10,5 |
| Частота ответов (оцениваемая популяция), % | 14,1 | 11,8 |
| Медиана продолжительности ответа, мес | 7,7 | 5,5 |
| Медиана выживаемости без прогрессирования заболевания, мес | 3,3 | 2,1 |
| Медиана выживаемости, мес | 9,4 | 7,9 |
В многоцентровом исследовании II фазы с участием 56 пациентов, получавших комбинацию цисплатина в дозе 100 мг/м2 (1-й день каждые 4 нед) с еженедельным применением винорелбина (в/в доза винорелбина 25 мг/м2 в 1-й день, пероральная доза винорелбина 60 мг/м2 в 8-й, 15-й и 22-й дни), была получена частота ответов 30% для всех зарегистрированных пациентов и 33% — для поддающихся оценке пациентов в терапии первой линии нерезектабельного, локализованного или метастатического НМРЛ. Медиана общей выживаемости и выживаемости без прогрессирования заболевания составила 8,9 и 5,5 мес соответственно.
Распространенный рак молочной железы
Монотерапия. Проведены два несравнительных многоцентровых исследования II фазы (96 CA 201 и 97 CA 206) терапии первой линии при распространенном раке молочной железы, в которых оценивали монотерапию винорелбином для перорального приема в дозе 60 мг/м2/нед в течение первых 3 нед, а затем увеличенной до 80 мг/м2. В общей сложности в исследование было включено 184 пациента.
На момент включения в исследования большинство пациентов имели метастатическое заболевание, висцеральные очаговые поражения и ранее получали гормонотерапию. Доля пациентов, ранее получавших неоадъювантную химиотерапию, составляла 49,2% (96 CA 201) и 26,5% (97 CA 206). Ни одна пациентка не получала химиотерапию по поводу прогрессирующего/метастатического заболевания.
Результаты изучения эффективности обобщены в таблице 5.
Таблица 5
Обобщенные результаты эффективности монотерапии винорелбином для перорального приема при распространенном раке молочной железы (исследования 96 CA 201 и 97 CA 206)
| Показатель | 96 CA 201 | 97 CA 206 |
| Количество пациентов | ||
| Получившие лечение | 120 | 64 |
| Поддающиеся оценке | 108 | 58 |
| Частота ответов | ||
| Популяция рандомизированных пациентов, получивших не менее одной дозы, % (95% ДИ) | 20,8 (14–29) | 29,7 (18–41) |
| Поддающиеся оценке пациенты, % (95% ДИ) | 23,2 16–32) | 31 (19–43) |
| Медиана выживаемости без прогрессирования заболевания (популяция рандомизированных пациентов, получивших не менее одной дозы), мес | 4,6 | 4,2 |
| Медиана выживаемости (популяция рандомизированных пациентов, получивших не менее одной дозы), мес | 19,3 | 23,9 |
Частота ответа составила 30% в исследовании 97 CA 206 и 21% в исследовании 96 CA 201. Более низкая частота ответа, наблюдаемая в последнем исследовании, может быть объяснена очень плохим прогнозом у пациентов, ранее не получавших адъювантную химиотерапию: 57% пациентов имели IIIB–IV стадию заболевания, 67% имели период без признаков заболевания менее 2 лет, а 62% имели поражения не менее 3 органов. В этой подгруппе пациентов частота ответов составила всего 14%.
Медиана выживаемости без прогрессирования заболевания и общей выживаемости были сходны в обоих исследованиях: 4,6 и 4,2 мес соответственно и 19,3 и 23,9 мес соответственно.
В рандомизированном исследовании II фазы (CA 221) параллельно оценивали эффективность и безопасность винорелбина для перорального приема в дозе 60 мг/м2 в 1-й и 8-й дни каждые 3 нед в течение 1-го цикла, затем увеличенной до 80 мг/м2 в 1-й и 8-й дни каждые 3 нед в последующих циклах, и винорелбина для в/в введения в дозе 25 мг/м2 в 1-й и 8-й дни каждые 3 нед в течение 1-го цикла, затем увеличенной до 30 мг/м2 в 1-й и 8-й дни каждые 3 нед в последующих циклах. Исследование было закрыто через 2,5 года после его начала из-за низкого включения в исследование (85 пациентов из 230 запланированных). Преждевременное закрытие исследования не позволило точно оценить эффективность винорелбина для перорального приема. Были получены следующие результаты: частота ответов составила 7% и уровень контроля заболевания — 47,4% в группе винорелбина для перорального приема и 22 и 51,9% соответственно в группе винорелбина для в/в введения. Медиана общей выживаемости была сходна в обеих группах исследования — 9,4 и 10,2 мес соответственно.
Винорелбин в комбинации с другими ЛС. Было проведено рандомизированное исследование фазы II (CA 222) с участием 139 пациентов с метастатическим раком молочной железы, ранее получавших терапию антрациклинами, в котором сравнивали применение комбинации винорелбина для перорального приема и капецитабина с последовательной схемой перорального приема винорелбина и капецитабина и комбинацией доцетаксел + капецитабин.
В комбинации с капецитабином винорелбин для перорального приема назначался в 1-й и 8-й дни 3-недельных циклов в дозе 60 мг/м2 в течение 1-го цикла, а затем в дозе 80 мг/м2. В последовательной схеме приема, пациенты получали винорелбин перорально в дозе 60 мг/м2/нед, затем 80 мг/м2/нед в течение трех 3-недельных циклов, а затем капецитамбин в течение 3 циклов. В контрольной группе применяли стандартную схему с приемом доцетаксела в дозе 75 мг/м2 в 1-й день и капецитабина каждые 3 нед. Во всех трех группах лечения доза капецитабина, вводимого с 1-го по 14-й день каждые 3 нед, составляла 2000 мг/м2/сут.
Результаты этого исследования обобщены в таблице 6.
Таблица 6
Обобщенные результаты изучения эффективности в рандомизированном исследовании II фазы CA 222
| Показатель | Винорелбин + капецитабин | Винорелбин с последующим применением капецитабина | Доцетаксел + капецитабин |
| Количество пациентов | |||
| Получившие лечение | 44 | 46 | 48 |
| Поддающихся оценке1 | 41 | 41 | 41 |
| Частота контроля заболевания1 | |||
| Популяция рандомизированных пациентов, получивших не менее одной дозы (95% ДИ), % | 70,5 (54,8–83,2) | 37 (23,2–52,5) | 70,8 (55,9–83) |
| Поддающиеся оценке пациенты (95% ДИ), % | 73,2 (57,1–85,8) | 39 (24,2–55,5) | 80,5 (65,1–91,2) |
| Частота ответов1 | |||
| Популяция рандомизированных пациентов, получивших не менее одной дозы (95% ДИ), % | 31,8 (18,6–47,6) | 8,7 (2,4–20,8) | 35,4 (22,2–50,5) |
| Поддающиеся оценке пациенты (95% ДИ), % | 34,1 (20,1–50,6) | 7,3 (1,5–19,9) | 39 (24,2–55) |
| Медиана выживаемости без прогрессирования заболевания (популяция рандомизированных пациентов, получивших не менее одной дозы)2 (95% ДИ), мес | 7,2 (5,3–8,9) | 3,4 (2,6–5,6) | 8,9 (7,2–12) |
| Медиана времени до констатации отсутствия эффекта терапии (популяция рандомизированных пациентов, получивших не менее одной дозы)2 (95% ДИ), мес | 5,6 (4,2–6,5) | 3 (1,8–4,4) | 4,3 (4–5) |
1 По данным независимой экспертной оценки.
2 По оценке исследователя.
Две комбинированные схемы, винорелбин для перорального приема + капецитабин и доцетаксел + капецитабин, продемонстрировали сходные показатели контроля заболевания (70,5% против 70,8% в популяции рандомизированных пациентов, получивших не менее одной дозы), частоты ответов (31,8% против 35,4%), сходную выживаемость без прогрессирования заболевания (7,2 мес против 8,9 мес) и сходное время до констатации отсутствия эффекта терапии (5,6 мес против 4,3 мес). Для сравнения, последовательная схема приема перорального винорелбина с последующим применением капецитабина уступала комбинированным схемам по всем рассматриваемым параметрам эффективности.
Применение винорелбина для перорального приема в комбинации с другими цитотоксическими ЛС оценивали в трех исследованиях I/II фазы: с эпирубицином (исследование CA 205), доцетакселом (CA 101) и паклитакселом (CA 102).
Результаты этих исследований приведены в таблице 7.
Таблица 7
Обобщенные результаты эффективности в популяции рандомизированных пациентов, получивших не менее одной дозы в исследованиях CA 205, CA 101 и CA 102
| Показатель | Исследование CA 205 (винорелбин в/в/перорально + эпирубицин) | Исследование CA 101 (винорелбин в/в/перорально + доцетаксел) | Исследование CA 102 (винорелбин перорально + паклитаксел) |
| Количество пациентов | 49 | 49 | 48 |
| Полный ответ | 2 | 1 | – |
| Частота ответа (95% ДИ), % | 51 (36,3–65,6) | 49 (34,4–63,7) | 33,3 (20,4–48,4) |
| Частота контроля заболевания (95% ДИ), % | 86 (76–96) | 82 (71–93) | 69 (55–82) |
| Медиана продолжительности ответа (95% ДИ), мес | 7,7 (6,9–12,1) | 9,4 (5,1–12,4) | Не рассчитано1 |
| Медиана выживаемости без прогрессирования заболевания (95% ДИ), мес | 8,1 (6,9–9,8) | 5,5 (4,2–7,2) | 5 (4,2–7,4) |
| Медиана выживаемости (95% ДИ), мес | 19,9 (15,3–25,3) | 33,1 (21,1–53) | 28 (22,4– не достигнуто] |
1 Не рассчитано из-за слишком большого количества выбывших из исследования пациентов.
Две схемы с чередованием перорального приема и в/в введения винорелбина в комбинации с эпирубицином или доцетакселом давали примерно 50% ответов. Медиана продолжительности общей выживаемости, как правило, была выше для комбинаций таксанов, чем для комбинации с эпирубицином.
Применение вещества Винорелбин
Парентеральное введение
В комбинации с цисплатином для терапии первой линии пациентов с местнораспространенным или метастатическим немелкоклеточным раком легкого; в качестве монотерапии для лечения пациентов с метастатическим немелкоклеточным раком легкого.
Пероральное введение
В качестве монотерапии или в комбинации с другими ЛС для терапии первой линии распространенного немелкоклеточного рака легкого; в качестве монотерапии или в комбинации с другими ЛС для лечения прогрессирующего рака молочной железы после неэффективности стандартной терапии.
Противопоказания
Повышенная чувствительность к винорелбину или другим алкалоидам барвинка; заболевания, существенно влияющие на всасывание; ранее проведенная значительная хирургическая резекция желудка или тонкой кишки; количество нейтрофилов <1500 клеток/мм3 или текущая или недавняя тяжелая инфекция вследствие нейтропении (в течение 2 нед); пациенты, нуждающиеся в длительной кислородотерапии; тяжелая печеночная недостаточность; беременность; кормление грудью.
Применение при беременности и кормлении грудью
Категория действия на плод по FDA — D.
Исследования с участием беременных женщин не проводились. Винорелбин может оказывать негативное влияние на плод при назначении беременной женщине. Имеющиеся данные о применении у человека недостаточны для того, чтобы определить связанный с введением винорелбина риск основных врожденных пороков развития, выкидыша или неблагоприятных исходов для матери или плода. Имеющиеся данные исследваний на животных указывают на возможность его тератогенного действия у человека. Следует информировать беременных женщин о потенциальном риске для плода.
Женщинам с сохраненным репродуктивным потенциалом следует рекомендовать избегать наступления беременности во время терапии винорелбином.
Нет данных о проникновении винорелбина в молоко женщины, его воздействии на новорожденных, находящихся на грудном вскармливании, или на выработку молока. В связи с возможностью развития серьезных побочных реакций, вызванных винорелбином у младенцев, находящихся на грудном вскармливании, женщинам, получающим винорелбин, рекомендуется отказаться от грудного вскармливания во время терапии и в течение 9 дней после введения последней дозы винорелбина.
Побочные действия вещества Винорелбин
Поскольку клинические исследования проводятся с разным дизайном и при участии различных популяций пациентов, частоту побочных реакций, зарегистрированную в одном клиническом исследовании, не следует сопоставлять с частотой, полученной в другом клиническом исследовании, и она может не отражать частоту, фактически наблюдаемую в клинической практике.
Опыт клинических исследований
Парентеральное введение
Монотерапия
Ниже приведены данные, полученные от 365 участников 3 контролируемых исследований лечения метастатического НМРЛ и распространенного рака молочной железы с применением винорелбина для в/в введения в виде монтерапии в дозе 30 мг/м2/нед. В популяцию вошли 143 пациента с ранее нелеченым метастатическим НМРЛ (исследование 3), которые получили в среднем 8 доз винорелбина. Возраст пациентов составлял от 32 до 79 лет (медиана 61 год), 71% — составляли мужчины, 91% — представители европеоидной расы, 48% пациентов имели гистологию аденокарциномы. Данные также отражают воздействие винорелбина на 222 пациентов с ранее леченым распространенным раком молочной железы, которые получили в среднем 10 доз винорелбина. Винорелбин для в/в введения не показан для лечения рака молочной железы.
Отдельные побочные реакции, о которых сообщалось в ходе данных исследований, представлены в таблицах 8 и 9. Наиболее частыми побочными реакциями (≥20%) при применении винорелбина в качестве монотерапии были лейкопения, нейтропения, анемия, повышение уровня АСТ, тошнота, рвота, запор, астения, реакция в месте введения (инъекции) и периферическая нейропатия. Наиболее частыми (≥5%) побочными реакциями 3-й или 4-й степени были нейтропения, лейкопения, анемия, повышение уровня общего билирубина, повышение уровня АСТ, реакция в месте введения (инъекции) и астения.
Приблизительно у 49% пациентов с НМРЛ, получавших винорелбин, снижение дозы производилось по крайней мере 1 раз из-за возникновения побочных реакций.
Терапию винорелбином для в/в введения из-за возникновения нежелательных реакций прекратили у 13% пациентов. Наиболее частыми нежелательными реакциями, приводившими к прекращению терапии винорелбином, были астения, одышка, тошнота, запор, анорексия, миастения и лихорадка.
Таблица 8
Гематологические побочные реакции, наблюдавшиеся у >5% пациентов, получавших винорелбин в/в1,2
| Побочная реакция | Все пациенты (n=365), % | Пациенты с НМРЛ (n=143), % | |
| Нейтропения | <2000 клеток/мм3 | 90 | 80 |
| <500 клеток/мм3 | 36 | 29 | |
| Лейкопения | <4000 клеток/мм3 | 92 | 81 |
| <1000 клеток/мм3 | 15 | 12 | |
| Тромбоцитопения | <100000 клеток/мм3 | 5 | 4 |
| Анемия | <11 г/дл | 83 | 77 |
| <8 г/дл | 9 | 1 | |
| Госпитализации по поводу осложнений, вызванных нейтропенией | 9 | 8 |
1 Оценка по модифицированным критериям Национального института рака, версия 1.
2 Пациенты с НМРЛ, ранее не получавшие химиотерапию. Большинство остальных пациентов ранее получали химиотерапию.
Таблица 9
Негематологические побочные реакции, наблюдавшиеся у ≥5% пациентов, получавших винорелбин в/в1,2
| Побочная реакция | Любая степень тяжести | Степень тяжести 3–4 | ||
| Все пациенты, % | Пациенты с НМРЛ, % | Все пациенты , % | Пациенты с НМРЛ, % | |
| Лабораторные данные (со стороны печени) | ||||
| Повышение уровня АСТ (n=346) | 67 | 54 | 6 | 3 |
| Повышение уровня билирубина (n=351) | 13 | 9 | 7 | 5 |
| Клинические данные | ||||
| Тошнота | 44 | 34 | 2 | 1 |
| Астения | 36 | 27 | 7 | 5 |
| Запор | 35 | 29 | 3 | 2 |
| Реакция в месте введения (инъекции) | 28 | 38 | 2 | 5 |
| Боль в месте введения (инъекции) | 16 | 13 | 2 | 1 |
| Периферическая невропатия3 | 25 | 20 | <2 | 1 |
| Рвота | 20 | 15 | 2 | 1 |
| Диарея | 17 | 13 | 1 | 1 |
| Алопеция | 12 | 12 | <1 | 1 |
| Флебит | 7 | 10 | <1 | 1 |
| Одышка | 7 | 3 | 3 | 2 |
1 Оценка по модифицированным критериям Национального института рака, версия 1.
2 Пациенты с НМРЛ, ранее не получавшие химиотерапию. Большинство остальных пациентов ранее получали химиотерапию.
3 Случаи парестезии и гипестезии.
Миелосупрессия. В клинических исследованиях нейтропения 3–4-й степени, анемия и тромбоцитопения наблюдались у 69; 9 и 1% пациентов соответственно, получавших винорелбин в качестве монотерапии. Нейтропения является основной дозолимитирующей побочной реакцией.
Нейротоксичность. Нейротоксичность чаще всего проявлялась в виде запора, парестезии, гиперестезии и гипорефлексии. Нейропатия 3-й и 4-й степени наблюдалась у 1% пациентов, получавших винорелбин в качестве монотерапии.
Реакции в месте введения (инъекции). Реакции в месте введения (инъекции), включая эритему, боль в месте введения (инъекции) и изменение цвета вен, наблюдались примерно у 1/3 пациентов, у 5% они были тяжелыми. Флебит (химический флебит) по ходу вены проксимальный к месту инъекции был отмечен у 10% пациентов.
Со стороны ССС. Боль в груди возникла у 5% пациентов, инфаркт миокарда развивался у <0,1% пациентов.
Легочная токсичность и дыхательная недостаточность. Одышка (затрудненное дыхание) отмечалась у 3% пациентов, у 2% она была тяжелой. Были зафиксированы интерстициальные изменения в легких.
Прочие. Геморрагический цистит и синдром неадекватной секреции АДГ были зарегистрированы у <1% пациентов.
В комбинации с цисплатином
В таблице 10 приведены данные по частоте развития отдельных побочных реакций, возникавших у ≥10% пациентов, получавших винорелбин в/в, о которых сообщалось в рандомизированном исследовании применения комбинации винорелбина в дозе 25 мг/м2, вводимого каждую нед каждого 28-дневного цикла, и цисплатина в дозе 100 мг/м2, вводимого в 1-й день каждого 28-дневного цикла, по сравнению с применением цисплатина в той же дозе и по той же схеме у пациентов с ранее нелеченым НМРЛ (исследование 1).
Пациенты, рандомизированные на получение винорелбина в комбинации с цисплатином, получили в среднем 3 цикла лечения, а пациенты, рандомизированные на прием цисплатина, получили в среднем 2 цикла лечения. Частота развития нейтропении 3-й и 4-й степени была значительно выше в группе получавших винорелбин + цисплатин (82%) по сравнению с получавшими только цисплатин (5%).
Прекращение лечения из-за развития побочных реакций потребовалось у 35% пациентов, получавших винорелбин + цисплатин, по сравнению с 19% в группе получавших только цисплатин.
Четыре пациента в группе получавших винорелбин и цисплатин умерли от нейтропенического сепсиса. В этой группе было зарегистрировано еще 7 случаев с летальным исходом: 2 — от сердечной ишемии, 1 — вследствие нарушения мозгового кровообращения, 1 — от полиорганной недостаточности вследствие передозировки винорелбина и 3 — от фебрильной нейтропении.
Таблица 10
Побочные реакции, наблюдавшиеся у ≥10% пациентов, получавших винорелбин в комбинации с цисплатином, по сравнению с монотерапией цисплатином1
| Побочная реакция | Винорелбин + цисплатин (n=212), % | Цисплатин (n=210), % | ||
| Любая степень | Степень 3–4 | Любая степень | Степень 3–4 | |
| Лабораторные данные | ||||
| Нейтропения | 89 | 82 | 26 | 5 |
| Анемия | 89 | 24 | 72 | <8 |
| Лейкопения | 88 | 58 | 31 | <1 |
| Тромбоцитопения | 29 | 5 | 21 | <2 |
| Фебрильная нейтропения2 | Не применимо | 11 | Не применимо | 0 |
| Повышение уровня креатинина крови | 37 | 4 | 28 | <5 |
| Клинические данные | ||||
| Недомогание/повышенная утомляемость/ вялость | 67 | 12 | 49 | 8 |
| Рвота | 60 | 13 | 60 | 14 |
| Тошнота | 58 | 14 | 57 | 12 |
| Снижение аппетита | 46 | 0 | 37 | 0 |
| Запор | 35 | 3 | 16 | 1 |
| Алопеция | 34 | 0 | 14 | 0 |
| Снижение массы тела | 34 | 1 | 21 | <1 |
| Лихорадка без инфекции | 20 | 2 | 4 | 0 |
| Нарушения слуха | 18 | 4 | 18 | <4 |
| Реакция в месте введения (инъекции) | 17 | <1 | 1 | 0 |
| Диарея | 17 | <3 | 11 | <2 |
| Парестезия | 17 | <1 | 10 | <1 |
| Нарушения вкуса | 17 | 0 | 15 | 0 |
| Периферическое онемение | 11 | 2 | 7 | <1 |
| Миалгия/артралгия | 12 | <1 | 3 | <1 |
| Флебит/тромбоз/эмболия | 10 | 3 | <1 | <1 |
| Слабость | 12 | <3 | 7 | 2 |
| Инфекционные заболевания | 11 | <6 | <1 | <1 |
| Инфекции дыхательных путей | 10 | <5 | 3 | 3 |
1 Оценка в соответствии со стандартными критериями SWOG (SouthWest Oncology Group), версия 1.
2 Категориальная степень токсичности не определена.
В таблице 11 представлены данные по частоте развития отдельных побочных реакций, отмеченных у ≥10% пациентов, получавших винорелбин в/в в рандомизированном исследовании с применением комбинаций винорелбин + цисплатин, виндезин + цисплатин и винорелбина в качестве монотерапии у пациентов с III или IV стадией НМРЛ, ранее не получавших химиотерапию. В общей сложности 604 пациента получали либо винорелбин в дозе 30 мг/м2/нед в комбинации с цисплатином в дозе 120 мг/м2 в 1-й и 29-й день, затем каждые 6 нед (n=207), либо виндезин в дозе 3 мг/м2 в течение 6 нед, затем каждую 2-ю нед в комбинации с цисплатином в дозе 120 мг/м2 в 1-й и 29-й день, затем каждые 6 нед (n=193), либо винорелбин в дозе 30 мг/м2/нед (n=204).
Пациенты, рандомизированные на получение комбинации винорелбин + цисплатин, получили в среднем 15 нед лечения, комбинации виндезин + цисплатин — 12 нед, а винорелбина в качестве монотерапии — 13 нед. Нейтропения 3-й и 4-й степени наблюдалась значительно чаще у получавших винорелбин + цисплатин (78%) по сравнению с получавшими виндезин + цисплатин (48%) или монотерапию винорелбином (53%). Нейротоксичность, включая периферическую нейропатию и запоры, была зарегистрирована у 44% (степень 3–4, 7%) пациентов, получавших комбинацию винорелбин + цисплатин, у 58% (степень 3–4, 17%) получавших комбинацию виндезин + цисплатин и у 44% (степень 3–4, 8,5%) у получавших винорелбин в качестве монотерапии.
Прекращение исследования из-за развития побочных реакций потребовалось у 27, 22 и 10% пациентов, рандомизированных в группы винорелбин + цисплатин, виндезин + цисплатин и монотерапии винорелбином соответственно.
Таблица 11
Побочные реакции, наблюдавшиеся у ≥10% пациентов в сравнительном исследовании комбинации винорелбин + цисплатином с комбинацией виндезин + цисплатин и монотерапией винорелбином1
| Побочная реакция | Винорелбин + цисплатин2, % | Виндезин + цисплатин3, % | Винорелбин4 | |||
| Любая степень | Степень 3–4 | Любая степень | Степень 3–4 | Любая степень | Степень 3–4 | |
| Лабораторные данные | ||||||
| Нейтропения | 95 | 78 | 79 | 48 | 85 | 53 |
| Лейкопения | 94 | 57 | 82 | 27 | 83 | 32 |
| Тромбоцитопения | 15 | 4 | 10 | 3,5 | 3 | 0 |
| Повышение уровня креатинина крови5 | 46 | Не применимо | 37 | Не применимо | 13 | Не применимо |
| Клинические данные | ||||||
| Тошнота/рвота | 74 | 30 | 72 | 25 | 31 | 2 |
| Алопеция | 51 | 7,5 | 56 | 14 | 30 | 2 |
| Нейротоксичность6 | 44 | 7 | 58 | 17 | 44 | 8,5 |
| Диарея | 25 | 1,5 | 24 | 1 | 12 | 0,5 |
| Реакция в месте введения (инъекции) | 17 | 2,5 | 7 | 0 | 22 | 2 |
| Ототоксичность | 10 | 2 | 14 | 1 | 1 | 0 |
1 Оценка в соответствии с критериями ВОЗ.
2 n=194–207, все пациенты, получавшие винорелбин + цисплатин, с лабораторными и нелабораторными данными.
3 n=173–192, все пациенты, получавшие виндезин + цисплатин, с лабораторными и нелабораторными данными.
4 n=165–201, все пациенты, получавшие винорелбин, с лабораторными и нелабораторными данными.
5 Категориальная степень токсичности не определена.
6 Нейротоксичность включает периферическую нейропатию и запор.
Пероральной введение
Общая зарегистрированная частота возникновения побочных реакций была определена по результатам клинических исследований с участием 316 пациентов (132 пациента с НМРЛ и 184 пациента с раком молочной железы), получавших рекомендованную схему дозирования винорелбина для перорального приема (первые 3 приема по 60 мг/м2/нед, затем 80 мг/м2/нед).
Побочные реакции, о которых сообщалось, перечислены ниже в таблице 12 по классам систем и органов и по частоте возникновения. Дополнительные побочные реакции, наблюдавшиеся в пострегистрационный период, были добавлены в соответствии с классификацией MedDRA как «частота неизвестна».
Частота побочных реакций определяется как очень часто (≥1/10); часто (≥1/100, <1/10); нечасто (≥1/1000, <1/100); редко (≥1/10000, <1/1000); очень редко (<1/10000); частота неизвестна (сообщения пострегистрационного периода применения).
Наиболее часто сообщалось о таких побочных реакциях, как угнетение функции костного мозга с нейтропенией, анемией и тромбоцитопенией, желудочно-кишечная токсичность с тошнотой, рвотой, диареей, стоматитом и запорами. Желудочно-кишечные нежелательные реакции чаще возникают при пероральном приеме винорелбина, чем при в/в введении. Также очень часто сообщалось о повышенной утомляемости и лихорадке.
Таблица 12
Побочные реакциии, отмечавшиеся при пероральном применении винорелбина
| Системно-органный класс и частота возникновения | Побочная реакция | Степень тяжести — частота возникновения, % |
| Инфекции и инвазии | ||
| Очень часто | Бактериальные, вирусные или грибковые инфекции без нейтропении различной локализации | 1–4 — 12,7; 3–4 — 4,4 |
| Часто | Бактериальные, вирусные или грибковые инфекции, возникающие в результате угнетения функции костного мозга и/или нарушений иммунной системы (нейтропенические инфекции). Обычно обратимы при соответствующем лечении | 3–4 — 3,5 |
| Частота неизвестна | Нейтропенический сепсис | − |
| Со стороны крови и лимфатической системы | ||
| Очень часто | Угнетение функции костного мозга, приводящее в основном к нейтропении, носит обратимый характер и является дозолимитирующей токсичностью | 1–4 — 71,5, 3 — 21,8, 4 — 25,9 |
| Лейкопения | 1–4 — 70,6; 3 — 24,7; 4 — 6 | |
| Анемия | 1–4 — 67,4, 3–4 — 3,8 | |
| Тромбоцитопения | 1–2 — 10,8 | |
| Часто | Нейтропения, связанная с повышением температуры тела выше 38 °C, включая фебрильную нейтропению | 4 — 2,8 |
| Со стороны обмена веществ и питания | ||
| Частота неизвестна | Тяжелая гипонатриемия | − |
| Нарушения психики | ||
| Часто | Бессонница | 1–2 — 2,8 |
| Со стороны нервной системы | ||
| Очень часто | Нейросенсорные нарушения, как правило, ограничивались потерей сухожильных рефлексов и в редких случая были тяжелыми | 1–2 — 11,1 |
| Часто | Нейромоторные (нервно-мышечные) нарушения | 1–4 — 9,2; 3–4 — 1,3 |
| Головная боль | 1–4 — 4,1; 3–4 — 0,6 | |
| Головокружение | 1–4 — 6; 3–4 — 0,6 | |
| Нарушения (расстройство) вкуса | 1–2 — 3,8 | |
| Нечасто | Атаксия | 3 — 0,3 |
| Со стороны органа зрения | ||
| Часто | Нарушения зрения | 1–2 — 1,3 |
| Со стороны сердца | ||
| Нечасто | Сердечная недостаточность, сердечная аритмия | − |
| Частота неизвестна | Инфаркт миокарда у пациентов с заболеваниями сердца в анамнезе или факторами риска | − |
| Со стороны сосудов | ||
| Часто | Артериальная гипертензия | 1–4 — 2,5; 3–4 — 0,3 |
| Артериальная гипотензия | 1–4 — 2,2; 3–4 — 0,6 | |
| Со стороны дыхательной системы, органов грудной клетки и средостения | ||
| Часто | Одышка | 1–4 — 2,8; 3–4 — 0,3 |
| Кашель | ||
| Со стороны ЖКТ | ||
| Очень часто | Тошнота | 1–4 — 74,7; 3–4 — 7,3 |
| Рвота | 1–4 — 54,7; 3–4 — 6,3 | |
| Диарея | 1–4 — 49,7; 3–4 — 5,7 | |
| Анорексия | 1–4 — 38,6; 3–4 — 4,1 | |
| Стоматит | 1–4 — 10,4; 3–4 — 0,9 | |
| Абдоминальная боль | 1–4 — 14,2 | |
| Запор | 1–4 — 19; 3–4 — 0,9 | |
| Желудочные расстройства | 1–4 — 11,7 | |
| Часто | Эзофагит | 1–3 — 3,8; 3 — 0,3 |
| Дисфагия | 1–2 — 2,3 | |
| Нечасто | Паралитическая кишечная непроходимость (в исключительных случаях с летальным исходом), лечение может быть возобновлено после восстановления нормальной подвижности кишечника | 3–4 — 0,9 |
| Частота неизвестна | Желудочно-кишечные кровотечения | − |
| Со стороны печени | ||
| Часто | Нарушения функции печени | 1–2 — 1,3 |
| Со стороны кожи и подкожной ткани | ||
| Очень часто | Алопеция, обычно легкой степени тяжести | 1–2 — 29,4 |
| Часто | Кожные реакции | 1–2 — 5,7 |
| Со стороны скелетно-мышечной системы и соединительной ткани | ||
| Часто | Артралгия, включая боль в челюсти, миалгия | 1–4 — 7; 3–4 — 0,3 |
| Со стороны почек и мочевыводящих путей | ||
| Часто | Дизурия | 1–2 — 1,6 |
| Другие заболевания мочеполовой системы | 1–2 — 1,9 | |
| Общие расстройства и нарушения в месте введения | ||
| Очень часто | Поваышенная утомляемость/недомогание | 1–4 — 36,7; 3–4 — 8,5 |
| Лихорадка | 1–4 — 13; 3–4 — 12,1 | |
| Часто | Боль, в том числе в месте опухоли | 1–4 — 3,8; 3–4 — 0,6 |
| Озноб | 1–2 — 3,8 | |
| Данные лабораторных и инструментальных исследований | ||
| Очень часто | Снижение массы тела | 1–4 — 25; 3–4 — 0,3 |
| Часто | Повышение массы тела | 1–2 — 1,3 |
Данные пострегистрационных наблюдений
Парентеральное введение
В ходе пострегистрационного применения винорелбина для в/в введения наблюдались следующие побочные реакции. Поскольку данные об этих реакциях поступали из спонтанных сообщений от популяции неопределенного размера, нет возможности достоверно оценить их частоту или установить причинно-следственную связь с воздействием винорелбина.
Инфекции: пневмония.
Со стороны иммунной системы: анафилактическая реакция, зуд, крапивница, ангионевротический отек.
Со стороны нервной системы: потеря глубоких сухожильных рефлексов, мышечная слабость, нарушение походки, головная боль.
Со стороны органа слуха и лабиринтные нарушения: вестибулярные нарушения, нарушение слуха.
Со стороны сердца: тахикардия.
Со стороны дыхательной системы: отек легких.
Со стороны сосудов: эмболия легочной артерии, ТГВ, артериальная гипертензия, артериальная гипотензия, гиперемия, вазодилатация.
Со стороны ЖКТ: воспаление слизистой оболочки, дисфагия, панкреатит.
Со стороны кожи: генерализованные кожные реакции (сыпь), ладонно-подошвенный синдром.
Со стороны скелетно-мышечной системы и соединительной ткани: боль в челюсти, миалгия, артралгия.
Общие расстройства и нарушения в месте введения: сыпь в месте введения (инъекции), крапивница, образование волдырей, шелушение кожи.
Травмы, отравления и осложнения, вызванные проведением исследовательских процедур: анамнестический радиационный феномен, дерматит, эзофагит.
Отклонения лабораторных показателей: электролитный дисбаланс, включая гипонатриемию.
Прочие: боль в опухоли, боль в спине, абдоминальная боль.
Пероральное введение
Винорелбин для перорального приема применяется в качестве монотерапии или в комбинации с другими химиотерапевтическими ЛС. Наиболее часто в пострегистрационном периоде сообщалось о побочных реакциях со стороны крови и лимфатической системы, ЖКТ, инфекциях и инвазиях и общих расстройствах и нарушениях в месте введения. Эта информация согласуется с дорегистрационными наблюдениями.
Кроме того, при применении винорелбина для в/в введения в до- и пострегистрационный периоды наблюдались некоторые побочные реакции, о которых не сообщалось при применении винорелбина для перорального приема. Нельзя исключать, что данные реакции могут возникать как при пероральном применении винорелбина, так и при применении других алкалоидов барвинка.
Инфекции и инвазии: нечасто — септицемия (очень редко с летальным исходом).
Со стороны иммунной системы: частота неизвестна — системные аллергические реакции в виде анафилаксии, анафилактического шока или реакций анафилактоидного типа.
Со стороны эндокринной системы: частота неизвестна — синдром неадекватной секреции АДГ.
Со стороны сердца: редко — ИБС (стенокардия, инфаркт миокарда); очень редко — сердечная недостаточность и отек легких, однако причинно-следственная связь не установлена.
Со стороны сосудов: нечасто — приливы крови и похолодание конечностей; редко — тяжелая артериальная гипотензия, коллапс.
Со стороны дыхательной системы, органов грудной клетки и средостения: нечасто — бронхоспазм, как и при применении других алкалоидов барвинка; редко — интерстициальная пневмопатия, особенно у пациентов, получавших винорелбин в комбинации с митомицином.
Со стороны ЖКТ: редко — панкреатит.
Со стороны кожи и подкожной ткани: редко — генерализованные кожные реакции.
Взаимодействие
Сообщалось об острых легочных реакциях при пероральном применении винорелбина и других алкалоидов барвинка в сочетании с митомицином. Винорелбин для перорального приема следует с осторожностью назначать в комбинации с митомицином.
Комбинация винорелбина для перорального приема и других ЛС с известной токсичностью для функции костного мозга, вероятно, усугубит миелосупрессивные нежелательные реакции.
В отсутствие специальных исследований, оценивающих взаимодействие с варфарином, следует тщательно наблюдать за состоянием пациентов, при назначении винорелбина в сочетании с варфарином.
Хотя одновременное применение цисплатина не влияет на фармакокинетику винорелбина, частота побочных реакций, в частности гранулоцитопении, при совместном применении винорелбина и цисплатина значительно выше, чем при применении винорелбина в качестве монотерапии.
В исследованиях на крысах антикоагулянтный эффект фениндиона усиливался при применении в сочетании с высокой дозой винорелбина (30 мг/м2/сут в течение 4 дней подряд или 15 мг/м2/сут в течение 5 дней подряд), совместное применение с вальпроатом натрия не вызывало усиления противосудорожной активности.
Винорелбин метаболизируется с участием CYP3A4. Хотя исследования взаимодействия не проводились, ожидается, что ингибиторы CYP3A4, такие как кетоконазол, итраконазол, ритонавир, приведут к повышению концентрации винорелбина в крови. Индукторы CYP3A4, такие как рифампицин и фенитоин, могут снижать концентрацию винорелбина. Поскольку величина индуцирующих или ингибирующих эффектов неизвестна, следует избегать таких сочетаний ЛС.
Следует соблюдать осторожность у пациентов, одновременно принимающих ЛС, ингибирующие CYP3A, т.к. это может вызвать более раннее начало и/или усиление тяжести побочных реакций.
Передозировка
Симптомы: о случаях передозировки винорелбина для перорального приема не сообщалось, однако основными предполагаемыми осложнениями при передозировке являются угнетение функции костного мозга и периферическая нейротоксичность.
Сообщалось о передозировках при введении винорелбина в дозах, в 10 раз превышающих рекомендуемую дозу (30 мг/м2). Описанные побочные реакции соответствовали приведенным в разделе «Побочные действия», включая паралитическую кишечную непроходимость, стоматит и эзофагит. Также сообщалось об аплазии костного мозга, сепсисе и парезе. При передозировке винорелбина для в/в введения зарегистрированы случаи с летальным исходом.
Лечение: в случае передозировки следует принять общие поддерживающие меры, провести соответствующие переливания крови и назначить антибиотики, если необходимо. Антидот неизвестен.
Способ применения и дозы
В/в, перорально. Режим дозирования зависит от схемы химиотерапии и определяется врачом. Парентерально в виде в/в инъекции или инфузии в течение 6–10 мин.
Внутрь рекомендуется принимать во время еды.
Меры предосторожности
Общие меры
Большинство побочных реакций, связанных с применением винорелбина, являются обратимыми. При возникновении тяжелых побочных реакций следует снизить дозу или прекратить применение винорелбина и принять соответствующие корректирующие меры. Возобновление терапии винорелбином должно проводиться с осторожностью и под тщательным контролем в отношении возможного рецидива токсичности.
Пациенты с ИБС должны находиться под тщательным наблюдением.
Нечасто сообщалось об острой одышке и тяжелом бронхоспазме наряду с редкими случаями интерстициальной пневмопатии после перорального приема винорелбина и других алкалоидов барвинка, чаще всего при их применении в комбинации с митомицином. Данные побочные реакции могут потребовать дополнительной кислородотерапии, терапии бронхолитиками (бронходилататорами) и/или ГКС, особенно при уже существующей легочной дисфункции.
Винорелбин внутрь следует применять под наблюдением врача, имеющего опыт применения химиотерапевтических средств против рака. При случайном разжевывании или рассасывании пероральной формы следует прополоскать рот водой или, что предпочтительнее, физиологическим раствором.
Если в течение нескольких часов после приема винорелбина возникла рвота, повторную дозу принимать не следует. Профилактическое лечение метоклопрамидом или пероральными противорвотными средствами может снизить частоту случаев рвоты. Рекомендуется принимать винорелбин внутрь с пищей.
Одновременный прием пищи с низким содержанием жира не влияет на экспозицию винорелбина.
Готовый раствор винорелбина следует вводить только в/в в течение 6–10 мин. Чрезвычайно важно правильно расположить в/в иглу или катетер перед введением винорелбина.
Миелосупрессия
Нейтропения является дозолимитирующей побочной реакцией применения винорелбина.
Миелосупрессия, проявляющаяся нейтропенией, анемией и тромбоцитопенией, возникает у пациентов, получающих винорелбин в/в в качестве монотерапии и в комбинации с цисплатином (см. «Побочные действия»). Нейтропения 3–4-й степени возникла у 53% пациентов, получавших винорелбин в/в в дозе 30 мг/м2/нед. Коррекция дозы в связи с миелосупрессией понадобилась 51% пациентов (исследование 2). В клинических исследованиях винорелбина в дозе 30 мг/м2/нед нейтропения привела к госпитализации по поводу пирексии и/или сепсиса у 8% пациентов. Смерть от сепсиса наступила у 1% пациентов. Максимальное снижение уровня нейтрофилов наблюдается в период с 7-го по 10-й день после введения винорелбина, а восстановление количества нейтрофилов обычно происходит в течение последующих 7–14 дней.
Перед каждым введением дозы винорелбина необходимо проводить полный анализ крови. Не следует назначать винорелбин в/в пациентам с количеством нейтрофилов <1000 клеток/мм3. Коррекция дозы винорелбина должна основываться на данных о количестве нейтрофилов, полученных в день проведения терапии.
Перед пероральным приемом каждой дозы винорелбина необходимо провести определение лейкоцитарной формулы и проанализировать результаты. Пациенты, получающие винорелбин перорально, должны тщательно наблюдаться на предмет развития миелосупрессии как во время, так и после терапии. Винорелбин перорально не следует назначать пациентам с количеством нейтрофилов <1500 клеток/мм3. Если количество нейтрофилов менее 1500/мм3 и/или количество тромбоцитов от 75000 до менее 100000/мм3, лечение следует отложить до восстановления показателей. Пациенты, у которых развивается тяжелая нейтропения, должны находиться под тщательным наблюдением на предмет наличия признаков инфекции и/или лихорадки. Если у пациентов появляются признаки или симптомы, указывающие на инфекцию, необходимо провести оперативное обследование.
Винорелбин перорально следует назначать с особой осторожностью пациентам, у которых резерв костного мозга может быть нарушен в результате предшествующей лучевой или химиотерапии, или пациентам, у которых функция костного мозга восстанавливается после воздействия предыдущей химиотерапии.
В ходе клинических исследований фебрильная нейтропения, в некоторых случаях с летальным исходом, наблюдалась примерно у 15% пациентов при начальной пероральной дозе 80 мг/м2 (соответствует в/в дозе 30 мг/м2 с точки зрения системного воздействия). Поэтому рекомендуется, начинать лечение с дозы 60 мг/м2 и увеличивать ее до 80 мг/м2 только при условии переносимости дозы.
Гепатотоксичность
Лекарственно-индуцированные повреждения печени, проявляющиеся повышением уровня АСТ и билирубина, возникают у пациентов, получающих винорелбин в/в в качестве монотерапии и в комбинации с цитотоксическими средствами. Следует контролировать функцию печени до начала и периодически во время терапии винорелбином. Пациентам, у которых общий уровень билирубин в 2 раза превышает ВГН, требуется снижение дозы.
Винорелбин для перорального приема противопоказан пациентам с тяжелой печеночной недостаточностью. Опыт применения винорелбина у пациентов с легкой или умеренной печеночной недостаточностью ограничен, однако имеющиеся данные свидетельствуют о том, что коррекция дозы не требуется. Следует тщательно контролировать гематологическую токсичность. Винорелбин для перорального приема не следует назначать одновременно с лучевой терапией, если область лечения включает печень.
Из-за низкого уровня почечной экскреции пациентам с нарушением функции почек коррекция дозы не требуется.
Тяжелые запоры и непроходимость кишечника
Тяжелая и жизнеугрожающая паралитическая кишечная непроходимость, запоры, кишечная непроходимость, некроз и перфорация наблюдаются у пациентов, получающих винорелбин в/в. Для облегчения возможных запоров, кишечной непроходимости и/или паралитической кишечной непроходимости следует поддерживать профилактический режим работы кишечника, учитывая достаточное потребление пищевых волокон, гидратацию и регулярное использование средств, размягчающих стул.
Экстравазация и повреждение тканей
Экстравазация винорелбина может привести к сильному раздражению, местному некрозу тканей и/или тромбофлебиту. При появлении признаков или симптомов экстравазации следует немедленно прекратить введение винорелбина и назначить симптоматическую терапию.
Неврологическая токсичность
Сенсорные и моторные невропатии, включая тяжелые, возникают у пациентов, получающих винорелбин в/в. Следует наблюдать за состоянием пациента на предмет появления новых или ухудшения имеющихся признаков и симптомов невропатии, таких как парестезия, гиперестезия, гипорефлексия и мышечная слабость, во время введения винорелбина. При наличии нейропатии 2-й степени или выше по классификации CTCAE терапию винорелбином следует прекратить.
Легочная токсичность и дыхательная недостаточность
Легочная токсичность, включая тяжелый острый бронхоспазм, интерстициальный пневмонит, острый респираторный дистресс-синдром, встречаются у пациентов, получающих винорелбин в/в. Интерстициальный пневмонит и острый респираторный дистресс-синдром приводили к летальному исходу. Среднее время до начала развития интерстициального пневмонита и острого респираторного дистресс-синдрома после введения винорелбина составляло 1 нед (диапазон 3–8 дней). Следует прервать применение винорелбина, если у пациента развивается необъяснимая одышка или имеются какие-либо признаки легочной токсичности. При подтвержденном интерстициальном пневмоните или остром респираторном дистресс-синдроме терапию винорелбином следует окончательно отменить.
Эмбриофетальная токсичность
Основываясь на результатах исследований на животных и механизме действия, винорелбин может оказывать негативное влияние на плод при назначении беременной женщине. В исследованиях репродуктивной функции, проведенных на мышах и кроликах, токсичность для эмбриона и плода наблюдалась при применении винорелбина в дозах, составляющих примерно 0,33 и 0,18 терапевтической дозы для человека соответственно.
Женщины и мужчины с сохраненным репродуктивным потенциалом
Тест на беременность. Женщинам с сохраненным репродуктивным потенциалом, следует проводить тест на наличие беременности до начала терапии винорелбином.
Контрацепция (женщины).Терапия винорелбином может оказывать негативное влияние на плод при назначении беременной женщине. Женщинам с сохраненным репродуктивным потенциалом следует использовать надежные методы (эффективные средства) контрацепции во время терапии винорелбином и в течение 6 мес после введения последней дозы.
Контрацепция (мужчины). Терапия винорелбином может оказывать негативное влияние на сперматозоиды. Мужчинам, имеющим половых партнеров женского пола с сохраненным репродуктивным потенциалом, следует использовать надежные методы контрацепции во время терапии винорелбином и в течение 3 мес после введения последней дозы.
Бесплодие (мужчины). По результатам исследований на животных, терапия винорелбином может нарушать фертильность у мужчин.
Особые группы пациентов
Дети. Безопасность и эффективность применения винорелбина у детей не установлены.
Пожилой возраст. Клинический опыт не выявил различий в реакции у пациентов пожилого возраста и более молодых пациентов, однако нельзя исключить более высокую чувствительность у пациентов пожилого возраста.
Печеночная недостаточность. Влияние печеночной недостаточности на фармакокинетику винорелбина для в/в введения не оценивалось, но печень играет важную роль в метаболизме винорелбина. Повышение уровня АСТ наблюдается у >60% пациентов, получающих винорелбин в качестве монотерапии (6% 3–4-й степени). Поэтому следует соблюдать осторожность у пациентов с печеночной недостаточностью. Для пациентов с повышенной концентрацией общего билирубина в сыворотке крови дозу винорелбина следует снизить.
Источники информации
www.rxlist.com и www.fda.gov, 2022.
Торговые названия с действующим веществом Винорелбин
| Торговое название | Цена за упаковку, руб. |
|---|---|
| Маверекс |
4650.00 |
| Навельбин |
от 3141.00 до 5017.00 |
Винорелбин (Vinorelbine)
💊 Состав препарата Винорелбин
✅ Применение препарата Винорелбин
Описание активных компонентов препарата
Винорелбин
(Vinorelbine)
Приведенная научная информация является обобщающей и не может быть использована для принятия
решения о возможности применения конкретного лекарственного препарата.
Дата обновления: 2020.03.25
Владелец регистрационного удостоверения:
Код ATX:
L01CA04
(Винорелбин)
Лекарственная форма
| Винорелбин |
Конц. д/пригот. р-ра д/инф. 10 мг/1 мл: фл. 1 мл или 5 мл 1 шт. рег. №: ЛП-004575 |
Форма выпуска, упаковка и состав
препарата Винорелбин
Концентрат для приготовления раствора для инфузий в виде прозрачного раствора от бесцветного до светло-желтого цвета.
Вспомогательные вещества: вода д/и — до 1 мл.
1 мл — флаконы вместимостью 2 мл (1) — пачки картонные.
1 мл — флаконы вместимостью 5 мл (1) — пачки картонные.
1 мл — флаконы вместимостью 10 мл (1) — пачки картонные.
5 мл — флаконы вместимостью 5 мл (1) — пачки картонные.
5 мл — флаконы вместимостью 10 мл (1) — пачки картонные.
Фармакологическое действие
Противоопухолевое средство из группы цитостатиков, является полусинтетическим производным одного из алкалоидов барвинка розового — винбластина. Подобно винбластину, винорелбин блокирует митоз клеток на стадии метафазы за счет связывания с белком тубулином.
Фармакокинетика
После в/в введения винорелбин широко распределяется в тканях, Vd составляет более 40 л/кг. Связывание с белками плазмы умеренное — 13.5%, с тромбоцитами — высокое — 78%.
Кинетика винорелбина в плазме трехфазная. Средний T1/2 активного вещества в конечной фазе составляет 40 ч. Системный клиренс — 1.3 л/ч/кг. Выводится преимущественно с желчью.
Показания активных веществ препарата
Винорелбин
Немелкоклеточный рак легкого, распространенный рак молочной железы, гормонорезистентный рак предстательной железы (в комбинации с лечением ГКС для приема внутрь в малых дозах).
Режим дозирования
Способ применения и режим дозирования конкретного препарата зависят от его формы выпуска и других факторов. Оптимальный режим дозирования определяет врач. Следует строго соблюдать соответствие используемой лекарственной формы конкретного препарата показаниям к применению и режиму дозирования.
Устанавливают индивидуально, в зависимости от показаний и стадии заболевания, состояния системы кроветворения, схемы противоопухолевой терапии.
Побочное действие
Со стороны системы кроветворения: гранулоцитопения, анемия.
Со стороны периферической нервной системы: возможно снижение (вплоть до полного угасания) остеосухожильных рефлексов; редко — парестезии; при длительном применении — повышенная утомляемость мышц нижних конечностей.
Со стороны пищеварительной системы: тошнота, реже — рвота; вследствие действия препарата на вегетативную иннервацию кишечника — запор; в отдельных случаях — парез кишечника; редко — паралитическая кишечная непроходимость.
Аллергические реакции: затруднение дыхания, бронхоспазм; в единичных случаях — кожные реакции.
Прочие: алопеция, боли в челюсти.
Местные реакции: флебит.
Противопоказания к применению
Исходное абсолютное число нейтрофилов <1500 клеток/мкл, исходное число тромбоцитов <100000 клеток/мкл; инфекционные заболевания в день начала терапии или перенесенные в течение последних 2 недель; совместное применение с вакциной против желтой лихорадки; беременность, период грудного вскармливания; детский и подростковый возраст до 18 лет, повышенная чувствительность к винорелбину.
С осторожностью
Пациенты с ИБС в анамнезе, тяжелое общее состояние пациентов, печеночная недостаточность тяжелой степени; совместное применение с сильными ингибиторами или индукторами изофермента CYP3A4, антагонистами витамина K, с макролидами, кобицистатом, ингибиторами протеазы, лапатинибом; пациенты из японской популяции (в связи с более частыми случаями развития интерстициальных легочных нарушений у данной категории пациентов).
Применение при беременности и кормлении грудью
Противопоказан к применению при беременности и в период грудного вскармливания.
Применение при нарушениях функции печени
С осторожностью применять при тяжелых нарушениях функции печени.
Применение при нарушениях функции почек
В связи с низкой почечной элиминацией у пациентов с нарушениями функции почек коррекция дозы не требуется.
Применение у детей
Противопоказано применение у детей и подростков.
Применение у пожилых пациентов
Нельзя полностью исключить усиление токсического действия винорелбина у пациентов пожилого возраста.
Особые указания
Лечение винорелбином следует проводить только в специализированном стационаре персоналом, имеющим опыт лечения химиотерапевтическими средствами. Перед началом лечения, а также перед каждым очередным применением винорелбина необходим контроль состава периферической крови. Если число гранулоцитов менее 2000/мкл, очередную инъекцию не производят, откладывая ее до достижения безопасного уровня гранулоцитов.
С осторожностью применяют винорелбин у пациентов с нарушением функции печени, в этом случае дозу снижают.
На фоне применения винорелбина не назначают рентгенотерапию на область печени.
При в/в вливании не допускать экстравазации. Попадание винорелбина в окружающие вену ткани приводит к возникновению болей, воспаления, в тяжелых случаях — некроза.
Следует избегать попадания раствора винорелбина в глаза.
Лекарственное взаимодействие
При одновременном применении с митомицином С повышается риск угнетения дыхания, бронхоспазма, особенно у предрасположенных пациентов; с цисплатином — повышение частоты развития токсических реакций.
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Состав
Активное вещество:
винорелбин — 20 мг.
Вспомогательные вещества:
этанол безводный — 5 мг, вода очищенная — 12.5 мг, глицерол — 2 мг, макрогол 400 — q.s. до 175 мг.
Фармакокинетика
Абсорбция
После приема внутрь винорелбин быстро всасывается из желудочно-кишечного тракта. Максимальное время всасывания Тmах находится в диапазоне от 1,5 до 3 часов с пиком концентрации в крови (Сmах) около 130 иг/мл после приема препарата в дозе 80 мг/м2. Абсолютная биодоступность в среднем составляет 40%, одновременный прием пищи не влияет на степень всасывания винорелбина.
Прием препарата внутрь в дозах 60 мг/м2 и 80 мг/м2 обеспечивает концентрацию винорелбина в крови, эквивалентную концентрации, достигающейся при внутривенном введении препарата в дозах 25 мг/м2 и 30 мг/м2 соответственно.
Концентрация винорелбина в плазме крови увеличивается пропорционально дозе при применении в дозах до 100 мг/м2.
Распределение
Связывание с белками плазмы незначительное — 13,5%, винорелбин в больших количествах связывается с клетками крови, особенно с тромбоцитами (около 78%).
Объем распределения винорелбина высокий, составляет в среднем 21,2 л/кг (диапазон 7,5-39,7 л/кг), что свидетельствует об экстенсивном распределении винорелбина в тканях. Наблюдается значительный захват винорелбина легочной тканью, где достигается концентрация в 300 раз выше, чем в плазме крови.
Винорелбин не обнаруживается в тканях головного мозга.
Метаболизм
Винорелбин биотрансформируется в печени под действием изофермента CYP3A4 цитохрома Р450. Все метаболиты идентифицированы и являются неактивными, за исключением 4-О-деацетилвинорелбина, являющегося основным активным метаболитом в плазме крови. Сульфо- и глюкуроновые конъюгаты не выявлены.
Выведение
Средний период полувыведения винорелбина в конечной фазе элиминации составляет около 40 часов (27,7-43,6 ч). Системный клиренс винорелбина высокий и приближается к скорости кровотока в печени, составляет в среднем 0,72 л/ч/кг (0,32-1,26 л/ч/кг). Винорелбин преимущественно выводится с желчью в неизмененном виде, а также в виде метаболитов. Почками выводится менее 5% дозы, в основном в виде исходного вещества.
Фармакокинетика у особых групп пациентов
Пациенты с нарушением функции почек
Фармакокинетика винорелбина у пациентов с нарушением функции почек не изучалась. В связи с низкой почечной элиминацией винорелбина не требуется снижение дозы препарата Навельбин капсулы при применении у пациентов данной группы.
Пациенты с нарушением функции печени
Фармакокинетика винорелбина не изменялась после применения в дозе 60 мг/м2 в неделю у пациентов с печеночной недостаточностью начальной степени (концентрация общего билирубина превышает верхнюю границу нормы (ВГН) не более чем в 1,5 раза, активность трансаминаз превышает ВГН от 1,5 до 2,5 раз) и в дозе 50 мг/м2 в неделю у пациентов с печеночной недостаточностью средней степени тяжести (концентрация общего билирубина превышает ВГН не более чем в 1,5-3 раза независимо от активности трансаминаз).
Фармакокинетика винорелбина у пациентов с печеночной недостаточностью тяжелой степени не изучалась. Препарат Навельбин капсулы не рекомендуется применять у пациентов данной группы.
Пациенты пожилого возраста (старше 70 лет)
Фармакокинетика винорелбина не изменяется у пациентов в возрасте старше 70 лет. Тем не менее, учитывая возможные сопутствующие заболевания у пациентов пожилого возраста, следует соблюдать осторожность при увеличении дозы препарата Навельбин у пациентов данной группы.
Показания к применению
- немелкоклеточный рак легкого;
- распространенный рак молочной железы.
Противопоказания
-
гиперчувствительность к винорелбину или другим алкалоидам барвинка, а также к любому из компонентов препарата;
-
заболевания и состояния, приводящие к снижению всасывания в желудочно-кишечном тракте;
-
значимая резекция желудка или двенадцатиперстной кишки в анамнезе;
-
исходное абсолютное число нейтрофилов <1 500 клеток/мкл крови;
-
исходное число тромбоцитов <100 000 клеток/мкл крови;
-
инфекционные заболевания в день начала терапии или перенесенные в течение последних 2-х недель;
-
потребность в продолжительной оксигенотерапии;
-
беременность и период грудного вскармливания;
-
детский возраст до 18 лет (безопасность и эффективность применения винорелбина у детей не изучены);
-
печеночная недостаточность тяжелой степени;
-
совместное применение с вакциной против желтой лихорадки.
С осторожностью:
Применять с осторожностью у пациентов с ишемической болезнью сердца в анамнезе, у пациентов с тяжелым общим состоянием, при печеночной недостаточности средней степени тяжести.
Следует соблюдать осторожность при совместном применении с сильными ингибиторами или индукторами изофермента CYP3A4, антагонистами витамина К, макролидами, кобицистатом, ингибиторами протеазы. Подробную информацию см. в разделе «Взаимодействие с другими лекарственными средствами и другие виды взаимодействия».
Способ применения и дозы
Препарат Навельбин капсулы применяют по назначению врача.
Для приема внутрь.
Капсулы следует проглатывать целиком, запивая водой, не разжевывая и не рассасывая во рту. Рекомендуется принимать капсулы во время еды.
Частоту приемов и продолжительность лечения определяет врач.
Дозу на прием определяет врач, исходя из результатов гематологического анализа.
При снижении абсолютного числа нейтрофилов менее 1500 клеток/мкл крови и/или тромбоцитопении <100000 клеток/мкл крови введение препарата откладывают до восстановления их количества.
Рекомендуется начинать применение препарата со стартовой дозы 60 мг/м2 и в дальнейшем увеличивать ее до 80 мг/м2 в случае хорошей переносимости.
Режим монотерапии
Первые три приема
Рекомендованная доза — 60 мг/м2 один раз в неделю.
Последующие приемы
После третьего приема рекомендуется увеличить дозу до 80 мг/м2 один раз в неделю.
Увеличение дозы до 80 мг/м2 возможно лишь в том случае, если в течение первых трех недель приема препарата в дозе 60 мг/м2 абсолютное число нейтрофилов (АЧН) ни разу не уменьшалось ниже 500 клеток/мкл, либо уменьшалось до уровня 500 — 1000 клеток/мкл не более одного раза.
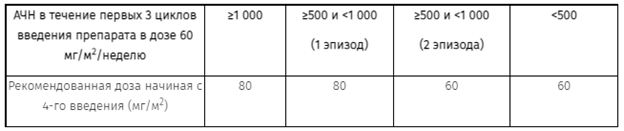
Коррекция дозы
Если в период применения препарата в дозе 80 мг/м2 АЧН становится ниже 500 клеток/мкл или более чем один раз уменьшается до уровня 500-1000 клеток/мкл, следует отложить следующее введение препарата до восстановления АЧН и уменьшить дозу до 60 мг/м2 для трех последующих введений.

Повторное увеличение дозы с 60 мг/м2 до 80 мг/м2 в неделю возможно только в том случае, если в течение трех педель приема препарата в дозе 60 мг/м2 в неделю АЧН ни разу не уменьшалось ниже 500 клеток/мкл, либо уменьшалось до уровня 500 — 1000 клеток/мкл не более одного раза.
Режим комбинированной химиотерапии
Для комбинированных режимов, в которых чередуется пероральное и внутривенное введение винорелбина, следует учитывать, что пероральный прием препарата Навельбин капсулы в дозах 60 мг/м2 и 80 мг/м2 обеспечивает концентрацию винорелбина в крови, эквивалентную концентрации, достигающейся при внутривенном введении препарата Навельбин концентрат для приготовления раствора для инфузий в дозах 25 мг/м2 и 30 мг/м2 соответственно.
Дозы и схемы должны быть адаптированы под протокол лечения.
Для пациентов с площадью поверхности тела более 2 м2 общая разовая доза не должна превышать 120 мг в неделю при назначении препарата в дозе 60 мг/м2 и 160 мг в неделю при назначении препарата в дозе 80 мг/м2.
Особые группы пациентов
Пациенты пожилого возраста (старше 70 лет)
Клинический опыт применения винорелбина у пациентов пожилого возраста не выявил значимых отличий в отношении развития ответа на терапию, однако нельзя полностью исключить возможность повышенной чувствительности к токсическим свойствам винорелбина у некоторых пациентов пожилого возраста.
Фармакокинетика винорелбина у пациентов пожилого возраста не изменяется.
Применение у детей
Безопасность и эффективность применения винорелбина у детей не изучены. Препарат Навельбин противопоказан у детей.
Пациенты с нарушением функции печени
При печеночной недостаточности начальной степени (концентрация общего билирубина превышает верхнюю границу нормы (ВГН) не более чем в 1,5 раза, активность трансаминаз превышает ВГН от 1,5 до 2,5 раз) препарат Навельбин капсулы можно применять в стандартной дозе 60 мг/м2 в неделю.
При печеночной недостаточности средней степени тяжести (концентрация общего билирубина превышает ВГН не более чем в 1,5-3 раза независимо от активности трансаминаз) рекомендуется применять препарат Навельбин капсулы в дозе 50 мг/м2 в неделю.
При печеночной недостаточности тяжелой степени не рекомендуется применять препарат Навельбин капсулы в связи с недостатком данных в отношении фармакокинетики, эффективности и безопасности винорелбина у пациентов данной группы.
Пациенты с нарушением функции почек
Почечная экскреция винорелбина незначительна, поэтому не требуется снижать дозу препарата Навельбин у пациентов с почечной недостаточностью.
Условия хранения
Хранить в недоступном для детей месте при температуре от 2°С до 8°С.
Срок годности
3 года. Не применять после истечения срока годности, указанного на упаковке.
Особые указания
Необходим тщательный гематологический контроль в период применения препарата Навельбин. Перед каждым очередным приемом препарата следует определять число лейкоцитов, нейтрофилов, тромбоцитов, концентрацию гемоглобина.
В случае подозрения на сопутствующую инфекцию в день начала терапии следует обследовать пациента и оценить соотношение пользы и риска при принятии решения о введении препарата.
При появлении одышки, кашля или гипоксии невыясненной этиологии следует обследовать пациента для исключения легочной токсичности.
Прием препарата Навельбин капсулы связан с риском развития тошноты/рвоты. Рекомендуется первичная профилактика с использованием противорвотных средств. В случае возникновения рвоты в течение нескольких первых часов после приема препарата не следует принимать повторную дозу препарата.
Содержимое капсулы обладает раздражающим действием. Если пациент по ошибке разжевал или рассосал капсулу, необходимо незамедлительно промыть полость рта 0,9% раствором натрия хлорида или водой.
В случае механического повреждения капсулы контакт с жидким содержимым может привести к ожогу кожи, слизистых оболочек, глаз. Если это случилось, пострадавшие участки следует немедленно тщательно промыть 0,9% раствором натрия хлорида или водой. Поврежденные капсулы нужно передать в медицинское учреждение с целью уничтожения должным образом.
Препарат Навельбин капсулы не следует применять одновременно с проведением рентгенотерапии, захватывающей область печени.
В состав оболочки капсулы входит сорбитол. Пациентам с непереносимостью фруктозы не следует принимать препарат Навельбин капсулы.
Не рекомендуется совместное применение с живыми аттенуированными вакцинами, фенитоином, итраконазолом, позаконазолом, кетоконазолом.
В составе препарата содержится незначительное количество этилового спирта (этанола) — менее 100 мг на дозу.
Влияние на фертильность
Мужчины и женщины должны использовать надежные способы контрацепции в период лечения препаратом Навельбин, а также в течение трех месяцев после окончания химиотерапии.
Пациентам, планирующим рождение детей после завершения лечения, рекомендуется генетическая консультация.
Вследствие возможности развития необратимой потери фертильности в результате химиотерапии, пациентам должна быть дана рекомендация по консервации спермы до начала курса лечения препаратом Навельбин.
Описание
Противоопухолевый препарат.
Лекарственная форма
Капсулы мягкие желатиновые, овальные, размер №3, светло-коричневого цвета, с красной надписью «N20»; содержимое капсул — вязкий раствор от светло-желтого до оранжево-желтого цвета.
Применение у детей
Противопоказание: детский возраст до 18 лет (безопасность и эффективность применения винорелбина у детей не изучены).
Фармакодинамика
Винорелбин — противоопухолевое средство растительного происхождения из группы полусинтетических винкаалкалоидов, выделенный из растения рода Vinca (барвинок). Нарушает полимеризацию тубулина в процессе клеточного митоза. Блокирует митоз клеток на стадии метафазы G2-M, вызывая гибель клеток во время интерфазы или при последующем митозе. Действует преимущественно на митотические микротрубочки; при применении высоких доз оказывает влияние также на аксональные микротрубочки. Эффект спирализации тубулина, вызываемый винорелбином, выражен слабее, чем у винкристина.
Побочные действия
Со стороны системы кроветворения: гранулоцитопения, анемия.Со стороны периферической нервной системы: возможно снижение (вплоть до полного угасания) остеосухожильных рефлексов; редко — парестезии; при длительном применении — повышенная утомляемость мышц нижних конечностей.Со стороны пищеварительной системы: тошнота, реже — рвота; вследствие действия препарата на вегетативную иннервацию кишечника — запор; в отдельных случаях — парез кишечника; редко — паралитическая кишечная непроходимость.Аллергические реакции: затруднение дыхания, бронхоспазм; в единичных случаях — кожные реакции.Прочие: алопеция, боли в челюсти.Местные реакции: флебит.
Применение при беременности и кормлении грудью
Беременность
Данные по применению винорелбина у беременных женщин отсутствуют.
В исследованиях на животных винорелбин продемонстрировал эмбриотоксическое и тератогенное действие. Данные доклинических исследований и фармакологическое действие винорелбина позволяют предположить существование потенциального риска токсического действия на эмбрион и плод.
Препарат Навельбин противопоказан во время беременности.
Грудное вскармливание
Неизвестно, выделяется ли винорелбин в грудное молоко. Невозможно исключить риск токсического действия винорелбина в период грудного вскармливания.
Препарат Навельбин противопоказан в период грудного вскармливания.
Грудное вскармливание должно быть прекращено до начала применения препарата.
Взаимодействие
Взаимодействия, характерные дли всех цитотоксических препаратов
- Совместное применение противопоказано
С вакциной против желтой лихорадки: риск развития генерализованной вакцинальной болезни с летальным исходом.
- Совместное применение не рекомендуется
С живыми аттенуированными вакцинами: риск развития генерализованной вакцинальной болезни с летальным исходом. Данный риск увеличивается у пациентов с иммуносупрессией, вызванной основным заболеванием. Рекомендуется использовать инактивированные вакцины в случае их существования.
Фенитоин: риск обострения судорожного синдрома из-за уменьшения всасывания фенитоина в желудочно-кишечном тракте при совместном применении с цитотоксическим препаратом; риск увеличения цитотоксичности, или потеря эффективности цитотоксического препарата в результате ускорения его метаболизма в печени.
Совместное применение с осторожностью
Антагонисты витамина К: риск кровотечений и тромбозов в случае опухолевых заболеваний. Кроме того, возможно взаимодействие между антикоагулянтами и цитотоксическими средствами. В случае применения у пациента пероральных антикоагулянтов требуется более частый контроль МНО (международного нормализованного отношения).
Макролиды (кларитромицин, эритромицин, телитромицин): риск повышения токсичности антимитотического агента вследствие снижения его метаболизма в печени. Тщательный клинический и лабораторный мониторинг. При возможности следует использовать альтернативные антибиотики.
Кобицистат: повышение нейротоксичности антимитотического агента вследствие снижения его метаболизма в печени. Тщательный клинический мониторинг. При возможности следует снизить дозу антимитотического агента.
- При совместном применении принять во внимание
Иммуносупрессоры (циклоспорин, эверолимус, сиролимус, такролимус): выраженная иммуносупрессия с риском лимфопролиферативного синдрома.
Взаимодействия, характерные для винкаалкалоидов
- Совместное применение не рекомендуется
Итраконазол, позаконазол, кетоконазол: повышение нейротоксичности винкаалкалоидов в результате снижения их метаболизма в печени.
- Совместное применение с осторожностью
Ингибиторы протеазы: повышение токсичности антимитотического агента в результате снижения его метаболизма в печени. Необходим тщательный клинический мониторинг, при возможности — корректировка дозы антимитотического агента.
- При совместном применении принять во внимание
Митомицин С: повышается риск легочной токсичности митомицина и винкаалкалоидов.
Индукторы и ингибиторы Р-гликопротеина: поскольку известно, что винкаалкалоиды являются субстратом для Р-гликопротеина, следует соблюдать осторожность при совместном применении препарата Навельбин с препаратами, изменяющими функцию данного транспортного белка.
Взаимодействия, характерные для винорелбина
Совместное применение винорелбина с другими препаратами с известной миелотоксичностью может усиливать выраженность миелосупрессивных нежелательных реакций.
В метаболизме винорелбина участвует главным образом CYP3A4. Совместное применение с сильными ингибиторами данного изофермента (кетоконазол, итраконазол) может повышать концентрацию винорелбина в плазме крови; комбинация с сильными индукторами данного изофермента (рифампицин, фенитоин) может снижать концентрацию винорелбина в плазме крови.
Отсутствует взаимное влияние при совместном применении винорелбина с цисплатином в течение нескольких циклов лечения. Однако частота встречаемости гранулоцитопении, ассоциированной с приемом винорелбина, в комбинации с цисплатином была выше, чем при применении винорелбина в монотерапии.
Не выявлено клинически значимого фармакокинетического взаимодействия при совместном применении винорелбина с паклитакселом, доцетакселом, капецитабином, пероральным циклофосфамидом.
Противорвотные средства из группы антагонистов 5НТ3 рецепторов (ондансетрон, гранисетрон) не влияют на фармакокинетику винорелбина.
Пищевые продукты не влияют на фармакокинетические свойства винорелбина.
Передозировка
Симптомы
Подавление функции костного мозга, иногда в сочетании с инфекцией, лихорадкой, паралитической кишечной непроходимостью и нарушениями функции печени.
Неотложная помощь
Госпитализация и тщательное мониторирование функций жизненно важных органов. Должны быть предприняты соответствующие терапевтические меры: переливание крови, введение антибиотиков, факторов роста.
Антидот
Специфический антидот неизвестен.
Влияние на способность к вождению автотранспорта и управлению механизмами
Специальных исследований по влиянию препарата на способность к вождению автотранспорта и управлению механизмами не проводилось. Тем не менее пациентам не рекомендуется управлять транспортными средствами и заниматься другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций, если они испытывают побочные реакции, способные повлиять на выполнение этой деятельности (например, головокружение, нарушение зрительного восприятия).
-
Винорелбин относится к семейству лекарственных препаратов из группы винкаалкалоидов и предназначен для лечения следующих злокачественных опухолей:
• немелкоклеточный рак легкого;
• метастатический рак молочной железы.
Этот препарат не рекомендуется детям и подросткам младше 18 лет.
Винорелбин представляет собой концентрат для приготовления раствора для инфузий («капельницы»), вводимый внутривенно.
• у Вас аллергия на Винорелбин
• у Вас аллергия на другие препараты из группы винкаалкалоидов, так как вы также можете иметь аллергию на Винорелбин
• у Вас низкий уровень нейтрофилов в крови
• Вы перенесли острое инфекционное заболевание в течение 2 недель перед началом лечения препаратом Винорелбин или еще болеете
• у Вас низкий уровень тромбоцитов в крови
• Вы планируете прививку против желтой лихорадки или только что сделали ее
• Вы беременны или думаете, что можете быть беременны
• Вы кормите ребенка грудью
Если Вы не уверены, относится ли к Вам что-либо из вышеперечисленного, сообщите об этом лечащему врачу перед применением Винорелбина.
Перед применением препарата Винорелбин проконсультируйтесь с лечащим врачом, если:
• у Вас когда-либо был сердечный приступ или сильная боль в груди
• Вы получали лучевую терапию и в зону облучения попадала печень
• у Вас есть признаки или симптомы инфекционного заболевания (такие как лихорадка, озноб, боль в суставах или кашель)
• Вы принимаете или недавно принимали какое-либо другое лекарство, включая препараты, которые отпускаются без рецепта врача
• Вы планируете делать прививку или недавно сделали ее
• у Вас проблемы с печенью
До и во время лечения препаратом Винорелбин Вам будут делать анализ крови, чтобы подтвердить, что лечение безопасно для Вас. Если результаты анализов будут неудовлетворительными, то лечение может быть приостановлено и Вам могут назначить дополнительные исследования до тех пор, пока показатели не восстановятся до нормы.
Дети и подростки
Винорелбин не следует давать детям или подросткам до 18 лет вследствие недостаточного количества данных о его эффективности и безопасности для детей и подростков.
Проконсультируйтесь с лечащим врачом, если Вы принимаете, недавно принимали или можете начать принимать любые другие препараты. Это относится к любым растительным препаратам и препаратам, отпускаемым без рецепта врача. Проконсультируйтесь с лечащим врачом, если Вы принимаете:
• противогрибковые препараты, такие как итраконазол, кетаконазол и позаконазол
• противоопухолевые препараты, такие как цисплатин, митомицин С и лапатиниб
• препараты, которые подавляют Вашу иммунную систему, такие как циклоспорин, такролимус, эверолимус, сиролимус
• фенитоин
• рифампицин
• препараты для разжижения крови (антикоагулянты)
• макролиды (класс антибиотиков), такие как кларитромицин, эритромицин, телитромицин
• кобицистат
• ингибиторы протеазы
Лечащий врач решит, следует ли использовать Винорелбин в сочетании с этими и другими лекарствами.
Во время лечения препаратом Винорелбин не рекомендуется делать прививки с использованием живых аттенуированных вакцин, таких как вакцины против кори, паротита, краснухи. Сообщите врачу, если Вам требуется вакцинация.
Если Вы принимаете Винорелбин одновременно с другими препаратами, которые влияют на костный мозг, некоторые побочные реакции могут усилиться.
Винорелбин с пищей, напитками и алкоголем
Винорелбин не взаимодействует с пищей и напитками. Проконсультируйтесь с Вашим лечащим врачом по поводу употребления алкоголя во время лечения Винорелбином.
Если Вы беременны или кормите грудью, думаете, что можете быть беременны, или планируете беременность, не принимайте Винорелбин. Если Вы беременны и Вам необходимо лечение Винорелбином или Вы забеременеете во время лечения, немедленно сообщите об этом лечащему врачу. Используйте эффективные средства контрацепции во время лечения и в течение трех месяцев после его окончания.
Фертильность мужчин
Если Вам необходимо лечение Винорелбином, используйте эффективные средства контрацепции во время лечения и в течение трех месяцев после его окончания. Проконсультируйтесь с врачом по поводу консервации спермы, так как Винорелбин может привести к необратимой утрате фертильности.
Исследования влияния на способность управлять транспортными средствами и работать с механизмами не проводились. Тем не менее, побочные эффекты Винорелбина (см. раздел «Возможные нежелательные реакции») могут повлиять на вождение и выполнение других задач. Соблюдайте осторожность и откажитесь от вождения, если Вы чувствуете себя плохо, или если врач порекомендовал Вам отказаться от вождения.
Винорелбин должен назначать квалифицированный врач, имеющий опыт лечения противоопухолевыми препаратами. Всегда принимайте этот препарат в полном соответствии с рекомендациями лечащего врача. При появлении сомнений, проконсультируйтесь с лечащим врачом.
Доза
Лечащий врач будет проверять показатели Вашей крови до и во время лечения Винорелбином. От результатов исследований будет зависеть решение о начале лечения либо о его невозможности в данный момент. Доза препарата будет зависеть от Вашего роста, веса и общего состояния. Лечащий врач подсчитает площадь поверхности Вашего тела и подберет ту дозу, которую Вы будете принимать.
Частота введения
Обычно Винорелбин назначают один раз в неделю. Частоту введения определит Ваш врач.
Продолжительность лечения
Продолжительность лечения определит Ваш лечащий врач.
Способ применения
Перед введением Винорелбин необходимо развести. Винорелбин вводят только внутривенно в течение 6-10 минут. После «капельницы» вену обильно промывают стерильным раствором.
Применение у детей и подростков
Винорелбин не следует применять для лечения детей и подростков младше 18 лет.
Если Вы применили препарата Винорелбин больше, чем следовало
Дозу Винорелбина тщательно контролирует Ваш лечащий врач. Тем не менее, несмотря на то, что Вы получите верную дозу препарата, у Вас могут возникнуть тяжелые нежелательные реакции. Признаками такой реакции могут служить симптомы инфекции (такие как лихорадка, озноб, кашель или боль в суставах), может возникнуть сильный запор. При появлении любых из этих симптомов немедленно обратитесь к врачу.
Если Вы досрочно прекращаете прием препарата Винорелбин
Ваш лечащий врач определит, когда Вам следует прекратить лечение. Если Вы желаете закончить лечение раньше, обратитесь к Вашему врачу, чтобы обсудить с ним другие варианты Вашего лечения.
При наличии вопросов по применению препарата, обратитесь к лечащему врачу.
Подобно всем лекарственным препаратам, Винорелбин может вызывать нежелательные реакции, однако они возникают не у всех.
Немедленно обратитесь к врачу, если Вы чувствуете любую из приведенных ниже нежелательных реакций – Вам может понадобиться неотложная медицинская помощь:
• признаки острой инфекции, такие как кашель, лихорадка или озноб
• сильный запор и боли в животе после того, как кишечник не опорожнялся несколько дней
• сильное головокружение или слабость при вставании, что может быть признаком резкого падения артериального давления
• сильная боль в груди, нетипичная для Вас, может быть признаком неправильной работы сердца из-за недостаточного притока крови (ишемическая болезнь сердца)
• признаки аллергии, такие как зуд, затрудненное дыхание, головокружение, снижение артериального давления, кожная сыпь по всему телу или отек век, губ или горла
Могут возникать следующие нежелательные реакции:
Очень часто (могут проявляться более чем у 1 из 10 человек):
• снижение уровня эритроцитов (анемия), что может стать причиной бледности кожи и вызвать слабость или одышку
• снижение уровня лейкоцитов в крови
• слабость нижних конечностей
• потеря некоторых рефлексов, иногда сопровождаемая ухудшением тактильной чувствительности
• выпадение волос, обычно умеренное при долговременном лечении
• тошнота, рвота
• запор
• воспаление или афтозные язвы во рту или горле
• повышение уровня печеночных ферментов в крови
• реакции в месте введения препарата, такие как покраснение, чувство жжения, изменение цвета вены, воспаление вены
Часто (могут проявляться менее чем у 1 из 10 человек):
• бактериальная, вирусная или грибковая инфекция
• снижение уровня тромбоцитов, что может повысить риск кровотечений или образования гематом
• боль в суставах, боль в челюстях
• мышечные боли
• усталость
• лихорадка
• боль в разных частях тела, в том числе боль в грудной клетке и боль в месте опухолевого образования
• диарея
Нечасто (могут проявляться менее чем у 1 из 100 человек):
• тяжелый сепсис, септицемия
• значительное затруднение в движениях и в тактильной чувствительности
• низкое или высокое кровяное давление
• головная боль
• головокружение
• ощущение внезапного жара и покраснение кожи лица и шеи
• ощущение холода в руках или ногах (холодные конечности)
• затрудненное или свистящее дыхание
Редко (могут проявляться менее чем у 1 из 1000 человек):
• сильная боль в груди, сердечный приступ (ишемическая болезнь сердца, стенокардия, инфаркт миокарда, иногда фатальный)
• затруднение дыхания (интерстициальная болезнь легких, иногда фатальная)
• воспаление поджелудочной железы
• крайне низкая концентрация натрия в крови, что может вызывать такие симптомы, как усталость, спутанность сознания, судороги и кому
• изъязвление в месте инъекции
• кожная сыпь
Очень редко (могут проявляться менее чем у 1 из 10 000 человек):
• учащенное сердцебиение, ощущение сердцебиения, нарушения сердечного ритма
Частота неизвестна:
• анорексия
• тяжелые аллергические реакции
• нарушение секреции антидиуретического гормона
• покраснение стоп и кистей (эритема)
Сообщение о нежелательных реакциях
Если у Вас возникают какие-либо нежелательные реакции, проконсультируйтесь с врачом. Это также относится к любым побочным эффектам, которые не указаны в данном листке-вкладыше. Вы также можете сообщить о нежелательных реакциях в информационную базу данных по нежелательным реакциям (действиям) на лекарственные препараты, включая сообщения о неэффективности лекарственных препаратов, выявленным на территории государства (УП «Центр экспертиз и испытаний в здравоохранении М3 РБ», rceth.by). Сообщая о нежелательных реакциях, Вы помогаете получить больше сведений о безопасности препарата.
Храните препарат в недоступном для детей месте.
Храните препарат в защищенном от света месте при температуре от 2°C до 8°C.
Храните препарат в оригинальной упаковке.
Не применяйте препарат после окончания срока годности, указанного на упаковке.
Датой истечения срока годности является последний день месяца.
Срок годности: 2 года.
Действующим веществом препарата Винорелбин является винорелбин (в виде винорелбина тартрата). 1мл раствора содержит 10 мг винорелбина. Каждый флакон содержит 10 мг или 50 мг винорелбина.
Вспомогательное вещество: вода для инъекций.
Винорелбин, концентрат для приготовления раствора для инфузий 10 мг/мл представляет собой прозрачный раствор бесцветного либо бледно-желтого цвета.
Винорелбин выпускается во флаконах стеклянных по 1 мл или 5 мл, укупоренных пробками резиновыми. Флакон вместе с листком-вкладышем помещен в пачку из картона.
по рецепту врача.
Держатель регистрационного удостоверения и производитель
РУП «Белмедпрепараты»,
Республика Беларусь, 220007, г. Минск,
ул. Фабрициуса, 30, тел./факс:(+375 17) 220 37 16,
e-mail: medic@belmedpreparaty.com
- Скачать инструкцию медикамента
Торговое название
Навельбин®
Международное непатентованное название
Винорелбин
Лекарственная форма
Мягкие капсулы, 20 мг, 30 мг
Состав
Одна капсула содержит:
активное вещество – винорелбина тартрата 27.70 мг 41.55 мг
эквивалентно винорелбину 20.00 мг 30.00 мг
вспомогательные вещества – глицерол, этанол безводный, вода очищенная, макрогол 400
состав мягких желатиновых капсул – желатин, глицерол 85 %, ANIDRISORB 85/70 (сорбитол – сорбитан – 1.4 – маннитол – высокомолеку-лярные спирты), железа (III) оксид желтый (Е172) или железа (III) оксид красный (Е172), титана диоксид (Е171), триглицериды, триглицериды средней цепи, смесь PHOSAL 53 MCT и триглицериды средней цепи (99.6/0.4)
состав чернил пищевых — гипромеллоза, пропиленгликоль, карминовая кислота (Е120)
Описание
Мягкие непрозрачные желатиновые капсулы размером 3 овальной формы, с гладкой блестящей поверхностью, однородного светло-коричневого цвета, с надписью «N20» нанесенной чернилами красного цвета (для дозировки 20 мг).
Мягкие непрозрачные желатиновые капсулы размером 3 продолговатой формы, с гладкой блестящей поверхностью, однородного розового цвета, с надписью «N30» нанесенной чернилами красного цвета (для дозировки 30 мг).
Содержимое капсул – вязкий, прозрачный раствор от светло-желтого до оранжево-желтого цвета, без видимых частиц.
Фармакотерапевтическая группа
Противоопухолевые препараты. Алкалоиды растительного происхождения. Барвинка алкалоиды и его аналоги. Винорелбин.
Код АТХ L01CA04
Фармакологические свойства
Фармакокинетика
Всасывание
После приема внутрь, винорелбин быстро всасывается и Т max достигается в промежутке времени от 1.5 до 3-х часов с максимумом концентрации в крови (C max) около 130 нг/мл после дозировки 80 мг/м². Абсолютная биологическая доступность около 40% и одновременный прием пищи не замедляет действие винорелбина.
Дозировки для приема внутрь 60 и 80 мг/м² действуют на показатели крови так же как дозировки Навельбин® концентрата для приготовления раствора для внутривенных инфузий 25 и 30 мг/м².
Распределение
Объем распределения обширен, в среднем 21.2 л.кг-¹ (область: 7.5 – 39.7 л.кг-¹), что показывает обширность распределения в тканях.
Связывание с белками плазмы крови низкое (13.5%), винорелбин прочно связывается с клетками крови, в особенности с тромбоцитами (78%).
Биотрансформация
Все метаболиты винорелбина преобразованы изоформой CYP 3A4 цитохромов Р450, за исключением 4-О-деацетилвинорелбина, обычно образуемые карбоксилестеразами. 4-О-деацетилвинорелбин является единственным активным метаболитом и одним из главных, наблюдаемых в крови.
Выведение
Средний период полувыведение винорелбина из организма составляет около 40 часов. Достигая печеночного кровотока, очищение крови становится высоким – 0.72 л/ч/кг (область: 0.32-1.26 л/ч/кг).
Выведение почками низкое (<5% принятой дозировки). Выведение желчью является преобладающим путем выведения неизмененного винорелбина, который является основным восстановленным компонентом, и его метаболитов.
Фармакодинамика
Навельбин® — противоопухолевый препарат из группы винкаалкалоидов.
Оказывает цитостатическое действие, связанное с ингибированием полимеризации тубулина в процессе клеточного митоза. Навельбин® блокирует митоз в фазе G2 +M (синтез белка митотического веретена, строительным белком является тубулин) и вызывает разрушение клеток в интерфазе или при последующем митозе. Препарат действует преимущественно на митотические микротрубочки; при применении в высоких дозах оказывает влияние и на аксональные микротрубочки. Эффект спирализации тубулина, вызываемый препаратом Навельбин®, выражен слабее, чем у винкристина.
Показания к применению
— немелкоклеточный рак лёгкого
— рак молочной железы с метастазированием.
Способ применения и дозы
Навельбин® мягкая капсула должна применяться только пероральным путем. Капсула должна быть проглочена, запивая небольшим количеством воды, не разжевывая или рассасывая капсулу. Рекомендуется принять капсулу вместе с пищей.
При монотерапии:
Первые три применения доза 60 мг/м² площади поверхности тела, принимать один раз в неделю. После третьего применения, рекомендуется увеличить дозу Навельбина® до 80 мг/м² один раз в неделю, за исключением тех пациентов, у которых было резкое снижение количества нейтрофилов ниже 500/мм³, или больше одного раза между 500 и 1000/мм³ в течении первых трех приемов по 60 мг/м².
При комбинированном режиме:
Доза для приема внутрь 80 мг/м² площади поверхности тела соответствует дозе для внутривенного введения 30 мг/м2, доза для приема внутрь 60 мг/м² площади поверхности тела соответствует дозе для внутривенного введения 25 мг/м2. Это является основанием для комбинированного режима внутривенного введения и приема внутрь для удобства пациента.
Побочные действия
Инфекционные и паразитарные заболевания
Очень часто
— бактериальные, вирусные или грибковые заболевания без нейтропении
Часто
— бактериальные, вирусные или грибковые заболевания, возникшие вследствие подавления деятельности костного мозга и/или при нарушении иммунной системы (инфекционное заболевание при нейтропении) в последствии обратимые, при правильном лечении
— инфекционное заболевание при нейтропении
Не известно
— нейтропенический сепсис
Нарушения со стороны системы кроветворения и лимфатической системы
Очень часто
— угнетение функции костного мозга с нейтропенией
— лейкопения
— анемия
— тромбоцитопения
Часто
— нейтропения, связанная с повышением температуры тела выше 38 ºС, включая фебрильную нейтропению
— гранулоцитопения
Нарушения со стороны обмена веществ и питания
Не известно
— гипонатриемия
Нарушения со стороны нервной системы
Очень часто
— нейросенсорные нарушения (сухожильный рефлекс)
— после длительного лечения может наблюдаться повышенная утомляемость
мышц нижних конечностей
Часто
— нервно-двигательное нарушение
— головная боль, головокружение
— вкусовые расстройства
— бессонница
Не часто
— атаксия
Нарушение со стороны органа зрения
Часто
— нечеткость зрения
Нарушения со стороны сердечно-сосудистой системы
Не часто
— паралич сердца и сердечная аритмия
Не известно
— инфаркт миокарда у пациентов с заболеваниями сердца в истории болезни или с факторами риска, влияющими на сердце
Нарушения со стороны сосудистой системы
Часто
— артериальная гипертензия
— артериальная гипотензия
Нарушения со стороны органов дыхания
Часто
— одышка
— кашель
Нарушения со стороны пищеварительной системы
Очень часто
— тошнота, рвота, диарея, запор
— анорексия
— стоматит
— абдоминальная боль
Часто
— эзофагит
— дисфагия
Не часто
— паралитическая кишечная непроходимость
Не известно
— желудочно-кишечное кровотечение
Нарушения со стороны печени и желчевыводящих путей
Часто
— заболевания печени
Нарушения со стороны кожи и подкожных тканей
Очень часто
— алопеция
Часто
— реакция кожи
Нарушения со стороны скелетно-мышечной и соединительной ткани
Часто
— артралгия, включая боль в челюсти
— миалгия
Нарушения со стороны мочевыводящей системы
Часто
— дизурия
— другие мочеполовые нарушения
Общие нарушения и состояние места введения препарата
Очень часто
— утомляемость, дисфория
— повышение температуры
Часто
— боль, включая боль в месте локализации опухоли
— озноб
Лабораторные и инструментальные данные
Очень часто
— потеря в весе
Часто
— прибавление в весе
Противопоказания
— гиперчувствительность к винорелбину или к другим алкалоидам барвинка или к одному из вспомогательных веществ
— заболевания, значительно влияющие на абсорбцию
— предшествующие хирургические операции на желудок или тонкую кишку
— число нейтрофилов < 1500/мм³
— число тромбоцитов < 100000/мм³
— серьезные нарушения функции печени
— беременность и период лактации
— выраженная нейтропения
— острое инфекционное заболевание в течение последних двух недель
— пациентам, нуждающимся в долгосрочной кислородной терапии
— в сочетании с вакциной от гепатита
Лекарственные взаимодействия
Лекарственные взаимодействия, общие для всех цитотоксических препаратов:
В связи с увеличением риска тромбоза в случае опухолевых заболеваний, часто применяют антикоагулянты. Высокий уровень внутренней индивидуальной изменчивости свертываемости крови во время заболевания, и вероятности взаимодействия между антикоагулянтами для приема внутрь и химиотерапии необходимо увеличить периодичность мониторинга МНО (международное нормализованное отношение) в случае, если было принято решение лечить пациента антикоагулянтами для приема внутрь.
Противопоказано одновременное применение с вакциной от гепатита в связи с риском летального исхода, вызванного вакциной.
Не рекомендуется одновременное применение с вакцинами, содержащими живые ослабленные микроорганизмы в связи с риском развития заболевания, вызванного вакциной и возможным летальным исходом. Риск увеличивается у пациентов, с сопутствующими иммунодепрессивными заболеваниями. Рекомендуется применять инактивированные вакцины (полиомиелит).
Фенитоин: риск обострения судорог, вызванный увеличением абсорбции фенитоина цитотоксическим препаратом, или риск увеличения токсичности или снижение эффективности цитотоксического препарата, из-за увеличения печеночного метаболизма фенитоина.
Одновременное применение для принятия к сведению:
Циклоспорин, такролимус: повышенный иммунодефицит с риском лимфопролиферации.
Лекарственные взаимодействия, характерные для алкалоидов барвинка:
Не рекомендуется комбинировать с итраконазолом в связи с увеличением нейротоксичности алкалоидов барвинка, из-за снижения их печеночного метаболизма.
При одновременном применении с митомицином С необходимо принять во внимание увеличение риска бронхоспазмов и одышки, в редких случаях был описан интерстициальный пневмонит.
Так как винка-алкалоиды известны как субстрат для Р-гликопротеина, и в связи с отсутствием подробного изучения, во время одновременного приема Навельбина® с сильными модуляторами данного мембранного переносчика, должны быть приняты меры предосторожности.
Лекарственные взаимодействия, характерные для винорелбина:
При одновременном приеме Навельбина® с другими лекарственными средствами, известными своим токсичным действием на костный мозг, может усугубиться миелосупрессивное побочное действие.
При комбинированном приеме Навельбина® с цисплатином в течение нескольких циклов применения, не наблюдается взаимное фармакокинетическое взаимодействие. Тем не менее, случаи возникновения гранулоцитопении, связанные с комбинированным приемом Навельбина® с цисплатином выше, чем во время монотерапии Навельбином®.
При комбинированном приеме Навельбина® с некоторыми другими химиотерапевтическими препаратами (паклитаксел, доцетаксел, капецитабин и циклофосфамид для приема внутрь), не было обнаружено значительных фармакокинетических взаимодействий.
Поскольку цитохром 3А4 задействован в метаболизме винорелбина, одновременное применение с сильными ингибиторами этого изофермента (такими как кетоконазол, итраконазол) может привести к увеличению концентрации винорелбина в крови и одновременное применение с сильными индукторами этого изофермента (такими как рифампицин, фенитоин) могут привести к снижению концентрации винорелбина в крови.
Противорвотные лекарственные средства, антагонисты 5НТ3 (такие как ондансетрон, гранисетрон) не изменяют фармакокинетику Навельбина® мягких капсул (см. раздел Особые указания).
Прием пищи не влияет на фармакокинетику винорелбина.
Особые указания
Препарат Навельбин® должен быть назначен врачом, имеющим опыт применения химиотерапии со специальным оборудованием для контроля за цитотоксическими лекарствами.
Если пациент по ошибке разжует или рассосет капсулу, жидкость окажет раздражающее действие. Прополощите рот водой или физиологическим раствором (0.9 % раствор натрия хлорида). В случае, если капсула будет разрезана или повреждена, жидкость окажет раздражающее действие, и при контакте может нанести вред коже, слизистой оболочке или глазам. Не рекомендуется употреблять поврежденную капсулу, капсулу необходимо вернуть в аптеку, или врачу для утилизации должным образом. Если контакт с жидкостью произошел, необходимо немедленно тщательно промыть место контакта водой или физиологическим раствором.
В случае рвоты в течение нескольких часов после приема препарата, необходимо прекратить его применение. Поддерживающее лечение противорвотными средствами, такими как антагонисты 5НТ₃ (например, ондансетрон, гранисетрон) может снизить воздействие винорелбина (см. раздел Лекарственные взаимодействия).
Навельбин® мягкие капсулы при приеме внутрь чаще вызывают тошноту/рвоту, чем при внутривенном введении Навельбин® концентрата для приготовления раствора для инфузий. Рекомендуется профилактический прием противорвотных средств.
Так как в препарате содержится сорбитол, капсулы не рекомендуется принимать пациентам с редким наследственным синдромом непереносимости фруктозы.
Контроль лабораторных показателей
Во время лечения препаратом Навельбин® необходимо проводить полный гематологический контроль (определить уровень гемоглобина, количество лейкоцитов, нейтрофилов и эритроцитов перед каждой очередной инъекцией или приемом внутрь).
Доза препарата должна быть установлена по результатам гематологического контроля.
Если количество нейтрофилов ниже 1500 /мм³ и/или количество эритроцитов ниже 100000/мм³, то лечение необходимо отложить до восстановления показателей крови.
В случае увеличения дозы с 60 до 80 мг/м² в неделю, после третьего приема — см. раздел Способ применения и дозы.
Если во время приема препарата по 80 мг/м² количество нейтрофилов окажется ниже 500/мм³ или больше одного раза между 500 и 1000/мм³, прием препарата следует отложить, и снизить дозу до 60 мг/м² в неделю. При необходимости увеличить дозу от 60 до 80 мг/м² в неделю, см. раздел Способ применения и дозы.
В результате клинических испытаний, во время лечения начальной дозой 80 мг/м², у некоторых пациентов наблюдались чрезмерные нейтропенические осложнения, включая тех, у кого уровень воздействия был невысоким. По этой причине рекомендуется начать с дозы 60 мг/м², увеличивая до дозы 80 мг/м², в случае если доза соответствует описанию в разделе Способ применения и дозы.
Если у пациента появились признаки или симптомы, свидетельствующие об инфекционном заболевании, следует незамедлительно пройти обследование.
Особые меры предосторожности при применении у пациентов
При назначении препарата должны быть предприняты особые меры предосторожности у пациентов
— с учетом ишемической болезни сердца в анамнезе (см. раздел Побочные действия)
— с неудовлетворительной гематологической картиной крови
Не рекомендуется одновременное назначение препарата Навельбин® и проведение лучевой терапии, если в область облучения включена печень.
Противопоказано одновременное назначение препарата Навельбин® с вакциной от гепатита и не рекомендуется одновременное применение с вакцинами, содержащими живые ослабленные микроорганизмы.
Необходимо принимать меры предосторожности во время одновременного применения препарата Навельбин® с сильными ингибиторами или индукторами CYP3A4 (См. раздел Лекарственные взаимодействия).
Не рекомендуется комбинированное применение с фенитоином (как все цитотоксические препараты) и с итраконазолом (как все алколоиды барвинка).
Применение у пациентов с нарушениями функции печени
Прием препарата Навельбин® перорально изучался у пациентов с печеночной недостаточностью в следующих дозах:
— 60 мг/м² у пациентов с легкой печеночной недостаточностью (билирубин < 1.5 раза верхней границы нормы и АлАТ и/или АсАТ от 1.5 до 2.5 раза больше верхней границы нормы);
— 50 мг/м² у пациентов с тяжелой печеночной недостаточностью (билирубин от 1.5 до 3-х раза больше верхней границы нормы, вне зависимости от уровня АлАТ и АсАТ).
Изученные дозы не показали изменения данных по безопасности и фармакокинетике винорелбина у пациентов.
В связи с тем, что прием препарата Навельбин® перорально не изучался у пациентов с тяжелой печеночной недостаточностью, поэтому применение препарата противопоказано у данной группы пациентов (см. разделы Противопоказания, Фармакокинетика).
Применение у пациентов с нарушениями функции почек
Так как уровень почечной экскреции не высок, с точки зрения фармакокинетики, нет никаких оснований для снижения дозы препарата Навельбин® пациентам с нарушением функции почек (см. раздел Фармакокинетика).
Применение в педиатрии
Безопасность и эффективность применения препарата Навельбин® у детей не изучена, поэтому применение препарата у детей не рекомендуется.
Женщины детородного возраста
Женщинам детородного возраста необходимо использовать методы контрацепции во время лечения и после окончания лечения в течение 3 месяцев.
Влияние на фертильность
Мужчинам, проходящим курс лечения препаратом Навельбин®, не рекомендуется становиться отцом в течении как минимум трех месяцев после курса лечения.
До начала курса лечения рекомендуется законсервировать сперму для последующего оплодотворения без негативного влияния для будущего ребенка после лечения винорелбином.
Особенности влияния лекарственного средства на способность управлять автотранспортом и потенциально опасными механизмами
Исследований влияния препарата на способность управлять автотранспортом и потенциально опасными механизмами не проводилось. На основе фармакодинамических свойств винорелбин не оказывает влияния на способность к вождению транспортным средством и управлению механизмами. Однако, стоит принять меры предосторожности, так как лечение винорелбином может привести к побочным действиям.
Передозировка
Симптомы: острая передозировка может вызвать гипоплазию костного мозга с повышенным риском заражения, лихорадкой и парезом кишечника.
Лечение: общая поддерживающая терапия наряду с переливанием крови и применением антибиотиков широкого спектра действия определяется врачом.
Форма выпуска и упаковка
По 1 капсуле помещают в контурную ячейковую упаковку из пленки поливинилхлоридной и фольги алюминиевой.
По 1 контурной упаковке вместе с инструкцией по медицинскому применению на государственном и русском языках вкладывают в пачку из картону.
Условия хранения
Хранить при температуре от 2 ºС до 8 ºС.
Хранить в недоступном для детей месте!
Срок хранения
3 года
Не применять по истечении срока годности.
Условия отпуска из аптек
По рецепту
Наименование и страна производителя
Пьер Фабр Медикамент Продакшн, Франция
Владелец регистрационного удостоверения
Пьер Фабр Медикамент Продакшн
45 пл. Абель Ганс 92100 Булонь, Франция
Адрес организации, принимающей на территории Республики Казахстан претензии от потребителей по качеству продукции (товара)
Представительство «EUROMEDEX»
050026, г. Алматы, ул. Гоголя, 180/2 — 13
Тел./Факс: +7(727) 378-70-91 e-mail: office.kz@euromedex.com
